Подготовка образца для улавливания белковой суспензии для слезной протеомики методом жидкостной хроматографии и тандемной масс-спектрометрии
* These authors contributed equally
In This Article
Summary
В этом протоколе описан метод сбора образцов слезы с использованием полосок Ширмера и интегрированный количественный рабочий процесс для обнаружения неинвазивных биомаркеров слезного белка. Рабочий процесс подготовки образцов с улавливанием суспензии обеспечивает быструю и надежную подготовку проб слезы и масс-спектрометрический анализ, что приводит к более высокому выходу пептидов и идентификации белков по сравнению со стандартными процедурами в растворе.
Abstract
Слезная жидкость является одной из легкодоступных биожидкостей, которую можно собирать неинвазивным способом. Слезная протеомика может открыть биомаркеры для некоторых глазных заболеваний и состояний. Сообщается, что колонна улавливания суспензии является эффективным и удобным рабочим процессом пробоподготовки для широкого применения последующего протеомного анализа. Тем не менее, эта стратегия не была хорошо изучена при анализе протеома слезы человека. Настоящий протокол описывает интегрированный рабочий процесс от клинических образцов слезы человека до очищенных пептидов для неинвазивного исследования биомаркеров слезоточивого белка с использованием масс-спектрометрии, которая дает представление о биомаркерах заболеваний и мониторинге в сочетании с биоинформатическим анализом. Была применена подготовка образцов для захвата белковой суспензии, которая продемонстрировала открытие слезного протеома с помощью быстрых, воспроизводимых и удобных для пользователя процедур в качестве универсальной, оптимизированной пробоподготовки для анализа слезной жидкости человека. В частности, процедура улавливания суспензии превзошла пробоподготовку в растворе с точки зрения извлечения пептидов, идентификации белков и сокращения времени пробоподготовки.
Introduction
Протеомика слез привлекла внимание к изучению потенциальных биомаркеров глазных заболеваний и состояний 1,2,3,4,5,6, чтобы получить доступ к патогенезу глазного и системного состояния, а также использовать преимущества неинвазивного сбора образцов слезы с помощью полосок Ширмера. Технологический прогресс масс-спектрометрии нового поколения позволил количественно определить количество белков в микролитровых слезах с точностью и прецизионностью, которые были невозможны в прошлом. Методы пробоподготовки еще не стандартизированы. Надежный и стандартизированный рабочий процесс пробоподготовки имеет важное значение для успеха клинического применения в исследованиях биомаркеров слезного белка. Рабочий процесс пробоподготовки с захватом суспензии (S-Trap) недавно был признан эффективным и чувствительным методом пробоподготовки для широкого последующего протеомного анализа 7,8. Тем не менее, эта стратегия не была хорошо описана при анализе протеома слезы человека, превзошла подготовку проб с помощью фильтра (FASP) и разложение в растворе с точки зрения эффективности ферментативного разложения и большего числа идентификаций белков с помощью масс-спектрометрического анализа9. Подход на основе S-Trap был продемонстрирован при препарировании ткани сетчатки 10, фиксированной формалином, залитой парафином ткани (FFPE)11, клеток 12, микроорганизмов13 и жидкостной биопсии 14,15.
Этот протокол описывает интегрированный количественный рабочий процесс от клинических образцов до ферментативно перевариваемого белка для обнаружения неинвазивной панели биомаркеров слезоточивого белка с быстрой, воспроизводимой и надежной технической стратегией. Вкратце, слезную жидкость собирали с помощью стандартной полоски Ширмера и сразу же высушивали с помощью офтальмологического обогревателя, чтобы предотвратить автолиз белка при комнатной температуре. Внедренные общие белки экстрагировали с помощью 5%-ного буфера для лизиса додецилсульфата натрия (SDS) в соответствии с предложением производителя с последующим измерением белка. Затем экстрагированный лизат подвергали стандартному восстановлению дитиотрейтолом (DTT) и алкилированию йодоацетамидом (IAA).
После подкисления фосфорной кислотой к агрегатным белкам добавляли буфер для осаждения белка с улавливающей суспензией, содержащий 90% метанола и 100 мМ бикарбоната триэтиламмония (TEAB). Затем образец переносили в новую микроколонку для улавливания суспензии. Ферментативное сбраживание проводили с секвенированием трипсина в соотношении 1:25 (w/w, трипсин: белок) при 47 °C в течение 1 ч. Полученные пептиды затем элюировали с помощью центрифугирования, последовательно с 50 мМ TEAB, 0,2% водной муравьиной кислоты (ЖК) и 50% ацетонитрила (ACN), содержащего 0,2% ЖК. Элюированные пептиды сушили в вакууме и восстанавливали в 0,1 % ЖК. Концентрацию пептида измеряли и доводили до 0,5 мкг/мкл для масс-спектрометрического анализа.
Protocol
Испытуемые предоставляли письменное информированное согласие перед участием в исследовании. Исследование было одобрено Комитетом по этике человека Гонконгского политехнического университета и соответствовало принципам Хельсинкской декларации.
1. Сбор слезной жидкости человека с помощью полоски Ширмера
- Наденьте перчатки и продезинфицируйте, чтобы избежать загрязнения образца.
- Убедитесь, что внутренняя упаковка не повреждена, стерильна и не просрочена.
- Слегка согните верхнюю часть полоски Ширмера внутрь на отметке 0 мм, как показано рядом с полукруглым кончиком полоски (Рисунок 1).
- Извлеките полоску из внутренней упаковки, держась за конец полоски, и избегайте прямого контакта с зоной забора пробы от 0 до 25 мм.
- Попросите испытуемого отвести взгляд от положения полоски, которую нужно разместить.
- Аккуратно опустите нижнее веко и зацепите конец полоски в нижнем своде возле латеральной области кантуса (рис. 2). Повторите ту же процедуру на другом глазу.
- Попросите испытуемого осторожно закрыть веки, чтобы свести к минимуму раздражение.
- Собирайте слезную жидкость в течение примерно 5 минут, а лучше 15-20 мм образца слезы.
- Попросите испытуемого открыть оба глаза, осторожно опустите нижнее веко и снимите полоски с объекта.
- Проверьте гидратированную длину на полоске Ширмера и запишите собранное количество в мм.
- Высушите полосу стандартным чистым нагревателем рамы до полного высыхания жидкости.
ПРИМЕЧАНИЕ: Следует избегать чрезмерного нагрева, который потенциально может обуглить фильтровальную бумагу. - Поместите каждую высушенную полоску Ширмера в маркированную криопробирку и храните ее предпочтительно в прохладном, сухом месте в темноте до дальнейшей обработки.
2. Приготовление химикатов и реагентов
- Лизисный буфер (5% SDS, 50 мМ TEAB, pH 7,5), 20 мл
- Пипетка 1 мл 1 М TEAB и 80 мкл 12% ортофосфорной кислоты. Вихрь и кратковременная ультразвуковая обработка для удаления пузырьков. Долейте до 20 мл деионизированной воды.
- Отвешивают 1 г СДС и добавляют в раствор с колебаниями до полного растворения.
- Буфер для осаждения белка (90% метанола, 100 мМ TEAB, pH 7,1), 10 мл
- Добавьте 893 мкл 1 М TEAB и 92 мкл деионизированной воды.
- Добавьте в раствор 15 мкл 85 мас.% фосфорной кислоты и 9 мл метанола и кратковременно перемешайте.
- Буфер для пищеварения (50 мМ TEAB), 1 мл
- Добавьте 50 мкл 1 M TEAB и долейте до 1 мл деионизированной воды.
- 200 мМ раствор дитиотрейтола (DTT), 500 мкл
- Взвесьте 15 мг ДТТ и растворите в 500 мкл деионизированной воды; вихрь кратко.
ПРИМЕЧАНИЕ: Подготовьте перед использованием.
- Взвесьте 15 мг ДТТ и растворите в 500 мкл деионизированной воды; вихрь кратко.
- Раствор йодоацетамида (IAA) 400 мМ, 200 мкл
- Взвесьте 15 мг IAA и растворите в 200 мкл деионизированной воды; вихрь кратко. ПРИМЕЧАНИЕ: Подготовьтесь перед использованием и избегайте света.
- 0,2% муравьиная кислота, 50% ацетонитрил, 10 мл
- Приготовьте 10 мл 50% ацетонитрила в деионизированной воде.
- Добавьте 20 мкл муравьиной кислоты и быстро перемешайте.
- 0,2% раствор муравьиной кислоты, 10 мл
- Добавьте 20 мкл муравьиной кислоты в 10 мл деионизированной воды и ненадолго взбейте в перемешательном режиме.
- 0,1% раствор муравьиной кислоты, 10 мл
- Добавьте 10 мкл муравьиной кислоты к 10 мл деионизированной воды; вихрь кратко.
3. Экстракция белка в полосе Ширмера
- Отрежьте и выбросьте передний конец за отметкой 0 мм полосы, чтобы удалить возможное загрязнение из-за контакта тканей конъюнктивы с чистыми ножницами из нержавеющей стали.
- Разрежьте полоску с интервалом 1 мм на пробирку для микроцентрифуги объемом 1,5 мл (Рисунок 3).
- Добавьте 100 мкл лизисного буфера в микроцентрифужную пробирку и встряхните при 1000 об/мин при комнатной температуре в течение 1 ч в термомиксере.
- Кратковременно центрифугируйте и перелейте надосадочную жидкость в новую микроцентрифужную пробирку объемом 1,5 мл.
- Переместите полоски в наконечники для пипеток объемом 200 мкл с помощью чистых щипцов. Поместите наконечники в ту же пробирку, что и на шаге 3.4, с держателем и центрифугой при комнатной температуре при 4 000 × г в течение 1 мин для максимального восстановления оставшегося образца на полоске.
- Измерьте концентрацию белка с помощью бисинхониновой кислоты (BCA) или анализа совместимого белка.
4. Подготовка образцов для улавливания суспензии
- Нормализовать образцы до 50 мкг белка в зависимости от результата анализа белка.
- Добавьте 200 мМ ДТТ в соотношении 1:10 (v/v, DTT: образец) до конечной концентрации 20 мМ ДТТ и инкубируйте при 95 °C в течение 10 мин.
- Остудите белковый раствор до комнатной температуры.
- Добавляют 400 мМ IAA в соотношении 1:10 (v/v, IAA: образец) до конечной концентрации 40 мМ IAA и инкубируют в темноте при комнатной температуре в течение 10 мин.
- Добавьте 12% водной фосфорной кислоты в соотношении 1:10 (v/v, кислота: образец) до конечной концентрации 1,2% фосфорной кислоты и кратковременно перемешайте.
- Добавьте буфер, связывающий белки в соотношении 1:6 (v/v, образец: буфер) и кратковременно встряхивайте.
ПРИМЕЧАНИЕ: На этом этапе должны образоваться коллоидные частицы белка, и раствор будет казаться полупрозрачным, если количество белка достаточно. - Снимите крышку микроцентрифуговой колонки с улавливанием суспензии и соберите ее на микроцентрифужную пробирку объемом 2 мл для сбора потока.
- Добавьте в колонку до 200 мкл подкисленной смеси лизата белка.
- Центрифугируют колонку при 4 000 × г в течение 20 с. Белковые частицы были захвачены; Повторяйте до тех пор, пока образцы не будут загружены в столбец.
- Добавьте 150 мкл буфера, связывающего белок, и центрифугу при 4000 × г в течение 20 с, чтобы промыть взвешенный белок. Повторить 3 раза.
- Установите микроколонку для улавливания суспензии на новую микроцентрифужную пробирку объемом 1,5 мл.
- Добавьте 20 мкл 50 мМ пищеварительного буфера TEAB, содержащего протеазу, в соотношении 1:25 (w/w, трипсин: белок) на фильтр внутри спиновой колонны, избегая пузырьков и воздушного зазора между фильтром и раствором для сбраживания.
- Закройте микроспин-колонку с улавливанием суспензии, чтобы предотвратить испарение. Выдерживают при 47 °С в течение 1 ч в термомиксере; Не встряхивайте и не встряхивайте во время пищеварения.
- Элюируют пептиды с 40 мкл 50 мМ TEAB под действием центробежной силы при 4 000 × г в течение 20 с.
- Добавьте 40 мкл 0,2% ТЖК и центрифугируйте при 4000 × г в течение 20 с.
- Добавьте 35 мкл 0,2% ЖК, 50% ацетонитрила и центрифугу при 4000 × г в течение 20 с.
- Три пула элюаты и сушка с помощью вакуумной центрифуги.
- Хранить при температуре -80 °C в сверхнизкотемпературной морозильной камере до дальнейшего анализа. ПРИМЕЧАНИЕ: Протокол можно приостановить здесь.
5. Восстановление пептидов для масс-спектрометрического анализа
- Восстановите образец с 12 мкл 0,1% ЖК, вихрями и центрифугой на короткое время.
- Измерьте концентрацию пептидов с помощью набора для анализа пептидов.
- Нормализовать концентрацию пептидов до 0,5 мкг/мкл в 0,1% ЖК.
- Пептидную смесь переложить во флакон с автосамплером и подготовить к масс-спектрометрическому анализу.
6. Отбор образцов методом жидкостной хроматографии и тандемной масс-спектрометрии
- Загружают 3 мкг пептида с буфером изократической загрузки (0,1% ЖК, 5% АКН) в колонку-ловушку (С18, 5 мкм, 100 мкм, 20 мм) со скоростью потока 2 мкл/мин в течение 15 мин.
- Фракционирование пептидов с помощью наноаналитической колонки с обращенной фазой (C18, 5 мкм, 100 мкм, 300 мм) со скоростью потока 350 нл/мин при градиенте разделения 155 мин. Используйте подвижную фазу А, содержащую смесь 0,1% муравьиной кислоты (v/v), 5% ACN (v/v) в воде и подвижную фазу B, содержащую 0,1% FA (v/v), 98% ACN (v/v) в воде. Используйте следующий градиент: 0-0,5 мин: 5% В, 0,5-90 мин: 10% В, 90-120 мин: 20% В, 120-130 мин: 28% В, 130-135 мин: 45% В, 135-141 мин: 80% В, 141-155 мин: 5% В.
- Выполняйте сбор данных (DDA) с диапазоном сканирования TOF-MS от 350 до 1800 м/z с временем накопления 250 мс и временем динамического исключения цели 18 с. Затем проводят сканирование МС/МС на скорости от 100 до 1800 м/з в режиме высокой чувствительности с временем накопления 50 мс для 50 верхних прекурсоров за цикл с порогом 125 сПс для сигнала МС/МС с состоянием заряда от +2 до +4.
- Анализируйте необработанные данные с помощью справочного программного обеспечения или других совместимых движков с эталонной базой данных в FASTA из общедоступной базы данных UniProt.
Representative Results
Этот протокол позволяет отбирать образцы слезы с помощью полосок Ширмера, которые хранятся в сухом виде при комнатной температуре перед последующей подготовкой образца для масс-спектрометрического анализа. Рабочий процесс подготовки образцов с помощью фильтра (FASP) с микроколонной, улавливающей суспензию, позволил быстро подготовить пробы за несколько часов по сравнению с обычными процедурами разложения в растворе за несколько дней, требующих ночной инкубации. Выход пептидного восстановления был значительно выше (p < 0,001), чем стандартный протокол разложения в растворе, и с хорошей воспроизводимостью при коэффициенте вариации (%CV) < 7%. Пул образцов слез был повторен в шести технических повторениях с восстановлением 74,2 ± 5,0% пептидов и 52,8 ± 1,6% пептидов в образцах, приготовленных с помощью процедур в растворе. Объединенный образец слезы с количеством белка 36,3 мкг наносили на полоску Ширмера и экстрагировали, как описано выше, эффективность экстракции белка составила 81% (29,5 ± 6,8 мкг, среднее ± SD).
Оба рабочих процесса загружали 3 мкг пептидов на MS, и поиск DDA дал в общей сложности 1183 ± 118 белков (5757 ± 537 различных пептидов) и 874 ± 70 белков (4400 ± 328 пептидов) при 1% FDR в группе захвата суспензии и группе в растворе соответственно. Анализ онтологии генов (ГО) с использованием системы классификации PANTHER выявил очень схожие протеомы для обоих подходов, основными молекулярными функциями которых являются связывание, каталитическая активность и регуляция молекулярных функций (рис. 4).

Иллюстрация 1: Перед нанесением согните верхнюю часть полосы Ширмера на отметке 0 мм. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
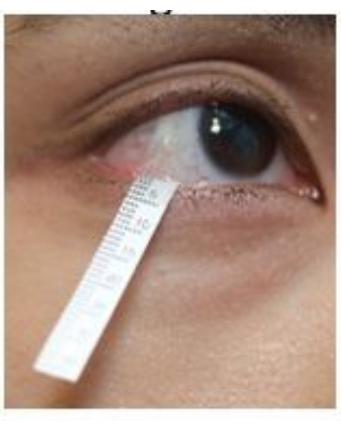
Иллюстрация 2: Положение полосы Ширмера во время сбора слез. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
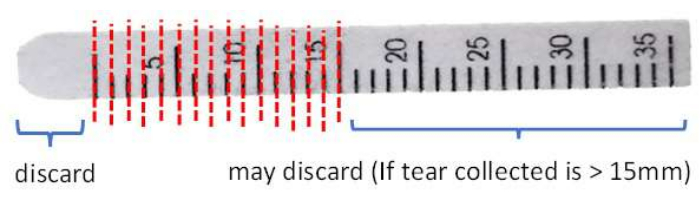
Рисунок 3: Иллюстрация обработки полосы Ширмера перед экстракцией белка. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
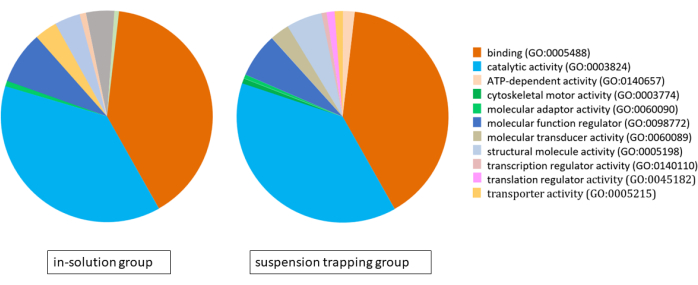
Рисунок 4: Круговая диаграмма, иллюстрирующая анализ онтологии генов для протеомов, идентифицированных с помощью рабочего процесса в растворе и рабочего процесса захвата суспензии с использованием системы классификации PANTHER. Пожалуйста, нажмите здесь, чтобы просмотреть увеличенную версию этого рисунка.
Discussion
Для достижения точных результатов с использованием этого метода во всех процедурах, начиная со сбора проб слезы, следует надевать одноразовые перчатки, чтобы избежать загрязнения пробы. Важно избегать образования пузырьков и воздушных зазоров между фильтром и раствором пробы на каждом этапе, используя микровращающиеся колонны. Если объем образца больше, чем вместимость колонок, рекомендуется повторить процесс. Этот протокол оказался более эффективным, чем традиционный протокол в растворе, с точки зрения времени приготовления, восстановления белка и идентификации общего белка. В значительной степени это связано с тем, что образцы проходят большинство необходимых процедур на одной и той же колонне, в отличие от метода в растворе, который включает в себя несколько этапов переноса, таких как осаждение ацетона, разложение и очистка (обессоливание), что увеличивает вероятность изменений в полученных данных.
В дополнение к образцам слезы, собранным с помощью микрокапиллярного метода16,17, этот рабочий процесс FASP с микроколонкой для улавливания суспензии обеспечивает альтернативный метод подготовки образцов, который позволяет быстро и надежно подготовить образцы слезы, собранные с помощью полосок Ширмера, с минимальной подготовкой материала и удобными для пользователя шагами. Это позволяет воспроизводить подготовку образцов слезы для больших когортных исследований при множественных глазных заболеваниях или состояниях с улучшенным восстановлением пептидов и идентификацией белка при рассеянном склерозе по сравнению с процедурами в растворе. Этот надежный процесс может быть регулярно использован при подготовке образцов слезных биомаркеров для исследований и других клинических целей. Самое главное, что он требует минимальной подготовки персонала для сбора на месте и исключает необходимость хранения образцов в морозильной камере. Образцы высушиваются на месте, чтобы свести к минимуму автолиз и разложение белка. Таким образом, это обеспечивает удобную отправку по почте для облегчения последующего анализа, в отличие от использования микрокапиллярных трубок.
Disclosures
У авторов нет конфликта интересов, о котором можно было бы заявлять.
Acknowledgements
Эта работа была поддержана инициативой InnoHK и правительством Специального административного района Гонконг; Научно-исследовательский центр SHARP Vision; и Исследовательский центр инноваций в китайской медицине (RCMI) при Гонконгском политехническом университете.
Materials
| Name | Company | Catalog Number | Comments |
| 9 mm Plastic Screw Thread Vials | Thermo Scientific | C4000-11 | |
| Acetonitrile, LCMS Grade | Anaqua | AC-1026 | |
| Centrifuge MiniSpin plus | Eppendorf | 5453000097 | |
| DL-dithiothreitol (DTT), BioUltra | Sigma-Aldrich | 43815 | |
| Eppendorf Safe-Lock Tubes, 1.5 mL | Eppendorf | 30120086 | |
| Formic acid, ACS reagent, ≥96% | Sigma-Aldrich | 695076 | |
| Frame Heater OPTIMONSUN Electronic | Breitfeld & Schliekert GmbH | 1203166 | |
| Iodoacetamide (IAA), BioUltra | Sigma-Aldrich | I1149 | |
| Methanol, HPLC Grade | Anaqua | MA-1292 | |
| Nunc Biobanking and Cell Culture Cryogenic Tubes, 2 mL | Thermo Fisher Scientific | 368632 | |
| Phosphoric acid, 85 wt.% in H2O | Sigma-Aldrich | 345245 | |
| Pierce Quantitative Colorimetric Peptide Assay | Thermo Fisher Scientific | 23275 | |
| Pierce Rapid Gold BCA Protein Assay Kit | Thermo Fisher Scientific | A53225 | |
| Quadrupole Time-of-Flight Mass Spectrometry | Sciex | TripleTOF 6600 | |
| Schirmer Ophthalmic Strips | Entod Research Cell UK Ltd | I-DEW Tearstrips | |
| S-Trap Micro Column | Protifi | C02-micro-80 | |
| SureSTART 9 mm Screw Caps | Thermo Scientific | CHSC9-40 | |
| Triethylammonium bicarbonate (TEAB), 1 M | Sigma-Aldrich | 18597 | |
| Ultra-performance Liquid Chromatography | Eksigent | NanoLC 400 | |
| UltraPure Sodium dodecyl sulfate (SDS) | Thermo Fisher Scientific | 15525017 |
References
- Ma, J. Y. W., Sze, Y. H., Bian, J. F., Lam, T. C. Critical role of mass spectrometry proteomics in tear biomarker discovery for multifactorial ocular diseases (Review). International Journal of Molecular Medicine. 47 (5), 83 (2021).
- Tse, J. S. H., et al. Integrating clinical data and tear proteomics to assess efficacy, ocular surface status, and biomarker response after orthokeratology lens wear. Translational Vision Science & Technology. 10 (11), 18 (2021).
- Cheung, J. K., et al. Human tear proteome dataset in response to daily wear of water gradient contact lens using SWATH-MS approach. Data in Brief. 36, 107120 (2021).
- Tse, J. S., et al. Data on assessment of safety and tear proteome change in response to orthokeratology lens - Insight from integrating clinical data and next generation proteomics. Data in Brief. 29, 105186 (2020).
- Zhan, X., Li, J., Guo, Y., Golubnitschaja, O. Mass spectrometry analysis of human tear fluid biomarkers specific for ocular and systemic diseases in the context of 3P medicine. The EPMA Journal. 12 (4), 449-475 (2021).
- Ponzini, E., et al. Mass spectrometry-based tear proteomics for noninvasive biomarker discovery. Mass Spectrometry Reviews. 41 (5), 842-860 (2022).
- HaileMariam, M., et al. S-Trap, an ultrafast sample-preparation approach for shotgun proteomics. Journal of Proteome Research. 17 (9), 2917-2924 (2018).
- Ding, H., et al. Urine proteomics: evaluation of different sample preparation workflows for quantitative, reproducible, and improved depth of analysis. Journal of Proteome Research. 19 (4), 1857-1862 (2020).
- Ludwig, K. R., Schroll, M. M., Hummon, A. B. Comparison of in-solution, FASP, and S-Trap based digestion methods for bottom-up proteomic studies. Journal of Proteome Research. 17 (7), 2480-2490 (2018).
- Sze, Y. H., et al. High-pH reversed-phase fractionated neural retina proteome of normal growing C57BL/6 mouse. Scientific Data. 8 (1), 27 (2021).
- Marchione, D. M., et al. HYPERsol: High-quality data from archival FFPE tissue for clinical proteomics. Journal of Proteome Research. 19 (2), 973-983 (2020).
- Chhuon, C., et al. A sensitive S-Trap-based approach to the analysis of T cell lipid raft proteome. Journal of Lipid Research. 61 (11), 1512-1523 (2020).
- Hayoun, K., et al. Evaluation of sample preparation methods for fast proteotyping of microorganisms by tandem mass spectrometry. Frontiers in Microbiology. 10, 1985 (2019).
- Templeton, E. M., et al. Comparison of SPEED, S-Trap, and in-solution-based sample preparation methods for mass spectrometry in kidney tissue and plasma. International Journal of Molecular Sciences. 24 (7), 6290 (2023).
- Ding, Z., Wang, N., Ji, N., Chen, Z. S. Proteomics technologies for cancer liquid biopsies. Molecular Cancer. 21 (1), 53 (2022).
- Nättinen, J., Aapola, U., Jylhä, A., Vaajanen, A., Uusitalo, H. Comparison of capillary and Schirmer strip tear fluid sampling methods using SWATH-MS proteomics approach. Translational Vision Science & Technology. 9 (3), 16 (2020).
- Bachhuber, F., Huss, A., Senel, M., Tumani, H. Diagnostic biomarkers in tear fluid: from sampling to preanalytical processing. Scientific Reports. 11 (1), 10064 (2021).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
ABOUT JoVE
Copyright © 2025 MyJoVE Corporation. All rights reserved