È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Imaging del calcio nel collicolo superiore del topo
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Questo protocollo descrive in dettaglio la procedura per l'imaging delle risposte del calcio nel collicolo superiore (SC) dei topi svegli, compreso l'imaging dell'attività di un singolo neurone con microscopia a due fotoni, lasciando intatta la corteccia nei topi wild-type, e l'imaging dell'intero SC con microscopia ad ampio campo nei topi mutanti a corteccia parziale.
Abstract
Il collicolo superiore (SC), una struttura del mesencefalo evolutivamente conservata in tutti i vertebrati, è il centro visivo più sofisticato prima dell'emergere della corteccia cerebrale. Riceve input diretti da ~30 tipi di cellule gangliari retiniche (RGC), ognuna delle quali codifica una specifica caratteristica visiva. Rimane incerto se il SC erediti semplicemente le caratteristiche retiniche o se si verifichi un'elaborazione aggiuntiva e potenzialmente de novo nel SC. Per rivelare la codifica neurale delle informazioni visive nel SC, forniamo qui un protocollo dettagliato per registrare otticamente le risposte visive con due metodi complementari nei topi svegli. Un metodo utilizza la microscopia a due fotoni per visualizzare l'attività del calcio a una risoluzione a singola cellula senza ablare la corteccia sovrapposta, mentre l'altro utilizza la microscopia ad ampio campo per visualizzare l'intero SC di un topo mutante la cui corteccia è in gran parte non sviluppata. Questo protocollo descrive in dettaglio questi due metodi, tra cui la preparazione dell'animale, l'iniezione virale, l'impianto della placca testa, l'impianto del tappo, l'acquisizione dei dati e l'analisi dei dati. I risultati rappresentativi mostrano che l'imaging del calcio a due fotoni rivela risposte neuronali evocate visivamente a una risoluzione a singola cellula e l'imaging del calcio ad ampio campo rivela l'attività neurale in tutto il SC. Combinando questi due metodi, si può rivelare la codifica neurale nel SC su scale diverse, e tale combinazione può essere applicata anche ad altre regioni del cervello.
Introduzione
Il collicolo superiore (SC) è un importante centro visivo in tutti i vertebrati. Nei mammiferi, riceve input diretti dalla retina e dalla corteccia visiva1. Mentre la registrazione ottica è stata ampiamente applicata alla corteccia 2,3,4,5, la sua applicazione nel SC è ostacolata da scarsi accessi ottici 6,7,8,9,10,11,12,13,14,15,16,17 ,18,19. L'obiettivo di questo protocollo è quello di fornire dettagli su due metodi complementari per la registrazione ottica dell'attività neurale nel SC.
L'SC si trova sotto la corteccia e il seno trasverso, il che limita l'accesso ottico ai neuroni collicolari. Un approccio per superare questa limitazione è quello di aspirare la corteccia sovrapposta ed esporre il SC antero-laterale 7,9,10,13,14,19. Tuttavia, poiché il SC riceve input corticali, tale operazione potrebbe influenzare il modo in cui i neuroni SC rispondono agli stimoli visivi. Per ovviare a questa limitazione, descriviamo qui un protocollo alternativo per visualizzare lo strato superficiale del SC posteriore-mediale con un tappo di silicio, lasciando intatta la corteccia 8,11. In particolare, per ottenere una risoluzione a singola cellula, abbiamo applicato la microscopia a due fotoni per visualizzare le risposte del calcio nel SC posteriore-mediale di topi wild-type. Inoltre, per ottenere un'ampia copertura, abbiamo applicato la microscopia ad ampio campo per visualizzare l'intero SC di un topo mutante la cui corteccia posteriore non si è sviluppata20.
I due metodi descritti in questo protocollo sono complementari l'uno all'altro. L'imaging del calcio a due fotoni senza ablazione della corteccia è appropriato per registrare l'attività neurale a risoluzione di una singola cellula con input corticali intatti. L'imaging del calcio ad ampio campo è appropriato per registrare l'attività neurale nell'intero SC sacrificando la risoluzione spaziale.
Protocollo
Tutte le procedure sperimentali sono state eseguite in conformità con le linee guida sul benessere degli animali e approvate dall'IACUC presso l'Istituto cinese per la ricerca sul cervello di Pechino.
NOTA: La tempistica per questo protocollo è la seguente: 1) fare la ventosa; 2) iniettare il virus; 3) impiantare la placca portatestina; 4) dopo 3 settimane, impiantare il tappo; 5) Dopo un recupero di ~ 3 giorni e l'assuefazione sul tapis roulant, eseguire l'imaging a due fotoni/ad ampio campo.
1. Preparazione di una ventosa (Figura 1A)
- Depositare una goccia di soluzione salina tamponata con fosfato (PBS, 1x) in un piatto acrilico e toccarla con un ago piatto da 21 G per riempire la punta per capillarità.
- Coprire la punta dell'ago con un adesivo siliconico traslucido e lasciare agire per circa ~10 min.
- Tagliare l'adesivo siliconico con le forbici su un disco con un diametro di ~2 mm.
2. Preparazione dei tappi (Figura 1B)
- Preparare uno spessore di plastica di 0,75 mm di spessore e ritagliare un quadrato di 1 cm x 1 cm al centro. Prepara due blocchi di acrilico. Pulisci il calcio di spessore e i blocchi acrilici con alcol e puliscili con carta per lenti.
- Metti lo spessore su un blocco acrilico, deposita l'adesivo siliconico al centro per riempire ~90% dell'apertura (evitare bolle), aggiungi un altro blocco acrilico e ~1 kg di forza e attendi 20 minuti.
- Sotto un microscopio operatorio, tagliare l'adesivo siliconico con un bisturi a prismi triangolari alti 1 mm e larghi 1,5 mm sopra un pezzo di carta con triangoli stampati sopra.
- Rimuovere la polvere dai prismi triangolari con del nastro adesivo di plastica e posizionarla su un vetrino coprioggetti di 5 mm di diametro e 0,15 mm di spessore.
- Mettere il vetrino coprioggetto con i prismi triangolari sotto un trattamento corona, accendere il trattamento corona e avvicinarlo al vetrino coprioggetti fino a quando non appare un chiarimento. Tienilo in quella posizione per alcuni minuti finché non sono attaccati l'uno all'altro.
NOTA: Questo passaggio potrebbe essere diverso per altri trattamenti corona. - Mettere i tappi in una capsula di Petri e metterla in un'incubatrice a 70 °C per una notte.
3. Preparazione degli animali e iniezione del costrutto virale
- Utilizzare topi C57BL/6J (wild-type) e Emx1-Cre:Pals1flox/wt (corteccia parziale)20 di entrambi i sessi a 6 settimane di età (9 settimane al momento dell'imaging).
- Sterilizzare tutti i materiali e gli strumenti utilizzati per la procedura chirurgica.
- Anestetizzare il topo con isoflurano al 5% e poi mantenere l'isoflurano all'1%-2% con una portata di 1 L/min durante l'intervento. Confermare il livello di anestesia dalla mancanza del riflesso di pizzicamento delle dita dei piedi.
- Fissa il mouse su un telaio stereotassico con barre auricolari. Durante l'intervento, applicare un unguento oftalmico sugli occhi del topo per evitare che si secchino e mantenere la temperatura corporea a 37 °C con un termoforo.
- Radere il pelo e sterilizzare la superficie della pelle con iodoforo ed etanolo al 75%. Iniettare lidocaina (5 mg/kg, iniezione sottocutanea [SQ]), tilidina (2 mg/kg, SQ) e meloxicam (2 mg/kg, SQ).
NOTA: La procedura chirurgica per la sterilizzazione, l'analgesia e l'anestesia locale può variare da un istituto all'altro. - Rimuovere la pelle sopra il SC con le forbici chirurgiche per esporre il cranio. Pulisci il cranio con un batuffolo di cotone.
- Regolare la cornice stereotassica fino a quando la superficie del cranio non è piatta. Praticare un foro di 0,5 mm lateralmente e 0,42 mm anteriormente alla fionda lambda fino a quando la dura non è esposta.
- Iniettare il virus adeno-associato (AAV) che esprime GCaMP6m (rAAV2/9-hsyn-GCaMP6m; 1 x10 13 GC/mL disciolti in 1x PBS) a profondità di 1 mm e 1,6 mm dalla lambda con una micropipetta di vetro smussata (il puntale è smussato a 25° con un diametro di 40-50 μm).
- Ad ogni profondità, iniettare 100 nL ad una velocità di 50 nL/min e attendere 5 min dopo ogni iniezione. Dopo l'iniezione, estrarre lentamente l'iniettore.
4. Impianto della placca portatestina
- Pulisci i muscoli e i tessuti sopra il cranio e gratta il cranio con una lama. In caso di sanguinamento, fermarlo con schiuma di gel e pulire il sangue. Fissare la placca della testina (Figura 1C) al cranio con un cemento resinoso adesivo dentale autopolimerizzante. In particolare, mescola 3/4 di cucchiaio di polimero, tre gocce di monomero e una goccia di catalizzatore in una ciotola di ceramica con ghiaccio. Applicare la miscela sulla piastra della testa e sul cranio. Attaccali insieme e attendi 5 minuti affinché l'adesivo si solidifichi.
- Iniettare antibiotici (ceftiofur sodico, 5 mg/kg, SQ) per prevenire le infezioni. Rimuovere il mouse dal telaio stereotassico e posizionarlo su un termoforo per il recupero. Rimettilo nella gabbia di casa dopo esserti ripreso dall'anestesia. Per la gestione del dolore, fornire acqua potabile contenente ibuprofene (0,5 ml/50 ml) al topo per 3 giorni dopo l'intervento chirurgico.
5. Impianto della spina (Figura 2)
- Impiantare il tappo 3 settimane dopo l'iniezione virale. Anestetizzare e fissare il mouse su un telaio stereotassico, come descritto nei passaggi 3.2-3.5. Preparare una schiuma di gel imbevuta di soluzione fisiologica per fermare potenziali emorragie.
- Forare un ovale di 3 mm x 2 mm con una micropunta centrata a 0,5 mm posteriormente al lambda. Assottigliare il contorno dell'ovale fino a quando non si rompe. Assottigliare il cranio davanti alla finestra di registrazione ovale per avvicinare il vetrino coprioggetto al SC.
- Rimuovere i lembi ossei usando una pinza fine. Fai un taglio sulla dura posteriore al seno trasverso e rimuovi il pezzo di dura. Se necessario, aggiungere liquido cerebrospinale artificiale (ACSF) al cervello con una siringa da 3 ml per evitare la secchezza. Asciugare il cranio e la finestra di registrazione con schiuma gel e tamponi di cotone.
- Depositare una goccia di adesivo siliconico nella finestra di registrazione. Utilizzare la ventosa per tenere la spina con pressione negativa. Utilizzare un micromanipolatore motorizzato per spostare la ventosa e abbassare il tappo nell'adesivo siliconico fino a quando il vetrino coprioggetto tocca il cranio. Quindi, spostare il tappo in avanti di ~1 mm per allontanare il seno trasverso ed esporre l'SC. Questo passaggio dovrebbe essere eseguito in 1-2 minuti prima che l'adesivo siliconico diventi appiccicoso.
- Pulire la piastra di testa e applicare cianoacrilato di butile e cemento resinoso attorno al bordo del tappo per fissarlo alla piastra di testa.
NOTA: Fornire assistenza postoperatoria, come descritto al punto 4.2.
6. Imaging a due fotoni (Figura 3)
- Fissare l'animale su un tapis roulant rotante con la sua piastra di testa. Posizionare il tapis roulant sotto un microscopio a due fotoni e regolare l'altezza in una posizione appropriata. Mettere un cono di alluminio nero tra l'obiettivo e la piastra principale per evitare la contaminazione della luce dal monitor per la stimolazione visiva. Abituare il mouse per ~15 min.
- Esegui l'imaging a due fotoni sul microscopio con un ingrandimento 16x, un'apertura numerica (NA) di 0,8 e una distanza di lavoro di 3 mm (WD). Utilizzare un laser Ti:zaffiro con tecnica di blocco della modalità controllata da due scanner galvo per eccitare GCaMP6m a 920 nm. Regolare la potenza del laser sul piano del campione tra 20-80 mW.
- Scansione di un campo visivo di 600 μm x 600 μm a 4,8 Hz con una risoluzione spaziale di 2,4 μ m/pixel e immagine dell'attività neurale fino a 350 μ m.
NOTA: La frequenza di campionamento e la risoluzione spaziale sono per gli scanner galvo e devono essere regolate per gli scanner risonanti. - Raccogliere la fluorescenza emessa con uno specchio dicroico e rilevarla utilizzando un tubo fotomoltiplicatore (PMT) dopo averla fatta passare attraverso un filtro passa-banda.
- Registra la locomozione del mouse sul tapis roulant con un encoder rotativo. Utilizzare una fotocamera con un obiettivo da 50 mm per registrare le dimensioni e la posizione della pupilla. Sincronizza queste registrazioni e acquisizioni di immagini con la stimolazione visiva registrando i trigger inviati dal computer di stimolazione.
7. Analisi delle risposte del calcio misurate mediante imaging a due fotoni
- Correggere il movimento cerebrale durante l'imaging utilizzando SIMA21 o NoRMCorre22.
- Disegna manualmente una regione di interesse (ROI) utilizzando lo strumento Bacchetta magica cellulare (ImageJ) e adattala con un'ellisse in MATLAB. Estrarre le tracce di fluorescenza di ogni ROI dopo aver rimosso la contaminazione neuropilica:
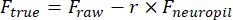
F true e Frawsono rispettivamente le ampiezze di fluorescenza corrette e grezze del ROI, F neuropil è l'ampiezza di fluorescenza del neuropil circostante e r è il fattore di contaminazione del neuropilfuori fuoco (0,7 per la nostra configurazione). L'r è stimato misurando i segnali su un vaso sanguigno per il quale Fvero = 0, come descritto in precedenza23,24. - Rimuovi le fluttuazioni lente della linea di base sottraendo il valore dell'ottavo percentile da una finestra di 15 s centrata su ciascun fotogramma25.
- Definire le risposte visive di un neurone come la variazione relativa dell'ampiezza della fluorescenza nel suo ROI durante il periodo di stimolo:
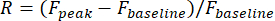
Il picco F è l'ampiezza di picco della traccia di fluorescenza durante la stimolazione visiva e il basaleFè l'ampiezza media durante un periodo di 0,5 s prima della stimolazione.
8. Imaging ad ampio campo e analisi dei dati (Figura 4)
- Costruire un macroscopio ad ampio campo con un obiettivo tandem4 (Figura 4A). Il macroscopio con obiettivo tandem è costituito da due obiettivi della fotocamera (50 mm e 105 mm) collegati tramite un adattatore e l'ingrandimento è ~2x.
- Preparare topi mutanti a corteccia parziale come descritto nei passaggi 3.2-3.5. Iniettare 100 nL di AAV che esprima GCaMP6m ad una profondità di 200 μm al centro di ciascun lato dell'SC.
- Dopo ~3 settimane, impiantare un vetrino coprioggetto di 5 mm di diametro sopra l'SC. Eseguire una craniotomia ovale di 4 mm x 3 mm centrata sull'SC e assottigliare l'osso intorno ad esso. Quindi, premere il vetrino coprioggetto direttamente sul SC e fissarlo con cemento resinoso.
- Eccita GCaMP6m con un diodo a emissione di luce blu (LED) con un filtro di eccitazione (469 nm ± 35 nm). Acquisire immagini utilizzando una fotocamera CMOS (Complementary Metal Oxide Semiconductor) dopo aver superato un filtro di emissione (525 nm ± 39 nm) a 10 Hz. La fotocamera copre un'area di 5,36 mm x 2,85 mm con una risoluzione spaziale di 2,63 μm/pixel.
- Convolgete ogni immagine acquisita con un filtro a scatola normalizzato e sottocampionatela a 1/4 della dimensione originale. Per ogni pixel dell'immagine, definire la risposta, come descritto al punto 7.4.
NOTA: Fornire assistenza postoperatoria, come descritto al punto 4.2.
Risultati
Le figure 1A,B mostrano come realizzare rispettivamente la ventosa e i tappi. La Figura 2 mostra come impiantare correttamente la spina. Dopo aver impiantato il tappo, l'SC posteriore-mediale viene esposto, come mostrato nella Figura 2D. La Figura 3 mostra le risposte del calcio dei neuroni SC da un esempio di topo wild-type ripreso utilizzando la microscopia a due fotoni. Il prisma tri...
Discussione
Passaggi critici del protocollo
La fase più critica è la craniotomia nelle fasi 5.2 e 5.3. Innanzitutto, l'osso a 0,5 mm dietro la lambda è spesso e ha vasi sanguigni all'interno, che possono causare sanguinamento durante il processo di perforazione. Deve essere preparata un'adeguata schiuma di gel per fermare l'emorragia. In secondo luogo, c'è una buona probabilità di angioressi quando si rimuove l'osso appena sopra il seno trasverso. Per la risoluzione dei problemi, un approccio alternativo con...
Divulgazioni
Gli autori non hanno nulla da rivelare.
Riconoscimenti
Questo lavoro è sostenuto dalla National Natural Science Foundation of China (32271060). Y.-t.L. progettò la ricerca, eseguì l'esperimento, analizzò i dati e scrisse il manoscritto. Z.L. e R.W. eseguirono l'esperimento.
Materiali
| Name | Company | Catalog Number | Comments |
| 16x objective | Nikon | ||
| 50-mm lens | Computar | M5018-MP2 | |
| 5-mm coverslip | Warner instruments | CS-5R | |
| bandpass filter | Chroma Technology | HQ575/250 m-2p | |
| butyl cyanoacrylate | Vetbond, World Precision Instruments | ||
| camera for monitoring pupil | FLIR | BFS-U3-04S2M-CS | |
| camera for widefield imaging | Basler | acA2000-165µm | |
| corona treater | Electro-Technic Products | BD-20AC | |
| dichroic | Chroma Technology | T600/200dcrb | |
| galvanometers | Cambridge Technology | ||
| glass bead sterilizer | RWD | RS1502 | |
| microdrill | RWD | 78001 | |
| micromanipulator | Sutter Instruments | QUAD | |
| photomultiplier tube | Hamamatsu | R3896 | |
| rotory encoder | USdigital | MA3-A10-125-N | |
| self-curing dental adhesive resin cement | SuperBond C&B, Sun Medical Co, Ltd. Moriyama, Japan | ||
| thermostatic heating pad | RWD | 69020 | |
| Ti:Sapphire laser | Spectra-Physics | Mai Tai HP DeepSee | |
| translucent silicone adhesive | Kwik-Sil, World Precision Instruments | ||
| treadmill | Xinglin Biology | ||
| Virus Strains | |||
| rAAV2/9-hsyn-Gcamp6m | Vector Core at Chinese Institute for Brain Research, Beijing | ||
| Animals | |||
| C57BL/6J wild type | Laboratory Animal Resource Center at Chinese Institute for Brain Research, Beijing | ||
| Emx1-Cre | The Jackson Laboratory | 5628 | |
| Pals1flox/wt | Christopher A. Walsh Lab | ||
| Software | |||
| ImageJ | NIH Image | ||
| Labview | National Instruments | ||
| MATLAB | Mathworks |
Riferimenti
- May, P. J. The mammalian superior colliculus: laminar structure and connections. Progress in Brain Research. 151, 321-378 (2006).
- Denk, W., Strickler, J. H., Webb, W. W. Two-photon laser scanning fluorescence microscopy. Science. 248 (4951), 73-76 (1990).
- Ohki, K., Chung, S., Ch'ng, Y. H., Kara, P., Reid, R. C. Functional imaging with cellular resolution reveals precise micro-architecture in visual cortex. Nature. 433 (7026), 597-603 (2005).
- Ratzlaff, E. H., Grinvald, A. A tandem-lens epifluorescence macroscope: Hundred-fold brightness advantage for wide-field imaging. Journal of Neuroscience Methods. 36 (2-3), 127-137 (1991).
- de Vries, S. E. J., et al. A large-scale standardized physiological survey reveals functional organization of the mouse visual cortex. Nature Neuroscience. 23 (1), 138-151 (2020).
- Mrsic-Flogel, T. D., et al. Altered map of visual space in the superior colliculus of mice lacking early retinal waves. The Journal of Neuroscience. 25 (29), 6921-6928 (2005).
- Cang, J., Wang, L., Stryker, M. P., Feldheim, D. A. Roles of ephrin-as and structured activity in the development of functional maps in the superior colliculus. The Journal of Neuroscience. 28 (43), 11015-11023 (2008).
- Feinberg, E. H., Meister, M. Orientation columns in the mouse superior colliculus. Nature. 519 (7542), 229-232 (2015).
- Ahmadlou, M., Heimel, J. A. Preference for concentric orientations in the mouse superior colliculus. Nature Communications. 6, 6773 (2015).
- de Malmazet, D., Kühn, N. K., Farrow, K. Retinotopic separation of nasal and temporal motion selectivity in the mouse superior colliculus. Current Biology. 28 (18), 2961-2969 (2018).
- Li, Y. T., Turan, Z., Meister, M. Functional architecture of motion direction in the mouse superior colliculus. Current Biology. 30 (17), 3304-3315 (2020).
- Gribizis, A., et al. Visual cortex gains independence from peripheral drive before eye opening. Neuron. 104 (4), 711-723 (2019).
- Inayat, S., et al. Neurons in the most superficial lamina of the mouse superior colliculus are highly selective for stimulus direction. The Journal of Neuroscience. 35 (20), 7992-8003 (2015).
- Barchini, J., Shi, X., Chen, H., Cang, J. Bidirectional encoding of motion contrast in the mouse superior colliculus. eLife. 7, 35261 (2018).
- Savier, E. L., Chen, H., Cang, J. Effects of locomotion on visual responses in the mouse superior colliculus. The Journal of Neuroscience. 39 (47), 9360-9368 (2019).
- Schröder, S., et al. Arousal modulates retinal output. Neuron. 107 (3), 487-495 (2020).
- Ge, X., et al. Retinal waves prime visual motion detection by simulating future optic flow. Science. 373 (6553), (2021).
- Chen, H., Savier, E. L., DePiero, V. J., Cang, J. Lack of evidence for stereotypical direction columns in the mouse superior colliculus. The Journal of Neuroscience. 41 (3), 461-473 (2021).
- Kasai, M., Isa, T. Effects of light isoflurane anesthesia on organization of direction and orientation selectivity in the superficial layer of the mouse superior colliculus. The Journal of Neuroscience. 42 (4), 619-630 (2022).
- Kim, S., et al. The apical complex couples cell fate and cell survival to cerebral cortical development. Neuron. 66 (1), 69-84 (2010).
- Kaifosh, P., Zaremba, J. D., Danielson, N. B., Losonczy, A. S. I. M. A. Python software for analysis of dynamic fluorescence imaging data. Frontiers in Neuroinformatics. 8, 80 (2014).
- Pnevmatikakis, E. A., Giovannucci, A. NoRMCorre: An online algorithm for piecewise rigid motion correction of calcium imaging data. Journal of Neuroscience Methods. 291, 83-94 (2017).
- Kerlin, A. M., Andermann, M. L., Berezovskii, V. K., Reid, R. C. Broadly tuned response properties of diverse inhibitory neuron subtypes in mouse visual cortex. Neuron. 67 (5), 858-871 (2010).
- Göbel, W., Helmchen, F. In vivo calcium imaging of neural network function. Physiology. 22 (6), 358-365 (2007).
- Dombeck, D. A., Khabbaz, A. N., Collman, F., Adelman, T. L., Tank, D. W. Imaging large-scale neural activity with cellular resolution in awake, mobile mice. Neuron. 56 (1), 43-57 (2007).
- Evans, D. A., et al. A synaptic threshold mechanism for computing escape decisions. Nature. 558 (7711), 590-594 (2018).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon