Uso do Cérebro de Embriões de Pintinhos como Modelo para Análises In Vivo e Ex Vivo do Comportamento Celular de Glioblastoma Humano
Neste Artigo
Resumo
Embriões de pintinhos são usados para estudar tumores cerebrais de glioblastoma humano (GBM) em co-culturas de ovo e de fatias cerebrais ex vivo . O comportamento das células GBM pode ser registrado por microscopia de lapso de tempo em co-culturas ex vivo , e ambas as preparações podem ser analisadas no desfecho experimental por análise confocal 3D detalhada.
Resumo
O embrião de pintinho tem sido um sistema modelo ideal para o estudo do desenvolvimento de vertebrados, particularmente para manipulações experimentais. O uso do embrião de pintinho foi estendido para estudar a formação de tumores cerebrais de glioblastoma humano (GBM) in vivo e a invasividade de células tumorais no tecido cerebral circundante. Os tumores GBM podem ser formados pela injeção de uma suspensão de células fluorescentemente marcadas no ventrículo mesencéfalo (tecto óptico) E5 em ovo.
Dependendo das células GBM, tumores compactos se formam aleatoriamente no ventrículo e dentro da parede cerebral, e grupos de células invadem o tecido da parede cerebral. Cortes de tecido espesso (350 μm) de tecta E15 fixa com tumores podem ser imunomarcados para revelar que as células invasoras frequentemente migram ao longo dos vasos sanguíneos quando analisadas pela reconstrução 3D de imagens confocais z-stack. Cortes vivos de mesencéfalo e prosencéfalo E15 (250-350 μm) podem ser cultivados em inserções de membrana, onde células GBM marcadas fluorescentemente podem ser introduzidas em locais não aleatórios para fornecer co-culturas ex vivo para analisar a invasão celular, que também pode ocorrer ao longo dos vasos sanguíneos, durante um período de cerca de 1 semana. Essas coculturas ex vivo podem ser monitoradas por microscopia de lapso de tempo de fluorescência confocal ou de campo largo para observar o comportamento de células vivas.
Os cortes co-cultivados podem então ser fixados, imunomarcados e analisados por microscopia confocal para determinar se a invasão ocorreu ou não ao longo dos vasos sanguíneos ou axônios. Além disso, o sistema de co-cultura pode ser usado para investigar potenciais interações célula-célula, colocando agregados de diferentes tipos e cores celulares em diferentes locais precisos e observando os movimentos celulares. Os tratamentos medicamentosos podem ser realizados em culturas ex vivo , enquanto esses tratamentos não são compatíveis com o sistema in ovo . Essas duas abordagens complementares permitem análises detalhadas e precisas do comportamento de células GBM humanas e da formação de tumores em um ambiente cerebral de vertebrados altamente manipulável.
Introdução
Estudos in vitro do comportamento de células cancerosas são frequentemente utilizados para dissecar potenciais mecanismos que operam durante o comportamento mais complexo que é observado durante a formação tumoral e invasão celular em modelos de xenoenxerto in vivo. Por exemplo, com glioblastoma (GBM), estudos in vitro descobriram mecanismos de como a L1CAM potencialmente opera durante a formação de tumor e invasão cerebral em um novo modelo de tumor cerebral de xenoenxerto de embrião de pintinho1,2,3,4,5. Embora os experimentos in vitro e in vivo se complementem de maneiras úteis, eles deixam uma lacuna substancial em como os resultados podem ser correlacionados. Por exemplo, análises mecanísticas da motilidade celular do GBM em uma placa é uma situação altamente artificial, e modelos in vivo de xenoenxerto só podem revelar análises estáticas de ponto de tempo ou ponto final da formação tumoral e comportamento celular. Estudos in vivo com roedores ou embriões de pintinhos não se prestam facilmente ao monitoramento do comportamento celular enquanto as células invadem o tecido cerebral nesses modelos de xenoenxerto. No entanto, o modelo de xenoenxerto de embrião de pintinho demonstrou que a proteína de adesão L1CAM desempenha um papel estimulatório na capacidade invasiva de células T98G GBM humanas 2,5.
Uma solução adequada para este problema pode ser alcançada através da ponte entre os métodos in vivo e in vitro usando um modelo organotípico de cultura de fatias cerebrais, referido como um modelo ex vivo . Neste modelo ex vivo, o tecido cerebral vivo pode ser mantido a uma espessura de várias centenas de mícrons por até algumas semanas, tornando possível implantar células cancerosas, observar seu comportamento no tecido real ao longo do tempo e, em seguida, realizar uma análise mais detalhada do marcador no final do experimento.
Um método popular de cultura organotípica de fatias tem sido cultivar uma fatia cerebral de várias centenas de mícrons de espessura em cima de uma membrana porosa translúcida ou transparente, deixando o tecido exposto ao ar, mas permitindo que os meios nutritivos sustentem o tecido abaixo da membrana (ver Stoppini et al.6). Diferentes variações deste método têm sido utilizadas para diferentes estudos, incluindo o uso de diferentes meios ou diferentes insertos de membrana. Diferentes inserções de membrana incluem uma inserção de membrana porosa (0,4 μm) de 30 mm de diâmetro em uma placa de cultura de 35 mm 6 e pastilhas de cultura celular (0,4 μm) para placasde 6 poços7. Diferentes meios incluem 50% de MEM/HEPES + 25% de soro de cavalo inativado pelo calor + 25% de solução salina balanceada de Hanks (HBSS)8, 50% de meios séricos reduzidos + 25% de soro de cavalo + 25% de HBSS9, entre outros. Se uma membrana translúcida ou transparente for usada juntamente com células GBM marcadas fluorescentemente, essas culturas podem ser obtidas por baixo usando um microscópio de campo largo invertido ou de fluorescência confocal 10,11,12,13,14,15.
Enquanto muitos modelos in vivo de xenoenxerto de tumor cerebral ortotópico e cultura de fatias cerebrais organotípicas ex vivo foram estabelecidos usando roedores, como citado acima, o embrião de pintinho (Gallus gallus) tem sido subutilizado para esses fins. No entanto, o embrião de pintinho tem se mostrado capaz de ser utilizado como modelo de xenoenxerto ortotópico in vivo para o estudo da invasão de glioma humano e de rato 1,2,5. Células xenoenxertadas em cérebros de embriões de pintinhos exibiram padrões de invasão semelhantes aos observados em modelos de roedores, apoiando ainda mais o uso de embriões de pintinhos como um modelo in vivo para análise de células tumorais de GBM. Os embriões de pintinhos também são baratos, podem ser mais facilmente mantidos do que os roedores (ou seja, em suas cascas de ovos em uma incubadora de laboratório) e são muito mais fáceis de trabalhar, tornando-os uma opção atraente para estudos in vivo de GBM de curto prazo. Um artigo recente descreveu o uso de culturas de fatias cerebrais de embriões de pintinhos para a formação e crescimento de axônios durante o desenvolvimento normal do cérebro, onde os cortes foram viáveis por pelo menos 7 dias16. No entanto, o uso dessas culturas de fatias cerebrais de embriões de pintinhos para análise ex vivo do comportamento de células GBM em um ambiente tecidual é escasso. Neste artigo, tanto o transplante de células GBM humanas quanto de células-tronco GBM (GSCs) no cérebro de embriões de pintinhos in vivo, bem como a introdução de células GBM em culturas de fatias cerebrais de embriões de pintinhos vivos ex vivo, são descritos. Alguns exemplos representativos dos tumores resultantes e padrões de invasão celular obtidos a partir dessas preparações também são fornecidos.
Protocolo
Nenhuma autorização ou aprovação foi necessária na Universidade de Delaware para realizar este trabalho.
1. Injeção de células GBM no tecto óptico de pintinhos
- Preparação de GSCs e células GBM para injeção
- GSCs de cultura em meios GSC (Tabela 1). A cultura estabeleceu linhagens celulares de GBM em meios GBM (Tabela 1).
- Enxaguar as células em placas com solução salina estéril tamponada com fosfato (PBS) e colocar 1 mL de solução de tripsina em uma placa de 10 cm. Deixe em uma incubadora de cultura celular por 2-3 min até que as células comecem a se destacar.
- Inative a tripsina adicionando 10 mL de meio de cultura apropriado contendo soro na placa de 10 cm e desprenda as células pipetando para cima e para baixo. Colocar a suspensão celular num tubo de centrífuga cónica de 15 ml.
- Pellet as células por centrifugação a 800 × g durante 5 min a 4 °C.
- Aspirar o meio do pellet de célula usando uma pipeta de vidro fino descartável conectada a um frasco de braço lateral e bomba de vácuo. Ressuspenda as células em meios de crescimento apropriados até uma concentração de 10.000 células por microlitro e coloque em um tubo de microfuga ou pequeno tubo de rosca sobre gelo.
- Misture as células com uma pequena quantidade de corante FCF Fast Green estéril a 1% (use uma proporção de 5 μL de corante/100 μL de suspensão celular).
- Injeção de células GBM no tecto óptico E5 em ovo. Ver Figura Suplementar 1.
- Incubar os ovos de galinha fertilizados em incubadora de ovos umedificada, com a extremidade pontiaguda virada para baixo, a 37,5 °C (o 1º dia de incubação é embrionário dia 0 [E0]). No 6º dia de incubação (E5), esterilizar a casca do ovo por pulverização com etanol 70%.
- Usando um veleiro de ovo, trace ao longo do perímetro do espaço aéreo acima do embrião com um lápis e cubra a área delineada com fita transparente.
- Usando tesoura curva, corte suavemente ao redor da área traçada, tomando cuidado para não cortar as membranas embrionárias ou vasos sanguíneos, e descarte a parte superior da casca do ovo.
- Coloque algumas gotas de soro fisiológico ou meio de cultura celular na membrana do espaço aéreo para molhá-la para que ela se desprenda facilmente. Usando pinças finas, perfure cuidadosamente a membrana do espaço aéreo sobre a parte superior do embrião, remova-o e localize a cabeça do embrião do pintinho.
- Use pinças finas para agarrar a membrana de âmnio transparente que envolve imediatamente o embrião para posicionar a cabeça de modo que o tecto óptico possa ser injetado com células. Com uma mão, use a pinça fina para segurar o âmnio para manter a cabeça no lugar durante o processo de injeção. Tenha cuidado para não danificar os vasos sanguíneos extraembrionários na membrana corioalantóide na gema.
NOTA: O procedimento acima requer alguma prática para ser capaz de agarrar eficientemente a membrana de âmnio transparente que envolve intimamente o embrião, uma vez que é invisível até ser agarrado e puxado. Pratique o uso de pinças finas para agarrar o âmnio transparente que envolve imediatamente o embrião. - Mantenha a cabeça firme segurando a membrana de âmnio com pinças finas. Usando uma micropipeta de vidro e uma picobomba pneumática, injete cerca de 50.000 células em 5 μL de meio de cultura celular adequado no tecto óptico (5 μL é aproximadamente 1/2 de uma micropipeta preenchida).
NOTA: Ver Cretu et al.1 para uma imagem de um embrião E5 que foi injetado com células GBM misturadas com corante. - Coloque algumas gotas de 50 mg/mL de ampicilina sobre o embrião.
- Cubra o orifício na parte superior dos ovos com fita adesiva transparente e deixe no umidificador até E15 para dissecção.
2. Dissecção de regiões cerebrais de embriões E15
NOTA: A dissecção de cérebros E15 aqui para fixação é semelhante à descrita na etapa 8.2 para cortes de cérebro vivo, mas a dissecção aqui não precisa ser feita em condições assépticas.
- Corte a fita ao redor da parte superior da concha, permitindo o acesso ao embrião.
- Decapitar o embrião no pescoço e colocar a cabeça em um prato de 10 cm com solução estéril de Tyrodes livre de cálcio e magnésio (CMF Tyrode's). Ver Figura Suplementar 2.
- Usando pinças finas, descasque a pele que cobre o cérebro para revelar a dura-máter subjacente. Remova os ossos do crânio em formação nos lados esquerdo e direito do cérebro. Os ossos do crânio em formação ainda não cobrem a maior parte do cérebro.
- Use suavemente pinças pontiagudas finas para rasgar as meninges que cobrem o centro do cérebro e descasque-as para cada lado para descobrir o cérebro.
- Use pinças curvas para colher o cérebro de baixo e retirá-lo suavemente de sua cavidade.
- Dissecção o cérebro em suas partes: prosencéfalo, tecta, cerebelo.
- Remova a pia-máter sobrejacente da tecta usando pinças finas. Note que a pia se separa facilmente da tecta, mas não do prosencéfalo ou cerebelo. Remova a pia do prosencéfalo tocando-a ou enrolando-a em um pequeno pedaço de papel de filtro.
- Coloque as regiões cerebrais dissecadas em um prato pequeno.
- Colocar as regiões cerebrais para fixação em um poço de placa de 24 poços e fixar em paraformaldeído (PFA) a 2% em tampão cacodilato de sódio 0,1 M. Deixar durante pelo menos 24 h a 4 °C.
- Após a fixação, enxaguar o tecido em PBS 3x por pelo menos 1 hora antes de incorporar em ágar.
3. Incorporar e fatiar regiões cerebrais colhidas
- Pré-aquecer uma solução de ágar 3,5% e sacarose a 8% em PBS até derreter e mantê-la em temperatura de fusão.
- Usando pinças curvas como uma colher, pegue suavemente o tecto óptico ou a região do prosencéfalo do cérebro do embrião de pintinho e borre levemente em papel de filtro para remover o líquido extra para garantir a adesão do ágar à superfície externa do cérebro.
- Usando uma pipeta de transferência estéril, encha o molde com solução de ágar.
NOTA: Um molde simples pode ser feito formando folha de alumínio em torno de um objeto de tamanho adequado, como pequenos blocos de corte de tecido vibratório retangular de metal. - Coloque a região do cérebro em ágar e deixe o ágar solidificar completamente.
- Remova a folha de alumínio ao redor do cérebro embutido e corte o excesso de ágar ao redor das laterais usando uma lâmina de barbear ou bisturi.
- Coloque uma gota de cola de cianoacrilato no quadrado de aço inoxidável da bandeja de fatiamento, coloque o bloco de agarose com o cérebro sobre a cola e deixe a cola grudar por 1 min. Coloque a bandeja no corte de tecido vibratório, aperte e encha a bandeja com PBS suficiente para cobrir a parte superior do bloco de ágar.
- Corte as fatias cerebrais em um cortador de tecido vibratório a uma espessura de 350 μm usando uma lâmina de barbear de aço.
- Como as fatias de cérebro são cortadas e flutuam livremente na bandeja de fatiamento, use uma espátula para colher e remover as fatias da bandeja. Deslize suavemente a seção para fora da espátula e para uma placa de Petri rotulada de 10 cm com PBS para que as seções flutuem livremente.
NOTA: O ágar que envolve a fatia cerebral pode se desprender se o cérebro não estiver suficientemente manchado com papel de filtro para remover o excesso de líquido antes de incorporar. Se isso ocorrer, o tecido cerebral pode ser suavemente removido do ágar solidificado e reincorporado após a mancha adequada do excesso de líquido.
4. Imunomarcação de fatias cerebrais com células tumorais
- Usando um microscópio estéreo equipado com epifluorescência, tria cortes individuais na placa de 10 cm, um a um, para a presença ou ausência de células tumorais.
- Preparar uma quantidade suficiente de solução salina tamponada com fosfato com Triton X-100 a 0,1% e soro normal de cabra a 5% (PBSTG) (ver Tabela 1) para imunomarcação e enxaguar as fatias a serem imunomarcadas.
- Poços de enchimento pela metade em uma placa de 24 poços que será usada para colorir seções cerebrais com PBS.
- Corte os cantos de ágar ao redor das fatias cerebrais com a borda de uma espátula ou um bisturi e coloque-os suavemente nos poços contendo PBS.
- Aspirar o PBS e substituir por 350 μL de solução de coloração de anticorpos primários em PBSTG (por exemplo, 2 μg/mL UJ127 em PBSTG).
- Incubar por 24 h em uma câmara fria com agitação suave para que a fatia se mova livremente dentro do poço.
- Após 24 h, remover a solução de anticorpos primários e enxaguar 3 x 1 h com PBSTG em uma câmara fria com agitação.
- Quando terminar o enxágue, incubar em 350 μL/poço de solução corante de anticorpos secundários em PBSTG (por exemplo, diluição de 1/200 de biotina-GAM em PBSTG). Incubar por 20 h em câmara fria com agitação.
NOTA: Se preceder o passo terciário e incubar com o anticorpo secundário contendo fluorocromo nesta etapa, cubra para proteger da luz durante a incubação agora e, em seguida, pule para a etapa 4.11. - Remova a solução de anticorpos secundários e lave 3 x 1 h em PBSTG em uma câmara fria com agitação.
- Remova o PBSTG e incube na solução terciária (por exemplo, diluição de 1:250 de estreptavidina Alexa Fluor 647 em PBSTG). Se desejado, corar os núcleos nesta etapa, adicionando 0,1 μg/mL de bisbenzimida à mistura. Incubar por 20 h em câmara fria com agitação.
- Retire a solução terciária e enxágue 3 x 1 h em PBSTG em uma câmara fria com agitação.
- Deixe em PBS até que esteja pronto para montar em lâminas de microscópio.
5. Montagem de fatias em lâminas de microscópio
- Prepare tantas lâminas de microscópio quantas forem as seções para montar.
- Para cada lâmina, coloque uma tira de 50 mm de comprimento de fita elétrica de vinil de 10 mil (254 μm) de espessura em um pedaço de parafilme.
- Usando um furo quadrado de 1 cm x 1 cm, perfure um orifício através do centro da fita elétrica e parafilme.
- Retire a fita do parafilme e coloque-a em cima da lâmina do microscópio, deixando espaço para a fita de marcação na lâmina.
- Usando uma micropipeta, coloque uma ou duas gotas de mídia de montagem anti-fade no orifício quadrado no centro da fita elétrica.
- Use uma espátula curva para levantar a seção de fatiamento de tecido vibratório desejada do PBSTG e elimine completamente a umidade com um lenço de laboratório limpo ou um pedaço de papel de filtro.
- Toque a borda da fatia até a gota do montador e use outra espátula para deslizar suavemente a seção para a mídia de montagem.
- Cubra a seção com mais algumas gotas de montador e coloque cuidadosamente uma tampa de 24 mm x 30 mm (espessura #1,5) sobre a seção e o suporte.
- Sele as bordas da tampa com esmalte para mantê-la no lugar.
6. Microscopia confocal de cortes cerebrais fixos
- Use fluorescência de campo largo para encontrar tumores fluorescentes na fatia cerebral montada usando a lente objetiva apropriada e conjunto(s) de filtro(s).
NOTA: Alguns tumores podem ser muito grandes e são facilmente visíveis com a objetiva de 4x, enquanto células únicas podem exigir a objetiva de 10x. - Mude para a microscopia confocal usando uma lente objetiva apropriada, laser(s), tamanho do orifício e configurações do detector. Para seguir esse protocolo, use uma objetiva de 20x (abertura numérica [N.A.] = 0,75) para imagens de rotina e uma objetiva de óleo de 60x (N.A. = 1,40) para imagens de alta resolução.
- Definir limites superior e inferior do eixo z e tamanho do passo (para a situação específica de acordo com as instruções do fabricante do microscópio confocal) para aquisição de seções ópticas. Adquira uma pilha z de seções ópticas.
- Use o software do microscópio confocal para criar uma renderização de volume 3D do tumor, de acordo com as instruções do fabricante.
7. Preparação esferoide
- Criação de placas de poli(2-hidroxietil metacrilato) (poli-HEMA)
- Criar uma solução de 10 μg/mL de poli-HEMA em etanol 95% e revestir placas de Petri de 35 mm (ou placas de cultura celular) com 1 mL desta solução.
- Deixe os pratos assentarem em um balancim descoberto durante a noite à temperatura ambiente para desenvolver um revestimento da superfície do prato.
NOTA: O solvente evaporará e deixará um revestimento translúcido no prato, que pode parecer irregular, mas isso não afetará a capacidade de fazer esferoides celulares. - Após a secagem, esterilizar as louças abertas sob luz UV em um armário de biossegurança por 1 h. Substitua as tampas após a esterilização. Os pratos revestidos já estão prontos para uso.
- Coloração DiD fluorescente para microscopia time-lapse
NOTA: Esta seção é para colorir células individuais com corante fluorescente DiD a ser usado para fazer esferoides, o que otimiza a visualização da motilidade celular para imagens de lapso de tempo ao vivo.- Suspender as células em meio de cultura sem soro.
- Adicionar 5 μL de DiD stock/mL de suspensão celular e misturar suavemente por pipetagem. Incubar durante 20 min a 37 °C.
- Centrifugar a suspensão de células marcadas a 800 × g a 5 °C durante 5 min.
- Aspirar o sobrenadante e ressuspender as células em meio quente para enxaguar.
- Repita esta centrifugação e enxágue mais duas vezes.
NOTA: Se desejar, pule para a etapa 7.3.6 para fazer esferoides imediatamente após esse processo.
- Fazendo esferoides celulares
- Aquecer a solução de tripsina/ácido etilenodiaminotetracético (EDTA) a 0,25% a 37 °C.
- GSCs de cultura em meio GSC17 (Tabela 1) e células de gloima maligno U-118 (MG) em meio de cultura U-118 (ver Tabela 1). Use uma placa confluente de 10 cm para a preparação de uma placa de 35 mm de esferoides. Adicionar fatores de crescimento bFGF (concentração final de 10 ng/mL) e TGF-α (concentração final de 20 ng/mL) às GSCs inicialmente e depois a cada 3 dias.
NOTA: As células usadas no presente estudo foram GSC15-2/K72 verde, GSC16-4/K72 verde, U-118/L1LE/mCherry2x vermelha e U-118/1879/mCherry2x vermelha. Uma placa de esferoides deve ser suficiente para duas placas de 6 poços de fatias cerebrais em inserções de membrana. - Enxaguar as células nas placas com PBS estéril e colocar 1 mL de solução de tripsina em uma placa de 10 cm. Coloque na incubadora de cultura celular por 2-3 min até que as células comecem a se desprender.
- Inative a tripsina adicionando 10 mL de meio de cultura apropriado contendo soro na placa de 10 cm e desprenda as células pipetando para cima e para baixo. Colocar a suspensão celular num tubo de centrífuga cónica de 15 ml.
- Pellet as células por centrifugação a 800 × g durante 5 min a 4 °C.
- Aspirar o meio do pellet celular e ressuspender as células em 10 mL de meio.
- Colocar 2 mL de suspensão celular em cada prato revestido com poli-HEMA de 35 mm e adicionar mais 2 mL de meio apropriado para obter 4 mL de meio total por prato. Se estiver usando GSCs, adicione fatores de crescimento.
- Incubar as células em uma incubadora celular até que os agregados atinjam um tamanho de 100-200 μm, o que pode ser de 1-2 dias, dependendo da densidade das células que foram plaqueadas.
8. Dissecção cerebral de embrião de pintinho vivo e fatiamento de fatiamento de tecido vibratório
- Preparação para dissecção
- Prepare uma placa de inserção de membrana de poliéster de 6 poços com 1 mL de meio de cultura de corte cerebral (ver Tabela 1) abaixo da inserção da membrana.
- Esterilizar a área de trabalho e as ferramentas com etanol 70%.
- Coloque a placa de inserção de 6 poços no gelo enquanto a dissecção está ocorrendo.
- Preparar 100 mL de fatiamento de tecido vibratório (Tabela 1) e colocar no gelo.
- Coloque um frasco para injetáveis de agarose de baixo derretimento a 4% em PBS em banho-maria até derreter num líquido (aproximadamente 50 °C).
- Encha a cuba de corte de tecido vibratório com gelo.
- Dissecção asséptica do cérebro do embrião de pintinho E14/15
- Usando um veleiro de ovo, trace ao longo do perímetro da bolsa de ar acima do embrião E14 ou E15 com um lápis e cubra a área delineada com fita transparente.
- Usando tesoura curva ou fina, corte suavemente ao redor da área traçada, tomando cuidado para não cortar a membrana do embrião ou vasos sanguíneos, e descarte o pedaço superior da casca.
- Usando pinças curvas, remova a membrana do espaço aéreo sobre a parte superior do embrião e localize a cabeça do embrião do pintinho.
- Decapitar o embrião e colocar a cabeça em uma placa de 10 cm com solução fria estéril de CMF. Ver Figura Suplementar 2.
- Usando pinças finas estéreis, descasque a pele que cobre o cérebro para revelar a dura-máter subjacente. Remova os ossos do crânio em formação nos lados esquerdo e direito do cérebro. Os ossos do crânio em formação ainda não cobrem a maior parte do cérebro.
- Use suavemente pinças pontiagudas finas (#5 ou #55) para rasgar as meninges que cobrem o centro do cérebro e descascá-las para cada lado para descobrir o cérebro.
- Usando pinças curvas finas, pegue o cérebro da frente inferior e puxe-o suavemente para fora de sua cavidade.
- Dissecção o cérebro em suas três partes principais: prosencéfalo, mesencéfalo (tecta óptica), cerebelo. Consulte um atlas de desenvolvimento de pintinhos, se necessário.
- Remova a pia-máter sobrejacente da tecta usando pinças finas.
NOTA: A pia separa-se facilmente da tecta, mas não do prosencéfalo ou cerebelo. A pia pode ser removida do prosencéfalo tocando-o ou enrolando-o em gaze estéril. - Coloque as regiões cerebrais dissecadas em uma pequena placa estéril sobre gelo.
- Incorporar e fatiar o cérebro
- Usando pinças curvas como uma colher, pegue suavemente o tecto óptico ou a região do prosencéfalo e borre levemente em gaze estéril para remover líquido extra para garantir a adesão da agarose à superfície externa do cérebro.
- Usando uma pipeta de transferência estéril, encha o molde com agarose de baixo derretimento. Prepare um molde simples formando papel alumínio em torno de um objeto de tamanho adequado. O pequeno bloco de corte de tecido vibratório retangular de metal é rotineiramente usado como objeto. Ver Figura Suplementar 3.
- Coloque rapidamente a região do cérebro em agarose e deixe-a solidificar (aproximadamente 4-5 min) no gelo.
NOTA: O cérebro pode afundar no fundo do molde antes que a agarose endureça. Se isso ocorrer, aguarde 1 min para deixar o ágar começar a se definir e, em seguida, coloque a região do cérebro na agarose. Tente suspender a região do cérebro diretamente no meio da agarose. - Remova a folha de alumínio ao redor do cérebro embutido na agarose solidificada e corte o excesso de agarose ao redor das laterais usando uma lâmina de barbear estéril ou bisturi.
- Coloque uma gota de cola de cianoacrilato no quadrado de aço inoxidável da placa/bandeja de fatiamento, coloque o bloco de agarose com o cérebro e deixe a cola grudar por 1 min. Coloque o prato/bandeja no corte de tecido vibratório, aperte e encha a bandeja com meio de corte para cobrir a parte superior do bloco de agarose.
- Corte as seções em um cortador de tecido vibratório a 250-350 μm usando uma faca de safira, que foi relatado para resultar em menos danos ao tecido vivo do que uma lâmina de barbear de aço.
- Como as fatias de cérebro são cortadas e flutuam livremente na bandeja de fatiamento, use uma espátula estéril para colher e remover a fatia da bandeja. Deslize suavemente a secção para fora da espátula e para uma inserção de membrana utilizando outra espátula estéril.
NOTA: Normalmente, duas ou três fatias cerebrais podem ser colocadas em cada inserção de membrana, se desejado. A agarose que envolve a fatia cerebral pode se desprender se o cérebro não estiver suficientemente manchado com gaze estéril para remover o excesso de líquido. Se isso ainda ocorrer após uma mancha suficiente antes de incorporar, pegue suavemente a fatia sem a agarose circundante e deslize-a para a inserção da membrana. - Coloque a placa de 6 poços de fatias cerebrais em inserções de membrana na incubadora de cultura celular a 37 °C e 5% de CO2.
- No dia seguinte ao revestimento, use uma pipeta Pasteur estéril para aspirar o meio por baixo da pastilha (há lacunas nas laterais das pastilhas para permitir que uma pipeta tenha acesso à mídia abaixo). Adicionar 1 ml de meio de fatia fresco a cada poço por baixo da inserção da membrana. Continue a mudar de mídia a cada dois dias depois disso.
- Espere alguns dias para que as fatias cerebrais se fixem firmemente às inserções da membrana e pareçam achatar um pouco. Este é um sinal de que as fatias são viáveis e prontas para a introdução de células GBM.
9. Introdução de células GBM em fatias cerebrais
- Método esferoide
- Depois que os esferoides celulares atingirem 150-200 μm de tamanho, use uma micropipeta de 20 μL ajustada para 5 μL para remover um a vários esferoides de sua placa de cultura. Ver Figura Suplementar 3.
- Expulse suavemente o meio com esferoides na fatia cerebral desejada.
NOTA: Os esferoides celulares devem estar visíveis na ponta da pipeta. Usar uma ponta de pipeta clara irá torná-los mais fáceis de ver na ponta. Se o esferoide cair da fatia cerebral quando o líquido for liberado, um cílio esterilizado por etanol colado a um bastão aplicador de madeira fino deve ser usado para empurrar suavemente o esferoide de volta para a fatia cerebral. - Deixe os esferoides para cultura nas fatias do cérebro por 2-5 dias.
NOTA: A limitação aqui parece ser a eventual degradação dos vasos sanguíneos e células cerebrais na fatia. Vasos sanguíneos degradados aparecerão como bolas descontínuas no corte quando corados para laminina.
- Método de punção de biópsia
- Permita que as fatias cerebrais se fixem, parecendo achatar na inserção da membrana (pode levar 2-5 dias em cultura).
- Descongelar a matriz celular no gelo.
- No gabinete de biossegurança da cultura celular, conecte um punch de biópsia estéril de 1 mm de diâmetro a um tubo aspirador a vácuo.
- Toque suavemente a fatia cerebral com o punch de biópsia para criar um orifício de 1 mm no centro da fatia cerebral.
OBS: O tecido no punch da biópsia será aspirado para dentro do punch pelo vácuo. - Preparar uma suspensão de matriz celular tripsinizando uma placa de células confluente de 10 cm a 60%-70% e ressuspendendo em 10 mL de meio; em seguida, misturar 1 mL dessa suspensão com 100 μL de matriz.
- Usando uma micropipeta de 20 μL, coloque 1 μL da mistura de matriz celular em cada orifício nas fatias cerebrais.
- Depois que a colocação da mistura de células for concluída, coloque o prato de fatias cerebrais com células embutidas de volta na incubadora e permita que a matriz se solidifique e as células potencialmente invadam a fatia cerebral circundante.
10. Microscopia de lapso de tempo de fluorescência de campo largo
- Coloque fita removível ao redor da borda da placa de 6 poços para evitar a evaporação do meio, deixando uma pequena lacuna de um lado para a troca gasosa.
- Coloque as placas em uma câmara de cultura personalizada em um estágio automatizado ajustável em um microscópio de epifluorescência invertido.
NOTA: A câmara foi mantida em condições atmosféricas de 5% de CO2 e 95% de ar usando um controlador de injeção de gás, e a temperatura foi mantida em 37 °C com um controlador de temperatura de ar quente e uma inserção de estágio com temperatura controlada. Veja Fotos et al.18 para detalhes do sistema utilizado aqui. - Usando um software de controle de microscópio adequado, crie um cronograma de aquisição de lapso de tempo que colete imagens fluorescentes das áreas de interesse uma vez a cada 10 min por 20 h.
NOTA: Se uma etiqueta fluorescente verde for usada em células (por exemplo, proteína fluorescente verde [GFP]), use a quantidade mínima de luz de excitação azul necessária para visualizar as células para evitar a fototoxicidade. Os rótulos vermelho (por exemplo, mCherry) e vermelho distante (por exemplo, DiD) não parecem ter esse problema potencial devido à excitação de comprimento de onda mais longo.
11. Imunomarcação de fatias cerebrais após microscopia de lapso de tempo
NOTA: Este protocolo de imunomarcação é otimizado para coloração de vasos sanguíneos com laminina e núcleos com bisbenzimida. Use anticorpos apropriados para a(s) molécula(s) desejada(s) de interesse.
- Aspirar o meio por baixo da inserção da membrana com uma pipeta de Pasteur e colocar 1 ml de PFA a 2% em tampão cacodilato de sódio 0,1 M por baixo da pastilha e 1 ml por cima da pastilha para cobrir a fatia cerebral. Deixe as fatias fixarem durante a noite a 4 °C.
- Remova o fixador abaixo da inserção da membrana e qualquer fixador remanescente na fatia cerebral (o fixador tende a vazar através da inserção da membrana para o poço abaixo).
- Retire a pastilha com fatias do poço de 35 mm e coloque-as em um prato plástico maior.
- Prepare uma placa de 24 poços adicionando 350 μL de PBS em tantos poços quantos forem as fatias cerebrais (uma fatia/poço quando a imunomarcação).
- Usando uma espátula fina, remova suavemente a agarose ao redor da fatia cerebral sem desprender a fatia cerebral da inserção da membrana. Certifique-se de que a agarose se desprende da borda externa da fatia cerebral facilmente. Caso contrário, deixe a agarose presa à fatia cerebral.
- Usando um bisturi afiado, corte a membrana ao redor da fatia cerebral até que a fatia com a membrana subjacente esteja livre do resto da inserção. Pegue a membrana com a fatia cerebral anexada, usando pinças finas para agarrar a membrana, e coloque-a em um poço da placa de 24 poços em PBS.
- Enxágue as fatias 3x com PBS durante 1 h na câmara fria com agitação suave constante ou balanço, para que a fatia se mova dentro do poço.
- Ao enxaguar, prepare a solução primária de anticorpos.
- Diluir a antilaminina para 2 μg/mL em PBSTG (ver Tabela 1).
- Retire o PBS dos poços e incube durante a noite em solução primária de anticorpos em uma câmara fria com agitação suave.
- Após pelo menos 20 h de incubação, aspirar a solução de anticorpos primários e lavar as seções 3x por 1 h em PBSTG.
- Durante o enxágue, prepare a solução de anticorpos secundários.
- Diluir o GAM fluorescente com o fluorocromo específico necessário para uma diluição de 1:200 em PBSTG juntamente com uma concentração de 0,1 μg/mL de bisbenzimida.
- Remover PBSTG e incubar durante a noite em uma câmara fria com agitação na solução de anticorpos secundários fluorescentes.
- Remova o anticorpo secundário e lave 2x durante 1 h em PBSTG e 1x durante 1 h em PBS.
- Deixe em PBS até que esteja pronto para montar em lâminas de microscópio (seção 5) e visualizar.
Resultados
Apresentam-se aqui várias figuras para mostrar alguns resultados representativos obtidos com a realização de injeções in vivo no tecto óptico (Figura 1 e Figura 2), cultura de cortes cerebrais vivos e avaliação de sua viabilidade (Figura 3), criação de culturas de cortes cerebrais ex vivo e implantação de células marcadas fluorescentemente usando o método de punção de biópsia (Figura 4), geração de esferoides celulares por cultura de células em poli-HEMA (Figura 5 ), criando co-culturas de fatias cerebrais ex vivo com esferoides celulares e registrando o comportamento celular invasivo usando microscopia confocal de lapso de tempo 4D (Figura 6), e analisando o comportamento de células invasivas de esferoides em relação aos vasos sanguíneos em preparações de cortes cerebrais fixos (Figura 7 e Figura 8). Esses resultados não são de forma alguma exaustivos, mas fornecem bons exemplos do que pode ser obtido usando o cérebro de embrião de pintinho como um modelo de xenoenxerto para pesquisa de GBM humano.
A Figura 1 mostra alguns resultados representativos dos tumores que se formaram no tecto óptico in vivo após a injeção de GSCs expressando GFP. As GSCs se ligam à superfície ventricular e formam tumores invasivos na parede cerebral. Os GSCs residem claramente perto dos vasos sanguíneos e parecem estar migrando ao longo deles. Filmes de renderizações de volume 3D rotativo de fatias fixas e imunocoradas de tumores GSC in vivo são dados em Vídeo Suplementar S1, Vídeo Suplementar S2, Vídeo Suplementar S3 e Vídeo Suplementar S4. Neste experimento, quatro cores foram usadas para identificar cinco características (GSCs verdes, núcleos brancos, vasos sanguíneos brancos, integrina alfa-6 azul e Sox2 vermelho ou nestina vermelha).
A Figura 2 mostra alguns resultados representativos dos tumores que se formaram no tecto óptico in vivo após a injeção de GSCs expressando GFP misturada com células U-118/L1LE2 expressando mCherry devido à transdução de vetor retroviral. Esses experimentos revelaram que, como esses tumores se formavam a partir de uma suspensão de células mistas, a triagem ocorria de tal forma que as GSCs residiam na periferia ou no centro, enquanto as células U-118 compunham um núcleo interno ou um córtex externo, dependendo da linha específica de GSC.
A Figura 3 mostra os resultados de viabilidade das culturas de fatias cerebrais ex vivo . Após 1 semana em cultura, a fixação e imunomarcação para laminina revelaram muitos vasos sanguíneos intactos e a expressão de Sox2, ambos usados aqui para demonstrar a viabilidade do corte cerebral. Isso mostrou que fatias cerebrais de embriões de pintinhos podem ser cultivadas em inserções de membrana por aproximadamente 2 semanas e permanecem viáveis com vasos sanguíneos de aparência normal e expressão de fator de transcrição.
A Figura 4 mostra os resultados da introdução de "plugs" de células vermelhas U-118/L1LE/mCherry (misturadas com matriz) em cortes cerebrais ex vivo após a criação de cavidades nos cortes usando o método de punção de biópsia. As células U-118 invadiram claramente o tecido cerebral, às vezes extensivamente, e muitas vezes ao longo dos vasos sanguíneos. No entanto, a invasão celular não foi uniforme ao redor da circunferência das células introduzidas. Os vasos sanguíneos às vezes também pareciam danificados ou ausentes em certos cortes, presumivelmente devido ao trauma adicional do método de punção ou ao tempo de cultura. Isso mostrou que o método de punção/plugue celular de biópsia pode ser usado para introduzir células GBM em locais específicos em um corte de cérebro ex vivo cultivado, após o qual as células invadem o corte cerebral.
A Figura 5 mostra esferoides vivos em cultura e vários exemplos de fluorescência de campo largo de esferoides de células GBM vivas introduzidas em fatias cerebrais ex vivo para experimentos de lapso de tempo. Filmes de invasão celular dos esferoides para a fatia cerebral são dados em Vídeo Suplementar S5 e Vídeo Suplementar S6. Isso mostrou que os esferoides celulares são outro método bem-sucedido de introdução de células GBM ou GSCs em locais específicos de uma fatia cerebral ex vivo, e o comportamento celular invasivo pode ser monitorado por microscopia de fluorescência de campo largo, embora a resolução de células individuais possa ser pobre.
A Figura 6 mostra imagens estáticas de experimentos confocais de time-lapse de invasão de células GSC16-4/GFP e U-118/L1LE/mCherry em fatias cerebrais. Imagens confocais z-stack foram adquiridas a cada 10 min durante um período de 20 h em um experimento de lapso de tempo multiponto. Filmes de invasão celular dos esferoides em fatias cerebrais tomadas como pilhas z confocais ao longo do tempo são apresentados em Vídeo Suplementar S7, Vídeo Suplementar S8, Vídeo Suplementar S9, Vídeo Suplementar S10 e Vídeo Suplementar S11. Este experimento revelou que a imagem confocal de lapso de tempo foi superior à fluorescência de campo largo para rastrear o comportamento invasivo de células individuais. As células U-118/L1LE foram visivelmente mais invasivas do que as GSCs nessas condições. Isso é até aparente nas imagens estáticas, com os GSCs sendo localizados mais centralmente e as células U-118 mais dispersas.
A Figura 7 mostra vários exemplos de preparações ex vivo de fatias cerebrais/esferoides, onde dois diferentes esferoides marcados separadamente (esferoides U-118/L1LE/mCherry e esferoides GSC16-4/GFP) foram colocados em fatias cerebrais, cultivados por vários dias e, posteriormente, fixados, imunocorados para laminina e imageados por corte óptico em microscópio confocal. Isso revelou que ambos os tipos de células invadiram a fatia cerebral e viajaram ao longo dos vasos sanguíneos. Quando os diferentes tipos de esferoides estavam próximos o suficiente para entrar em contato uns com os outros, parecia haver pouca ou nenhuma invasão de um tipo celular no esferoide do outro tipo celular, e os esferoides permaneciam segregados.
A Figura 8 mostra vários exemplos de preparações ex vivo de fatias cerebrais/esferoides em que esferoides do tipo "células mistas" gerados em cultura usando dois tipos de células marcadas de forma diferente (U-118/L1LE/mCherry misturado com GSC16-4/GFP) foram colocados em fatias cerebrais, cultivados por vários dias e, posteriormente, fixados, imunocorados para laminina e imageados por corte óptico em microscópio confocal. Isso revelou que as células vermelhas U-118/L1LE/mCherry migraram para fora dos esferoides e se dispersaram muito mais evidentemente do que as células verdes GSC16-4/GFP, que tenderam a permanecer em aglomerados próximos ao centro dos esferoides. Adicionalmente, células U-118/L1LE/mCherry também foram coradas com DiD para que os dois rótulos separados (mCherry e DiD) pudessem ser comparados diretamente nas preparações fixas ex vivo . O rótulo DiD ainda podia ser detectado, mesmo em células únicas que haviam invadido a fatia cerebral; no entanto, tratava-se de punções intracelulares.
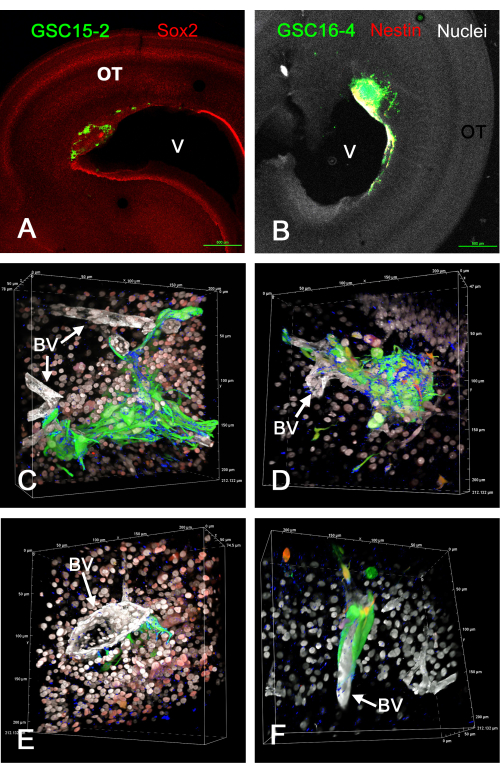
Figura 1: Tumores em E15 resultantes da injeção de GSCs no tecto óptico E5 in vivo. Os GSCs são verdes devido à expressão de GFP. As células GSC15-2 são mostradas nos painéis A, C e E, e as células GSC16-4 são mostradas nos painéis B, D e F. (A) Visão de baixa magnificação do tecto óptico com tumor próximo ao ventrículo (V). A coloração de Sox2 é mostrada em vermelho, que cora a maioria dos núcleos das células OT. (B) Imagem semelhante a A, mas com células GSC16-4 que também são coradas para nestina em vermelho, que pode aparecer amarelo ou branco na imagem devido à mistura de cores e exposição da imagem. Os núcleos OT aparecem brancos devido à contracoloração com bisbenzimida. (C-F) Diferentes perspectivas de renderizações de volume geradas a partir de z-stacks usando uma objetiva de imersão em óleo de 60x. Os núcleos celulares aparecem brancos devido à coloração de bisbenzimida, e alguns aparecem vermelhos nos painéis C e E devido à imunomarcação para Sox2. A coloração vermelha nos painéis D e F é proveniente da coloração para nestina. Note que devido ao "Alpha Blending" para renderizações de volume no software do microscópio confocal, as cores não se misturam como fariam usando uma projeção de intensidade máxima, e a cor mais prevalente predomina e obscurece a cor menos intensa. Os vasos sanguíneos são corados de branco devido à imunomarcação para laminina. A coloração de integrina alfa-6 do marcador GSC é mostrada em azul e aparece pontual nas superfícies de GSC. Escalas de mícrons são mostradas ao longo das bordas das renderizações de volume. Vídeos de rotações de renderizações de volume em painéis C-F são apresentados em Vídeo Suplementar S1, Vídeo Suplementar S2, Vídeo Suplementar S3 e Vídeo Suplementar S4. Barras de escala = 500 μm (A,B). Abreviações: GSCs = células-tronco de glioblastoma; OT = tecto óptico; GFP = proteína fluorescente verde; VB = vaso sanguíneo. Clique aqui para ver uma versão maior desta figura.
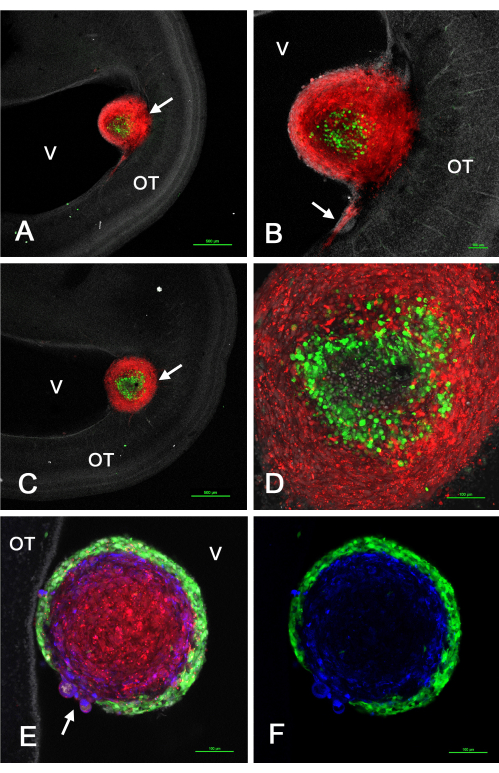
Figura 2: Tumores em E15 resultantes de uma mistura de GSCs e células U-118 GBM injetadas no tecto óptico E5. As GSCs são verdes devido à expressão de GFP e as células U-118/L1LE são vermelhas devido à expressão de mCherry. GSC15-2 são mostrados nos painéis A-D, e GSC16-4 são mostrados nos painéis E e F. (A) Baixo aumento confocal único plano z de um tumor de células mistas (seta) próximo ao ventrículo. Os núcleos são contracorados de branco com bisbenzimida. (B) Maior aumento (objetivo de 10x) do tumor mostrado em A com invasão de células vermelhas U-118 no ST próximo à superfície ventricular. (C) Um plano de corte óptico ligeiramente diferente daquele em A mostrando o tumor (seta) embutido mais profundamente na parede do ST. (D) Projeção máxima (objetiva de 20x) de múltiplos planos z do tumor em C mostrando detalhes das células classificadas dentro do tumor. (E) Imagem única no plano z (objetiva de 20x) de um tumor misto com células GSC16-4, mostrando que a triagem dentro do tumor ocorreu em um padrão oposto às células GSC15-2, com as GSCs verdes criando um córtex fino e uniforme ao redor das células vermelhas U-118. A área de fixação do tumor à parede do TO não é mostrada neste plano z. Observar a área do tumor onde há uma descontinuidade do córtex de GSC com células U-118/L1LE abaulando (seta). A imunomarcação para L1CAM é mostrada em azul. (F) Mesma imagem que em E, mas mostrando apenas os GSCs verdes e a coloração L1CAM azul. Barras de escala = 500 μm (A,C), 100 μm (B,D,E,F). Abreviações: GSCs = células-tronco de glioblastoma; OT = tecto óptico; GFP = proteína fluorescente verde; V = ventrículo. Clique aqui para ver uma versão maior desta figura.
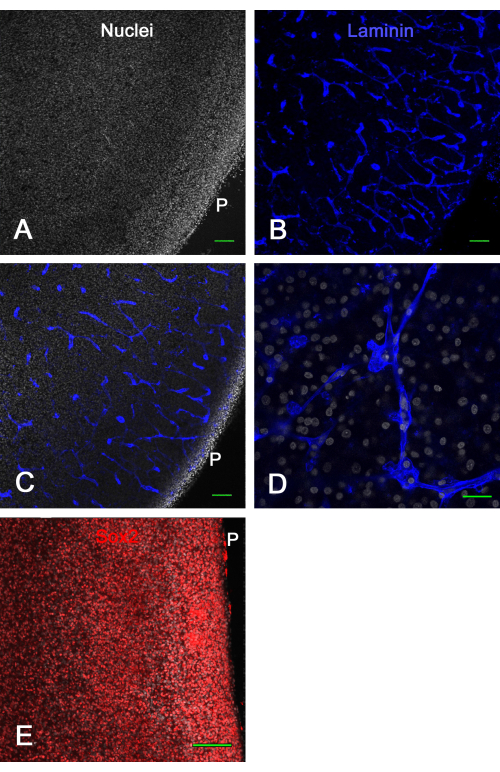
Figura 3: Viabilidade de cortes ex vivo de tecto óptico após 1 semana em cultura. Cortes de tecto óptico E14 foram cultivados em insertos de membrana por 1 semana e, em seguida, fixados e imunomarcados. Em A e B são mostradas imagens confocais (objetiva 10x) de um corte cerebral corado para núcleos com bisbenzimida (A) e imunocorado para laminina (B), que mostra claramente vasos sanguíneos normais e intactos opticamente seccionados em várias configurações em virtude da coloração de laminina. (C) Imagem confocal semelhante à mostrada nos painéis A e B, onde núcleos e coloração de laminina são visíveis. (D) Imagem confocal de maior magnificação (objetiva de óleo de 60x) mostrando detalhes da coloração nuclear e laminina. (E) Imagem de projeção máxima da pilha z confocal (objetiva 20x) de corte cerebral corado pelo fator de transcrição Sox2 em vermelho e núcleo total com bisbenzimida em branco. Observe que a maioria dos núcleos exibe coloração de Sox2, como mostrado in vivo (ver Figura 1). Barras de escala = 100 μm (A,B,C,E), 25 μm (D). Abreviação: P = superfície pial. Clique aqui para ver uma versão maior desta figura.
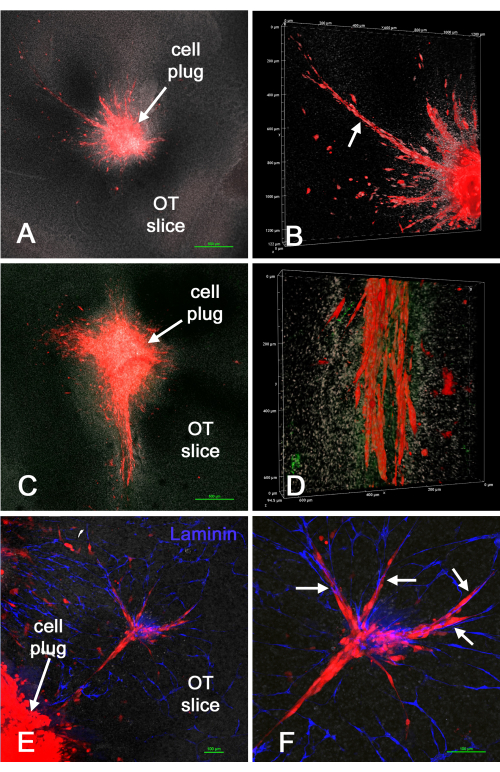
Figura 4: Células U-118/mCherry colocadas em um corte cerebral ex vivo através do método de punção por biópsia. Cavidades foram criadas em cortes cerebrais usando um punch de biópsia de 1 mm e, em seguida, células vermelhas U-118/L1LE/mCherry misturadas com matriz foram implantadas como um "plug". Após vários dias, os cortes cerebrais foram fixados, imunocorados para laminina e montados em lâminas para análise confocal ao microscópio. Os painéis A e C mostram imagens de baixo aumento, confocais, no plano z único (objetiva 4x) do "tumor" resultante e das células vizinhas que invadiram o corte cerebral. (B) Renderização volumétrica de uma pilha z da preparação no painel A em maior aumento (objetiva de 20x), mostrando extensa invasão de células U-118 (seta). (D) A imagem mostra uma renderização de volume semelhante da parte inferior das células extensivamente invasoras mostradas no painel C. A coloração de laminina é mostrada em verde, mas nenhum vaso sanguíneo claro é aparente. (E) Imagem mostra parte de um tampão celular e grupo de células que invadiram a fatia cerebral, juntamente com a coloração de laminina para vasos sanguíneos em azul. (F) Maior ampliação das células invasoras mostradas no painel E, e as células podem ser claramente vistas alinhadas ao longo dos vasos sanguíneos (setas). Todos os painéis mostram contracoloração nuclear branca com bisbenzimida. Barras de escala = 500 μm (A,C), 100 μm (E,F). A escala para os painéis B e D está ao longo dos eixos de renderização de volume. Abreviação: OT = tecto óptico. Clique aqui para ver uma versão maior desta figura.

Figura 5: Esferoides de células vivas em cultura e imagens de fluorescência de campo largo de células GBM vivas em cortes cerebrais ex vivo. Os painéis A e B são mostrados imagens de contraste de fase (usando uma objetiva de 10x em um microscópio invertido) de células U-118/L1LE GBM (A) e GSCs (B) crescendo como esferoides (setas). Mostrado no fundo do painel A é o desnível fora de foco do revestimento poli-HEMA que pode ocorrer no prato de cultura celular. Os painéis C-F mostram imagens de fluorescência de campo largo de esferoides celulares U-118/L1LE e células invasoras (setas) durante um experimento de lapso de tempo para monitorar o comportamento vivo de invasão nos cortes ex vivo (usando uma objetiva de 20x em um sistema de microscópio de lapso de tempo personalizado18). Nos painéis C e E, as células são coradas com o corante de membrana fluorescente vermelho-distante DiD, e nos painéis D e F, as células são imageadas através de sua expressão mCherry vermelha. Barras de escala = 100 μm. Vídeos de experimentos de time-lapse de fluorescência de campo largo mostrados nos painéis C e D estão localizados em Vídeo Suplementar S5 e Vídeo Suplementar S6, respectivamente. Abreviações: GBM = glioblastoma; GSCs = células-tronco GBM; S = esferoide. Clique aqui para ver uma versão maior desta figura.
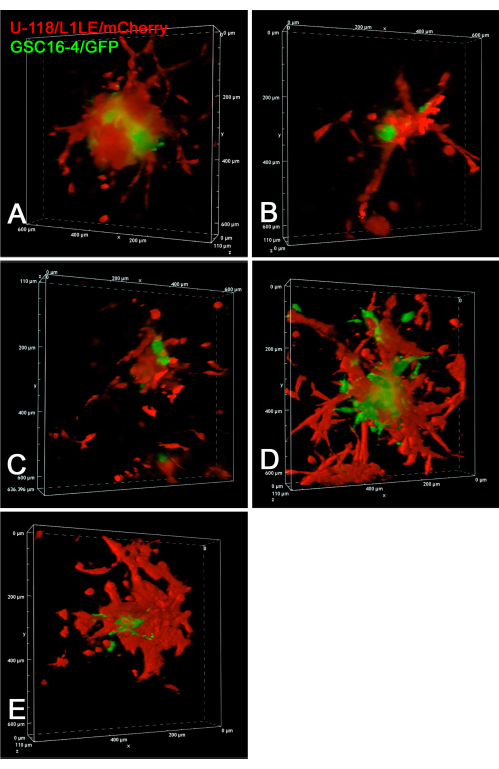
Figura 6: Renderização de volume de imagens de time-lapse 4D confocal de GSCs ao vivo e células GBM. Em todos os painéis, são mostradas as imagens finais de cinco diferentes enxertos esferoides de células mistas em fatias cerebrais separadas. Para os painéis A-E, imagens confocais z-stack foram adquiridas a passos de 10 μm a cada 10 min durante um período de 20 h. As preparações incluíram fatias cerebrais com esferoides de células mistas implantadas de células vermelhas U-118/L1LE/mCherry e células verdes GSC16-4/GFP. Imagens confocais foram obtidas enquanto fatias cerebrais foram cultivadas em inserções de membrana em uma placa de cultura de células plásticas de 6 poços usando uma lente objetiva de 20x (0,45 NA) de distância de trabalho extralonga (ELWD), que forneceu a distância de trabalho extra necessária. Renderizações volumétricas foram geradas usando o software de microscópio confocal "Alpha Blending", que dá um efeito 3D aparente. Os vídeos de lapso de tempo dessas renderizações de volume confocal ao longo do tempo são apresentados em Vídeo Suplementar S7, Vídeo Suplementar S8, Vídeo Suplementar S9, Vídeo Suplementar S10 e Vídeo Suplementar S11. Abreviações: GBM = glioblastoma; GSCs = células-tronco GBM; GFP = proteína fluorescente verde; NA = abertura numérica. Clique aqui para ver uma versão maior desta figura.
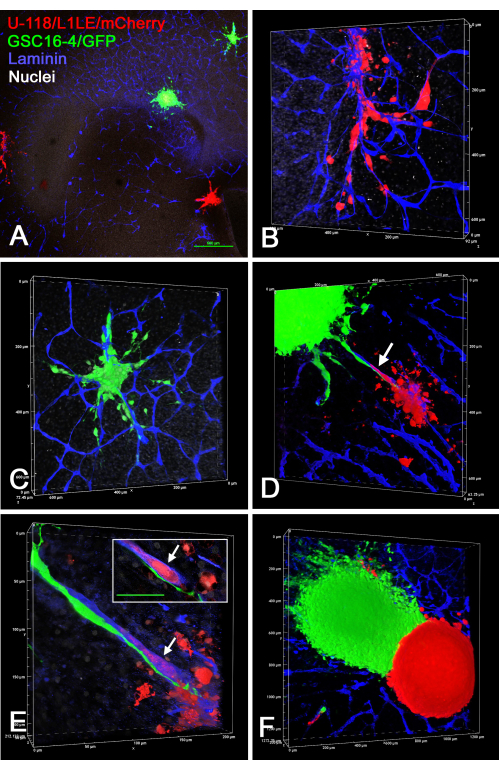
Figura 7: Imagens confocais de cortes cerebrais fixos com células GBM invasivas de esferoides de diferentes tipos celulares. Os esferoides verdes foram compostos por células GSC16-4/GFP e os esferoides vermelhos por células U-118/L1LE/mCherry. Mostrados nos painéis A-F são diferentes visões de fatias cerebrais, nas quais vários esferoides vermelhos e verdes foram cultivados por vários dias antes da fixação e imunomarcação para laminina (azul). Os painéis A-C são da mesma fatia OT onde A foi tirado com uma objetiva de 4x, e os painéis B e C são renderizações de maior volume de ampliação (objetiva de 20x) de células que invadiram a fatia cerebral de dois dos esferoides mostrados no painel A. Ambos os tipos celulares invadiram claramente o tecido ao longo dos vasos sanguíneos. O painel D mostra uma renderização de volume (objetiva de 20x) de um corte cerebral diferente, onde dois esferoides diferentes estavam localizados próximos, e células de ambos são vistas migrando ao longo do mesmo vaso sanguíneo que está localizado entre eles (seta). O painel E é uma renderização volumétrica de alta magnificação (objetiva de óleo de 60x) revelando que as células verdes estão migrando ao longo da superfície externa do vaso sanguíneo, enquanto a hemácia está migrando dentro do vaso sanguíneo (seta). O inset mostra uma única seção óptica no plano z, onde a hemácia é claramente cercada pela coloração azul do vaso sanguíneo (seta), e a célula verde está claramente fora do vaso sanguíneo. Barra de escala em inset = 50 μm. O painel F mostra uma renderização de volume (objetiva de 10x) de uma fatia de prosencéfalo com dois esferoides de cores diferentes apostos de perto. Muito pouco, ou nenhum, invasão celular ocorreu de um esferoide para o outro, e uma fronteira nítida existia entre eles. Os painéis A, B, C e E também mostram contracoloração nuclear branca com bisbenzimida. Barra de escala = 500 μm (A). As escalas para painéis B-F estão ao longo dos eixos de renderização de volume. Abreviações: GBM = glioblastoma; GSCs = células-tronco GBM; GFP = proteína fluorescente verde; OT = tecto óptico. Clique aqui para ver uma versão maior desta figura.
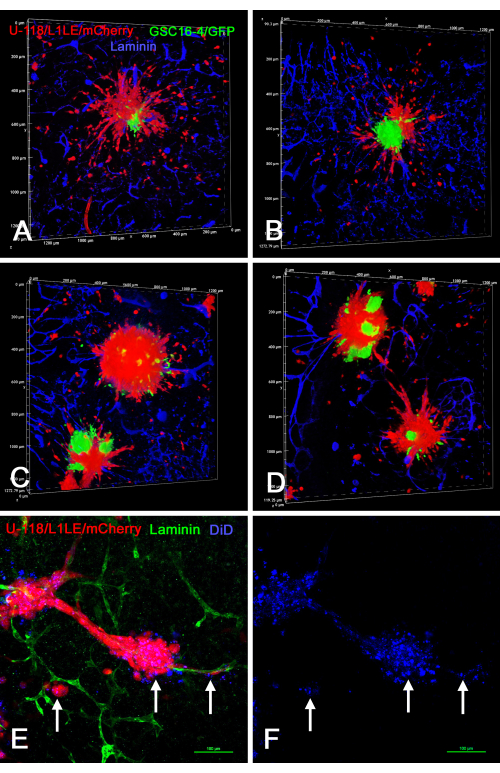
Figura 8: Imagens confocais de cortes cerebrais fixos com células GBM invasivas de esferoides e esferoides de células mistas marcados com DiD. Os painéis A-D mostram renderizações volumétricas de fatias cerebrais que continham esferoides celulares mistos compostos de células verdes GSC16-4/GFP e células vermelhas U-118/L1LE/mCherry. Numerosas células vermelhas U-118 dispersaram-se dos esferoides e invadiram o corte cerebral em todas as direções, enquanto as GSCs verdes não se dispersaram e permaneceram nos locais centrais dos esferoides. Os painéis E e F mostram uma preparação de fatias ex vivo com esferoides vermelhos U-118/L1LE/mCherry também marcados com corante de membrana vermelho-distante DiD (mostrado como azul). Após a fixação, o corte foi imunomarcado para laminina em verde. O rótulo DiD era visível nas hemácias como coloração puntiforme (setas) e era visível mesmo nas células que se dispersavam dos esferoides ao longo dos vasos sanguíneos. A contracoloração nuclear com bisbenzimida não é mostrada nesta figura para que a outra coloração seja mais claramente visível. Barras de escala = 100 μm (E,F). Abreviações: GBM = glioblastoma; GSCs = células-tronco GBM; GFP = proteína fluorescente verde. Clique aqui para ver uma versão maior desta figura.
| Meio/solução | Composição | ||
| Mídia GSC | Mistura 1:1 de DMEM/F12, soro fetal bovino (SFB) 1%, tampão HEPES 15 mM, L-glutamina 2 mM, penicilina-estreptomicina 100 μg/mL, suplemento B27 a 2% sem vitamina A e 2,5 μg/mL de heparina. | ||
| Mídia GBM | DMEM (glicose alta), FBS a 10%, pen/strep e L-glutamina 2 mM. | ||
| Buffer de fixação | PFA 2% em tampão cacodilato de sódio 0,1 M | ||
| Meio de incorporação | 3,5% ágar e 8% sacarose em PBS | ||
| PBSTG | 0,1% Triton X-100 + 5% soro normal de cabra (NGS) em PBS | ||
| Meio de cultura celular U-118 MG | DMEM + 10% SFB + caneta/strep + L-glutamina | ||
| Meios de cultura de fatias cerebrais | 50% MEM + 25% HBSS + 25% Soro de Cavalo + B27 + caneta/strep + L-glut + tampão HEPES 15 mM | ||
| Mídia de fatiamento de tecido vibratório | Meio 199 + caneta/strep + buffer HEPES de 15 mM | ||
Tabela 1: Composição dos meios e buffers utilizados neste protocolo.
Figura suplementar 1: Injeção no tecto óptico E5. (A) Depois que um orifício é cortado na casca do ovo sobre o espaço de ar, e a membrana do espaço aéreo é molhada com soro fisiológico ou meio, a membrana é removida com pinça fina. (B) Para injetar células no tecto óptico, o âmnio é pinçado e mantido com pinça fina para posicionar a cabeça de modo que o tecto óptico seja acessível. Em seguida, a micropipeta é inserida no tecto óptico e as células são injetadas sob pressão nele. (C) Após a injeção das células, algumas gotas de solução de ampicilina são adicionadas em cima do embrião usando uma seringa e agulha fina. Clique aqui para baixar este arquivo.
Figura 2 Suplementar: Dissecção das regiões cerebrais do E15. (A) Após a decapitação, a cabeça do embrião E15 é colocada em uma placa com solução estéril de CMF. (B) A pele que recobre o cérebro é então removida com pinças finas. (C) Os dois ossos do crânio são então removidos da sobreposição dos dois hemisférios do prosencéfalo (FB). (D) A dura-máter do tecido conjuntivo é então suavemente removida do entorno do prosencéfalo (CE), do tecto óptico e do cerebelo. (E) Todo o cérebro é então removido da cabeça, retirando-o suavemente da cavidade cerebral por baixo usando pinças curvas. (F ) É mostrada a visão dorsal de todo o cérebro removido com prosencéfalo (FB), tecto óptico (OT) e cerebelo (CB). (G ) O cérebro isolado é então dissecado em prosencéfalo (FB), hemisférios do tecto óptico (OT) e cerebelo (CB) usando tesouras finas. (H ) A delicada pia de tecido conjuntivo é então facilmente removida dos hemisférios do tecto óptico (OT) usando pinças finas. Clique aqui para baixar este arquivo.
Figura complementar 3: Incorporação e fatiamento do tecto óptico E15 e colocação de esferoides celulares. (A) Um hemisfério do tecto óptico é submerso em agarose de fusão baixa usando pinças curvas. (B) Após o endurecimento da agarose no gelo, o bloco que contém o tecto óptico é aparado e colado ao pedestal de aço inoxidável na placa/bandeja de corte. (C) Depois que a cola secar, o prato/bandeja de fatiamento é colocado no mandril do cortador de tecido vibratório e preenchido com meio de corte frio. As fatias são então cortadas com a faca de safira do bloco de tecido submerso. As fatias cortadas flutuarão no prato/bandeja e podem ser removidas usando uma espátula. (D) As fatias cortadas são retiradas do prato/bandeja e colocadas diretamente sobre as inserções de membrana com o meio de cultura de corte subjacente em uma placa de vários poços. (E) Depois que os esferoides celulares são cultivados em placas revestidas de poli-HEMA, um esferoide é removido da placa em uma quantidade mínima de meio usando um micropipetador de 20 μL. (F) O esferoide isolado é então colocado diretamente sobre o corte cerebral no meio mínimo. (G) Se o esferoide cair da fatia cerebral devido ao fluxo da mídia, então ele pode ser empurrado de volta para a fatia cerebral usando um cílio colado a um bastão aplicador de madeira. Clique aqui para baixar este arquivo.
Vídeo Suplementar S1: Vídeo de renderização de volume de alta magnificação de um pequeno tumor GSC15-2 em E15. Os GSCs são verdes devido à expressão de GFP. O vídeo corresponde à Figura 1C e mostra as células GSC15-2. O vídeo mostra a rotação de uma renderização de volume gerada a partir de uma pilha z usando uma objetiva de imersão em óleo de 60x. Os núcleos celulares aparecem brancos devido à coloração de bisbenzimida, e alguns aparecem vermelhos devido à imunomarcação para Sox2. Note que devido ao "Alpha Blending" para renderizações de volume no software do microscópio confocal, as cores não se misturam como fariam usando uma projeção de intensidade máxima, e a cor mais intensa predomina e obscurece a cor menos intensa. Os vasos sanguíneos são corados de branco devido à imunomarcação para laminina. A coloração alfa-6 da integrina do marcador GSC é mostrada em azul e aparece pontuada em superfícies verdes de GSC. Escalas de mícrons são mostradas ao longo das bordas da renderização de volume. Clique aqui para baixar este vídeo.
Vídeo Suplementar S2: Vídeo de renderização de volume de alta magnificação de pequeno tumor GSC16-4 em E15. Os GSCs são verdes devido à expressão de GFP. O vídeo corresponde à Figura 1D e mostra as células GSC16-4. O vídeo mostra a rotação de uma renderização de volume gerada a partir de uma pilha z usando uma objetiva de imersão em óleo de 60x. Os núcleos celulares aparecem brancos devido à coloração de bisbenzimida, e alguns GSCs aparecem vermelhos devido à imunomarcação para nestina. Note que devido ao "Alpha Blending" para renderizações de volume no software do microscópio confocal, as cores não se misturam como fariam usando uma projeção de intensidade máxima, e a cor mais intensa predomina e obscurece a cor menos intensa. Os vasos sanguíneos são corados de branco devido à imunomarcação para laminina. A coloração alfa-6 da integrina do marcador GSC é mostrada em azul e aparece pontuada em superfícies verdes de GSC. Escalas de mícrons são mostradas ao longo das bordas da renderização de volume. Clique aqui para baixar este vídeo.
Vídeo Suplementar S3: Vídeo de renderizações de volume de alta ampliação de pequeno tumor GSC15-2 em E15. Os GSCs são verdes devido à expressão de GFP. O vídeo corresponde à Figura 1E e mostra as células GSC15-2. O vídeo mostra a rotação de uma renderização de volume gerada a partir de uma pilha z usando uma objetiva de imersão em óleo de 60x. Os núcleos celulares aparecem brancos devido à coloração de bisbenzimida, e alguns aparecem vermelhos devido à imunomarcação para Sox2. Note que devido ao "Alpha Blending" para renderizações de volume no software do microscópio confocal, as cores não se misturam como fariam usando uma projeção de intensidade máxima, e a cor mais intensa predomina e obscurece a cor menos intensa. Os vasos sanguíneos são corados de branco devido à imunomarcação para laminina. A coloração alfa-6 da integrina do marcador GSC é mostrada em azul e aparece pontuada em superfícies verdes de GSC. Escalas de mícrons são mostradas ao longo das bordas da renderização de volume. Clique aqui para baixar este vídeo.
Vídeo suplementar S4: Vídeo de renderizações de alto volume de aumento de pequenos tumores GSC16-4 em E15. Os GSCs são verdes devido à expressão de GFP. O vídeo corresponde à Figura 1F e mostra as células GSC16-4. O vídeo mostra a rotação de uma renderização de volume gerada a partir de uma pilha z usando uma objetiva de imersão em óleo de 60x. Os núcleos celulares aparecem brancos devido à coloração de bisbenzimida, e alguns aparecem vermelhos devido à imunomarcação para nestina. Note que devido ao "Alpha Blending" para renderizações de volume no software do microscópio confocal, as cores não se misturam como fariam usando uma projeção de intensidade máxima, e a cor mais intensa predomina e obscurece a cor menos intensa. Os vasos sanguíneos são corados de branco devido à imunomarcação para laminina. A coloração alfa-6 da integrina do marcador GSC é mostrada em azul e aparece pontuada em superfícies verdes de GSC. Escalas de mícrons são mostradas ao longo das bordas da renderização de volume. Clique aqui para baixar este vídeo.
Vídeo suplementar S5: Vídeo de células GBM ao vivo em fatia cerebral ex vivo . O vídeo corresponde à Figura 5C e mostra imagens de fluorescência de campo largo de esferoides celulares U-118/L1LE e células invasoras durante um experimento de lapso de tempo para monitorar o comportamento vivo de invasão no corte ex vivo (usando uma objetiva de 20x em um sistema de microscópio de lapso de tempo personalizado). As células U-118/L1LE foram coradas com o corante fluorescente DiD vermelho-distante. As imagens foram adquiridas com câmera monocromática. Clique aqui para baixar este vídeo.
Vídeo suplementar S6: Vídeo de células GBM ao vivo em fatia cerebral ex vivo . O vídeo corresponde à Figura 5D e mostra imagens de fluorescência de campo largo de esferoides celulares U-118/L1LE e células invasoras durante um experimento de lapso de tempo para monitorar o comportamento vivo de invasão no corte ex vivo (usando uma objetiva de 20x em um sistema de microscópio de lapso de tempo personalizado). As células foram fotografadas através de sua expressão mCherry vermelha. As imagens foram adquiridas com câmera monocromática. Clique aqui para baixar este vídeo.
Vídeo suplementar S7: Vídeo de renderização de volume de imagens de time-lapse 4D confocal de GSCs ao vivo e células GBM. O vídeo corresponde à Figura 6A. Imagens confocais z-stack foram adquiridas a passos de 10 μm a cada 10 min durante um período de 20 h. A preparação foi de um corte cerebral com esferoides de células mistas implantadas de células vermelhas U-118/L1LE/mCherry e células verdes GSC16-4/GFP. Imagens confocais foram obtidas enquanto o corte cerebral era cultivado em uma inserção de membrana em uma placa de cultura de células plásticas de 6 poços usando uma lente objetiva ELWD 20x (0,45 NA), que fornecia a distância de trabalho extra necessária. A renderização volumétrica foi gerada usando o software de microscópio confocal "Alpha Blending", que dá um efeito 3D aparente. Escalas de mícrons são mostradas ao longo das bordas da renderização de volume. O vídeo é melhor observado arrastando manualmente o controle deslizante de progresso do vídeo no player de vídeo para frente e para trás para observar o movimento da célula, em vez de permitir que o player de vídeo prossiga em sua velocidade lenta normal. Clique aqui para baixar este vídeo.
Vídeo suplementar S8: Vídeo de renderização de volume de imagens de time-lapse 4D confocal de GSCs ao vivo e células GBM. O vídeo corresponde à Figura 6B. Imagens confocais z-stack foram adquiridas a passos de 10 μm a cada 10 min durante um período de 20 h. A preparação foi de um corte cerebral com esferoides de células mistas implantadas de células vermelhas U-118/L1LE/mCherry e células verdes GSC16-4/GFP. Imagens confocais foram obtidas enquanto o corte cerebral era cultivado em uma inserção de membrana em uma placa de cultura de células plásticas de 6 poços usando uma lente objetiva ELWD 20x (0,45 NA), que fornecia a distância de trabalho extra necessária. A renderização volumétrica foi gerada usando o software de microscópio confocal "Alpha Blending", que dá um efeito 3D aparente. Escalas de mícrons são mostradas ao longo das bordas da renderização de volume. O vídeo é melhor observado arrastando manualmente o controle deslizante de progresso do vídeo no player de vídeo para frente e para trás para observar o movimento da célula, em vez de permitir que o player de vídeo prossiga em sua velocidade lenta normal. Clique aqui para baixar este vídeo.
Vídeo suplementar S9: Vídeo de imagens de renderização de volume de time-lapse 4D confocal de GSCs ao vivo e células GBM. O vídeo corresponde à Figura 6C. Imagens confocais z-stack foram adquiridas a passos de 10 μm a cada 10 min durante um período de 20 h. A preparação foi de um corte cerebral com esferoides de células mistas implantadas de células vermelhas U-118/L1LE/mCherry e células verdes GSC16-4/GFP. Imagens confocais foram obtidas enquanto o corte cerebral era cultivado em uma inserção de membrana em uma placa de cultura de células plásticas de 6 poços usando uma lente objetiva ELWD 20x (0,45 NA), que fornecia a distância de trabalho extra necessária. A renderização volumétrica foi gerada usando o software de microscópio confocal "Alpha Blending", que dá um efeito 3D aparente. Escalas de mícrons são mostradas ao longo das bordas da renderização de volume. O vídeo é melhor observado arrastando manualmente o controle deslizante de progresso do vídeo no player de vídeo para frente e para trás para observar o movimento da célula, em vez de permitir que o player de vídeo prossiga em sua velocidade lenta normal. Clique aqui para baixar este vídeo.
Vídeo suplementar S10: Vídeo de imagens de renderização de volume de time-lapse 4D confocal de GSCs ao vivo e células GBM. O vídeo corresponde à Figura 6D. Imagens confocais z-stack foram adquiridas a passos de 10 μm a cada 10 min durante um período de 20 h. A preparação foi de um corte cerebral com esferoides de células mistas implantadas de células vermelhas U-118/L1LE/mCherry e células verdes GSC16-4/GFP. Imagens confocais foram obtidas enquanto o corte cerebral era cultivado em uma inserção de membrana em uma placa de cultura de células plásticas de 6 poços usando uma lente objetiva ELWD 20x (0,45 NA), que fornecia a distância de trabalho extra necessária. A renderização volumétrica foi gerada usando o software de microscópio confocal "Alpha Blending", que dá um efeito 3D aparente. Escalas de mícrons são mostradas ao longo das bordas da renderização de volume. O vídeo é melhor observado arrastando manualmente o controle deslizante de progresso do vídeo no player de vídeo para frente e para trás para observar o movimento da célula, em vez de permitir que o player de vídeo prossiga em sua velocidade lenta normal. Clique aqui para baixar este vídeo.
Vídeo suplementar S11: Vídeo de renderização de volume de imagens de time-lapse 4D confocal de GSCs ao vivo e células GBM. O vídeo corresponde à Figura 6E. Imagens confocais z-stack foram adquiridas a passos de 10 μm a cada 10 min durante um período de 20 h. a preparação incluiu uma fatia cerebral com esferoides de células mistas implantadas de células vermelhas U-118/L1LE/mCherry e células verdes GSC16-4/GFP. Imagens confocais foram obtidas enquanto o corte cerebral era cultivado em uma inserção de membrana em uma placa de cultura de células plásticas de 6 poços usando uma lente objetiva ELWD 20x (0,45 NA), que fornecia a distância de trabalho extra necessária. A renderização volumétrica foi gerada usando o software de microscópio confocal "Alpha Blending", que dá um efeito 3D aparente. Escalas de mícrons são mostradas ao longo das bordas da renderização de volume. O vídeo é melhor observado arrastando manualmente o controle deslizante de progresso do vídeo no player de vídeo para frente e para trás para observar o movimento da célula, em vez de permitir que o player de vídeo prossiga em sua velocidade lenta normal. Clique aqui para baixar este vídeo.
Discussão
As etapas críticas no protocolo para a injeção de células no ventrículo do mesencéfalo (tecto óptico) incluem não danificar os vasos sanguíneos na membrana corioalantóica no ovo ou ao redor do embrião antes e durante a injeção, embora a membrana de âmnio imediatamente ao redor do embrião possa ser suavemente puxada e mantida para posicionar a cabeça ao injetar as células no mesencéfalo. O âmnio é relativamente resistente e pode ser puxado com pinças finas para posicionar a cabeça e mantê-la firme com uma mão, para a injeção de células com a outra mão no tecto óptico, que é a grande estrutura redonda no meio do cérebro. Geralmente, a viabilidade dos embriões injetados varia de 25% a 75%, dependendo de fatores desconhecidos, e praticamente todo embrião que sobrevive contém pelo menos um pequeno tumor no tecto óptico. Etapas críticas na geração de fatias cerebrais viáveis incluem manchar o tecido do excesso de líquido para que a agarose adera ao cérebro durante o corte e para manter o tecido e fatias frias até ser colocado na inserção da membrana. Como diferentes tipos celulares formam esferoides de forma diferente (em velocidade e tamanho), a densidade celular plaqueada em placas poli-HEMA e o tempo antes da colheita dos esferoides devem ser otimizados para cada tipo celular.
O trabalho aqui não foi submetido a um estudo longitudinal formal da viabilidade da fatia cerebral. utilizaram culturas de fatias cerebrais de embriões de pintinhos semelhantes às aqui utilizadas e mostraram boa viabilidade dos cortes por pelo menos 7 dias16. Trabalhos anteriores mostraram que, quando o tecido OT foi mantido em meios subótimos, muitos núcleos picnóticos apareceram no tecido, o que não ocorreu nos cortes aqui apresentados. Além disso, quando as fatias degeneram em condições subótimas, os vasos sanguíneos se fragmentam e aparecem como fileiras de esferas laminina-positivas (não mostradas). Assim, embora a viabilidade aqui não tenha sido verificada por métodos como eletrofisiologia ou expressão ativa de caspase-3, nenhum dos indicadores de morte celular observados em condições de cultura subótimas apareceu aqui.
O ST tem sido focado em experimentos de tumores cerebrais in vivo por ser a região mais facilmente injetada com o maior ventrículo. No E5, que é o último dia em que o embrião é pequeno o suficiente para permanecer acessível em cima da gema, as injeções devem ser feitas em um ventrículo, pois todas as regiões cerebrais nada mais são do que uma fina zona ventricular. No entanto, essas injeções resultam com sucesso em tumores embutidos com células que invadem o parênquima cerebral. Às vezes, os tumores resultantes são encontrados no prosencéfalo ou cerebelo, mas isso não é comum. Fatias ex vivo do tecto óptico E15 têm sido usadas principalmente para experimentos aqui, de modo que os resultados da co-cultura ex vivo podem ser correlacionados com os experimentos de injeção in vivo . No entanto, os cortes de prosencéfalo também são adequados e têm uma área de superfície maior e um ventrículo muito fino em comparação com o tecto óptico, o que pode tornar o prosencéfalo mais adequado para coculturas ex vivo que não estão sendo correlacionadas com injeções in vivo .
Foi demonstrado aqui que injeções in vivo , seguidas de fixação tecidual, corte de fatiamento de tecido vibratório e imunomarcação para laminina e outros marcadores, resultaram em imagens de alta resolução de células GBM e GSCs no tecido cerebral em estreita proximidade com os vasos sanguíneos. A capacidade de determinar as inter-relações entre células tumorais e vasos sanguíneos foi muito facilitada pela criação de renderizações de volume 3D a partir de pilhas z de seções ópticas confocais usando o software confocal e as instruções do fabricante. Imagens de lapso de tempo usando microscopia de fluorescência de campo largo de células marcadas com GFP, mCherry e DiD foram possíveis; no entanto, as células migratórias que estavam próximas aos esferoides altamente fluorescentes às vezes eram obscurecidas pelo "brilho" do esferoide. Esse efeito indesejado pode ser um pouco minimizado ajustando cuidadosamente os tempos de exposição para coletar imagens de campo amplo. A imagem de lapso de tempo usando pilhas z confocais ao longo do tempo (4D) eliminou o brilho fora de foco dos esferoides e resultou em células migratórias nitidamente definidas com um fundo escuro. Isso não foi descrito no protocolo, mas foi realizado de forma semelhante à imagem de lapso de tempo de campo largo, que foi realizada enquanto cortes cerebrais estavam nas inserções transparentes da membrana em uma placa plástica de 6 poços. Embora a imagem de lapso de tempo confocal resulte em imagens marcadamente mais claras de células individuais e seu comportamento, um experimento de lapso de tempo multiponto coletando pilhas z de 10 planos/ponto z, em intervalos de 10 minutos durante um período de 20 horas, é um uso extensivo dos galvanômetros de cabeça de varredura. Como isso poderia diminuir significativamente a vida útil dos galvanômetros, este método é usado criteriosamente.
Embora o sistema embrionário de pintinhos seja muito adequado para experimentos de injeção in vivo e co-cultivo ex vivo que investigam o comportamento de células GBM, existem várias limitações para este sistema modelo. Como acontece com qualquer sistema de xenoenxerto, o ambiente em que as células humanas são implantadas não é o cérebro humano, mas o comportamento das células GBM parece imitar isso em modelos de roedores e em pacientes humanos. Após a realização de experimentos de injeção in vivo em E5, os tumores são normalmente deixados formar por 10 dias, até E15. Isso claramente não é tempo suficiente para estudar todos os aspectos da tumorigênese e invasão celular. No entanto, foi demonstrado aqui que tumores sólidos se formam no parênquima cerebral, as células interagem e se rearranjam dentro do tumor, e uma invasão cerebral significativa ocorre tanto ao longo dos vasos sanguíneos quanto difusamente dentro desse período de tempo relativamente curto. Outra limitação do sistema embrionário in vivo de pintinhos é que ele não é adequado para medicamentos ou outros tratamentos devido à grande gema e sistema circulatório extraembrionário que opera durante o desenvolvimento do embrião de pintinho. Tratamentos medicamentosos líquidos tópicos resultariam em uma concentração altamente variável e desconhecida no cérebro devido à difusão do embrião para a massa gema muito maior. Da mesma forma, a injeção intravenosa de drogas no sistema circulatório extraembrionário muito delicado vazaria ou se difundiria para fora dos vasos sanguíneos e também resultaria em concentrações desconhecidas no cérebro. Esta é uma das principais razões pelas quais o método de cultura de fatias ex vivo foi adotado, de modo que não apenas o comportamento celular pudesse ser observado e rastreado por meio de microscopia de lapso de tempo, mas também para que tratamentos que foram bem-sucedidos em alterar o comportamento de células GBM em uma placa4 pudessem ser testados em um ambiente de tecido cerebral mais relevante.
O desenvolvimento do sistema modelo de tumor cerebral ortotópico de embrião de pintinho é visto como uma adição significativa aos sistemas e ferramentas disponíveis para o estudo da formação de tumores GBM e comportamento celular invasor. Ovos de galinha fertilizados provavelmente estarão prontamente disponíveis na maioria das áreas, são baratos em comparação com roedores, não há custos de cuidados com os animais, os embriões são muito resistentes e resistentes à infecção (ou seja, a maioria do trabalho é feito em uma bancada), os embriões são altamente manipuláveis e podem ser cultivados em cultura sem casca19, e os embriões de pintinhos não são considerados animais vertebrados e, portanto, não exigem aprovação da IACUC pelas diretrizes do NIH (requisitos institucionais pode variar). Assim, essas múltiplas vantagens tornam o sistema embrionário de pintinhos muito atraente se limitarmos suas perguntas e experimentos àqueles que se enquadram em suas limitações. Estudos com múltiplas células GBM foram realizados por outros utilizando o embrião de pintinhos, mas estes utilizaram quase exclusivamente a membrana corioalantóide (CAM) do embrião 20,21,22,23,24,25,26,27,28,29 e broto do membro 30, e não o cérebro. Também há relato de implante de meduloblastoma no cérebro de pintinhos em E231. Sem dúvida, o uso do embrião de pintinho como um sistema modelo de xenoenxerto ortotópico, como descrito aqui, deve produzir resultados muito mais significativos para a biologia tumoral humana de GBM do que estudos usando o CAM.
Embora esses estudos só tenham começado a utilizar totalmente o sistema modelo de tumor cerebral de embrião de pintinho para estudos de células GBM humanas e comportamento de GSC, espera-se que outros estendam os usos e encontrem mais aplicações potenciais. Pode-se imaginar que esse sistema não apenas descobrirá mecanismos que regulam a formação de tumores GBM e o comportamento celular, mas também permitirá testes pré-clínicos de drogas e substâncias específicas em células de pacientes específicos. Por exemplo, se as culturas de fatias cerebrais fossem previamente estabelecidas, as células tumorais, as peças de ressecções cirúrgicas do tumor ou os organoides GBM derivados do paciente32 poderiam ser colocados diretamente na co-cultura ex vivo , e vários tratamentos poderiam ser avaliados em questão de dias. Da mesma forma, células dissociadas do paciente poderiam ser injetadas diretamente no mesencéfalo E5 para avaliar sua capacidade de formar tumores e invadir o parênquima cerebral. Assim, espera-se que as descrições dos métodos e resultados representativos aqui possam facilitar e incentivar o aumento do uso deste sistema altamente subutilizado para a pesquisa do câncer cerebral.
Divulgações
Nenhum dos autores tem conflitos de interesse.
Agradecimentos
Este trabalho foi financiado em parte por uma doação ao D.S.G. do Instituto Nacional do Câncer (R03CA227312) e por uma generosa doação da Fundação Lisa Dean Moseley. Espécimes vivos de GBM foram obtidos com o consentimento do paciente através do Centro de Procura de Tecidos do Helen F. Graham Cancer Center and Research Institute. O financiamento para A.R. foi fornecido pelo National Center for Research Resources e pelo National Center for Advancing Translational Sciences, National Institutes of Health (UL1TR003107). Bolsas de iniciação científica de verão para N.P., A.L., Z.W. e K.S. foram fornecidas pelo Programa de Pesquisa de Graduação da Universidade de Delaware.
Materiais
| Name | Company | Catalog Number | Comments |
| 1 cm x 1 cm square hole paper punch | Birabira | N/A | |
| 1 mm biopsy punch pen | Robbins Instruments | 20335 | |
| 6 well insert plate (Corning Transwell) | Millipore Sigma | CLS3450 | |
| 9" Disposable Pasteur Pipets | Fisher Scientific | 13-678-20C | |
| 15 mL centrifuge tubes | Fisher Scientific | 05-539-12 | |
| 24 well plate | Corning Costar | 3526 | |
| 50 mL centrifuge tubes | Fisher Scientific | 05-539-9 | |
| Agar | Fisher BioReagents | BP1423-500 | for embedding fixed brains |
| Alexafluor 488-conjugated GAM IgG | Jackson Immunoresearch | 115-605-146 | |
| Alexafluor 647-conjugated GAM IgG | Jackson Immunoresearch | 115-545-146 | |
| Aluminum foil | ReynoldsWrap | N/A | |
| Ampicillin | Sigma Aldrich | A-9518 | |
| anti-integrin alpha-6 monoclonal antibody GOH3 | Santa Cruz Biotechnology | sc-19622 | |
| anti-L1CAM monoclonal antibody UJ127 | Santa Cruz Biotechnology | sc-53386 | |
| anti-laminin monoclonal antibody | Developmental Studies Hybridoma Bank | 3H11 | |
| anti-nestin monoclonal antibody 10c2 | Santa Cruz Biotechnology | sc-23927 | |
| anti-Sox2 monoclonal antibody E-4 | Santa Cruz Biotechnology | sc-365823 | |
| B27 supplement without vitamin A | GIBCO | 17504-044 | |
| bisbenzimide (Hoechst 33258) | Sigma-Aldrich | B2883 | nuclear stain |
| Cell culture incubator | Forma | standard humidified CO2 incubator | |
| Centrifuge | Beckman Coulter | ||
| Confocal microscope | Nikon Instruments | C2si+ | With custom-made cell incubator chamber |
| Confocal microscope objective lenses | Nikon Instruments | Plan Apo lenses, except S Plan Fluor ELWD 20x 0.45 NA objective lens for confocal time-lapse imaging | |
| Confocal microscope software | Nikon Instruments | NIS Elements | Version 5.2 |
| Curved foreceps | World Precision Intruments | 504478 | |
| Curved scissors | Fine Science Tools | ||
| Curved spatula | Fisher Scientific | 14-375-20 | |
| Cyanoacrylate glue | Krazy Glue | KG-585 12R | |
| D-Glucose | Millipore Sigma | G8270 | |
| DiD far red fluorescent dye | Invitrogen | V22887 | Vybrant DiD |
| DMEM | Sigma Aldrich | D5671 | |
| DMEM/F12 | Sigma Aldrich | D8437 | |
| DMSO | Sigma Aldrich | D4540 | |
| Dulbecco's Phosphate buffered saline (PBS) | Sigma Aldrich | P5493-1L | |
| egg incubator | Humidaire | ||
| electrical tape (10 mil thick/254 µm) | Scotch | N/A | |
| Ethanol 200 proof | Decon Laboratories | 2701 | |
| Fast green FCF dye | Avocado Research Chemicals | 16520 | |
| FBS | Gemini Bio-products | 900-108 | |
| filter paper | Fisher Scientific | ||
| Gauze | Dynarex | 3353 | |
| Glass Capillaries for microinjection | World Precision Instruments | TW100-4 | |
| Glycerol | Fisher BioReagents | BP228-1 | for mounting media |
| GSCs (human glioblastoma stem cells) | Not applicable | Isolated from patient GBM specimens in Galileo laboratory in GSC media and then transduced with a GFP encoding lentiviral vector. Cells used were between passage 10 and 30. | |
| Hanks Balanced Salt Solution (HBSS) | Corning | 21-020-CV | |
| Hemacytometer | Hausser scientific | ||
| Heparin | Fisher Scientific | BP2524-100 | |
| HEPES buffer | Sigma Aldrich | H0887 | |
| Horse Serum (HI) | Gibco | 26050-088 | |
| Human FGF-2 | BioVision | 4037-1000 | |
| Human TGF-α | BioVision | 4339-1000 | |
| Inverted phase contrast microscope | Nikon Instruments | TMS | for routine viewing of cultured cells |
| KCl | Fisher Scientific | BP366 | |
| KH2PO4 | Fisher Scientific | P284 | |
| Laboratory film | Parafilm | ||
| Labquake Shaker | LabIndustries | T400-110 | |
| L-Glut:Pen:Strep | Gemini Bio-products | 400-110 | |
| Low-melt agarose | Fisher Scientific | BP1360 | for embedding live brains |
| Matrix | Corning Matrigel | 354234 | |
| Medium 199 | GIBCO | 11150-059 | |
| MEM | Corning | 10-010-CV | |
| Metal vibratome block | |||
| Micropipette tips (20, 200, 1,000 µL) | Fisherbrand | ||
| Micropipettors (20, 200, 1,000 µL) | Gilson | ||
| Microscope Coverglass (no. 1.5 thickness) | Fisherbrand | 12544A | |
| NaCl | Fisher Scientific | S271 | |
| NaH2PO4 + H2O | Fisher Scientific | S369 | |
| NaHCO3 | Fisher Scientific | BP328 | |
| Normal goat serum | Millipore Sigma | 526-M | |
| N-propyl gallate | Sigma Aldrich | P3130 | for mounting media |
| Parafilm | Parafilm | ||
| Paraformaldehyde | Electron Microscopy Sciences | 15710 | |
| PBS | Sigma Aldrich | P5493-1L | |
| Pencil | |||
| Plain Microscope slides | Fisherbrand | 12-550-A3 | |
| Plastic 35 mm Petri dish | Becton Dickinson | 351008 | |
| pneumatic picopump | World Precision Intruments | PV830 | |
| Poly(2-hydroxyethyl methacrylate) (poly-HEMA) | Sigma Aldrich | P-3932 | |
| razor blade- double edge | PACE | for cutting fixed brain slices | |
| sapphire knife | Delaware Diamond Knives | for cutting live brain slices | |
| Scalpel | TruMed | 1001 | |
| Sodium cacodylate buffer 0.2 M pH 7.4 | Electron Microscopy Sciences | 11652 | |
| Specimen chamber for vibratome | custom-made | ||
| Stereo Dissecting Microscope | Nikon Instruments | SMZ1500 | Equipped with epifluorescence |
| straight foreceps | World Precision Intruments | 500233 | |
| straight scissors | Fine Science Tools | ||
| Sucrose | Mallinckrodt | 7723 | |
| Time-lapse fluorescence microscope (widefield fluorescence) | Nikon Instruments | TE2000-E | With custom-made cell incubator chamber (see Fotos et al., 2006) |
| Tissue culture dish polystyrene 100 mm | Thermo Fisher Scientific | 130182 | for cell culturing |
| Tissue culture dish polystyrene 60 mm | Becton Dickinson | 353004 | for cell culturing |
| Transfer pipette | American Central Scientific Co. | FFP011 | |
| Transparent tape | Scotch | ||
| Triton X-100 | Sigma Aldrich | T-8787 | |
| Trypsin (0.25%) + 2.21 mM EDTA | Corning | 25-053-CI | |
| U-118 MG human GBM cell line | ATCC | HTB-15 | Cells were transduced with a lentiviral vector encoding the entire ectodomain sequence of the L1CAM adhesion protein and then with lentiviral vector pUltra-hot encoding mCherry. Passage numbers are unknown. |
| Vacuum pump | Cole-Parmer | EW-07532-40 | "Air Cadet" |
| Vibrating tissue slicer | Vibratome | 3000 | for cutting live and fixed brain slices |
Referências
- Cretu, A., Fotos, J. S., Little, B. W., Galileo, D. S. Human and rat glioma growth, invasion, and vascularization in a novel chick embryo brain tumor model. Clinical & Experimental Metastasis. 22 (3), 225-236 (2005).
- Yang, M., et al. L1 stimulation of human glioma cell motility correlates with FAK activation. Journal of Neuro-Oncology. 105 (1), 27-44 (2011).
- Mohanan, V., Temburni, M. K., Kappes, J. C., Galileo, D. S. L1CAM stimulates glioma cell motility and proliferation through the fibroblast growth factor receptor. Clinical & Experimental Metastasis. 30 (4), 507-520 (2013).
- Anderson, H. J., Galileo, D. S. Small-molecule inhibitors of FGFR, integrins and FAK selectively decrease L1CAM-stimulated glioblastoma cell motility and proliferation. Cellular Oncology. 39 (3), 229-242 (2016).
- Pace, K. R., Dutt, R., Galileo, D. S. Exosomal L1CAM stimulates glioblastoma cell motility, proliferation, and invasiveness. International Journal of Molecular Sciences. 20 (16), 3982 (2019).
- Stoppini, L., Buchs, P. A., Muller, D. A simple method for organotypic cultures of nervous tissue. Journal of Neuroscience Methods. 37 (2), 173-182 (1991).
- Ohnishi, T., Matsumura, H., Izumoto, S., Hiraga, S., Hayakawa, T. A novel model of glioma cell invasion using organotypic brain slice culture. Cancer Research. 58 (14), 2935-2940 (1998).
- Humpel, C. Organotypic brain slice cultures: A review. Neuroscience. 305, 86-98 (2015).
- Aaberg-Jessen, C., et al. Invasion of primary glioma- and cell line-derived spheroids implanted into corticostriatal slice cultures. International Journal of Clinical and Experimental Pathology. 6 (4), 546-560 (2013).
- Matsumura, H., Ohnishi, T., Kanemura, Y., Maruno, M., Yoshimine, T. Quantitative analysis of glioma cell invasion by confocal laser scanning microscopy in a novel brain slice model. Biochemical and Biophysical Research Communications. 269 (2), 513-520 (2000).
- Ren, B., et al. Invasion and anti-invasion research of glioma cells in an improved model of organotypic brain slice culture. Tumori. 101 (4), 390-397 (2015).
- Fayzullin, A., et al. Time-lapse phenotyping of invasive glioma cells ex vivo reveals subtype-specific movement patterns guided by tumor core signaling. Experimental Cell Research. 349 (2), 199-213 (2016).
- Jensen, S. S., et al. Establishment and characterization of a tumor stem cell-based glioblastoma invasion model. PloS One. 11 (7), e0158746 (2016).
- Marques-Torrejon, M. A., Gangoso, E., Pollard, S. M. Modelling glioblastoma tumour-host cell interactions using adult brain organotypic slice co-culture. Disease Models & Mechanisms. 11 (2), 031435 (2018).
- Tamura, R., et al. Visualization of spatiotemporal dynamics of human glioma stem cell invasion. Molecular Brain. 12 (1), 45 (2019).
- Yang, C., et al. Organotypic slice culture based on in ovo electroporation for chicken embryonic central nervous system. Journal of Cellular and Molecular Medicine. 23 (3), 1813-1826 (2019).
- Murrell, W., et al. Expansion of multipotent stem cells from the adult human brain. PloS One. 8 (8), e71334 (2013).
- Fotos, J. S., et al. Automated time-lapse microscopy and high-resolution tracking of cell migration. Cytotechnology. 51 (1), 7-19 (2006).
- Tufan, A. C., Akdogan, I., Adiguzel, E. Shell-less culture of the chick embryo as a model system in the study of developmental neurobiology. Neuroanatomy. 3 (1), 8-11 (2004).
- Shoin, K., et al. Chick embryo assay as chemosensitivity test for malignant glioma. Japanese Journal of Cancer Research. 82 (10), 1165-1170 (1991).
- Hagedorn, M., et al. Accessing key steps of human tumor progression in vivo by using an avian embryo model. Proceedings of the National Academy of Sciences. 102 (5), 1643-1648 (2005).
- Balciūniene, N., et al. Histology of human glioblastoma transplanted on chicken chorioallantoic membrane. Medicina. 45 (2), 123-131 (2009).
- De Magalhães, N., et al. Applications of a new In vivo tumor spheroid based shell-less chorioallantoic membrane 3-D model in bioengineering research. Journal of Biomedical Science and Engineering. 3 (1), 20-26 (2010).
- Szmidt, M., et al. Morphology of human glioblastoma model cultured in ovo. Journal of Veterinary Research. 56 (2), 261-266 (2012).
- Jaworski, S., et al. Comparison of tumor morphology and structure from U87 and U118 glioma cells cultured on chicken embryo chorioallantoic membrane. Journal of Veterinary Research. 57 (4), 593-598 (2013).
- Yuan, Y. J., Xu, K., Wu, W., Luo, Q., Yu, J. L. Application of the chick embryo chorioallantoic membrane in neurosurgery disease. International Journal of Medical Sciences. 11 (12), 1275-1281 (2014).
- Urbańska, K., et al. The effect of silver nanoparticles (AgNPs) on proliferation and apoptosis of in ovo cultured glioblastoma multiforme (GBM) cells. Nanoscale Research Letters. 10, 98 (2015).
- DeBord, L. C., et al. The chick chorioallantoic membrane (CAM) as a versatile patient-derived xenograft (PDX) platform for precision medicine and preclinical research. American Journal of Cancer Research. 8 (8), 1642-1660 (2018).
- Han, J. M., Jung, H. J. Synergistic anticancer effect of a combination of berbamine and arcyriaflavin A against glioblastoma stem-like cells. Molecules. 27 (22), 7968 (2022).
- Ruiz-Ontañon, P., et al. Cellular plasticity confers migratory and invasive advantages to a population of glioblastoma-initiating cells that infiltrate peritumoral tissue. Stem Cells. 31 (6), 1075-1085 (2013).
- Cage, T. A., et al. Distinct patterns of human medulloblastoma dissemination in the developing chick embryo nervous system. Clinical & Experimental Metastasis. 29 (4), 371-380 (2012).
- Darrigues, E., et al. Biobanked glioblastoma patient-derived organoids as a precision medicine model to study inhibition of invasion. International Journal of Molecular Sciences. 22 (19), 10720 (2021).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoExplore Mais Artigos
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados