このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
マウスにおける視運動性反射の視覚特徴選択性の定量化
要約
ここでは、視運動性反射を定量化するための標準プロトコルについて説明します。仮想ドラム刺激とビデオ眼球撮影を組み合わせることで、行動の特徴選択性とその適応可塑性を正確に評価することができます。
要約
視運動性反射(OKR)は、視覚環境の全体的な動きによって引き起こされ、網膜画像を安定させるのに役立つ重要な先天的な眼球運動です。OKRは、その重要性と堅牢性から、視覚運動学習の研究や、遺伝的背景、年齢、薬物治療の異なるマウスの視覚機能の評価に使用されてきました。ここでは、頭部固定マウスのOKR応答を高精度に評価するための手順を紹介します。頭部固定は、前庭刺激が眼球運動に寄与することを除外することができ、視覚運動のみによって引き起こされる眼球運動を測定することが可能になります。OKRは、3台のコンピュータモニターに表示される垂直グレーティングが、水平方向に振動的に、または一方向に等速でドリフトする仮想ドラムシステムによって引き出されます。このバーチャルリアリティシステムにより、空間周波数、時間/振動周波数、コントラスト、輝度、回折格子の方向などの視覚パラメータを体系的に変更し、視覚特徴選択性のチューニング曲線を定量化することができます。高速赤外線ビデオ眼球撮影により、眼球運動の軌跡を正確に測定できます。個々のマウスの目は、年齢、性別、遺伝的背景の異なる動物間でOKRを比較する機会を提供するように調整されています。この手法の定量的な力により、この行動が加齢、感覚経験、または運動学習によって可塑的に適応するときの OKR の変化を検出できます。したがって、この手法は、眼の行動の可塑性を調査するために使用されるツールのレパートリーに貴重な追加になります。
概要
環境内の視覚刺激に反応して、私たちの目は、視線を移動したり、網膜画像を安定させたり、移動するターゲットを追跡したり、観察者から異なる距離にあるターゲットに2つの目の中心窩を合わせたりするために動きます1,2。動眼行動は、少なくとも部分的には眼球運動系が単純であることから、健康と疾患の神経回路を理解するための感覚運動統合の魅力的なモデルとして広く用いられてきた3。眼球は3対の外眼筋によって制御され、眼窩内で主に3つの対応する軸を中心に回転します:横軸に沿った挙上と下降、垂直軸に沿った内転と外転、前後軸に沿ったねじれと外転1,2。このようなシンプルなシステムにより、研究者は実験室環境でマウスの動眼行動を簡単かつ正確に評価することができます。
主な動眼運動行動の1つは、視運動性反射(OKR)です。この不随意眼球運動は、網膜上の画像のゆっくりとしたドリフトまたはスリップによって引き起こされ、動物の頭部またはその周囲が動くときに網膜画像を安定させるのに役立ちます2,4。行動パラダイムとしてのOKRは、いくつかの理由で研究者にとって興味深いものです。第一に、確実に刺激し、正確に定量することができる5,6。第二に、この行動を定量化する手順は比較的単純で標準化されており、動物の大規模なコホートの視覚機能を評価するために適用することができます7。第三に、この生得的な振る舞いは高度に可塑的である5,8,9。その振幅は、反復的な網膜スリップが長時間発生する場合5,8,9、または前庭入力2によって引き起こされる網膜画像を安定化する別のメカニズムである作業パートナーの前庭眼反射(VOR)が損なわれる場合に増強され得る5。OKR増強のこれらの実験パラダイムは、研究者が眼球運動学習の根底にある回路基盤を明らかにする力を与えます。
以前の研究では、主に 2 つの非侵襲的な方法が OKR の評価に使用されてきました: (1) ビデオ眼球撮影と物理ドラムの組み合わせ 7,10,11,12,13 または (2) 仮想ドラムと組み合わせたヘッドターンの任意の決定 6,14,15,16 .これらのアプリケーションは、眼球運動可塑性の分子および回路メカニズムを理解する上で実りある発見をもたらしましたが、これら2つの方法にはそれぞれいくつかの欠点があり、OKRの特性を定量的に調べる能力が制限されています。第一に、黒と白の縞模様やドットのパターンが印刷された物理的なドラムは、視覚パターンを簡単かつ迅速に変更することができず、空間周波数、方向、移動格子のコントラストなどの特定の視覚的特徴に対するOKRの依存性の測定を大きく制限します8,17。代わりに、これらの視覚的特徴に対する OKR の選択性のテストは、視覚的特徴を試行ごとに便利に変更できるコンピューター化された視覚刺激の恩恵を受けることができます。このようにして、研究者は多次元の視覚パラメータ空間でOKRの挙動を体系的に調べることができます。さらに、OKRアッセイの2番目の方法は、識別可能なOKRをトリガーする視覚パラメータの閾値のみを報告し、目または頭の動きの振幅は報告しません6,14,15,16。したがって、定量的検出力の欠如は、同調曲線の形状と好ましい視覚的特徴の分析、または正常状態と病理学的状態における個々のマウス間の微妙な違いの検出を妨げます。上記の制限を克服するために、ビデオ眼画像とコンピューター化された仮想視覚刺激を組み合わせて、最近の研究でOKRの行動をアッセイしました5,17,18,19,20。しかし、これらの以前に発表された研究は、十分な技術的詳細やステップバイステップの指示を提供しておらず、その結果、研究者が自分の研究のためにそのようなOKRテストを確立することは依然として困難です。
ここでは、ビデオ眼球撮影とコンピュータ化された仮想視覚刺激の組み合わせにより、明所視またはスコトープ条件下でのOKR行動の視覚特徴選択性を正確に定量化するプロトコルを提示します。マウスは、前庭刺激によって引き起こされる眼球運動を避けるために頭を固定します。高速度カメラを使用して、視覚パラメータを変化させた移動する格子を見ているマウスの眼球の動きを記録します。個々のマウスの眼球の物理的大きさは、眼球運動の角度を導出する精度を確保するために較正される21。この定量的手法により、年齢や遺伝的背景の異なる動物間でOKRの行動を比較したり、薬理学的治療や視覚運動学習によって引き起こされる変化をモニタリングしたりすることができます。
プロトコル
この研究で実施されたすべての実験手順は、トロント大学動物管理委員会およびカナダ動物管理評議会によって確立されたガイドラインに従って、生物科学地域動物管理委員会によって承認されました。
1.頭蓋骨の上にヘッドバーを埋め込む
注: VOR の動作が眼球運動に寄与するのを避けるため、OKR テスト中はマウスの頭部が固定されます。そのため、頭蓋骨の上にヘッドバーを外科的に埋め込みます。
- マウス(生後2〜5ヶ月の雌雄C57BL/6)をガス室で4%イソフルラン(v/v)とO2 の混合物で麻酔する。マウスをカスタマイズされた手術プラットフォームに移し、イソフルランの濃度を1.5%〜2%に下げます。手術中のつま先つまみ反応と呼吸数をチェックして、麻酔の深さを監視します。
- 動物の体温を維持するために、動物の下に温熱パッドを置きます。両眼に潤滑剤の眼軟膏を塗って、乾燥から保護します。目をアルミホイルで覆い、光の照射から保護します。
- 痛みを軽減するために、20 mg / kgの用量でカルプロフェンを皮下注射します。.グルコン酸クロルヘキシジンスキンクリーナーで毛皮を濡らした後、頭蓋骨の上の毛皮を剃ります。露出した頭皮を70%イソプロピルアルコールとクロルヘキシジンアルコールで2回消毒します。
- 切開部位にブピバカイン(8mg/kg)を皮下注射し、ハサミで頭皮(~1cm2)を切除し、後頭前頭骨、頭頂骨、頭頂間骨を含む頭蓋骨の背側表面を露出させます。
- 露出した頭蓋骨に1%リドカインと1:100,000エピネフリンを数滴塗布して、局所的な痛みと出血を軽減します。Meyhoeferキュレットで頭蓋骨をこすり落として筋膜を取り除き、リン酸緩衝生理食塩水(PBS)で洗浄します。
注:側頭筋は頭蓋骨から分離されており、ヘッドバーを取り付けるための表面積を増やします。 - 水分がなくなり、骨が白っぽくなるまで、頭蓋骨の表面に向かって圧縮空気をそっと吹き付けて、頭蓋骨を乾かします。カットした頭皮の端を含む頭蓋骨の露出した表面に瞬間接着剤の薄い層を塗布し、続いてアクリル樹脂の層を塗布します。
注意: 瞬間接着剤を塗布する前に、頭蓋骨の表面に血液や水が付着していない必要があります。 - 頭蓋骨の上の正中線に沿ってステンレス鋼のヘッドバー( 図1Aを参照)を配置します。ヘッドバーの端から始めて、ヘッドバーのベースがアクリル樹脂に完全に埋め込まれるまで、さらにアクリル樹脂を塗布します。アクリル樹脂を2〜3回塗布して厚みを増します。
- アクリル樹脂が固まるまで15分ほど待ちます。1 mLの授乳リンガー溶液を皮下に注射します。.次に、動物が完全に動くようになるまで、マウスを加熱パッドの上に置かれたケージに戻します。
- 手術後少なくとも5日間はホームケージでマウスを回復させます。動物の体調が良いら、OKRセットアップでヘッドバーで頭を15〜30分間固定して、頭の固定と実験環境に慣れさせます。習熟を1日1回、少なくとも3日間繰り返します。
2. バーチャルドラムとビデオオキュログラフィーのセットアップ
- 3台のモニターを互いに直交して取り付け、視認空間の方位角~270°、仰角63°をカバーする正方形の筐体を形成します(図1B左)。
- ディスクリートグラフィックカードを使用して、3台のモニターをシンプルなディスプレイに統合し、すべてのモニター間で同期を確保します。
- 以下で説明するように、モニターの輝度を調整します。
- モニターが接続されているコンピューターの電源を入れ、15分間待ちます。ウォームアップは、安定した輝度を得るために不可欠です。
- モニターの明るさ設定を0から100まで25段階で体系的に変更します。
- 輝度値ごとに、輝度計を使用して、さまざまなピクセル値(0〜255、15ステップ)でモニターの輝度を測定します。
- ピクセル値 255 の輝度と明るさの関係を線形回帰で当てはめ、160 cd/m2 になる明るさの値を推定します。
- 輝度測定(ステップ2.3.3)で用いた画素値ごとに、ステップ2.3.4で導出した輝度値の輝度を線形回帰に基づいて推定します。べき関数 lum = A * pixel γ を使用して、新しい輝度値のセット (2.3.4 で導出された輝度値の下) とそれに対応するピクセル値との関係を当てはめ、ガンマ係数 γと係数 A を導出します。これらは、所望の輝度値の正弦波格子を生成するために使用されます。
- 3 台すべてのモニターの明るさを手順 2.3.4 で取得した値に設定して、同じピクセル値に対して輝度値が同じになるようにします。
- 以下で説明するように、視覚刺激ツールキットを使用して、OKR の動作を刺激するために使用される仮想ドラムを生成します。
- モニターに垂直正弦波格子を提示し、方位角に沿って周期(ストライプ間の間隔)を調整して、目への格子の投影が一定の空間周波数を持つようにします(ドラムグレーチング;図1B中と右)。
- 動物の頭がエンクロージャーの中央に固定されていることを確認して、格子が仮想ドラムの表面全体で一定の空間周波数を持っていることを確認します。
- 振動振幅、空間周波数、時間/振動周波数、方向、コントラストなど、移動回折格子のパラメータを視覚刺激コードで変更します。2種類の視覚的動きを使用する:(1)回折格子は、正弦波関数に従って振動的に時計回りまたは反時計回りにドリフトします。
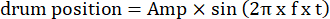
ここで、Ampはドラム軌道の振幅、fは発振周波数、tは時間(発振振幅:5°、グレーティング空間周波数:0.04-0.45cpd、発振周波数:0.1-0.8Hz、刺激のピーク速度3.14-25.12°/sに相当[ドラム速度=Amp x 2π x f x cos(2π x f x t);コントラスト: 80%-100%;平均輝度:35-45 cd / m2;(2)グレーティングは等速で一方向にドリフトします。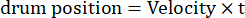
(空間周波数:0.04-0.64 cpd、時間周波数:0.25-1 Hz、ドラム速度=時間周波数/空間周波数)
- 以下の説明に従ってビデオ眼球撮影を設定します。
- 動物の視野の閉塞を避けるために、正中線から60°のところに赤外線(IR)ミラーを配置して、右目の画像を形成します。
- マウスの後ろの右側にIRカメラを配置し(図1C左)、右目の画像をキャプチャします。
- カメラアームに高速IRカメラを取り付けて、右目の画像を中心にカメラを±10°回転させます(図1C右)。
- モニターの1つに取り付けられたフォトダイオードを使用して、ビデオオキュログラフィーと視覚刺激のタイミングを同期させるための電気信号を提供します。
- グースネックアームで支えられた4つのIR発光ダイオード(LED)を右目の周りに配置して、目のIR照明を提供します。
- 角膜反射(CR)基準を提供するために、カメラに2つのIR LEDを配置します:1つはカメラの上に固定され(X-CR)、もう1つはカメラの左側(Y-CR; 図1D)。
- ビデオ眼球撮影システムの光学倍率をキャリブレーションスライドで測定します。
注: 参照 CR は、回転する眼球運動に基づいて眼角が計算されるときに、並進眼球運動を打ち消すために使用されます。
- 以下に説明するように、モニターによって形成された囲いの中央に動物の頭を固定します。
- 動物の頭をヘッドプレートでリグの中央に固定し、前を向くようにします。左右の目が水平になり、鼻と側頭が水平になるように頭の傾きを調整します(図1E)。
- 動物の右目がカメラのライブビデオに現れるまで、頭部固定装置による粗調整と2D並進ステージによる微調整によって動物の頭を水平に動かし、頭部固定装置と支柱/支柱ホルダーのペアを介して垂直に動かします。眼球運動のキャリブレーションと測定の前に、ホットミラーで反射された動物の右目の画像をカメラアームのピボットポイントに重ね合わせます(以下の手順3.4の詳細を参照)。
- OKRリグの周囲にカスタマイズされたエンクロージャーを構築して、部屋の光を遮断します(図1F)。
3.眼球運動のキャリブレーション
注:回転眼球運動は、瞳孔の動きと瞳孔運動の軌道半径(Rp、瞳孔の中心から眼球の中心までの距離)に基づいて計算されます。個々のマウスごとに、この半径は実験的に測定される21。
- ステップ2.6.1の説明に従って、3つのモニターで形成された囲いの中央に動物の頭を固定します。
- カメラの電源を入れ、右目を取り囲む4つのLEDを調整して、均一なIR照明を実現します。
- 視覚的なガイダンスの下で、手順2.6.2の説明に従って、右目の位置をビデオの中央に表示されるまで調整します。
- 以下で説明するように、右目の虚像をカメラアームのピボットポイントに合わせます。
- カメラアームを手動で左端(-10°)に回転させます。X-CRが画像の水平中央に来るまで、2D並進段階(図1C、緑色の矢印)を微調整しながら、水平面上の動物の右目の位置を光軸に垂直に手動で移動します。
- カメラアームを手動でもう一方の端(+ 10°)に回転させます。X-CRが画像の中心から離れる場合は、X-CRが中央に来るまで微調整しながら右目を動かします(図1C、青い矢印)。
- 手順3.4.1〜3.4.2を数回繰り返して、カメラアームが左右に振ったときにX-CRが中央にとどまるようにします。1回の繰り返しの途中で右目が動いた場合は、調整プロセスを再開します。
- カメラアームを中央位置にロックした後、Y-CRとX-CRの間の垂直距離を測定します。Y-CR LEDをオンにしてその位置をビデオに記録してから、X-CR LEDに切り替えてその位置を記録します。
注意: Y-CRとX-CRの間の垂直距離は、X-CR LEDのみが点灯している眼球運動の測定中にY-CRの位置を導き出すために使用されます。 - 以下で説明するように、瞳孔回転半径Rpを測定します。
- カメラアームを左端(-10°)に回転させ、瞳孔(Pp1)とX-CR(PCR1)の位置をビデオに記録します。
- 次に、カメラアームを右端(+ 10°)に回転させ、瞳孔(Pp2)とX-CR(PCR2)の位置をビデオに記録します。この手順を複数回繰り返します。
注:映画の瞳孔の動きの量がカメラアームの揺れの程度を正確に反映するように、動物の右目は各繰り返しの間静止したままにする必要があります。 - 上記で記録した値に基づいて、次の式で瞳孔回転半径Rp (図2A)を計算します。
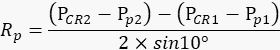
注:物理空間における角膜反射と瞳孔中心の間の距離は、ムービー内の距離に基づいて計算されます。
PCR - Pp = 動画の画素数 x カメラチップの画素サイズ x 倍率
- 以下に説明するように、Rpと瞳孔径の関係を作成します。Rpは、瞳孔が拡張または収縮すると変化します。その値は瞳孔の大きさに反比例します(図2B上)。
- モニターの輝度を0から160cd / m2 まで体系的に変更して、瞳孔サイズを調整します。
- 輝度値ごとに、手順3.6を8〜10回繰り返し、瞳孔の直径を記録します。
- 上記で測定した値に基づいて、Rpと瞳孔径の関係に線形回帰を適用し、傾きと切片を導き出します(図2B下)。
注: 時折の眼球運動によって引き起こされる外れ値は、線形フィッティングの前に除去されます。複数のセッションで繰り返し測定する場合、実験中に目が大きくならない限り、1匹の動物に対して1回だけキャリブレーションを行う必要があります。
4. OKRの眼球運動を記録する
- 手順3.1〜3.4に従って、リグにマウスをヘッド固定します。キャリブレーションが完了した直後に記録が行われる場合は、この手順をスキップしてください。カメラアームを中央の位置にロックします。
- 以下で説明するように、スコトピック OKR のモニターと動物を設定します。明所視 OKR については、この手順をスキップします。
- 各モニターの画面を、5層の1.2減光(ND)フィルムで作られたカスタマイズされたフィルターで覆います。フィルターとモニターの隙間から光が漏れないようにしてください。
- 部屋の明かりを消します。次の手順は、IRゴーグルを使用して実行されます。
- ピロカルピン溶液(生理食塩水2%)を右目に1滴塗布し、15分間待ちます。滴が目にとどまり、マウスで拭き取られないようにします。溶液が動物によって拭き取られた場合は、ピロカルピン溶液をもう一滴塗布します。.これにより、瞳孔がスコトープ条件下でのアイトラッキングに適したサイズに縮小されます。
注:スコトープ条件下では、瞳孔は大幅に拡張し、その端がまぶたの後ろに部分的に隠れます。これは、ビデオ眼球撮影による瞳孔中心の推定の精度に影響を与えます。右眼の瞳孔を薬理学的に縮小すると、その視覚入力が減少するため、視覚刺激が左眼に提示されます。 - 右目を生理食塩水で洗い流し、ピロカルピン溶液を完全に洗い流します。カーテンを引き下げて筐体を完全に密閉し、迷光がスコトープ視力に干渉するのを防ぎます。
- OKRテストを開始する前に、動物がスコトープ環境に完全に適応するために5分間与えます。
- 視覚刺激ソフトウェアと視線追跡ソフトウェアを実行します。明所視OKR測定では、ドラムグレーティングが正弦波軌道で水平に振動することを確認します。スコトープOKR測定では、ドラムグレーチングが左目から右(左目に対する側頭鼻方向)に一定の速度でドリフトすることを確認します。
注:スコトープ条件下でピロカルピンによって、左眼ではなく右眼の瞳孔が縮小した場合、振動ドラム刺激によって誘発されるOKRは非常に非対称です。このように、スコトピックOKR測定では、右目の動きをモニターしながら、左眼を刺激します。 - アイトラッキングソフトウェアは、各フレームの瞳孔サイズ、CR位置、瞳孔位置を自動的に測定し、次の式に基づいて眼位置の角度を計算します(図2C)。
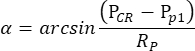
ここで、PCRはCR 位置、Ppは 瞳位置、Rpは 瞳孔回転半径である。物理空間における角膜反射と瞳孔中心の間の距離は、ムービー内の距離に基づいて計算されます。
PCR - Pp = 動画の画素数 x カメラチップの画素サイズ x 倍率
対応する瞳孔サイズのRpは、ステップ3.7.3の線形回帰モデルに基づいて導き出されます(図2B下)。
5. 視線解析ソフトによるOKRの眼球運動の解析
- メディアンフィルタ(フィルタウィンドウ = 0.05秒)を使用してアイトレースを処理し、高周波ノイズを除去します(図3A中央)。
- 以下に説明するように、サッカードまたは眼振を取り除きます。
- 眼球運動の1次導関数を計算して、眼球速度を推定します(図3A下)。50°/sの速度閾値を適用して、サッカードまたは眼振を特定します(図3A下)。
- 線形回帰に基づいて、サッカードまたは眼振の前のセグメントからこれらの高速眼球運動中の眼球位置を外挿することにより、サッカードまたは眼振を置き換えます(図3B)。
- ドラムグレーティングが振動する場合(図3C)、またはドラムグレーティングが一方向に等速で移動する場合(図3B下)は、視覚刺激中の眼球運動の平均速度を計算します。
注:フーリエ変換から得られる振動眼球運動の振幅は、正弦波関数による眼球軌道のフィッティングから得られる振幅に似ています(図3D)。 - OKR ゲインを計算します。振動ドラムの動きの場合、OKRゲインは、ドラムの動きの振幅に対する目の動きの振幅の比率として定義されます(図3C右)。ドラムの単方向動作の場合、OKRゲインは、ドラムのグレーティング速度に対するアイ速度の比として定義されます(図3B下)。
結果
上記の手順で、いくつかの視覚的特徴に対する OKR の依存関係を評価しました。ここに示すトレース例は、補足コーディング・ファイル1で提供されている分析コードを使用して導出されたもので、トレースのrawファイルの例は、補足コーディング・ファイル2にあります。ドラムグレーティングが正弦波軌道(0.4Hz)で漂流すると、動物の目は自動的に同様の振動方法で?...
ディスカッション
ここで紹介するOKR行動アッセイの方法には、いくつかの利点があります。第一に、コンピュータで生成された視覚刺激は、物理的なドラムの本質的な問題を解決します。物理的なドラムが空間周波数、方向、またはコントラストチューニングの体系的な検査をサポートしていないという問題に対処するために8、仮想ドラムはこれらの視覚的パラメータを試行的に変更するこ...
開示事項
著者らは、競合する利害関係がないことを宣言します。
謝辞
方向調整のデータを共有してくれたYingtian Heに感謝します。この研究は、Canadian Foundation of Innovation and Ontario Research Fund (CFI/ORF project no. 37597)、NSERC (RGPIN-2019-06479)、CIHR (Project Grant 437007)、Connaught New Researcher Awardsからの助成金によって支援されました。
資料
| Name | Company | Catalog Number | Comments |
| 2D translational stage | Thorlabs | XYT1 | |
| Acrylic resin | Lang Dental | B1356 | For fixing headplate on skull and protecting skull |
| Bupivacaine | STERIMAX | ST-BX223 | Bupivacaine Injection BP 0.5%. Local anesthesia |
| Carprofen | RIMADYL | 8507-14-1 | Analgesia |
| Compressed air | Dust-Off | ||
| Eye ointment | Alcon | Systane | For maintaining moisture of eyes |
| Graphic card | NVIDIA | Geforce GTX 1650 or Quadro P620. | For generating single screen among three monitors |
| Heating pad | Kent Scientific | HTP-1500 | For maintaining body temperature |
| High-speed infrared (IR) camera | Teledyne Dalsa | G3-GM12-M0640 | For recording eye rotation |
| IR LED | Digikey | PDI-E803-ND | For CR reference and the illumination of the eye |
| IR mirror | Edmund optics | 64-471 | For reflecting image of eye |
| Isoflurane | FRESENIUS KABI | CP0406V2 | |
| Labview | National instruments | version 2014 | eye tracking |
| Lactated ringer | BAXTER | JB2324 | Water and energy supply |
| Lidocaine and epinephrine mix | Dentsply Sirona | 82215-1 | XYLOCAINE. Local anesthesia |
| Luminance Meter | Konica Minolta | LS-150 | for calibration of monitors |
| Matlab | MathWorks | version xxx | analysis of eye movements |
| Meyhoefer Curette | World Precision Instruments | 501773 | For scraping skull and removing fascia |
| Microscope calibration slide | Amscope | MR095 | to measure the magnification of video-oculography |
| Monitors | Acer | B247W | Visual stimulation |
| Neutral density filter | Lee filters | 299 | to generate scotopic visual stimulation |
| Nigh vision goggle | Alpha optics | AO-3277 | for scotopic OKR |
| Photodiode | Digikey | TSL254-R-LF-ND | to synchronize visual stimulation and video-oculography |
| Pilocarpine hydrochloride | Sigma-Aldrich | P6503 | |
| Post | Thorlabs | TR1.5 | |
| Post holder | Thorlabs | PH1 | |
| PsychoPy | open source software | version xxx | visual stimulation toolkit |
| Scissor | RWD | S12003-09 | For skin removal |
| Superglue | Krazy Glue | Type: All purpose. For adhering headplate on the skull |
参考文献
- Gerhard, D. Neuroscience. 5th Edition. Yale Journal of Biology and Medicine. , (2013).
- Distler, C., Hoffmann, K. P. . The Oxford Handbook of Eye Movement. , 65-83 (2011).
- Sereno, A. B., Bolding, M. S. . Executive Functions: Eye Movements and Human Neurological Disorders. , (2017).
- Giolli, R. A., Blanks, R. H. I., Lui, F. The accessory optic system: basic organization with an update on connectivity, neurochemistry, and function. Progress in Brain Research. 151, 407-440 (2006).
- Liu, B. H., Huberman, A. D., Scanziani, M. Cortico-fugal output from visual cortex promotes plasticity of innate motor behaviour. Nature. 538 (7625), 383-387 (2016).
- Prusky, G. T., Alam, N. M., Beekman, S., Douglas, R. M. Rapid quantification of adult and developing mouse spatial vision using a virtual optomotor system. Investigative Ophthalmology & Visual Science. 45 (12), 4611-4616 (2004).
- Stahl, J. S., van Alphen, A. M., De Zeeuw, C. I. A comparison of video and magnetic search coil recordings of mouse eye movements. Journal of Neuroscience Methods. 99 (1-2), 101-110 (2000).
- Faulstich, B. M., Onori, K. A., du Lac, S. Comparison of plasticity and development of mouse optokinetic and vestibulo-ocular reflexes suggests differential gain control mechanisms. Vision Research. 44 (28), 3419-3427 (2004).
- Katoh, A., Kitazawa, H., Itohara, S., Nagao, S. Dynamic characteristics and adaptability of mouse vestibulo-ocular and optokinetic response eye movements and the role of the flocculo-olivary system revealed by chemical lesions. Proceedings of the National Academy of Sciences. 95 (13), 7705-7710 (1998).
- Cahill, H., Nathans, J. The optokinetic reflex as a tool for quantitative analyses of nervous system function in mice: application to genetic and drug-induced variation. PLoS One. 3 (4), 2055 (2008).
- Cameron, D. J., et al. The optokinetic response as a quantitative measure of visual acuity in zebrafish. Journal of Visualized Experiments. (80), 50832 (2013).
- de Jeu, M., De Zeeuw, C. I. Video-oculography in mice. Journal of Visualized Experiments. (65), e3971 (2012).
- Kodama, T., du Lac, S. Adaptive acceleration of visually evoked smooth eye movements in mice. The Journal of Neuroscience. 36 (25), 6836-6849 (2016).
- Doering, C. J., et al. Modified Ca(v)1.4 expression in the Cacna1f(nob2) mouse due to alternative splicing of an ETn inserted in exon 2. PLoS One. 3 (7), e2538 (2008).
- Shi, C., et al. Optimization of optomotor response-based visual function assessment in mice. Scientific Reports. 8 (1), 9708 (2018).
- Waldner, D. M., et al. Transgenic expression of Cacna1f rescues vision and retinal morphology in a mouse model of congenital stationary night blindness 2A (CSNB2A). Translational Vision Science & Technology. 9 (11), 19 (2020).
- Tabata, H., Shimizu, N., Wada, Y., Miura, K., Kawano, K. Initiation of the optokinetic response (OKR) in mice. Journal of Vision. 10 (1), 1-17 (2010).
- Al-Khindi, T., et al. The transcription factor Tbx5 regulates direction-selective retinal ganglion cell development and image stabilization. Current Biology. 32 (19), 4286-4298 (2022).
- Harris, S. C., Dunn, F. A. Asymmetric retinal direction tuning predicts optokinetic eye movements across stimulus conditions. eLife. 12, e81780 (2023).
- van Alphen, B., Winkelman, B. H., Frens, M. A. Three-dimensional optokinetic eye movements in the C57BL/6J mouse. Investigative Ophthalmology & Visual Science. 51 (1), 623-630 (2010).
- Stahl, J. S. Calcium channelopathy mutants and their role in ocular motor research. Annals of the New York Academy of Sciences. 956, 64-74 (2002).
- Endo, S., et al. Dual involvement of G-substrate in motor learning revealed by gene deletion. Proceedings of the National Academy of Sciences. 106 (9), 3525-3530 (2009).
- Thomas, B. B., Seiler, M. J., Sadda, S. R., Coffey, P. J., Aramant, R. B. Optokinetic test to evaluate visual acuity of each eye independently. Journal of Neuroscience Methods. 138 (1-2), 7-13 (2004).
- Burroughs, S. L., Kaja, S., Koulen, P. Quantification of deficits in spatial visual function of mouse models for glaucoma. Investigative Ophthalmology & Visual Science. 52 (6), 3654-3659 (2011).
- Wakita, R., et al. Differential regulations of vestibulo-ocular reflex and optokinetic response by β- and α2-adrenergic receptors in the cerebellar flocculus. Scientific Reports. 7 (1), 3944 (2017).
- Dehmelt, F. A., et al. Spherical arena reveals optokinetic response tuning to stimulus location, size, and frequency across entire visual field of larval zebrafish. eLife. 10, e63355 (2021).
- Magnusson, M., Pyykko, I., Jantti, V. Effect of alertness and visual attention on optokinetic nystagmus in humans. American Journal of Otolaryngology. 6 (6), 419-425 (1985).
- Collins, W. E., Schroeder, D. J., Elam, G. W. Effects of D-amphetamine and of secobarbital on optokinetic and rotation-induced nystagmus. Aviation, Space, and Environmental Medicine. 46 (4), 357-364 (1975).
- Reimer, J., et al. Pupil fluctuations track fast switching of cortical states during quiet wakefulness. Neuron. 84 (2), 355-362 (2014).
- Sakatani, T., Isa, T. PC-based high-speed video-oculography for measuring rapid eye movements in mice. Neuroscience Research. 49 (1), 123-131 (2004).
- Sakatani, T., Isa, T. Quantitative analysis of spontaneous saccade-like rapid eye movements in C57BL/6 mice. Neuroscience Research. 58 (3), 324-331 (2007).
- Vinck, M., Batista-Brito, R., Knoblich, U., Cardin, J. A. Arousal and locomotion make distinct contributions to cortical activity patterns and visual encoding. Neuron. 86 (3), 740-754 (2015).
- Bradley, M. M., Miccoli, L., Escrig, M. A., Lang, P. J. The pupil as a measure of emotional arousal and autonomic activation. Psychophysiology. 45 (4), 602-607 (2008).
- Hess, E. H., Polt, J. M. Pupil size as related to interest value of visual stimuli. Science. 132 (3423), 349-350 (1960).
- Di Stasi, L. L., Catena, A., Canas, J. J., Macknik, S. L., Martinez-Conde, S. Saccadic velocity as an arousal index in naturalistic tasks. Neuroscience and Biobehavioral Reviews. 37 (5), 968-975 (2013).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved