Riproducibilità e armonizzazione nella ricerca utilizzando standard biologici: l'esempio del peptide correlato al collagene agonista piastrinico
In questo articolo
Riepilogo
Qui presentiamo un metodo per standardizzare il peptide correlato al collagene agonista piastrinico cross-linked (CRP-XL) utilizzando l'aggregometria a trasmissione luminosa. Sebbene il protocollo sia mirato alla funzione piastrinica, il processo sperimentale può essere applicato alla maggior parte delle molecole biologiche e dei saggi biologici per garantire rigore scientifico e riproducibilità.
Abstract
La metrologia - la scienza della misura - è una materia che pochi scienziati biologici vengono istruiti nella loro formazione a loro danno; L'applicazione di semplici processi di standardizzazione alle pratiche di lavoro quotidiane fornisce fiducia nei dati e riproducibilità a distanza e nel tempo.
Questo metodo dimostra come standardizzare un esperimento di laboratorio di base ampiamente utilizzato nella ricerca sull'emostasi e nella pratica clinica, in particolare, misurando le risposte al peptide correlato al collagene agonista del recettore piastrinico (glicoproteina [GP]VI), reticolato (CRP-XL) mediante aggregometria a trasmissione luminosa (LTA). L'utilizzo di questo approccio garantirà la riproducibilità intra-laboratorio e l'armonizzazione inter-laboratorio, indipendentemente dallo stock o dal fornitore di agonisti. È importante sottolineare che questo metodo è applicabile ad altri agonisti piastrinici e, in effetti, a molte altre molecole biologiche e saggi biologici.
Il processo descritto di seguito prevede la creazione di una serie di diluizioni a 6-8 punti dello "standard" e del "test" (il materiale che si sta controllando) e l'esecuzione fianco a fianco in un saggio scelto (in questo caso, LTA). Il CRP-XL viene utilizzato a concentrazioni di massa/volume, ma non tutti i materiali danno la stessa attività biologica a una data concentrazione, quindi viene effettuata una serie di diluizioni per confrontare il materiale standard e quello di prova e determinare quale concentrazione è necessaria per dare un'attività equivalente. La serie di diluizione deve estendersi da 0 a 100% di aggregazione. I dati vengono tracciati utilizzando la regressione non lineare e viene determinato il valore EC50 di ciascun campione (standard e test). Per assegnare l'attività, dividere il valore EC50 dello standard per quello del test per determinare quanto è più o meno potente e regolare la concentrazione di conseguenza. Questo approccio garantirà che la stessa "attività" biologica venga aggiunta al test più e più volte.
Introduzione
Molti di noi usano agonisti e antagonisti biologici nei nostri esperimenti, il più delle volte in un saggio biologico che quantifica il loro effetto sulla funzione cellulare in condizioni specifiche. Il metodo qui descritto è per l'agonista piastrinico collagene-related peptide, cross-linked (CRP-XL), un agonista della glicoproteina VI che attiva le piastrine e la cui attività può essere misurata in una varietà di saggi (aggregometria a trasmissione luminosa, microscopia, citometria a flusso, rilascio di Ca2+ , ecc.), ma il protocollo di standardizzazione dell'agonista è applicabile a qualsiasi agonista/antagonista biologico e/o biodosaggio. Le scienze fisiche sono esperte nell'uso degli standard nelle loro pratiche di lavoro quotidiane e le aziende che sviluppano farmaci bioterapeutici nel settore commerciale comprendono il valore dell'utilizzo di standard di riferimento1, ma rimangono sottoutilizzati da molti scienziati biologici, specialmente nella comunità di ricerca accademica, e la loro mancanza di utilizzo ha un impatto negativo sulla qualità della produzione scientifica.
CRP-XL è un agonista specifico specifico per GPVI che il campo piastrinico ha utilizzato per decenni dalla sua descrizione nel 19952, aiutando la comunità a delineare il ruolo di GPVI da quello di altre proteine piastriniche leganti il collagenesin da 3,4. Questo agonista può essere procurato da una varietà di fonti commerciali o prodotto internamente. Il monomero peptidico può essere acquistato da un fornitore e poi reticolato internamente oppure può essere fatto dal fornitore a un costo aggiuntivo. Un ulteriore risparmio sui costi può essere ottenuto riducendo la purezza richiesta al momento della consegna (70% contro 95%, ad esempio). Inoltre, non c'è consenso su come il CRP-XL dovrebbe essere conservato, con alcuni che optano per la crioconservazione e altri per la refrigerazione, alcuni mantengono il materiale liofilizzato fino all'uso e altri lo conservano in soluzione (acqua o tampone, a seconda delle preferenze). Pertanto, la qualità e la composizione delle scorte di laboratorio non sono standardizzate o armonizzate. Poiché questo agonista viene utilizzato a una concentrazione definita (massa/volume) piuttosto che a unità di attività, la potenza di CRP-XL in un laboratorio, ad esempio a 1 μg/mL, non sarà la stessa di un altro. Vale la pena notare che altri agonisti piastrinici utilizzati nel campo sono già standardizzati (ad esempio, la trombina, che viene fornita e utilizzata in unità di attività piuttosto che in massa/volume), quindi il passaggio da massa/volume a unità di biologico non dovrebbe essere troppo impegnativo per la comunità. Va inoltre notato che le risposte dei pazienti agli agonisti piastrinici, inclusa la CRP-XL, sono variabili in termini di sensibilità agli agonisti e di capacità di risposta (entità della risposta)5, quindi è ancora più importante utilizzare quantità costanti di attività agonista nei test.
Se gli agonisti piastrinici possono essere armonizzati utilizzandoli in un'attività definita piuttosto che in peso/volume, si può garantire che un esperimento in un laboratorio sia direttamente paragonabile a quello in altri laboratori e possa essere riprodotto accuratamente con sicurezza. Fino a quando il settore non raggiungerà un accordo su come immagazzinare e standardizzare l'attività di CRP-XL, è essenziale eseguire controlli regolari sul materiale per garantirne la coerenza nel corso dei mesi/anni in cui viene utilizzato.
L'assegnazione del valore di attività per gli standard biologici deve essere effettuata attraverso studi collaborativi multicentrici (ad esempio 6,7) e richiede competenze specialistiche. La necessità di stabilire standard biologici per gli agonisti piastrinici è stata recentemente evidenziata da uno studio multicentrico collaborativo8 sostenuto dalla Società Internazionale per la Trombosi e l'Emostasi (ISTH); fino a quando non sarà disponibile uno standard internazionale CRP-XL, i ricercatori possono standardizzare il proprio materiale a livello locale per garantire la coerenza nel tempo e che il nuovo materiale proveniente commercialmente o internamente sia di attività paragonabile alle preparazioni precedenti, così come a quelle del resto della comunità.
Protocollo
Il sangue deve essere raccolto da volontari sani consenzienti e trattato in conformità con le norme locali. Questo protocollo misura l'aggregazione piastrinica indotta da agonisti nel plasma ricco di piastrine (PRP) mediante aggregometria a trasmissione luminosa (LTA). L'ISTH fornisce protocolli standardizzati, tra cui un metodo del 2013 per la preparazione del PRP e LTA9. Raccogliere il sangue intero in citrato di sodio al 4% secondo le raccomandazioni ISTH in conformità con le regole del comitato etico locale. Escludere i donatori che hanno assunto FANS nelle ultime 2 settimane.
1. Procedura di analisi
- Prelevare un'aliquota di CRP-XL di riserva e diluirla nel tampone del saggio (Tyrodes10) (Tabella 1) fino a una concentrazione iniziale che provochi la massima aggregazione (vedere la NOTA al punto 1.3).
NOTA: In letteratura, una concentrazione di 1 μg/mL induce la massima aggregazione, ma alcuni laboratori hanno bisogno di concentrazioni più elevate per ottenere lo stesso effetto: regolare di conseguenza la serie di diluizione - Effettuare una serie di diluizioni corrispondente con lo standard (vedere la NOTA sotto il punto 1.3 e la Figura 1) in modo che le concentrazioni siano le stesse del reagente in esame.
- Produrre una serie di diluizioni da 6 a 8 punti per il test e lo standard, sempre nel tampone del saggio, che porta la risposta di aggregazione dal 100% allo 0% di aggregazione. Un esempio che mostra una curva di concentrazione della serie di diluizione a 8 punti è mostrato nella Tabella 2.
NOTA: Alcuni laboratori aggiungono un agonista a un volume totale del 10%, ad esempio 50 μL di agonista a 450 μL di piastrine, in modo tale da diluire una concentrazione 10x a una concentrazione finale di 1x nel saggio, mentre altri aggiungono volumi più piccoli (più concentrati) di agonista, ad esempio 5 μL di agonista a 495 μL di piastrine - assicurarsi solo che la serie di diluizione sia appropriata per il test tenendo presente come lo spostamento di volume influisce sulla concentrazione piastrinica - ancora una volta, sii coerente. Nell'esempio, 30 μL di agonista 10x vengono aggiunti a 270 μL di plasma ricco di piastrine (PRP). - Una volta che le piastrine sono riposate e pronte per l'uso, aliquotarle in cuvette LTA, aggiungere una barra di agitazione e lasciare che raggiungano i 37 °C nei pozzetti di contenimento.
- Una volta raggiunta la temperatura, posizionare le cuvette nell'aggregometro e iniziare a registrare le tracce. Aggiungere l'agonista (con agitazione) e registrare i dati.
- Ripetere il passaggio 1.4 per ciascuna concentrazione della prova e dello standard fino a quando non sono stati raccolti i dati necessari per tracciare le curve (curve di esempio mostrate nella Figura 2).
- Calcolare la potenza del reagente in esame rispetto a quella dello standard; Anche in questo caso, utilizzare qualsiasi metrica (aggregazione massima o area sotto la curva), purché vi sia coerenza e il modello di analisi si adatti in modo appropriato ai dati.
2. Controllo delle curve di concentrazione
- Innanzitutto, verificare che le curve concentrazione-risposta siano parallele. Esistono molti pacchetti software che lo fanno, ma qui il processo è descritto per Graphpad Prism (vedere la Figura 3).
- Immettere i dati in modo che log(concentrazione) si trovi sull'asse X e la risposta (% aggregazione massima/AUC) sia sull'asse Y (Figura 3A)
- Trasformare le concentrazioni di CRP-XL (Figura 3B)
- Selezionare Regressione non lineare dalle funzioni di analisi e utilizzare l'equazione per la stimolazione/inibizione dose-risposta.
- Selezionare log (agonista) rispetto alla risposta (pendenza variabile) - utilizzare l'adattamento a 3 o 4 vie a seconda di quale sia il migliore per i dati.
- Determinare se le curve sono parallele utilizzando la scheda Confronta (come mostrato nella Figura 3C) e fare clic sul pulsante per confrontare i set di dati per assicurarsi che la pendenza (pendenza Hill) e gli asintoti (la parte superiore e inferiore delle curve) siano equivalenti. In questo esempio, la pendenza di Hill per il test è 2,279 e quella dello standard è 2,025 con un rapporto di 1,125.
- Se i pendii sono paralleli (ad esempio, un criterio di accettazione del rapporto di pendenza compreso tra 0,8 e 1,25) e gli asintoti sono equivalenti, procedere con il calcolo della potenza (EC50) utilizzando i passaggi 2.1.3 e 2.1.4. Nell'esempio mostrato qui, gli asintoti sono stati vincolati poiché la valutazione nel passaggio 2.1.5 ha confermato che gli asintoti sono equivalenti.
- Dividere il valore EC50 dello standard per quello del test per determinare la potenza relativa. Nell'esempio mostrato qui, test/standard (0,07259/0,1498) = 0,4846, cioè il 'test' è potente la metà dello standard.
- Regolare le concentrazioni di massa/volume per tenere conto della differenza di potenza, ad esempio, se lo standard è stato utilizzato in precedenza a 1 μg/mL, il nuovo materiale verrebbe utilizzato a 1/0,4846 = 2,063 μg/mL) per garantire che negli esperimenti vengano utilizzate quantità comparabili di materiale attivo
Risultati
La Figura 1 è una rappresentazione schematica di una serie di diluizioni e ha lo scopo di evidenziare che una serie di diluizioni è necessaria sia per lo standard che per il test. La Figura 2A mostra le tracce di aggregazione per lo standard, mentre i dati di test sono mostrati nella Figura 2B. A 0,075 μg/mL, c'è una risposta chiara allo standard, mentre per il test, la concentrazione corrispondente (0,075 μg/mL) è piatta, cioè nessuna risposta. Questi dati vengono utilizzati per tracciare i grafici successivi per ottenere l'EC50. Nell'esempio mostrato qui, è stata utilizzata l'aggregazione massima del 100% per tracciare la curva concentrazione-risposta e determinare EC50, come mostrato nella Figura 3.
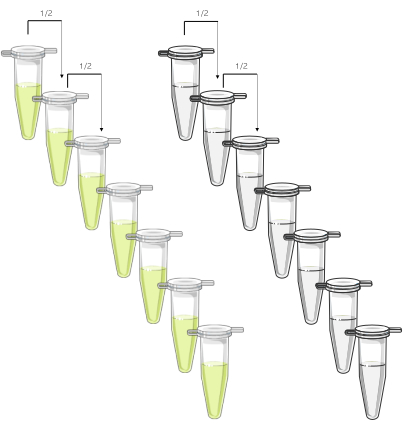
Figura 1: Descrizione grafica delle due serie di diluizioni del test (a sinistra) e dello standard (a destra). A partire dalla concentrazione massima (concentrazione consigliata: 10 μg/mL CRP-XL), le diluizioni sequenziali 1 su 2 vengono effettuate in parallelo su 8 punti (>3 unità logaritmiche). Fare clic qui per visualizzare una versione più grande di questa figura.
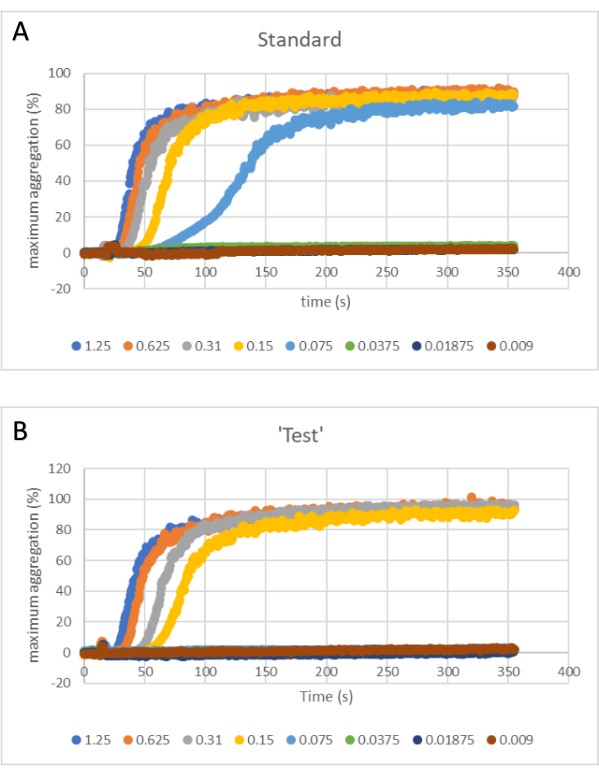
Figura 2: Tracce di aggregazione per la serie di diluizioni standard (a sinistra) e di prova (a destra). Man mano che l'aggregazione piastrinica procede (asse x), la quantità di luce che passa attraverso il campione e raggiunge il sensore aumenta (asse y). (A) Norma. (B) Test. Fare clic qui per visualizzare una versione più grande di questa figura.
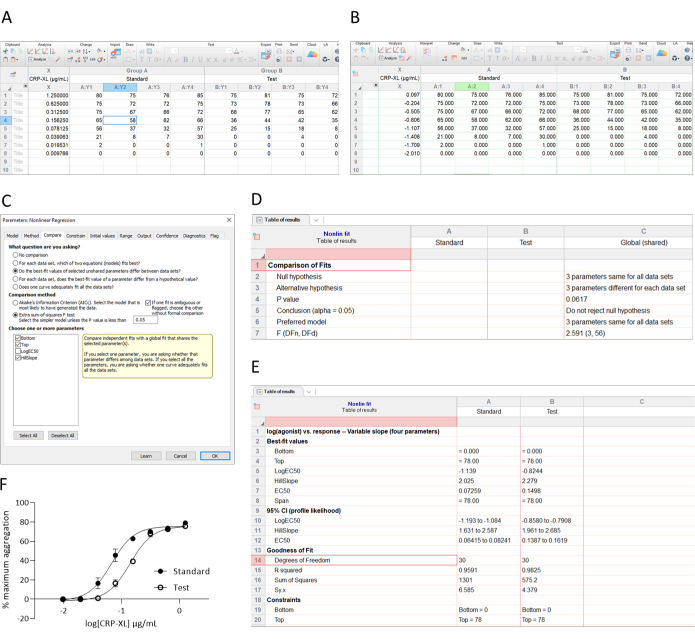
Figura 3: Inserimento e analisi dei dati. (A) I dati vengono inseriti, (B) trasformati e (C,D) analizzati per il parallelismo (chiedere al software di dire se le pendenze e gli asintoti di Hill sono comparabili [C]). (E) Se le curve sono parallele, determinare la potenza (EC50) utilizzando l'adattamento della curva di regressione non lineare. (F) Dati trasformati tracciati. Si prega di fare riferimento al metodo per maggiori dettagli. Fare clic qui per visualizzare una versione più grande di questa figura.
| Tampone dei tidi9 | ||
| Costituenti | Concentrazione | Commenti |
| NaCl | 134 millimetri | |
| Na2HPO4 | 0,34 mM | |
| Kcl | 2,9 millimetri | |
| NaHCO3 | 12 milioni di minuti | |
| Acido 4-(2-idrossietil)-1-piperazineetanosolfonico (HEPES) | 20 millimetri | |
| Glucosio | 5 milioni di metri | |
| MgCl2 | 1 millimetro | pH 7,3 |
Tabella 1: Composizione del tampone dei tirodi.
| Serie di diluizione a 8 punti | |
| Diluizione 1 | 10 μg/mL |
| Diluizione 2 | 5 μg/mL |
| Diluizione 3 | 2,5 μg/mL |
| Diluizione 4 | 1,25 μg/mL |
| Diluizione 5 | 0,625 μg/mL |
| Diluizione 6 | 0,3125 μg/mL |
| Diluizione 7 | 0,15625 μg/mL |
| Diluizione 8 | 0,073125 μg/mL |
Tabella 2: Un esempio che mostra una serie di diluizioni a 8 punti.
Discussione
Come mostrato qui, il processo di standardizzazione dei materiali è molto semplice. Sebbene richieda un po' di tempo per valutare nuovi lotti di materiale e/o per verificare che il lotto corrente sia stabile e non perda attività nel tempo, la ricompensa è che gli esperimenti sono riproducibili più e più volte e confrontabili nel corso degli anni piuttosto che solo la durata di un lotto di reagenti. Significa anche che altri ricercatori possono ricreare accuratamente le condizioni del saggio e che la comunità è armonizzata a livello globale. Le fasi critiche del protocollo includono la raccolta del sangue intero e la preparazione del PRP9, nonché la precisione durante la realizzazione della serie di diluizione. È inoltre importante assicurarsi che le curve di prova e standard siano parallele prima di procedere con il confronto EC50 . Se le linee non sono parallele o gli asintoti non sono equivalenti, potrebbe indicare che il materiale di prova e quello standard sono diversi in una certa misura.
Chiunque lavori nelle scienze biologiche sa che i saggi biologici non sempre funzionano in modo coerente, quindi è necessario essere consapevoli di questo quando si valutano i dati. Nell'esempio mostrato qui, anche se stiamo usando gli stessi donatori per misurare la potenza di due materiali molto simili, se non identici, i pendii e gli asintoti della collina non sono identici. Tuttavia, accettiamo un certo grado di variabilità e concludiamo che le curve sono, in questo caso, parallele, e quindi adatte per confrontare e regolare la potenza. Le molecole biologiche sono grandi e complesse e le modifiche post-traduzionali durante la produzione possono influenzare la loro potenza nei saggi biologici. La standardizzazione delle biomolecole e dei saggi biologici non può essere effettuata utilizzando solo la massa o il volume e deve essere effettuata quantificando e confrontando l'attività biologica in un test biologico11. È necessario utilizzare la propria formazione ed esperienza per valutare i dati nel contesto del saggio.
I limiti della tecnica sono che, sebbene i dati possano indicare un problema con i reagenti, non possono indicare quale sia il problema. Saranno necessari ulteriori studi per determinare il motivo per cui i materiali non sono comparabili. In un mondo ideale, qualsiasi materiale critico per gli esperimenti e le successive conclusioni scientifiche verrebbe verificato mediante spettroscopia di massa, ma questa non è sempre un'opzione. Tuttavia, se i dati non sono comparabili, sono comunque necessarie ulteriori indagini. Un altro limite di questo approccio è il tempo e le risorse necessarie per farlo. Idealmente, il test e lo standard dovrebbero essere confrontati in 3-6 donatori per fornire una certa sicurezza nell'assegnazione dell'attività biologica al materiale, ma riteniamo che ciò sia giustificato dal supporto della riproducibilità e dell'affidabilità. La standardizzazione del materiale biologico non è necessaria ogni volta che vengono eseguiti esperimenti, ma come minimo, dovrebbe essere fatta per ogni nuovo lotto di agonisti, preferibilmente più frequentemente, a seconda della stabilità e dell'uso. In effetti, se uno standard dovesse essere reso disponibile, questo è qualcosa su cui le organizzazioni internazionali di standardizzazione possono fare chiarezza.
Mentre l'esempio mostrato qui è per CRP-XL nel contesto della misurazione dell'aggregazione piastrinica, il protocollo di confronto dell'attività biologica delle biomolecole nei saggi biologici è ampiamente applicabile in tutto il settore.
Divulgazioni
Gli autori non hanno nulla da dichiarare.
Riconoscimenti
Nessuno.
Materiali
| Name | Company | Catalog Number | Comments |
| 4% sodium citrate | Sigma-Aldrich | S1804 | Anticoagulant dissolved in water9 |
| 4-(2- hydroxyethyl)-1-piperazineethanesulfonic acid (HEPES) | Sigma-Aldrich | 54457 | |
| CRP-XL | Peptide Protein Research Ltd. | A crosslinked, triple-helical peptide2,4 with the sequence GCP*(GPP*)GCP*G (single letter amino acid code: P* = hydroxyproline was obtained as a custom order from Peptide Protein Research Ltd. | |
| Cuvettes and stir bars | Stago | 86921 | Consumables for aggregometer |
| Glucose | Sigma-Aldrich | G7021 | |
| KCl | Sigma-Aldrich | P5405 | |
| MgCl2 | Sigma-Aldrich | M4880 | |
| Na2HPO4 | Sigma-Aldrich | S5136 | |
| NaCl | Sigma-Aldrich | Sigma-Aldrich | |
| NaHCO3 | Sigma-Aldrich | S6014 | |
| Prism | Graphpad | Analysis software package | |
| Platelet rich plasma | Isolated from whole blood from healthy volunteers free of non-steroidal anti-inflammatory drugs for a minimum of 10 days8. |
Riferimenti
- Faya, P., et al. Potency assignment of biotherapeutic reference standards. Journal of Pharmaceutical and Biomedical Analysis. 191, 113577 (2020).
- Morton, L. F., et al. Integrin alpha 2 beta 1-independent activation of platelets by simple collagen-like peptides: collagen tertiary (triple-helical) and quaternary (polymeric) structures are sufficient alone for alpha 2 beta 1-independent platelet reactivity. The Biochemical Journal. 306 (2), 337-344 (1995).
- Pugh, N., et al. Synergism between platelet collagen receptors defined using receptor-specific collagen-mimetic peptide substrata in flowing blood. Blood. 115 (24), 5069-5079 (2010).
- Farndale, R. W., et al. Cell-collagen interactions: the use of peptide Toolkits to investigate collagen-receptor interactions. Biochemical Society Transactions. 36 (Pt 2), 241-250 (2008).
- Dunster, J. L., et al. Multiparameter phenotyping of platelet reactivity for stratification of human cohorts. Blood Advances. 5 (20), 4017-4030 (2021).
- Hubbard, A. R., et al. Establishment of the WHO 2nd International Standard Factor V, plasma (16/374): communication from the SSC of the ISTH. Journal of Thrombosis and Haemostasis. 17 (4), 695-697 (2019).
- Sergaki, C., et al. Developing whole cell standards for the microbiome field. Microbiome. 10 (1), 123 (2022).
- Alessi, M. C., et al. Multi-center evaluation of light transmission platelet aggregation reagents: Communication from the ISTH SSC Subcommittee on Platelet Physiology. Journal of Thrombosis and Haemostasis. (23), (2023).
- Cattaneo, M., et al. Recommendations for the standardization of light transmission aggregometry: A consensus of the working party from the platelet physiology subcommittee of SSC/ISTH. Journal of Thrombosis and Haemostasis. , (2013).
- Taylor, L., et al. Discovery of novel GPVI receptor antagonists by structure-based repurposing. PLoS One. 9 (6), e101209 (2014).
- Coxon, C. H., Longstaff, C., Burns, C. Applying the science of measurement to biology: Why bother. PLoS Biology. 17 (6), e3000338 (2019).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon