このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
アイソフォーム特異的レチノイン酸受容体による生きた神経細胞ミトコンドリアの恒常性調節の最適化された自動解析(英語)
要約
ミトコンドリアネットワークは非常に複雑で、解析が非常に困難です。新しいMATLABツールは、タイムラプス画像でライブ共焦点画像化されたミトコンドリアを解析しますが、出力量が大きく、個別の手動操作が必要です。この問題に対処するために、ルーチン最適化が開発され、迅速なファイル分析が可能になりました。
要約
ミトコンドリアネットワークが複雑なため、生細胞のセグメント化、追跡、解析が非常に困難です。MATLAB ツールを使用すると、タイムラプス ファイル内のミトコンドリアを解析できるため、画像処理のプロセスが大幅に簡素化され、高速化されます。それにもかかわらず、既存のツールは大量の出力を生成するため、個々の手作業による注意が必要であり、基本的な実験セットアップでは数千のファイルが出力され、それぞれが広範で時間のかかる処理を必要とします。
これらの問題に対処するために、MATLAB コードとライブ スクリプト形式の両方でルーチン最適化が開発され、迅速なファイル解析が可能になり、ドキュメントの読み取りとデータ処理が大幅に削減されました。100ファイル/分の速度で、最適化により全体的に迅速な分析が可能になります。最適化では、個々のミトコンドリアのフレーム固有のデータを時間枠全体で平均化し、既存のツールからの出力と一致する定義された方法でデータを分析することにより、結果出力を達成します。色素テトラメチルローダミンメチルエステルを使用してライブ共焦点イメージングを行い、神経細胞をレチノイン酸受容体(RAR)アゴニストで処理することにより、ルーチンの最適化を検証しました。結果は文献と一致しており、アイソフォーム特異的RAR調節に応答するミトコンドリアネットワークの挙動をさらに特徴付けることができました。
この新しい方法論により、ニューロン全体のミトコンドリアネットワークの迅速で検証済みの特性評価が可能になりましたが、神経科学分野に適用するために不可欠な機能である軸索と細胞体ミトコンドリアの分化も可能になりました。また、速効性治療を用いた実験にも適用でき、治療前後で同じ細胞のイメージングが可能で、神経科学の分野を超越しています。
概要
細胞ミトコンドリアはあらゆる生理状態の中心に位置しており、がんやアルツハイマー病など幅広い疾患の薬理学的治療法を特定するためには、ミトコンドリアの恒常性(ミトスタシス)と挙動を完全に理解することが最も重要です1,2。
ミトコンドリアは、エネルギー恒常性、ATP生成、カルシウム緩衝、ROS調節において重要な細胞の役割を担っており、分子シャペロンはエネルギー依存性であるため、タンパク質の恒常性を維持するためには有糸分裂が不可欠です3。これらには、細胞のニーズを効率的に満たすために、一定かつ動的なネットワークの変調と適応が必要であり、ミトコンドリアの輸送はさまざまなシグナル伝達経路によって制御されています。以前の研究では、そのような経路の1つであるレチノイン酸受容体(RAR)4,5が説明されています。レチノイン酸(RA)は、RAR活性化を介して軸索および神経突起の成長を促進します。マウスの初代皮質ニューロンでは、RAR-βの活性化により、神経突起におけるミトコンドリアの成長、速度、および可動性が促進される6。
ミトコンドリアネットワークの適応性と動態を考慮すると、エネルギー恒常性を調べるだけでなく、プロテオスタシス、細胞の健康、増殖、シグナル伝達を調べるためにも、有糸分裂を「リアルタイム」で評価する可能性が不可欠です。有糸分裂を評価するために一般的に使用される方法は、蛍光色素またはマーカーを使用してミトコンドリアを強調した後の共焦点顕微鏡検査、および温度および/またはCO2調節を可能にする特定の顕微鏡検査セットアップに依存しています7。このタイプの実験セットアップでは、一度に1つの実験の複製を実行する必要があります。さまざまな処理の実験の繰り返しに加えて、ほとんどの実験では、一連の焦点面(zスタック)を一連の時点で記録して、技術的な複製(プレートごとに複数の位置を画像化)を行う必要があることを考慮する必要があります。したがって、1 つのコントロールと 2 つの処理を 3 回繰り返し、プレートごとに 5 つのイメージング位置、15 のタイムポイントを使用する実験計画では、225 スタックが処理されます。古典的には、生きたミトコンドリアのビデオは、キモグラフをプロットして分析され、個別に分析される8が、コンピュータツールに頼る場合でも、大量の手入力を必要とする時間のかかるプロセスであった。
最近、生細胞の2Dおよび3Dタイムラプスファイルにおけるミトコンドリアの自動セグメンテーションと追跡を可能にするアルゴリズムが 記述されました9。他の定量化手法も利用可能であり、すべてに限界があります10。自動化されたオープンソースアプリケーションであるMitometerは、タイムラプスやミトコンドリアダイナミクス分析に特に適しています。このアプリケーションには、他の既存のMATLABベースのツールに比べて、最大13の異なるパラメータを使用して個々のTIFスタックを自動処理できるという一連の利点があり、核周辺ミトコンドリアと遠隔核ミトコンドリアを区別するため、神経科学にとって特に興味深いものです。
ただし、上記のような実験では、これら 13 個のパラメーターを 225 個のスタックに適用すると、2,925 個の個別の出力ファイルが作成されます。これらには4つの個別のコンピューター入力が必要であり、すべての出力ファイルをダウンロードするには合計で10,000を超える手動入力が必要です。大規模な実験計画では、各ファイルの解析とデータ統合に不必要に非常に時間がかかります。ここでは、迅速なファイル分析を可能にし、ドキュメントの読み取りとデータ処理を大幅に削減し、既存のツールからの出力と一貫性のある定義された方法でデータを分析できるルーチン最適化を紹介します。
プロトコル
注:このプロトコルには、細胞培養とライブ共焦点顕微鏡検査で生きたミトコンドリア(図1)の画像を得るウェットラボステップと、得られた画像(図2)を分析するインシリコステップの2つの主要なステップがあります。3Dライブ画像化されたミトコンドリアの自動データ解析には、Lefebvreらが提供するMATLABアプリケーションMitometerを使用しました9。ルーチン最適化は MATLAB で記述されます。ソフトウェア、更新バージョン、および処理 ImageJ マクロは、https://github.com/JoseJoaoMV/Routine_Optimization_Mitometer_APP_MATLAB の GitHub からオンラインで無料で入手できます。
1. ライブ顕微鏡
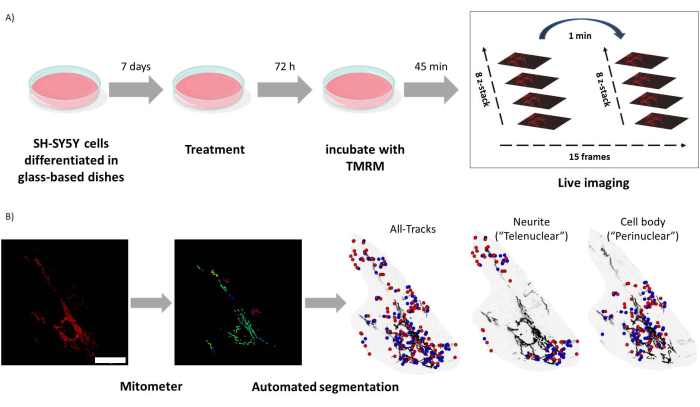
図1:実験プロトコル。SH-SY5Y細胞を分化させ、レチノイドで処理した。 (A)TMRMを用いて、共焦点顕微鏡を用いて処理細胞内の健康なミトコンドリアをライブイメージングし、5視野のタイムラプスZスタックを撮影した。(B)マイトメーターアプリケーション MATLAB は、ミトコンドリア画像を自動的にセグメント化して解析します。このソフトウェアは、分析に加えて、核の近接性に応じてミトコンドリアを自動的に識別します。青い点はミトコンドリアの初期位置です。赤い点は最終位置です。スケールバー = 30 μm。略語:TMRM =テトラメチルローダミン、メチルエステル。 この図の拡大版をご覧になるには、ここをクリックしてください。
- 細胞培養
- SH-SY5Y細胞を5%CO2 および95%空気の加湿雰囲気中で37°Cでインキュベートし、MEM(Minimal Essential Medium)およびF12(Ham's F12 Nutrient Mix)培地を等量ずつ培養し、10%ウシ胎児血清(FBS)を添加します。
- SH-SY5Y細胞をガラス底の細胞皿に15×104 細胞/mLの密度で播種します。
- 1% FBS含有培地中で10 μMの オールトランス レチノイン酸で5日間処理し、続いて10 ƞg/mLの脳由来神経栄養因子(BDNF)で2日間処理して細胞を分化させます。
- 細胞処理
- 細胞を滅菌リン酸緩衝生理食塩水(PBS)で洗浄し、10-7 M RARアイソフォームアゴニストで、MEM(Minimal Essential Medium)およびF12(Ham's F12 Nutrient Mix)培地を等量で72時間処理し、1%FBSを添加します。
注:使用したRARαアゴニストはAM580でした。使用したRARβアゴニストはCD2314でした。Ch55はRARαおよびβアゴニストとしてアゴニストとして使用されました。 でRAはポジティブコントロールとして使用されました。BMS493はRAR 汎アンタゴニストとして使用されました。
- 細胞を滅菌リン酸緩衝生理食塩水(PBS)で洗浄し、10-7 M RARアイソフォームアゴニストで、MEM(Minimal Essential Medium)およびF12(Ham's F12 Nutrient Mix)培地を等量で72時間処理し、1%FBSを添加します。
- ライブ共焦点イメージング
- 培地を、20 nMテトラメチルローダミン、メチルエステル(TMRM)を含む新鮮な1%FBS含有培地と交換し、45分間加熱します。
注:TMRMは細胞透過性蛍光色素であり、活性ミトコンドリアによって隔離され、このインキュベーション期間により、TMRMは平衡に達し、分極ミトコンドリアに取り込まれます11。イメージング中にTMRM信号強度が人為的に増加する可能性があるため、平衡が確立される前にイメージングを開始する必要があります。 - レーザー走査型共焦点顕微鏡に取り付けたインキュベーターに細胞を37°Cで入れます。
- 63倍油浸アポクロマート対物レンズを使用して画像を撮影し、画像サイズは512 x 512ピクセルで、ピンホール開口は1エアリーユニットで、各細胞プレートの5つの異なる視野から15フレームの時系列をキャプチャし、8つの等距離z平面のzスタックをキャプチャします。結果の .lsm ファイルは、時間、位置、および Z スタックです。
注:ゲイン、コントラスト、および輝度の設定は、検出器のダイナミックレンジ全体を使用するために必要な最小限のレーザー出力を使用して最初に最適化し、研究全体を通して一定に保ち、すべてのイメージングが同じ条件下で実行されるようにする必要があります。このハードウェアとソフトウェアの組み合わせで最大9つの異なる位置を記録でき、顕微鏡はイメージング位置を自動的に切り替えます。
- 培地を、20 nMテトラメチルローダミン、メチルエステル(TMRM)を含む新鮮な1%FBS含有培地と交換し、45分間加熱します。
2. 画像解析
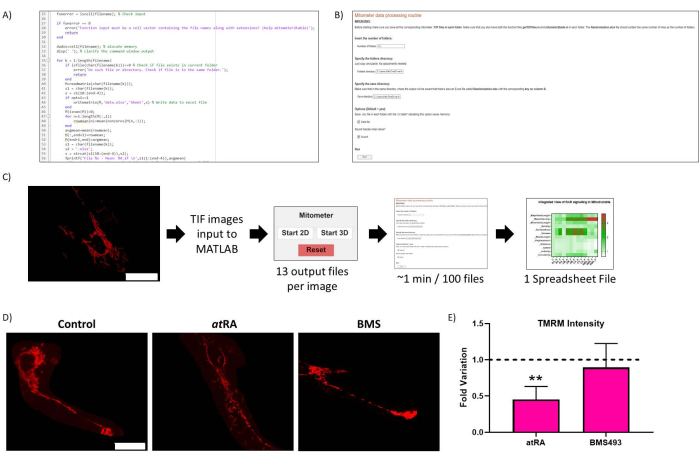
図2:ルーチンの最適化。 (A)ルーチン最適化の代表的なコード。(B) ルーチン最適化 Live-Script。(C)ルーチン最適化ワークフロー。(D)ルーチン最適化結果のバリデーション:未処理細胞中のミトコンドリアの代表画像(左パネル)、atRAで処理(10-7 M、72時間、中央パネル)、RARアンタゴニストBMS493で処理(10-7 M、72時間、右パネル)、TMRMでインキュベーションした後の画像(20 nM、45分間のインキュベーション)。スケールバー = 30 μm。 (E) TMRM 細胞体ミトコンドリアの強度。RAR拮抗薬(BMS493、10-7 M、72時間)で治療した場合、対照(p = 0,0062)と比較して、オールトランスレチノイン酸治療(RA、10-7 M、72時間)で有意な減少は観察されません。.条件ごとに3回の繰り返しのそれぞれから5つの細胞を定量化しました。この図の拡大版をご覧になるには、ここをクリックしてください。
- 画像処理
- ImageJ 2.1.0 でファイルを開き、視野ごとに位置スタックを分ける: ImageJ を開き、[ メニュー バー] |画像|複製 |入力スライス/フレーム番号 |[OK]をクリックします。
注:ソフトウェアへの繰り返し入力を減らすために、視野画像の複製と保存を容易にするImageJマクロが開発されました。
- ImageJ 2.1.0 でファイルを開き、視野ごとに位置スタックを分ける: ImageJ を開き、[ メニュー バー] |画像|複製 |入力スライス/フレーム番号 |[OK]をクリックします。
- マクロ・プロトコル
- 自由選択ツールを使用して、セルの周囲に関心領域 (ROI) を描画します。
- ImageJ を開き、[ メニュー バー] |プラグイン |マクロ |背景をクリアして画像を保存するマクロを実行します。
注:このプロセスでは、画像をランダム化し、最適化要件に従ってソリューションキーを保存できます。 - ピクセルサイズとボクセル深度を決定する: ImageJ | 画像 を開き、 メニューバー |画像|[プロパティ] をクリックします。
- 代替直接プロトコル
注: この代替手段では、画像の処理にマクロは使用されません- ピクセルサイズとボクセル深度を求める: ImageJ |画像を開き 、 メニューバー |画像|[プロパティ] をクリックします。
- 自由選択ツールを使用してセルの周囲に ROI を描画し、15 フレームにわたってセル全体を囲むようにします。
- メニューバーに移動する |編集 |外をきれいにします。
- メニューバーに移動する |ファイル |名前を付けて保存 |[Tiff] を選択します。
- [フォルダの保存]を選択し、[ 保存]をクリックします。
注:分析を続行する前に、この時点で画像を手動で盲検化/ランダム化できます。
- 自動画像解析
- 分析ファイル用のフォルダーを準備します。
- 「All tracks」、「Perinuclear tracks」、「Telenuclear tracks」というタイトルの 3 つのメイン フォルダーを作成します。
注:これらは、メインの自動トラックオプションと一致します。 - 各メインフォルダに、処理する画像ごとにサブフォルダを作成し、1から上までの数値で識別します。
- 2つのルーチン最適化補足ファイル(mitometer2table.mおよびgetTXTfiles.m)のコピーを各イメージ・フォルダーに追加します。
注:これらのファイルは、データ分析と最終的なフォーマットの配置に役立ちます。フォルダの数は、ランダム化されたスプレッドシート(.xlsx)の要素数と一致する必要があります。1 つのデータセットの補足ファイルを含むすべての番号付きサブフォルダーを作成した後、それらをバッチでコピーして残りのデータセットに貼り付けることができます。
- 「All tracks」、「Perinuclear tracks」、「Telenuclear tracks」というタイトルの 3 つのメイン フォルダーを作成します。
- 分析ファイル用のフォルダーを準備します。
- MATLAB アプリケーションマイトメーターを使用してイメージを解析します。
注: このプロトコルは、MATLAB R2022a にインストールされたマイトメーターで実行されました。画像を 30 のバッチで読み込み、最適な時間実行と出力バランスを実現します。MAT ファイルの最大サイズはネイティブ ファイル システムによって制限されます: 既定では、"保存" 操作で 231 バイト (~2 GB) <ファイルを作成できます。保存形式 MAT ファイル バージョン 7.3 は、2 GB を超える最大可変サイズを使用できるため、代わりに使用できます。- 既定の MAT ファイル バージョンの識別/変更: [ホーム ] タブの [ 環境 ] セクションで、[ 基本設定 ] をクリックして [MATLAB |全般 |MAT ファイル。
- MATLAB ツール Mitometer を使用した解析: MATLAB を開き、 メニュー バー |アプリ |マイトメータを開く |[3D を開始] |入力データ (画素サイズ (μm): 0.1395089/フレーム間時間: 2/z面数: 8/z面間距離 (μm): 0.418809 |入力する画像を選択します。
- マイトメータのサイドメニューに移動し、[画像]を選択し、[ハイライトの選択]をクリックして、マイトメータのメニューバーに移動します。トラックを選択 |トラック ビュー |All-Tracks、Telenuclear または Perinuclear を選択 | マイトメーターメニューバー |解析 |要素(長さ)を選択する |[Save to ".txt" ("" に保存) を選択します。
注:同時に選択した場合は、複数のパラメータを一度にダウンロードできます。 - 作成したフォルダに結果ファイルを抽出します(2.2.1)。
- ルーチンの最適化とデータ分析
- 画像エンコード用のキーを含む「Randomization.xlsx」ファイルを準備/調整します。
- 1 から上の連続する整数のリストを列 A に挿入します。
注:元の名前の画像を含む複製フォルダを保持することをお勧めします。 - 英数字で構成される分析変数を列Bに配置します。
注: ドキュメント内の行数は、メイン データセットに存在するフォルダーの数と一致している必要があります。この「Randomization.xlsx」ファイルをコピーして、他の2つのメインデータセットに貼り付けます。
- 1 から上の連続する整数のリストを列 A に挿入します。
- 最適化されたデータ分析
- 「executable.mlx」をダブルクリックし、フォルダ数を入力し、 フォルダディレクトリ(フォルダの先頭からディレクトリをコピー)|保存ディレクトリ(フォルダの先頭からディレクトリをコピー)|出力ファイルのスプレッドシート名を指定し て、[ 実行]をクリックします。
- 必要に応じて統計分析を実行します。
注:各フォルダに.xlsxファイルを作成し、.txtデータと分析終了時の警告音を表示するオプションを選択できます。ライブ スクリプトは、1 つのスプレッドシート ファイルを表形式で出力します。この出力では、列は分析されたパラメータを表します(例:「 長軸の長さ」;"Intensity")と線は分析変数の視野を表します(例:「コントロール」)。
- 画像エンコード用のキーを含む「Randomization.xlsx」ファイルを準備/調整します。
結果
.txtフォーマットの出力ファイルの分析を強化および高速化するために、マイトメータ.txt出力ファイルと一致するデータを読み取るルーチン最適化がコード化され、列はフレームを表し、線は識別されたミトコンドリアを表します。ルーチン最適化では、識別された各ミトコンドリアのフレームを平均化し、視野ごとにすべてのミトコンドリアの結果を平均化することにより、パラメーター?...
ディスカッション
生細胞イメージングでは、本格的なコンピューティング処理を必要とする大きなファイルが生成されますが、最新のツールでさえ、処理に大量の手動入力が必要です。このルーチン最適化は、マイトメーターでのミトコンドリア分析のプロセスを簡素化することに重点を置いていますが、これは、このツールがユーザー入力とデータ出力のバランスが非常に良いためです。ミトコンドリア画?...
開示事項
著者は、宣言すべき利益相反を持っていません。
謝辞
画像取得は、PPBI(Portuguese Platform of BioImaging)のノードであるiBiMEDのLiM施設で行われました:POCI-01-0145-FEDER-022122。この研究は、FCT (EXPL/BTM-SAL/0902/2021) LCF (CI21-00276)、Fundação para a Ciência e Tecnologia of the Ministério da Educação e Ciência (2020.02006.CEECIND) からの DT への助成金、ATG-The Gabba Alumni Association から VP への助成金、およびアヴェイロ大学生物医学研究所 (Institute for Biomedicine-iBiMED) の支援を受けました。
資料
| Name | Company | Catalog Number | Comments |
| AM580 | Sigma-Aldrich | A8843 | |
| BDNF | Thermo-Fisher | RP8642 | |
| BMS493 | Tocris Bioscience | 3409 | |
| CD2314 | Tocris Bioscience | 3824 | |
| Ch55 | Tocris Bioscience | 2020 | |
| Foetal Bovine Serum | Thermo-Fisher | 10270106 | |
| GraphPad Prism v4.0 | GraphPad Software, La Jolla | n/a | |
| Ham’s F12 Nutrient Mix | Thermo-Fisher | 21765029 | |
| MATLAB R2022a | MathWorks | n/a | |
| Minimal Essential Medium | Thermo-Fisher | 31095 | |
| Nunc Glass Bottom Dishes | Thermo-Fisher | 150680 | |
| Phosphate Buffer Saline Solution | Thermo-Fisher | 28372 | |
| Retinoic acid | Sigma-Aldrich | R2625 | |
| TMRM | Thermo-Fisher | T668 | |
| Zeiss LSM 510 | Carl Zeiss | n/a | Equiped with live-cell imaging culture chamber and 63x oil immersion objective |
参考文献
- Trigo, D., Avelar, C., Fernandes, M., Sa, J., da Cruz, E. S. O. Mitochondria, energy, and metabolism in neuronal health and disease. FEBS Letters. 596 (9), 1095-1110 (2022).
- Zong, W. X., Rabinowitz, J. D., White, E. Mitochondria and cancer. Molecular Cell. 61 (5), 667-676 (2016).
- Clare, D. K., Saibil, H. R. ATP-driven molecular chaperone machines. Biopolymers. 99 (11), 846-859 (2013).
- Tourniaire, F., et al. All-trans retinoic acid induces oxidative phosphorylation and mitochondria biogenesis in adipocytes. Journal of Lipid Research. 56 (6), 1100-1109 (2015).
- Psarra, A. M., Sekeris, C. E. Nuclear receptors and other nuclear transcription factors in mitochondria: regulatory molecules in a new environment. Biochimica et Biophysica Acta. 1783 (1), 1-11 (2008).
- Trigo, D., Goncalves, M. B., Corcoran, J. P. T. The regulation of mitochondrial dynamics in neurite outgrowth by retinoic acid receptor beta signaling. FASEB Journal. 33 (6), 7225-7235 (2019).
- Mitra, K., Lippincott-Schwartz, J. Analysis of mitochondrial dynamics and functions using imaging approaches. Current Protocols in Cell Biology. Chapter 4 (Unit 4), 1-21 (2010).
- Sajic, M., et al. Impulse conduction increases mitochondrial transport in adult mammalian peripheral nerves in vivo. PLoS Biology. 11 (12), e1001754 (2013).
- Lefebvre, A., Ma, D., Kessenbrock, K., Lawson, D. A., Digman, M. A. Automated segmentation and tracking of mitochondria in live-cell time-lapse images. Nature Methods. 18 (9), 1091-1102 (2021).
- Chu, C. -. H., Tseng, W. -. W., Hsu, C. -. M., Wei, A. -. C. Image analysis of the mitochondrial network morphology with applications in cancer research. Frontiers in Physics. 10, 855775 (2022).
- Creed, S., McKenzie, M. Measurement of mitochondrial membrane potential with the fluorescent dye tetramethylrhodamine methyl ester (TMRM). Methods in Molecular Biology. 1928, 69-76 (2019).
- Kovalevich, J., Langford, D. Considerations for the use of SH-SY5Y neuroblastoma cells in neurobiology. Methods in Molecular Biology. 1078, 9-21 (2013).
- Sahin, M., Oncu, G., Yilmaz, M. A., Ozkan, D., Saybasili, H. Transformation of SH-SY5Y cell line into neuron-like cells: Investigation of electrophysiological and biomechanical changes. Neuroscience Letters. 745, 135628 (2021).
- Trigo, D., et al. Mitochondria dysfunction and impaired response to oxidative stress promotes proteostasis disruption in aged human cells. Mitochondrion. 69, 1-9 (2022).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
ISSN 1940-087X
Copyright © 2023 MyJoVE Corporation. All rights reserved
当社はcookieを使用しています。
「続行」をクリックすることで、当社のcookieへの同意となります。