Un ensayo de microplacas basado en densidad óptica adaptado para caracterizar la infección por actinobacteriófagos
En este artículo
Resumen
Se describe un método de microplaca basado en densidad óptica para cuantificar el crecimiento bacteriano a largo plazo en presencia de bacteriófagos, adecuados para actinomicetos y otras bacterias de crecimiento lento. Este método incluye modificaciones para reducir la evaporación y la condensación de la tapa y código R para calcular las métricas de infección por virus, incluido el área bajo la curva, el máximo de crecimiento y la virulencia relativa.
Resumen
Los bacteriófagos son una parte clave de los entornos naturales, y tienen una poderosa capacidad para dar forma a las poblaciones bacterianas. Para comprender cómo los fagos individuales interactúan con huéspedes bacterianos de crecimiento lento, como los actinomicetos, se necesita un método fácil y confiable para cuantificar el crecimiento bacteriano a largo plazo en presencia de fagos. Los lectores espectrofotométricos de microplacas permiten mediciones repetidas de alto rendimiento, pero incubar un volumen pequeño durante un tiempo prolongado puede presentar desafíos técnicos. Este procedimiento adapta una microplaca estándar de 96 pocillos para permitir el cocultivo de fagos y bacterias sin submuestreo durante 96 h, con el crecimiento bacteriano registrado cada 8 h utilizando valores de absorbancia espectrofotométrica. Estos valores de densidad óptica se analizan utilizando R para obtener métricas de infección, incluido el porcentaje de inhibición del crecimiento, la virulencia relativa y el índice de Stacy-Ceballos. Los métodos descritos aquí proporcionan una forma efectiva de realizar y analizar experimentos de curva de crecimiento de microplacas de duración prolongada e incluyen modificaciones para reducir la evaporación y la condensación de la tapa. Estos protocolos facilitan los ensayos basados en microplacas de las interacciones entre los huéspedes bacterianos de crecimiento lento y sus bacteriófagos.
Introducción
Los bacteriófagos o fagos son virus que infectan bacterias. Son las entidades biológicas más numerosas del planeta1, y generalmente se acepta que los bacteriófagos influyen en la evolución bacteriana y en los procesos ecosistémicos 2,3,4. Existen varios métodos para describir, medir y analizar el rango de huéspedes bacteriófagos 8 y la dinámica de infección5,6, incluidos los métodos basados en agar comoel método 7 de agar de doble capa y los métodos de microplacas basados en densidad óptica 8,9,10,11,12. Cada método tiene sus propias ventajas y desventajas. Debido a su eficiencia, las pruebas de recubrimiento que utilizan el método de agar de doble capa son el "estándar de oro" para los ensayos de rango de huésped, pero este método requiere mucho tiempo y mano de obra9. Los métodos rápidos de microplacas, que devuelven resultados en 24 h o menos, dan excelentes resultados para huéspedes bacterianos de crecimiento rápido como Escherichia coli 9,10,11,12, pero son demasiado breves para mostrar la progresión de la infección por bacteriófagos en huéspedes bacterianos de crecimiento más lento como actinomicetos7,13,14,15.
Un ensayo de microplacas basado en densidad óptica diseñado para bacterias de crecimiento rápido no se puede ejecutar durante los múltiples días necesarios para caracterizar la dinámica de la infección en una bacteria huésped de crecimiento lento sin que se produzca evaporación y dando densidades bacterianas artificialmente altas. Por lo tanto, la obtención de datos comparables de alto rendimiento sobre la dinámica de la infección por bacteriófagos para especies bacterianas de crecimiento lento requiere técnicas especializadas adaptadas para estas bacterias.
El método de microplaca presentado aquí reduce la evaporación, lo que permite que las bacterias de crecimiento lento se cocultiven con un fago durante un período prolongado de 96 h y permite investigaciones sobre la dinámica de la infección por fagos y el rango de huéspedes. Este método también muestra el índice16 de Stacy-Caltos, una métrica basada en la densidad óptica que permite comparaciones de virulencia entre sistemas de virus huésped dispares.
Protocolo
Si bien este protocolo está escrito para Gordonia terrae, también se ha utilizado con éxito para Gordonia lacunae, Gordonia rubripertincta y Gordonia westfalica.
1. Preparación de bacterias
- En un gabinete de bioseguridad, utilice una buena práctica microbiológica17 para inocular una sola colonia de Gordonia terrae CAG3 en un matraz deflector estéril de 1 L con 200 ml de caldo cálcico de levadura peptona18 (PYCa) que contiene 0,01 mg/ml de cicloheximida (ver la Tabla de materiales).
- Incubar el matraz a 30 °C agitando a 250 rpm hasta que el cultivo esté saturado o durante 3 días7.
- Diluir en serie el cultivo saturado de G. terrae en caldo PYCa y extender en placa 100 μL cada una de las diluciones 10−4, 10−5 y 10−6 en placas PYCa19,20. Refrigerar el cultivo saturado sin diluir a 4 °C.
- Incubar las placas extendidas invertidas durante 3 días a 30 °C.
- Después de la incubación, identifique una "placa contable", una placa con 20-200 colonias. Cuente el número de colonias en esa placa y calcule las unidades formadoras de colonias por mililitro (ufc/ml)19,20.
- Diluir el cultivo saturado con caldo PYCa a 4.0 x 106 ufc/ml bacterias.
2. Preparación de fagos
NOTA: Los resultados representativos reportados se obtuvieron con el fago de Gordonia DelRio21, un bacteriófago templado aislado en G. terrae. Estos métodos también se han utilizado con éxito con otros fagos de Gordonia .
- Comenzando con un bacteriófago aislado, diluir en serie la muestra de fagos en tampón de fagos 7 a una diluciónde 1 x 10−8 . Realizar un ensayo de título de fagos de agar de doble capa7 infectando 0,3 ml del cultivo saturado de G. terrae con 10 μL de cada dilución de fagos. Después de una incubación a temperatura ambiente de 5-10 minutos, combine la mezcla de bacterias y fagos con 3 ml de agar superior PYCa y vierta en placas de agar PYCa.
- Incubar las placas invertidas a 30 °C durante 3 días o hasta que se formenplacas 7.
- Después de la incubación, identifique una "placa contable", una placa con 20-200 placas. Cuente el número de placas en esa placa y calcule las unidades formadoras de placa por mililitro (ufp/ml)7.
3. Preparación de microplacas
NOTA: Para este método se deben utilizar microplacas de fondo plano de 96 pocillos (consulte la Tabla de materiales). Toda la preparación y carga de la placa debe completarse en un gabinete de bioseguridad, y se deben utilizar buenas prácticas microbiológicas17.
- Prepare la solución de recubrimiento de la tapa antivaho combinando 100 μL de Triton-X 100, 40 mL de isopropanol al 100% y 160 ml de agua desionizada22. Revuelva para mezclar y guárdelo a temperatura ambiente.
- En un gabinete de bioseguridad, agregue 6 ml de solución de recubrimiento de tapa a la superficie interior de una tapa estéril de microplaca de 96 pocillos, sosteniendo la tapa por los bordes y girándola para asegurarse de que esté cubierta por la solución. Deje que la solución repose en la tapa durante 20 s, luego vierta la solución e invierta la tapa en una toalla de papel esterilizada en autoclave en ángulo hasta que la tapa esté completamente seca, lo que generalmente toma 35-45 minutos. Tenga cuidado de sostener la tapa por los bordes.
- Prepare 20 ml de agarosa al 0,1% en agua para cada microplaca de 96 pocillos, en el microondas para derretir la agarosa.
- Una vez que la agarosa se haya enfriado a 50-60 °C, pipetear 100 μL de agarosa al 0,1% en todos los espacios entre los pocillos de la placa y 200 μL de agarosa en los pocillos de la fila A y la fila H y la columna 1, columna 2, columna 11 y columna 1223 (figura 1).
4. Cargar la placa con bacterias y fagos
NOTA: Toda la preparación y carga de la placa debe completarse en un gabinete de bioseguridad, y se deben usar buenas prácticas microbiológicas17 .
- La placa de 96 pocillos contendrá 75 μL de 2.0 x 106 ufc/ml de bacterias en cada pocillo9. Diluir el cultivo bacteriano 4.0 x 10 6 ufc/ml 1:1 con 2x caldo PYCa a 2.0 x 106 ufc/ml. Prepare 5 ml por placa de 96 pocillos.
- Diluir el lisado de fagos usando el tampón de fagos7 para hacer 1 ml de concentraciones de 2.0 x 106 ufp/ml, 2.0 x 105 ufc/ml y 2.0 x 104 ufc/ml. Esto permitirá una multiplicidad de infección (MOI) de 1, 0.1 y 0.01 dentro de la microplaca9.
- Para cargar la microplaca, tome una placa preparada con solución antivaho y agarosa, y pipete 75 μL de las bacterias 2.0 x 106 ufc/ml en las columnas 3-10, siguiendo la Figura 1.
- A la columna 3 y a la columna 4, añadir 75 μL de tampón fágico estéril a cada pocillo para que sirva como control positivo sin fagos, siguiendo la figura 1, y pipetear hacia arriba y hacia abajo para mezclar después de cada adición. Añadir 75 μL del fago 2,0 x 10 6 ufp/ml a la columna 5 y a la columna6 , 75 μL del fago 2,0 x 105 ufc/ml a la columna 7 y a la columna 8, y 75 μL del fago 2,0 x 104 ufc/ml a la columna 9 y a la columna 10, pipeteando hacia arriba y hacia abajo para mezclar después de cada adición.
- Pegue con cinta adhesiva ambos lados cortos de la placa con cinta de etiquetado de 0.5 pulgadas para sellar parcialmente la placa y permitir el intercambio de gases.
5. Incubación y medición de absorbancia
- Una vez que las placas estén cargadas de bacterias y fagos, colóquelas en un agitador de microplacas a 250 rpm e incube a 30 °C.
- Incubar las placas durante 96 h, tomando una medición de densidad óptica a 600 nm en un lector de microplacas cada 8 h a partir de la hora 16. Devuelva las placas al agitador entre mediciones.
NOTA: Se evaluaron los períodos de medición de 4, h 6 h, 8 h y 12 h, comenzando en la hora 0, y se determinó que un período de muestreo de 8 h que comenzó a las 16 h después de la infección capturó mejor las interacciones Gordonia-fagos. - Controle la tapa para detectar condensación durante todo el experimento. Si se observa condensación, sustituir la tapa por otra tapa recubierta según el paso 3.2.
- Generar curvas de crecimiento de control e infección siguiendo la sección 6 del protocolo.
6. Análisis de datos
- Utilice un programa de hoja de cálculo para calcular la desviación promedio y estándar para cada dilución de fagos, siguiendo el diseño de hoja de cálculo en el repositorio de GitHub Stacy-Ceballos-Index (https://github.com/eichristenson/Stacy-Ceballos-Index).
- Cree curvas de control y crecimiento infectadas, y calcule métricas de infección usando R (consulte la Tabla de materiales) con los paquetes DescTools 24, dplyr 25, ggplot226 y readxl 27 y siguiendo el script R en el repositorio de GitHub Stacy-Ceballos-Index (https://github.com/eichristenson/Stacy-Ceballos-Index).
- AUCcon es el área bajo la curva de control no infectada, mientras que AUCinf es el área bajo la curva infectada16. Calcule el AUC y, a continuación, calcule el porcentaje de inhibición del crecimiento en función del área bajo los valores de la curva, PIAUC16, utilizando la siguiente ecuación:
(1 - [AUCinf/AUCcon]) × 100 - Las líneas horizontales discontinuas en cada curva muestran el crecimiento máximo, con el pico de crecimiento no infectado etiquetado como N asíntota(con) y el pico de crecimiento infectado etiquetado como Nasíntota(inf). Identifique los valores deasíntota N y luego calcule el porcentaje de inhibición del crecimiento en función de estos valores de crecimiento máximo, PImax16, utilizando la siguiente ecuación:
(1 - [N asíntota(inf)/ Nasíntota(con)]) × 100 - Calcule el índice de Stacy-Ceballos, ISC16, a partir de los valoresPI AUC y PImax , de la siguiente manera:
(PI AUC × PImax) 0.5 Español
Calcular la virulencia relativa integrando el índice de Stacy-Ceballos a lo largo del tiempo16.
- AUCcon es el área bajo la curva de control no infectada, mientras que AUCinf es el área bajo la curva infectada16. Calcule el AUC y, a continuación, calcule el porcentaje de inhibición del crecimiento en función del área bajo los valores de la curva, PIAUC16, utilizando la siguiente ecuación:
Resultados
Un experimento tiene éxito si la curva de crecimiento resultante muestra un aumento en la población bacteriana de control positivo a lo largo del tiempo sin fluctuación repentina en la absorbancia. Ejemplos de un experimento exitoso en un MOI de 1 con y sin una infección productiva por fagos se muestran en la Figura 2 y la Figura 3, respectivamente. Una infección productiva a un MOI de 0,01 se representa en la Figura 4. El patrón de crecimiento de control positivo (curva verde) visto en las tres figuras indica que las bacterias están creciendo, no se están aglutinando durante el crecimiento y no hay contaminantes presentes. La aglutinación y la contaminación se indican mediante una absorbancia inusualmente alta en un solo punto de tiempo. Las desviaciones estándar suelen aumentar a lo largo del tiempo de un experimento; Sin embargo, un aumento drástico o desviaciones estándar superpuestas entre las curvas de control e infectadas pueden indicar contaminación o aglutinación en uno o más pozos.
La curva de crecimiento que representa una infección productiva por fagos, representada por la Figura 2, muestra una absorción bacteriana reducida a lo largo del tiempo en pozos con el fago agregado. Esta reducción en la densidad bacteriana no se verá si la bacteria está fuera del rango de huéspedes del fago, como se muestra en la Figura 3.
Las métricas de infección se muestran para todos los experimentos representativos, con un I SC relativamente grande para las infecciones productivas en la Figura 2 y la Figura 4 y un ISC muy pequeño en la Figura 3 para el fago que no infectó eficientemente a la bacteria huésped.
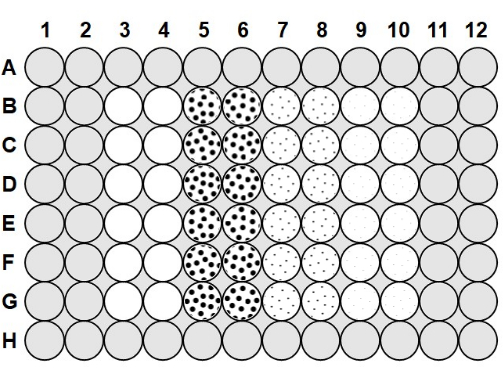
Figura 1: Diseño de microplacas. Las áreas grises están llenas de 0.1% de agarosa. Los pocillos en blanco en la columna 3 y la columna 4 son pocillos de control positivos sin fagos que contienen solo tampón de fagos y 2.0 x 106 ufc/ml bacterias. Los pocillos punteados contienen fagos y bacterias 2.0 x 106 ufc/ml; los puntos grandes en la columna 5 y la columna 6 indican un MOI de 1 con 2.0 x 106 ufp/ml de fago; los puntos medios de la columna 7 y la columna 8 indican un MOI de 0,1 con 2,0 x 105 ufp/ml de fago; y los pequeños puntos en la columna 9 y la columna 10 indican un MOI de 0.01 con 2.0 x 104 ufp/mL de fago. Haga clic aquí para ver una versión más grande de esta figura.
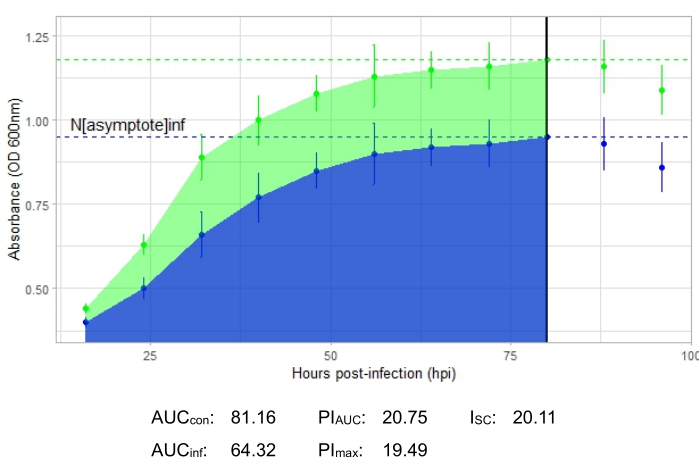
Figura 2: Un experimento exitoso de la curva de crecimiento con un fago en un MOI de 1 que infecta productivamente a la bacteria huésped. Los valores medios de absorbancia (± desviación estándar) se muestran para bacterias no infectadas (verde) y bacterias con el fago añadido (azul). Abreviaturas: AUC = área bajo la curva; PI AUC = porcentaje de inhibición del crecimiento calculado a partir del área bajo la curva; Nasíntota = valor máximo de crecimiento; PImax = porcentaje de inhibición del crecimiento calculado a partir de los valores de crecimiento máximo; ISC = Índice de Stacy-Ceballos. Este gráfico representa el fago templado de Gordonia DelRio infectando a G. terrae, la bacteria en la que fue aislada. Haga clic aquí para ver una versión más grande de esta figura.
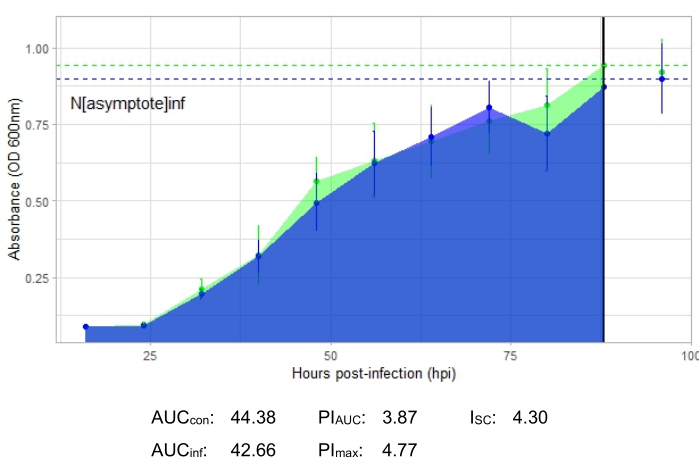
Figura 3: Un experimento exitoso de la curva de crecimiento con un fago en un MOI de 1 que no infecta eficientemente a la bacteria huésped. Los valores medios de absorbancia (± desviación estándar) se muestran para bacterias no infectadas (verde) y bacterias con el fago añadido (azul). Abreviaturas: AUC = área bajo la curva; PI AUC = porcentaje de inhibición del crecimiento calculado a partir del área bajo la curva; Nasíntota = valor máximo de crecimiento; PImax = porcentaje de inhibición del crecimiento calculado a partir de los valores de crecimiento máximo; ISC = Índice de Stacy-Ceballos. Este gráfico representa la infección por G. rubripertincta por DelRio. Haga clic aquí para ver una versión más grande de esta figura.
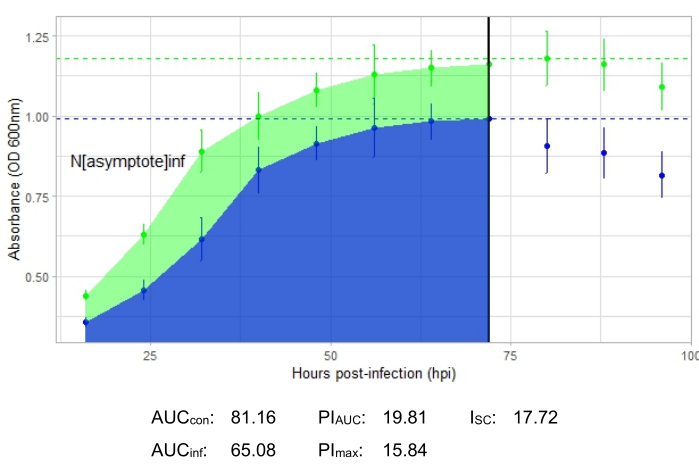
Figura 4: Un experimento exitoso de la curva de crecimiento con un fago en un MOI de 0.01. Los valores medios de absorbancia (± desviación estándar) se muestran para bacterias no infectadas (verde) y bacterias con el fago añadido (azul). Abreviaturas: AUC = área bajo la curva; PI AUC = porcentaje de inhibición del crecimiento calculado a partir del área bajo la curva; Nasíntota = valor máximo de crecimiento; PImax = porcentaje de inhibición del crecimiento calculado a partir de los valores de crecimiento máximo; ISC = Índice de Stacy-Ceballos. Este gráfico representa la infección por G. terrae por DelRio. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
Este método de microplaca basado en densidad óptica permite investigar el rango de huéspedes de bacteriófagos y la dinámica de infección11 y muestra la utilidad del índice16 de Stacy-Ceballos como medida de la virulencia de los bacteriófagos. Si bien este método podría utilizarse con cualquier sistema bacteriófago-huésped, fue diseñado específicamente para adaptar ensayos rápidos de crecimiento de microplacas 9,10,11 para su uso con bacterias de crecimiento más lento como los actinomicetos. Los ensayos rápidos de microplacas no se pueden usar para bacterias de crecimiento lento sin modificaciones para abordar la evaporación y la condensación de la tapa. Este método describe estas modificaciones necesarias y demuestra, por primera vez, el uso del índice de Stacy-Ceballos y métricas relacionadas16 para describir la infección por bacteriófagos.
La evaporación puede ser un desafío sustancial en ensayos de curva de crecimiento en placa de 96 pocillos de varios días; Este método resuelve ese problema agregando agarosa a los pozos fronterizos y los espacios entre los pozos. El margen de agarosa, combinado con el tratamiento antivaho de la tapa22, proporciona la humedad necesaria dentro de la microplaca y permite mediciones fiables de densidad óptica. Sin la humedad añadida, se produce una evaporación sustancial del efecto borde23 durante el largo período de incubación requerido, lo que lleva a lecturas de densidad óptica artificialmente altas. El tratamiento antivaho de la tapa es una modificación necesaria porque la condensación de la tapa también puede elevar artificialmente los valores de densidad óptica. Agitar las placas durante el período de incubación es una modificación recomendada, ya que las bacterias actinomicetos pueden agruparse durante el crecimiento, dando valores de densidad óptica artificialmente altos y disminuyendo efectivamente la multiplicidad de la infección.
La proporción de bacterias a fagos en experimentos que caracterizan la dinámica de la infección es crítica, ya que debe haber suficientes fagos para mostrar un efecto de infección, pero no tantos como para que la población bacteriana huésped se estrelle inmediatamente9 o la frecuencia de lisogenia aumente dramáticamente28. En este método, la razón que resultó ser más efectiva para obtener resultados consistentes fue un MOI de 1, pero también se obtuvieron resultados utilizables con MOI de 0.1 y 0.01. Al implementar este método, se recomienda elegir una concentración de bacterias y probar múltiples concentraciones de fagos en el rango MOI de 0.01-1 9,10,11.
Esta técnica descrita aquí permite evaluar las interacciones bacteriófago-huésped para detectar bacterias de crecimiento lento en ensayos de microplacas de alto rendimiento en lugar de con submuestreo de un matraz de cultivo más grande en cada intervalo de medición29. Además, al demostrar cómo se pueden adaptar los ensayos de crecimiento de microplacas 9,10,11, esta técnica aumenta la utilidad de otros ensayos de bacteriófagos basados en microplacas para bacterias de crecimiento más lento, incluida la caracterización de fagos 5,6,12 y estudios de evolución 30,31. Finalmente, este método demuestra el uso del índice de Stacy-Ceballos16 para describir la infección por bacteriófagos. Esta métrica se desarrolló inicialmente con datos de un sistema modelo de virus arqueal y se calcula a partir de valores de densidad óptica, lo que le da una utilidad generalizada en sistemas de virus dispares.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Este trabajo fue apoyado por una subvención del Instituto de Integración de Biología (BII) de NSF DBI (premio no. 2119968; PI-Ceballos) y por el programa Arkansas INBRE, con una beca del Instituto Nacional de Ciencias Médicas Generales, (NIGMS), P20 GM103429 de los Institutos Nacionales de Salud. Los autores también aprecian el apoyo del Programa de Investigación de Pregrado de Verano Patterson en la Universidad Bautista de Ouachita.
Materiales
| Name | Company | Catalog Number | Comments |
| Agarose | Omni-Pur | 2090 | for filling border wells of microplate |
| Costar 96 Well Lid Low Evaporation Corner Notch | Corning | 3931 | replacement microplate lid |
| Isopropanol | Fisher Chemical | A461-4 | for lid coating |
| Microplate reader | Tecan Spark 20M | ||
| Microplate Shaker with 4-Place Platform | Thermo Fisher Scientific | 88-861-023 | to shake plates during incubation |
| Non-Tissue Culture-Treated Plate 96 well | Falcon (a Corning Brand) | 351172 | microplate for growth curve assay |
| Peptone yeast calcium (PYCa) agar | Homemade | 1 g peptone 15 g yeast extract 15 g agar 990 mL dd H2O 4.5 mL 1 M CaCl2 2.5 mL 40% dextrose 1 mL 10 mg/mL cycloheximide | |
| Peptone yeast calcium (PYCa) broth | Homemade, from Reference 16 | 1 g peptone 15 g yeast extract 990 mL dd H2O 4.5 ml 1 M CaCl2 2.5 mL 40% dextrose 1 mL 10 mg/mL cycloheximide | |
| Peptone yeast calcium (PYCa) top agar | Homemade | 1 g peptone 15 g yeast extract 4 g agar 990 mL dd H2O 4.5 mL 1M CaCl2 2.5 mL 40% dextrose | |
| Petri plates | Thermo Fisher Scientific | FB0875713 | for determination of bacterial concentration and phage titer assay |
| Phage Buffer | Homemade, from Reference 7 | 10 mL 1 M Tris, pH 7.5 10 mL 1 M MgSO4 4 g NaCl 980 ml dd H2O | |
| R software | https://www.r-project.org/ | version 4.3.0 | |
| Sterile Disposable PETG Flask Baffled Bottom w/Vented Closure | Thermo Fisher Scientific | 4116-1000 | for bacterial culture |
| Triton X-100 | Sigma Aldrich | 9036-19-5 | for lid coating |
Referencias
- Mushegian, A. R. Are there 1031 virus particles on Earth, or more, or fewer. Journal of Bacteriology. 202 (9), e00052-e00020 (2020).
- Chevallereau, A., Pons, B. J., van Houte, S., Westra, E. R. Interactions between bacterial and phage communities in natural environments. Nature Reviews Microbiology. 20 (1), 49-62 (2022).
- Olszak, T., Latka, A., Roszniowski, B., Valvano, M. A., Drulis-Kawa, Z. Phage life cycles behind bacterial biodiversity. Current Medicinal Chemistry. 24 (36), 3987-4001 (2017).
- Weitz, J. S., et al. Phage-bacteria infection networks. Trends in Microbiology. 21 (2), 82-91 (2013).
- Turner, P. E., Draghi, J. A., Wilpiszeski, R. High-throughput analysis of growth differences among phage strains. Journal of Microbiological Methods. 88 (1), 117-121 (2012).
- Storms, Z. J., Teel, M. R., Mercurio, K., Sauvageau, D. The virulence index: A metric for quantitative analysis of phage virulence. PHAGE. 1 (1), 27-36 (2020).
- . Phage Discovery Guide Available from: https://seaphagesphagediscoveryguide.helpdocsonline.com/home (2012)
- Martinez-Soto, C. E., et al. PHIDA: A high throughput turbidimetric data analytic tool to compare host range profiles of bacteriophages isolated using different enrichment methods. Viruses. 13 (11), 2120-2137 (2021).
- Rajnovic, D., Muñoz-Berbel, X., Mas, J. Fast phage detection and quantification: An optical density-based approach. PLoS One. 14 (5), e0216292 (2019).
- Xie, Y., Wahab, L., Gill, J. J. Development and validation of a microtiter plate-based assay for determination of bacteriophage host range and virulence. Viruses. 10 (4), 189-204 (2018).
- Sørensen, P. E., et al. Classification of in vitro phage-host population growth dynamics. Microorganisms. 9 (12), 2470-2486 (2021).
- Konopacki, M., Grygorcewicz, B., Dołęgowska, B., Kordas, M., Rakoczy, R. PhageScore: A simple method for comparative evaluation of bacteriophages lytic activity. Biochemical Engineering Journal. 161, 107652 (2020).
- Holt, J. G., Krieg, N. R., Sneath, P. H. A., Staley, J. T., Williams, S. T. . Bergey's Manual of Determinative Bacteriology., 9th edition. , (1994).
- Fusconi, R., Godinho, M. J. L., Bossolan, N. R. S. Culture and exopolysaccharide production from sugarcane molasses by Gordonia polyisoprenivorans CCT 7137, isolated from contaminated groundwater in Brazil. World Journal of Microbiology and Biotechnology. 24 (7), 937-943 (2007).
- Bujold, A. R., Lani, N. R., Sanz, M. G. Strain-to-strain variation of Rhodococcus equi growth and biofilm formation in vitro. BMC Research Notes. 12 (1), 519 (2019).
- Ceballos, R. M., Stacy, C. L. Quantifying relative virulence: When µmax fails and AUC alone just is not enough. Journal of General Virology. 102 (1), 001515 (2021).
- Siddiquee, S. The basic concept of microbiology. Practical Handbook of the Biology and Molecular Diversity of Trichoderma Species from Tropical Regions. , 1-15 (2017).
- Petrovski, S., Seviour, R. J., Tillett, D. Genome sequence and characterization of the Tsukamurella bacteriophage TPA2. Applied and Environmental Microbiology. 77 (4), 1389-1398 (2011).
- Growth curves: Generating growth curves using colony forming units and optical density measurements. JoVE Science Education Database. Microbiology Available from: https://www.jove.com/v/10511/growth-curvesgenerating-growth-curves-using-colony-forming-units (2023)
- Preparing spread plates protocols. American Society for Microbiology Available from: https://asm.org/ASM/media/Protocol-Images/Preparing-Spread-Plates-Protocols.pdf (2006)
- Mathes, H. N., et al. Complete genome sequences of Chop, DelRio, and GrandSlam, three Gordonia phages isolated from soil in Central Arkansas. Microbiology Resource Announcements. 12 (5), e0002323 (2023).
- Krishnamurthi, V. R., Niyonshuti, I. I., Chen, J., Wang, Y. A new analysis method for evaluating bacterial growth with microplate readers. PLoS One. 16 (1), 0245205 (2021).
- DescTools: Tools for descriptive statistics, R package version 0.99.49. DescTools Available from: https://CRAN.R-project.org/package=DescTools (2023)
- . dplyr: A grammar of data manipulation, R package version 1.1.2 Available from: https://CRAN.R-project.org/package=dplyr (2023)
- . ggplot2: Create elegant data visualisations using the grammar of graphics, R package version 3.4.2 Available from: https://CRAN.R-project.org/package=ggplot2 (2023)
- . readxl: Read excel files, R package version 1.4.2 Available from: https://CRAN.R-project.org/package=readxl (2023)
- Yao, T., Coleman, S., Nguyen, T. V. P., Golding, I., Igoshin, O. A. Bacteriophage self-counting in the presence of viral replication. Proceedings of the National Academy of Sciences of the United States of America. 118 (51), 2104163118 (2021).
- Fang, Q., Feng, Y., McNally, A., Zong, Z. Characterization of phage resistance and phages capable of intestinal decolonization of carbapenem-resistant Klebsiella pneumoniae in mice. Communications Biology. 5, 48 (2022).
- Burrowes, B. H., Molineux, I. J., Fralick, J. A. Directed in vitro evolution of therapeutic bacteriophages: The Appelmans protocol. Viruses. 11 (3), 241 (2019).
- Shapiro, J. W., Williams, E. S. C. P., Turner, P. E. Evolution of parasitism and mutualism between filamentous phage M13 and Escherichia coli. PeerJ. 4, e2060 (2013).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados