איתור שברים דו-גדיליים בדנ"א בביציות עכבר
In This Article
Summary
שמירה על שלמות גנום הביצית נחוצה כדי להבטיח את הנאמנות הגנטית בעובר המתקבל. כאן, אנו מציגים פרוטוקול מדויק לאיתור שברים דו-גדיליים בדנ"א בתאי נבט נקביים של יונקים.
Abstract
הביציות הן בין התאים הגדולים ומאריכי החיים ביותר בגוף הנשי. הם נוצרים בשחלות במהלך ההתפתחות העוברית ונשארים נעצרים בשלב של מיוזה I. המצב השקט עשוי להימשך שנים עד שהביציות מקבלות גירוי לגדול ולקבל את היכולת לחדש את המיוזה. מצב מעצר ממושך זה הופך אותם לרגישים ביותר לצבירת עלבונות מזיקים לדנ"א, המשפיעים על השלמות הגנטית של הגמטות הנקביות, ולכן, על שלמותו הגנטית של העובר העתידי.
לפיכך, יש חשיבות מכרעת לפיתוח שיטה מדויקת לאיתור נזק לדנ"א, שהיא הצעד הראשון להקמת מנגנוני תגובה לנזקי דנ"א. מאמר זה מתאר פרוטוקול נפוץ לבדיקת נוכחות והתקדמות של נזק לדנ"א בביציות שנעצרו בשלב במהלך תקופה של 20 שעות. באופן ספציפי, אנו מנתחים שחלות עכברים, שולפים את קומפלקסי קומולוס-ביציות (COC), מסירים את תאי הקומולוס מה-COC, ומתרבתים את הביציות בתווך Μ2 המכיל 3-איזובוטיל-1-מתיל-קסנטין כדי לשמור על מצב המעצר. לאחר מכן, הביציות מטופלות בתרופה ציטוטוקסית, אנטי-ניאופלזמה, אטופוסיד, כדי לגרום לשברים דו-גדיליים (DSB).
על ידי שימוש באימונופלואורסנציה ובמיקרוסקופ קונפוקלי, אנו מזהים ומכמתים את רמות חלבון הליבה γH2AX, שהוא הצורה הזרחנית של ההיסטון H2AX. H2AX הופך לפוספורילציה באתרים של DSB לאחר נזק לדנ"א. חוסר היכולת לשחזר את שלמות הדנ"א בעקבות נזק לדנ"א בביציות עלול להוביל לאי פוריות, למומים מולדים ולשיעורים מוגברים של הפלות ספונטניות. לכן, הבנת מנגנוני התגובה לנזק לדנ"א, ובה בעת ביסוס שיטה שלמה לחקר מנגנונים אלה, חיוניים לחקר הביולוגיה של הרבייה.
Introduction
תהליך המיוזה בתאי נבט נקביים של יונקים מתחיל בשחלות לפני הלידה. המספר הכולל של הביציות נקבע בשחלות בעיקר במהלך embryogenesis. הביציות נכנסות למיוזה ונשארות עצורות בשלב I1. לאחר תחילת ההתבגרות המינית והייצור והפעולה האנדוקרינית של הורמון מגרה זקיק (FSH) והורמון luteinizing (LH), הביציות עשויות ליזום מחדש ולהשלים מיוזה2. אצל בני אדם, מעצר שלב יכול להימשך עד 50 שנה3. חלוקות התאים לאחר הכניסה למיוזה I אינן סימטריות, וכתוצאה מכך נוצר גוף קוטבי קטן וביצית השומרת על גודלה. לכן, רוב המרכיבים cytoplasmic מאוחסנים ooplasm במהלך embryogenesis מוקדם4. לאחר מכן, הביציות נכנסות למיוזה II, מבלי לשנות מחדש את הגרעין שלהן או לפרק את הכרומוזומים שלהן, ונשארות כלואות במטא-פאזה II עד להפריה5.
מאפיין ייחודי המבדיל בין ביציות לתאים סומטיים הוא מצב המעצר בשלב I, כאשר לביצית יש גרעין שלם (מעצר שלפוחית נבט [GV]), המכונה שלבGV 6. בהתבסס על ארגון הכרומטין, הביציות בשלב GV מסווגות לשתי קטגוריות: גרעין לא מוקף (NSN) וגרעין מוקף (SN)7,8. בביציות בשלב ה-GV של NSN, הכרומטין מתפשט בכל האזור הגרעיני, והשעתוק פעיל, ואילו בביציות SN, הכרומטין יוצר טבעת קומפקטית המקיפה את הגרעין, והשעתוק שקט9. שני סוגי הביציות בשלב GV מראים יכולת מיוטית; הן נכנסות למיוזה באותו קצב, אך הביציות של NSN מציגות יכולת התפתחותית נמוכה ואינן יכולות להתפתח מעבר לעובר בן שני התאים10.
המצב הממושך של מעצר שלב I מעלה את שכיחות הצטברות הנזק לדנ"א11. לכן, מנגנוני התגובה לנזק לדנ"א בביציות חיוניים כדי לאפשר ייצור של גמטות בעלות שלמות גנטית ולהבטיח שלעובר שנוצר יש תוכן כרומוזומלי פיזיולוגי.
היבט מרכזי של תגובת הנזק לדנ"א הוא תיקון דנ"א. המסלולים העיקריים לתיקון DSB בתאים אאוקריוטים כוללים הצטרפות קצה לא הומולוגית (NHEJ), רקומבינציה הומולוגית (HR) וחלופה NHEJ 12,13,14,15. NHEJ הוא מנגנון מהיר יותר אך נוטה יותר לשגיאות, בעוד HR דורש יותר זמן כדי להשלים אבל יש נאמנות גבוהה16.
אין מספיק ידע על המנגנונים שבהם הביציות משתמשות לתיקון נזקי דנ"א. מחקרים הראו כי נזק לדנ"א הנגרם בביציות יונקים בוגרות לחלוטין על ידי שימוש בחומרים גנוטוקסיים, כגון אטופוסיד, דוקסורוביצין או UVB או קרינה מייננת, אינו משפיע על העיתוי וקצב היציאה משלב I מעצר17. ביציות יכולות לעבור פירוק GV (GVBD) גם בנוכחות רמות גבוהות של נזק. נזק זה יכול להיקבע על ידי תצפית של γH2AX. צורה זרחנית זו של H2AX (γΗ2ΑΧ) היא סמן DSB, הממוקם באתר של שברים ומתפקד כפיגום כדי לסייע בתיקון גורמים וחלבונים להצטבר בקצוות שבורים18.
היעדר מעצר מחזור התא בעקבות נזק לדנ"א נובע ממחסום נזק DNA לא מספיק המאפשר לביציות עם DNA לא מתוקן להיכנס מחדש למיוזה. בעקבות רמות גבוהות של נזק לדנ"א, מחסום יכול לשמור על מעצר שלב באמצעות הפעלת מסלול תלוי ATM/Chk1. תגובת הבידוק המוגבלת ל-DSB נובעת מההפעלה המוגבלת של כספומט17,19. בשלב M של מיוזה I, מחקרים הראו כי נזק לדנ"א עשוי להפעיל מחסום מיוזה I המושרה על ידי ציר (SAC), אשר מונע את ההפעלה של E3 ubiquitin ligase anaphase-promoting complex/cyclosome (APC/C) ולכן, יציאה משלב M. יתר על כן, אבלציה של חלבוני SAC מתגברת על מצב של מעצר שלב M, ובכך מדגישה את חשיבותו של SAC בביסוס המיוזה I chekpoint20.
כפי שמחקרים קודמים מראים בבירור, DSBs אינם יכולים לגרום למחסום פאזה חזק בביציות עכבר. אם נזק כזה לא יתוקן, הוא עלול להוביל לעוברים הנושאים הפרעות כרומוזומליות. לכן, חשוב לחקור את תגובת הנזק לדנ"א בשלבים שונים של הגמטוגנזה הנשית כדי להבין טוב יותר את המסלולים הייחודיים שבהם הביציות משתמשות כדי להתמודד עם עלבונות גנטיים פוטנציאליים.
Protocol
כל ניסויי העכברים אושרו על ידי הרשויות המקומיות (אזור יואנינה, יוון) ונערכו בהתאם להנחיות מועצת הקהילות האירופית 2010/63/EU. ניסויים נערכו ביחס לעקרונות של 3Rs. כל עכברי CD-1 ששימשו לניסויים הוחזקו במתקן בית החיות של אוניברסיטת יואנינה, יוון, בחדר עם טמפרטורה מבוקרת (22 מעלות צלזיוס) ולחות (60%) והוזנו אד ליביטום. לבית החיות רישיון להפעלת מתקן לרבייה (EL33-BIObr01), אספקה (EL33-BIOsup01) וניסויים (EL33BIO-exp01).
1. הכנת ריאגנטים
- יש לדלל אבקת 3-איזובוטיל-1-מתיל-קסנטין (IBMX) (ראו טבלת חומרים) בדימתיל סולפוקסיד (DMSO) (ראו טבלת חומרים) לריכוז סופי של 200 מילימול. Μake 10 μL aliquots, ולאחסן ב -20 ° C. השתמש בפתרון תוך חודש.
הערה: אבקת IBMX נשמרת בטמפרטורה של -20°C. - הכינו את כל מאגרי האימונופלואורסנציה ואחסנו אותם ב -4 מעלות צלזיוס.
- הכינו מלח סטרילי חוצץ פוספט (PBS) על ידי דילול טבלית PBS אחת (ראו טבלת חומרים) ב-200 מ"ל של ddH2Ο.
- צור מאגר PHEM על ידי הוספת 80 מ"ל של ddH 2 Ο, 0.59575 גרם HEPES, 1.81422 גרם של PIPES, 0.38035 גרם של EGTA ו- 0.04066 גרם של MgCl2(ראה טבלת חומרים) תוך כדי התסיסה עם מערבל מגנטי (ראה טבלת חומרים), ובמקביל הוסף NaOH (ראה טבלת חומרים) עד שה- pH מגיע ל- 6.9 (בדוק באמצעות מד pH/ORP [ראה טבלת חומרים]). לאחר מכן, הוסף ddH2Ο לנפח סופי של 100 מ"ל.
- הכינו חיץ פרפורמאלדהיד-טריטון-X-100 (PFA-Tx-100) על ידי דילול אבקת PFA (ראו טבלת חומרים) במאגר PHEM תוך כדי התסיסה עם מערבל מגנטי תחת חימום בריכוז סופי של 4% PFA. לאחר מכן, סנן את המאגר באמצעות מזרק ומסנן 0.2 מיקרומטר (ראה טבלת חומרים), והוסף 0.5% Tx-100 (ראה טבלת חומרים). להכין כ 10 מ"ל של PFA-Tx-100 (0.4 גרם של PFA, 50 μL של Tx-100), וזה מספיק עבור ניסוי אחד. יש לאחסן אותו בטמפרטורה של 4°C למשך שבוע אחד לכל היותר.
אזהרה: יש ללבוש כפפות לטיפול ב-PFA, ולהימנע ממגע עם העור והעיניים. - הכינו את חיץ הכביסה על ידי הוספת אלבומין בסרום בקר (ריכוז סופי: 0.5% w/v BSA) (ראו טבלת חומרים) ב-PBS, והתסיסו באופן מכני. יש להוסיף חיץ 10% w/v NaN3 (נתרן אזיד) בדילול של 1:1,000 כדי למזער את הסיכון לזיהום פטרייתי וחיידקי. צור חיץ של 10% w/v NaN 3 על ידי הוספת 1 גרם של אבקת NaN3 (ראה טבלת חומרים) ל- 10 מ"ל של ddH2O; יש לאחסן את מאגר NaN3 בטמפרטורת החדר.
- הכן את מאגר החסימה על ידי הוספת BSA (ריכוז סופי: 3% w/v) ב- PBS ותסיסה מכנית. הוסף חיץ NaN3 של 10% בדילול של 1:1,000.
2. איסוף ביציות GV משחלות מנותחות והשראת DSB
הערה: כל הכלים והפתרונות צריכים להיות סטריליים. הטיפול בביציות מתבצע באמצעות פיפטה בפה תחת מיקרוסקופ סטריאו (ראו טבלת חומרים), וכל הטיפות מכוסות בשמן מינרלי (ראו טבלת חומרים ואיור 1E).
- יש להזריק לעכברים תוך צפקית 7 יחידות בינלאומיות (IU) של גונדוטרופין בסרום של סוסה הרה (PMSG) (ראה טבלת חומרים) 46-48 שעות לפני הדחת העכברים על ידי פריקת צוואר הרחם.
הערה: כל העכברים המשמשים צריכים להיות בני 8-12 שבועות. - סנן מדיום תרבית M2 (ראה טבלת חומרים) עם מזרק ומסנן 0.2 מיקרומטר, והוסף IBMX 200 מילימטר לריכוז סופי 200 מיקרומטר בצינור עגול בעל תחתית עגולה של 14 מ"ל (ראה טבלת חומרים) כדי לשמור על הביציות נעצרות בשלב I. לאחר מכן, הכינו טיפות של מדיום M2-IBMX בכלי תרבית רקמת פלסטיק (ראו טבלת חומרים), והניחו אותו על בלוק חם (ראו טבלת חומרים) בטמפרטורה של 37°C למשך 30 דקות לפחות לפני בידוד הביציות. אחסן את M2 בטמפרטורה של 4°C.
- הקריבו את העכברות על ידי פריקת צוואר הרחם, נתחו את השחלות, והניחו אותן בצינור תחתון עגול של 5 מ"ל (ראו טבלת חומרים) עם M2-IBMX.
- להעביר את השחלות למכסה פלסטיק המכיל 1.5 מ"ל של M2-IBMX, להסיר כל רקמת שומן פרי-שחלתית או מקטעי חצוצרות, ולשחרר את COC על ידי ניקוב מכני של השחלות עם מחט 27 G (ראה טבלת חומרים ואיור 1A-C).
- מעבירים את COC לצלחת תרבית עם טיפות של M2-IBMX (בערך 25-30 μL כל אחד), ולהסיר את תאי הקומולוס על ידי פיפט חוזר באמצעות פיפטה פסטר זכוכית צרה (ראו טבלת חומרים ואיור 1D).
- בחרו ביציות בשלב SN GV, והעבירו אותן בטיפה (25 μL) של תווך M2-IBMX על בלוק חם ב-37°C המוגן מפני אור (איור 1F).
- חפשו ביציות SN בהתבסס על גודלן הגדול יותר והגרעינים הממוקמים במרכז בניגוד לביציות NSN, בהן הגרעינים ממוקמים באופן היקפי21. בכל מקרה, התבונן בתצורת ה- DNA תחת מיקרוסקופ קונפוקלי לפני קבלת ההחלטה הסופית לגבי סוג הביציות GV (SN או NSN).
- השראת DSB באמצעות אטופוסיד (ראה טבלת חומרים). הניחו את הביציות בשלב GV בטיפות (25 μL כל אחת) של החומר הגנוטוקסי למשך שעה אחת על הבלוק החם בטמפרטורה של 37°C בתנאים חשוכים.
הערה: Etoposide הוא מעכב topoisomerase II המציג DSB ל- DNA22. שמור את etoposide ב 10 μL aliquots של 20 מ"ג / מ"ל בטמפרטורת החדר מוגן מפני אור. הריכוזים שנבדקו הם 5 מק"ג/מ"ל, 20 מק"ג/מ"ל ו-50 מק"ג/מ"ל. - כדי לשמור על הביציות בשלב GV עצורות לתקופה ממושכת, הניחו את הביציות בטיפות של מדיום תרבית M16 (ראו טבלת חומרים) בתוספת 400 מיקרומטר IBMX באינקובטור (ראו טבלת חומרים) בטמפרטורה של 37°C ו-5% CO2. אחסנו את M16 בטמפרטורה של 4°C, סננו את המדיום בעזרת מזרק ומסנן 0.2 מיקרומטר, ודגרו עליו לפחות שעה אחת לפני השימוש.
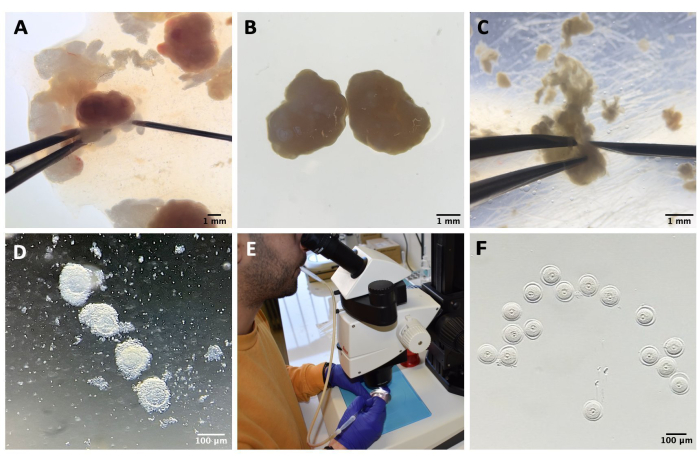
איור 1: תהליך בידוד ביציות . (A) הסרת רקמת שומן פרי-שחלתית ושאריות מקטעי חצוצרה משחלות בתווך M2 עם IBMX. התצלום מתקבל דרך עיניות המיקרוסקופ הסטריאופוני. סרגל קנה מידה = 1 מ"מ. (B) שחלות מבודדות בתווך M2 עם IBMX. התמונה התקבלה דרך עיניות המיקרוסקופ הסטריאופוני. סרגל קנה מידה = 1 מ"מ. (C) ניקוב מכני של השחלות באמצעות מחט 27 G בתווך M2 עם IBMX. התמונה התקבלה דרך עיניות המיקרוסקופ הסטריאופוני. סרגל קנה מידה = 1 מ"מ. (D) COC המשתחררים מהשחלות לאחר ניקוב בתווך M2 עם IBMX. התמונה התקבלה דרך עיניות המיקרוסקופ הסטריאופוני. סרגל קנה מידה = 100 מיקרומטר. (E) איסוף ביציות באמצעות פיפטה בפה. (F) ביציות דנודיות, לאחר הסרת תאי הקומולוס שמסביב, בתווך M2 עם IBMX. התמונה התקבלה דרך עיניות המיקרוסקופ הסטריאופוני. סרגל קנה מידה = 100 מיקרומטר. לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
3. קיבוע ביציות ואימונופלואורסנציה
הערה: הטיפול בביציות מתבצע באמצעות פיפטה בפה תחת מיקרוסקופ סטריאו, וכל הטיפות מכוסות בשמן מינרלי.
- הניחו את ביציות GV המטופלות בבקרה וטופוזיד בצלחות תרבית פלסטיק שונות עם חיץ PFA-Tx-100 למשך 40 דקות בטמפרטורת החדר.
- שטפו את הביציות בשלוש טיפות שונות של חיץ כביסה (50 מיקרוליטר כל אחת) בטמפרטורת החדר. השאירו את הביציות למשך 5 דקות בכל טיפה.
- הניחו את הביציות בטיפות של חיץ חוסם (25 μL כל אחת) למשך שעה אחת על בלוק חם ב 37 ° C.
- הכינו את הנוגדן הראשוני המזהה γH2AX (ארנב פוספו-Η2ΑΧ) (Ser139) (ראו טבלת חומרים) (תמיסת מלאי: 1 מ"ג/מ"ל). השתמש דילול 1:200 בחיץ חוסם, ומניחים את הביציות בטיפות של נוגדן ראשוני (15 μL כל אחת) ב 4 ° C במשך הלילה.
הערה: Phospho-Η2ΑΧ (γH2AX) הוא סמן נפוץ לגילוי DSB הן בתאים סומטיים והן בביציות GV18,23. - למחרת, שטפו את הביציות בשלוש טיפות שונות של חיץ כביסה (50 מיקרוליטר כל אחת) בטמפרטורת החדר. השאירו את הביציות למשך 5 דקות בכל טיפה.
- הכינו את הנוגדן המשני, Alexa Fluor 488-conjugated goat goat anti-rabbit (ראו טבלת חומרים) (תמיסת מלאי: 2 מ"ג/מ"ל). השתמשו בדילול בקנ"מ 1:200 בחיץ חוסם, והניחו את הביציות בטיפות של נוגדן משני (15 מיקרוליטר כל אחת) למשך שעה אחת על בלוק חם בטמפרטורה של 37°C המוגנת מפני אור.
- מעבירים את הביציות לטיפות של DRAQ7 (25 μL כל אחת) (תמיסת מלאי: 0.3 מילימול; ראו טבלת חומרים), שהוא צבע דנ"א פלואורסצנטי אדום רחוק שמכתים DNA רק בתאים חדירים. יש להשתמש בדילול בקנ"מ 1:250 במאגר הכביסה למשך 10 דקות בטמפרטורת החדר בתנאי חושך.
- שטפו את הביציות בשלוש טיפות שונות של חיץ כביסה (50 מיקרוליטר כל אחת) בטמפרטורת החדר. השאירו אותם למשך 5 דקות בכל טיפה, ואז העבירו אותם לטיפות קטנות (כ-5 מיקרוליטר כל אחת) של חיץ כביסה בצלחת פטרי בקוטר 35 מ"מ עם תחתית זכוכית (ראו טבלת חומרים) למיקרוסקופ קונפוקלי (איור 2A).
הערה: שטיפת כתם הדנ"א והנוגדן המשני מתבצעת בו זמנית.
4. מיקרוסקופ קונפוקלי
הערה: יש לבצע מיקרוסקופ קונפוקלי באופן מיידי כדי למנוע את הירידה בעוצמת הפלואורסצנטיות לאחר מיקום הביציות בכלים בעלי תחתית זכוכית. נדרשת גישה למיקרוסקופ קונפוקלי (ראה טבלת חומרים) עם במה ממונעת.
- הגדרת מיקרוסקופ
- במערכת הקונפוקלית הפעילו את בקר הלייזר, את הלייזרים, את בקר המיקרוסקופ, את המנורות עבור האור המשודר ואת המחשב האישי (איור 2B, D).
- פתח את תוכנת confocal, ובחר עדשת שמן 40x.
- הניחו את המנה במחזיק הדגימה, ונסו להתמקד בביציות על-ידי הזזת הבמה על צירי XY ו-Z באמצעות הג'ויסטיק (איור 2C).
- סריקת הביציות
- הגדר את עוצמת הלייזר, את הרווח ואת גודל חור הסיכה בנפרד עבור כל ניסוי על מנת למזער כל רוויה.
- עבור כל ביצית, הגדר את אזור העניין, במיוחד בגרעין באזור ה- DNA. הגדירו את גבולות אזור הדנ"א והתאימו את גודל צעד z ל-3 מיקרומטר. לאחר מכן, התחל בסריקה.
- שמרו את התמונות לכל תא בתיקייה שנבחרה.
- בסיום הסריקה, צא מהתוכנה, כבה את המחשב וכבה את בקר הלייזר, את הלייזרים, את בקר המיקרוסקופ ואת המנורות עבור האור המשודר.
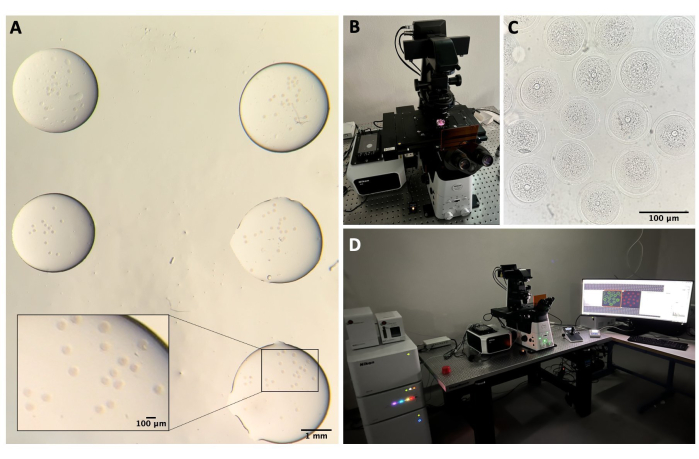
איור 2: מיקרוסקופ קונפוקלי. (A) ביציות קבועות לאחר ביצוע פרוטוקול אימונופלואורסנציה וצביעת דנ"א, שנמצאות בטיפות נפרדות של חיץ כביסה, מכוסות בשמן מינרלי, מונחות בכלי עם תחתית זכוכית ומוכנות להדמיית מיקרוסקופ קונפוקלי. כל טיפה מכילה קטגוריה ניסיונית אחרת. התמונה התקבלה דרך עיניות המיקרוסקופ הסטריאופוני. סרגל קנה מידה = 1 מ"מ/100 מיקרומטר עבור החלק המוגדל. (B) פלטה בעלת תחתית זכוכית המונחת על במת המיקרוסקופ הקונפוקלי. (C) תמונת שדה בהיר של ביציות המתקבלת באמצעות מיקרוסקופ קונפוקלי. סרגל קנה מידה = 100 מיקרומטר. (D) מערכת המיקרוסקופ הקונפוקלי. אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
5. ניתוח הדמיה
- הורד את Fiji ImageJ-win64 בדפדפן (https://imagej.net/software/fiji/downloads), פתח אותו וייבא את הנתונים כקבצי מחסנית TIFF.
הערה: פתח כל קובץ ביציות בנפרד. - לחץ על תמונה | צבע | פצל ערוצים כדי לפצל את כל הערוצים.
- לחץ על LUT (חפש טבלה) ובחר את הצבעים המועדפים עבור כל ערוץ.
- לחץ על תמונה | צבע | מזג ערוצים כדי למזג את הערוצים עבור γΗ2ΑΧ ו- DNA. השאר את ערוץ brightfield לא ממוזג.
- בביציות NSN וביציות SN עם רמות נמוכות של נזק לדנ"א, γΗ2ΑΧ מזוהה כמוקדים באזור הדנ"א. במקרה זה, לחץ על הפקודה " Multi-point" או point , ובחר כל מוקד γΗ2ΑΧ שעולה בקנה אחד עם ה- DNA. חזור על שלב זה עבור כל הערימות.
- בביציות SN עם רמות גבוהות של נזק לדנ"א, אות γΗ2ΑΧ מופץ בכל אזור הדנ"א. במקרה זה, לחץ על תמונה | ערימות | פרויקט Z, ובעזרת הפקודה Freehand selections , בחר את כל אזור ה- DNA.
- כדי למדוד את הפלואורסצנטיות γΗ2ΑΧ, לחץ על נתח | מדדו והעתיקו את המדידות לקובץ .xlsx. לאחר מכן, חשב את הפלואורסצנטיות הממוצעת, נרמל את הערכים וספור את מספר המוקדים לפני יצירת גרפים כלשהם.
- לחץ על נתח | הגדר קנה מידה כדי להגדיר את קנה המידה ולאחר מכן על נתח | כלים | סרגל קנה מידה כדי להוסיף סרגל קנה מידה לערוצים.
Representative Results
באמצעות ההליך שהודגם כאן, נותחו שחלות עכברים, הוסר השומן ונאספו ביציות מלאות בשלב GV. לאחר מכן, תאי הקומולוס הוסרו על-ידי פיפטינג חוזר ונשנה באמצעות פיפטה צרה, והונחו בטיפות טריות של מדיום M2-IBMX וכוסו בשמן מינרלי על בלוק חם (37°C) (איור 1A-F). הוכנו שלושה ריכוזי אטופוסיד שונים (5 מק"ג/מ"ל, 20 מק"ג/מ"ל ו-50 מק"ג/מ"ל) באמצעות ריכוז אטופוסיד מלאי של 20 מ"ג/מ"ל. הביציות בשלב GV הוכנסו לשלושה ריכוזים אטופוזידים נפרדים למשך שעה אחת בטיפות המכוסות בשמן מינרלי ומוגנות מפני אור בטמפרטורה של 37°C. לאחר מכן בוצע פרוטוקול האימונופלואורסנציה, כפי שמתואר בסעיף הפרוטוקול בפירוט, והביציות הונחו בצלחות עם תחתית זכוכית ונצפו במיקרוסקופ קונפוקלי (איור 2).
בביציות בשלב SN GV, מיד לאחר נזק לדנ"א, נוכחות γH2AX עלתה בכל ריכוזי האטופוזידים (5 מיקרוגרם/מ"ל, 20 מק"ג/מ"ל ו-50 מק"ג/מ"ל), וה-γH2AX פוזר בכל אזור הדנ"א (איור 3). כימות ואומדן DSB בוצעו על ידי צפייה בעוצמת הפלואורסצנטיות γH2AX באתרי DNA. הפלואורסצנטיות γH2AX התעצמה באופן יחסי עם עליית ריכוזי האטופוסידים. יתר על כן, לאחר מעצר שלב ממושך (20 שעות לאחר טיפול אטופוסידי), הביציות בשלב GV הראו את היכולת להפחית את מספר מוקדי γH2AX ואת עוצמתם, מה שמרמז על נוכחות של תהליכי תיקון פעילים בביציות שנעצרו בשלב GV (איור 3E).
בניגוד לביציות SN, שבהן הפלואורסצנטיות γH2AX הופצה דרך הדנ"א, בביציות NSN, γH2AX הוצג במוקדים מיד לאחר הטיפול באטופוסיד ב 20 מיקרוגרם / מ"ל. הערכנו את מספר המוקדים שחפפו לאזור הדנ"א, חישבנו את הפלואורסצנטיות של כל מוקד, והצגנו את הפלואורסצנטיות הממוצעת של כל הביציות. גם הפלואורסצנטיות וגם מספר המוקדים הראו הבדלים מובהקים סטטיסטית בין שתי קטגוריות הביציות (איור 4).
מיקרוסקופ קונפוקלי מספק מידע על מספר ועוצמת המוקדים בערימות Z שונות, ובכך מסייע לזהות את נוכחות הנזק לדנ"א ואת דינמיקת התיקון בנקודות זמן שונות. סריקת Galvano מספקת סריקה מדויקת עם רקע נמוך וניתוח טוב יותר של תמונות הסריקה.
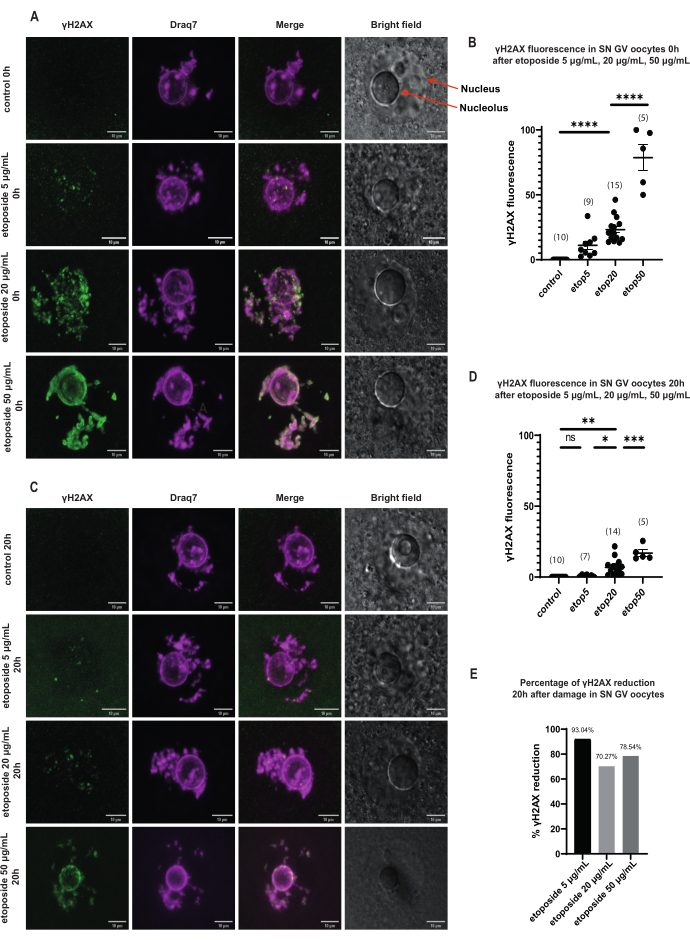
איור 3: הפחתה של γH2AX בביציות בשלב SN GV שטופלו בשלושה ריכוזי אטופוסיד שונים לאחר מעצר GV ממושך. (A) פלואורסצנטיות γH2AX בביציות SN GV שלב 0 שעות לאחר טיפול אטופוסידי. γH2AX עולה מיד לאחר החשיפה בכל ריכוזי האטופוסידים, והעלייה תלויה בריכוז (ירוק: γΗ2ΑΧ, מגנטה: DNA). התמונות הן הקרנות Z-stack, והבהירות/ניגודיות הותאמו לכל ערוץ באמצעות Fiji / ImageJ. סרגל קנה מידה = 10 מיקרומטר. (B) גרף של פלואורסצנטיות γH2AX בביציות SN GV שלב 0 שעות לאחר הטיפול עם ריכוזי אטופוסיד מובהקים. הנתונים מייצגים ממוצע ± SEM. כל נקודה מייצגת ביצית אחת (מספר הביציות מוצג בגרף), (ns = לא מובהק, ** p < 0.005, **** p < 0.0001, ANOVA חד כיווני עם מבחן השוואות מרובות של Tukey). (C) γH2AX פלואורסצנטיות בביציות בשלב SN GV 20 שעות לאחר טיפול אטופוסידי. γH2AX מפחית 20 שעות לאחר החשיפה בכל ריכוזי האטופוסיד (ירוק: γΗ2ΑΧ, מגנטה: DNA). התמונות הן הקרנות מסוג Z-stack, והבהירות/ניגודיות הותאמו לכל ערוץ באמצעות Fiji/ImageJ. סרגל קנה מידה = 10 מיקרומטר. (D) גרף של פלואורסצנטיות γH2AX בביציות SN GV שלב 20 שעות לאחר הטיפול עם ריכוזי אטופוסיד מובהקים. הנתונים מייצגים ממוצע ± SEM. כל נקודה מייצגת ביצית אחת (מספר הביציות מוצג בגרף), (ns = לא מובהק, * p < 0.05, * * p < 0.005, *** p < 0.0005, **** p < 0.0001, ANOVA חד כיווני עם מבחן השוואות מרובות של Tukey). (E) גרף עמודות של הפחתת פלואורסצנטיות γH2AX בביציות בשלב SN GV לאחר מעצר שלב בביציות שטופלו באטופוזיד. המספר מעל כל עמודה מציין את אחוז הירידה בפלואורסצנטיות γH2AX. אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
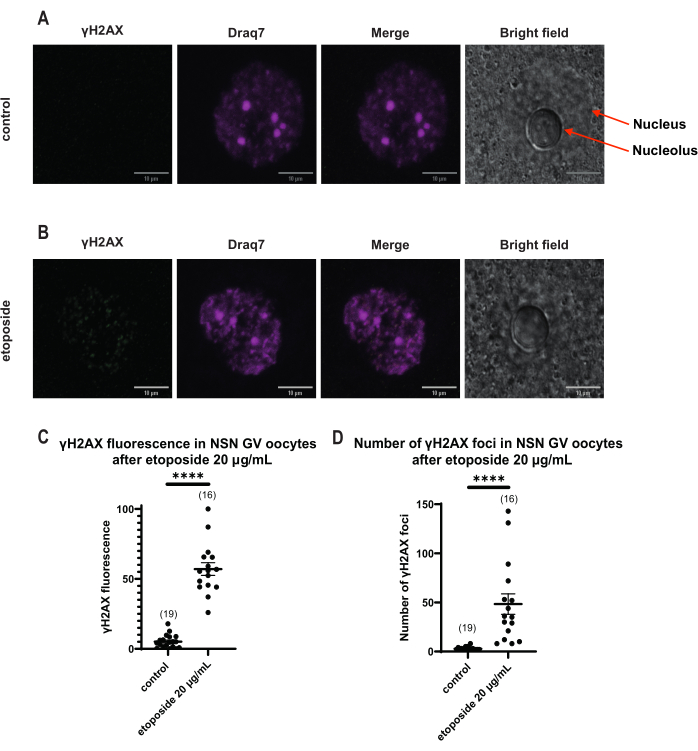
איור 4: זרחן של Η2ΑΧ בביציות בשלב GV של NSN לאחר טיפול באטופוסיד ב-20 מיקרוגרם/מ"ל. (A) תמונות קונפוקליות מייצגות של ביצית NSN GV אחת (ירוק: γΗ2ΑΧ, מגנטה: DNA). התמונות הן הקרנות מסוג Z-stack, והבהירות/ניגודיות הותאמו לכל ערוץ באמצעות Fiji/ImageJ. סרגל קנה מידה = 10 מיקרומטר. (B) תמונות קונפוקליות מייצגות של ביצית NSN GV אחת שטופלה באטופוסיד (ירוק: γΗ2ΑΧ, מגנטה: DNA). הביציות תוקנו 0 שעות לאחר טיפול אטופוסידי. התמונות הן הקרנות מסוג Z-stack, והבהירות/ניגודיות הותאמו לכל ערוץ באמצעות Fiji/ImageJ. סרגל קנה מידה = 10 מיקרומטר. (C) הפלואורסצנטיות γΗ2ΑΧ המנורמלת בביציות בשלב GV של NSN לאחר טיפול אטופוסיד של 20 מיקרוגרם/מ"ל. הנתונים מייצגים ממוצע ± SEM. כל נקודה מייצגת ביצית אחת (מספר הביציות מוצג בגרף), שנלקחה משני ניסויים עצמאיים (**** p < 0.0001, מבחן t לא פרמטרי לא מזווג, מבחן U-Mann-Whitney). (D) מספר מוקדי γΗ2ΑΧ בביציות בשלב NSN GV לאחר טיפול אטופוסיד של 20 מיקרוגרם/מ"ל. הנתונים מייצגים ממוצע ± SEM. כל נקודה מייצגת ביצית אחת (מספר הביציות מוצג בגרף), שנלקחה משני ניסויים עצמאיים (**** p < 0.0001, מבחן t לא פרמטרי לא מזווג, מבחן U-Mann-Whitney). אנא לחץ כאן כדי להציג גרסה גדולה יותר של איור זה.
Discussion
באמצעות השיטה המתוארת כאן, זיהינו DSB בביציות יונקים. שיטה זו מאפשרת איתור ולימוד של תהליך תיקון הדנ"א בביציות. אותו פרוטוקול יכול לשמש גם לניתוח חלבונים אחרים המשתתפים בתהליכים פיזיולוגיים בביציות יונקים. חשוב לחקור כיצד הביציות מגיבות לנזק פוטנציאלי לדנ"א על מנת להבין טוב יותר את הגורם לתת-פוריות נשית בבני אדם.
חקר תגובת הנזק לדנ"א בביציות יונקים יכול להיות מאתגר בגלל הרגישות של הביציות. טיפול בביציות דורש טמפרטורות ספציפיות וריכוזי CO 2ו-O 2. יחד עם זאת, הביציות חייבות להיות מוגנות מפני אור. הטיפול צריך להיעשות על ידי שימוש בפיפטות זכוכית שאינן צרות, שכן הדבר עלול להזיק לביציות, אך גם לא לרוחב, שכן הדבר עלול לגרום לדילול המדיום ובכך להשפיע לרעה על הליך הקיבוע. בכל שלב של קיבוע, כמה טיפות של חוצצים משמשים כדי למזער את אפקט דילול. דרך חלופית לתצפית ב-DSB היא בדיקת השביט24. למרות שטכניקה זו רגישה יותר, היא מורכבת יותר. יחד עם זאת, באמצעות שימוש בניסוי השביט לא ניתן לזהות את אזור הדנ"א המדויק שבו מתרחש הנזק, ובתאים עם מולקולות רנ"א בשפע, כמו ביציות בשלב GV 25, הרקע יכול להיות מוגבר, מה שיוביל לאות נזק כוזבלדנ"א26.
על ידי שימוש בפרוטוקול immunofluorescence המתואר כאן, אנו יכולים לזהות DSB בדיוק ולהעריך את התקדמות התיקון בביציות בשלב GV, כפי שמצוין על ידי הפחתת פלואורסצנטיות γH2AX לאורך זמן. עם זאת, מגבלה אחת של שיטה זו היא כי נוגדנים מסוימים עשויים להציג פיזור לא ספציפי ברחבי ooplasm, ובכך להוביל תמונות עם פלואורסצנטיות רקע גבוהה. מאגר PFA-Tx-100 משמש במקום PFA רציף ו- Tx-100, כפי שראינו כי הוא משפר את תהליך הקיבוע בכך שהוא מאפשר זיהוי של פחות רקע ופלואורסצנטיות לא ספציפית. מגבלה שנייה של שימוש ב- γH2AX לזיהוי DSB היא שלא ניתן להעריך נזק לאחר GVBD בגלל הזרחן הספונטני של γH2AX במיוזה23.
בפרוטוקול אימונופלואורסנציה זה, הביציות נשארות במאגר נוזלי ולא ניתן לאחסן אותן בתוך שקופיות. עובדה זו מקשה על שימור התאים הקבועים במשך ימים לאחר הוספת הנוגדן המשני. על מנת להשיג תמונות באיכות טובה ולא לאבד אות, עדיף לבצע את ההדמיה תוך מספר שעות לאחר הוספת הנוגדן המשני. כמו כן יש לציין כי סריקת הגרעינים דרך ציר Z עלולה לגרום לאות להיחלש עקב חשיפת יתר. מסיבה זו, עדיף להוריד את עוצמת הלייזר ולהגביר את מהירות הסריקה.
לבסוף, מגבלה נוספת של פרוטוקול האימונופלואורסנציה היא שניתן להשתמש בו רק עבור תאים קבועים / לא חיים. לכן, אנו יכולים להעריך רק את נוכחותם והיעדרם של גורמים בנקודות זמן ספציפיות מבלי לדעת אם יש תנודות בריכוזם או שינויים בהתנהגותם לאורך זמן. ניתן להתגבר על בעיה זו באמצעות דימות תאים חיים וסמנים מתויגים פלואורסצנטית.
Disclosures
למחברים אין ניגודי עניינים.
Acknowledgements
אנו מודים על תמיכה בעבודה זו מהפרויקט "הקמת תשתיות 'בניית יכולות' במחקר ביו-רפואי (BIOMED-20)" (MIS 5047236), המיושם במסגרת הפעולה "חיזוק תשתית המחקר והחדשנות", במימון התוכנית האופרטיבית "תחרותיות, יזמות וחדשנות" (NSRF 2014-2020), ובמימון משותף של יוון והאיחוד האירופי (הקרן האירופית לפיתוח אזורי).
Materials
| Name | Company | Catalog Number | Comments |
| 3 mL Pasteur pipettes in LDPE, graduated | APTACA | 1502 | |
| 10 cc syringes | SoftCare | 114.104.21 | |
| Alexa Fluor 488-conjugated goat anti-rabbit Secondary Ab | Biotium | 20012 | |
| Anti-phospho-H2A.X (Ser139) | Merck Millipore | 07-164 | |
| ARE Heating Magnetic Stirrer | VELP Scientifica | F20500162 | |
| BD FALCON 5 mL Polystyrene Round-Bottom Tubes | BD Biosciences | 352054 | |
| BD Microlance 3 Needles 27 G - 0.40 x 13 mm | Becton Dickinson | 300635 | |
| Bovine Serum Albumin Fraction V | Roche | 10735078001 | |
| DMSO Anhydrous | Biotium | 90082 | |
| DRAQ7 DNA dye | BioStatus | DR71000 | |
| EGTA | Sigma-Aldrich | E4378-25G | |
| EMSURE MgCl2. 6H2O | Merck Millipore | 1058330250 | |
| Etoposide | CHEMIPHARM | L01CB01 | |
| FALCON 14 mL Polystyrene Round-Bottom Tubes | Corning Science | 532057 | |
| FALCON Tissue Culture Dishes, Easy-Grip, 35 x 10 mm Style | Corning Science | 353001 | |
| Glass Bottom Culture Dishes (35 mm Petri dish/ 14 mm Microwell, No. 0 coverglass) | MatTek Corporation | P35G-0-14-C | |
| HEPES | Sigma-Aldrich | H6147-25G | |
| HERACELL 150i CO2 Incubator | ThermoFisher Scientific | 50116048 | |
| IBMX powder | Sigma-Aldrich | I5879-100MG | |
| Leica M125 Stereo Microscope | Leica Microsystems | ||
| M16 Medium | Sigma-Aldrich | M7292 | |
| M2 Medium | Sigma-Aldrich | M7167 | |
| Mineral Oil | Sigma-Aldrich | M5310 | |
| NaN3 | Honeywell | 13412H | |
| NaOH | Merck Millipore | 1064981000 | |
| Nikon AX ECLIPSE Ti2 Confocal Microscope | Nikon Corporation | ||
| Nikon SMZ800N Stereo Microscope | Nikon Corporation | ||
| Paraformaldehyde | Sigma-Aldrich | 158127 | |
| Pasteur pippettes, glass, long form 230 mm | DURAN WHEATON KIMBLE | 357335 | |
| pH/ORP meter | Hanna Instruments Ltd | HI2211 | |
| Phosphate buffered saline tablets | Sigma-Aldrich | P4417-100TAB | |
| PIPES | Sigma-Aldrich | P1851 | |
| PMSG Protein Lyophilised | Genway Biotech (now AVIVA Systems Biology) | GWB-2AE30A (now OPPA01037) | |
| QBD4 Dry block heater | Grant Instruments (Cambridge) Ltd | A25218 | |
| Triton X-100 | Sigma-Aldrich | T8787 | |
| Whatman Puradisc 25 mm 0.2 μm filters | GE Healthcare | 6780-2502 |
References
- Wang, X., Pepling, M. E. Regulation of meiotic prophase one in mammalian oocytes. Frontiers in Cell and Developmental Biology. 9, 667306 (2021).
- Filatov, M., Khramova, Y., Semenova, M. Molecular mechanisms of prophase I meiotic arrest maintenance and meiotic resumption in mammalian oocytes. Reproductive Sciences. 26 (11), 1519-1537 (2019).
- Adhikari, D., et al. Inhibitory phosphorylation of Cdk1 mediates prolonged prophase I arrest in female germ cells and is essential for female reproductive lifespan. Cell Research. 26 (11), 1212-1225 (2016).
- Sun, S. C., Kim, N. H. Molecular mechanisms of asymmetric division in oocytes. Microscopy and Microanalysis. 19 (4), 883-897 (2013).
- Jones, K. T. Mammalian egg activation: From Ca2+ spiking to cell cycle progression. Reproduction. 130 (6), 813-823 (2005).
- Solc, P., Schultz, R. M., Motlik, J. Prophase I arrest and progression to metaphase I in mouse oocytes: comparison of resumption of meiosis and recovery from G2-arrest in somatic cells. Molecular Human Reproduction. 16 (9), 654-664 (2010).
- Parfenov, V., Potchukalina, G., Dudina, L., Kostyuchek, D., Gruzova, M. Human antral follicles: oocyte nucleus and the karyosphere formation (electron microscopic and autoradiographic data). Gamete Research. 22 (2), 219-231 (1989).
- Zuccotti, M., Piccinelli, A., Giorgi Rossi, P., Garagna, S., Redi, C. A. Chromatin organization during mouse oocyte growth. Molecular Reproduction and Development. 41 (4), 479-485 (1995).
- Sun, X., et al. Comprehensive analysis of nonsurrounded nucleolus and surrounded nucleolus oocytes on chromatin accessibility using ATAC-seq. Molecular Reproduction and Development. 90 (2), 87-97 (2023).
- Zuccotti, M., Bellone, M., Longo, F., Redi, C. A., Garagna, S. Fully-mature antral mouse oocytes are transcriptionally silent but their heterochromatin maintains a transcriptional permissive histone acetylation profile. Journal of Assisted Reproduction and Genetics. 28 (12), 1193-1196 (2011).
- Winship, A. L., Stringer, J. M., Liew, S. H., Hutt, K. J. The importance of DNA repair for maintaining oocyte quality in response to anti-cancer treatments, environmental toxins and maternal ageing. Human Reproduction Update. 24 (2), 119-134 (2018).
- Lieber, M. R. The mechanism of human nonhomologous DNA end joining. The Journal of Biological Chemistry. 283 (1), 1-5 (2008).
- Chiruvella, K. K., Liang, Z., Wilson, T. E. Repair of double-strand breaks by end joining. Cold Spring Harbor Perspectives in Biology. 5 (5), 012757 (2013).
- Chang, H. H. Y., Pannunzio, N. R., Adachi, N., Lieber, M. R. Non-homologous DNA end joining and alternative pathways to double-strand break repair. Nature Reviews. Molecular Cell Biology. 18 (8), 495-506 (2017).
- Shibata, A., Jeggo, P. A. Roles for the DNA-PK complex and 53BP1 in protecting ends from resection during DNA double-strand break repair. Journal of Radiation Research. 61 (5), 718-726 (2020).
- Mohiuddin, I. S., Kang, M. H. DNA-PK as an emerging therapeutic target in cancer. Frontiers in Oncology. 9, 635 (2019).
- Marangos, P., Carroll, J. Oocytes progress beyond prophase in the presence of DNA damage. Current Biology. 22 (11), 989-994 (2012).
- Paull, T. T., et al. A critical role for histone H2AX in recruitment of repair factors to nuclear foci after DNA damage. Current Biology. 10 (15), 886-895 (2000).
- Bakkenist, C. J., Kastan, M. B. DNA damage activates ATM through intermolecular autophosphorylation and dimer dissociation. Nature. 421 (6922), 499-506 (2003).
- Marangos, P., et al. DNA damage-induced metaphase I arrest is mediated by the spindle assembly checkpoint and maternal age. Nature Communications. 6, 8706 (2015).
- Lavrentyeva, E. A., Shishova, K. V., Zatsepina, O. V. Differences in nuclear dynamics in mouse GV oocytes with a diverse chromatin configuration. Biology Bulletin Russian Academy of Sciences. 46, 332-341 (2019).
- Montecucco, A., Zanetta, F., Biamonti, G. Molecular mechanisms of etoposide. EXCLI Journal. 14, 95-108 (1998).
- Mayer, A., et al. DNA damage response during mouse oocyte maturation. Cell Cycle. 15 (4), 546-558 (2016).
- Olive, P., Banáth, J. The comet assay: A method to measure DNA damage in individual cells. Nature Protocols. 1, 23-29 (2006).
- Wu, D., Dean, J. EXOSC10 sculpts the transcriptome during the growth-to-maturation transition in mouse oocytes. Nucleic Acids Research. 48 (10), 5349-5365 (2020).
- Simon, L., Emery, B., Carrell, D., Agarwal, A., Henkel, R., Majzoub, A. DNA damage: COMET assay. Manual of Sperm Function Testing in Human Assisted Reproduction. , 202-212 (2021).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionThis article has been published
Video Coming Soon
ABOUT JoVE
Copyright © 2025 MyJoVE Corporation. All rights reserved