生細胞STEDイメージングを用いた神経細胞モデルにおけるミトコンドリア内膜の微細構造の可視化
要約
このプロトコルは刺激された放出枯渇(STED)の顕微鏡検査を使用してミトコンドリアの微細構造の視覚化および分析のための培養されたSH-SY5Yのセルそして第一次ラットの海馬ニューロンの伝播、微分および汚損のためのワークフローを示す。
要約
ミトコンドリアは、エネルギー産生、Ca2+ ホメオスタシスの調節、脂質生合成、活性酸素種(ROS)の産生など、細胞内で多くの重要な役割を果たしています。これらのミトコンドリアを介したプロセスは、ニューロンにおいて特殊な役割を担い、これらの細胞の高エネルギー需要を満たすために好気性代謝を調整し、Ca2+ シグナル伝達を調節し、軸索の成長と再生のための脂質を供給し、ニューロンの発達と機能のためにROS産生を調整します。したがって、ミトコンドリアの機能不全は神経変性疾患の中心的な要因です。ミトコンドリアの構造と機能は密接に関連しています。形態学的に複雑な内膜は、クリステと呼ばれる構造的な折り目を持ち、ミトコンドリアの特徴的なプロセスを実行する多くの分子システムを持っています。内膜の構造的特徴は超微細構造であるため、従来の回折限界分解顕微鏡では小さすぎて可視化できません。したがって、ミトコンドリアの超微細構造に関するほとんどの洞察は、固定されたサンプルの電子顕微鏡から得られています。しかし、超解像蛍光顕微鏡の新技術により、数十ナノメートルまでの分解能が得られ、生細胞の微細構造の特徴を可視化できるようになりました。したがって、超解像イメージングは、ミトコンドリア構造、ナノスケールのタンパク質分布、およびクリステの動態の細部を直接画像化する前例のない能力を提供し、ミトコンドリアを人間の健康や病気に結び付ける基本的な新しい洞察を提供します。このプロトコルは生きている人間のneuroblastomaのセルおよび第一次ラットのニューロンのミトコンドリアの微細構造を視覚化するのに刺激された放出の枯渇(STED)の超解像の顕微鏡検査の使用を示す。この手順は、(1)SH-SY5Y細胞株の増殖と分化、(2)初代ラット海馬ニューロンの単離、プレーティング、および増殖、(3)ライブSTEDイメージングのための細胞の染色手順、(4)参照用のSTED顕微鏡を使用した生細胞STED実験の手順、および(5)内膜の形態学的特徴を測定および定量するための例を使用したセグメンテーションと画像処理のガイダンスの5つのセクションで構成されています。
概要
ミトコンドリアは、中間代謝やATP産生、イオンホメオスタシス、脂質生合成、プログラム細胞死(アポトーシス)など、いくつかの重要な細胞プロセスの調節に関与する内部共生起源の真核生物細胞小器官です。これらの細胞小器官はトポロジー的に複雑であり、複数のサブコンパートメント1を確立する二重膜系を含んでいます(図1A)。外側のミトコンドリア膜(OMM)は細胞質と界面し、細胞小器官間の直接的な接触を確立する2,3。ミトコンドリア内膜(IMM)は、主に電気膜電位(ΔΨm)として蓄えられたイオン勾配を維持し、ATP合成やその他のエネルギーを必要とするプロセスを駆動するエネルギー保存膜です4,5。IMMはさらに、OMMに密着した内界膜(IBM)と、クリステ膜(CM)に結合したクリステと呼ばれる突出構造に細分化されます。この膜は、最も内側のマトリックスコンパートメントを、胴体内腔(ICS)と膜間腔(IMS)から区別します。
ミトコンドリアは、ダイナミンスーパーファミリー6のメカノ酵素によって支配される核分裂と融合の連続的かつバランスの取れたプロセスに基づく動的な形態を持っています。融合は接続性の向上と網状ネットワークの形成を可能にするが、核分裂はミトコンドリアの断片化を引き起こし、マイトファジーによる損傷したミトコンドリアの除去を可能にする7。ミトコンドリアの形態は、組織タイプ8および発生段階9によって異なり、細胞がエネルギー的ニーズ10,11およびストレッサー12などの要因に適応できるように制御されている。ミトコンドリアの標準的な形態学的特徴、例えばネットワーク形成の程度(相互接続または断片化)、周囲長、面積、体積、長さ(アスペクト比)、真円度、分岐の程度など)は、これらの特徴のサイズが光の回折限界(~200 nm)よりも大きいため、標準的な光学顕微鏡で測定および定量化できます13。
クリステの構造は、ミトコンドリアの内部構造を定義しています(図1B)。クリステの形態の多様性は、扁平(層状または円盤状)または管状小胞に大別できる14。すべてのクリステは、クリステジャンクション(CJ)と呼ばれる管状またはスロット状の構造を介してIBMに取り付けられ、IMSとICSを、IBMとCM15を区切るのに役立ちます。クリステの形態は、(1)CJに常駐し、IMM-OMM接触を安定化するミトコンドリア接触部位およびクリステ組織化系(MICOS)16、(2)クリステリモデリングを調節する視神経萎縮1(OPA1)GTPアーゼ17,18,19、および(3)クリステ先端(CT)で安定化オリゴマー体集合体を形成するF1FOATP合成酵素を含む、IMMの主要なタンパク質複合体によって調節される20。21。さらに、IMMは、高度に湾曲したIMM22を安定化する非二層リン脂質ホスファチジルエタノールアミンおよびカルジオリピンを豊富に含んでいる。クリステも動的であり、異なる代謝状態23,24、異なる呼吸基質25、飢餓および酸化ストレス26,27、アポトーシス28,29、老化30など、さまざまな条件下で形態学的変化を示します.最近、クリステは数秒のタイムスケールで大きな改造イベントを受ける可能性があることが示され、そのダイナミックな性質が強調されています31。個々のクリスタ内の構造の寸法(例えば、CJ幅、クリスタの長さ、幅)や、個々のクリスタを他の構造と関連付けるパラメータ(例えば、クリステ内の間隔やOMMに対するクリステ入射角)など、クリステのいくつかの特徴を定量化することができる32。これらの定量化可能なクリステパラメータは、関数との直接的な相関関係を示しています。例えば、ミトコンドリアのATP産生の程度は、クリステの存在量と正の相関があり、クリステ密度またはクリステ数として定量化され、別の特徴(例えば、OMM面積あたりのクリステ)に正規化される33,34,35。IMMの形態はナノスケールの特徴によって定義されるため、ミトコンドリアの超微細構造で構成されており、光回折限界を超える分解能を提供するイメージング技術が必要です。後述するように、このような技術には、電子顕微鏡法および超解像顕微鏡法(ナノスコピー)が含まれる。
中枢神経系(CNS)の神経細胞とグリア細胞は、特にミトコンドリア機能に依存しています。平均して、脳は総体重の2%しか構成していませんが、全身のグルコースの25%を利用し、体の酸素消費量の20%を占めているため、エネルギー代謝の障害に対して脆弱です36。アルツハイマー病(AD)、筋萎縮性側索硬化症(ALS)、ハンチントン病(HD)、多発性硬化症(MS)、パーキンソン病(PD)などの進行性神経変性疾患(ND)は、これまでで最も広く研究されている病態の一部であり、これらの疾患の分子基盤の理解から潜在的な治療予防と介入の探求まで、さまざまな研究努力が行われています。NDは、ミトコンドリアの電子伝達系(ETC)37によって生成される活性酸素種(ROS)や、ミトコンドリアのカルシウム処理38、ミトコンドリアの脂質代謝の変化39に部分的に起因した酸化ストレスの増加と関連している。これらの生理学的変化は、AD 40、41、42、43、44、ALS 45、46、HD 47、48、49、MS50、およびPD51、52、53に関連するミトコンドリア形態の顕著な欠陥を伴います.これらの構造的および機能的欠陥は、複雑な因果関係によって結合される可能性があります。例えば、クリステの形態がOXPHOS酵素を安定化させる54とすれば、ミトコンドリア活性酸素はETCによって生成されるだけでなく、ETCが存在するインフラにダメージを与える働きをし、酸化的損傷に対する感受性を高めるフィードフォワード活性酸素サイクルを促進する。さらに、クリステの解体は、ミトコンドリアDNA(mtDNA)の放出や、自己免疫疾患、代謝疾患、加齢性疾患に関連する炎症経路などのプロセスを引き起こすことが示されている55。したがって、ミトコンドリア構造の解析は、NDとその分子基盤を完全に理解するための鍵となります。
透過型電子顕微鏡、電子線トモグラフィー、クライオ電子線トモグラフィー(クライオET)、X線トモグラフィー、特にクライオ軟X線トモグラフィーなどの一般的なクリステの観察方法は、重要な発見を明らかにし、さまざまなサンプルタイプで作業しています56,57,58,59,60.近年、オルガネラの超微細構造の観察が進んでいますが、これらの方法にはサンプルの固定が必要であるため、クリステのリアルタイムダイナミクスを直接捉えることができないという注意点があります。超解像蛍光顕微鏡は、特に構造化照明顕微鏡(SIM)、確率光学再構成顕微鏡(STORM)、光活性化局在顕微鏡(PALM)、拡大顕微鏡(ExM)、誘導放出枯渇(STED)顕微鏡の形態で、従来の光学顕微鏡法を制約する回折限界以下の分解能を必要とする構造を観察するための一般的な方法となっています。ExMを別の超解像技術と組み合わせて使用すると、結果は印象的であるが、試料を固定し、ゲル61で染色しなければならない。比較すると、SIM、PALM/STORM、およびSTEDはすべてライブサンプルで成功裏に使用されており、IMMを一般的に染色する新しい有望な色素は、ミトコンドリアクリステダイナミクスのライブイメージングに斬新で簡単なアプローチを提供します62、63、64、65、66。STEDイメージング用のライブ色素の最近の進歩により、色素の輝度と光安定性が向上しており、これらの色素は以前の色素よりも高い特異性でIMMを標的としています。これらの開発により、超解像イメージングによる長期のタイムラプスおよびzスタック実験の収集が可能になり、ミトコンドリアの超微細構造とダイナミクスのより良い生細胞解析への扉が開かれます。
本明細書では、STED63を用いてPKmito Orange(PKMO)色素で染色した未分化および分化SH-SY5Y細胞の生細胞イメージングのためのプロトコルが提供される。SH-SY5Y細胞株は、転移性神経芽腫67,68,69,70の骨髄生検から生成された親細胞株SK-N-SHから3回サブクローニングされた誘導体です。この細胞株は、特にミトコンドリアの機能障害が深く関与するAD、HD、PDなどの疾患において、ND研究において一般的に使用されるin vitroモデルである10,43,71,72,73。培地を操作することでSH-SY5Y細胞をニューロン様表現型の細胞に分化させる能力は、初代神経細胞に頼らずに神経科学研究に適したモデルであることが証明されています10,74。このプロトコルでは、レチノイン酸(RA)を細胞培養培地に添加して、SH-SY5Y細胞の分化を誘導しました。関節リウマチはビタミンA誘導体であり、細胞周期を調節し、ニューロンの分化を調節する転写因子の発現を促進することが示されている75。また、ラット海馬から単離されたニューロンの培養および生細胞イメージングのためのプロトコルも提供されています。海馬はミトコンドリア変性の影響を受けることが示されており、皮質とともに老化とND76,77,78,79,80に重要な役割を果たしています。
プロトコル
1. SH-SY5Y細胞の増殖と分化
- 細胞増殖および維持のための培地の調製
- 完全な高グルコースダルベッコ改変イーグル培地(DMEM、4.5 g/L D-グルコース、4 mM L-グルタミン、110 mg/Lピルビン酸ナトリウム)を調製し、最終的な1%(v/v)抗生物質-抗真菌薬(10,000単位/mLペニシリン、10,000 μg/mLストレプトマイシン、および25 μg/mLアムホテリシンB)およびさまざまな量のウシ胎児血清(FBS)( 材料表を参照)を添加します。分化培地中のFBS量は、最終的な10%、5%、または2%(v/v)のFBSの間で変化します。
- セルのメンテナンス
- 細胞を10%(v/v)FBSを添加したDMEMで維持し、37°C、5%CO2で静置し、5%(v/v)FBSを含むDMEMで播種して分化させます。凍結細胞ストックを、10%(v/v)ジメチルスルホキシド(DMSO)とともに1-2 x 107 細胞/mLでFBSに保存しました。
- レチノイン酸(RA)の調製
- 7.51 mg のオールトランス-RA(材料表を参照)を新たに調製した 95% エタノール 5 mL に溶解し、5 mM ストック溶液を得ます。メーカーのプロトコル81 の製品情報シートから得られた 350 nm の吸光度 (ɛ = 44,300 M-1 cm-1) で、エタノール中で 5 μM の原液を希釈して濃度を確認します。5 mM ストックを 4 °C で光から保護して最大 6 週間保管します。
- カバーガラスコーティングのためのポリ-D-リジンの調製
注:ベンダーサイト82のDocuments & Downloadsセクションにあるpoly-D-lysine(PDL)製品プロトコルは、さまざまな培養容器をコーティングするための情報を提供します。- このプロトコルには、無菌#1.5ホウケイ酸カバーガラス底部を備えたウェルあたり4cm2 の面積を持つ2ウェルチャンバー容器に基づくボリュームが含まれています( 材料表を参照)。PDLの原液をダルベッコPBS(DPBS、カルシウム、マグネシウムなし)で2倍に希釈して50 μg/mLにします。
注:#1.5または#1.5Hカバーガラスはどちらも許容可能な厚さであり、画質に不可欠です。他の厚さは球面収差を誘発するため、避ける必要があります。
- このプロトコルには、無菌#1.5ホウケイ酸カバーガラス底部を備えたウェルあたり4cm2 の面積を持つ2ウェルチャンバー容器に基づくボリュームが含まれています( 材料表を参照)。PDLの原液をダルベッコPBS(DPBS、カルシウム、マグネシウムなし)で2倍に希釈して50 μg/mLにします。
- PDLによるカバーガラスコーティング
注意: カバーガラスは、バイオセーフティキャビネット内で紫外線(UV)に10〜15分間さらして、さらに滅菌することができます。- 1.2 mL の 50 μg/mL PDL 溶液を細胞培養キャビネット内の滅菌チャンバーカバーガラスの各ウェルに塗布し、室温で 1 時間インキュベートします。PDL溶液を除去し、3.6 mLの蒸留水で3回すすぎます。最終洗浄が完了したら、コーティングチャンバーを空気にさらして2時間乾燥させてから、すすぎ、すぐに使用するか、4°Cの密閉容器で最大2週間保管します。
注:過剰なPDLは細胞に有毒である可能性があるため、カバーガラスを完全にすすいでください。
- 1.2 mL の 50 μg/mL PDL 溶液を細胞培養キャビネット内の滅菌チャンバーカバーガラスの各ウェルに塗布し、室温で 1 時間インキュベートします。PDL溶液を除去し、3.6 mLの蒸留水で3回すすぎます。最終洗浄が完了したら、コーティングチャンバーを空気にさらして2時間乾燥させてから、すすぎ、すぐに使用するか、4°Cの密閉容器で最大2週間保管します。
- RAによるSH-SY5Y細胞の分化
注:継代15より上のセルは使用しないでください。細胞は80%〜90%のコンフルエントで継代されます。区別手順は異なりますが、同様の手順に従います。神経芽細胞腫から成熟ニューロンへの追加の分化は、脳由来神経栄養因子(BDNF)68,83,84,85によるさらなる治療で得られますが、このプロトコルでは行われませんでした。
オプション:カバーガラスに播種する前に、少なくとも24時間細胞を確立します。凍結ストックから細胞を調製するには、1 mLの凍結バイアルを急速に解凍し、10%FBSを添加した9 mLの予熱培地に添加し、350 x g で10分間(室温)スピンダウンし、上清を捨ててDMSOを除去します。細胞ペレットを予熱した培地5 mLに再懸濁し、細胞をT-25フラスコに播種します。細胞が80%〜90%のコンフルエントに達したら、細胞をカウントして播種し、該当する場合は分化させます。- 0日目:細胞を播種します。
- 凍結ストックまたは作業用フラスコからチャンバー付きカバーグラスに細胞を播種します。播種密度は1.5×104 セル/cm2。
注:培養面積が 4 cm 2 の標準的な2 ウェルチャンバーカバーグラスの 1 つのウェルには、6.0 x 104 セルが必要です。未分化のままの細胞には、10%(v/v)FBSを添加したDMEMを播種し、分化させる細胞には、5%(v/v)FBSを添加したDMEMを播種する必要があります。
- 凍結ストックまたは作業用フラスコからチャンバー付きカバーグラスに細胞を播種します。播種密度は1.5×104 セル/cm2。
- 1日目:関節リウマチ分化治療開始。
- 5%(v/v)FBS、1%(v/v)抗生物質-抗真菌薬、および最終濃度10 μMのRAまたは同じ添加量のエタノールを添加したDMEMを調製し、この鑑別手順のビヒクルコントロールとして使用します。播種に使用したチャンバー付きカバーガラスの培地を取り除き、1x PBSですすぎ、新しいDMEMをウェルに加えます。
- 3日目:培地を新しいRAまたはエタノール含有培地と交換します。
- 1日目から培地を除去し、2%(v/v)FBS、1%(v/v)抗生物質-抗真菌薬、および10 μM RAまたは同添加量の95%エタノールを添加した新しい培地と交換して、この分化手順のビヒクルコントロールとして使用します。播種に使用したチャンバー付きカバーガラスの培地を取り除き、1x PBSですすぎ、ウェルに新しい培地を追加します。
- 6日目:細胞のイメージングを行います。
注:細胞分化時間はプロトコルによって異なるが、RAへの6日間の曝露は、SH-SY5Y細胞にニューロン様表現型を誘導するのに十分である86。- セクション3と4で詳細を記載したライブイメージングを実行します(図2)。
- 0日目:細胞を播種します。
2. 初代ラット海馬ニューロン培養
- ラット海馬ニューロン単離のための材料調製。
- 新たに添加したDMEMを調製します。
- 10%(v/v)熱不活化FBS、1%(v/v)ピルビン酸ナトリウム溶液、および1%(v/v)ペニシリン-ストレプトマイシン(10,000 U/mL)を添加したDMEM(高グルコース、ピルビン酸ナトリウムなし)の混合物をろ過滅菌します。4°Cで最大2週間保存してください。
- 新しい補充されたニューロン増殖培地を調製します。
- 2%(v/v)のB27サプリメント、0.25%(v/v)のグルタミンサプリメント、および1%(v/v)のペニシリン-ストレプトマイシンを添加したニューロン増殖培地の混合物をろ過滅菌します( 材料表を参照)。4°Cで最大2週間保存してください。
- 新たに添加したDMEMを調製します。
- 初代海馬ニューロン培養を準備します。
- 以前に発表された研究87 に従って、および解剖されたE18ラット海馬が得られる製造元のサイトの製品プロトコル88 ( 材料表を参照)に従って、一次海馬ニューロン培養を準備します。このプロトコルは<2%のastrocytesが付いている大抵ニューロンの人口で起因する。
注:この組織が出荷される休止状態培地は、このプロトコルの将来のステップに使用されます。廃棄しないでください。 - 組織解離のための材料と培地を準備します。
- パスツールピペットを炎で焼いて開口部の直径を小さくし、ホイルで保管して、使用まで汚染を防ぎます。調製したDMEM、1X Hank's Buffered Salt Solution(HBSS)、およびニューロン増殖培地を37°Cに予熱します。 15 mLのコニカルチューブに滅菌ピンセットでDNAaseのフレークを2つ加えます。
- 組織解離を行います。
- 解剖したE18ラット海馬が保管されている冬眠培地をできるだけ多く除去してから、DNAaseを含む15 mLのコニカルチューブに組織を入れ、37°Cで短時間インキュベートします。 900 μL の 1X HBSS を加え、続いて 100 μL の 0.5% トリプシンを加えます。組織を37°Cで15分間インキュベートします。
注:PDLコーティングプレートは、このインキュベーション時間中に使用されるまで、保管から取り出してインキュベーターに入れることができます。
- 解剖したE18ラット海馬が保管されている冬眠培地をできるだけ多く除去してから、DNAaseを含む15 mLのコニカルチューブに組織を入れ、37°Cで短時間インキュベートします。 900 μL の 1X HBSS を加え、続いて 100 μL の 0.5% トリプシンを加えます。組織を37°Cで15分間インキュベートします。
- 組織のホモジナイズと細胞カウントを行います。
- トリプシンとインキュベーションした後、培地を除去し、前のステップで予熱した冬眠培地DNAase 1 mLを組織に加え、パスツールピペットでホモジナイズします。メディアは不透明に見えますが、均質化が進むにつれて徐々に透明になります。
- 解離したニューロンを予熱した 4 mL の DMEM で新しいチューブに追加し、セルカウンターを使用して細胞をカウントします。
- 細胞プレーティングを行い、初代細胞を増殖させます。
- DMEMで約1.65 x 104 cells/cm2 の密度で細胞を播種します。2ウェルチャンバーカバーグラス(4 cm 2)の場合、2 mL DMEMでウェルあたり65,000〜70,000個の細胞を播種します。細胞を37°C、5%CO2 で2時間インキュベートしてから、接着性を確認します。細胞が接着し始めたら、1 mLの培地を取り除き、同量の休止状態培地と交換し、穏やかに攪拌して混合します。培地が混合されたら、このプロセスを繰り返し、存在する培地の半分を取り除き、同じ量のニューロン増殖培地と交換してから、穏やかに混合します。
注:プレーティングの日は in vitro (DIV) 0 と見なされ、細胞は DIV 7 でイメージングする準備ができています(図 2)。
- DMEMで約1.65 x 104 cells/cm2 の密度で細胞を播種します。2ウェルチャンバーカバーグラス(4 cm 2)の場合、2 mL DMEMでウェルあたり65,000〜70,000個の細胞を播種します。細胞を37°C、5%CO2 で2時間インキュベートしてから、接着性を確認します。細胞が接着し始めたら、1 mLの培地を取り除き、同量の休止状態培地と交換し、穏やかに攪拌して混合します。培地が混合されたら、このプロセスを繰り返し、存在する培地の半分を取り除き、同じ量のニューロン増殖培地と交換してから、穏やかに混合します。
- 以前に発表された研究87 に従って、および解剖されたE18ラット海馬が得られる製造元のサイトの製品プロトコル88 ( 材料表を参照)に従って、一次海馬ニューロン培養を準備します。このプロトコルは<2%のastrocytesが付いている大抵ニューロンの人口で起因する。
3. 生細胞イメージング用細胞の調製
注:細胞の種類と起源(すなわち、培養細胞と初代細胞)は、染色要件が異なる場合があります。詳細については、公開されたレポートを参照してください62,63.
- PKmitoオレンジの調製
注:一般的にIMMを染色する他の色素は64,65,66報告されており、市販されている。PKMOは、このプロトコルで使用される唯一のものです。- 粉末PKMO( 材料表を参照)を、製造元の指示に従ってDMSOに再懸濁する89。細胞から培地を吸引し、予熱したフェノールレッド遊離培地で洗浄します。分化状態に応じて2%(v/v)のFBSまたは10%(v/v)、最終濃度20 mMまでのHEPES、および1%(v/v)の抗生物質-抗真菌剤を添加した、予熱したフェノールレッドフリーDMEMにPKMOのストックを調製してから、メーカーの指示に従って細胞を染色します。PKMOを含まないこの製剤は、生細胞イメージング培地です。
- PKMOによる細胞染色
- 細胞を色素とともに37°C、5%CO2 で30分間インキュベートします。生細胞イメージング培地で細胞を3回洗浄し、最終洗浄では37°C、5%CO2で30分間インキュベートします。
- あらかじめ温めた新鮮な生細胞イメージング培地を添加します。これで、細胞をイメージングする準備が整いました。
注:急性治療(薬物やストレッサーなど)は、使用する場合、ライブイメージングの前に追加されます。「考察」セクションおよび 補足図1を参照してください。
4. STED顕微鏡による生細胞のイメージング
注:このプロトコルは、倒立顕微鏡を中心に構築されたSTEDシステムを使用し、 材料表で指定されているシステムを使用します。このシステムには、パルス励起レーザー(公称出力~300μWの561nmレーザー)とパルス775nmのSTED空乏レーザー(公称出力1.2W)、連続調整可能なガルバノスキャナー、および615/20nmフィルターベースのアバランシェフォトダイオード検出器(APD)が装備されています。ここでは、STED用の100倍/1.40の油浸レンズを使用しています。画像取得にはライトボックスソフトウェアを使用します。提供されるすべての詳細は、このソフトウェアとシステムのセットアップに直接関連しています。
- イメージングの一般的なガイドラインと手順
- 細胞の生存率を維持するためにステージトップインキュベーターまたは環境チャンバーを使用しますが、短期間の室温実験も許容されます。これらの手順は、上記の STED セットアップに固有です。
- イメージング用のレーザーセットとフィルターセットを選択します。
- オレンジ色の色素のパラメータを使用するには、染色に使用する染料を [Dye List] から選択するか、使用する色素に最も近いスペクトル特性を持つ色素を選択します。これらをダブルクリックするか、サンプルリストにドラッグしてアクティブにします。サンプルリストには「ここに染料をドラッグしてください」と表示されます。
- 画像化する領域を選択します。
- 概要で、四角形の ROI ボタン を選択し、クリックしてドラッグして領域を形作ることで、関心のあるミトコンドリアの周囲に関心領域 (ROI) を作成します。ROI のサイズ変更と回転は、コーナーの上にマウスを置いたときに表示される ROI のコーナー または 曲線エッジ を使用して行うことができます。
メモ: 推奨されるイメージングパラメータの概要を 表 1 に示します。これらのパラメータは、このSTEDセットアップおよび色素の組み合わせについて以前に報告されたものを用いて経験的に調整された63。
- 概要で、四角形の ROI ボタン を選択し、クリックしてドラッグして領域を形作ることで、関心のあるミトコンドリアの周囲に関心領域 (ROI) を作成します。ROI のサイズ変更と回転は、コーナーの上にマウスを置いたときに表示される ROI のコーナー または 曲線エッジ を使用して行うことができます。
- ゲートを設定します。
- 「一般」(General) メニューの横で、「ゲート」(Gating) メニューを選択するか、クリックしたままにしてメニューをビューに追加します。STED検出器のゲーティングは、ここに示すように、1-1.05〜7.85 nsに調整することをお勧めします。ゲーティング時間はさまざまで、1-1.05 nsから7-7.05 nsまで短くなります。
- サンプルに応じて強度を適切に調整してください。
注:一般的に、STEDに使用される励起電力は共焦点に使用される出力の2〜3倍であるため、共焦点に使用される5%の励起レーザー出力を必要とするサンプルは、STED取得中に10%〜15%の励起レーザー出力を使用できます。- STEDの励起レーザーを15%-20%に設定し、STED空乏レーザーを20%-25%に設定し、10ラインの蓄積を行います。20〜25nmのピクセルサイズで4μsのピクセル滞留時間を使用します。ピンホールは、より密集したミトコンドリアの光学的切片を改善するために、培養細胞では1.0 AU、初代ラット海馬細胞では0.7 AUに保たれました。
注:共焦点画像とSTED画像の両方を取得して並べて比較することもできます(図3A、B、図4A)、またはSTEDのみを取得することもできます。
- STEDの励起レーザーを15%-20%に設定し、STED空乏レーザーを20%-25%に設定し、10ラインの蓄積を行います。20〜25nmのピクセルサイズで4μsのピクセル滞留時間を使用します。ピンホールは、より密集したミトコンドリアの光学的切片を改善するために、培養細胞では1.0 AU、初代ラット海馬細胞では0.7 AUに保たれました。
- 時系列/z 系列の追加情報
- 時系列を選択します。
- [時間] ドロップダウン メニューを選択します。タイムラプスに必要な反復回数(ここでは5秒を使用)と時間間隔(ここでは25秒または30秒を使用)を定義します(図3C、D、図4B)。
注:間隔が取得時間よりも短い場合、反復は遅延なく続行されます。タイムラプスを実行するときは、潜在的なドリフトを避けるために、完璧なフォーカスユニットまたは同様のフォーカストラッキングを使用することを強くお勧めします。
- [時間] ドロップダウン メニューを選択します。タイムラプスに必要な反復回数(ここでは5秒を使用)と時間間隔(ここでは25秒または30秒を使用)を定義します(図3C、D、図4B)。
- 音量範囲を設定します。
- 必要に応じて Z ボリューム範囲を設定するには、 Volume オプションを有効にし、範囲の両端を調整します。2Dイメージ投射のためのこのプロトコルで使用されるステップサイズは150-200 nmだった。生のSTEDのデコンボリューションに必要なナイキストサンプリングに関する推奨ステップサイズは、オンラインツール90で計算することができる。
注:STEDの枯渇レーザー出力と画像化された平面の数により、色素の光退色と細胞への光曝露が有害なレベルに増加する可能性があります。取得後に光毒性および光損傷の兆候がないか確認します。
- 必要に応じて Z ボリューム範囲を設定するには、 Volume オプションを有効にし、範囲の両端を調整します。2Dイメージ投射のためのこのプロトコルで使用されるステップサイズは150-200 nmだった。生のSTEDのデコンボリューションに必要なナイキストサンプリングに関する推奨ステップサイズは、オンラインツール90で計算することができる。
- 時系列を選択します。
5. ミトコンドリア超微細構造の加工・解析ツール
注:画像処理(デコンボリューション)はオプションですが、通常、公開用のSTED画像を作成および分析するときに使用されます。以下で説明するように、個々のクリステの最適なセグメンテーションには、コントラストを改善し、ノイズを低減するためのデコンボリューションを強くお勧めします(図2)。
- STED画像デコンボリューション
注:このプロトコルでデコンボリューションに使用されるソフトウェアは、 材料表に記載されています。- 画像の微視的パラメータを設定します。
注:顕微鏡のメタデータが画像の 顕微鏡パラメータに正しく入力されていることを確認してください。これには、封入媒体の屈折率が含まれます。浸漬媒体;ピクセルサイズ;励起波長、発光波長、および枯渇波長。およびその他の関連情報。これらのパラメーターを持つテンプレートは、再利用のために保存できます。 - ソフトウェアアルゴリズムで生のSTED画像をデコンボリューションします。
- デコンボリューションソフトウェアで自動デコンボリューションアルゴリズムにアクセスすることで、ハンズオフのデコンボリューション画像処理が可能になります。 [Express ] ボタンを選択し、デコンボリューションの種類を Fast、Standard、Aggressive、または Conservative に設定して、さまざまな程度のデコンボリューションパワーを設定します。Express DeconvolutionをAggressive設定で使用した代表的な画像を示します(図3、図 4、 図5)。
- デコンボリューションソフトウェアからICS2形式で画像を保存します。
- 手動デコンボリューションの場合は、次の手順を実行します。
- 簡単に言うと、手動デコンボリューションを実行する場合は、一貫性を保つためにデコンボリューションウィザードのテンプレートを保存し、ウィザードの開始時にテンプレートをロードするオプションを用意します。測定点像分布関数(PSF)情報は、アクイジションの設定とパラメータで生成された場合に使用します。
- 必要に応じて、デコンボリューションソフトウェアで画像を自動安定化する前に、生のSTED画像を切り抜きます。デコンボリューションソフトウェアパッケージへのアドオンにより、熱ドリフトや色収差などのイメージングアーチファクトの可能性を特定の補正することができます。
- 次に、対数ヒストグラムを生成して、手動または自動でバックグラウンド減算を実行します。従来の最尤推定 (CMLE) デコンボリューション アルゴリズムを選択します。
注: デコンボリューションの場合、調整する主な値は、S/N 比のしきい値、反復回数、および品質しきい値です。これらの値は調整でき、デコンボリューションをプレビューして最適な設定を決定できます。
- 画像の微視的パラメータを設定します。
- セグメンテーションと粒子解析
注: このプロトコルは、オープンソースソフトウェアである FIJI (Is Just ImageJ) を使用します ( 材料表)を使用して、セグメンテーションと分析を行います。CellProfiler、Icy、Ilastik、QuPathなど、他の同等のソフトウェアもこれらの目的に利用できます。- セグメンテーション用の画像を準備します。
- デコンボリューションソフトウェアから .obf raw STED イメージまたは .ics2 ファイルを開くには、[ファイル] → [開く] に移動するか、ファイルをクリックして ImageJ ツールバーにドラッグします。ここから、セグメンテーションの前に画像をセグメント化しやすいようにする処理を行うことができます。
- 変更の一貫性を保つには、「プラグイン → マクロ (Plugins Macros )」→「プラグイン (Plugins )」→「新規 → マクロ (New Macro) からキーコマンドを記録し、コピーして新しいマクロにペーストします。マクロを実行する前に、処理するイメージを必ず選択してください。
注:サイズと形状の定量化で一般的に許容される変更には、トリミング、Zスタックの投影、およびスムージングを無効にした背景の減算が含まれます。変更は、データセット内の画像間で一貫して実行し、報告する必要があります。
- トレーニング可能なWekaセグメンテーション設定の調整
注:ミトコンドリアの半自動セグメンテーションツールおよびダウンストリーム分析の使用に関するステップバイステップの説明を含む追加の詳細が公開されている91。- [Plugins → Segmentation → Trainable Weka Segmentation] にある Trainable Weka Segmentation (TWS)92 プラグインで、デコンボリューションされた STED 画像を開きます。セグメンテーション設定で、ガウスぼかし、膜投影、ソーベルフィルター機能を選択します。膜厚の既定値は 1 で、膜パッチ サイズの既定値は 19 です。
- クラス1または2のいずれかを「Cristae」としてラベル付けし、もう一方を「Background」としてラベル付けします(図2)。モデルは、[ 分類子の保存 ] ボタンで保存することもできます。[ 分類子の読み込み ] を選択して、これらの設定を他の画像に再利用します。
- TWS クラス・トレースを実行します。
- 線ツールまたはその他の図形を使用して、クリステまたは背景の一部を強調します。少なくともいくつかの背景の選択には、クリステの間にスペースを含める必要があります。いずれかのクラスに割り当てる構造の上に線を引き、右側の [追加 ] ボタンを選択して cristae または background を選択します。トレースをダブルクリックすると、そのラベルから構造が削除されます。
- TWS 分類トレーニングを実行します。
- 左側の [分類子のトレーニング] ボタンを選択して、プラグインに提供された情報に基づいてマップを生成します。セグメント化されたクラスのオーバーレイは、[オーバーレイの切り替え]ボタンでオンとオフを切り替えることができ、オーバーレイの不透明度は[設定]で調整できます。分類器は、追加のラベルで再トレーニングできます。問題がなければ、 [Get Probability](確率の取得) ボタンを選択します。
- 粒子を測定します。
- クリステ確率マップを使用して、イメージのしきい値を設定してマスクを生成し、[ 解析] →[ パーティクルの解析]に移動します。一般的には、デフォルトの閾値タイプを使用し、範囲を調整して、クリステ全体が考慮されるようにすることができます。粒子の解析によって得られる測定値は、測定値 の解析 →設定(Analyze Set Measurements)で調整できます。
注:クリステの面積、周囲長、真円度、アスペクト比などのサイズと形状のパラメータの例は、選択した測定値に基づいて測定および表示されます(図2、 図5A、 補足表1)。 - オプション: デコンボリューションされたイメージと同じ次元の生の STED イメージを選択し、マネージャーから ROI を適用してから、ROI マネージャーで [測定 ] を選択して強度値を取得します。
- クリステ確率マップを使用して、イメージのしきい値を設定してマスクを生成し、[ 解析] →[ パーティクルの解析]に移動します。一般的には、デフォルトの閾値タイプを使用し、範囲を調整して、クリステ全体が考慮されるようにすることができます。粒子の解析によって得られる測定値は、測定値 の解析 →設定(Analyze Set Measurements)で調整できます。
- ラインプロットを取得します。
- ラインプロットは、デコンボリューションされたSTED画像から生成されました。多点線を描き、線の太さを数ピクセル幅に調整してノイズを平均化し、ミトコンドリアに合うように線をスプラインします(図2、 図5B)。生成された折れ線グラフは、ピークtoピーク距離を測定し、特定の範囲におけるクリステの周期性と分布を報告するために使用されます。
注:関連して、クリステ密度は、ミトコンドリアの外側部分を測定することによって決定される、特定の領域内の独立したクリステの数として報告できます。ミトコンドリア領域は、デコンボリューションまたは生のSTED画像にフィルタを適用してマスクを生成することによって決定することができる。面積を測定する前に、マスクがミトコンドリアの輪郭に正確にフィットしていることを確認してください。
- ラインプロットは、デコンボリューションされたSTED画像から生成されました。多点線を描き、線の太さを数ピクセル幅に調整してノイズを平均化し、ミトコンドリアに合うように線をスプラインします(図2、 図5B)。生成された折れ線グラフは、ピークtoピーク距離を測定し、特定の範囲におけるクリステの周期性と分布を報告するために使用されます。
- セグメンテーション用の画像を準備します。
結果
このプロトコルはミトコンドリアのcristaeの生きているセルSTEDイメージ投射そしてそれに続く分析に焦点を合わせて培養された、一次セルのためのセル成長の状態を記述する。未分化のSH-SY5Y細胞(図3A)およびRA分化SH-SY5Y(図3B)細胞のミトコンドリアのImageJによる投影は、従来の共焦点およびSTEDでzスタックとして収集し、生のSTED画像をデコンボリューションすることができます。タイムラプスイメージングも実行でき、その後デコンボリューションされます(図3C、D)。初代ラット海馬ニューロン(表1)のわずかに異なるイメージングパラメータを使用して、共焦点画像と生のSTED画像をzスタックとして取得し、生のSTED画像をデコンボリューションすることができます(図4A)。初代ニューロンからのミトコンドリアのタイムラプスイメージングも可能です(図4B)。一般に、タイムラプス画像はミトコンドリアの動的イベントを表示できる必要があります。
セグメンテーションに使用したサンプルからの生の STED とデコンボリューションされた STED の Z スタック投影が一貫しているように見える場合、定量的測定が実行されます。TWSプラグインは、デコンボリューションされたSTED画像を使用してセグメント化して確率マスクを作成し、それを使用してクリステのバイナリマスクを作成し、サイズと形状のパラメータを取得します(図5A)。このマスクの領域は ROI マネージャーに保存され、必要に応じて生の STED イメージに適用して相対強度の差を測定できます。デコンボリューションされたSTED投影法は、特定の領域におけるクリステの周期性と密度を決定するためにも使用できます(図5B)。
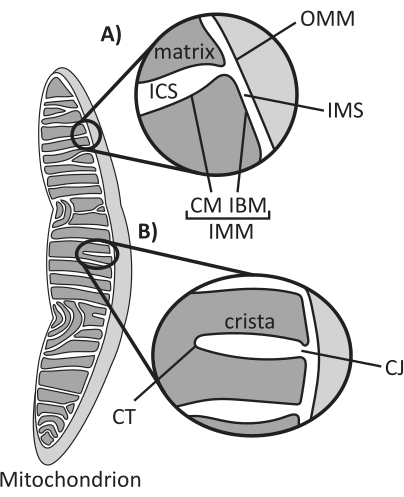
図1:ミトコンドリアの形態。 ミトコンドリアには、異なるサブコンパートメント(A)を定義する2つの膜システムがあります。クリステは、定義された特徴(B)を持つ内膜の折り目です。略語:OMM、外側ミトコンドリア膜;ICS、胴腔内空間;IMS、膜間空間;CM、クリステ膜;IBM、内側境界膜;IMM、内ミトコンドリア膜;CT、クリステチップ;CJ、クリステジャンクション。 この図の拡大版をご覧になるには、ここをクリックしてください。
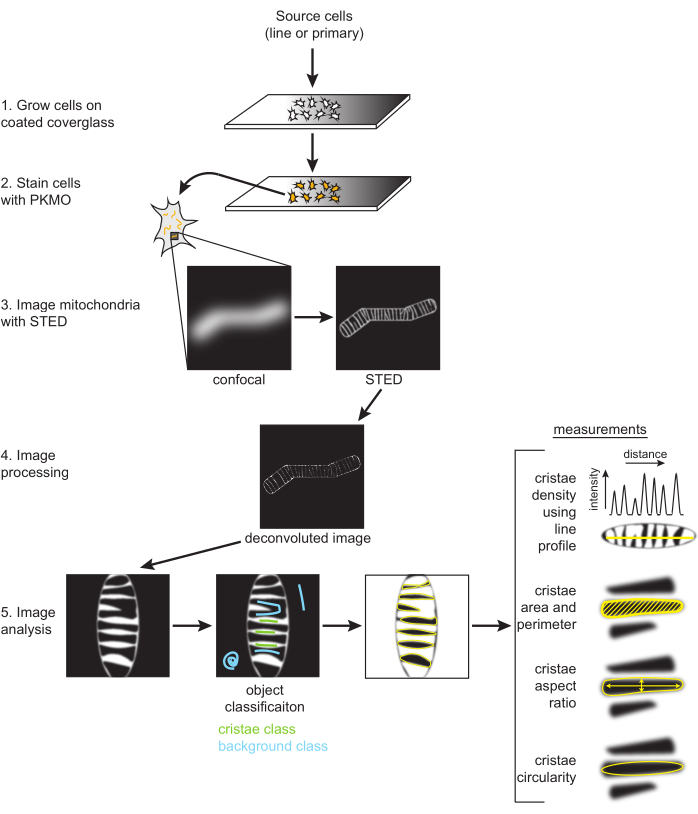
図2:ワークフローの概略図。SH-SY5Y細胞または初代ラット海馬ニューロンは、PDLコーティングされたカバーガラス上で増殖します。SH-SY5Y細胞は、未分化のまま、またはRA分化を6日間にわたって並行して増殖させます。初代ラット海馬ニューロンは、海馬切片から7日間単離された後、PDLコーティングされたカバーガラス上で増殖した。イメージングの準備が整ったら、細胞をPKMOで染色し、STEDでイメージングしました。次に、生のSTED画像をデコンボリューションし、デコンボリューションした画像をフィジーで処理して、クリステ密度、面積、周囲長、真円度、アスペクト比などのサイズと形状の測定値を取得します。この図の拡大版をご覧になるには、ここをクリックしてください。
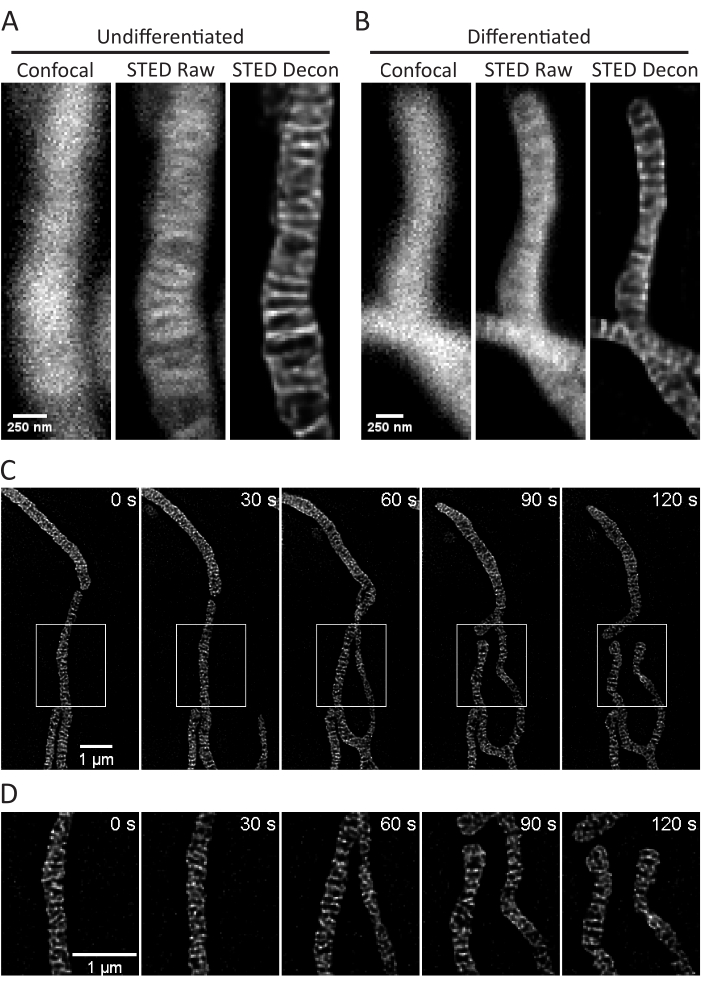
図3:SH-SY5Y細胞におけるミトコンドリアのイメージング。 PKMO染色を施した未分化(A)およびRA分化(B)SH-SY5Y細胞のミトコンドリアの代表的な共焦点(左)、生のSTED(中央)、およびホイヘンスデコンボリューションSTED画像(右)を示す。30秒間隔でRA分化したSH-SY5Y細胞を5回繰り返したタイムラプス(C)と、選択した領域(白いボックス)を補間せずに拡大した領域(D)を示します。スケールバー:A、 B、250 nm; C、D、1 μm。 この図の拡大版をご覧になるには、ここをクリックしてください。
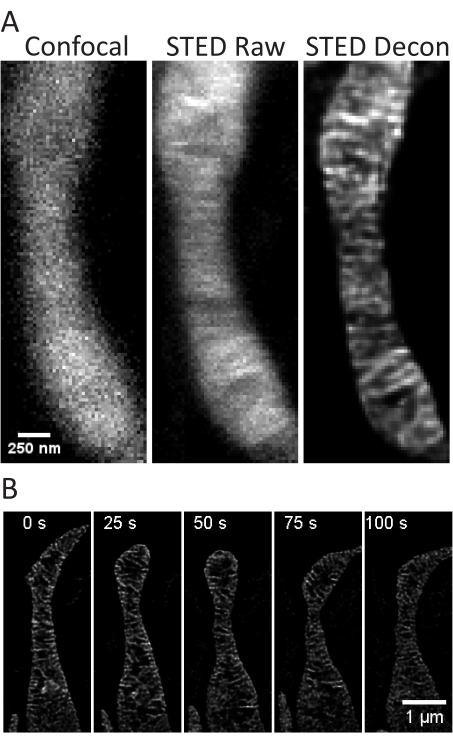
図4:初代ラット海馬ニューロンにおけるミトコンドリアのイメージング。 代表的な共焦点(左)、生のSTED(中央)、ホイヘンスデコンボリューションSTED(右)の画像は、初代ラット海馬ニューロンからのミトコンドリアのzスタック投影を示しています(A)。これらのニューロンのミトコンドリアを25秒間隔で5回繰り返したタイムラプスが示されています(B)。スケールバー: A、 250 nm; B、 1μm。 この図の拡大版をご覧になるには、ここをクリックしてください。
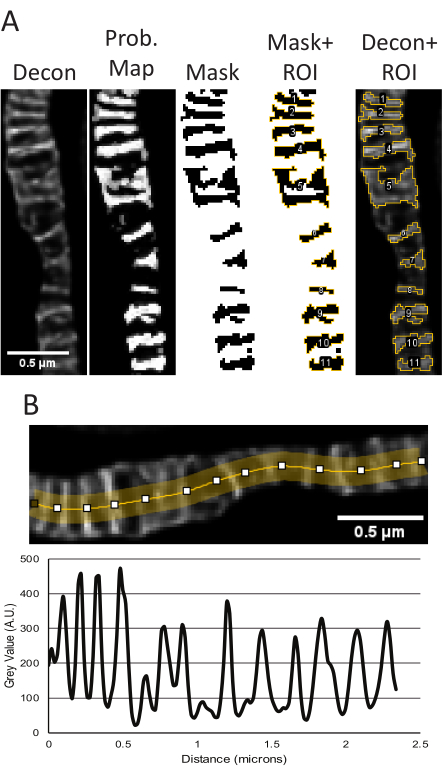
図5:ImageJでのデコンボリューションされたSTED画像の処理。 Trainable Weka Segmentationプラグインを使ってクリステのサイズと形状を測定した代表的な使い方を示す(A)。左から右に、デコンボリューションされたSTED画像、TWSプラグインからのセグメンテーションに基づく確率マップ、確率マップを入力として使用したフィジーでのしきい値処理からのマスク、ROIのアウトラインを持つマスク、および元のデコンボリューションされたSTED画像にオーバーレイされたROIが示されています。これらのオブジェクトに対応する結果の面積、周囲長、真円度、およびアスペクト比の測定値は、 補足表1に記載されています。クリステ密度の読み出しとして、デコンボリューションされたSTED画像を使用してピークtoピーク距離を測定した折れ線グラフを示します(B)。スケールバー:0.5 μm。 この図の拡大版をご覧になるには、ここをクリックしてください。
| ピクセルサイズ(nm) | 滞留時間(μs) | 回線接続 | STED取得時の561 nm励起(%) | 775 nm STEDの空乏電力(%) | ステップサイズ(nm) | ピンホール(AU) | タイムラプス間隔(秒) | タイムラプスの反復 | |
| 非異種SH-SY5Y | 20 | 4 | 10 | 15 | 20 | 200 | 1.0 | 30 | 5 |
| RA-ディフェール-ntiated SH-SY5Y | 20-25 | 4 | 10-12 | 15 | 20-22 | 150-200 | 1.0 | 30 | 5 |
| 一次ニューロン | 20-25 | 4 | 10 | 10 | 25 | 200 | 0.7 | 30 | 5 |
| 注:ピクセルサイズは、イメージング要件とイメージのデコンボリューションの意図によって異なる場合があります。デコンボリューションには適切なサンプリングが必要です。デコンボリューションなしの生のSTED画像のピクセルサイズは、最大30nmまで可能です。 | |||||||||
表1:STED取得パラメータの概要。 細胞種別、未分化SH-SY5Y、RA分化SH-SY5Y、初代ラット海馬ニューロンの2D STEDイメージングに用いた設定値を表示します。すべてのタイムラプスについて、ROIサイズに基づいてさまざまな間隔で5回の反復が行われました。
補足図1:アミロイドβ(Aβ)を添加したSH-SY5Y細胞のイメージング。 PKMO染色を有するRA分化SH-SY5Y細胞(上)およびAβ-HiLyte647(下)の代表的な共焦点画像(左)、生STED(中央)、およびデコンボリューションSTED(右)画像(A)を示します。生のPKMO STED(緑)と生のAβ STED(マゼンタ)(B)またはデコンボリューションされたPKMO STED(緑)とデコンボリューションされたAβ STED(マゼンタ)(C)のマージされたzスタック投影を示します。スケールバー:0.5 μm。 このファイルをダウンロードするには、ここをクリックしてください。
補足表1:セグメント化されたクリステのサイズと形状の測定。 セグメント化されたミトコンドリアから図5Aに概説されたオブジェクトに対応する、面積(μm2)、周囲長(μm)、真円度、およびアスペクト比のサイズおよび形状の測定値が示されています。このファイルをダウンロードするには、ここをクリックしてください。
補足表2:アミロイドβサンプルの取得パラメータの概要。 未分化およびRA分化SH-SY5Y細胞におけるPKMOおよびAβ-HiLyte647の2D STEDイメージングに用いた設定を表示します。Aβ-HiLyte647の共焦点は、分離する特定の構造がないため、単独で使用できます。Aβ-HiLyte647のSTED画像は、粒子径が小さい場合のものです。 このファイルをダウンロードするには、ここをクリックしてください。
補足ファイル1:アミロイドβ治療プロトコル。このファイルをダウンロードするには、ここをクリックしてください。
ディスカッション
このプロトコルは生きているセルSTEDイメージ投射のための新しいIMM目標とするPKMOの染料が付いている人間のneuroblastomaのセルラインSH-SY5Yおよび第一次ラットの海馬ニューロンの使用を示す。PKMOの新規性により、この色素をライブSTEDイメージングに使用した論文は、現在ほとんど発表されていません。これらの細胞タイプをSTEDイメージングに使用すると、特に神経細胞のミトコンドリアが狭いため、課題が生じます。このプロトコルの1つの限定は細胞に有毒である場合もあるので、使用されるPKMOの染料である。細胞や細胞株が異なれば、色素に対する反応も異なるため、細胞を傷つけることなく強いシグナルが得られるように結果を最適化するために、色素濃度とインキュベーション時間を調整する必要がある場合があります。推奨される解決策は、濃度を下げ、染色時間を長くすることです63;しかし、これにより、細胞生存率を高めることなく染色が悪くなる可能性があります。
PKMOと同様に、市販の色素であるLive Orange mito(材料表)も細胞毒性を示します。この色素は様々な培養細胞に使用されましたが、RA分化したSH-SY5Y細胞では、未分化細胞と同じパラメータで同等の染色を示すことができませんでした(未発表の観察結果)。ただし、適切な染色プロトコルは、このプローブおよび選択した細胞タイプに最適化できます。この色素では、1〜1.05〜7.05nsの検出器ゲーティング時間を使用し、 表1 の他のすべてのパラメータは同じままでした。一般に、200-250 nM Live Orange mitoで細胞を45分間染色すると、PKMOの結果と同程度の結果が得られました。より短い時間で高濃度の染色を行ったり、同じ時間またはわずかに長く低濃度の染色を行ったりすると、異なる結果が得られる可能性があり、他の細胞タイプや増殖条件に有利である可能性があります。
ラットの初代海馬ニューロンのイメージングは、軸索と樹状突起の性質、およびイメージング時のミトコンドリア分布により、不死化細胞とは異なります。プロトコルのこの部分の難しさの1つは、播種密度によって、初代培養物が健全に接着して成長できるかどうかが決まり、密度が高くなると、予測がDIV 10で過剰に成長する傾向があることです。したがって、これらの一次ニューロンから画像化されたミトコンドリアは、突起ではなく細胞体に由来する可能性があります。しかし、より低い開始細胞密度からの増殖が成功すると、後の増殖時間でより良いイメージング結果が得られます。重要なのは、STEDに最適なコントラストを得るために、低背景と焦点の合っていない光を確保することです。細胞集団に関する懸念に対処するために、B27を添加したニューロン増殖培地で初代海馬細胞を培養するとグリア細胞の増殖が妨げられ、細胞の<5%がアストロサイトであり、増殖培地にNbActiv1サプリメントが存在しないと、培養中のアストロサイトの数が<2%に減少すると報告されています87。培養SH-SY5Y細胞と初代ラット海馬ニューロンの両方について、増殖に使用されるPDLコーティングは、画像の背景のかすみに寄与します。(表1)で報告した設定で十分なS/N比が得られ、デコンボリューションによって観察されたバックグラウンドのほとんどが除去されます。
ここで取り上げたイメージングに加えて、イメージング前またはイメージング中に細胞に処理やストレスを加えることも可能です。例えば、tert-ブチル過酸化水素(tBHP)を添加すると酸化ストレスが誘発され、添加後のミトコンドリアの経時変化をモニターすることができます。アミロイドβ(Aβ)を蛍光タグで添加することで、ミトコンドリアに関連するこのペプチドの分布やミトコンドリア構造を経時的にモニタリングすることができます。ミトコンドリアの健康はADに深く関与しており、Aβ毒性に関与することが広く支持されている43,71,72。特に、SH-SY5Y細胞の分化状態はAβタンパク質前駆体(AβPP)の局在に影響を及ぼす85ため、AβPPを用いた実験は慎重に構築する必要がある。
このプロトコルをどのように適応させることができるかの一例として、イメージングの15分前に蛍光変異体Aβ(1-42)-HiLyte 647をPKMO染色細胞に添加できることが示されています(補足図1)。イメージングパラメータは類似していますが(補足表2)、主な違いは、狭いミトコンドリアをイメージングする場合、より小さなピンホールが必要になることです。Aβ-HiLyte647をSTEDでイメージングするには、全体的な励起(6%-8%)とSTEDの枯渇(10%-12%)のレーザー出力が少なく、蓄積が少なくて済みます(6)。検出器のゲーティングも0.1nsから10nsに拡張されています。AβのSTED分解能は必須ではありませんが、生STEDの全体的なS/N比とAβ粒子径は共焦点画像よりも優れており、その後のデコンボリューションも実行できます。STED画像を収集し、Aβの生のSTEDzスタック投影をデコンボリューションすることは、PKMO染色の生のSTEDまたはデコンボリューションSTED画像とマージする場合に特に有用であると考えられます(補足図1B、C)。両方のチャンネルを 1 フレーム ステップで収集しました。図 2 にリストされているものと同様の時間依存の局在化の測定値と、該当する場合は 図5に示されているもの、およびクリステ構造の違いは、応力処理またはその他の追加後に取得できます。
ミトコンドリアの生細胞STEDにおける二重標識の他の可能な方法には、SNAPタグ付きタンパク質93、ハロタグ付きタンパク質の使用、およびmtDNA63などの一般的な標的を持つ他の細胞透過性色素の使用が含まれます。特に、SNAPおよびHaloタグ付けの標識戦略は、イメージング時に得られる蛍光シグナル強度および寿命に影響を与える94。さらに、このプロトコルは、セグメント化されたミトコンドリアに適用できる分析の例をいくつか示していますが、ソフトウェアパッケージがこれらの画像に対して実行できる他の多くの分析があります。
開示事項
著者は何も開示していません。
謝辞
初代ラット海馬ニューロンは、コネチカット大学(米国コネチカット州ストーラーズ)の生物医学工学科のGeorge Lykotrafitis博士とShiju Gu博士によって提供されました。Center for Open Research Resources and EquipmentのAdvanced Light Microscopy Facility(先端光学顕微鏡施設)に収容されているAbberior STED装置は、NIHの助成金を得て取得S10OD023618 Christopher O'Connell氏に授与されました。この研究は、NIHの助成金によって資金提供されR01AG065879 Nathan N. Alderに授与されました。
資料
| Name | Company | Catalog Number | Comments |
| 0.05% Trypsin-EDTA | Gibco | 25300054 | |
| 0.4% Trypan blue | Invitrogen | T10282 | |
| 0.5% Trypsin-EDTA, no phenol red | Gibco | 15400054 | |
| 100 X antibiotic-antimycotic | Gibco | 15240062 | |
| 100 X/1.40 UPlanSApo oil immersion lens | Olympus | Equipped in Olympus IX83 microscope for STED setup described in Section 4 | |
| All-trans-retinoic acid | Sigma | R2625 | |
| Amyloid-β (1-42, HiLyte Fluor647, 0.1 mg) | AnaSpec | AS-64161 | Other fluorescent conjugates available |
| B27 supplement (50 X), serum free | Gibco | 17504044 | |
| Cell Counter (Countess II FL) | Life Technologies | AMQAF1000 | |
| Centrifuge | Eppendorf | 5804-R | |
| Counter slides | Invitrogen | C10283 | |
| Conical tubes (15 mL) | Thermo Fisher Scientific | 339650 | |
| Cuvettes (Quartz Cells) | Starna Cells, Inc. | 9-Q-10 | Used with Spectrometer as described in Section 1.3 |
| DMEM (high glucose with sodium pyruvate) | Gibco | 11995073 | Used for SH-SY5Y cell materials as described in Section 1 |
| DMEM (high glucose no sodium pyruvate) | Gibco | 11965092 | Used for primary cell materials as described in Section 2 |
| DMEM (phenol red-free) | Gibco | 31053028 | Used for imaging as described in Section 3 |
| DMSO | Sigma | D8418 | |
| DNAase I from bovine pancreas | Sigma | DN25 | Used for primary cell materials as described in Section 2.2.1 and 2.2.2 |
| DPBS (no calcium, no magnesium) | Gibco | 14190144 | |
| E18 Rat Hippocampus | Transnetyx Tissue | SDEHP | |
| Ethanol (200 proof) | Fisher Bioreagents | BP28184 | |
| Fetal bovine serum (FBS), not heat-inactivated | Gibco | 26140079 | For cultured cells, in Section 1 |
| Fetal bovine serum (heat inactivated) | Gibco | 10082147 | For primary cell culture, Section 2 |
| Filter sterilization unit (0.1 µm, 500 mL) | Thermo Fisher Scientific | 5660010 | |
| FIJI (Is Just ImageJ) and Trainable Weka Segmentation (TWS) plug-in | -- | -- | Free, open-source image analysis software that includes plug-ins including Trainable Weka Segmentation described in Section 5; TWS plug-in from ref. 90 of the main text |
| GlutaMAX supplement (100 X) | Gibco | 35050061 | Glutamine supplement used for primary cell materials described in Section 2.1.2 |
| Hausser Scientific bright-Line and Hy-Lite Counting Chambers | Hausser Scientific | 267110 | |
| HBSS (no calcium, no magnesium) | Gibco | 14170120 | Used for primary cell materials described in Section 2.2.1 and 2.2.2 |
| HEPES | Gibco | 15630080 | |
| Huygens Professional deconvolution software (V. 20.10) | Scientific Volume Imaging (SVI) | -- | The deconvolution software used in this protocol and described in Section 5 |
| IX83 inverted microscope with Continuous Autofocus | Olympus | -- | This paper uses a STED Infinity Line system built around an Olympus IX83 inverted microscope, described in Section 4 |
| Lightbox software (V. 16.3.16118) | Abberior | -- | Vendor software used for STED image acquisition, described in Section 4 |
| Live Orange Mito dye | Abberior | LVORANGE-0146-30NMOL | Live cell imaging IMM-targeting dye described in Discussion |
| Neurobasal media | Gibco | 21103049 | Used for primary cell materials referred to in Section 2.1.2 |
| Nunc Lab-Tek II 2-well chambered coverglass | Nunc | 155379 | Can purchase a variety of chambers but make sure the coverglass is #1.5 |
| Pasteur Pipets (Fisherbrand) | Thermo Fisher Scientific | 22183632 | |
| Penicillin-Streptomycin (10,000 U/mL) | Gibco | 15140122 | |
| PKmito Orange dye | Spirochrome | SC053 | |
| Poly-D-lysine | Gibco | A3890401 | |
| SH-SY5Y Cell line | ATCC | CRL2266 | |
| Sodium pyruvate (100 mM) | Gibco | 11360070 | Used for primary cell materials described in Section 2 |
| Spectrometer (GENESYS 180 UV-Vis) | Thermo Fisher Scientific | 840309000 | |
| STED Expert Line microscope | Abberior | -- | STED setup can be customized, but at time of purchase instrument was considered Abberior’s Expert Line; brief description of setup is available in Section 4 of protocol |
| T25 flask (TC-treated, filter cap) | Thermo Fisher Scientific | 156367 | Other culture vessels and sizes available |
参考文献
- Iovine, J. C., Claypool, S. M., Alder, N. N. Mitochondrial compartmentalization: emerging themes in structure and function. Trends in Biochemical Sciences. 46 (11), 902-917 (2021).
- Gupta, A., Becker, T. Mechanisms and pathways of mitochondrial outer membrane protein biogenesis. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1862 (1), 148323 (2021).
- Gordaliza-Alaguero, I., Cantó, C., Zorzano, A. Metabolic implications of organelle-mitochondria communication. EMBO Reports. 20 (9), e47928 (2019).
- Klecker, T., Westermann, B. Pathways shaping the mitochondrial inner membrane. Open Biology. 11 (12), 210238 (2021).
- Navarro, A., Boveris, A. The mitochondrial energy transduction system and the aging process. American Journal of Physiology-Cell Physiology. 292 (2), C670-C686 (2007).
- Yu, R., Lendahl, U., Nistér, M., Zhao, J. Regulation of mammalian mitochondrial dynamics: opportunities and challenges. Frontiers in Endocrinology. 11, 374 (2020).
- Horn, A., Raavicharla, S., Shah, S., Cox, D., Jaiswal, J. K. Mitochondrial fragmentation enables localized signaling required for cell repair. The Journal of Cell Biology. 219 (5), e201909154 (2020).
- Glancy, B., Kim, Y., Katti, P., Willingham, T. B. The functional impact of mitochondrial structure across subcellular scales. Frontiers in Physiology. 11, 541040 (2020).
- Bahat, A., et al. MTCH2-mediated mitochondrial fusion drives exit from naïve pluripotency in embryonic stem cells. Nature Communications. 9 (1), 5132 (2018).
- Detmer, S. A., Chan, D. C. Functions and dysfunctions of mitochondrial dynamics. Nature Reviews Molecular Cell Biology. 8, 870-879 (2007).
- Bertholet, A. M., et al. Mitochondrial fusion/fission dynamics in neurodegeneration and neuronal plasticity. Neurobiology of Disease. 90, 3-19 (2016).
- Zemirli, N., Morel, E., Molino, D. Mitochondrial dynamics in basal and stressful conditions. International Journal of Molecular Sciences. 19 (2), 564 (2018).
- Harwig, M. C., et al. Methods for imaging mammalian mitochondrial morphology: a prospective on mitograph. Analytical Biochemistry. 552, 81-99 (2018).
- Pánek, T., Eliáš, M., Vancová, M., Lukeš, J., Hashimi, H. Returning to the fold for lessons in mitochondrial crista diversity and evolution. Current Biology. 30 (10), R575-R588 (2020).
- Gottschalk, B., Madreiter-Sokolowski, C. T., Graier, W. F. Cristae junction as a fundamental switchboard for mitochondrial ion signaling and bioenergetics. Cell Calcium. 101, 102517 (2022).
- Khosravi, S., Harner, M. E. The MICOS complex, a structural element of mitochondria with versatile functions. Biological Chemistry. 401 (6-7), 765-778 (2020).
- Frezza, C., et al. OPA1 controls apoptotic cristae remodeling independently from mitochondrial fusion. Cell. 126 (1), 177-189 (2006).
- Meeusen, S., et al. Mitochondrial inner-membrane fusion and crista maintenance requires the dynamin-related GTPase Mgm1. Cell. 127 (2), 383-395 (2006).
- Patten, D. A., et al. OPA1-dependent cristae modulation is essential for cellular adaptation to metabolic demand. The EMBO Journal. 33 (22), 2676-2691 (2014).
- Paumard, P., et al. The ATP synthase is involved in generating mitochondrial cristae morphology. The EMBO Journal. 21 (3), 221-230 (2002).
- Strauss, M., Hofhaus, G., Schröder, R. R., Kühlbrandt, W. Dimer ribbons of ATP synthase shape the inner mitochondrial membrane. The EMBO Journal. 27 (7), 1154-1160 (2008).
- Basu Ball, W., Neff, J. K., Gohil, V. M. The role of nonbilayer phospholipids in mitochondrial structure and function. FEBS Letters. 592 (8), 1273-1290 (2018).
- Hackenbrock, C. R. Ultrastructural bases for metabolically linked mechanical activity in mitochondria. I. Reversible ultrastructural changes with change in metabolic steady state in isolated liver mitochondria. The Journal of Cell Biology. 30 (2), 269-297 (1966).
- Dlasková, A., et al. Mitochondrial cristae narrowing upon higher 2-oxoglutarate load. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1860 (8), 659-678 (2019).
- Pérez-Hernández, C. A., et al. Mitochondrial ultrastructure and activity are differentially regulated by glycolysis-, krebs cycle-, and microbiota-derived metabolites in monocytes. Biology. 11 (8), 1132 (2022).
- Mannella, C. A. Structural diversity of mitochondria: functional implications. Annals of the New York Academy of Sciences. 1147, 171-179 (2008).
- Plecitá-Hlavatá, L., Ježek, P. Integration of superoxide formation and cristae morphology for mitochondrial redox signaling. The International Journal of Biochemistry & Cell Biology. 80, 31-50 (2016).
- Scorrano, L., et al. A distinct pathway remodels mitochondrial cristae and mobilizes cytochrome c during apoptosis. Developmental Cell. 2 (1), 55-67 (2002).
- Heath-Engel, H. M., Shore, G. C. Mitochondrial membrane dynamics, cristae remodelling and apoptosis. Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1763 (5-6), 549-560 (2006).
- Brandt, T., et al. Changes of mitochondrial ultrastructure and function during ageing in mice and Drosophilia. eLife. 6, e24662 (2017).
- Kondadi, A. K., et al. Cristae undergo continuous cycles of membrane remodelling in a MICOS-dependent manner. EMBO Reports. 21, e49776 (2020).
- Quintana-Cabrera, R., Mehrotra, A., Rigoni, G., Soriano, M. E. Who and how in the regulation of mitochondrial cristae shape and function. Biochemical and Biophysical Research Communications. 500 (1), 94-101 (2018).
- Nielsen, J., et al. Plasticity in mitochondrial cristae density allows metabolic capacity modulation in human skeletal muscle: Enlarged mitochondrial cristae density in athletes. The Journal of Physiology. 595 (9), 2839-2847 (2017).
- Afzal, N., Lederer, W. J., Jafri, M. S., Mannella, C. A. Effect of crista morphology on mitochondrial ATP output: A computational study. Current Research in Physiology. 4, 163-176 (2021).
- Heine, K. B., Parry, H. A., Hood, W. R. How does density of the inner mitochondrial membrane influence mitochondrial performance. American Journal of Physiology-Regulatory, Integrative and Comparative Physiology. 324 (2), R242-R248 (2023).
- Wang, W., Zhao, F., Ma, X., Perry, G., Zhu, X. Mitochondria dysfunction in the pathogenesis of Alzheimer's disease: recent advances. Molecular Neurodegeneration. 15, 30 (2020).
- Singh, A., Kukreti, R., Saso, L., Kukreti, S. Oxidative stress: a key modulator in neurodegenerative diseases. Molecules. 24, 1583 (2019).
- Pchitskaya, E., Popugaeva, E., Bezprozvanny, I. Calcium signaling and molecular mechanisms underlying neurodegenerative diseases. Cell Calcium. 70, 87-94 (2018).
- Estes, R. E., Lin, B., Khera, A., Davis, M. Y. Lipid metabolism influence on neurodegenerative disease progression: is the vehicle as important as the cargo. Frontiers in Molecular Neuroscience. 14, 788695 (2021).
- Calkins, M. J., Manczak, M., Mao, P., Shirendeb, U., Reddy, P. H. Impaired mitochondrial biogenesis, defective axonal transport of mitochondria, abnormal mitochondrial dynamics and synaptic degeneration in a mouse model of Alzheimer's disease. Human Molecular Genetics. 20 (23), 4515-4529 (2011).
- Petersen, C. A. H., et al. The amyloid beta-peptide is imported into mitochondria via the TOM import machinery and localized to mitochondrial cristae. Proceedings of the National Academy of Sciences of the United States of America. 105 (35), 13145-13150 (2008).
- Gan, X., et al. Inhibition of ERK-DLP1 signaling and mitochondrial division alleviates mitochondrial dysfunction in Alzheimer's disease cybrid cell. Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1842 (2), 220-231 (2014).
- Baloyannis, S. J., Costa, V., Michmizos, D. Mitochondrial alterations Alzheimer's disease. American Journal of Alzheimer's Disease & Other Dementias. 19 (2), 89-93 (2004).
- Tillement, L., Lecanu, L., Papadopoulos, V. Alzheimer's disease: Effects of β-amyloid on mitochondria. Mitochondrion. 11 (1), 13-21 (2011).
- Choi, S. Y., et al. C9ORF72-ALS/FTD-associated poly(GR) binds Atp5a1 and compromises mitochondrial function in vivo. Nature Neuroscience. 22 (6), 851-862 (2019).
- Smith, E. F., Shaw, P. J., De Vos, K. J. The role of mitochondria in amyotrophic lateral sclerosis. Neuroscience Letters. 710, 132933 (2019).
- Costa, V., et al. Mitochondrial fission and cristae disruption increase the response of cell models of Huntington's disease to apoptotic stimuli. EMBO Molecular Medicine. 2 (12), 490-503 (2010).
- Costa, V., Scorrano, L. Shaping the role of mitochondria in the pathogenesis of Huntington's disease: Mitochondrial and Huntington's disease. The EMBO Journal. 31 (8), 1853-1864 (2012).
- Vanisova, M., et al. Mitochondrial organization and structure are compromised in fibroblasts from patients with Huntington's disease. Ultrastructural Pathology. 46 (5), 462-475 (2022).
- de Barcelos, I. P., Troxell, R. M., Graves, J. S. Mitochondrial dysfunction and multiple sclerosis. Biology. 8 (2), 37 (2019).
- Park, J., et al. Mitochondrial dysfunction in Drosophila PINK1 mutants is complemented by parkin. Nature. 441, 1157-1161 (2006).
- Meng, H., et al. Loss of Parkinson's disease-associated protein CHCHD2 affects mitochondrial crista structure and destabilizes cytochrome c. Nature Communications. 8, 15500 (2017).
- Lu, L., et al. CHCHD2 maintains mitochondrial contact site and cristae organizing system stability and protects against mitochondrial dysfunction in an experimental model of Parkinson's disease. Chinese Medical Journal. 135 (13), 1588-1596 (2022).
- Cogliati, S., et al. Mitochondrial Cristae shape determines respiratory chain supercomplexes assembly and respiratory efficiency. Cell. 155 (1), 160-171 (2013).
- He, B., et al. Mitochondrial cristae architecture protects against mtDNA release and inflammation. Cell Reports. 41 (10), 111774 (2022).
- Polo, C. C., et al. Three-dimensional imaging of mitochondrial cristae complexity using cryo-soft X-ray tomography. Scientific Reports. 10, 21045 (2020).
- Rybka, V., et al. Transmission electron microscopy study of mitochondria in aging brain synapses. Antioxidants. 8 (6), 171 (2019).
- Mannella, C. A. Structure and dynamics of the mitochondrial inner membrane cristae. Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1763 (5-6), 542-548 (2006).
- Fry, M. Y., et al. In situ architecture of Opa1-dependent mitochondrial cristae remodeling. biorxiv. , (2023).
- Barad, B. A., Medina, M., Fuentes, D., Wiseman, R. L., Grotjahn, D. A. Quantifying organellar ultrastructure in cryo-electron tomography using a surface morphometrics pipeline. The Journal of Cell Biology. 222 (4), 202204093 (2023).
- Kunz, T. C., Götz, R., Gao, S., Sauer, M., Kozjak-Pavlovic, V. Using expansion microscopy to visualize and characterize the morphology of mitochondrial cristae. Frontiers in Cell and Developmental Biology. 8, 617 (2020).
- Yang, Z., et al. Cyclooctatetraene-conjugated cyanine mitochondrial probes minimize phototoxicity in fluorescence and nanoscopic imaging. Chemical Science. 11 (32), 8506-8516 (2020).
- Liu, T., et al. Multi-color live-cell STED nanoscopy of mitochondria with a gentle inner membrane stain. Proceedings of the National Academy of Sciences. 119 (52), e2215799119 (2022).
- Yang, X., et al. Mitochondrial dynamics quantitatively revealed by STED nanoscopy with an enhanced squaraine variant probe. Nature Communications. 11, 3699 (2020).
- Zheng, S., et al. Long-term, super-resolution HIDE imaging of the inner mitochondrial membrane in live cells with a cell-permeant lipid probe. biorxiv. , (2022).
- Wang, C., et al. A photostable fluorescent marker for the superresolution live imaging of the dynamic structure of the mitochondrial cristae. Proceedings of the National Academy of Sciences of the United States of America. 116 (32), 15817-15822 (2019).
- Feles, S., et al. Streamlining culture conditions for the neuroblastoma cell line sh-sy5y: a prerequisite for functional studies. Methods and Protocols. 5 (4), 58 (2022).
- Shipley, M. M., Mangold, C. A., Szpara, M. L. Differentiation of the SH-SY5Y human neuroblastoma cell line. Journal of Visualized Experiments. (108), e53193 (2016).
- Kovalevich, J., Langford, D., Amini, S., White, M. K. Considerations for the use of SH-SY5Y neuroblastoma cells in neurobiology. Neuronal Cell Culture. 1078, 9-21 (2013).
- Biedler, J. L., Helson, L., Spengler, B. A. Morphology and growth, tumorigenicity, and cytogenetics of human neuroblastoma cells in continuous culture. Cancer Research. 33 (11), 2643-2652 (1973).
- Swerdlow, R. H. Mitochondria and mitochondrial cascades in alzheimer's disease. Journal of Alzheimer's Disease. 62 (3), 1403-1416 (2018).
- Wang, W., Zhao, F., Ma, X., Perry, G., Zhu, X. Mitochondria dysfunction in the pathogenesis of Alzheimer's disease: recent advances. Molecular Neurodegeneration. 15, 30 (2020).
- Reddy, P. H. Mitochondrial dysfunction in aging and alzheimer's disease: strategies to protect neurons. Antioxidants & Redox Signaling. 9 (10), 1647-1658 (2007).
- Horn, A., Raavicharla, S., Shah, S., Cox, D., Jaiswal, J. K. Mitochondrial fragmentation enables localized signaling required for cell repair. Journal of Cell Biology. 219 (5), e201909154 (2020).
- Korecka, J. A., et al. Phenotypic characterization of retinoic acid differentiated SH-SY5Y cells by transcriptional profiling. PLoS ONE. 8 (5), e63862 (2013).
- Baghel, M. S., Thakur, M. K. Vdac1 downregulation causes mitochondrial disintegration leading to hippocampal neurodegeneration in scopolamine-induced amnesic mice. Molecular Neurobiology. 56 (3), 1707-1718 (2019).
- Jiang, S., et al. Mfn2 ablation causes an oxidative stress response and eventual neuronal death in the hippocampus and cortex. Molecular Neurodegeneration. 13 (1), 5 (2018).
- Mu, Y., Gage, F. H. Adult hippocampal neurogenesis and its role in Alzheimer's disease. Molecular Neurodegeneration. 6, 85 (2011).
- Rao, Y. L., et al. Hippocampus and its involvement in Alzheimer's disease: a review. 3 Biotech. 12 (2), 55 (2022).
- Weerasinghe-Mudiyanselage, P. D. E., Ang, M. J., Kang, S., Kim, J. -. S., Moon, C. Structural Plasticity of the hippocampus in neurodegenerative diseases. International Journal of Molecular Sciences. 23 (6), 3349 (2022).
- . Poly-D-Lysine Available from: https://www.thermofisher.com/order/catalog/product/A3890401 (2023)
- Dravid, A., Raos, B., Svirskis, D., O'Carroll, S. J. Optimised techniques for high-throughput screening of differentiated SH-SY5Y cells and application for neurite outgrowth assays. Scientific Reports. 11, 23935 (2021).
- Hromadkova, L., et al. Brain-derived neurotrophic factor (BDNF) promotes molecular polarization and differentiation of immature neuroblastoma cells into definitive neurons. Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1867 (9), 118737 (2020).
- Riegerová, P., et al. Expression and Localization of AβPP in SH-SY5Y cells depends on differentiation state. Journal of Alzheimer's Disease. 82 (2), 485-491 (2021).
- Hoffmann, L. F., et al. Neural regeneration research model to be explored: SH-SY5Y human neuroblastoma cells. Neural Regeneration Research. 18 (6), 1265-1266 (2022).
- Abiraman, K., Tzingounis, A. V., Lykotrafitis, G. K. Ca 2 channel localization and regulation in the axon initial segment. The FASEB Journal. 32 (4), 1794-1805 (2018).
- E18 Rat Hippocampus. Transnetyx Tissue Available from: https://tissue.transnetyx.com/E18-Rat-Hippocampus_4 (2023)
- Kmito ORANGE - Probe for live cell imaging of mitochondria. Spirochrome Available from: https://spirochrome.com/product/pkmito_orange/ (2023)
- Nyquist Calculator. Scientific Volume Imaging Available from: https://svi.nl/Nyquist-Calculator (2023)
- Segawa, M., et al. Quantification of cristae architecture reveals time-dependent characteristics of individual mitochondria. Life Science Alliance. 3 (7), e2019000620 (2020).
- Arganda-Carreras, I., et al. Trainable Weka Segmentation: a machine learning tool for microscopy pixel classification. Bioinformatics. 33 (15), 2424-2426 (2017).
- Stephan, T., Roesch, A., Riedel, D., Jakobs, S. Live-cell STED nanoscopy of mitochondrial cristae. Scientific Reports. 9, 12419 (2019).
- Erdmann, R. S., et al. Labeling strategies matter for super-resolution microscopy: A comparison between HaloTags and SNAP-tags. Cell Chemical Biology. 26 (4), 584-592 (2019).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved