É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Um estudo randomizado e controlado por simulação de estimulação elétrica craniana para dor e função física da fibromialgia, usando biomarcadores de imagem cerebral
Neste Artigo
Resumo
O presente estudo é um estudo randomizado e controlado por placebo para determinar a eficácia da estimulação elétrica craniana (CES) para melhorar a dor e a função na fibromialgia e desenvolver ainda mais a ressonância magnética de conectividade funcional em repouso (rs-fcMRI) como uma ferramenta clínica para avaliar os correlatos neurais e mecanismos de dor crônica e resposta analgésica.
Resumo
A fibromialgia é uma síndrome de dor crônica que se apresenta com uma constelação de sintomas amplos, incluindo diminuição da função física, fadiga, distúrbios cognitivos e outras queixas somáticas. As terapias disponíveis geralmente são insuficientes no tratamento dos sintomas, com controle inadequado da dor geralmente levando ao uso de opioides para tentativa de tratamento. A estimulação elétrica craniana (CES) é uma opção promissora de tratamento não farmacológico para condições de dor que usa estimulação por corrente elétrica pulsada para modificar a função cerebral por meio de eletrodos transcutâneos. Esses mecanismos neurais e as aplicações do CES no alívio dos sintomas da fibromialgia requerem uma exploração mais aprofundada.
Um total de 50 participantes do Atlanta Veterans Affairs Healthcare System (VAHCS) diagnosticados com fibromialgia foram inscritos e, em seguida, randomizados em bloco em um grupo placebo mais terapia padrão ou CES ativo mais terapia padrão. As avaliações iniciais foram obtidas antes do início do tratamento. Ambas as intervenções ocorreram ao longo de 12 semanas, e os participantes foram avaliados 6 semanas e 12 semanas após o início do tratamento. O desfecho primário investigou se a dor e as melhorias funcionais ocorrem com a aplicação da CES. Além disso, a ressonância magnética de conectividade funcional em estado de repouso basal e de acompanhamento (rs-fcMRI) foi obtida nos pontos de tempo de 6 e 12 semanas para avaliar as aplicações clínicas dos biomarcadores de conectividade neural e as associações neurais subjacentes relacionadas aos efeitos do tratamento.
Este é um estudo randomizado e controlado por placebo para determinar a eficácia do CES para melhorar a dor e a função na fibromialgia e desenvolver ainda mais o rs-fcMRI como uma ferramenta clínica para avaliar os correlatos neurais e mecanismos de dor crônica e resposta analgésica.
Introdução
Dos muitos estados existentes de dor crônica, uma das doenças mais notoriamente difíceis de diagnosticar, avaliar clinicamente e tratar é a fibromialgia. A fibromialgia é uma síndrome de dor crônica debilitante que envolve dor crônica generalizada, diminuição da função física, fadiga, distúrbios psicoemocionais e do sono e várias queixas somáticas que afetam aproximadamente 2-3% da população em geral nas Américas (cerca de 8 milhões de pessoas nos EUA). 1. O diagnóstico da doença depende fortemente da compreensão do paciente sobre seu próprio perfil de sintomas e experiência de dor, e sem essa compreensão adequada da doença pelo médico e pelo paciente, os métodos de tratamento perdem eficácia considerável2. Uma melhor definição das origens e do impacto da fibromialgia, bem como um biomarcador clínico confiável para orientar o diagnóstico e o tratamento da fibromialgia, são necessários para melhor atender a todos os pacientes.
Mesmo com um diagnóstico confirmado, as dificuldades com o processo de tratamento só aumentam. Como um todo, a dor crônica afeta mais indivíduos do que doenças cardíacas, diabetes e câncer combinados. A natureza subjetiva de sua avaliação o coloca como o principal impulsionador da epidemia de opioides, especialmente dada a dificuldade em discernir a dor física incompletamente tratada do transtorno por uso de substâncias e do comportamento de busca de drogas3. Em 2020, 91.799 mortes por overdose de drogas ocorreram nos Estados Unidos (um aumento de 30% em relação a 2019), e os opioides foram considerados a principal causa dessas mortes (74,8% de todas as mortes por overdose de drogas em 2020)4. Assim, alternativas não farmacológicas são necessárias para o tratamento da dor crônica e da fibromialgia para retardar a epidemia de opioides, o que é particularmente importante na população veterana, onde o risco de suicídio e transtorno por uso de opioides é maior5. As terapias não farmacológicas e complementares são, portanto, frequentemente utilizadas como tratamentos de primeira linha6.
A busca por novas e eficazes intervenções para a fibromialgia levou muitos pesquisadores e clínicos a métodos de estimulação cerebral não invasiva, incluindo a estimulação craniana. Embora os mecanismos fisiopatológicos que resultam no desenvolvimento da doença não tenham sido definitivamente determinados, as evidências existentes apóiam a ideia de que a fibromialgia é um distúrbio da disfunção do sistema nervoso autônomo e mecanismos centrais (ou seja, cérebro e medula espinhal) de processamento da dor 7,8. A estimulação de certas áreas do cérebro pode levar a uma melhor função nessas áreas de processamento. A estimulação magnética transcraniana repetitiva (EMTr) e a estimulação transcraniana por corrente contínua (ETCC) têm sido correlacionadas com reduções na dor, mas também têm sido associadas à irritação do couro cabeludo no local de ativação, dores de cabeça e inacessibilidade fora das instalações de tratamento9. A estimulação não invasiva do nervo vago (nVNS), que pode fornecer neuromodulação por meio da estimulação sobre a pele no pescoço ou no nível da orelha, tem potencial para o tratamento da dor crônica, e a estimulação invasiva do nervo vago (VNS) demonstrou melhorar os sintomas de dor crônica10. No entanto, nem o VNS invasivo nem o não invasivo foram suficientemente explorados na literatura ou totalmente validados para uso no tratamento da fibromialgia 11,12,13,14.
A estimulação elétrica craniana (CES) é um tratamento de estimulação cerebral não farmacológico e não invasivo que consiste em microcorrente pulsada e alternada (menos de 0,5 mA) aplicada por meio de eletrodos transcutâneos colocados nos lóbulos das orelhas15. É extremamente acessível e pode ser entregue por meio de dispositivos portáteis usados por pacientes em seus próprios espaços de convivência. Em comparação com outros métodos de estimulação craniana, a natureza não invasiva e a conveniência da autoaplicação do paciente em casa aumentam o potencial da CES como uma opção benéfica para o uso generalizado do tratamento da fibromialgia e o autogerenciamento da dor. Foi liberado pela Food and Drug Administration (FDA) dos EUA como um tratamento para insônia, depressão, ansiedade e dor15.
O presente estudo avalia a eficácia do CES como uma modalidade de tratamento da fibromialgia, comparando o CES ativo (administrado por um dispositivo de estudo verdadeiro) versus o CES simulado (administrado por um dispositivo de estudo simulado). Existem algumas evidências preliminares para apoiar o uso da CES no tratamento de condições de dor, como a fibromialgia16,17. Um estudo de 2001 com 60 participantes randomizados para CES ativo ou simulado por 3 semanas de sessões diárias de 60 minutos revelou uma melhora de 28% nos escores de pontos dolorosos, 27% de melhora nos escores gerais de dor e nenhum efeito placebo18. A CES não foi avaliada em uma população de veteranos, nem foi adequadamente avaliada em homens com fibromialgia. Uma revisão sistemática da CES financiada pela Veterans Affairs (VA) publicada em 2018 concluiu que as evidências são insuficientes para que a CES tenha efeitos clinicamente importantes na fibromialgia, uma vez que a maioria dos ensaios teve amostras pequenas, durações curtas e um alto risco de viés devido ao cegamento inadequado. No entanto, a revisão sugere que a CES não causa efeitos colaterais graves, e há evidências de baixa força que sugerem benefícios modestos em pacientes com ansiedade e depressão19. Portanto, mais pesquisas são necessárias sobre o uso deste dispositivo de baixo risco aprovado pela FDA, particularmente na fibromialgia.
Para avaliar completamente a eficácia, os pesquisadores avaliaram a aptidão física juntamente com biomarcadores neurais e experiência de dor. O objetivo do tratamento de estados de dor crônica é melhorar a função física. A fibromialgia está consistentemente correlacionada com efeitos negativos tanto na função física quanto na percepção dos pacientes sobre suas próprias habilidades físicas20. Estudos anteriores utilizaram avaliações simples de aptidão física para determinar a resistência e a mobilidade, como o Teste de Caminhada de 6 Minutos (TC6)20,21, Sentar e Levantar Cinco Vezes (5TSTS)20 e várias medidas de capacidade de carga e força no contexto das atividadesdiárias22. Para levar em conta as medidas padrão e, ao mesmo tempo, mitigar a quantidade de atividade extenuante necessária antes de uma ressonância magnética, a equipe do estudo usou o teste de 30 segundos para sentar na cadeira como uma medida de resistência e mobilidade e ambos os bíceps e um teste de preensão manual como medidas de força23. Os movimentos exigidos em cada uma dessas avaliações são muito comuns nas atividades cotidianas, por isso é uma medida clara de como as pessoas estão funcionando fisicamente em seu dia-a-dia, com e sem tratamento.
Mesmo com avaliações subjetivas da dor e medidas de eficácia da função física, os mecanismos da CES não são totalmente compreendidos. Estudos anteriores de neuroimagem buscaram uma melhor compreensão, explorando o efeito direto do CES na conectividade de rede no cérebro. Feusner et al.24 verificaram que o CES está associado à desativação cortical para estimulação de 0,5 Hz e 100 μA das regiões frontal, parietal e da linha média posterior bilaterais e postularam que a frequência de estimulação pode ter mais efeito do que a intensidade da corrente em relação à desativação cortical. Seu grupo encontrou efeitos significativos em alguns, mas não em todos os nós da rede de modo padrão (DMN). Os autores sugerem que, com base nesses dados, o CES pode afetar a conectividade funcional do estado de repouso. A fibromialgia e outros estados de dor crônica demonstraram afetar a conectividade cerebral intrínseca em regiões associadas à dor e à percepção25,26, de modo que os tratamentos que alteram a conectividade funcional em resposta podem ser benéficos e eficazes. Uma exploração mais aprofundada dos efeitos a longo prazo do tratamento diário em relação à melhora clínica, bem como como a ativação do falecido no cérebro se relaciona com as diminuições observadas anteriormente nas frequências do eletroencefalograma, é necessária para entender melhor o mecanismo terapêutico de ação27.
A ressonância magnética de conectividade funcional em estado de repouso (rs-fcMRI) é o método de neuroimagem que permite a observação dessas alterações de conectividade funcional. A ressonância magnética funcional longitudinal em estado de repouso permite que médicos e pesquisadores estabeleçam uma linha de base da conectividade do estado de repouso e rastreiem as alterações ao longo do tempo em resposta aos métodos de tratamento da CES. Também ajuda a determinar como as mudanças na conectividade funcional estão correlacionadas às diferenças na experiência da dor. Os estudos iniciais de neuroimagem para fibromialgia usaram tomografia por emissão de pósitrons (PET) e tomografia computadorizada por emissão de fóton único (SPECT) para examinar o cérebro, mas há problemas com ambas as técnicas a esse respeito: o SPECT tem uma resolução mais baixa do que o PET e os exames de PET são invasivos, o que não é preferível para pacientes com dor crônica. As imagens de ressonância magnética funcional (fMRI) têm maior resolução do que o SPECT, mas examinam a atividade cerebral em resposta às ações ou percepções específicas dos pacientes sobre os estímulos28. São as varreduras rs-fcMRI que podem delinear a conectividade funcional entre as regiões do cérebro e podem determinar onde e como a fibromialgia existe, bem como os melhores métodos de tratamento28.
Avaliar a eficácia de tratamentos não farmacológicos para condições de dor, como a fibromialgia, é de extrema importância tanto no cenário atual da epidemia de opioides quanto no exame da dor crônica como fator de risco para suicídio29,30, que é substancialmente aumentada entre a população veterana. Além disso, a falta de biomarcadores clínicos adequados para a dor é uma lacuna de conhecimento reconhecida. Usar uma combinação de medidas comportamentais e neuroimagem em vários pontos de tempo para avaliar a resposta ao tratamento é uma nova abordagem para a avaliação da fibromialgia, assim como a utilização do CES auricular como tratamento.
O protocolo visa abordar a lacuna na pesquisa da fibromialgia, investigando os efeitos do CES nos resultados da dor e da função física e avaliando a neuroimagem como uma ferramenta para biomarcadores preditivos e de resposta relacionados aos resultados clínicos da terapia CES31.
Protocolo
O estudo foi conduzido sob a aprovação dos Conselhos de Revisão Institucional da Emory University (IRB 112768) e Atlanta VA (1585632-2; Número de Referência Interno: 003), bem como o Comitê de P&D do Atlanta VA (Número de Referência do Conselho: 3881). Todos os sujeitos assinaram o termo de consentimento livre e esclarecido para inclusão antes de participarem deste estudo. Para uma representação visual da linha do tempo do protocolo do estudo, consulte a Figura 1).
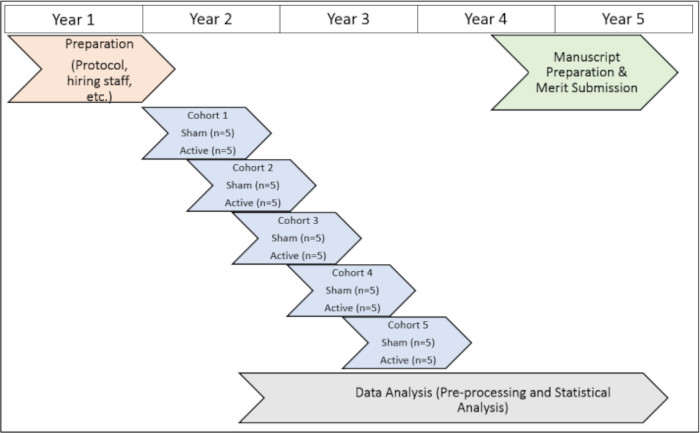
Figura 1: Linha do tempo do estudo. Uma representação visual do cronograma para a execução dos procedimentos do estudo durante o período experimental. Clique aqui para ver uma versão maior desta figura.
1. Recrutamento de participantes através dos métodos disponíveis
- Siga as respectivas diretrizes institucionais exigidas para divulgar materiais de recrutamento de estudos (panfletos, postagens, e-mails, chamadas, etc.) e métodos de recrutamento aprovados.
NOTA: O estudo atual recrutou por meio de cartas de recrutamento para coortes específicas e telefonemas de acompanhamento para participantes em potencial. Os detalhes sobre o pedido dos dispositivos CES para o estudo estão incluídos nas instruções suplementares de pedido de dispositivos CES (Arquivo Suplementar 1). - Quando alguém manifestar interesse em participar do estudo, examine-o por telefone para garantir que atenda a todos os critérios de inclusão e exclusão.
- Incluir participantes que se enquadrem nos critérios de elegibilidade: idade de 20 a 60 anos (limite estabelecido durante o estudo preliminar para minimizar as alterações estruturais cerebrais devido ao envelhecimento)31; diagnóstico de fibromialgia pelos critérios32 do American College of Rheumatology 2016; destro (a fim de fornecer consistência na estrutura e função do cérebro); escore de dor de 4 ou mais na Escala de Avaliação de Dor de Defesa e Veteranos (DVPRS)33 nos 3 meses anteriores à inscrição; medicação consistente e estável relacionada à FM por pelo menos 4 semanas antes da inscrição34; e capacidade de tolerar com segurança a RNM.
- Para a parte de triagem de fibromialgia, preencha os novos critérios clínicos de diagnóstico de fibromialgia32 com o participante em potencial para obter sua pontuação de índice de dor generalizada (WPI) e pontuação de gravidade (SS). Pontue de acordo com as diretrizes listadas na parte inferior da página.
- Para a parte de triagem do escore de dor, peça aos participantes em potencial que avaliem verbalmente sua dor média e consistente nos últimos 3 meses em uma escala de zero a dez.
- Para a parte de triagem de ressonância magnética, preencha um formulário de triagem de segurança de ressonância magnética com o participante em potencial fornecido por uma instituição ou pela própria instalação do scanner.
- Pergunte aos participantes sobre todos os possíveis critérios de exclusão. Os critérios de exclusão incluem história de convulsões ou condições neurológicas que alteram o cérebro; gravidez; claustrofobia, implantes incompatíveis com ressonância magnética ou outras condições incompatíveis com ressonância magnética; e história de doença psiquiátrica não controlada ou doença autoimune que leva à dor e pode explicar melhor os sintomas31.
- Se algum dos critérios de exclusão se aplicar a eles, eles falharão na triagem. Não os inclua no estudo.
- Incluir participantes que se enquadrem nos critérios de elegibilidade: idade de 20 a 60 anos (limite estabelecido durante o estudo preliminar para minimizar as alterações estruturais cerebrais devido ao envelhecimento)31; diagnóstico de fibromialgia pelos critérios32 do American College of Rheumatology 2016; destro (a fim de fornecer consistência na estrutura e função do cérebro); escore de dor de 4 ou mais na Escala de Avaliação de Dor de Defesa e Veteranos (DVPRS)33 nos 3 meses anteriores à inscrição; medicação consistente e estável relacionada à FM por pelo menos 4 semanas antes da inscrição34; e capacidade de tolerar com segurança a RNM.
- Quando alguém passar na triagem, agende-o para a consulta de consentimento e a ressonância magnética de linha de base. Agende 2 h para o consentimento e o tempo de verificação.
2. Administração de consultas de estudo de linha de base, intermediárias e pós-participantes (ver Tabela 1)
NOTA: Todas as consultas ocorrem no local do scanner de ressonância magnética.
| Hora | Atividade de Pesquisa | |
| Fase 1 | Semana 1 | Recrutamento, Triagem, Inscrição |
| Fase 2 | Semana 2–3 | Avaliações de linha de base, rs-fcMRI |
| Fase 3 | Semanas 2–14 | Intervenção |
| Fase 4 | Semana 6–10 | Acompanhamento agudo, rs-fcMRI (6 semanas de tratamento) |
| Fase 5 | Semana 12–16 | Acompanhamento de longo prazo, rs-fcMRI (12 semanas de tratamento) |
Tabela 1: Desenho da pesquisa. Uma linha do tempo das fases de participação individual ao longo das 12 semanas do estudo.
- Antes de cada visita inicial, prepare um dispositivo CES para levar a cada participante.
- Abra o estojo para garantir que o dispositivo esteja dentro (deve estar em plástico bolha). Remova a parte traseira do dispositivo e insira duas pilhas AAA.
- Recoloque o dispositivo de volta. Ligue o dispositivo para garantir que funcione antes de levá-lo ao participante. Mantenha pressionado o botão superior por cerca de 2 s até que a tela acenda para ligá-lo e mantenha-o pressionado por cerca de 2 s até que a tela fique em branco para desligá-lo.
- Certifique-se de que cada estojo contenha o dispositivo, baterias extras, um cordão, um pequeno aplicador de solução e clipes de ouvido. Certifique-se de que a bolsa a ser entregue aos participantes contenha o estojo do dispositivo, um frasco de solução condutora, uma tampa extra para encher o aplicador de solução pequena e almofadas de eletrodo de clipe de orelha extras.
- Uma vez que seu consentimento e ressonância magnética de linha de base tenham sido agendados, encontre o participante no local do scanner de ressonância magnética para a consulta com duas cópias do formulário de consentimento, um dispositivo CES e seus materiais, documentação de teste de elegibilidade e um pacote de questionário para eles preencherem. Além disso, traga o dispositivo de transferência de dados através do qual os dados de ressonância magnética serão transferidos para o local de análise.
NOTA: Este estudo utilizou uma unidade USB criptografada.- Para a papelada de elegibilidade, inclua os novos critérios clínicos de diagnóstico de fibromialgia32 e o DVPRS33.
NOTA: O DVPRS deve ser incluído para cada visita. - Para os testes de função física, incluir um formulário para registrar os resultados de cada teste 20,21,35.
- Para os questionários que os participantes preencherão, inclua as medidas PROMIS apropriadas (Escala PROMIS v1.2 - Saúde Global, Banco de Itens Neuro-QOL v2.0 - Função de Cognição - Formulário Curto, Banco de Itens PROMIS v1.0 - Uso de Substâncias/Álcool: Uso de Álcool, Banco de Itens PROMIS v1.0 - Sofrimento Emocional - Ansiedade - Formulário Abreviado 7a, Banco de Itens PROMIS v1.0 - Angústia Emocional-Depressão - Formulário Curto 4a, Banco de Itens PROMIS v1.0 - Fadiga - Formulário Curto 6a, PROMIS Item Bank v1.0 - Interferência da Dor - Formulário Abreviado 4a, PROMIS Item Bank v1.2 - Função Física - Formulário Abreviado 8b, PROMIS Item Bank v2.0 - Isolamento Social - Formulário Abreviado 4a)36.
- Para a papelada de elegibilidade, inclua os novos critérios clínicos de diagnóstico de fibromialgia32 e o DVPRS33.
- No local da ressonância magnética, administre a visita inicial. Ligue para o participante com antecedência para confirmar.
- Leia o formulário de consentimento completo com o participante, garantindo que ele entenda as informações. Pergunte se eles gostariam de participar e, se concordarem, peça-lhes que imprimam seu nome, assinem e coloquem a data no formulário.
- Após o consentimento, se o participante optar por participar do estudo, preencha a papelada do teste de inclusão com ele. Se eles estiverem qualificados para continuar, conclua as etapas abaixo; se eles não forem elegíveis, encerre sua participação no estudo neste momento.
- Certifique-se de que a papelada do teste de elegibilidade inclua os novos critérios clínicos de diagnóstico de fibromialgia e o DVPRS.
- Se um participante for elegível após o teste de inclusão, explique ao participante como usar o dispositivo CES.
- Remova o dispositivo do estojo e mostre aos participantes como ligá-lo e desligá-lo com o botão na parte superior. Lembre aos participantes que o dispositivo será desativado automaticamente após 60 minutos.
- Mostre aos participantes como prender o cordão do clipe de orelha na lateral. A extremidade oposta do cabo dos clipes se conecta a um pequeno orifício no lado esquerdo do dispositivo rotulado com um "1".
- Demonstre como remover as almofadas de eletrodo antigas dos clipes de ouvido e colocar novas. Para remover as almofadas antigas, puxe o adesivo de onde ele se conecta aos clipes. Para prender novas almofadas, alinhe o orifício nas almofadas do eletrodo sobressalente com a área elevada no centro do clipe e pressione com firmeza.
NOTA: Não puxe as almofadas do eletrodo pela parte macia na parte superior. É propenso a rasgar e deixará o adesivo grudado nos clipes. - Demonstre como prender os clipes de orelha nos lóbulos das orelhas e peça que experimentem uma vez. Aperte as pontas verdes do clipe para abri-lo, posicione o lóbulo da orelha entre eles e feche suavemente o clipe para prendê-lo.
- Mostre-lhes como remover a tampa de plástico do aplicador de solução pequena e enchê-la com a solução do frasco maior (consulte as etapas 2.3.3.6-2.3.3.8). Lembre-os de que a solução é necessária para que o dispositivo funcione corretamente.
- Para remover a parte superior do aplicador de solução pequena, remova a tampa e pressione firmemente contra a lateral da ponta. A ponta de plástico se desprenderá do resto da garrafa.
- Coloque a tampa alternativa para encher o aplicador pequeno na parte superior do frasco de solução maior. Empurre o bico pequeno para cima, deslize-o para dentro do aplicador pequeno e aperte o frasco grande para encher.
- Diga aos participantes que eles devem adicionar apenas cerca de 1-2 gotas da solução a cada almofada de eletrodo de clipe de ouvido. Qualquer excesso de solução deve ser removido antes do uso.
- Instrua os participantes a usar o dispositivo todos os dias da semana por 60 minutos à noite, cerca de 1 h antes de ir para a cama. Instrua os participantes a usar o dispositivo em repouso (ou seja, sentados ou deitados, sem se movimentar).
NOTA: Tanto para o tempo quanto para a posição, os participantes tiveram permissão para variações normais em seu ambiente doméstico de uso para aumentar a natureza prática dessa terapia para uso doméstico. Nenhum parâmetro foi definido para o som permitido no ambiente ou armazenamento necessário do dispositivo. - Dê aos participantes um registro do dispositivo em branco e explique que eles precisam inserir cada data de uso do dispositivo, sua pontuação de dor antes e depois do uso do dispositivo e o tempo de uso do dispositivo.
- Se os participantes não puderem usar o dispositivo por um período de tempo durante as 6 semanas entre as consultas, mas puderem fazer as consultas de acompanhamento, deixe-os permanecer no estudo. Se eles não puderem usar o dispositivo ou comparecer às visitas do estudo, encerre sua participação. Consulte o log de dispositivo CES suplementar (Arquivo Suplementar 2) para o log de dispositivo usado por este estudo.
NOTA: As etapas a seguir serão repetidas durante as três visitas.
- Após a explicação do dispositivo, peça ao participante que complete três pequenos testes de função física23. Para cada teste, um número máximo será registrado para a pontuação (total de repetições para os dois primeiros e força por tentativa para o terceiro).
NOTA: O cronômetro usado para este estudo foi um Apple iPhone 12.- Administre o teste de sentar na cadeira de 30 s. Siga as etapas 2.3.4.2-2.3.4.6.
- Coloque uma cadeira com as costas contra a parede da sala de testes. Peça ao participante que se sente na cadeira com as costas contra o encosto da cadeira.
- Instrua o participante a se levantar para uma posição totalmente em pé e, em seguida, sentar-se totalmente com as costas contra o encosto da cadeira quantas vezes puder em 30 segundos.
NOTA: Se eles baterem na cadeira, mas não colocarem totalmente o peso de volta na posição sentada, a repetição não conta. - Diga aos participantes quando começar. Inicie o cronômetro quando eles começarem a se mover.
- Peça aos participantes que façam flexões de braço com um haltere de cada lado por 30 s de cada lado. Comece com o braço direito primeiro e depois vá para a esquerda.
- Registre o número total de cachos por lado. Use um peso de 5 libras para mulheres e um peso de 8 libras para homens. Certifique-se de que os participantes estejam sentados para o teste de rosca direta de braço.
- Peça aos participantes que façam três testes de força de preensão com cada braço em um dinamômetro. Siga as etapas 2.3.4.8-2.3.4.11. Comece com o braço direito primeiro e depois vá para a esquerda.
- Coloque o dinamômetro na mão do participante. Eles devem apertar a alça na parte inferior e não tocar no mostrador na parte superior.
- Diga aos participantes para apertar o dinamômetro o mais forte que puderem e depois soltá-lo. A agulha no mostrador irá parar no nível mais alto de força de preensão que eles exibiram.
- Registre seus resultados de força de preensão anotando o número que a agulha atinge no mostrador. Redefina o mostrador entre as repetições girando o pequeno botão na frente do mostrador no sentido anti-horário até que a agulha fique em zero.
- Certifique-se de que os participantes estejam sentados para o teste de preensão manual.
NOTA: Entre cada série, os participantes recebem cerca de 15 a 20 segundos de descanso enquanto mudam o equipamento para a outra mão. Entre cada teste, os participantes receberão cerca de 2 minutos de descanso enquanto o equipamento e a documentação para o próximo são preparados.
- Após os testes de função física, peça aos participantes que preencham o pacote de questionário com uma caneta. Verifique o pacote depois para ter certeza de que eles responderam a todas as perguntas.
- Depois que todas as revisões, testes e questionários forem concluídos, leve os participantes até o próprio scanner de ressonância magnética (para obter todas as informações do protocolo de ressonância magnética, consulte a seção 3). Revise o formulário de triagem com os técnicos de ressonância magnética e certifique-se de que os participantes removeram todo o metal de sua pessoa.
- Certifique-se de que os membros da equipe de estudo não tenham metal em suas pessoas.
- Ajude os técnicos de ressonância magnética a colocar os participantes no scanner confortavelmente. Administre o protocolo de ressonância magnética.
- Instruir os participantes sobre os procedimentos de segurança (botão de chamada de teste e alto-falantes).
- Lembre os participantes de não se moverem durante a varredura.
- Lembre os participantes da duração total do exame, que deve ser de 60 min.
- Quando a verificação for concluída, ajude os participantes a sair do scanner.
- Após a varredura, termine a visita inicial dos participantes e agende sua visita intermediária para 6 semanas depois. Os participantes terão três visitas de estudo no total, cada uma com 6 semanas de intervalo. Envie os dados de ressonância magnética para os servidores seguros do estudo para análise.
- No dia agendado, administre a visita intermediária seguindo as etapas da visita inicial. Ligue para o participante com antecedência para confirmar.
- Administre o DVPRS. Peça aos participantes que devolvam o primeiro registro de dispositivo preenchido e forneçam um segundo registro de dispositivo.
- Execute as etapas 2.3.4-2.3.6 (o mesmo que na visita inicial).
- Termine a visita intermediária dos participantes e agende sua pós-visita para 6 semanas depois. Envie os dados de ressonância magnética para os servidores seguros do estudo para análise.
- No dia agendado, administrar o pós-visita seguindo os passos do meio da visita. Ligue para o participante com antecedência para confirmar.
- Administre o DVPRS. Peça aos participantes que devolvam o segundo registro de dispositivo concluído.
- Execute as etapas 2.3.4-2.3.6 (o mesmo que na linha de base e nas visitas intermediárias). Nenhum agendamento de visita adicional é necessário para a última visita.
- Se alguma informação for necessária para compensar os participantes, prepare e solicite essa informação nesta visita.
NOTA: Este estudo exigia seu nome e endereço para emitir cheques do Atlanta VA para compensação. - Termine a pós-visita dos participantes. Envie os dados de ressonância magnética para os servidores seguros do estudo para análise.
NOTA: Ao longo do estudo, certifique-se de ligar e verificar com os participantes entre as visitas para garantir que eles estejam usando o dispositivo, preenchendo os registros do dispositivo e cientes de quando será a próxima visita.
3. Configurando protocolos de varredura de ressonância magnética
- Para o protocolo de varredura de ressonância magnética, adquira o BOLD rs-fMRI em um scanner de ressonância magnética 3T com uma bobina de cabeça phased array de 32 canais usando uma sequência de imagem ecoplanar gradiente (EPI). Use os seguintes parâmetros de RM: FOV (Campo de Visão) = 220 mm2; TR (Tempo de Repetição)/TE (Tempo de Eco) = 1500/25 ms, fator de aceleração multibanda =3; ângulo de inversão = 50°; Tamanho da matriz 110 x 110; espessura do corte = 2 mm; Fator GRAPPA = 2; Fourier parcial de 6/8; 34 linhas de referência codificadas por fase, 72 fatias axiais intercaladas cobrindo todo o cérebro, cerca de 350 volumes de varredura para produzir 8 minutos de dados de fMRI em estado de repouso para estimativa estável de redes de conectividade.
- No protocolo para a magnetização anatômica T1w preparada eco gradiente rápido (MPRAGE), defina TR = 2530 ms, TE = 3 ms, ângulo de inversão = 7°, espessura do corte = 0,8 mm, resolução de fase de 1 mm. A aquisição do T1w dura aproximadamente 6 min.
- Adquira varreduras de imagem ponderada por difusão (DWI) em um scanner de ressonância magnética 3T com uma bobina de cabeça Phased Array de 32 canais usando um esquema de imagem de espectro de difusão. Colete um total de 129 direções de amostragem de difusão com um valor b máximo de 3000 s/mm2, uma resolução no plano de 2x2 mm2 e uma espessura de corte de 2 mm.
- Adquira dados fisiológicos (dados cardiorrespiratórios utilizando um cinto de monitor respiratório e oximetria de pulso) simultaneamente (bloqueado por tempo) aos dados de fMRI.
- Transfira com segurança os dados de ressonância magnética do local do scanner para um local seguro para pré-processamento e análise. Converta DICOMS em NIFTIs para cumprir a formatação BIDS utilizando dc2bids v2.1.6.
- Limpe os dados de identificadores individuais. Use um número de sujeito de estudo em todos os dados, sempre que aplicável. Realize uma verificação de qualidade para garantir que nenhum artefato anômalo, como movimento excessivo, tenha ocorrido nos dados por meio do MRIQC v21.0.0.
4. Pré-processamento e análises
- Uma vez que os dados de ressonância magnética do estudo tenham sido recebidos, utilize dois pipelines separados para analisá-los: um para analisar a conectividade funcional entre os participantes e outro para analisar a tractografia da substância branca.
- Pré-processe os dados estruturais T1w e rsfMRI dos indivíduos via fMRIPrep v20.2.5, incluindo extração cerebral, segmentação de tecido e normalização das imagens ponderadas em T1 (T1w), bem como estimativa de volume de referência, estimativa de movimento da cabeça, correção de tempo de corte e registro no T1w para as imagens funcionais. Esse processo resulta nos dados T1w e rsfMRI normalizados no espaço MNI152NLin2009cAsym.
- Use os dados de ressonância magnética pré-processados na análise de conectividade funcional (CONN).
- Consulte o documento suplementar fMRIPrep Boilerplate (Arquivo Suplementar 3: 37-56). Para mais detalhes, consulte o link: https://fmriprep.org/en/stable/
- Importe o conjunto de dados pré-processado para o CONN Toolbox v22a para processamento posterior.
NOTA: O CONN Toolbox foi atualizado de v21a para v22a durante este estudo.- Na fase de configuração, estabeleça covariáveis de2º nível para definir os grupos de estudo (TRUE vs. SHAM) para análise posterior e garantir a qualidade das imagens T1w e rsfMRI. Dados de fMRI suaves via kernel gaussiano de 8 mm.
- Após o pré-processamento, reduza o ruído dos dados para remover ruídos estranhos e fisiológicos.
NOTA: Este estudo calculou a análise de primeiro nível, mas não a avaliou ou usou, pois os pesquisadores não estão interessados em resultados de um único sujeito. - Escolha sementes/ROIs e covariáveis de assunto e defina contrastes. Execute uma análise de semente para voxel em nível de grupo.
- Depois que as etapas de configuração, pré-processamento e redução de ruído forem concluídas para os pipelines, defina os limites de cluster e voxel para exibir os padrões de conectividade.
- Consulte a Figura Suplementar 1 e o documento suplementar CES CONN Instructions (Supplementary File 4).
- Usar tractografia correlacional57 determinar as mudanças longitudinais na integridade da substância branca correlacionadas com o grupo experimento para identificar feixes de tratos e regiões associadas ao tratamento CES. Abaixo estão as principais etapas de análise:
- Converta as imagens DWI brutas do .dcm (DICOM) para o formato .nii.gz (NIfTI).
- Pré-processe as imagens para corrigir distorções induzidas por suscetibilidade usando o FSL (versão 6.0.6) TOPUP 58,59 e para distorções de correntes parasitas usando a ferramenta EDDY60 do FSL.
- Gere métricas de controle de qualidade de imagem (QC) DWI relacionadas ao movimento em um único assunto e níveis de estudo usando as ferramentas EDDY QC da FSL.
- Execute uma ANOVA de medidas repetidas bidirecionais nessas métricas de CQ para identificar qualquer variação entre grupos que possa confundir os resultados da tractografia do grupo. Se uma métrica mostrar uma variância entre grupos significativa (p > 0,05), ela deve ser contabilizada como uma covariável na análise da tractografia correlacional.
- Importe os dados pré-processados para o DSI Studio (versão "Chen" 21 de novembro de 2022), onde eles são convertidos em arquivos .src (origem). Para obter mais informações sobre o DSI Studio, consulte o site do software (https://dsi-studio.labsolver.org).
- Reconstrua os dados de difusão importados usando Q-Space Diffeomorphic Reconstruction (QSDR) 61 para determinar as orientações das fibras da substância branca no espaço do modelo MNI. Um arquivo .fib (orientação de fibra) é gerado para cada imagem. As opções de seleção para a reconstrução são:
(seleção do método de reconstrução) - QSDR
param0 (comprimento de amostragem de difusão) - 1,25 (este é o padrão)
predefinição (para qual espaço de predefinição reconstruir os dados) - ICBM152
align_acpc (se o volume da imagem deve ser girado para alinhar AC-PC) - 0 (falso) - Crie um banco de dados de conectometria a partir desses arquivos .fib, que extrai os valores quantitativos de anisotropia (QA) dos dados de difusão reconstruídos. Calcule a mudança longitudinal no controle de qualidade para cada assunto no banco de dados. Adicione dados demográficos, como grupo de experimento, idade, sexo, juntamente com quaisquer covariáveis identificadas na etapa de controle de qualidade por meio de um arquivo .csv ao banco de dados.
- Em seguida, carregue o banco de dados de conecometria na GUI de análise de conecometria de grupo.
- Selecione as covariáveis a serem consideradas na análise. Uma dessas covariáveis selecionadas é designada como variável de estudo.
- Para esta análise, selecione Grupo como variável de estudo. Setores com mudanças longitudinais no QA correlacionados com o Grupo serão identificados, enquanto o efeito das outras covariáveis selecionadas será regredido.
- As seleções de opções para a análise de conectometria de grupo são:
- Controle FDR (corte de taxa de descoberta falsa, apenas setores com correlação significativa abaixo de FDR serão produzidos) - 0,05
- Limite de comprimento (valor em voxels de comprimento mínimo do trato usado como hipótese nula) - 20 voxels (ou 40 mm para tamanhos de voxels de 2 mm)
- Limite T (limiar de medição t-stat para efeito de correlação) - 2,5
- Região de estudo (este painel permite que as regiões sejam incluídas/excluídas da análise) - selecione Whole Brain com - Excluir cerebelo marcado
NOTA: Para este estudo, o cerebelo foi excluído devido a algumas das varreduras de difusão terem partes do cerebelo cortadas durante a aquisição.
- Pressione o botão Executar conectometria para executar a análise, que gera vários arquivos:
- Um arquivo .fib que armazena as estatísticas t e pode ser aberto no DSI Studio para visualizar as estatísticas t de tratos com controle de qualidade crescente (armazenado como "inc_t") ou controle de qualidade decrescente (armazenado como "dec_t"), que se correlacionam com o Grupo.
- Um .fdr_dist.values.txt, que lista os valores de FDR em relação ao comprimento do trato
- Um .inc.tt.gz que é um arquivo de tractografia que armazena os setores com aumento do controle de qualidade longitudinal correlacionado com a variável do estudo. (Grupo no nosso caso). Um arquivo de .dec.tt.gz armazena os setores com redução do controle de qualidade longitudinal correlacionado com a variável de estudo.
- Um arquivo .report.html que relata convenientemente os resultados da conectometria junto com gráficos de trato embutidos, fotos, bem como as informações padronizadas sobre as etapas de análise da tractografia correlacional para publicação.
NOTA: Para ver exemplos do código R usado para este estudo, consulte os gráficos de código R CES suplementares (Arquivo Suplementar 5) e os arquivos Anova EDDY-qc CES do Código R suplementar (Arquivo Suplementar 6).
Resultados
Em termos de resultados de recrutamento, os participantes foram recrutados principalmente por meio de cartas de recrutamento e telefonemas de acompanhamento com base nos regulamentos descritos do Atlanta VA Healthcare System. A equipe do estudo recrutou um total de 50 participantes, comprovando a eficácia dos métodos usados para atingir a meta de recrutamento (ver Figura 2). O uso dos novos critérios diagnósticos clínicos de fibromialgia permitiu que a e...
Discussão
Os métodos do presente estudo fornecem não apenas a possibilidade de uma modalidade de tratamento altamente eficaz para a fibromialgia, mas também a oportunidade de melhorar o processo diagnóstico da fibromialgia desde a primeira instância de seu perfil de sintomas de dor. O uso de CES ativo e CES simulado, com a descoberta do tipo de cada dispositivo individual dependente de números de série e uma chave separada, permitiu o cegamento de sujeitos e pesquisadores até o final da participação, protegendo assim a v...
Divulgações
Os autores declaram que não têm interesses financeiros concorrentes conhecidos ou relacionamentos pessoais que possam ter influenciado o trabalho relatado neste artigo. As opiniões expressas neste artigo são de responsabilidade dos autores e não refletem necessariamente a posição ou política do Departamento de Assuntos de Veteranos ou do governo dos Estados Unidos.
Agradecimentos
Os autores gostariam de agradecer o apoio dos investigadores do Centro de Reabilitação Visual e Neurocognitiva, incluindo o Dr. Bruce Crosson e a Dra. Lisa Krishnamurthy, por sua contribuição para o trabalho. Os autores também agradecem a Grace Ingham por sua inestimável ajuda no processo de filmagem. Este trabalho foi apoiado em parte pelo Prêmio de Desenvolvimento de Carreira do Serviço de Pesquisa e Desenvolvimento de Pesquisa e Desenvolvimento do Departamento de Assuntos de Veteranos dos Estados Unidos IK2 RX003227 (Anna Woodbury) e Center Grant 5I50RX002358. O financiador não tem nenhum papel no desenho do estudo, coleta de dados, gerenciamento, análise, interpretação ou relatório.
Materiais
| Name | Company | Catalog Number | Comments |
| 3T Siemens MAGNETOM Prisma Scanner | Siemens Healthineers | N/A | From Emory's website: "The Siemens Magnetom Prisma 3T whole-body MR system is equipped with: a state-of-the art gradient system with a maximum (per axis) strength of 80 mT/m and slew rate of 200 T/m/sec 64 independent RF receiver channels capable of 204 receiver connections a 2-channel RF transmitter. Multiple coils are available, including: a 64-channel head/neck coil with 52 channels for imaging of the head region a 32-channel head-only coil a 20-channel head/neck coil with 16 channels for head spine array coil flexible chest coil large and small flexible coil for extremity imaging. |
| Alpha-Stim AID Kit | Electromedical Products International Inc. | SKU: 500KIT | A total of 50 devices ordered for research purposes. From the site: "A prescription or order from a licensed healthcare professional is required to purchase this device (within the USA). FDA cleared for anxiety, insomnia and pain only, with approval for depression outside of the United States." |
| CONN Toolbox v21a16 (RRID:SCR_009550) | Whitfield-Gabrieli and Nieto-Castanon | Version v21a16 (RRID:SCR_009550) | CONN is an open-source SPM-based cross-platform software for the computation, display, and analysis of functional connectivity Magnetic Resonance Imaging (fcMRI). CONN is used to analyze resting state data (rsfMRI) as well as task-related designs. |
| DSI Studio (RRID:SCR_009557) | Fang-Cheng (Frank) Yeh | RRID:SCR_009557 | DSI Studio is a tractography software tool that maps brain connections and correlates findings with neuropsychological disorders. It is a collective implementation of several diffusion MRI methods, including diffusion tensor imaging (DTI), generalized q-sampling imaging (GQI), q-space diffeomorphic reconstruction (QSDR), diffusion MRI connectometry, and generalized deterministic fiber tracking. |
| fMRIPrep 20.2.5 (RRID:SCR_016216) | NiPreps (NeuroImaging PREProcessing tools) | Version 20.2.5. (RRID:SCR_016216) | A functional magnetic resonance imaging (fMRI) data preprocessing pipeline that is designed to provide an easily accessible, state-of-the-art interface that is robust to variations in scan acquisition protocols and that requires minimal user input, while providing easily interpretable and comprehensive error and output reporting. It performs basic processing steps (coregistration, normalization, unwarping, noise component extraction, segmentation, skull-stripping, etc.) providing outputs that can be easily submitted to a variety of group level analyses, including task-based or resting-state fMRI, graph theory measures, and surface or volume-based statistics. |
| MRIQC | NiPreps (NeuroImaging PREProcessing tools) | MRIQC extracts no-reference IQMs (image quality metrics) from structural (T1w and T2w) and functional MRI (magnetic resonance imaging) data. (not directly used for analyses) | |
| Sammons Preston Jamar Hydraulic Hand Dynamometer | Alpha Med Inc. | SKU SAMP5030J1 | From the website: Ideal for routine screening of grip strength and initial and ongoing evaluation of clients with hand trauma and dysfunction. Unit comes with carrying/storage case, certificate of calibration and complete instructions. Warranted for one full year. The warranty does not cover calibration. Latex free. |
| SPRI 5-Pound Vinyl-Coated Weight | SPRI | Amazon | N/A | Color: (E) Dark Blue | 5-Pound. Appears on Amazon: Dumbbells Hand Weights Set of 2 - Vinyl Coated Exercise & Fitness Dumbbell for Home Gym Equipment Workouts Strength Training Free Weights for Women, Men (1-10 Pound, 12, 15, 18, 20 lb), https://www.amazon.com/stores/SPRI/Weights/page/9D10835A-CFAB-4DA1-BEE9-AE993C6B5BC1 |
| SPRI 8-Pound Vinyl-Coated Weight | SPRI | Amazon | N/A | Color: (H) Black |8-Pound. Appears on Amazon: Dumbbells Hand Weights Set of 2 - Vinyl Coated Exercise & Fitness Dumbbell for Home Gym Equipment Workouts Strength Training Free Weights for Women, Men (1-10 Pound, 12, 15, 18, 20 lb), https://www.amazon.com/stores/SPRI/Weights/page/9D10835A-CFAB-4DA1-BEE9-AE993C6B5BC1 |
Referências
- Heidari, F., Afshari, M., Moosazadeh, M. Prevalence of fibromyalgia in general population and patients, a systematic review and meta-analysis. Rheumatology International. 37 (9), 1527-1539 (2017).
- Dennis, N. L., Larkin, M., Derbyshire, S. W. G. A giant mess' - making sense of complexity in the accounts of people with fibromyalgia. British Journal of Health Psychology. 18 (4), 763-781 (2013).
- Woodbury, A. Opioids for nonmalignant chronic pain. AMA Journal of Ethics. 17 (3), 202-208 (2015).
- Hedegaard, H., Minino, A. M., Spencer, M. R., Warner, M. Drug overdose deaths in the United States, 1999-2020. NCHS Data Brief. 428, 1-8 (2021).
- Department of Veterans Affairs. Opioid prescribing to high-risk veterans receiving VA purchased care. Office of Healthcare Inspections. , (2017).
- Perry, R., Leach, V., Davies, P., Penfold, C., Ness, A., Churchill, R. An overview of systematic reviews of complementary and alternative therapies for fibromyalgia using both AMSTAR and ROBIS as quality assessment tools. Systematic Reviews. 6 (1), 97 (2017).
- Martinez-Lavin, M., Hermosillo, A. G. Dysautonomia in Gulf War syndrome and in fibromyalgia. The American Journal of Medicine. 118 (4), 446 (2005).
- Petersel, D. L., Dror, V., Cheung, R. Central amplification and fibromyalgia: disorder of pain processing. Journal of Neuroscience Research. 89 (1), 29-34 (2011).
- Marlow, N. M., Bonilha, H. S., Short, E. B. Efficacy of transcranial direct current stimulation and repetitive transcranial magnetic stimulation for treating fibromyalgia syndrome: A systematic review. Pain Practice. 13 (2), 131-145 (2013).
- Molero-Chamizo, A., et al. Noninvasive transcutaneous vagus nerve stimulation for the treatment of fibromyalgia symptoms: A study protocol. Brain sciences. 12 (1), 95 (2022).
- Cimpianu, C. L., et al. Vagus nerve stimulation in psychiatry: A systematic review of the available evidence. Journal of Neural Transmission. 124 (1), 145-158 (2017).
- Napadow, V., et al. Evoked pain analgesia in chronic pelvic pain patients using respiratory-gated auricular vagal afferent nerve stimulation. Pain Medicine (Malden, Mass). 13 (6), 777-789 (2012).
- Zhang, Y., et al. Transcutaneous auricular vagus nerve stimulation (taVNS) for migraine: an fMRI study. Regional Anesthesia and Pain Medicine. 46 (2), 145-150 (2021).
- Tassorelli, C., et al. Noninvasive vagus nerve stimulation as acute therapy for migraine: The randomized PRESTO study. Neurology. 91 (4), e364-e373 (2018).
- NBC4 Washington - Electrotherapy Device Treats Anxiety, Insomnia, Depression. Alpha-Stim Available from: https://alpha-stim.com/blog/nbc4-washington-electrotherapy-device-treats-anxiety-insomnia-depression/ (2021)
- Taylor, A. G., Anderson, J. G., Riedel, S. L., Lewis, J. E., Bourguignon, C. A randomized, controlled, double-blind pilot study of the effects of cranial electrical stimulation on activity in brain pain processing regions in individuals with fibromyalgia. Explore (NY). 9 (1), 32-40 (2013).
- Taylor, A. G., Anderson, J. G., Riedel, S. L., Lewis, J. E., Kinser, P. A., Bourguignon, C. Cranial electrical stimulation improves symptoms and functional status in individuals with fibromyalgia. Pain Management Nursing. 14 (4), 327-335 (2013).
- Lichtbroun, A. S., Raicer, M. M., Smith, R. B. The treatment of fibromyalgia with cranial electrotherapy stimulation. Journal of Clinical Rheumatology. 7 (2), 72-78 (2001).
- Shekelle, P. G., Cook, I. A., Miake-Lye, I. M., Booth, M. S., Beroes, J. M., Mak, S. Benefits and harms of cranial electrical stimulation for chronic painful conditions, depression, anxiety, and insomnia: A systematic review. Annals of Internal Medicine. 168 (6), 414-421 (2018).
- Dailey, D. L., et al. Perceived function and physical performance are associated with pain and fatigue in women with fibromyalgia. Arthritis Research & Therapy. 18, 68 (2016).
- Gowans, S. E., deHueck, A., Voss, S., Silaj, A., Abbey, S. E., Reynolds, W. J. Effect of a randomized, controlled trial of exercise on mood and physical function in individuals with fibromyalgia. Arthritis & Rheumatism. 45 (6), 519-529 (2001).
- Jones, J., Rutledge, D. N., Jones, K. D., Matallana, L., Rooks, D. S. Self-Assessed physical function levels of women with fibromyalgia: A national survey. Women's Health Issues. 18 (5), 406-412 (2008).
- Rikli, R. E., Jones, C. J. Development and validation of criterion-referenced clinically relevant fitness standards for maintaining physical independence in later years. The Gerontologist. 53 (2), 255-267 (2013).
- Feusner, J. D., et al. Effects of cranial electrotherapy stimulation on resting state brain activity. Brain and Behavior. 2 (3), 211-220 (2012).
- Harris, R. E., et al. Pregabalin rectifies aberrant brain chemistry, connectivity, and functional response in chronic pain patients. Anesthesiology. 119 (6), 1453 (2013).
- Napadow, V., Harris, R. E. What has functional connectivity and chemical neuroimaging in fibromyalgia taught us about the mechanisms and management of 'centralized' pain. Arthritis Research & Therapy. 16 (5), 425 (2014).
- Schroeder, M. J., Barr, R. E. Quantitative analysis of the electroencephalogram during cranial electrotherapy stimulation. Clinical Neurophysiology. 112 (11), 2075-2083 (2001).
- Cordes, D., et al. Mapping functionally related regions of brain with functional connectivity MR imaging. American Journal of Neuroradiology. 21 (9), 1636 (2000).
- Hassett, A. L., Aquino, J. K., Ilgen, M. A. The risk of suicide mortality in chronic pain patients. Current Pain and Headache Reports. 18 (8), 436 (2014).
- Stenager, E., Christiansen, E., Handberg, G., Jensen, B. Suicide attempts in chronic pain patients. A register-based study. Scandinavian Journal of Pain. 5 (1), 4-7 (2014).
- Woodbury, A., et al. Feasibility of auricular field stimulation in fibromyalgia: Evaluation by functional magnetic resonance imaging, randomized trial. Pain Medicine. 22 (3), 715-726 (2021).
- Wolfe, F., et al. Revisions to the 2010/2011 fibromyalgia diagnostic criteria. Seminars in Arthritis and Rheumatism. 46 (3), 319-329 (2016).
- Polomano, R. C., et al. Psychometric testing of the defense and veterans pain rating scale (DVPRS): A new pain scale for military population. Pain Medicine. 17 (8), 1505-1519 (2016).
- Electromedical Products International, Inc. Scientific and clinical literature examination for the Alpha-Stim M microcurrent and cranial electrotherapy stimulator. Electromedical Products International, Inc. , (2016).
- Lein, D. H., Alotaibi, M., Almutairi, M., Singh, H. Normative reference values and validity for the 30-second chair-stand test in healthy young adults. International Journal of Sports Physical Therapy. 17 (5), 907 (2022).
- Revicki, D. A., Cook, K. F., Amtmann, D., Harnam, N., Chen, W. H., Keefe, F. J. Exploratory and confirmatory factor analysis of the PROMIS pain quality item bank. Quality of Life Research. 23 (1), 245-255 (2014).
- Tustison, N. J., et al. N4ITK: improved N3 bias correction. IEEE Transactions on Medical Imaging. 29 (6), 1310 (2010).
- Avants, B. B., Epstein, C. L., Grossman, M., Gee, J. C. Symmetric diffeomorphic image registration with cross-correlation: evaluating automated labeling of elderly and neurodegenerative brain. Medical Image Analysis. 12 (1), 26-41 (2008).
- Zhang, Y., Brady, M., Smith, S. Segmentation of brain MR images through a hidden Markov random field model and the expectation-maximization algorithm. IEEE Transactions on Medical Imaging. 20 (1), 45 (2001).
- Dale, A. M., Fischl, B., Sereno, M. I. Cortical surface-based analysis: I. Segmentation and surface reconstruction. NeuroImage. 9 (2), 179-194 (1999).
- Klein, A., et al. Mindboggling morphometry of human brains. PLoS Computational Biology. 13 (2), 1005350 (2017).
- Fonov, V. S., Evans, A. C., McKinstry, R. C., Almli, C. R., Collins, D. L. Unbiased nonlinear average age-appropriate brain templates from birth to adulthood. NeuroImage. 47, 102 (2009).
- Evans, A. C., Janke, A. L., Collins, D. L., Baillet, S. Brain templates and atlases. NeuroImage. 62 (2), 911-922 (2012).
- Greve, D. N., Fischl, B. Accurate and robust brain image alignment using boundary-based registration. NeuroImage. 48 (1), 63-72 (2009).
- Jenkinson, M., Bannister, P., Brady, M., Smith, S. Improved optimization for the robust and accurate linear registration and motion correction of brain images. NeuroImage. 17 (2), 825 (2002).
- Cox, R. W., Hyde, J. S. Software tools for analysis and visualization of fMRI data. NMR in Biomedicine. 10 (4-5), 171-178 (1997).
- Pruim, R. H. R., Mennes, M., van Rooij, D., Llera, A., Buitelaar, J. K., Beckmann, C. F. ICA-AROMA: A robust ICA-based strategy for removing motion artifacts from fMRI data. NeuroImage. 112, 267-277 (2015).
- Power, J. D., Mitra, A., Laumann, T. O., Snyder, A. Z., Schlaggar, B. L., Petersen, S. E. Methods to detect, characterize, and remove motion artifact in resting state fMRI. NeuroImage. 84, 320-341 (2014).
- Behzadi, Y., Restom, K., Liau, J., Liu, T. T. A component based noise correction method (CompCor) for BOLD and perfusion based fMRI. NeuroImage. 37 (1), 90-101 (2007).
- Satterthwaite, T. D., et al. An improved framework for confound regression and filtering for control of motion artifact in the preprocessing of resting-state functional connectivity data. NeuroImage. 64, 240-256 (2013).
- Lanczos, C. Evaluation of noisy data. Journal of the Society for Industrial and Applied Mathematics Series B Numerical Analysis. 1 (1), (1964).
- Oscar, E., et al. fMRIPrep: A robust preprocessing pipeline for functional MRI. Nature Methods. 16, 111-116 (2019).
- Oscar, E., et al. FMRIPrep. Software. Zenodo. , (2018).
- Gorgolewski, K. J., et al. Nipype: a flexible, lightweight and extensible neuroimaging data processing framework in python. Frontiers in Neuroinformatics. 5, 13 (2011).
- Gorgolewski, K. J., et al. Nipype. Software. Zenodo. , (2018).
- Abraham, A., et al. Machine learning for neuroimaging with scikit-learn. Frontiers in Neuroinformatics. 8, 14 (2014).
- Yeh, F. -. C., Badre, D., Verstynen, T. Connectometry: A statistical approach harnessing the analytical potential of the local connectome. NeuroImage. 125 (2016), 162-171 (2015).
- Andersson, J. L. R., Skare, S., Ashburner, J. How to correct susceptibility distortions in spin-echo echo-planar images: application to diffusion tensor imaging. NeuroImage. 20 (2), 870-888 (2003).
- Smith, S. M., et al. Advances in functional and structural MR image analysis and implementation as FSL. NeuroImage. 23, 208-219 (2004).
- Andersson, J. L. R., Sotiropoulos, S. N. An integrated approach to correction for off-resonance effects and subject movement in diffusion MR imaging. NeuroImage. 125, 1063-1078 (2016).
- Yeh, F. -. C., Tseng, W. -. Y. I. NTU-90: a high angular resolution brain atlas constructed by -q-space diffeomorphic reconstruction. Neuroimage. 58 (1), 91-99 (2011).
- Nieto-Castanon, A. . Cluster-Level Inferences. Handbook of Functional Connectivity Magnetic Resonance Imaging Methods in CONN. , (2020).
- Hemington, K. S., Wu, Q., Kucyi, A., Inman, R. D., Davis, K. D. Abnormal cross-network functional connectivity in chronic pain and its association with clinical symptoms. Brain Structure & Function. 221 (8), 4203-4219 (2016).
- Ichesco, E., et al. Altered resting state connectivity of the insular cortex in individuals with fibromyalgia. Journal of Pain. 15 (8), 815-826 (2014).
- Kim, J., et al. The somatosensory link in fibromyalgia: functional connectivity of the primary somatosensory cortex is altered by sustained pain and is associated with clinical/autonomic dysfunction. Arthritis & Rheumatology. 67 (5), 1395-1405 (2015).
- Napadow, V., LaCount, L., Park, K., As-Sanie, S., Clauw, D. J., Harris, R. E. Intrinsic brain connectivity in fibromyalgia is associated with chronic pain intensity. Arthritis and Rheumatism. 62 (8), 2545-2555 (2010).
- Napadow, V., Kim, J., Clauw, D. J., Harris, R. E. Decreased intrinsic brain connectivity is associated with reduced clinical pain in fibromyalgia. Arthritis and Rheumatism. 64 (7), 2398-2403 (2012).
- Puiu, T., et al. Association of alterations in gray matter volume with reduced evoked-pain connectivity following short-term administration of pregabalin in patients with fibromyalgia. Arthritis & Rheumatology. 68 (6), 1511-1521 (2016).
- Fallon, N., Chiu, Y., Nurmikko, T., Stancak, A. Functional Connectivity with the default mode network is altered in fibromyalgia patients. PLoS One. 11 (7), 0159198 (2016).
- Wang, Y., Kang, J., Kemmer, P. B., Guo, Y. An efficient and reliable statistical method for estimating functional connectivity in large scale brain networks using partial correlation. Frontiers in Neuroscience. 10, 123 (2016).
- Mease, P. J., et al. Estimation of minimum clinically important difference for pain in fibromyalgia. Arthritis Care and Research (Hoboken). 63 (6), 821-826 (2011).
- Bingel, U., et al. Somatotopic organization of human somatosensory cortices for pain: a single trial fMRI study). NeuroImage. 23 (1), 224-232 (2004).
- Wager, T. D., et al. Pain in the ACC. Proceedings of the National Academy of Sciences of the United States of America. 113 (18), E2474-E2475 (2016).
- Nieto-Castanon, A. . FMRI Denoising Pipeline. Handbook of Functional Connectivity Magnetic Resonance Imaging Methods in CONN. , (2020).
- Friston, K. J., Williams, S., Howard, R., Frackowiak, R. S., Turner, R. Movement-related effects in fMRI time-series. Magnetic Resonance in Medicine. 35 (3), 346-355 (1996).
- Hallquist, M. N., Hwang, K., Luna, B. The nuisance of nuisance regression: spectral misspecification in a common approach to resting-state fMRI preprocessing reintroduces noise and obscures functional connectivity. NeuroImage. 82, 208-225 (2013).
- Chai, X. J., Nieto-Castanon, A., Ongur, D., Whitfield-Gabrieli, S. Anticorrelations in resting state networks without global signal regression. NeuroImage. 59 (2), 1420-1428 (2012).
- Nieto-Castanon, A. . General Linear Model. Handbook of Functional Connectivity Magnetic Resonance Imaging Methods in CONN. , (2020).
- Worsley, K. J., Marrett, S., Neelin, P., Vandal, A. C., Friston, K. J., Evans, A. C. A unified statistical approach for determining significant signals in images of cerebral activation. Human Brain Mapping. 4 (1), 58-73 (1996).
- Chumbley, J., Worsley, K., Flandin, G., Friston, K. Topological FDR for neuroimaging. NeuroImage. 49 (4), 3057-3064 (2010).
- Page, S. J., Persch, A. C. Recruitment, retention, and blinding in clinical trials. The American Journal of Occupational Therapy. 67 (2), 154-161 (2013).
- McGrath, R. E., Mitchell, M., Kim, B. H., Hough, L. Evidence for response bias as a source of error variance in applied assessment. Psychological Bulletin. 136 (3), 450 (2010).
- Robinson-Papp, J., George, M. C., Dorfman, D., Simpson, D. M. Barriers to chronic pain measurement: A qualitative study of patient perspectives. Pain Medicine. 16 (7), 1256-1264 (2015).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados
Usamos cookies para melhorar sua experiência em nosso site.
Ao continuar usando nosso site ou clicando em 'continuar', você concorda em aceitar nossos cookies.