È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Misurazione della capacità di diffusione polmonare del gas a doppio test durante l'esercizio fisico nell'uomo utilizzando il metodo del respiro singolo
In questo articolo
Riepilogo
Questo protocollo presenta un metodo per valutare la riserva alveolare-capillare polmonare misurata mediante la misurazione combinata a respiro singolo della capacità di diffusione al monossido di carbonio (D,L,CO) e all'ossido nitrico (D, L,NO) durante l'esercizio. I presupposti e le raccomandazioni per l'uso della tecnica durante l'esercizio costituiscono la base di questo articolo.
Abstract
La misurazione combinata a respiro singolo della capacità di diffusione del monossido di carbonio (D,L, CO) e dell'ossido nitrico (D,L, NO) è una tecnica utile per misurare la riserva alveolare-capillare polmonare sia nella popolazione sana che in quella dei pazienti. La misurazione fornisce una stima della capacità del partecipante di reclutare e distendere i capillari polmonari. Il metodo è stato recentemente segnalato per mostrare un'elevata affidabilità test-retest in volontari sani durante l'esercizio di intensità da leggera a moderata. Da notare che questa tecnica consente fino a 12 manovre ripetute e richiede solo un singolo respiro con un tempo di apnea relativamente breve di 5 secondi. Vengono forniti dati rappresentativi che mostrano le variazioni graduali di DL, NO e DL,CO dal riposo all'esercizio a intensità crescenti fino al 60% del carico di lavoro massimo. La misurazione della capacità di diffusione e la valutazione della riserva alveolo-capillare è uno strumento utile per valutare la capacità del polmone di rispondere all'esercizio sia nella popolazione sana che in quella di pazienti come quelli con malattia polmonare cronica.
Introduzione
L'esercizio fisico porta ad un notevole aumento della domanda di energia rispetto allo stato di riposo. Il cuore e i polmoni rispondono aumentando la gittata cardiaca e la ventilazione con conseguente espansione del letto alveolare-capillare, principalmente il reclutamento e la distensione dei capillari polmonari1. Ciò garantisce un sufficiente scambio gassoso polmonare, che può essere misurato da un aumento della capacità di diffusione polmonare (DL)2,3,4. I primi tentativi di misurareD L durante l'esercizio risalgono a più di un secolo fa 5,6,7. La capacità di aumentare la DL dallo stato di riposo è spesso indicata come riserva alveolare-capillare 8,9.
Sperimentalmente, i contributi relativi della capacità di diffusione della membrana alveolare-capillare (DM) e del volume ematico capillare polmonare (VC) alla riserva alveolo-capillare possono essere valutati con diversi metodi, incluso il classico metodo delle frazioni multiple di ossigeno inspirato (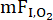 )10. Una tecnica alternativa che può essere utile in questo contesto è il metodo del gas a doppia prova, in cuiil DL in monossido di carbonio (CO) e ossido nitrico (NO) (DL,CO/NO) sono misurati contemporaneamente11. Questa tecnica è stata sviluppata negli anni '80 e sfrutta il fatto che la velocità di reazione dell'NO con l'emoglobina (Hb) è sostanzialmente maggiore di quella del CO, in modo tale che la diffusione polmonare del CO dipende più dal VC che dal NO. Quindi, il principale sito di resistenza (~75%) alla diffusione del CO si trova all'interno del globulo rosso, mentre la principale resistenza (~60%) alla diffusione di NO è a livello della membrana alveolare-capillare e del plasma polmonare12. La misurazione simultanea di DL,CO e DL,NO consente quindi di valutare i contributi relativi di DM e VC a DL12, dove la variazione di DL,NO osservata durante l'esercizio riflette quindi in gran parte l'espansione della membrana alveolare-capillare. Un ulteriore vantaggio di questo metodo quando si ottengono misurazioni durante l'esercizio è che comporta un tempo di apnea relativamente breve (~5 s) e meno manovre rispetto alla tecnica classica
)10. Una tecnica alternativa che può essere utile in questo contesto è il metodo del gas a doppia prova, in cuiil DL in monossido di carbonio (CO) e ossido nitrico (NO) (DL,CO/NO) sono misurati contemporaneamente11. Questa tecnica è stata sviluppata negli anni '80 e sfrutta il fatto che la velocità di reazione dell'NO con l'emoglobina (Hb) è sostanzialmente maggiore di quella del CO, in modo tale che la diffusione polmonare del CO dipende più dal VC che dal NO. Quindi, il principale sito di resistenza (~75%) alla diffusione del CO si trova all'interno del globulo rosso, mentre la principale resistenza (~60%) alla diffusione di NO è a livello della membrana alveolare-capillare e del plasma polmonare12. La misurazione simultanea di DL,CO e DL,NO consente quindi di valutare i contributi relativi di DM e VC a DL12, dove la variazione di DL,NO osservata durante l'esercizio riflette quindi in gran parte l'espansione della membrana alveolare-capillare. Un ulteriore vantaggio di questo metodo quando si ottengono misurazioni durante l'esercizio è che comporta un tempo di apnea relativamente breve (~5 s) e meno manovre rispetto alla tecnica classica 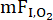 , in cui vengono eseguite più manovre ripetute con una apnea standardizzata di 10 s a diversi livelli di ossigeno. Anche se
, in cui vengono eseguite più manovre ripetute con una apnea standardizzata di 10 s a diversi livelli di ossigeno. Anche se 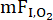 recentemente è stato applicato con un tempo di apnea più breve e meno manovre ad ogni intensità13. Ciononostante,
recentemente è stato applicato con un tempo di apnea più breve e meno manovre ad ogni intensità13. Ciononostante, 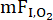 consente solo un totale di sei manovre DL,CO per sessione, mentre è possibile eseguire fino a 12 manovre DL,CO/NO ripetute senza alcun effetto misurabile sulle stime risultanti14. Queste sono considerazioni importanti quando si ottengono misurazioni durante l'esercizio poiché sia una lunga apnea che più manovre possono essere difficili da eseguire a intensità molto elevate o in popolazioni di pazienti che soffrono di dispnea.
consente solo un totale di sei manovre DL,CO per sessione, mentre è possibile eseguire fino a 12 manovre DL,CO/NO ripetute senza alcun effetto misurabile sulle stime risultanti14. Queste sono considerazioni importanti quando si ottengono misurazioni durante l'esercizio poiché sia una lunga apnea che più manovre possono essere difficili da eseguire a intensità molto elevate o in popolazioni di pazienti che soffrono di dispnea.
Il presente lavoro fornisce un protocollo dettagliato, che include considerazioni teoriche e raccomandazioni pratiche sulla misurazione di DL,CO/NO durante l'esercizio e il suo utilizzo come indice della riserva alveolare-capillare. Questo metodo è facilmente applicabile in ambito sperimentale e permette di valutare come la limitazione della diffusione nei polmoni possa influenzare l'assorbimento di ossigeno in diverse popolazioni.
Teoria e principi di misura
Il metodo DL,CO/NO prevede un singolo respiro di una miscela di gas con l'ipotesi che i gas si distribuiscano equamente nello spazio alveolare ventilato dopo l'inalazione. La miscela di gas è costituita da diversi gas tra cui un gas tracciante inerte. La diluizione del gas tracciante nello spazio alveolare ventilato, in base alla sua frazione in aria di fine espirazione, può essere utilizzata per calcolare il volume alveolare (VA)15. La miscela di gas comprende anche i gas di prova CO e NO, entrambi diluiti nello spazio alveolare ventilato e diffusi attraverso la membrana alveolare-capillare. Sulla base delle loro frazioni alveolari, è possibile calcolare i loro tassi individuali di scomparsa (k), chiamati anche costanti di diffusione, dallo spazio alveolare. Per convenzione, la DL per un gas di prova misurato durante una manovra a respiro singolo, è derivata dalla seguente equazione16:
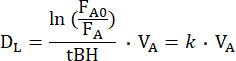
dove FA0 è la frazione alveolare del gas di prova (CO o NO) all'inizio della apnea della singola manovra DL , mentre FA è la frazione alveolare del gas di prova alla fine dell'apnea e tBH è il tempo di apnea. D L è meccanicamente equivalente alla conduttanza del gas di prova attraverso la membrana alveolare-capillare, attraverso il plasma e l'interno dei globuli rossi fino all'emoglobina. Dipende quindi sia dalla conduttanza di DM che dalla cosiddetta conduttanza specifica del sangue capillare polmonare (θ), di cui quest'ultima dipende sia dalla conduttanza del gas in esame nel sangue che dalla sua velocità di reazione con l'emoglobina10. Dato che il reciproco di conduttanza è la resistenza, la resistenza totale al trasferimento di un gas di prova dipende dalle seguenti resistenze della serie10:
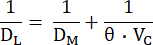
Queste componenti possono essere distinte misurando contemporaneamente il valore di DL a CO e NO, perché questi hanno valori θ diversi e i loro rispettivi valori di DL dipendono quindi in modo diverso da VC. La diffusione polmonare del CO dipende più pesantemente dal VC rispetto al NO, con il principale sito di resistenza (~75%) alla diffusione del CO che si trova all'interno del globulo rosso12. Al contrario, la principale resistenza (~60%) alla diffusione dell'NO è a livello della membrana alveolare-capillare e del plasma polmonare, perché la velocità di reazione dell'NO con l'emoglobina è sostanzialmente maggiore di quella del CO. Quindi, misurando contemporaneamente DL,CO e DL,NO, i cambiamenti sia in DM che in VC influenzeranno notevolmente il primo, mentre quest'ultimo dipenderà molto meno da VC, consentendo così una valutazione integrativa dei fattori che determinano DL.
La segnalazione delle metriche DL, CO/NO può essere effettuata utilizzando unità diverse. Quindi, la European Respiratory Society (ERS) utilizza mmol/min/kPa, mentre l'American Thoracic Society (ATS) utilizza mL/min/mmHg. Il fattore di conversione tra le unità è 2,987 mmol/min/kPa = mL/min/mmHg.
Protocollo
Il Comitato Etico Scientifico per la Regione della Capitale della Danimarca ha precedentemente approvato la misurazione di DL,CO/NO a riposo, durante l'esercizio fisico e in posizione supina sia in volontari sani che in pazienti con broncopneumopatia cronica ostruttiva (BPCO) presso il nostro istituto (protocolli H-20052659, H-21021723 e H-21060230).
NOTA: Prima di misurareD L, CO/NO durante l'esercizio, è necessario eseguire una spirometria dinamica e un test da sforzo cardiopolmonare (CPET). La spirometria dinamica viene utilizzata per il controllo di qualità delle singole manovre DL,CO/NO, mentre la CPET viene utilizzata per determinare il carico di lavoro al quale DL,CO/NO deve essere misurato durante l'esercizio. Nei pazienti con limitazione del flusso d'aria, in particolare a causa di malattia polmonare ostruttiva, può essere vantaggioso integrare la spirometria dinamica con una pletismografia di tutto il corpo per ottenere una valida misura della capacità vitale. Si raccomanda un controllo medico sanitario per escludere eventuali controindicazioni note prima di iniziare la CPET17. È importante sottolineare che il CPET deve essere eseguito almeno 48 ore prima della misurazione DL,CO/NO ottenuta durante l'esercizio, poiché un precedente esercizio vigoroso può influenzareD L per almeno 24 ore18,19.
1. Spirometria dinamica
NOTA: La spirometria dinamica deve essere eseguita in conformità con le attuali linee guida cliniche dell'ERS e dell'ATS20.
- Misurare il peso (con l'approssimazione di 100 g) e l'altezza (con l'approssimazione di 1 mm).
- Chiedi al partecipante di sedersi su una sedia verticale.
- Eseguire una spirometria dinamica durante una manovra di espirazione forzata per identificare il volume forzato espirato, in 1 s (FEV1) e la capacità vitale forzata (FVC) del partecipante, come descritto altrove20.
2. Test da sforzo cardiopolmonare (CPET)
NOTA: La CPET deve essere eseguita in linea con le attuali raccomandazioni cliniche21.
- Regolare il cicloergometro in base all'altezza del partecipante e posizionare un cardiofrequenzimetro (FC) sul petto.
- Posizionare il partecipante sul cicloergometro. Dotare il partecipante di una maschera collegata a un sistema di misurazione metabolica, per misurare la ventilazione e lo scambio gassoso polmonare durante tutto il test.
- Chiedi al partecipante di iniziare a pedalare a un ritmo autoselezionato ≥60 round al minuto (RPM) ed eseguire un periodo di riscaldamento di 5 minuti con un carico di lavoro submassimale in base al livello di attività auto-riferito, alla forma fisica giornaliera e allo stato della malattia (ad esempio, 15-150 W).
- Aumentare il carico di lavoro di 5-20 W ogni minuto fino a quando il partecipante non raggiunge l'esaurimento volontario. Gli incrementi dovrebbero essere basati sull'attuale livello di forma fisica del partecipante, in modo che il test dovrebbe terminare 8-12 minuti dopo l'inizio della fase incrementale.
- Istruire il partecipante ad evitare altri esercizi vigorosi per le successive 48 ore.
3. Taratura dell'apparecchiatura a capacità di diffusione del respiro singolo
NOTA: È necessario calibrare i sensori di flusso e gli analizzatori di gas per garantire che le misurazioni siano valide e affidabili. La procedura esatta è specifica del produttore e del dispositivo. La procedura di taratura, compresa la lotta biologica, deve essere completata in ogni giorno di studio e, se viene eseguito meno di un giorno di studio alla settimana, devono essere effettuate ulteriori tarature settimanali. La configurazione sperimentale è mostrata nella Figura 1.
- Aprire il programma software sul computer e verrà avviato un periodo di riscaldamento automatico di 50 minuti per garantire una temperatura sufficiente dello pneumotaco.
- Assicurarsi che i contenitori con i gas di prova siano aperti (vedere la figura 1D).
- Eseguire una calibrazione del gas collegando prima la linea di campionamento dallo pneumotach al plug-in dell'unità di analisi MS-PFT denominato CAL (vedere la Figura 1B).
- Avviare la calibrazione del gas selezionando Calibrazione nella Home Page (vedere la Figura 2A) e scegliere Calibrazione del gas. Avviare la calibrazione premendo Start o F1 (vedere la Figura 2B).
- Collegare la linea di campionamento allo pneumotach quando la calibrazione del gas è stata completata e accettata.
- Eseguire una calibrazione del volume utilizzando una siringa valida da 3 L. Avviare la calibrazione del volume selezionando Calibrazione nella Home Page (vedere la Figura 2A) e scegliere Calibrazione volume. Avviare la calibrazione premendo F1 e seguire le istruzioni fornite dal software (vedere la Figura 2C).
- Assicurarsi che la sacca inspiratoria sia collegata all'unità analizzatore MS-PFT (vedere la Figura 1C).
- Completare la procedura di taratura eseguendo una misurazione di controllo biologico a riposo in posizione seduta. Questo dovrebbe essere eseguito da un non fumatore sano per garantire l'affidabilità del metodo. Se la variazione settimanale di DL,CO o DL,NO varia di settimana in settimana del soggetto in questione più di 1,6 e 6,5 mmol/min/kPa (5 e 20 mL/min/mmHg), rispettivamente, la variazione può essere dovuta a un errore della macchina e deve essere ulteriormente studiata12, 22.
4. Preparazione del partecipante
- Calcolare il carico di lavoro desiderato dai risultati CPET precedenti per l'intensità scelta (% del carico di lavoro massimo (Wmax)) alla quale verrà misurato il DL,CO/NO .
- Almeno 48 ore dopo che il partecipante ha eseguito la CPET, chiedere al partecipante di tornare in laboratorio per ottenere la misurazione DL,CO/NO durante l'esercizio.
- Misurare l'altezza (in cm fino al mm più vicino), il peso (in kg fino a 100 g più vicino) e l'Hb dal sangue capillare (in mmol/L fino a 0,1 mmol/L) del paziente.
- Nella Home Page del programma scegliere Paziente > Nuovo paziente (Vedi Figura 2A) e inserire i dati richiesti: Identificazione, Cognome, Nome, Data di nascita, Sesso, Altezza e Peso del partecipante. Continuare selezionando OK o F1 (vedere la Figura 2D).
5. Misurazione DL, CO/NO durante il riposo eretto
Nota: Le misurazioni DL,CO/NO vengono eseguite in conformità con le attuali raccomandazioni cliniche della task force12 dell'ERS.
- Nella Home Page scegliere Misura > NO Diffusione a membrana (vedere la Figura 2E).
- Avviare il reset automatico del software, azzerare l'analizzatore di gas per tutti i gas di prova e avviare la miscelazione dei gas di prova nella sacca inspiratoria collegata. Avviare il ripristino automatico premendo F1 (vedere la Figura 2F).
- Il ripristino automatico richiede 140-210 s. Osservare le istruzioni fornite dal software per riconoscere quando avviare la misurazione. È importante avviare immediatamente la misurazione quando il software indica di collegare il paziente.
- Posizionare il partecipante su una sedia verticale dotata di clip per il naso. Istruire il partecipante su come eseguire la manovra come descritto di seguito.
- Chiedere al partecipante di utilizzare la clip nasale e di iniziare le normali respirazioni correnti attraverso un boccaglio collegato allo pneumotachico. Per garantire un sistema chiuso per le misurazioni, assicurarsi che le labbra del partecipante siano tenute chiuse attorno al boccaglio.
- Dopo tre respirazioni normali, istruire il partecipante ad eseguire una rapida espirazione massimale per raggiungere il volume residuo (RV).
- Quando viene raggiunto il ventricolo destro, istruire immediatamente il partecipante a eseguire una rapida inspirazione massimale alla capacità polmonare totale (TLC), mirando a un tempo inspiratorio di < 4 secondi. Durante l'inspirazione massima, una valvola si apre, consentendo al partecipante di inalare la miscela di gas miscelata con una concentrazione nota di NO (800 ppm NO/N2 ) in una sacca inspiratoria appena prima dell'inalazione.
- Chiedere al partecipante di effettuare un'apnea di 5 (4-8) s a TLC. Durante l'inspirazione viene mirato un volume inspirato (VI) ≥90% della FVC (o capacità vitale basata sulla pletismografia) con un tempo di apnea di 4-8 s23 (Tabella 1).
- Dopo l'apnea, istruire il partecipante ad eseguire un'espirazione massima forte e costante senza interruzioni.
- Dopo l'espirazione massima, chiedere al partecipante di lasciare andare il boccaglio e la clip per il naso. Il software calcolerà quindi DL, NO e DL, CO senza alcun comando.
- Usa l'incoraggiamento verbale durante la manovra per assicurarti che il partecipante raggiunga RV e TLC. Valutare l'accettabilità della manovra come da Tabella 1.
- Eseguire nuovamente la manovra dopo un periodo di lavaggio di almeno 4 minuti e fino a quando due manovre soddisfano i criteri di accettabilità (Tabella 1) o fino a quando non sono state eseguite un totale di 12 manovre (vedi sotto) nella stessa sessione.
- I DL,NO e DL,CO sono riportati secondo i criteri delineati nella tabella 2. Si consiglia inoltre di mantenere il tempo di apnea, il volume inspirato e il volume alveolare come riportato. Inoltre, deve essere riportato il numero di manovre accettabili e ripetibili e i risultati basati su manovre che non soddisfano i criteri di accettabilità o ripetibilità devono essere interpretati con cautela.
6. Misurazione DL, CO/NO durante l'esercizio
NOTA: Nella Figura 3 è riportata una cronologia delle misurazioni DL, CO/NO durante l'esercizio.
- Posizionare il cicloergometro a una distanza che consenta al partecipante di respirare attraverso il boccaglio senza dover cambiare la posizione della pedalata. Aumentare l'altezza dell'attrezzatura in modo che le misurazioni possano essere eseguite con una corretta posizione di lavoro sulla bicicletta (Vedi Figura 2).
- Posizionare il partecipante sul cicloergometro e posizionare un monitor della frequenza cardiaca sul petto. Istruire il partecipante a eseguire ogni manovra come descritto al punto 5.3.
- Chiedi al partecipante di iniziare a pedalare per 5 minuti con un carico di lavoro submassimale, come riscaldamento prima della misurazione.
- Aumentare il carico di lavoro fino all'intensità desiderata avviando contemporaneamente il ripristino automatico del dispositivo premendo F1 (vedere il passaggio 5.2). Il ripristino automatico richiede 140-210 s, sufficienti per garantire che il partecipante abbia raggiunto lo stato stazionario.
- Al termine del ripristino automatico, ruotare il boccaglio verso il partecipante ed eseguire una manovra come descritto di seguito mentre il partecipante continua a pedalare all'intensità target.
- Seguire i passaggi da 5.4 a 5.5. Valutare i criteri di accettabilità e ripetibilità (Tabella 1) per ogni carico di lavoro e riferire come per le misurazioni durante il riposo (vedere il passaggio 5.6 e la Tabella 2).
- Al termine della manovra, rimuovere il boccaglio e diminuire il carico di lavoro a 15-40 W. Eseguire la fase di recupero attivo per 2 minuti, dopodiché ripetere i passaggi 6.4 e 6.5. I 2 minuti di recupero attivo e i 140-210 s durante il ripristino automatico forniscono un periodo di lavaggio sufficiente di 4-5 minuti.
Risultati
Il protocollo è stato implementato nel 2021 e al momento in cui scriviamo sono state eseguite un totale di 124 misurazioni durante l'esercizio fisico (ovvero 51 in volontari sani e 73 in pazienti con BPCO di varia gravità). Le manovre, così come i dati sui criteri di accettabilità e ripetibilità soddisfatti e il tasso di guasto sono tutti forniti nella Tabella 3.
Calcoli
A titolo di esempio, i calcoli di una singola manovra DL,CO/...
Discussione
Il protocollo fornisce un approccio standardizzato alla misurazione di DL,CO/NO durante l'esercizio utilizzando la tecnica del doppio test gas a singolo respiro. Poiché i parametri DL,CO/NO ottenuti aumentano a causa del reclutamento e della distensione dei capillari polmonari, il metodo fornisce una misura fisiologicamente significativa della riserva alveolare-capillare.
Passaggi critici del protocollo
Il metodo richiede un'espirazione al volume resi...
Divulgazioni
L'attrezzatura e il software presentati nell'articolo non sono gratuiti. Nessuno degli autori è associato ad alcuna società che fornisce la licenza per il software. Tutti gli autori dichiarano di non avere interessi finanziari concorrenti.
Riconoscimenti
Lo studio ha ricevuto il sostegno finanziario della Fondazione Svend Andersen. Il Centro per la ricerca sull'attività fisica è supportato dalle sovvenzioni TrygFonden ID 101390, ID 20045 e ID 125132. JPH è finanziato da HelseFonden e dall'Ospedale Universitario di Copenaghen, Rigshospitalet, mentre HLH è finanziato dalla Fondazione Beckett.
Materiali
| Name | Company | Catalog Number | Comments |
| HemoCue Hb 201+ | HemoCue, Brønshøj, Denmark | Unkown | For measurements of hemoglobin |
| Jaeger MasterScreen PFT pro (Lung Function Equipment) | CareFusion, Höchberg, Germany | Unkown | For measurements of DLCO/NO |
| Mouthpiece | SpiroBac, Henrotech, Aartselaar, Belgium | Unkown | Used together with the Lung Fuction Equipment. (dead space 56 ml, resistance to flow at 12 L s−1 0.9 cmH2O) |
| Nose-clip | IntraMedic, Gentofte, Denmark | JAE-892895 | |
| Phenumotach | IntraMedic, Gentofte, Denmark | JAE-705048 | Used together with the Lung Fuction Equipment |
| SentrySuite Software Solution | Vyaire's Medical GmbH, Leibnizstr. 7, D-97204 Hoechberg Germany | Unkown | |
| Test gasses | IntraMedic, Gentofte, Denmark | Unkown | Concentrations: 0.28% CO, 20.9% O2, 69.52% N2 and 9.3% He |
Riferimenti
- Johnson Jr, R. L., Heigenhauser, G. J. F., Hsia, C. C., Jones, N. L., Wagner, P. D. Determinants of gas exchange and acid-base balance during exercise. Compr Physiol. , 515-584 (2011).
- Rampulla, C., Marconi, C., Beulcke, G., Amaducci, S. Correlations between lung-transfer factor, ventilation, and cardiac output during exercise. Respiration. 33 (6), 405-415 (1976).
- Tedjasaputra, V., Bouwsema, M. M., Stickland, M. K. Effect of aerobic fitness on capillary blood volume and diffusing membrane capacity responses to exercise. J Physiol. 594 (15), 4359-4370 (2016).
- Tamhane, R. M., Johnson, R. L., Hsia, C. C. W. Pulmonary membrane diffusing capacity and capillary blood volume measured during exercise from nitric oxide uptake. Chest. 120 (6), 1850-1856 (2001).
- Bohr, C. On the determination of gas diffusion through the lungs and its size during rest and work. Zentralblatt für Physiologie. 23 (12), 374-379 (1909).
- Krogh, A., Krogh, M. On the rate of diffusion of carbonic oxide into the lungs of man. Skandinavisches Archiv Für Physiologie. 23 (1), 236-247 (1910).
- Krogh, M. The diffusion of gases through the lungs of man. J Physiol. 49 (4), 271-300 (1915).
- Hsia, C. C., Herazo, L. F., Ramanathan, M., Johnson, R. L. Cardiopulmonary adaptations to pneumonectomy in dogs IV. Membrane diffusing capacity and capillary blood volume. J Appl Physiol. 77 (2), 998-1005 (1994).
- Behnia, M., Wheatley, C. M., Avolio, A., Johnson, B. D. Alveolar-capillary reserve during exercise in patients with chronic obstructive pulmonary disease. Int J Chron Obstruct Pulmon Dis. 12, 3115-3122 (2017).
- Roughton, F. J., Forster, R. E. Relative importance of diffusion and chemical reaction rates in determining rate of exchange of gases in the human lung, with special reference to true diffusing capacity of pulmonary membrane and volume of blood in the lung capillaries. J Appl Physiol. 11 (2), 290-302 (1957).
- Borland, C., Higenbottam, T. A simultaneous single breath measurement of pulmonary diffusing capacity with nitric oxide and carbon monoxide. Eur Respir J. 2 (1), 56-63 (1989).
- Zavorsky, G. S., et al. Standardisation and application of the single-breath determination of nitric oxide uptake in the lung. Eur Respir J. 49 (2), 1600962 (2017).
- Tedjasaputra, V., Van Diepen, S., Collins, S., Michaelchuk, W. M., Stickland, M. K. Assessment of pulmonary capillary blood volume, membrane diffusing capacity, and intrapulmonary arteriovenous anastomoses during exercise. J Vis Exp. (120), e54949 (2017).
- Zavorsky, G. S. The rise in carboxyhemoglobin from repeated pulmonary diffusing capacity tests. Respir Physiol Neurobiol. 186 (1), 103-108 (2013).
- Graham, B. L., et al. ERS/ATS standards for single-breath carbon monoxide uptake in the lung. Eur Respir J. 49 (1), 1600016 (2017).
- Hughes, J. M., Pride, N. B. Examination of the carbon monoxide diffusing capacity (DLCO) in relation to its KCO and VA components. Am J Respir Crit Care Med. 186 (2), 132-139 (2012).
- Balady, G. J., et al. Clinician's guide to cardiopulmonary exercise testing in adults: a scientific statement from the American heart association. Circulation. 122 (2), 191-225 (2010).
- Hanel, B., Clifford, P. S., Secher, N. H. Restricted postexercise pulmonary diffusion capacity does not impair maximal transport for O2. J Appl Physiol. 77 (5), 2408-2412 (1994).
- Sheel, A. W., Coutts, K. D., Potts, J. E., McKenzie, D. C. The time course of pulmonary diffusing capacity for carbon monoxide following short duration high intensity exercise. Respir Physiol. 111 (3), 271-281 (1998).
- Graham, B. L., et al. Standardization of spirometry 2019 update an official American Thoracic Society and European Respiratory Society technical statement. Am J Respir Crit Care Med. 200 (8), e70-e88 (2019).
- Glaab, T., Taube, C. Practical guide to cardiopulmonary exercise testing in adults. Respir Res. 23 (1), 9 (2022).
- Munkholm, M., et al. Reference equations for pulmonary diffusing capacity of carbon monoxide and nitric oxide in adult Caucasians. Eur Respir J. 52 (1), 1500677 (2018).
- Dressel, H., et al. Lung diffusing capacity for nitric oxide and carbon monoxide: dependence on breath-hold time. Chest. 133 (5), 1149-1154 (2008).
- Madsen, A. C., et al. Pulmonary diffusing capacity to nitric oxide and carbon monoxide during exercise and in the supine position: a test-retest reliability study. Exp Physiol. 108 (2), 307-317 (2023).
- Ross, B. A., et al. The supine position improves but does not normalize the blunted pulmonary capillary blood volume response to exercise in mild COPD. J Appl Physiol. 128 (4), 925-933 (2020).
- Zavorsky, G. S., Lands, L. C. Lung diffusion capacity for nitric oxide and carbon monoxide is impaired similarly following short-term graded exercise. Nitric Oxide. 12 (1), 31-38 (2005).
- Alves, M. M., Dressel, H., Radtke, T. Test-retest reliability of lung diffusing capacity for nitric oxide during light to moderate intensity cycling exercise. Respir Physiol Neurobiol. 304, 103940 (2022).
- Jorgenson, C. C., Coffman, K. E., Johnson, B. D. Effects of intrathoracic pressure, inhalation time, and breath hold time on lung diffusing capacity. Respir Physiol Neurobiol. 258, 69-75 (2018).
- Zavorsky, G. S., Quiron, K. B., Massarelli, P. S., Lands, L. C. The relationship between single-breath diffusion capacity of the lung for nitric oxide and carbon monoxide during various exercise intensities. Chest. 125 (3), 1019-1027 (2004).
- Coffman, K. E., Boeker, M. G., Carlson, A. R., Johnson, B. D. Age-dependent effects of thoracic and capillary blood volume distribution on pulmonary artery pressure and lung diffusing capacity. Physiol Rep. 6 (17), e13834 (2018).
- Borland, C. D. R., Hughes, J. M. B. Lung diffusing capacities (DL) for nitric oxide (NO) and carbon monoxide (CO): The evolving story. Compr Physiol. 11 (1), 1371 (2021).
- Tedjasaputra, V., Van Diepen, S., Collins, S. &. #. 2. 0. 1. ;., Michaelchuk, W. M., Stickland, M. K. Assessment of pulmonary capillary blood volume, membrane diffusing capacity, and intrapulmonary arteriovenoua anastomoses during exercise. J. Vis. Exp. (120), e54949 (2017).
- Thomas, A., et al. The single-breath diffusing capacity of CO and NO in healthy children of European descent. PLoS One. 12 (6), e0179097 (2017).
- Blakemore, W. S., Forster, R. E., Morton, J. W., Ogilvie, C. M. A standardized breath holding technique for the clinical measurement of the diffusing capacity of the lung for carbon monoxide. J Clin Invest. 36 (1), 1-17 (1957).
- Cotes, J. E., et al. Iron-deficiency anaemia: its effect on transfer factor for the lung (diffusiong capacity) and ventilation and cardiac frequency during sub-maximal exercise. Clin Sci. 42 (3), 325-335 (1972).
- Mann, T., Lamberts, R. P., Lambert, M. I. Methods of prescribing relative exercise intensity: Physiological and practical considerations. Sports Med. 43 (7), 613-625 (2013).
- Forster, R. E. Exchange of gases between alveolar air and pulmonary capillary blood: pulmonary diffusing capacity. Physiol Rev. 37 (4), 391-452 (1957).
- Tedjasaputra, V., et al. Pulmonary capillary blood volume response to exercise is diminished in mild chronic obstructive pulmonary disease. Respir Med. 145, 57-65 (2018).
- Nymand, S. B., et al. Exercise adaptations in COPD: the pulmonary perspective. Am J Physiol Lung Cell Mol Physiol. 323 (6), L659-L666 (2022).
- Rodríguez-Roisin, R., et al. Ventilation-perfusion imbalance and chronic obstructive pulmonary disease staging severity. J Appl Physiol. 106 (6), 1902-1908 (2009).
- Hsia, C. C., Johnson, R. L., Shah, D. Red cell distribution and the recruitment of pulmonary diffusing capacity. J Appl Physiol. 86 (5), 1460-1467 (1999).
- Wilhelm, E., Battino, R., Wilcock, R. J. Low-pressure solubility of gases in liquid water. Chem Rev. 77 (2), 219-262 (1977).
- Forster, R. E. . Diffusion of gases across the alveolar membrane. , (1987).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneThis article has been published
Video Coming Soon