Криоконсервация первичных зародышевых клеток и возрождение штаммов дрозофилы
* These authors contributed equally
In This Article
Summary
Крайне желателен метод длительного сохранения штаммов дрозофилы в качестве альтернативы частому переносу взрослых мух в флаконы со свежими кормами. Этот протокол описывает криоконсервацию первичных половых клеток дрозофилы и возрождение штамма путем их трансплантации в агаметные эмбрионы хозяина.
Abstract
Штаммы дрозофилы необходимо поддерживать за счет частой пересадки взрослых мух в новые флаконы. Это чревато мутационной деградацией и фенотипическими изменениями. Поэтому необходимо разработать альтернативный метод долговременной консервации без таких изменений. Несмотря на предыдущие успешные попытки, криоконсервация эмбрионов дрозофилы до сих пор не имеет практического применения из-за низкой воспроизводимости. В данной статье мы опишем протокол криоконсервации первичных зародышевых клеток (ПГК) и возрождения штамма путем трансплантации криоконсервированных ПГК в агаметические эмбрионы Drosophila melanogaster (D. melanogaster). PGC обладают высокой проницаемостью для криопротекторов (CPA), а вариации в развитии и морфологии между штаммами менее проблематичны, чем при криоконсервации эмбрионов. В этом методе PGC собираются примерно из 30 донорских эмбрионов, загружаются в иглу после обработки CPA, а затем криоконсервируются в жидком азоте. Для получения донорских гамет криоконсервированные PGC в игле размораживают, а затем помещают примерно в 15 агаметных эмбрионов-хозяев. С помощью этого протокола была достигнута частота не менее 15% фертильных мух, а количество потомства на фертильную пару всегда было более чем достаточным для возрождения исходного штамма (среднее число потомства составляло 77,2 ± 7,1), что указывает на способность криоконсервированных PGC становиться стволовыми клетками зародышевой линии. Среднее количество фертильных мух на одну иглу составляло 1,1 ± 0,2, и 9 из 26 иголок производили два или более фертильных потомства. Было обнаружено, что 11 игл достаточно для получения 6 и более потомства, в которое, вероятно, входит как минимум одна самка и один самец. Агаметический хозяин позволяет быстро реанимировать штамм, просто скрещивая вновь появившихся самок и самцов мух. Кроме того, PGC могут быть использованы в приложениях генной инженерии, таких как редактирование генома.
Introduction
Поддержание штаммов дрозофилы путем переноса взрослых мух в новые пищевые флаконы неизбежно приводит к накоплению мутаций и эпигенетических изменений с течением времени. Разработка альтернативного метода для долгосрочного сохранения штаммов дрозофилы без таких изменений является императивом, особенно для референсных штаммов, в которых должен поддерживаться весь геном. Описано несколько успешных попыток криоконсервации эмбрионов или яичников дрозофилы 1,2,3. К сожалению, они до сих пор не имеют практического применения из-за низкой воспроизводимости. Действительно, эмбрионы на ранних стадиях имеют низкую выживаемость после криоконсервации из-за высокого содержания желтка, что препятствует проникновению и диффузии криопротектора (CPA) 2,3. Проницаемость CPA также сильно ограничена восковыми слоями эмбрионов на поздних стадиях. Трудно и долго находить период времени, в течение которого эмбрионы имеют высокую выживаемость и более тонкий восковой слой. Недавно Zhan et al.4 усовершенствовали методы пермеабилизации эмбрионов, загрузки CPA и витрификации и успешно криоконсервировали эмбрионы нескольких штаммов. Тем не менее, эти методы непросты в применении, потому что жизнеспособность эмбрионов после пермеабилизации, как правило, низкая. Поэтому дальнейшее совершенствование и разработка альтернативных подходов по-прежнему необходимы. Методы, включающие криоконсервацию первичных половых клеток (ПГК), являются альтернативным подходом для долгосрочного сохранения штаммов дрозофилы.
Трансплантация PGC (также называемая полюсными клетками) была использована для получения химер зародышевой линии, особенно самок, для изучения таких процессов, как материнские эффекты зиготных летальных мутаций и определение пола половых клеток 5,6,7,8,9,10,11,12 . PGC намного меньше, чем эмбрионы, и, вероятно, обладают высокой проницаемостью для большинства криопротекторов. Кроме того, эволюционная и морфологическая изменчивость между штаммами менее проблематична, а агаметический хозяин позволяет быстро восстанавливать целые геномы. Недавно мы разработали новый метод криоконсервации PGC13, который предотвращает неизбежные генетические и эпигенетические изменения в штаммах дрозофилы. Здесь мы представляем подробный протокол.
Этот метод криоконсервации требует специальных знаний в области обращения с PGC и инструментов. В то время как пошаговый подход может быть эффективным решением для тех, кто не знаком с ним, он может быть неподходящим для небольших лабораторий из-за требований к приборам. Этот протокол криоконсервации PGC может быть легче адаптирован для использования с различными видами дрозофил и различными видами насекомых, чем протоколы криоконсервации эмбрионов, из-за меньших различий в развитии и морфологии. PGC также потенциально могут быть использованы в приложениях генной инженерии, таких как редактирование генома 14,15,16. Таким образом, этот метод может быть использован в складских центрах и других лабораториях для поддержания мух и других штаммов насекомых в течение длительных периодов времени без изменений.
Protocol
1. Подготовка оборудования
- Система микроманипулятора: Соберите систему микроманипулятора для сбора и пересадки клеток (Рисунок 1A).
- Предметные стекла из коллекции PGC (рис. 2A)
- Для приготовления гептанового клея отрежьте двусторонний скотч длиной примерно 30 см и замочите его на ночь в 7 мл технического (обычного) раствора гептана.
- Нарисуйте две параллельные опорные линии для выравнивания эмбрионов на обратной стороне предметного стекла.
- Нанесите капли вышеуказанного гептанового клея на предметное стекло (со стороны без линий) с помощью пипетки Пастера. Высушите поверхность предметного стекла на воздухе, пока она не станет белой.
- Повторите добавление и распределение капель гептанового клея и снова высушите предметное стекло.
ПРИМЕЧАНИЕ: Клей предотвращает растекание жидких растворов по плоской поверхности и облегчает загрузку водных растворов в иглу. - Чтобы сделать каркасы для бассейна для эмбрионов, наклейте на разделочную доску три слоя стандартной виниловой ленты толщиной 0,2 мм, например, изоленты. Разрежьте ленту на прямоугольники шириной 1,5 см. Затем отрежьте все три слоя скотча, оставив рамку от 2 до 3 мм.
ПРИМЕЧАНИЕ: Рамка для эмбриопула прикрепляется после выравнивания эмбрионов, чтобы сформировать пул для эмбрионов.
- Иглы для трансплантации
ПРИМЕЧАНИЕ: Все коммерчески доступные иглы на момент проведения этого исследования были слишком узкими или слишком широкими для криоконсервации PGC.- Сделайте иглу, используя стеклянный капилляр и съемник. Мы используем съемник NARISHIGE PN-31 с уровнем нагревателя 85,0-98,4, основным уровнем магнита 57,8 и подуровнем магнита 45,0.
- Чтобы изготовить иглу с приблизительной толщиной стенки 1 мкм и наконечником длиной около 200 мкм с внутренним диаметром 10-12 мкм, отполируйте кончик иглы в следующем трехступенчатом процессе (Рисунок 3). Сначала шлифуйте кончик иглы под углом 30° со скоростью 780 об/мин, пока наконечник не достигнет внутреннего диаметра 10-12 мкм. Этот первый этап шлифования занимает примерно 1 час.
ПРИМЕЧАНИЕ: Чтобы не сломать кончик иглы, сначала поверните точильный камень, а затем осторожно переместите иглу вниз на точильный камень. - Нарисуйте линию на верхней части иглы, чтобы отследить нужный угол. Поверните иглу против часовой стрелки на 90° и снова отполируйте ее со скоростью 180 об/мин. Это займет примерно 5 минут.
- Поверните иглу по часовой стрелке на 45° и отполируйте ее со скоростью 180 об/мин в течение одной секунды.
- Поместите предметное стекло с каплей смеси хромовой кислоты (ОСТОРОЖНО: токсично) на предметный столик микроскопа. Приложите иглу к капилляродержателю (рис. 1D) под углом 10°-13° относительно поверхности предметного стекла, осторожно переместите иглу вниз и погрузите наконечник в смесь хромовой кислоты.
- Вытягивая и толкая поршень (рисунок 1Б), несколько раз механически загружайте и выгружайте раствор из иглы, чтобы удалить стеклянный мусор в игле. Обязательно очистите и внешнюю стенку.
- Промойте внутреннюю и внешнюю часть иглы два раза дистиллированной водой, чтобы полностью удалить хромовую кислоту.
2. Сбор и криоконсервация ПГК
- Сбор эмбрионов
- Пересадите соответствующее количество мух интересующего донорского штамма (примерно 450 мух каждого пола для чашки для сбора эмбрионов) в чашку для сбора эмбрионов с планшетом для сбора эмбрионов (рис. 1E) и инкубируйте их при температуре 25 °C. Обычно мы используем 3-5-дневных мух-родителей, которых выращивают в менее скученных условиях при комнатной температуре (23-25 °C).
- Проведите два 30-минутных предварительных сбора и выбросьте все отложенные яйца. Поскольку самки могут сохранять оплодотворенные яйца, которые развиваются в яйцеводе, этот этап необходим для синхронизации яйцекладки на этапе 2.1.3 (рис. 4).
- После двух предварительных сборов собирайте эмбрионы в течение 50 минут, а затем инкубируйте собранные эмбрионы во влажной камере при температуре 25 °C, чтобы эмбрионы могли развиться до стадии бластодермы (ранняя стадия 517). Время инкубации обычно составляет 100 мин, но может быть увеличено до 120 мин, в зависимости от штамма (рис. 4).
ПРИМЕЧАНИЕ: Увлажненная камера создается путем размещения влажного бумажного полотенца на дне пластиковой коробки и опрыскивания его водяным туманом перед использованием. У эмбрионов на ранней стадии 5 формирование ПГК завершено, но соматическая клеточная нет. Точная стадия эмбриона определяется под сложным микроскопом на шаге 2.4.
- Дехорионирующие эмбрионы
- Нанесите каплю дистиллированной воды на сетчатый фильтр из нержавеющей стали (150 меш, отверстие 109 мкм, диаметр проволоки 60 мкм; Рисунок 1F). С помощью щипцов возьмите эмбрионы из пластины для сбора эмбрионов и поместите их в каплю воды.
- Прижмите папиросную бумагу к ситечку снизу, чтобы впитать воду. Добавьте капли свежего 5% (в виде Cl) раствора гипохлорита натрия к эмбрионам и непрерывно постукивайте по ситечку в течение 10 с.
- Промойте эмбрионы, обрызгав их дистиллированной водой, и прижмите папиросную бумагу к ситечку снизу, чтобы впитать воду. Повторите этот шаг 3 раза.
- Выравнивание дехорионированных эмбрионов
- Под стереомикроскопом используйте щипцы для переноса эмбрионов. Выровняйте дехорионированные эмбрионы в два ряда на предметном стекле для сбора PGC вдоль двух контрольных линий (рис. 2A). Эмбрионы ориентированы передней стороной вправо (сторона, с которой будут манипулировать) и вентральной стороной вверх.
ПРИМЕЧАНИЕ: Этот этап должен быть завершен через 20 минут, в течение которых мы обычно выравниваем около 40 эмбрионов. - Прикрепите рамку для бассейна эмбрионов вокруг эмбрионов на предметное стекло из коллекции PGC. Капните 1 мкл раствора CPA (1x раствор Ephrussi-Beadle Ringer, EBR, содержащий 20% этиленгликоля и 1 М сахарозы; 1x EBR: 130 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2 и 10 мМ Hepes при pH 6,9) в двух отдельных точках в области, огороженной рамой, и наполните бассейн силиконовым маслом, чтобы предотвратить высыхание эмбрионов (Рисунок 2A).
ПРИМЕЧАНИЕ: Для приготовления раствора CPA полностью растворите 10,26 г сахарозы примерно в 20 мл дистиллированногоH2O, содержащего 3 мл 10 x EBR раствора. Добавьте 6 мл этиленгликоля, а затем добавьте дистиллированныйH2Oдо 30 мл. После тщательного перемешивания процеживают раствор через одноразовую мембрану 0,22 мм.
- Под стереомикроскопом используйте щипцы для переноса эмбрионов. Выровняйте дехорионированные эмбрионы в два ряда на предметном стекле для сбора PGC вдоль двух контрольных линий (рис. 2A). Эмбрионы ориентированы передней стороной вправо (сторона, с которой будут манипулировать) и вентральной стороной вверх.
- Сбор PGC
- Поместите предметное стекло PGC-коллекции шага 2.3.2 на предметный столик микроскопа, оснащенного системой микроманипулятора. Приложите иглу к капилляродержателю и поместите первый эмбрион в левом ряду и кончик иглы в одну фокальную плоскость. Загрузите силиконовое масло в иглу на 2-3 с.
- Начните сбор ПГК с эмбрионов в левом ряду. Используя объектив с 20-кратным увеличением, осторожно переместите кончик иглы к поверхности переднего конца эмбриона и проникните в эмбрион к заднему концу, не перемещая иглу, а перемещая столик микроскопа.
- Когда кончик иглы достигнет заднего конца, слегка втяните иглу и полностью выпустите желток в игле прямо внутри слоя соматической клетки.
- Поддерживая постоянное давление в игле, переместите кончик иглы к ПГК внутри заднего полюса и осторожно, но не занимая много времени, загрузите ПГК.
- Быстро вытащите иглу из эмбриона и выпустите желток и другие загрязнения из иглы в бассейн с силиконовым маслом, удерживая PGC в игле. Затем загрузите чистое силиконовое масло из бассейна.
- Повторите шаги 2.4.2 - 2.4.5 для других эмбрионов в левом ряду. Перед сбором PGC из нового эмбриона поместите как можно больше силиконового масла, загруженного на этапе 2.4.5, внутрь слоя соматической клетки, сохраняя загруженные PGC в игле. Это гарантирует, что вновь загруженные PGC будут соседствовать с ранее собранными PGC без какого-либо промежуточного материала между ними.
- После завершения сбора ПГК от эмбрионов в левом ряду максимально отделите ПГК от желтка и других загрязняющих веществ. Для этого поместите все PGC в игле на поверхность эмбриона и удалите желток или другие загрязнения другому соседнему эмбриону.
- Затем соберите PGC с эмбрионов в правом ряду. Объедините PGC, собранные из правого и левого рядов.
- Нанесение криопротектора (КПА) на ПГК
- После промывки иглы с КПА в одной капле, загрузите свежий ЦПА в другой капле в иглу и добавьте ЦПА к ПГК, отложенным на эмбрионе. Объем CPA должен быть эквивалентен объему PGC.
- Удалите как можно больше CPA из кластера PGC через 1-2 с после добавления CPA. PGC немного сжимаются и приобретают квадратную форму сразу после добавления CPA.
- Опорожните иглу, а затем залейте силиконовое масло на 5 секунд или дольше. Загрузите все собранные PGC, а затем снова залейте силиконовое масло в течение 5 с или дольше. Теперь PGC зажаты между двумя слоями силиконового масла (рис. 2B).
ПРИМЕЧАНИЕ: Важно удалить как можно больше желтка, CPA и других загрязнений.
- Криоконсервирующие ПГК
- Откройте трехходовой запорный кран (рис. 1C), а затем отсоедините иглу от микроманипулятора. Промокните масло с поверхности иглы мягкой папиросной бумагой. Не прикасайтесь салфеткой непосредственно к кончику иглы.
- Прикрепите иглу к иглодержателю и зафиксируйте ее в нужном положении у основания с помощью виниловой ленты (Рисунок 1H). Прикрепите этикетку к трубке держателя.
- Мгновенно заморозьте держатель иглой, направленной вниз, погрузив его в жидкий азот. Не отпускайте держатель до тех пор, пока жидкость не перестанет шипеть из стойки.
- Храните держатель в резервуаре для хранения жидкого азота в зоне жидкой фазы, а не в зоне паровой фазы.
3. Размораживание и пересадка ПГК
- Сбор, дехорионирование и выравнивание эмбрионов агатетических мух-хозяев
- Соберите и дехорионатируйте эмбрионы у мух-агаметных хозяев, выполнив шаг 2.
- Выровняйте агаметные эмбрионы хозяина 5-й стадии на предметном стекле для трансплантации. Однако на этот раз ориентируйте заднюю часть вправо (сторону, которой нужно манипулировать) и вентральную вверху (рис. 5). Выровняйте примерно 30 эмбрионов в два ряда за 20 минут.
- Во время выравнивания эмбрионов включите увлажнитель воздуха в течение 2-10 минут, если этого требует влажность в помещении (Таблица 1). Идеальная влажность составляет от 30% до 40%, но она может варьироваться в зависимости от тепловых условий.
- Размораживание и трансплантация ПЗК в эмбрионы хозяина
- Чтобы быстро разморозить криоконсервированные PGC, поместите держатель с иглой в раствор 1x EBR комнатной температуры иглой вниз и держите его погруженным в воду в течение 10 с.
- Поместите предметное стекло для трансплантации на предметный столик микроскопа. Прикрепите замораживающе-размороженную иглу к капилляродержателю и поместите первый эмбрион в левом ряду и кончик иглы в одну фокальную плоскость.
- Используя объектив с 20-кратным увеличением, осторожно переместите кончик иглы к поверхности заднего конца эмбриона.
- Осторожно протолкните каждый эмбрион снаружи и убедитесь, что они медленно возвращаются к своей первоначальной форме. Прощупывание подтвердит, что внутреннее давление эмбриона не слишком высокое или слишком низкое.
- Осторожно перемещают иглу и проникают в эмбрион от заднего полюса.
- Аккуратно поместите примерно 10-20 PGC непосредственно внутри заднего полюса, точно между вителлиновой мембраной и слоем соматических клеток эмбриона. Избегайте их депонирования в слое соматических клеток. Если перивителлиновая жидкость вытекает из эмбриона, засосите вытекшую жидкость в иглу и удалите ее.
- Втяните иглу из эмбриона. Повторите шаги 3.2.5 и 3.2.6 для последующих эмбрионов.
4. Инкубация эмбрионов и восстановление донорских штаммов
- Удалите все эмбрионы, которые не получили трансплантированные PGC, и инкубируйте оставшиеся эмбрионы в увлажненной камере (рис. 1G) при температуре 25 °C.
- Через 24 ч или более после трансплантации и как можно скорее после вылупления используют щипцы для захвата и переноса вылупившихся личинок в стандартные пищевые флаконы дрозофилы и инкубируют при 25 °C.
- Чтобы возродить штамм, скрещивайте недавно появившихся самок и самцов (рис. 6).
ПРИМЕЧАНИЕ: Агаметические хозяева позволяют восстанавливать сразу весь геном без скрещивания с балансирно-хромосомными штаммами. Сосуществование агаметных самцов в пробирке не будет иметь значения, потому что самки, даже если они спариваются с ними, не демонстрируют долгосрочных реакций после спаривания, включая снижение восприимчивости к повторному спариванию18,19.
Representative Results
Эффективность криоконсервированной трансплантации ПГК была описана Asaoka et al.13 и приведена в таблице 2 для трансплантации ПГК, криоконсервированных в течение 1 дня или дольше в жидком азоте. Частота вылупления составила 168/208 трансплантированных эмбрионов (80,8%), а жизнеспособность эмбриона до взрослой особи составила 87/208 (41,8%). Частота плодовитых мух составила 28/87 (32,2%). Эта частота не различалась между ПГК, криоконсервированными в течение 8–30 дней, и криоконсервированными в течение 31–150 дней (20/57 против 8/30, G' = 0,63, p >0,1, d.f. = 1). Среднее количество потомства на пару составило 77,2 ± 7,1 (n = 18, 28-122), что указывает на способность криоконсервированных ПЗК становиться стволовыми клетками зародышевой линии. Из 26 иголок 10 не произвели фертильного потомства, 7 игл произвели 1 фертильное потомство, 7 игл произвели 2 фертильных потомства, а 2 иглы произвели 3 или 4 фертильных потомства. Среднее количество фертильных мух на одну иглу составляло 1,1 ± 0,2. Исходя из этих данных, с 95% уверенностью, достаточно 11 игл для получения 6 и более потомства, в которое, вероятно, входит хотя бы одна самка и один самец.
В вышеуказанных экспериментах в качестве агамета-хозяина использовались эмбрионы, экспрессирующие мРНК ово-А в ПГК (нанос>ово-А, OvoA_OE эмбрионы). Из 669 самок F1 и 720 самцов F1, полученных от трансплантированных пар nanos>ovo-A, не было ни одного эскейпера, который был бы получен от PGC-хозяина. Некоторые мутанты oskar (osk) также чувствительны к температуреагаметические 20,21. Поскольку osk-мутант с высокой гомозиготной жизнеспособностью и агаметическим фенотипом больше не доступен, мы воссоздали osk[8] миссенс-мутант20 с помощью редактирования генома с помощью CRISPR/Cas9. Эти мухи были полностью агаметными (0 убегающих из 230 самок и 192 самца) при 25 °C, но несколько ускользающих появились при 23 °C (1 из 248 самок и 1 из 290 самцов). Таким образом, nanos>ovo-A рекомендуются в качестве агаметических эмбрионов-хозяев. Запасы UASp-ovo-A и nanos-Gal4 13 скоро поступят в продажу в Центре запасов дрозофилы KYOTO.

Рисунок 1: Необходимое оборудование. (А) Микроманипуляторная система для сбора и пересадки клеток. i) перевернутый микроскоп, ii) механический микроманипулятор, iii) шприц, iv) капиллярный держатель, v) трехходовой запорный кран, vi) увлажнитель и vii) стереомикроскоп. (Б) Шприц. (C) Трехходовой запорный кран и силиконовые трубки соединяют шприц и капилляродержатель. (D) Игла и капилляродержатель прикреплены к микроманипулятору. (E) Чашка для сбора эмбрионов с пластиной для сбора эмбрионов (диаметр 6 см, высота 7,7 см). (F) Сетчатый фильтр из нержавеющей стали. (G) Контейнер, используемый в качестве влажной камеры со стеклянным предметным стеклом. Для поддержания влажности положите на дно влажную бумагу и закройте крышкой. (H) Иглодержатель с иглой для криоконсервации. (I) Стеллаж для хранения криоконсервации и коробка с иглами. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
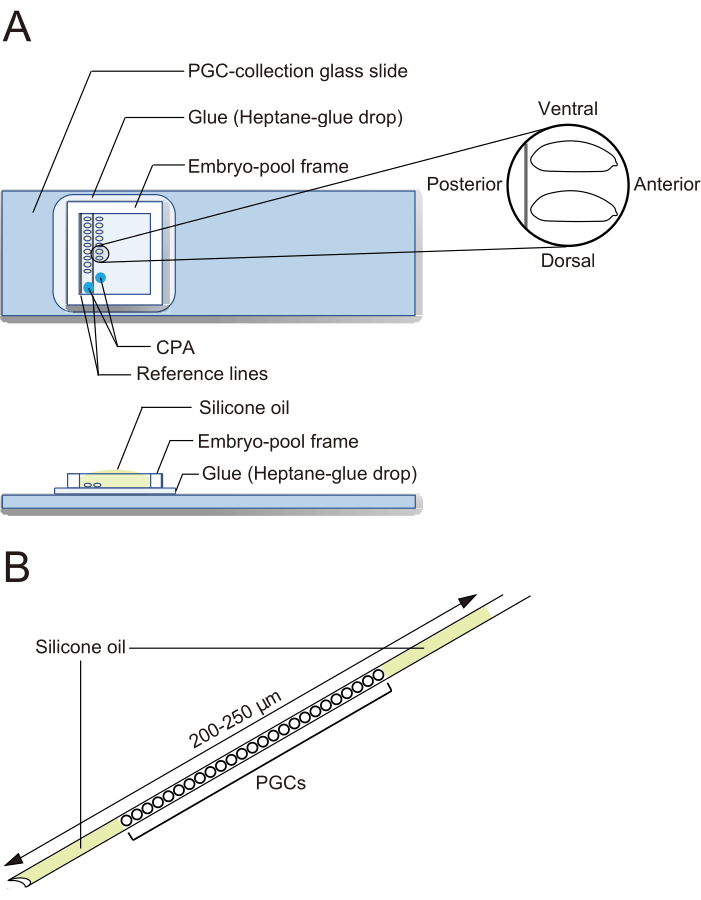
Рисунок 2: Предметное стекло для сбора ПГК и игла для криоконсервации. (А) Предметное стекло из первичной зародышевой клетки (ПГК), покрытое клеем. Дехорионизированные эмбрионы выровнены в два ряда и ориентированы передней стороной вправо (сторона, подлежащая манипулированию) и вентральной стороной вверх. Прикрепляется каркас эмбрио-бассейна, наносятся две капли раствора криопротекторов (КПА) и бассейн заполняется силиконовым маслом. (Б) Игла должна содержать как можно меньшее количество желтка и других загрязнений. PGC зажаты между двумя слоями силиконового масла при криоконсервации в жидком азоте. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
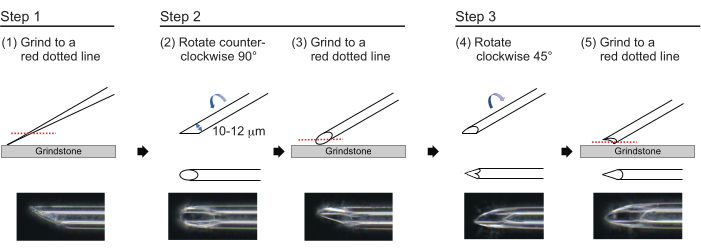
Рисунок 3: Изготовление иглы. Трехступенчатый метод полировки кончика для изготовления иглы с соответствующим размером отверстия и острым кончиком. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
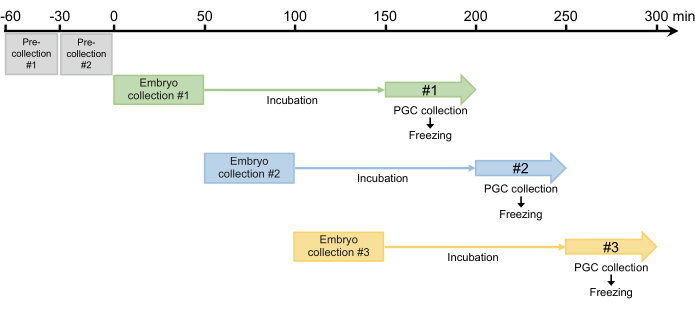
Рисунок 4: Схема забора эмбрионов. После двух предварительных сборов мы обычно собираем три-четыре раза в день. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
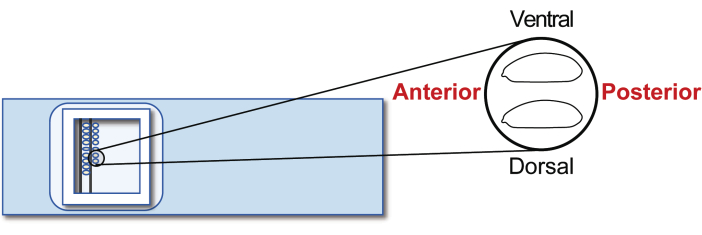
Рисунок 5: Выравнивание эмбриона хозяина. Выравнивание эмбрионов-хозяев на предметном стекле. Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
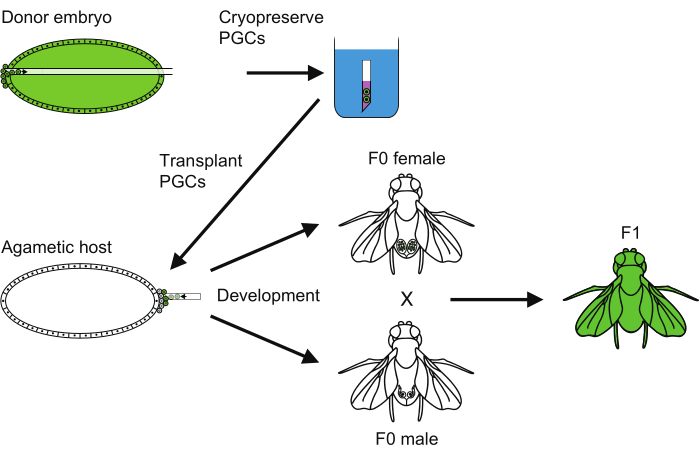
Рисунок 6: Обзор метода криоконсервации PGC. Обзор всех шагов, предпринятых для проведения криоконсервации первичных половых клеток (PGC). Пожалуйста, нажмите здесь, чтобы увидеть увеличенную версию этого рисунка.
| Влажность в помещении | |||
| < 30% | ~ 30% | > 30% | |
| Выравнивание эмбрионов-хозяев (~20 мин) | Используйте увлажнитель воздуха в течение 2 - 10 минут | Используйте увлажнитель периодически в течение 1 минуты | Не используйте увлажнитель воздуха |
| Размораживание донорских ПЗК | Неприменимо | Неприменимо | Неприменимо |
| Сухое на воздухе ПГК | Пропустите этот шаг | Пропустите этот шаг | 5 мин |
| Нанесите силиконовое масло | Неприменимо | Неприменимо | Неприменимо |
| Трансплантация PGC | Неприменимо | Неприменимо | Неприменимо |
| Все эти шаги должны быть выполнены за 50 минут. | |||
Таблица 1: Сушка эмбрионов при выравнивании эмбрионов и размораживании PGC.
| Донорский штамм | Период криоконсервации | Количество трансплантированных эмбрионов (А) | Количество вылупившихся личинок (В) (выводимость, B/A) | Количество взрослых особей (C) (жизнеспособность яйцеклетки до взрослой особи, C/A) | Количество фертильных взрослых особей (D) (частота плодовитых мух, D/C) |
| М17 | 8 - 30 дней | 134 | 108 (80.6%) | 57 (42.5%) | 20 (35.1%) |
| М17 | 31 - 150 дней | 74 | 60 (81.1%) | 30 (40.5%) | 8 (26.7%) |
| М17: тис; TM6B, P{Dfd-GMR-nvYFP}4, Sb[1] Tb[1] ca[1]/ Pri[1] | |||||
Таблица 2: Эффективность криоконсервированной трансплантации ПГХ. Эта таблица изменена по сравнению с13. Все данные взяты из агаметических хостов.
Discussion
Решающим фактором успеха в криоконсервации и возрождении ПГК является использование хороших эмбрионов. Для забора эмбрионов следует использовать молодых самок (например, от 3 до 5 дней). Эмбрионы донора и реципиента оцениваются с помощью микроскопического исследования, и используются только эмбрионы на стадии бластодермы (стадия 5)12. Для сбора ПГК мы обычно выравниваем около 40 донорских эмбрионов в течение 20 минут и собираем ПГК примерно из 30 эмбрионов на ранней стадии 5; Более старые и дефектные эмбрионы не используются. После криоконсервации и размораживания PGC должны сохранять свою форму; ПЗК разрываются при неудачной консервации. Эмбрионы хозяина также должны находиться на 5 стадии и иметь умеренное внутреннее давление; Эмбрионы должны медленно возвращаться к своей первоначальной форме после легкого подталкивания. Чрезмерно и недостаточно высушенные эмбрионы не будут нормально развиваться после трансплантации. Поскольку гетеросексуальная трансплантация PGC не приводит к образованию гамет у дрозофилы 5,10, трансплантация PGC от нескольких донорских эмбрионов в эмбрионы хозяина с большей вероятностью приведет к появлению фертильных взрослых особей. С этой целью мы обычно собираем PGC примерно из 30 эмбрионов на одну иглу.
В качестве криопротекторов мы пробовали этиленгликоль, диметилсульфоксид и глицерин вместе с сахарозой в различных концентрациях. Мы определили, что EBR, содержащий 20% этиленгликоля и 1 М сахарозу, является лучшим13; однако использование различных криопротекторов может улучшить сохранность PGC22.
Этот метод криоконсервации требует специальных навыков в обращении с ПГК, и для комфортного сбора и пересадки ПГК требуется примерно 6 недель обучения. Для оценки и улучшения навыков можно разбить его на шесть этапов обучения: 1) выравнивание эмбрионов на предметном стекле, 2) управление манипулятором, 3) трансплантация ПГК от эмбриона к другому эмбриону без криоконсервации, 4) трансплантация ПГК от 10 или более эмбрионов в 5-10 эмбрионов, 5) трансплантация ПГК после применения КПА и 6) пересадка ПГК после замораживания-размораживания. Каждый этап может занять 1 неделю. Краткосрочными целями на этапе 3 являются коэффициент вылупления 40%, жизнеспособность эмбриона до взрослой особи 10%-20% и частота фертильных мух 20%.
Криоконсервация PGC требует дорогостоящего оборудования и высококвалифицированного персонала. Поэтому этот метод может быть принят не многими лабораториями. Тем не менее, современный метод PGC имеет несколько важных аспектов. Во-первых, ПГК намного меньше эмбрионов и очень проницаемы для криопротекторов. Напротив, проницаемость криопротекторов сильно ограничена восковыми слоями эмбрионов дрозофилы, что является наиболее серьезной проблемой при криоконсервации эмбрионов. Действительно, предыдущие исследования приложили большие усилия, чтобы найти временное окно, в котором эмбрионы имеют высокий уровень выживаемости и более тонкий слой воска. Второй связан с развитием и морфологической изменчивостью между штаммами. ПГК собирают с эмбрионов 5-й стадии (2 ч 30 мин-3 ч 20 мин после яйцекладки), а криоконсервацию эмбрионов проводят на эмбрионах 16 стадии (14-22 ч после яйцекладки). Таким образом, эмбрионы намного старше и демонстрируют гораздо большую вариабельность штаммов в оптимальном временном окне для криоконсервации по сравнению с криоконсервацией PGC. Действительно, частота хозяев, производящих донорское потомство, не различалась среди пяти штаммов, изученных Asaoka et al.13, хотя хозяева не были агаметическими. Кроме того, PGC могут быть использованы в приложениях генной инженерии, таких как редактирование генома14, 15, 16.
Acknowledgements
Мы благодарим Центр запасов дрозофилы KYOTO за штаммы мух. Мы также благодарим г-жу Ванду Мияту за редактирование рукописи на английском языке и д-ра Джереми Аллена из Edanz (https://jp.edanz.com/ac) за редактирование черновика этой рукописи. Эта работа была поддержана грантами (JP16km0210072, JP17km0210146, JP18km0210146) от Японского агентства медицинских исследований и разработок (AMED) для T.T.-S.-K., грантами (JP16km0210073, JP17km0210147, JP18km0210145) от AMED для S.K., грантом (JP20km0210172) от AMED для T.T.-S.-K. и S.K., грант на научные исследования (C) (JP19K06780) от Японского общества содействия науке (JSPS) для T.T.-S.-K. и грант для научных исследований в инновационных областях (JP18H05552) от JSPS для S.K.
Materials
| Name | Company | Catalog Number | Comments |
| Acetic acid | FUJIFILM Wako Pure Chemical Corporation | 017-00256 | For embryo collection |
| Agar powder | FUJIFILM Wako Pure Chemical Corporation | 010-08725 | For embryo collection |
| Calcium chloride | FUJIFILM Wako Pure Chemical Corporation | 038-24985 | For EBR solution |
| Capillary | Sutter Instrument | B100-75-10-PT | BOROSILICATE GLASS; O.D: 1.0mm, I.D: 0.75mm , length: 10cm, 225Pcs |
| Capillary holder | Eppendorf | 5196 081.005 | Capillary holder 4; for micromanipulation |
| Chromic acid mixture | FUJIFILM Wako Pure Chemical Corporation | 037-05415 | For needle washing |
| CPA solution | 1x EBR containing 20% ethylene glycol and 1M sucrose | ||
| Double-sided tape | 3M | Scotch w-12 | For glue extracting |
| Ephrussi–Beadle Ringer solution (EBR) | 130 mM NaCl, 5 mM KCl, 2 mM CaCl2, and 10 mM Hepes at pH 6.9 | ||
| Ethanol (99.5) | FUJIFILM Wako Pure Chemical Corporation | 057-00451 | For embryo collection |
| Ethylene glycol | FUJIFILM Wako Pure Chemical Corporation | 054-00983 | For CPA solution |
| Falcon 50 mm x 9 mm bacteriological petri dish | Corning Inc. | 351006 | For embryo collection |
| Forceps | Vigor | Type5 Titan | For embryo handling |
| Grape juice | Asahi Soft Drinks Co., LTD. | Welch's Grape 100 | For embryo collection |
| Grape juice agar plate | 50% grape juice, 2% agar, 1% ethanol, 1% acetic acid | ||
| Heptane | FUJIFILM Wako Pure Chemical Corporation | 084-08105 | For glue extracting |
| Humidifier | APIX INTERNATIONAL CO., LTD. | FSWD2201-WH | For embryo preparation |
| Inverted microscope | Leica Microsystems GmbH | Leica DM IL LED | For micromanipulation |
| Luer-lock glass syringe | Tokyo Garasu Kikai Co., Ltd. | 0550 14 71 08 | Coat a plunger with silicon oil (FL-100-450CS);for micromanipulation |
| Mechanical micromanipulator | Leica Microsystems GmbH | For micromanipulation | |
| Micro slide glass | Matsunami Glass Ind., Ltd. | S-2441 | For embryo aligning |
| Microgrinder | NARISHIGE Group | Custom order | EG-401-S combined EG-401 and MF2 (with ocular lens MF2-LE15 ); for needle preparation |
| Microscope camera | Leica Microsystems GmbH | Leica MC170 HD | For micromanipulation |
| Needle holder | Merck KGaA | Eppendorf TransferTip (ES) | For cryopreservation |
| Potassium chloride | Nacalai Tesque, Inc. | 28514-75 | For EBR solution |
| Puller | NARISHIGE Group | PN-31 | For needle preparation; the heater level is set to 85.0-98.4, the magnet main level to 57.8, and the magnet sub level to 45.0. |
| PVC adhesive tape for electric insulation | Nitto Denko Corporation | J2515 | For embryo-pool frame |
| Silicon oil | Shin-Etsu Chemical, Co, Ltd. | FL-100-450CS | For embryo handling |
| Sodium chloride | Nacalai Tesque, Inc. | 31320-05 | For EBR solution |
| Sodium hypochlorite solution | FUJIFILM Wako Pure Chemical Corporation | 197-02206 | Undiluted and freshly prepared; for embryo breaching |
| Sucrose | Nacalai Tesque, Inc. | 30404-45 | For CPA solution |
References
- Brüschweiler, W., Gehring, W. A method for freezing living ovaries of Drosophila melanogaster larvae and its application to the storage of mutant stocks. Experientia. 29, 134-135 (1973).
- Steponkus, P. L., et al. Cryopreservation of Drosophila melanogaster embryos. Nature. 345, 170-172 (1990).
- Mazur, P., Cole, K. W., Hall, J. W., Schreuders, P. D., Mahowald, A. P. Cryobiological preservation of Drosophila embryos. Science. 258 (5090), 1932-1935 (1992).
- Zhan, L., Li, M. G., Hays, T., Bischof, J. Cryopreservation method for Drosophila melanogaster embryos. Nat Comm. 12, 2412 (2021).
- Van Deusen, E. B. Sex determination in germ line chimeras of Drosophila melanogaster. Development. 37 (1), 173-185 (1977).
- Breen, T. R., Duncan, I. M. Maternal expression of genes that regulate the bithorax complex of Drosophila melanogaster. Dev Biol. 118, 442-456 (1986).
- Schupbach, T., Wieschaus, E. Germline autonomy of maternal-effect mutations altering the embryonic body pattern of Drosophila. Dev Biol. 113, 443-448 (1986).
- Irish, V., Lehmann, R., Akam, M. The Drosophila posterior-group gene nanos functions by repressing hunchback activity. Nature. 338, 646-648 (1989).
- Hülskamp, M., Schröder, C., Pfeifle, C., Jäckle, H., Tautz, D. Posterior segmentation of the Drosophila embryo in the absence of a maternal posterior organizer gene. Nature. 338, 629-632 (1989).
- Steinmann-Zwicky, M., Schmid, H., Nöthiger, R. Cell-autonomous and inductive signals can determine the sex of the germ line of Drosophila by regulating the gene Sxl. Cell. 57 (1), 157-166 (1989).
- Stein, D., Roth, S., Vogelsang, E., Nüsslein-Volhard, C. The polarity of the dorsoventral axis in the drosophila embryo is defined by an extracellular signal. Cell. 65 (5), 725-735 (1991).
- Kobayashi, S., Yamada, M., Asaoka, M., Kitamura, T. Essential role of the posterior morphogen nanos for germline development in Drosophila. Nature. 380, 708-711 (1996).
- Asaoka, M., et al. Offspring production from cryopreserved primordial germ cells in Drosophila. Comm Biol. 4 (1), 1159 (2021).
- Blitz, I. L., Fish, M. B., Cho, K. W. Y. Leapfrogging: primordial germ cell transplantation permits recovery of CRISPR/Cas9-induced mutations in essential genes. Development. 143 (15), 2868-2875 (2016).
- Koslová, A., et al. Precise CRISPR/Cas9 editing of the NHE1 gene renders chickens resistant to the J subgroup of avian leukosis virus. Proc Natl Acad Sci U S A. 117 (4), 2108-2112 (2020).
- Zhang, F. Efficient generation of zebrafish maternal-zygotic mutants through transplantation of ectopically induced and Cas9/gRNA targeted primordial germ cells. J Genet Genom. 47 (1), 37-47 (2020).
- Campos-Ortega, J. A., Hartenstein, V. Stages of Drosophila Embryogenesis. The Embryonic Development of Drosophila. , (1997).
- Manning, A. A sperm factor affecting the receptivity of Drosophila melanogaster females. Nature. 194, 252-253 (1962).
- Kubli, E. Sex-peptides: seminal peptides of the Drosophila male. Cell Mol Life Sci. 60, 1689-1704 (2003).
- Lehmann, R., Nüsslein-Volhard, C. Abdominal segmentation, pole cell formation, and embryonic polarity require the localized activity of oskar, a maternal gene in drosophila. Cell. 47 (1), 141-152 (1986).
- Kiger, A. A., Gigliotti, S., Fuller, M. T. Developmental genetics of the essential Drosophila Nucleoporin nup154: allelic differences due to an outward-directed promoter in the P-element 3′ end. Genetics. 153 (2), 799-812 (1999).
- Rienzi, L. F., et al. Perspectives in gamete and embryo cryopreservation. Semin Reprod Med. 36 (5), 253-264 (2018).
Explore More Articles
This article has been published
Video Coming Soon
ABOUT JoVE
Copyright © 2025 MyJoVE Corporation. All rights reserved