Method Article
Epstein-Barr Virus Büyüme dönüştürülmüş lenfoblastoid hücre dizilerinde kurulması
Bu Makalede
Özet
Epstein-Barr virüsü ile transforme B hücre hatları üretmek için bir yöntem açıklanmaktadır. Ayrıca, üç gün sonra enfeksiyon gibi erken olarak dönüşüm geçirmesi mukadder B hücreleri belirleyebilir bir roman tahlil göstermektedir.
Özet
B hücreleri Epstein-Barr virüsü (EBV) enfeksiyonu lenfoblastoid hücre hatları in vitro (LCL) kurulması ile sonuçlanan, proliferasyonu ve daha sonraki ölümsüzleşme yol açar . LCL latent EBV ile enfekte olduğundan, onlar EBV gecikme ve virüs kaynaklı B hücre proliferasyonu ve tümörogenez 1 araştırmak için bir model sistem sağlar. LCL immünolojik testleri 2, 3 çeşitli antijenleri için kullanılır olmuştur. Buna ek olarak, LCL, insan monoklonal antikorlar 4, 5 birincil biyolojik materyallere erişim 6, 7 sınırlı bir potansiyel olarak sınırsız bir kaynak oluşturmak ve sağlamak için kullanılabilir.
LCL oluşturmak için çeşitli yöntemler tarif edilmiştir. Önceki yöntemleri fitohemaglütininle, lipopolisakkarid 8 mitojenler kullanımı dahil ve EBV-aracılı ölümsüzleşme verimliliğini artırmak için mitojenle 9 pokeweed. Daha yakın zamanlarda, diğerleri immunosuppr kullanılansiklosporin gibi essive ajanlar, enfekte B hücrelerinin 7, 10-12 T hücre-aracılı öldürme inhibe .
EBV enfeksiyonu hücre hatlarının kurulması için zaman önemli uzunluğu sürücüler EBV-odaklı B hücre büyümesini dönüşüm için daha hızlı ve daha güvenilir yöntemleri için gereklilik. Yüksek titrede EBV ve immünsupresif ajan bir arada kullanarak, sürekli olarak, enfekte, dönüşümü, ve periferik kan B hücreleri LCL oluşturmak mümkün. Bu yöntem, hücrelerin in vitro kümeler bulaşmış periferik kan mononükleer hücreler küçük bir miktar ortaya konabilir kullanır . FK506, immünosupresan bir T hücre varlığı ile EBV CD23 varlığı. Geleneksel olarak, prolifere olan B hücreleri akıbet EBV enfeksiyonu sonrası yaklaşık bir hafta hücrelerin mikroskobik kümeler görselleştirme tarafından izlenir. LCL kümeleri birkaç hafta sonra çıplak gözle görülebilir. Belirlemek için bir test tarif eğer erken EBV-aracılı growth dönüşüm mikroskobik hücre kümeleri ortaya konabilir önce bile başarılı olur. CD23, varlığı yüksek CD58 + hücreleri gözlenen en erken üç gün sonrası enfeksiyon başarılı bir sonuç gösterir.
Protokol
1. EBV stok Preparation
- 75cm 2 doku kültürü şişesi steril tekniği kullanarak 3 x 5 10 hücre / ml; katlanarak büyüyen B95-8 hücreleri (13 ATCC # CRL 1612) Altkültür. Hücreler 37 0.5 mikrogram / ml tam RPMI 1640 yılında sırasıyla% 10 ısı inaktive fetal sığır serumu (FBS), Penisilin / 100U/ml az Streptomisin ve 100 mcg / ml içeren yetiştirilen ve Amfoterisin B ° C varlığında % 5 CO 2.
- Kırk sekiz saat sonra, 1 x 10 6 hücre / ml taze tam RPMI 1640 yılında tekrar süspansiyon hücreleri. Virüs üretim ikna etmek için, standart bir CO 2 inkübatör 1 saat 20ng/ml tetradecanoyl phorbol asetat (TPA) ve hücreleri uyarır. RPMI 1640 TPA kaldırmak için hücreleri üç kez yıkayın.
- Tam RPMI 1640 orijinal hacmi (1.2) hücreleri yeniden süspanse edin ve 96 saat için CO 2 inkübatör şişesi yerleştirin. Bu yöntem, bulaşıcı bir virüs par yüksek titreleri olduğu gösterilmiştirpartikülleri 6.
- 4 az 10 dakika süreyle 600 x g Santrifüj ° C hücreleri EBV içeren kültür süpernatant ayrı. Bir yıl boyunca -70 0.45 mikron filtre, kısım, ve mağaza ° C süzülür süpernatant.
ATCC (VR-1492) EBV içeren B95-8 hücreleri süpernatant ATCC tarafından önerilen seyreltme elde etmek ve kullanmak için bir alternatif.
2. Izolasyonu periferik kan mononükleer hücreleri (hücre)
- Heparinize şırınga veya heparinize kan tüpü içine vericiden alınan 10 ml kan çizin. Oda sıcaklığında 50 ml konik bir tüp içerisinde 20 ml PBS ile kan sulandırınız.
- 15 ml Ficoll Hypaque lenfosit ayırma orta Underlay seyreltilmiş kan. 30 dakika oda sıcaklığında frensiz, 225 x g'de santrifüjleyin .
- Yeni bir 50 ml konik tüp içine buffy coat ve transfer çıkarın. PBS ile 50 ml hacim kaldırın ve 10 dakika oda sıcaklığında 600 xg'de döndürün.
- Pour süpernatant kapalı. 50 ml PBS içinde pelet resuspending ve 10 dakika oda sıcaklığında 600 x g iplik hücreleri yıkayın. Benzer bir şekilde iki kez daha yıkayın.
- Süspanse edin 1 ml tam RPMI hücreler yıkanır. Tripan mavisi 1 / 10 dilüsyon hazırlamak için 5 mcL hücre kullanın. Hemasitometre kullanarak canlı hücre sayımı.
- 2 x 10 6 / ml, bir hücre konsantrasyonunu elde etmek için 25 cm 2 doku kültürü şişesi tam RPMI kullanarak ses seviyesini ayarlayın.
3. EBV enfeksiyonu
- 2.6 20 nM son bir konsantrasyonu hücre süspansiyonu FK506 (AG Bilimsel). 37 CO 2 inkübatör Yeri balon ° C 'de bir saat.
- Hızla EBV bir kısım Çözülme. Inkübatör balonun çıkarın ve 1 / 10 dilüsyon hücreleri EBV ekleyin. Tipik olarak, bu seyreltme bir İçişleri Bakanlığı 50-100 sağlar. 37 mix ve CO 2 inkübatör dik yerleştirmek Swirl balon ° C
Not incibaşarılı bir sonuç tahmin etmek için yapılan Adım 4, isteğe bağlı bir adımdır. Adım 4 yapılacak ise, kontrol olarak 2 x 10 6 hücre / ml un-enfekte hücre ek bir balon inkübe gerekecektir.
4. Hücrelerin hızla çoğalan nüfus (Opsiyonel adımı) belirlenmesi
- FACS tampon PBS +% 5 FBS: hazırlayın. Mağaza, 4 ° C
- Aşağıdaki antikor hücre boyama Adım 4.6 50 mcL hacmi her karışımları olun. Antikor dilüsyonları içeren 1mg/ml fare IgG (Sigma) antikorlarının non-spesifik bağlama inhibe FACS tampon yapılmalıdır.
- PE konjuge anti-CD23 antikoru (1 / 50 dilüsyon) ile tek lekeli
- FITC konjuge anti-CD58 antikoru (1 / 50 dilüsyon) ile tek lekeli
- PE-Cy5 konjuge anti-CD19 antikoru (1 / 50 dilüsyon) ile tek lekeli
- triple-lekeli CD23, CD58 ve CD19 (1 / 50 dilüsyon her)
- PE konjuge izotip kontrolü ile tek lekeliantikor CD23-PE için uygun (anti-CD23 antikoru ile aynı konsantrasyonda)
- FITC konjuge izotip kontrol antikoru (anti-CD58 antikoru ile aynı konsantrasyonda), CD58-FITC uygun tek lekeli
- tek lekeli PE-Cy5 konjuge izotip kontrol antikor uygun CD19-PE-Cy5 (anti-CD19 antikoru ile aynı konsantrasyonda)
- Her üç izotip kontrol antikorları ile triple-boyandı.
- EBV günde üç maruziyet sonrası, yavaşça girdap şişesi daha homojen bir hücre süspansiyonu elde etmek için. Şişeden 2ml Eppendorf tüpe 2ml çıkarın. 3000 rpm'de 3 dakika boyunca oda sıcaklığında bir mikrosantrifüj tüp Spin.
- 5 x 10 6 1 x 10 7 hücre / ml FACS tampon supernatant ve tekrar süspansiyon hücreleri aspire edin.
- Bireysel Eppendorf tüpleri içine sekiz 50μl bölüntülerin veya 96-iyi bir V-alt plaka çıkarın. Spin tüpler veya 1500 x g plaka3 dakika.
- Süpernatant ve vorteks tüpler / plaka atın. Her bir tüp içinde süspanse edin hücreleri / 4.2 hazırlanan uygun antikor dilüsyonları içeren FACS tampon 50 mcL.
- Tüpler / plaka, 30 dakika boyunca karanlıkta buz üzerinde inkübe edin. 3000 rpm'de 3 dakika Santrifüj hücreleri, süpernatant kaldırmak ve FACS tampon 200 mcL ekleyin. Hücrelerin tekrar santrifüj ve yıkama tamamlamak için süpernatant kaldırmak. Iki yıkar daha tekrarlayın.
- 200 mcL FACS yeniden süspanse hücreler 20.000 olaylar / tüp elde bir akış sitometresinin kullanarak veri tampon ve kazanır.
- WinMDI (PC FACS veri analizi için ücretsiz) kullanarak verileri analiz edin. Ileri ve yan dağılım profilleri kullanarak canlı hücreler üzerinde Kapısı. Daha sonra, canlı hücreleri CD19 + (B hücre belirteci), anti-CD19 antikoru uygun izotip kontrol antikoru ile boyanan hücreler ile karşılaştırırken sonra ifade için kapı . Arsa CD19 + canlı B hücreleri CD23 floresan ile y ekseni üzerinde x-ekseni ve CD58 için floresan. Belirleyin CD23 + ve CD58 + EBV maruz kalan hücrelerin eşleşen izotip kontrol antikorları ile boyandı karşılaştırarak hücreler. EBV maruz kalan kültür CD23 yüksek CD58 + hücreler (Şekil 2C) varlığı, EBV ile infekte büyüme transforme hücreler başarılı bir akıbet öngörüyor. Hücrelerinin EBV (Şekil 2A) maruz kalan ya da EBV (Şekil 2B) olmayan bir immortalizing zorlamalara maruz değildir aksine, CD23 yüksek CD58 + hücreler ortaya yoktur. CD23 yüksek CD58 + hücrelerin çoğalması tabi deneysel olarak gösterilmiş ve daha sonra LCL (14) kurulması olmuştur.
5. LCL genişletilmesi ve kriyoprezervasyon
- Işık mikroskobu ile hücrelerin Görselleştirme: EBV enfeksiyonundan bir hafta sonra, hücre kümeleri, ışık mikroskobu ile görülebilir. Şekil 3 balonuna erken mikroskobik kümeler (Şekil 3B) bir örnek gösterir.
- Zaman ilerledikçe, mikroskobik kümeler, büyük, yığınlarda görünür halemakroskobik balondaki. Şekil 3C, ışık mikroskobu ile kurulan LCL hücrelerin daha büyük kümeler gösterir.
- Hücreleri Besleme: 12 günlük kültür şişelerinde kültür ortamı hacmi ikiye katlayın. Daha sonra, tam RPMI kullanarak hacmi 2-3 kat artmaktadır kültür genişletin.
- Besleyen hücreleri periyodikliği hücre büyüme oranı esas alınarak tespit edilmelidir. Kültür ortamı, sarı yandığında, genellikle yukarıdaki gibi medya değiştirme zamanı. Genellikle, haftada bir kere ortaya çıkar. Ancak, bazı hücre hatları daha fazla veya daha az sık sık beslenen gerekebilir. Önümüzdeki birkaç hafta içinde 75-100 ml kültür genişletin.
- Kriyoprezervasyon hücreleri aşağı dondurma, oda sıcaklığında 10 dakika boyunca 600 x g santrifüj hücreleri. 1 x 10 7 hücre / ml 'de% 90 FBS içeren soğuk dondurucu orta ve% 10 dimethylsülfoksit supernatant ve tekrar süspansiyon hücre pelletini çıkarın. Sıvı azot tüpü yerleştirin.
6. Temsilcisi sonuçları:
CD23 yüksek CD58 + hücrelerin varlığı ile başarılı bir sonuç tahmin ediliyor. Bu profili (Şekil 2C) EBV maruz kaldıktan sonra 3-4 gün canlı hücrelerin yaklaşık% 2-3 olmalıdır. Diğer CD23 alt-popülasyonları +, CD23 -, CD58 + ve CD58 hücreler EBV maruz kaldıktan sonra en az 14 çoğalması göstermek gözlenmektedir. EBV olmayan bir immortalizing gerginlik barındıran HH514-16 hücreleri (Şekil 2B), EBV maruz Un-enfekte olmuş hücreleri (Şekil 2A) ve hücreler CD23 yüksek CD58 + hücreler olduğunu göstermez.
Bir hafta içinde, Daha önce de belirtildiği gibi EBV enfeksiyonu sonrası, balon hücrelerin küçük kümeler tarafından görülebilir ışık mikroskobu (Şekil 3B): Aynı zamanda başarılı bir sonuç izlemek için ışık mikroskobu ile hücrelerin görselleştirmek olabilir. Zaman ilerledikçe ve hücreleri LCL geliştikçe, mikroskobik kümeler kümeleri balon makroskopik olarak görünür olduğundan (3C Şekil) daha büyük olur.
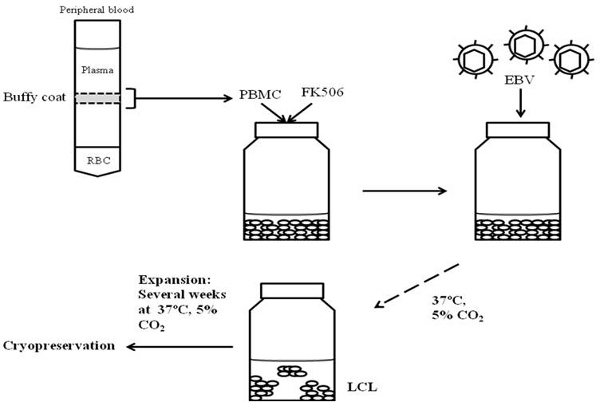
Şekil 1 lenfoblastoid hücre hatları üretimi ve dondurulması için iş akışı. Periferik kan bir Ficoll degrade ile santrifüj edilir. Kurulmuş bir degrade buffy coat PBMC mevcut EBV ilavesi ile takip FK506 maruz kalmaktadır. EBV maruz kalan hücreleri 37 ° C daha sonra dondurulması için LCL kurmak ve genişletmek için 5% CO 2 varlığında yetiştirilmektedir.
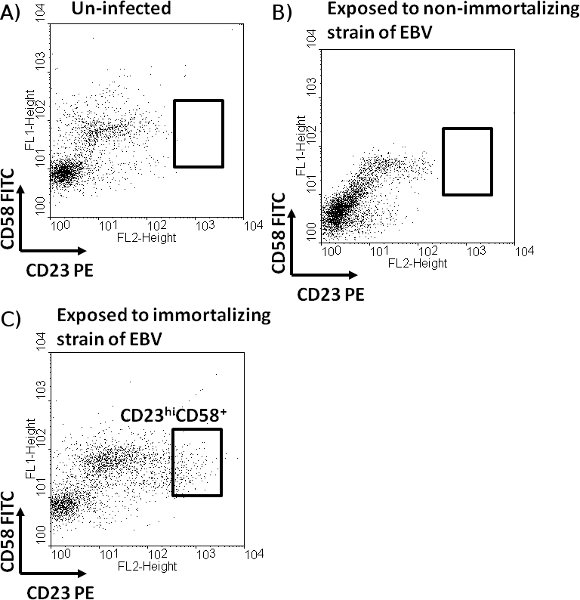
Şekil 2 B hücreleri EBV maruz kaldıktan sonra yayılması geçmesi beklenen bir alt nüfusun belirlenmesi . Un-enfekte hücre (A) veya hücre HH514-16 hücreleri (B) veya B95-8 FK506 varlığı hücreleri (C) elde edilen EBV maruz 3. günde hasat edildi. Hücreler, CD19, CD23 ve CD58 yöneltilen florokrom-konjuge antikor ile boyandı. Yolluk sonra canlı hücres, un-enfekte (A) ve EBV maruz kalan (B ve C) CD19 + B hücreleri CD23 ve CD58 ekspresyonu incelendi. B hücreleri CD23, CD58 ve yüksek düzeyde (CD23 yüksek CD58 +), ifade bir alt nüfus tasvir, sadece dönüşüm yetkin EBV (B95-8 hücreleri elde) maruz kalan hücrelerde gözlemlemiştir.
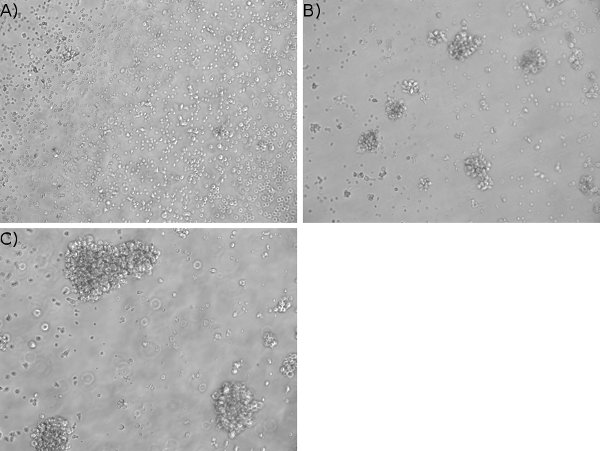
Şekil 3 EBV ile enfekte hücrelerde hücre kümeleri Görselleştirme. PBMC FK506 ile tedavi edilen ve EBV ile enfekte edildi. Un-enfekte (A) ve EBV maruz kalan (B) hücrelerin faz kontrast mikroskobu (10X büyütme) bir hafta sonrası enfeksiyon incelendi. Beş haftalık lenfoblastoid hücre hattı C ile gösterilir
Tartışmalar
Bu makalede açıklanan yöntemi hızlı ölümsüzleşme ve kriyoprezervasyon kez vericinin periferik kan LCL üretir. FK506 kullanımı sayesinde, T immünosupresan hücre ve bulaşıcı virüsün yüksek titreleri periferik kan mononükleer hücrelerinin EBV ile enfekte B hücrelerinin yayılması teşvik etmek mümkün. Bu müdahaleler, daha sonraki deneyler için hücreleri hızlı bir şekilde genişlemesi sonucunda açıklanan yöntem daha verimli olun.
Geleneksel olarak, büyüme dönüşümü maruz kaldıktan sonra yaklaşık bir hafta EBV 6, 15 ışık mikroskobu ile hücre kümeleri görselleştirme tarafından izlenir olmuştur. Ancak, hücre kümelenme EBV-aracılı büyüme dönüşüm belirli bir göstergesi değildir. Daha önce, üç gün kıç, en erken zamanda başarılı sonucunu belirlemek için doğru bir ve belirli bir yöntem sağlayan, flow sitometri 14 ile proliferatif hücre popülasyonu tutarlı bir kimlik gösterdiB hücrelerinin EBV er maruz kalma.
Açıklamalar
Çıkar çatışması ilan etti.
Teşekkürler
Bu araştırma NIH hibe programı K08 AI062732, K12 HD001401 ve 1UL1RR024139-02 ve SB-M Charles H. Hood Vakfı Çocuk Sağlığı Eğitim ve Araştırma Burs tarafından finanse edildi. Stony Brook, New York Eyalet Üniversitesi Araştırma Vakfı tarafından.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Şirket | Katalog numarası | ||
| Amfoterisin B | Fisher Bioreagents | BP 928-250 | |
| Dimethylsülfoksit | Sigma | D 2650 | |
| Fetal sığır serumu, ısı ile inaktive | Sigma | F 4135 | |
| Ficoll Hypaque lenfosit ayrılması medya | Mediatech | 25-072 | |
| FK506 | AG Bilimsel | F 1030 | |
| Fare serumu ile IgG | Sigma | Ben 8765 | |
| PE konjuge fare anti-insan CD23 | BD Pharmingen | 555711 | |
| PE konjuge Fare izotip IgG1 | BD Pharmingen | 554680 | |
| FITC için konjuge fare anti-insan CD58 | Pierce Thermo SCientific | MA1-82.159 | |
| FITC için konjuge Fare izotip IgG1 | BD Pharmingen | 550616 | |
| PE-Cy5 konjuge fare anti-insan CD19 | BD Pharmingen | 555414 | |
| PE-Cy5 konjuge Fare izotip IgG1 | Dako | X 0955 | |
| Penisilin / Streptomisin | Gibco | 15140-122 | |
| RPMI 1640 medya | Sigma | R 8758 | |
| Tetradecanoyl phorbol asetat (TPA) | Calbiochem | 407952 | |
| FACS Tampon (1X Fosfat Tamponlu Salin +% 5 fetal sığır serumu) |
Referanslar
- Thorley-Lawson, D. A., Gross, A. Persistence of the Epstein-Barr virus and the origins of associated lymphomas. N. Engl. J. Med. 350, 1328-1337 (2004).
- Kubuschok, B. Use of spontaneous Epstein-Barr virus lymphoblastoid cell lines genetically modified to express tumor antigen as cancer vaccines: mutated p21 ras oncogene in pancreatic carcinoma as a model. Hum. Gene Ther. 13, 815-827 (2002).
- Kuppers, R. B cells under influence: transformation of B cells by Epstein-Barr virus. Nat. Rev. Immunol. 3, 801-812 (2003).
- Traggiai, E. An efficient method to make human monoclonal antibodies from memory B cells: potent neutralization of SARS coronavirus. Nat. Med. 10, 871-875 (2004).
- Bernasconi, N., Traggiai, E., Lanzavecchia, A. Maintenance of serological memory by polyclonal activation of human memory B cells. Science. 298, 2199-2202 (2002).
- Oh, H. -M. An efficient method for the rapid establishment of Epstein-Barr virus immortalization of human B lymphocytes. Cell Prolif. 36, 191-197 (2003).
- Ventura, M. Use of a simple method for the Epstein-Barr virus transformation of lymphocytes from members of large families of Reunion Island. Hum. Hered. 38, 36-43 (1988).
- Henderson, E. Efficiency of transformation of lymphocytes by Epstein-Barr virus. Virology. 76, 152-163 (1977).
- Bird, A. G. Characteristics of Epstein-Barr virus activation of human B lymphocytes. J. Exp. Med. 154, 832-839 (1981).
- Neitzel, H. A routine method for the establishment of permanent growing lymphoblastoid cell lines. Hum. Genet. 73, 320-326 (1986).
- Pelloquin, F., Lamelin, J. P., Lenoir, G. M. Human B lymphocytes immortalization by Epstein-Barr virus in the presence of cyclosporin A. In Vitro Cell Dev. Biol. 22, 689-694 (1986).
- Pressman, S., Rotter, J. I. Epstein-Barr virus transformation of cryopreserved lymphocytes: prolonged experience with technique. Am. J. Hum. Genet. 49, 467-467 (1991).
- Miller, G. Epstein-Barr virus: Transformation, cytopathic changes, and viral antigens in squirrel monkey and marmoset leukocytes. Proc. Nat. Acad. Sci. 69, 383-387 (1972).
- Megyola, C., Ye, J., Bhaduri-McIntosh, S. Identification of a sub-population of B cells that proliferates after infection with Epstein-Barr virus. Virol. J. 8, 84-84 (2011).
- Tosato, G., Cohen, J. Generation of Epstein-Barr virus (EBV)-immortalized B cell lines. Current Protocols of Immunology. Chapter 7, 22-22 (1991).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır