Method Article
INTERCEPT Kan Sistemi kullanılarak hazırlanması ve Çift Doz Buffy Coat Trombosit Ürünleri Patojen inaktivasyon
Bu Makalede
Özet
Bu makalede, tam kan bağışlarından hazırlanmıştır ve patojen inaktivasyonu için INTERCEPT Kan Sistemi ile tedavi çift doz buffy coat trombosit konsantreleri üretmek için Örebro Üniversitesi Hastanesi tarafından kullanılan işlem açıklanmaktadır. In vitro kaliteli depolama 7 gün içinde değerlendirilir.
Özet
Kan merkezleri maksimize üretim aldıkları kan ürünü bağışlardan verimi yanı sıra transfüzyon bulaşan hastalıklardan korunma dahil transfüzyon hastalar için güvenlik en üst düzeyde sağlanması da dahil olmak üzere pek çok sorun ile karşı karşıyayız. Bu sarf malzemeleri, ekipman, atık, ve diğerleri arasında personel giderleri de dahil olmak üzere işletme giderleri en aza indiren bir mali açıdan sorumlu bir şekilde yerine getirmesi gerekir.
Çeşitli yöntemler trombosit transfüzyonu konsantreleri üretmek için kullanılabilir. En yaygın olanlarından biri, tek bir terapötik trombosit ünitesi (birim başına ya da yerel yönetmeliklere başına ≥ 2,0 x10 11 trombositler) altı tam kan bağış kadar gelen buffy coat tabakası havuzu tarafından hazırlanan olduğu buffy coat yöntemdir. "Çift doz" tam kan türetilmiş trombosit üretimi için bir prosedür sadece son zamanlarda geliştirilmiştir.
Hazırlanması için yeni bir yöntem olup burada sunulançift doz tam kan türetilmiş trombosit 7 buffy mont ve sonradan patojen inaktivasyonu için INTERCEPT Kan Sistemi ile çift doz birimleri tedavi havuzları yoğunlaşmaktadır. INTERCEPT virüsler, bakteriler, parazitler ve bağışlanan kan mevcut olabilir kirlenmesine donör beyaz hücreleri etkisiz hale geliştirilmiştir. , Çift Saklama Kapları ("DS kümesi") ile ayarlayın INTERCEPT İşleme kullanarak çift doz buffy coat yöntemi ile KESMENOKTASI eşleştirme böylece hasta güvenliği maksimize, kan merkezleri tek bir patojen inaktivasyonu işleme seti kendi çift doz birimlerinin her tedavi sağlar maliyetleri en aza indirirken. Çift doz buffy coat yöntemi az buffy kat gerektirir ve tek doz buffy coat trombosit birimlerin hazırlanması ve tedavi ile karşılaştırıldığında% 50 (örneğin havuzlama setleri, filtre setleri, trombosit katkı çözümü ve steril bağlantı gofret) varan sarf kullanımını azaltır . Diğer maliyet tasarrufu daha az atık, daha az ekipman Maintenan dahilce, düşük güç gereksinimleri, personel zamanı azalır ve daha düşük toplama maliyeti aferez teknikle karşılaştırıldığında.
Protokol
1. Tam Kan Toplama
- 450 ml üst gönüllü bağışçılardan kan toplayın / alt koleksiyonu lokal kan toplama kurallarına göre ayarlar.
- Tam kan santrifüjleme ve ayırmasından önce bir soğutucu plaka üzerinde 2 saat arasında, en az saklanır.
2. Buffy Coat Hazırlık
- Kırmızı kan hücreleri, buffy coat, ve plazma: üç kat içine kan ayırmak için bir sabit döndürme ile tam kan santrifüjleyin. Ikinci Santrifüj değerleri ± 2 ° C'de 22 dakika süreyle 4,880 11 RCF idi
- Toplama kaplarına buffy coat bırakarak, üst uydu çantası ve alt uydu torbaya kırmızı kan hücreleri (RBC) içine plazma ifade etmek için bir otomatik kan ayırıcı kullanılır. Buffy kat sırasıyla yaklaşık 48 ml ve% 37, olan hacim ve hematokrit aralıkları demek hedefleyin.
- Buffy-mont 22 ± 2 ° C'de trombosit karıştırıcı gecede saklanır
3. Buffy Coat Pooling
- Steril connect 7 buffy mont ve paralel çizgiler bulunan bir tren yapılandırmada SSP + trombosit katkı çözeltisi (PAS), 300 ml tren uzunluğunu azaltmak için; PAS trenin üstünde olmalıdır. PAS ve ilk buffy coat arasındaki çizgi Kelepçe.
- Buffy coat birimler arasındaki steril bağlantıları açın ve buffy kat son kabın içine boşaltın.
- Kaynak ve PAS ve ilk buffy coat arasındaki kelepçesini açın. Katkı çözelti üçte biri sırayla buffy coat kapların her biri yoluyla durulama izin verin. 2 kez daha kalan PAS yarısını kullanarak her zaman tekrarlayın.
- Ortalama buffy coat havuz hacminin yaklaşık olarak 600 ml olmalıdır. Bireysel buffy kat hedef hacmi ve hematokrit yerine getirilirse, plazma oranı 32 olacak -% 47 daha sonra işlem içinde INTERCEPT patojen inaktivasyonu tedavisi için gerekli olduğu gibi.
- Boş SSP + ve buffy atınkat kaplar.
- Optimum trombosit kurtarma için, santrifüj önce 1 saat boyunca karıştırıcı üzerinde havuz tutmak.
- Steril buffy coat havuza entegre leukoreduction filtre ile trombosit saklama kabı bağlayın.
- Süspansiyon trombositlerin (9 dak, 20 sn için 462 RCF) gelen kırmızı kan hücreleri ayırmak için buffy coat havuz "yumuşak spin" gerçekleştirin. Trombosit saklama kabı içine leukoreduction filtre üzerinden otomatik bir kan ayırıcı kullanarak trombosit süspansiyonu ifade.
- 420 ml'lik hacim, 2,5-7,0 x 10 11 trombosit dozu ve ≤ 4 x 10 6 / ml kırmızı hücreleri - Daha önce açıklandığı gibi, işleme gereklilikleri trombosit süspansiyonu INTERCEPT 300 ml işleme özelliklerine uygun olduğundan emin olun.
4. Tedavi KESMENOKTASI
- Toplandıktan sonra, 1. Gün sonunda (gün 0 toplama günü) önce INTERCEPT tedaviyi gerçekleştirin.
- INTERCEPT İşleme Seti unwrapŞeffaf plastik torbadan Çift Saklama Kapları ile.
- Steril INTERCEPT işleme sette amotosalen kabın hortumuna trombosit süspansiyonu konteyner bağlayın.
- Yerel gereksinimler aşağıdaki uygun kan ürünü tanımlama ile INTERCEPT işleme seti saklama kapları etiketleyin.
- Trombositler asın ve aydınlatma kabına akmaya amotosalen çözüm sağlayan, ilk amotosalen kapsayıcısındaki alt kanül bölünürler. Trombositler aydınlatma kabına amotosalen konteyner akmasına izin amotosalen kapsayıcısındaki üst kanül kırın.
- Yavaşça trombosit ve amotosalen karışımı karıştırın ve amotosalen kabına aydınlatma kabından hava ifade.
- Hortumun yaklaşık 4 cm, doldurma borusuna trombosit karışım küçük bir miktar ifade eder. Bu tüp ve aydınlatma kabı hem de trombositler patojen inactivati geçmesi sağlanırtedavi.
- Aydınlatma konteyner ve amotosalen konteyner arasındaki boru mühürleyin. Aydınlatma konteyner uzanan boru yaklaşık 4 cm'den daha bırak. Çıkarın ve atın boş trombosit ve amotosalen kaplar ve örnekleme torbalar üzerindeki kelepçe kapatın.
- Soldaki büyük bölme içinde aydınlatma kap ve sağ tarafta daha küçük bölme içinde düzenleyici ile aydınlatıcı içine işleme grubu yerleştirin.
- Aydınlatıcı içine bağışı kimliği, ürün kodu, ve işleme set lot numarası girmek için el barkod aygıtı kullanın. Metal kapağını kapatın ve aydınlatıcı grafik arayüzü istendiğinde, çekmeceyi kapatın. Aydınlatma başlatmak için "Başlat" düğmesine basın.
- Aydınlatma sonra aydınlatıcıdan işleme seti kaldırın. Aydınlatıcı otomatik işlenmiş trombosit birim (ler) için tedavi raporu yazdırır.
- Organizatörü konteyner açmak ve p asmaklatelets ve işlem seti, aydınlatma kabın çıkışındaki kanül kırmak ve trombositler bileşik emme cihazı (CAD) bir kaba akmasına izin verir.
- Bir plazma çıkarıcı kullanarak aydınlatma kabına CAD kabından hava ifade, CAD gofret eğmemeye bakımı.
- CAD konteynerin giriş noktasına yakın boru kapatılmalıdır. Çıkarın ve boş aydınlatma kabı atın.
- En az 6 saat boyunca bir karıştırıcı üzerinde trombosit bağlı depolama kapları ile CAD konteyner, ancak en fazla 16 saat yerleştirin. Bu ≤ 2 uM'lik bir konsantrasyona kalıntı amotosalen azalma ile sonuçlanacaktır.
- CAD Tedaviden sonra, karıştırıcı gelen trombosit birimleri çıkarın. Trombositler asın. Kanül kırın ve trombosit saklama kapları içine akmasına izin verin.
- CAD kabına saklama kapları havayı ifade eder. Rezidüel trombosit konsantresi geri akışı saklama kapları içine tarafından Letyerçekimi. Y-uydurma Yukarıda tüp mühür ve boş CAD kabı çıkarın.
- Gerektiği gibi saklama kapları arasındaki yeniden dağıtın hacmi. Cilt ayarlamalar depolama konteynerleri tartı ile yapılır. Bir kaç santimetre saklama kabının giriş yukarıdaki her bir depolama konteyner için hortum mühür; 5.2 'de tarif edildiği gibi bu, son ürünün bir steril bir örnek elde kolaylaştırır.
5. Ürün Örnekleme
- Rutin QC test için nihai depolama kapları saklama kapları üzerinde örnekleme kese kullanılarak kez tadılabilir. Bunu yapmak için, platelet birim iyice karıştırılmış sağlamak, daha sonra torba için kelepçeyi açmak ve birkaç kez sıkın. Kese trombositler ile doldurduktan sonra tüp mühürleyin. Uygun bir laboratuvar tüpüne trombosit örneği aktarın ve hemen testleri gerçekleştirin.
- Bu tür bir çalışmada, doğrulama için olduğu gibi, depolama boyunca birden çok zaman noktasında örnekler elde etmek için, steril bağlamakTrombosit saklama kabı boru için yeni bir numune kabı. Trombositler de örnekleme konteynere aktarmak için önce karıştırılmalıdır emin olun.
6. In vitro Fonksiyonunun Değerlendirilmesi
- Bu validasyon çalışması için, in vitro değerlendirilmesi CAD tedavisi (Gün 1 veya Gün 2, CAD süresine bağlı olarak) sonra tekrar 4. Gün yapıldı (veya Gün 5) ve Günlük 7. Vitro ölçümlerde hacmi, trombosit sayımı, pH, dahil kan gazı (pO 2, pCO 2), glikoz, laktat ve dönen.
- Cilt katkı maddesi çözelti içinde, trombositler 'in özgül ağırlık olarak 1.01 g / ml ile ağırlık ile tespit edildi.
- Hemoglobin kontaminasyon bir renk skalası ile karşılaştırma kullanılarak görsel olarak değerlendirildi.
- Dönen bir görsel olarak tespit edilmiştir.
- Diğer testlerin metodolojisi için "ekipman Tablosu" na bakınız.
7. Temsilcisi Sonuçlar
D üretme süreciouble doz buffy coat trombosit hacmi ve hematokrit için hedef özelliklerine uygun bireysel buffy mont üretimi ile başlar. Bu son işlem doğrulama sırasında bireysel buffy kat hematokrit ölçmek için pratik olmadığı gibi, biz sürekli olarak hedef hacmi ve hematokrit karşılamak olabilir sağlamak için elimizden buffy kat optimize etmek için ayrı bir çaba üstlenerek başladı. Tablo 1 de gösterildiği gibi, Optimize buffy kat 46, hacim ve hematokrit her ikisi de ± 2 ml ve 37 ±% 3, sırasıyla için hedef değerleri ile karşılaştırıldığında olumlu.
Havuzlama sonra, buffy coat havuz hacminin ve hematokrit, sırasıyla, yumuşak sıkma santrifüj işleminden önce yaklaşık olarak 600 mL% 20 olmalıdır. Tablo 2 de gösterildiği gibi, havuzlar buffy coat 615 ortalama ± 5 ml; hematokrit 19 ortalama ±% 1.
Bir çift doz trombosit kons içinde yumuşak sıkma santrifüj sonuçlarıINTERCEPT Kan Sistemi DS işleme seti kullanılarak patojen inaktivasyonu için girdi şartlarını karşılayacak entrate. INTERCEPT tedavi için anahtar giriş parametreleri hacmi, trombosit, plazma oranı ve RBC içerik bulunmaktadır. Ayrıca, buffy coat havuzu ile karşılaştırıldığında trombosit konsantresi içinde trombositlerin ≥% 75 kurtarmak hedefliyoruz. Yerel gereksinimlere Per, beyaz kan hücresi (WBC) kirlenme <1x10 6 / birim olmalıdır. Trombosit, doğrulama içinde konsantre KESMENOKTASı tedavisi yanı sıra WBC kirlenme ve Tablo 3'te gösterildiği gibi trombosit kurtarma için hedefler için anahtar parametreler araya.
Patojen inaktivasyonu için INTERCEPT işlemi tek bir INTERCEPT işleme seti kullanarak çift doz trombosit konsantresi yapılır. Işlem seti, tedavi edilen birim yol tamamlanmasından az iki ayrı terapötik trombosit doz halinde bölünebilir izin veren iki tamamlayıcı depolama konteynerleri içermektedirogen inaktivasyonu süreci. Avrupa yönergeleri test birimlerinin% 75 ≥ 200x10 9 trombositler içermesini gerektirir başına terapötik dose1; İsveç'teki yerel gereksinimler test birimlerinin% 75 içerdikleri> doz başına 240x10 9 trombositler gerektirir. INTERCEPT Tedaviden sonra, ortalama trombosit içeriği 265 oldu ± 22 x10 9 (n = 24). Ayrıca, ünitelerin% 88 yerine veya terapötik doz başına 240x10 9 trombositler aştı; Bu Avrupa yönergeleri ve İsveç yasalarına hem dahilindedir. Çift doz buffy coat hazırlanması ve sırasıyla KESMENOKTASı tedavi süreçlerinin bir örnek için Şekil 1 ve 2'ye bakınız.
Bu doğrulama için, trombosit in vitro özellikleri INTERCEPT tedavisi (bireysel depolama kapları içine bölünmüş sonra yani) sonra konsantreleri ölçülür; parametreleri depolama 7 gün boyunca ölçüldü. Ortalama ve standart sapma için toplandıtrombosit dozunun, pH, pO2, pCO 2, laktat üretim ve glukoz tüketimi.
Şekil 3, depolama, 7 gün boyunca KESMENOKTASı tedavi sonrası bölünme ürünlerinin her biri içinde KESMENOKTASı tedavi ve ortalama trombosit doz verilmeden önce iki doz trombosit konsantresi trombosit başlangıç dozu ortalaması gösterilmiştir. Depolama sırasında Trombosit kaybı yaklaşık% 9 idi. Bu azalma konvansiyonel trombositlerin depolama sırasında trombositlerin beklenen kayıp farklı değildir. 2
Tablo 4 tek birimler halinde tedavi ve bölme sonra INTERCEPT trombositlerin in vitro özelliklerini özetlemektedir.
Avrupa standartlarına Per, trombositlerin pH raf ömrünün sonuna kadar 6.4 üzerinde kalmalıdır. Işlem sırasında, trombosit pH değeri hafifçe trombosit konsantrasyon, ses ve trombosit sto gaz geçirgenliği esas damla konsantreöfke konteyner. Şekil 4, depolama, 7 gün boyunca bölünmüş trombosit ürünlerin pH göstermektedir. Depolama sırasında, pH kararlı olduğunu ve iyi işleme ihtiyaç içinde yapılmaktadır.
Olarak Şekil 5A ve 5B, trombosit O2 tüketimi ve CO 2 de gösterildiği depolama 7 gün boyunca PL2410 kap içinde INTERCEPT trombositlerinde solunum devam etmektedir. Şekil 6A ve 6B, depolama, 7 gün boyunca laktat ve glikoz düzeyleri göstermektedir . Trombosit glukoz tüketimi ve laktat üretimi depolama 7 gün boyunca birbirleri ile tutarlıdır. 5 birim glikoz seviyesi daha az 1.11 mmol / l (glükoz tahlil için alt sınır) vardı.
Özellikle, hacmi, trombosit, plazma oranı ve kırmızı bl; buffy coat hazırlanması ve havuzlama doğrulama üretilen trombosit olduğunu KESMENOKTASı tedavisi için giriş kriterlerini karşılayan konsantreleriood hücre kontaminasyonu. Nihai birimleri trombosit dozu ve pH dahil depolama 7 gün içinde geçerlilik kriterlerini karşıladı.
| Parametre | Hedef Aralığı | Sonuçlar ± SD |
| Hacim (ml) | ~ 48 | 46 ± 2 |
| Hematokrit (%) | ~ 37 | 37 ± 3 |
| Havuzlama önce zaman tutun | Karıştırıcı üzerinde Overnight | Karıştırıcı üzerinde Overnight |
Bireysel Buffy Palto (n = 19) Tablo 1. Özellikler.
| Parametre | Hedef Aralığı | Sonuçlar ± SD |
| Hacim (ml) | ~ 600 | 615 ± 5 |
| Hematocrit (%) | ~ 20 | 19 ± 1 |
| Santrifüj önce zaman tutun | Karıştırıcı üzerinde 1 saat | Karıştırıcı üzerinde 1 saat |
Buffy Coat Havuzları (n = 12) Tablo 2. Özellikler.
| Parametre | Hedef | Sonuçlar ± SD |
| Hacim (ml) | 370-420 | 404 ± 8 |
| Trombosit sayımı (x10 9 / birim) | 250 - 700 | 577 ± 62 |
| Trombosit kurtarma (%) Ortalama | ≥ 75 | 75 ± 4 |
| Plazma oranı (%) | 32-47 | 38 ± 1 |
| RBC (x10 6 / ml) | ≤ 4 | 1.2 ± 0.4 |
| WBC (x10 6 / birim) | ≤ 1 | 0.11 ± 0.1 |
| INTERCEPT (saat) önce zaman tutun | Günde 1 ≤ sonu | Günde 1 ≤ sonu |
Çift Doz Trombosit Tablo 3. Özellikleri (n = 12) konsantreler.
| Ortalama ± SD | Min | Maksimum | |
| Hacim (ml) | 199 ± 16 | 182 | 236 |
| Trombosit sayımı (x10 9 / birim) | 265 ± 22 | 225 | 292 |
| pH (22 ° C) | 6.9 ± 0.1 | 6.8 | 7 |
| pO 2 (kPa) | 21.4 ± 4.8 | 12.8 | 27.3 |
| pCO 2 (kPa) | 4.3 & plusmn; 0.4 | 3.3 | 4.9 |
| Laktat (mmol / l) | 9.1 ± 1.7 | 6.8 | 12.4 |
| Glukoz (mmol / l) | 5.3 ± 0.9 | 3.7 | 6.5 |
INTERCEPT Tedavi Trombositler Gün 1/2 (Tek Üniteleri, n = 24) Tablo 4. Özellikler.
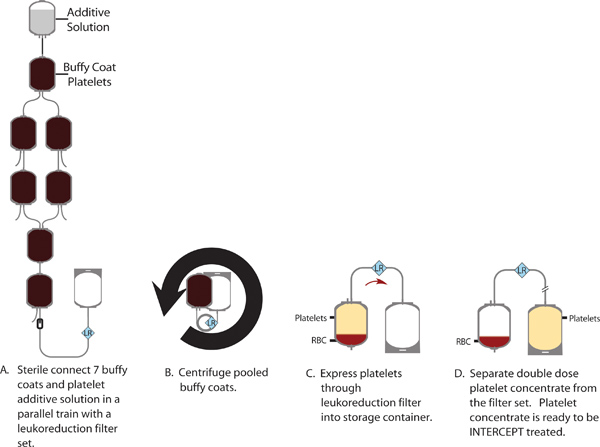
Şekil 1. 7 buffy kat havuzundan bir çift doz trombosit konsantresi üretimi.
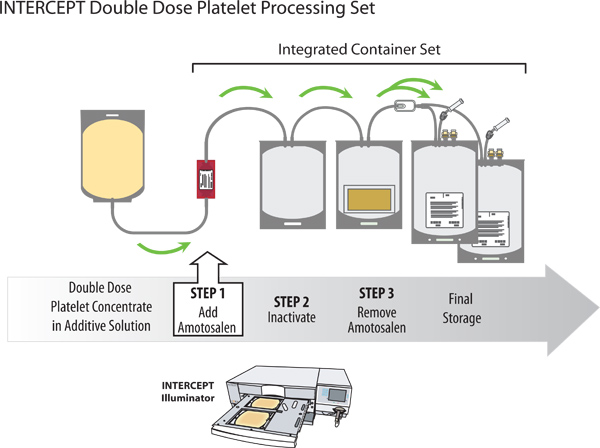
Şekil 2. INTERCEPT Kan Sistemi ile çift doz trombosit konsantresi Patojen inaktivasyon.
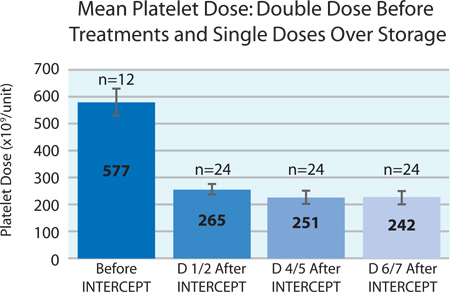
Şekil 3. Önce ve için trombosit dozu ortalamaINTERCEPT uygulamadan sonra 7 gün (n KESMENOKTASı önce = 12; KESMENOKTASı sonra n = 24).
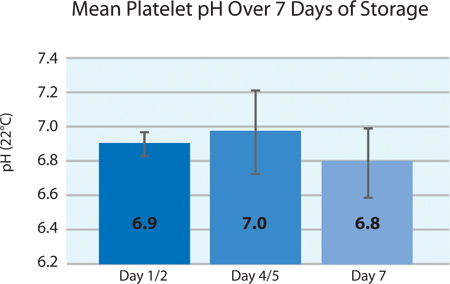
Şekil 4. KESMENOKTASI tedavisi (n = 24) sonra trombosit pH ± SD.
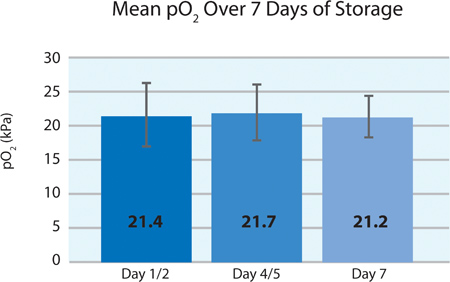
Şekil 5A. KESMENOKTASI tedavisi (n = 24) sonra pO 2 ± SD.
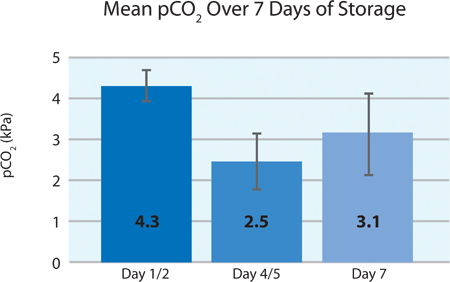
Şekil 5B. KESMENOKTASI tedavisi (n = 24) sonra pO 2 ± SD.
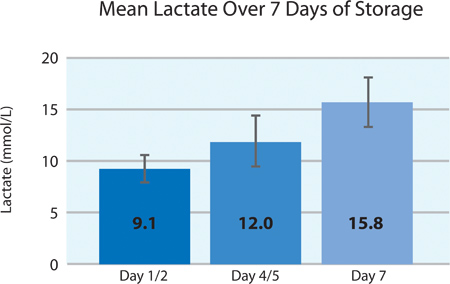
Şekil 6A. KESMENOKTASI tedavisi (n = 24) sonra laktat düzeyleri ± SD.
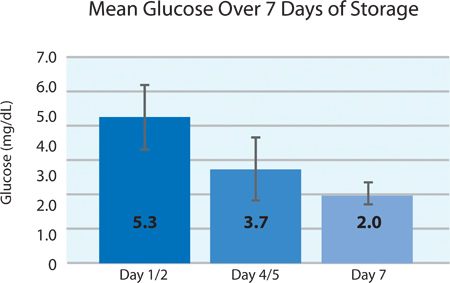
Şekil 6B. & Glukoz düzeyi ortalamaplusmn; SD KESMENOKTASI tedaviden sonra (n = 24).
Tartışmalar
Buffy coat trombositler birkaç işlem adımları gerektiren trombosit adet üretim toplam maliyeti çarpanlarına olmalıdır personeli zaman, sarf malzemeleri, ekipman ve atıklar dahil post-toplama maliyetleri, sonuç. Her buffy coat gelen trombosit verimi (buffy coat hacmi ve hematokrit optimize yoluyla) Geliştirilmesi yedi buffy kat havuzundan bir çift doz buffy coat trombosit ünitesi üretimini sağlar. Bu iyileştirme işlemi gerçekleştirildiğinde, buffy kat sayısı trombosit doz, sabit bir sayı üretmek için gerekli azaltılabilir, böylece buffy kat genel kullanımını geliştirmek ve ilave trombosit üretimi (PC) konsantre olanak tanır. Personel zaman yanı sıra havuzlama setleri, trombosit katkı çözeltisi, steril bağlantısı gofret, filtre setleri ve santrifüj işlemleri gibi sarf ve ekipman maliyetlerini% 50 kadar azalır. Trombosit üretimini optimize edip, thi ilişkili maliyetleri azaltmanın yanı sıras havuzlama yöntemi bize de bizim transfüzyon alıcılara gelişmiş koruma sağlamak için izin, KESMENOKTASI ikili saklama kabı işleme seti ile kullanmak için giriş gereksinimi karşılayan bir trombosit konsantresi (PC) üretebilirsiniz.
Patojen inaktivasyonu için INTERCEPT Kan Sistemi nükleik asit çoğaltma ve hastalığa neden yapamaz render patojenlerin önlenmesi, kovalent çapraz bağ DNA ve RNA amotosalen ve ultraviyole A (UVA) ışık kullanır. 3. Bu etkili virüs, bakteri gibi patojenlerin geniş bir yelpaze inaktive , parazitler ve kirletici donör beyaz kan hücreleri. 4-6 KESMENOKTASI yeni bir test geliştirdi ve sonuçta uygulamak için önemli bir finansal yatırım gerektiriyor ise tarihsel önemli bir gecikme içerir çıkan patojenler için mevcut test paradigma, bir alternatif sağlar zaman bir test kullanılabilir hale gelir. 7,8 ayrıca gereksiz emniyet measu bir alternatif sağlayabilirbakteriyel algılama 9 ve gama ışınlama gibi res. Ayrıca 10-12, KESMENOKTASI bize çift doz trombosit birimleri tedavi sağlayan üretim verimliliği faydaları ve bize bizim bütçe uygun olur.
KESMENOKTASı ve çift doz buffy coat yöntemi kan merkezi iş akışları çeşitli adapte edilebilir. Örnek olarak, tam kan koleksiyon 500 ml 'ye edilebilir; koleksiyonları da 22 gece boyunca saklanabilir ° C ayırma ile elde edilebilir. Buna ek olarak, alternatif bir buffy coat biriktirme yöntemi mümkün değildir (örneğin bir ahtapot yöntem yerine bir tren metod) ve / veya otomatik bir cihaz (örneğin TACSI) geri kalan kırmızı hücrelerden ikinci santrifüjleme ve trombosit süspansiyonu ayrılması için kullanılabilmektedir .
Artmış trombosit içerik gerekiyorsa, çeşitli teknikler trombosit sayımı, tam kan gecelik inkübasyon, adjus dayalı donörlerin ön seçimi de dahil olmak üzere mevcutsantrifüj ayarlar tment, 7 ya da yerine 8 buffy kat bir havuz sunulabilir.
Araya gelme sınırlaması nedeniyle mevcut ve santrifüj kova kapasitesi setleri, buffy coat havuzunun toplam hacmi yaklaşık 600 ml olmalıdır. Bu protokolü açıklanan santrifüj işlemi ve ayarlar 7 buffy kat bir havuz için KESMENOKTASI parametreleri karşılayan ürünü elde etmek için optimize edilmiştir. Havuzda buffy kat sayısı değiştirilirse santrifüj ayarlarını modifiye edilmelidir.
Bazı ülkelerde, asgari trombosit dozu yüksek ve QC gereksinimleri İsveç'te daha katıdır. Bu nedenle, bizim sonuçlar evrensel olarak uygulanabilir olmayabilir. Bu ülkelerde, önceki KESMENOKTASI tedaviye çift doz PC KESMENOKTASI tedavi ve bölünme sonra yerel gereksinimlerini karşılamak amacıyla trombositlerin sayıda içermesi gerekir. Çünkü maksimum trombosit içeriği ve tedavi volümü for INTERCEPT sırasıyla 7x10 11 trombosit ve 420 ml 'dir, KESMENOKTASI işleme gereksinimlerini aşan veya iki terapötik doz bölünebilir yetersiz trombosit içeriğe sahip birimlerinin yüzdesi gibi trombosit dozu, QC kriterler için yerel gereksinimler gibi faktörlere bağlı olarak değişir buffy coat optimizasyon sonuçları ve üretim istikrarı.
Bir çift doz PC INTERCEPT işleme gereksinimlerini aşarsa, elle gereksinimlerini karşılamak için ayarlanabilir ve daha sonra tedavi edilebilir. 7-buffy coat havuzu KESMENOKTASI sonra bir çift doz ürün için yetersiz trombosit verir bu birkaç kez, biz KESMENOKTASI tedavi gerçekleştirmek için değil seçer. Alternatif olarak, diğer kan merkezleri açarak tüm birimler üzerinde patojen inaktivasyonu gerçekleştirerek, tek doz KESMENOKTASI işleme seti (Büyük Hacimli kümesi yani) ile PC tedavi ve tek bir büyük terapötik doz olarak PC saklamayı seçebilirsiniz. Biz karşılamak sağlamak için bizimQC gereksinimleri ve patojen mümkün olan trombosit birimlerinin çok, biz havuza zaman havuzda 5.6x10 11 trombositlerin az trombosit içeriği neden olur, donör trombosit sayımı esas buffy kat seçin inaktive eder. Bu INTERCEPT tedavi sonrası iki tedavi edici dozlarda üretmek için yeterli trombosit içeriği sağlar.
Bizim doğrulama 7 tam kan türetilmiş buffy coat birimleri başarıyla toplanmış ve trombositler için INTERCEPT işlemi ile tedavi, imalat (İsveççe gereksinimleri ve Avrupa kılavuzlar) ve hastaların desteği için kabul kriterlerini karşılayan 2 patojen inaktive trombosit ürünler elde edilebileceğini göstermektedir klinik uygulama kılavuzları ve İsveç'te standart trombosit infüzyonu yöntemlere göre trombosit transfüzyonu gerektiren.
Açıklamalar
Bu makalenin Üretim ve Serbest Giriş Cerus tarafından desteklenmektedir.
Teşekkürler
Yayın için Harçlar Cerus Corp, INTERCEPT Kan Sistemi üreticisi tarafından sağlanır.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Whole blood donation, primary separation, and platelet production | |||
| Blood collection pack | Fenwal | R6485 | Top/Bottom set |
| Automated component extractor | Fenwal | Optipress-II | |
| Blood mixer and balance system | Baxter | Easymix V3 | |
| Platelet leukocyte filtration set | Fenwal | K4R7042 | |
| Centrifuge | Hettich | Roto Silenta 63 RS | Version 5.5 |
| Platelet additive solution - SSP+ | MacoPharma | SSP2030U | 300 ml |
| Sterile tubing welder | Terumo | T-SCD | |
| INTERCEPT treatment & storage | |||
| INTERCEPT processing set |  Cerus Cerus | INT2503 | Dual Storage (DS) set |
| INTERCEPT Illuminator |  Cerus Cerus | INT100 | |
| PC sample pack | Fenwal | FTX 1122 | |
| Incubator | Helmer | PC2200/PC3200 | |
| Agitator | Helmer | PF48H/PF96H | |
| Evaluation of in vitro Platelet Function | |||
| Blood gas analyzer | Radiometer | ABL 735 | Used for pH, blood gases, and lactate measurement |
| Chemistry system | Ortho Clinical Diagnostic | Vitros 5.1 | Used for glucose measurement |
| Hematology analyzer | Boule Medical AB | Medonic CA620-Cellguard | Used for platelet count measurement |
| Flow cytometer | BD | FACSCanto | Used for white blood cell measurement |
Referanslar
- . . Guide to the preparation, use and quality assurance of blood components. , (2010).
- Van Rhenen, D. J., Vermeij, J., Mayaudon, V., et al. Functional characteristics of S-59 photochemically treated platelet concentrates derived from buffy coats. Vox Sang. 79, 206-214 (2000).
- Wollowitz, S. Targeting DNA and RNA in pathogens: mode of action of amotosalen HCl. Transfus. Med. Rev. 31, 11-16 (2004).
- Irsch, J., Lin, L. Pathogen Inactivation of Platelet and Plasma Blood Components for Transfusion Using the INTERCEPT Blood SystemTM. Transfus. Med. Hemother. 38, (2011).
- Lin, L., Dikeman, R., Molini, B., et al. Photochemical treatment of platelet concentrates with amotosalen and long-wavelength ultraviolet light inactivates a broad spectrum of pathogenic bacteria. Transfusion. 44, 1496-1504 (2004).
- Lin, L., Hanson, C., Alter, H., et al. Inactivation of viruses in platelet concentrates by photochemical treatment with amotosalen and long-wavelength ultraviolet light. Transfusion. 45, 580-590 (2005).
- Allain, J. P., Cianco, C., Blajchman, A., et al. Protecting the blood supply from emerging pathogens: the role of pathogen inactivation. Transfus. Med. Rev. 19, 110-126 (2005).
- Stramer, S., Hollinger, F., Katz, L., et al. Emerging infectious disease agents and their potential threat to transfusion safety. Transfusion. 49, 1S-29S (2009).
- Nussbaumer, W., Allesdorfer, D., Grabmer, C., et al. Prevention of transfusion of platelet components contaminated with low levels of bacteria: a comparison of bacteria culture and pathogen inactivation methods. Transfusion. 47, 1125-1133 (2007).
- Schlenke, P. Protection against Transfusion-Associated Graft-versus-Host Disease in Blood transfusion: Is Gamma-Irradiation the Only Answer? Transfus. Med. Hemother. 31, 24-31 (2004).
- Lin, L., Corash, L., Osselear, J. C. Protection Against TA-GVHD Due to Platelet Transfusion By Using Pathogen Inactivation with the INTERCEPT Blood SystemTM - Gamma Irradiation is Not the Only Answer. Haematologica. 95 (Extra 1), 230-237 (2010).
- Corash, L., Lin, L. Novel processes for inactivation of leukocytes to prevent transfusion-associated graft-verus-host disease. Bone Marrow Transplant. 33, 1-7 (2004).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır