Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
bir
Bu Makalede
Özet
Burada pulmoner tüberküloz lezyonlarından ve boşluklardan alınan kaseum ile ilacın bağlanmasını ölçmek için hızlı bir denge diyaliz (RED) yöntemi anlatılmaktadır. Protokol, aynı zamanda, kaseum için etkili bir vekil olan köpüklü makrofaj kaynaklı bir matriste de kullanılır.
Özet
Tüberküloz hastalığının ortadan kaldırılması, kompleks pulmoner lezyonların çok katmanına nüfuz edebilen ilaç rejimleri gerektirir. Çukurların ve lezyonların kazeöz damarlarındaki ilaç dağılımı, özellikle persistan olarak da adlandırılan uyuşturucuya dirençli bakterilerin alt popülasyonlarını barındırdığı için çok önemlidir. Tüberküloz lezyonlarında ilaç penetrasyonunun ölçülmesine ilişkin mevcut metotlar, biyoanalitik veya görüntüleme teknikleriyle birleştirilen yüksek maliyetli ve zaman alan in vivo farmakokinetik çalışmaları içerir. Kozmetik makromoleküllere bağlanan ilacın in vitro ölçümü, bu tür teknikler için bir alternatif olarak önerildi çünkü bu bağlanma, ilaç moleküllerinin kaseum yoluyla pasif difüzyonunu engelledi. Hızlı denge diyalizi plazma proteini ve doku bağlama çalışmalarında hızlı ve güvenilir bir sistemdir. Bu protokolde, kazanın homojenatlarına ilaç bağlanmasını ölçmek için hızlı denge diyaliz (RED) cihazı kullandık.Tüberküloz ile enfekte tavşanların lezyonlarından ve boşluklarından türetilmiştir. Protokol ayrıca, kaseum yerine kullanılacak lipid yüklü THP-1 makrofajlarından bir vekil matrisi nasıl oluşturulacağını açıklar. Bu kaseum / vekil bağlanma testi, tüberküloz ilaç keşfi için önemli bir araçtır ve lezyonlarda veya apselerde diğer hastalıkların yol açtığı ilaç dağılımının araştırılmasına yardımcı olmak için uyarlanabilir.
Giriş
akciğer tüberkülozu hastalığının tedavisi lezyonlar farklı içine ilaç etkin dağıtım gerektirir. Nekrotik lezyonlar ve boşluklar ilaç toleranslı veya 'kalıcı' bakteri alt-popülasyonunu liman peynir merkez içerir. 1, 2 kaviter hastalık alt kür oranları ve kötü prognoz ile ilişkilidir. 3, 4 önceki çalışmalar caseum nüfuz kabiliyeti önemli ölçüde bir ilaç sınıfı diğerine değişir, nicel ve görüntüleme teknikleri kullanılarak, göstermiştir. 5, 6 Ancak bu yöntemler, yavaş ve zahmetlidir hayvan enfeskiyon modellerinden kullanılmasını gerektirir. Ex vivo olarak caseum bağlanma ilaç ölçen bir in vitro deney tasarlanmıştır. Bu ters nedenle, peynir granülomada ilaç nüfuzunun ile ilişkili ve bulunmuştur bağlanma, birTahmin edici bir araç olarak kullanılmıştır. 7
Dengeleme diyalizi, plazma protein bağlama çalışmalarına altın standart yaklaşım olarak görülür. Hızlı denge diyalizi (RED) cihazı, bu tür testleri gerçekleştirmek için hızlı, kullanımı kolay ve güvenilir bir sistem sağlar. 8 Cihaz iki bileşenden oluşur: yarı geçirgen zarın dikey bir silindiri ile ayrılmış 2 hazneden oluşan tek kullanımlık, tek kullanımlık uçlar; Ve aynı anda 48 ek parça tutabilen tekrar kullanılabilir taban plakaları. Diyaliz membranı, ilaç-makromolekül bağlama çalışmaları için ideal olan 8 kDa moleküler ağırlıklı bir kesime (MWCO) sahiptir. Membran kompartmanının yüksek yüzey alanı / hacim oranı, hızlı diyaliz ve dengeleme sağlar. Hem ekler hem de taban plakası, asgari spesifik olmayan bağlanma için onaylanmıştır. RED cihazının biyoanalitik tekniklerle kombinasyonu, ilaçların bağlanmamış fraksiyonlarının kesin tahminlerini plasma. 8 , 9
Başlangıçta plazma protein bağlanmasını ölçmek için tasarlanmış olmasına rağmen, RED cihazı homojenatları kullanarak çeşitli doku bağlama çalışmalarında kullanılmıştır. 10 , 11 Bu protokolde, tüberkülozla enfekte tavşanların nekrotik lezyonlarından ve boşluklarından eksize edilen nekrotik çöpler, kaseum ile ilacın bağlanmasını ölçüyoruz. Caseus materyalinin asellüler ve non-vascular özelliği, tahlil ile uyumlu homojen bir süspansiyona homojenleştirilmesini kolaylaştırır.
Kaseum üretmek için sıkıcı ve zor gelmesi nedeniyle, protokol de köpüklü makrofajlardan hazırlanan bir vekil matris ile kullanım için onaylanmıştır. THP-1 monosit türevi makrofajlar, onlara 'köpüklü' görünüm veren çoklu lipid cisimcikleri biriktirmek için oleik asit ile indüklenir. Bu lipit yüklü hücreler hasat edilir veBiz caseum için bir ikame olarak kullanmak, bir matris üretmek üzere işlenir. Bu çalışma, bu taşıyıcı matris etkin bir granülomlar ve boşlukların peynir çekirdek ilacın nüfuz etmesine engel in vivo işlemi taklit caseum bağlanma ile iyi bir korelasyon ile bağlanan ilaç göstermiştir.
Access restricted. Please log in or start a trial to view this content.
Protokol
Tüm hayvan çalışmaları NIAID Kurumsal Hayvan Bakımı ve Kullanımı Komitesi (NIH), Bethesda, MD onayı ile Ulusal Sağlık Enstitüleri Laboratuvar Hayvanları Bakım ve Kullanımı Kılavuzu uyarınca gerçekleştirilmiştir. M. tuberculosis içeren tüm çalışmalarda biyo-güvenlik tutucu seviye 3 (BSL-3) ile birlikte bir laboratuarda gerçekleştirilmiştir.
1. Tavşan Enfeksiyon Modeli ve Caseum Koleksiyonu
- Daha önce tarif edildiği gibi bir sadece burundan bir aerosol uygulama sistemi kullanılarak Yeni Zelanda M. tuberculosis ile beyaz tavşan Infect. 12, 13 enfeksiyon 12-16 hafta boyunca ilerlemeye izin verin. Oturaklı 35 mg / kg ketamin ve 5 mg / kg ksilazin kas içinden, birlikte tavşan 0.22 ml / kg pentobarbital sodyum ve fenitoin sodyum ile tavşan damar ötenazi ve nekropsilerden devam edin.
- cımbız ve bir neşter kullanılarak, göğüs ca akciğerleri kaldırmakvity. Her akciğer lobundan, bir neşter yardımıyla bireysel boşlukları ve geniş nekrotik granülomları inceleyin. Kaseyi dikkatli bir şekilde boşluk ve granülom duvarlarından kazıyın. 2 mL vidalı kaptaki tüpleri tartın, kaydedin ve depolayın -20 ° C'de kullanıma hazır oluncaya kadar saklayın.
- Kuru buz üzerinde 3 MegaRad'de bulaşıcı kazein örneklerini gamma radyasyona maruz bırakarak onları bir bulaşıcı olmayan ve güvenli bir BSL-2 laboratuarında kullanın.
2. THP-1 Hücrelerinden Kaseum Vekilinin in vitro Üretimi
- T175 hücre kültürü şişeleri (80 mL / şişe) içinde RPMI 1640 ortamında (2 mM L-glutamin ve% 10 sığır fetüsü serumu) THP-1 monositleri büyütün. Şişeleri 37 ° C'de% 5 CO 2 atmosferinde 3-4 gün inkübe edin.
- Kültürü, 150 xg'de iki 50 mL konik tüp içinde T175 bir şişeden 5 dakika boyunca santrifüjleyin. Süpernatantı atın ve 10 mL RPMI 1640 ortamda pelet askıya alınız.
- 45 uL t içeren 1.5 mL tüp içine bu kültürden 5 μL pipetleMavi rippan. Pipetleme ile iyice karıştırın. 10 μL'lik bir hemositometreye aktarın ve canlı bir THP-1 monosit sayısını (renklendirilmemiş) bir ışık mikroskopu (10X büyütme) kullanarak sayın. Kültür mL başına canlı hücrelerin sayısını hesaplayın. RPMI ortamı ile 1.25 x 106 hücre / mL nihai yoğunluğa kadar seyreltin.
- Büyük bir hücre kültürü plakasına (50 x 10 6 hücre / tabağa) 40 mL kültür yükleyin. 40 uL 100 uM PMA (etanol içinde hazırlanmış forbol 12-miristat 13-asetat) ilave edin ve hücrelerin inkübatöre gece boyunca yapışmasına izin verin.
NOT: PMA'nın nihai konsantrasyonu 100 nM'dir. - Saf oleik asit (OA) (0.89 g / mL), 0.1 M konsantrasyonunda etanol içinde ( yani , 968.3 uL etanolde 31.7 μL OA) seyreltin. Bu çözeltiyi taze önceden ısıtılmış RMPI ortamında 10 mM'lik bir konsantrasyona kadar seyreltin. Bu OA süspansiyonunu önceden 37 ° C'ye ısıtılmış RPMI ortamında 0,4 mM'ye (son çalışma konsantrasyonu) seyreltin.
- Mevcut medyayı çıkarın veYapışmış hücreleri hücre kültür plakalarından hafifçe ilave edin ve THP-1 makrofajlarına (THP-M) 40 mL 0.4 mM OA ekleyin. Gece inkübatörde 37 ° C'de inkübe edin.
- Her bir THP-M'de sayısız lipid cesedi kapanımının varlığını teyit etmek için 40x büyütmede hafif bir mikroskop kullanın. Hücre kültürü plakalardan tüm RPMI orta çıkarın ve 50 ml serolojik pipet kullanarak fosfat tamponlu salin (PBS) ile yapışkan hücreleri hafifçe yıkayın.
NOT: THP-M'nin sitoplazmasındaki lipit cisimler küçük, net, küresel yapılar olarak görünür. - PBS içinde 40 mL 5 mM etilendiamintetraasetik asit (EDTA) her bir tabağa ilave edilir. 37 ° C'de 15 dakika inkübe edin.
- Köpüklü makrofajları (FM), 10 mL'lik bir serolojik pipet kullanarak tüm plakanın yüzeyinde tekrar tekrar pipetleme ile ayırın. Hücre süspansiyonunu 50 mL'lik bir konik tüpe aktarın ve 5 dakika boyunca 150 xg'de aşağı doğru döndürün.
- 10 mL PBS (üçüncü PBS yıkama) içinde hücre topağını tekrar süspansiyon haline getirin.nd önceden tartılmış 15 mL'lik konik tüplere aktarın. 5 dakika boyunca 150 x g hızında tekrar Spin. Dikkatle bir serolojik pipet ve imha edilmesini kullanarak süpernatant aspire.
- hücreler lize edildi ve matris proteinleri denatüre etmek için 20-30 dakika süreyle 75 ° C'de inkübe etmek 3 dondurma-çözme döngüsüne FM pelet Konu. Kullanım için hazır olana kadar -20 ° C 'de pelet saklayın.
3. hızlı bir dengeleme Diyaliz (kırmızı) Deneyi
- dimetil sülfoksit tüm test bileşikleri (DMSO) içinde 10 mM stok çözelti hazırlayın. Her bir deney öncesinde DMSO içinde çözüm çalışan 500 uM'ye seyreltilir.
- caseum vekil pelet içeren tüp tartılır. tek başına pelet ağırlığı elde etmek için boş bir borunun ağırlığı çıkarılır. (: Ağırlık / hacim 1: 9), her matrisin 10x seyreltilmiş süspansiyonu elde etmek için caseum veya PBS ile taşıyıcı matris bozabilir 1 dakika / dakika 1200 vuruş bir doku homojenleştirici kullanılarak, tüp başına 2-3 metal boncuk ekleyin ve.
- 500 6.5 uL başakΜM solüsyonu, 5 uM (≤% 1 DMSO) nihai konsantrasyonunu elde etmek için 643.5 uL homojenata ve vorteks içine yerleştirin.
- KIRMIZI insertleri taban plakasına yerleştirin. Her alıcı bölmesine her RED girişi ve 350 μL PBS verici bölmesine (kırmızı halka) ilaç-spiked matris 200 mcL ekleyin. Her bir test bileşiği için üç eklenti hazırlayın (üçlü örnekler). Plakayı yapışkan plakalı bir conta ile yapıştırın ve 4 saat boyunca 200 rpm'de (1 xg) termomiksör üzerinde 37 ° C'de inkübe edin.
- Kuluçka işleminden sonra verici ve alıcı odalarının içindekileri hafifçe 2-3 defa yukarı ve aşağı pipetleyerek karıştırın. Donör odalardan 20 μL'lik homojenat kısımları pipetleyin ve 1.5 mL'lik bir tüpe (1: 1) 20 μL temiz PBS ekleyin. Benzer şekilde, alıcı odalardan PBS örnekleri 20 mcL alikotları pipetle ve temiz homojenat (matris eşleme) 20 mcL ekleyin. 8
NOT: Matris eşleştirme işlemi,Kantitatif analiz için yapılacak 2 ayrı kalibrasyon eğrisi (homojenat ve PBS'de) için. Donör odasının içeriği zamanla sedimantasyon yapabilir. Alikotları çıkarmadan önce içeriğini pipetle hafifçe karıştırın.
4. LC-MS Niceleme ve Veri Analizi
- Her bir tüpe 500 ng / mL diklofenak veya 10 ng / mL verapamil (iç standart) içeren 160 uL 1: 1 metanol: asetonitril ekleyin ve proteinleri çökeltmek için girdap ekleyin. Çökeltiyi tortu haline getirmek ve süpernatantları sıvı kromatografi-kütle spektrometresi (LCMS) analizi için 96 oyuklu derin plakalara aktarmak için 5 dakika boyunca 10,000 xg'de santrifüjleyin. 7
- Yukarıdaki numunelerle aynı matris bileşimini koruyarak, her test bileşiği için 1-1000 nM'den kalibrasyon eğrileri oluşturun. Bir LC-MS yöntemi kullanarak verici ve alıcı odalarından alınan numunelerdeki test bileşiğinin konsantrasyonunu hesaplayın.
- Bağsız fraksiyonu hesapla ( f u ) of denklem 1 kullanılarak seyreltilmiş matris içinde ilaç denklem 2 (D = 10 seyreltme faktörü) kullanılarak seyreltilmemiş matris içinde f u hesaplayın. 14
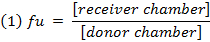
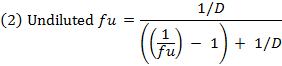
- stabilite / metabolizma / spesifik olmayan bağlanma konularla bileşimleri belirlemek için Denklem 3 kullanılarak her bileşiğin kurtarma (kütle dengesi) kontrol edin.
NOT: Kurtarma tipik% 70 ve% 130 arasında düşer. 15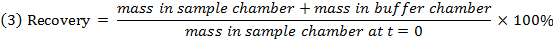
Access restricted. Please log in or start a trial to view this content.
Sonuçlar
Bu protokolü kullanarak, yüzlerce tüberküloz ilaç geliştirme bileşiğini penetran kaseumda tahmin edilen etkinlikleri için test ettik. Şekil 1 , RED testinin temel kavramlarını görüntüler. RED eklentilerinin diyaliz zarları bağlanmamış kük moleküllerin donör kuyudan alıcı kuyusuna dağılmasına ve son olarak da her iki bölme arasında denge elde edilmesine olanak tanır. Proteinler veya lipidler gibi makromoleküllere bağlı olan küçük molek?...
Access restricted. Please log in or start a trial to view this content.
Tartışmalar
Tüberkülozla enfekte hastalarda pulmoner nekrotik lezyonlar ve boşluklar, ilaç tedavisine dirençli bakteri alt popülasyonlarını içerir. Bu yapıların kazeöz çekirdeği, özellikle, bu persisörleri ekstraselüler bir ortamda barındırmaktan sorumludur. Anti-bakteriyel maddelerin bu uzak yerlere olumlu dağılımının tüberküloz ilaç etkinliğinin önemli bir belirleyicisi olduğuna inanılmaktadır. Bu protokolün onaylanmasından önce, konstitüsyonel lezyonlarda ilaç keşfi bileşiklerinin dağılı...
Access restricted. Please log in or start a trial to view this content.
Açıklamalar
Rakip finansal çıkarlar yoktur.
Teşekkürler
Biz sırasıyla, PA-824 (pretomanid), AZD5847, radezolid ve tedizolid Bedaquiline sağlamak için Johnson & Johnson, TB Alliance, Astra Zeneca, Kaburga-X ve Trius Therapeutics teşekkür etmek istiyorum. Brendan Prideaux Matthew Zimmerman, Stephen Juzwin Emma Rey-Jurado Nancy Ruel, Leyan Li ve Danielle Weiner MALDI analizi, biyoanalitik yöntemler, caseum vekil hazırlanması, kimyasal sentez ve tavşan caseum izolasyonu ile destek sağlamıştır. Bu çalışma V. Dartois NIH Paylaşılan Enstrümantasyon Grant S10OD018072 yanı sıra Mükemmellik Bir Merkezi için Bill ve Melinda Gates Vakfı ve Wellcome Trust ortak finansmanı için Bill ve Melinda Gates Vakfı tarafından finanse ödül # OPP1044966 ve OPP1024050 ile yürütülmüştür P. VVyatt'a Gelişen Dünya Hastalıklar Kurşun Optimizasyonu için.
Access restricted. Please log in or start a trial to view this content.
Malzemeler
| Name | Company | Catalog Number | Comments |
| New Zealand White Rabbits | Covance | - | |
| HN878 Mycobacterium tuberculosis | BEI Resources | NR-13647 | |
| Ketathesia (Ketamine) 100 mg/mL C3N | Henry Schein Animal Health | 56344 | |
| Anased (Xylazine) 100 mg/mL | Henry Schein Animal Health | 33198 | |
| Euthasol (pentobarbital sodium and phenytoin sodium) Solution | Virbac | 710101 | |
| THP-1 monocytic cell line | ATCC | ATCC TIB-202 | |
| 175 cm² TC-Treated Flask (T175) | Fisher Scientific | T-3400-175 | |
| RPMI 1640 media w/o glutamine | Fisher Scientific | MT-15-040-CV | |
| Hyclone Fetal Bovine Serum, Gamma irradiated | Fisher Scientific | SH3091003IR | |
| Hyclone L-glutamine, 200 mM | Fisher Scientific | SH3003401 | |
| Cellstar TC dish, 145 mm x 20 mm, vented | Fisher Scientific | T-2881-1 | |
| Phorbol 12-myristate 13-acetate (PMA) | Fisher Scientific | BP685-1 | |
| Ethylenediaminetetraacetic acid | Sigma | E6758 | |
| Oleic acid | Fisher Scientific | ICN15178101 | |
| Pierce RED Device Reusable Base Plate | Fisher Scientific | PI-89811 | |
| Pierce RED Device Inserts, 50/box | Fisher Scientific | PI-89809 | |
| Pierce RED insert removal tool | Fisher Scientific | 89812 | |
| Adhesive plate seal | Fisher Scientific | 08-408-240 | |
| PBS, pH 7.4, 10x 500 mL (Gibco) | Life Technologies | 10010-049 | |
| DMSO | Sigma | 472301 | |
| Acetonitrile | Sigma | 34998 | |
| Methanol | Sigma | 34860 | |
| Verapamil hydrochloride | Sigma | V4629 | |
| Diclofenac sodium salt | Sigma | 93484 | |
| Trypan Blue Solution, 0.4% | Fisher Scientific | 15-250-061 | |
| Ethanol, 200 proof | Fisher Scientific | 04-355-451 | |
| 2010 Geno/Grinder | SPEX SamplePrep | 2010 | |
| Bead Mill Homogenizer Accessory, Metal Bulk Beads | Fisher Scientific | 15-340-158 | |
| 484R Cobalt 60 Irradiator | JL Shepard | 7810-484-1 | |
| INCYTO C-Chip Disposable Hemacytometers | Fisher Scientific | 22-600-100 | |
| Upright Light Microscope | Leica | DM1000 | |
| Binary Liquid Chromatography system | Agilent | 1260 | Multi-compenent |
| Mass spectrometer | AB Sciex | 4000 |
Referanslar
- Sacchettini, J. C., Rubin, E. J., Freundlich, J. S. Drugs versus bugs: in pursuit of the persistent predator Mycobacterium tuberculosis. Nat Rev Microbiol. 6 (1), 41-52 (2008).
- Zhang, Y. Persistent and dormant tubercle bacilli and latent tuberculosis. Front Biosci. 1 (9), 1136-1156 (2004).
- Aber, V. R., Nunn, A. J. Short term chemotherapy of tuberculosis. Factors affecting relapse following short term chemotherapy. Bull Int Union Tuberc. 53 (4), 276-280 (1978).
- Chang, K. C., Leung, C. C., Yew, W. W., Ho, S. C., Tam, C. M. A nested case-control study on treatment-related risk factors for early relapse of tuberculosis. Am J Respir Crit Care Med. 170 (10), 1124-1130 (2004).
- Dartois, V. The path of anti-tuberculosis drugs: from blood to lesions to mycobacterial cells. Nature Rev Microbiol. 12 (3), 159-167 (2014).
- Prideaux, B., et al. The association between sterilizing activity and drug distribution into tuberculosis lesions. Nat Med. 21 (10), 1223-1227 (2015).
- Sarathy, J. P., et al. Prediction of Drug Penetration in Tuberculosis Lesions. ACS Infect Dis. 2 (8), 552-563 (2016).
- Waters, N. J., Jones, R., Williams, G., Sohal, B. Validation of a rapid equilibrium dialysis approach for the measurement of plasma protein binding. J Pharm Sci. 97 (10), 4586-4595 (2008).
- Singh, J. K., Solanki, A., Maniyar, R. C., Banerjee, D., Shirsath, V. S. Rapid Equilibrium Dialysis (RED): an In-vitro High-Throughput Screening Technique for Plasma Protein Binding using Human and Rat Plasma. J Bioequiv Availab. 14, 1-4 (2012).
- Liu, X., et al. Unbound drug concentration in brain homogenate and cerebral spinal fluid at steady state as a surrogate for unbound concentration in brain interstitial fluid. Drug Metab Dispos. 37 (4), 787-793 (2009).
- Able, S. L., et al. Receptor localization, native tissue binding and ex vivo occupancy for centrally penetrant P2X7 antagonists in the rat. Br J Pharmacol. 162 (2), 405-414 (2011).
- Subbian, S., et al. Chronic pulmonary cavitary tuberculosis in rabbits: a failed host immune response. Open Biol. 1 (4), 1-14 (2011).
- Via, L. E., et al. Tuberculous Granulomas are Hypoxic in Guinea pigs, Rabbits, and Non-Human Primates. Infect Immun. 76 (6), 2333-2340 (2008).
- Kalvass, J. C., Maurer, T. S. Influence of nonspecific brain and plasma binding on CNS exposure: implications for rational drug discovery. Biopharm Drug Dispos. 23 (8), 327-338 (2002).
- Di, L., Umland, J. P., Trapa, P. E., Maurer, T. S. Impact of recovery on fraction unbound using equilibrium dialysis. J Pharm Sci. 101 (3), 1327-1335 (2012).
- Lenaerts, A. J., et al. Location of persisting mycobacteria in a Guinea pig model of tuberculosis revealed by r207910. Antimicrob Agents Chemother. 51 (9), 3338-3345 (2007).
- Prideaux, B., et al. High-sensitivity MALDI-MRM-MS imaging of moxifloxacin distribution in tuberculosis-infected rabbit lungs and granulomatous lesions. Anal Chem. 83 (6), 2112-2118 (2011).
Access restricted. Please log in or start a trial to view this content.
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır