Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
Klorheksidin Glukonat Kaynaklı Periton Hasarının Bir Fare Modeli
* Bu yazarlar eşit katkıda bulunmuştur
Bu Makalede
Özet
Bu protokol, klorheksidin glukonat (CG) ile indüklenen periton fibrozisinin periton diyalizi (PD) fare modelini oluşturmaktadır. Mevcut model, diğer PD hayvan modellerine kıyasla basit ve kullanımı kolaydır.
Özet
Periton fibrozisi, periton diyalizinin (PD) önemli bir komplikasyonudur. Bu sorunu araştırmak ve ele almak için, uygun bir PD hayvan modeli gereklidir. Mevcut protokol, PD'li bir hastanın durumunu taklit eden bir klorheksidin glukonat (CG) ile indüklenen peritoneal fibroz modeli oluşturmaktadır. Peritoneal fibroz, erkek C57BL / 6 farelerde toplam dokuz kez, 3 hafta boyunca% 15 etanol içinde% 0.1 CG'nin% 0.1'inin intraperitoneal enjeksiyonu ile indüklenmiştir. Daha sonra 22. günde periton fonksiyonel testleri yapıldı. Fareler kurban edildikten sonra, karın duvarının parietal peritonu ve karaciğerin viseral peritonu toplandı. Masson'un trikrom boyamasından sonra mikroskobik olarak analiz edildiğinde daha kalın ve daha fibrotiktiler. Ultrafiltrasyon hızı azaldı ve glikoz kütle taşınması periton geçirgenliğinde CG kaynaklı bir artışa işaret etti. Bu şekilde oluşturulan PD modeli, PD teknolojisini, diyaliz etkinliğini iyileştirmede ve hasta sağkalımını uzatmada uygulamalara sahip olabilir.
Giriş
Periton diyalizi (PD) bir tür renal replasman tedavisidir. Ancak PH'nin çözülemeyen sorunları vardır. Örneğin, uzun süreli PD tedavisi periton hasarına neden olabilir, sonuçta ultrafiltrasyon başarısızlığına ve tedavinin geri çekilmesine neden olabilir 1,2,3,4,5,6. Peritoneal fibrozis en ciddi komplikasyonlardan biridir 7,8. Peritoneal fibrozis, interstisyum içinde hücre dışı matriksin birikmesi ve birikmesi ve periton 9,10'un neo-anjiyogenezi ve vaskülopatisi ile karakterizedir.
Bu peritoneal değişikliklerin başlıca nedenleri tekrarlayan peritonit ve diyalizatın biyouyumlu olmamasıdır, bunlar hiperozmotik, yüksek glukoz, düşük pH ve glukoz yıkımı ürün birikimidir11,12. Bu nedenle, uygun hayvan deney modelleri, araştırmacıların PD tedavisi sırasında peritondaki fizyolojik ve patolojik değişiklikleri daha iyi incelemelerine yardımcı olabilir. Bu nedenle, bir hayvan PD modelinin oluşturulması, PD teknolojisinin ve diyaliz etkinliğinin iyileştirilmesi ve hasta sağkalımının uzatılması açısından önemlidir. Bu çalışma, daha önce13,14 olarak tarif edildiği gibi, klorheksidin glukonatın (CG) intraperitoneal (i.p.) enjeksiyonu ile bir PD fare modeli oluşturmayı amaçlamıştır. Bu PD fare modeli, diğer PD hayvan modellerine kıyasla basit, kullanımı kolay ve uygulanabilirdir.
Access restricted. Please log in or start a trial to view this content.
Protokol
Tüm fare deneyleri, E-DA Hastanesi / I-Shou Üniversitesi Laboratuvar Hayvanları Merkezi tarafından onaylandı ve "Laboratuvar Hayvanlarının Bakımı ve Kullanımı Kılavuzu" na göre ele alındı (NRC, ABD 2011). Bu çalışmada 7-8 haftalık erkek C57BL/6 fareler kullanıldı.
1. Kimyasal preparat
- % 0.1 klorheksidin glukonatı (CG, Malzeme Tablosuna bakınız) % 15 etanol içinde seyrelterek kimyasal tahriş edici maddeyi hazırlayın.
2. Hayvan tedavisi
- Kontrol grubu olarak üç fare atayın. 3 hafta boyunca her gün 1 mL/kg %0.9 normal salin (NS) intraperitoneal enjeksiyon (i.p.) 3 hafta boyunca her gün toplam dokuz kez uygulayın.
- Peritoneal fibroz grubuna üç fare atayın. Klorheksidin glukonat (CG) kullanarak, 12.5 μL / g vücut ağırlığı dozunda% 15 etanol (adım 1.1) içinde% 0.1 CG enjeksiyonları uygulayarak periton fibrozunu indükleyin. Bunu 3 hafta boyunca her gün, toplam dokuz kez gerçekleştirin.
3. Periton fonksiyon testleri (modifiye periton denge testi)
- % 4.25 glikoz içeren bir diyaliz çözeltisi hazırlayın. Bir şırınga ile 0,5 mL diyalizat numunesi çizin ve ardından diyalizat numunesindeki glikoz konsantrasyonunu kontrol edin.
NOT: Glikoz konsantrasyonu hekzokinaz/G6PD yöntemine göre belirlenir. Diyalizat örneklerine L-tipi Glu 2 testine erişildi ve bir biyokimyasal analizör ile araştırıldı (bakınız Malzeme Tablosu). Bu ilk diyalizat glikoz konsantrasyonudur. - Fareleri, 20 μL / 20 gw'lik bir dozda Zoletil ve Xylazin'in kas içi enjeksiyonu (hacimce 1: 2 oranında hazırlanır, Malzeme Tablosuna bakınız) ile uyuşturun. Ek olarak, anestezi altında kuruluğu önlemek için gözlerde veteriner merhemi kullanın.
- Diyaliz solüsyonunun i.p. damlatılmasını gerçekleştirin (2 mL/20 g vücut ağırlığı).
- 30 dakika sonra, ayak parmağı sıkışma refleksi eksikliği ile anestezi derinliğini değerlendirin ve doğrulayın. Daha sonra, karın orta hattında (ksifoid işlemin altında) dikey bir kesi yapın, ardından farelerin karnını açın ve intraperitoneal sıvıyı bir şırınga ile toplayın ("hacim 1" olarak tanımlanır). Daha sonra, temiz ve kuru bir pamuğun ağırlığını ölçün ve kalan intraperitoneal sıvıyı emmek için pamuğu farelerin karın boşluğuna koyun. Son olarak, pamuk ağırlığını tekrar ölçün.
NOT: Pamuğun kilo alımı, kalan intraperitoneal sıvının ağırlığına eşittir. Ardından, elde edilen hacme dönüştürün (özgül ağırlık: 1 g /cm3; "hacim 2" olarak tanımlanır). Son diyalizat hacmi cilt 1 artı cilt 2'dir. - Glikoz konsantrasyonunu ölçmek için 0,5 mL diyalizat numunesi (son diyalizat) kullanın. Bu son diyalizat glikoz konsantrasyonudur.
- Formül15'i kullanarak net ultrafiltrasyonunu hesaplayın:
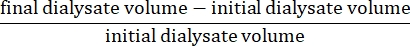
- Aşağıdaki formül15'i kullanarak periton geçirgenliğini hesaplayın:
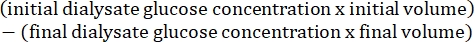
4. Karın duvarı, kas ve karaciğerin doku hazırlığı ve histolojik analiz
- Fareleri kardiyak ponksiyon (flebotomi) yoluyla kurban edin3,16.
- Karın duvarını kesin (1 cm x 1 cm) ve total hepatektomi. Farelerin karın duvarını ve karaciğer dokularını gece boyunca% 10 nötr tamponlu formalin içinde sabitleyin.
- Karın duvarı kası ve karaciğerin 3 μm kalınlığında parafin kesitleri hazırlayın ve daha önce yayınlanan rapor17'yi takiben histolojik analiz yapın.
- Karın duvarının parietal peritonunu ve farelerin karaciğer yüzeylerinin viseral peritonunu morfometri kullanarak değerlendirin18.
- İstatistik ve grafik yazılımı kullanarak istatistiksel analizler gerçekleştirin (bkz. Tüm verileri ortalama ± SD olarak ifade edin ve bir t-testi19 kullanarak istatistiksel anlamlılık açısından analiz edin. P < 0,05 ile değerleri anlamlı sonuçlar olarak tanımlayın.
Access restricted. Please log in or start a trial to view this content.
Sonuçlar
Şekil 1A,B'de, karın duvarının parietal peritonu, Masson'un trikrom boyama 17'si altında belirgin şekilde daha kalın ve daha fibrotikti, bu da CG'ye maruz kalan grupta periton fibrozisinin kontrol salin grubundan (NS) daha şiddetli olduğunu göstermektedir. Şekil 2A, B'de, karaciğer yüzeylerinin viseral peritonunun da belirgin şekilde daha kalın ve daha fibrotik olduğu kanıtlanmıştır, b...
Access restricted. Please log in or start a trial to view this content.
Tartışmalar
Bu çalışmada, CG'nin i.p. enjeksiyonu ile bir fare PD modeli sunulmuş ve sonuçlar bu modelde PD hastasının durumunu taklit eden periton fibrozu ve fonksiyonel bozulma göstermiştir.
Protokolde birkaç kritik adım vardır. İlk olarak, CG veya NS'nin bir i.p. enjeksiyonunu gerçekleştirmek için, farenin karın duvarı derisi, delinmeye bağlı intraperitoneal organ hasarını önlemek için forseps kullanılarak alınmalıdır. İkincisi, histolojik analizler için karın duvarının...
Access restricted. Please log in or start a trial to view this content.
Açıklamalar
Yazarların açıklayacak hiçbir şeyi yok.
Teşekkürler
Shin-Han Tseng'e eleştirel tartışma ve çalışmanın kısmi yürütülmesi için içtenlikle teşekkür ederiz. Bu çalışma, E-DA Hastanesi Araştırma Vakfı ve Tayvan Ulusal Cheng Kung Üniversitesi'nden EDAHP110003 ve NCKUEDA110002 tarafından desteklenmiştir.
Access restricted. Please log in or start a trial to view this content.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 0.9% Normal Saline | Y F CHEMICAL CORP., New Taipei City, Taiwan | - | |
| 10% neutral buffered formalin | Taiwan Burnett International Co., Ltd., Taipei City, Taiwan | 00002A | |
| Automatic biochemical analyzer | Hitachi Ltd., Tokyo, Japan | Labospect Series 008 | for determining glucose concentration |
| Chlorhexidine digluconate solution, 20% in H2O | Sigma-Aldrich, MO, USA | C9394 | diluted to 0.1% with 15% ethanol for injection |
| Ethanol | Avantor Performance Materials, LLC, PA, USA | BAKR8006-05 | diluted to 15% with normal saline for working concentration |
| Glucose (Dianeal) | Baxter International, Inc., IL, USA | FNB9896 | Commercial dialysis solution (4.25%) |
| GraphPad Prism 8.0 | GraphPad Software, Inc., CA, US | ||
| L-type Glu 2 assay | FUJIFILM Wako, Japan | 461-32403 | |
| Xylazine 20 | Juily Pharmaceutical Co., Ltd., New Taipei City, Taiwan | - | |
| Zoletil 50 | Virbac Laboratories, Carros, France | - |
Referanslar
- Han, S. H., et al. Improving outcome of CAPD: twenty-five years' experience in a single Korean center. Peritoneal Dialysis International. 27 (4), 432-440 (2007).
- Kawaguchi, Y., Hasegawa, T., Nakayama, M., Kubo, H., Shigematu, T. Issues affecting the longevity of the continuous peritoneal dialysis therapy. Kidney International Supplements. 62, 105-107 (1997).
- Lee, Y. C., et al. Vitamin D can ameliorate chlorhexidine gluconate-induced peritoneal fibrosis and functional deterioration through the inhibition of epithelial-to-mesenchymal transition of mesothelial cells. BioMed Research International. 2015, 595030(2015).
- Nakamoto, H., Kawaguchi, Y., Suzuki, H. Is technique survival on peritoneal dialysis better in Japan. Peritoneal Dialysis International. 26 (2), 136-143 (2006).
- Schaefer, F., Klaus, G., Muller-Wiefel, D. E., Mehls, O. Current practice of peritoneal dialysis in children: results of a longitudinal survey. Mid European Pediatric Peritoneal Dialysis Study Group (MEPPS). Peritoneal Dialysis International. 19, Suppl 2 445-449 (1999).
- Woodrow, G., Turney, J. H., Brownjohn, A. M. Technique failure in peritoneal dialysis and its impact on patient survival. Peritoneal Dialysis International. 17 (4), 360-364 (1997).
- Schmidt, D. W., Flessner, M. F. Pathogenesis and treatment of encapsulating peritoneal sclerosis: basic and translational research. Peritoneal Dialysis International. 28, Suppl 5 10-15 (2008).
- Augustine, T., Brown, P. W., Davies, S. D., Summers, A. M., Wilkie, M. E. Encapsulating peritoneal sclerosis: clinical significance and implications. Nephron Clinical Practice. 111 (2), 149-154 (2009).
- Di Paolo, N., Nicolai, G. A., Garosi, G. The peritoneum: from histological studies to mesothelial transplant through animal experimentation. Peritoneal Dialysis International. 28, Suppl 5 5-9 (2008).
- Fusshoeller, A. Histomorphological and functional changes of the peritoneal membrane during long-term peritoneal dialysis. Pediatric Nephrology. 23 (1), 19-25 (2008).
- Goffin, E. Peritoneal membrane structural and functional changes during peritoneal dialysis. Seminars in Dialysis. 21 (3), 258-265 (2008).
- Ito, T., Yorioka, N. Peritoneal damage by peritoneal dialysis solutions. Clinical and Experimental Nephrology. 12 (4), 243-249 (2008).
- Io, K., et al. SAHA suppresses peritoneal fibrosis in mice. Peritoneal Dialysis International. 35 (3), 246-258 (2015).
- Yoh, K., Ojima, M., Takahashi, S. Th2-biased GATA-3 transgenic mice developed severe experimental peritoneal fibrosis compared with Th1-biased T-bet and Th17-biased RORgammat transgenic mice. Experimental Animals. 64 (4), 353-362 (2015).
- Karl, Z. J. T., et al. Peritoneal Equilibration Test. Peritoneal Dialysis International. 7 (3), 138-148 (1987).
- Lee, Y. C., et al. The clinical implication of vitamin D nanomedicine for peritoneal dialysis-related peritoneal damage. International Journal of Nanomedicine. 14, 9665-9675 (2019).
- Goldner, J. A. Modification of the masson trichrome technique for routine laboratory purposes. The American Journal of Pathology. 14 (2), 237-243 (1938).
- Cheng, F. Y., et al. Novel application of magnetite nanoparticle-mediated vitamin D3 delivery for peritoneal dialysis-related peritoneal damage. International Journal of Nanomedicine. 16, 2137-2146 (2021).
- Ross, A., Willson, V. L. Basic and Advanced Statistical Tests: Writing Results Sections and Creating Tables and Figures. , SensePublishers. 13-16 (2017).
- Suga, H., et al. Preventive effect of pirfenidone against experimental sclerosing peritonitis in rats. Experimental and Toxicologic Pathology. 47 (4), 287-291 (1995).
- Ishii, Y., et al. An experimental sclerosing encapsulating peritonitis model in mice. Nephrology Dialysis Transplantation. 16 (6), 1262-1266 (2001).
- Nishino, T., et al. Antisense oligonucleotides against collagen-binding stress protein HSP47 suppress peritoneal fibrosis in rats. Kidney International. 64 (3), 887-896 (2003).
- Mishima, Y., et al. Enhanced expression of heat shock protein 47 in rat model of peritoneal fibrosis. Peritoneal Dialysis International. 23 (1), 14-22 (2003).
- Kushiyama, T., et al. Effects of liposome-encapsulated clodronate on chlorhexidine gluconate-induced peritoneal fibrosis in rats. Nephrology Dialysis Transplantation. 26 (10), 3143-3154 (2011).
- Nishino, T., et al. Involvement of lymphocyte infiltration in the progression of mouse peritoneal fibrosis model. Renal Failure. 34 (6), 760-766 (2012).
- Lua, I., Li, Y., Pappoe, L. S., Asahina, K. Myofibroblastic conversion and regeneration of mesothelial cells in peritoneal and liver fibrosis. The American Journal of Pathology. 185 (12), 3258-3273 (2015).
- Kitamura, M., et al. Epigallocatechin gallate suppresses peritoneal fibrosis in mice. Chemico-Biological Interactions. 195 (1), 95-104 (2012).
Access restricted. Please log in or start a trial to view this content.
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiDaha Fazla Makale Keşfet
This article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır