Method Article
Florometrik Tahlil veya Akış Sitometrisi Kullanarak Kaspaz Aktivitesinin Ölçülmesi
Bu Makalede
Özet
Mevcut protokol, akış sitometrisi veya spektroflorometre kullanarak florojenik bir substrat yoluyla kaspaz aktivitesini ölçmek için iki yöntem tanımlamaktadır.
Özet
Kaspazlar olarak bilinen sistein proteazlarının aktivasyonu, birçok hücre ölümü formunda önemli bir süreç olmaya devam etmektedir. Kaspazlar, programlanmış hücre ölümünün en çok çalışılan şekli olan apoptozun kritik başlatıcıları ve uygulayıcılarıdır. Apoptozis gelişimsel süreçlerde ortaya çıkar ve doku homeostazında gerekli bir olaydır. Piroptoz, kaspazları kullanan başka bir hücre ölümü şeklidir ve enflamatuarın aktivasyonu yoluyla bağışıklık sistemini aktive etmede kritik bir süreçtir, bu da interlökin-1 (IL-1) ailesinin üyelerinin salınmasına neden olur. Kaspaz aktivitesini değerlendirmek için hedef substratlar değerlendirilebilir. Bununla birlikte, tek hücreleri veya düşük seviyeli aktiviteyi incelerken duyarlılık bir sorun olabilir. Florojenik bir substratın, popülasyon bazlı bir tahlil veya akış sitometrisi ile tek hücreli bir tahlil ile nasıl kullanılabileceğini gösteriyoruz. Uygun kontrollerle, hangi kaspazların aktif olduğunu belirlemek için farklı amino asit dizileri kullanılabilir. Bu tahliller kullanılarak, tümör nekroz faktörü (TNF) stimülasyonu üzerine apoptoz proteinlerinin inhibitörlerinin eşzamanlı kaybı tanımlanmıştır, bu da öncelikle diğer hücre ölümü biçimlerinden ziyade makrofajlarda apoptozu indükler.
Giriş
Kaspazlar, programlanmış hücre ölümünün çeşitli biçimlerinde rol oynar. Apoptoz, programlanmış hücre ölümünün en çok çalışılan şeklidir ve kaspaz aktivitesi1 ile ilişkilidir. Tüm kaspazlar büyük ve küçük bir katalitik alt birime sahiptir. Kaspaz-1, kaspaz-4, kaspaz-5, kaspaz-9 ve kaspaz-11 bir kaspaz aktivasyon ve işe alım alanına (CARD) sahiptir ve kaspaz-8 ve kaspaz-10 ölüm efektör alanları (DED) 2,3,4,5 içerir (Tablo 1). Apoptoz iki ana yolla başlatılabilir: ekstrinsik yol ve intrinsik yolak. Ekstrinsik apoptotik yolak, tümör nekroz faktörü süper ailesinin (TNFSF) bir parçası olan ölüm reseptörleri tarafından tetiklenir. Ölüm reseptörleri DED alanlarına sahiptir ve kaspaz-8 aktivitesini kolaylaştırır6. İntrinsik apoptotik yolak, apoptozom oluşumundan sonra kaspaz-9'un aktivasyonunu içerir ve sitokrom c ve Apaf-17'nin salınmasını gerektirir. Başlatıcı kaspaz, kaspaz-8 veya kaspaz-9'un aktivasyonu, kaspaz-3, kaspaz-6 ve kaspaz-7 olan cellat kaspazlarının bölünmesine ve ardından aktivasyonuna yol açar. Cellat kaspazlarının aktif olduğunu belirlemek, hücrelerin apoptoza uğradığını gösterir ve bu aktivasyon, hücre ölümünün modunu tanımlamada önemli bir faktör olarak kabul edilir.
Kaspaz aktivasyonu ayrıca inflamasyonu düzenlemek ve programlanmış hücre ölümünün alternatif formlarının indüksiyonu için kritik bir kavşaktır. Örneğin, kaspaz-1 aktivasyonu, interlökin-1 ailesinin pro-inflamatuar sitokinlerinin olgunlaşmasına yol açar8. Bu aileden, özellikle IL-1β ve IL-18'den sitokinlerin salınımı ve aktivasyonu, plazma zarı 9,10'da gasdermin D bölünmesi ve gözenek oluşumundan kaynaklanır. Gazdermin D gözeneklerinin yetersiz membran onarımı, pirotoz11 olarak bilinen bir tür hücre ölümüne neden olabilir. Ayrıca, kaspaz-8 aktivitesi, nekrotoz12 olarak bilinen kaspazdan bağımsız hücre ölümünün inhibisyonu ile sonuçlanır. Reseptör etkileşiminde bulunan serin / treonin protein kinaz 1 (RIPK1), nekroptozda ve NF-kB tarafından düzenlenen inflamasyonun yönlendirilmesinde kritik faktörlerden biridir. modeller, RIPK1'in kaspaz-8 tarafından bölündüğünü ve NF-kB sinyalini, apoptozu ve nekroptozu13,14'ü sınırladığını göstermiştir. Bu nedenle, farklı kaspazların aktivitesini tanımlamak, ortaya çıkan inflamasyonu ve hücre ölümü modalitesini anlamada yardımcı olabilir.
Hücre ölümü modalitelerinin düzenlenmesinde kaspazların işlevinden bağımsız olarak, kaspaz aktivitesi enfeksiyona yanıt olarak interferon (IFN) gibi diğer sitokin ailelerini de düzenleyebilir15,16. Ek olarak, kaspazlar hücre kaderi kararları, doku onarımı ve rejenerasyonu, DNA onarımı yoluyla tümörigenez ve nöronal sinaps fonksiyonu dahil olmak üzere hücre dışı ölüm fonksiyonlarında rol oynar. Bu ölümcül olmayan rollerdeki kaspazların aktivitesinin hücresel lokalizasyon ve kaspaz miktarı ile sınırlı olduğu düşünülmektedir. Bu nedenle, kaspaz aktivitesinin seviyesini ölçmek, bir hücrenin hücre ölümüne maruz kalıp kalmadığını veya kaspazın hücre dışı bir ölüm fonksiyonunda rol oynayıp oynamadığını iyi tanımlayabilir 4,17,18.
Kaspaz aktivitesi birden fazla yöntemle değerlendirilebilir. Parçalanmış kaspazlar ve substratları için batı lekelenmesi aktivitenin bir göstergesi olarak kullanılmıştır, ancak bu testler en iyi ihtimalle nitelikseldir. Kaspaz aktivitesinin hücre ölümü ile ilişkili olup olmadığını belirlemek için, nicel bir ölçüm idealdir. Kaspazlar substratları dört amino asitten oluşan bir tanıma bölgesinde parçaladığından, kolorimetrik, lüminesans veya florometrik yöntemler geliştirilmiştir. Bununla birlikte, kaspazların substrat tanıma 19,20'lerinde plastisiteye sahip oldukları görülmektedir. Tanıma dizisi protein alanları ile ilişkili değildir (Tablo 1). Bununla birlikte, tetrapeptit dizisi DEVD, kaspaz-3 ve kaspaz-7 aktivitesi 20,21'i tespit etmek için kullanılabilir.
Smac mimetikleri, apoptoz proteinlerinin (IAP'ler) inhibitörlerini hedef alan bileşiklerdir. Kanser hücrelerinin bir alt kümesinde Smac mimetiklerinin kullanılması, hücrelerin TNF kaynaklı hücre ölümüne duyarlı hale gelmesine neden olur22. Primer makrofajlarda, Smac mimetikleri, TNF 23,24'ün eksojen ilavesi olmadan hücre ölümüne neden olur. Smac mimetik kaynaklı bozunma ile cIAP1 kaybı, TNF üretimi ile sonuçlanır. Kaspaz aktivitesi tespit edilirse, bu, hücrelerin nekroptozla değil, apoptotik bir şekilde öldüğü anlamına gelir. Bu yöntemde, yarıklı DEVD substratının tespiti, kaspaz-3/kaspaz-7 aktivitesini tanımlamak için kullanılır. Apoptotik hücre ölümünü doğrulamak için daha fazla deney daha önceyayınlanmıştır 24.
Protokol
Bu çalışma, Zürih Üniversitesi hayvan etik komitesinin onayı ve yönergeleri doğrultusunda gerçekleştirilmiştir (#ZH149/19). Bu çalışmada 8-16 haftalık erkek C57Bl/6J fareleri, spesifik patojensiz (SPF) koşullarda yetiştirilmiş ve barındırılmıştır. Bozulmamış kemikler, steril Hank'in tamponlanmış salin çözeltisinde (HBSS) buz üzerinde tutulabilir ve %2 ısı ile inaktive fetal sığır serumu (FBS) elde edilebilir. Kemik iliği, farklılaşma gününde fare25'in femur ve tibiasından toplandı. Kaspaz aktivitesini değerlendirmek için her iki yöntem de hem birincil hem de dönüştürülmüş dahil olmak üzere diğer hücre tipleri için kullanılabilir.
1. Kemik iliği kaynaklı makrofajları (BMDM'ler) ayırt etme
NOT: Bir doku kültürü laminer akış başlığındaki tüm adımları uygulayın ve steril aseptik teknikler kullanın.
- 21 G iğne ile 1 mL'lik bir şırınga hazırlayın.
- 15 mL'lik bir tüpe 5 mL HBSS + %2 FBS ekleyin.
- Steril forseps kullanarak, eksize edilmiş bir femur alın ve iğneyi femur açıklığına yerleştirin. Femuru HBSS +% 2 FBS'de tutarak, kemik iliğini kemik beyaz olana kadar yıkayın. Tibianı aynı şekilde yıkayın. Tek hücreli bir süspansiyon elde etmek için çözeltiyi yıkamaya devam edin.
- Tek hücreli süspansiyonu oda sıcaklığında (RT) 4 dakika boyunca 200 x g'de santrifüj yapın.
- Bir vakum aspiratörü kullanarak süpernatantı çıkarın. Peleti nazikçe askıya almak için tüpe dokunun. 1 mL kırmızı hücre lizis tamponu ekleyin ( bkz. Malzeme Tablosu) ve bir P1.000 pipetle nazikçe karıştırın. RT'de 1 dakika boyunca inkübe edin.
- 10 mL HBSS + %2 FBS ekleyin ve RT'de 4 dakika boyunca 200 x g'de santrifüj yapın.
- Süpernatanı çıkarın ve 10 mL kemik iliği kaynaklı makrofaj (BMDM) kültür ortamında yeniden askıya alın.
NOT: BMDM kültür ortamı,% 10 FBS, 20 ng / ml M-CSF, penisilin (50 U / mL) ve streptomisin (50 μg / mL) ilavesiyle düşük glikozlu DMEM'den oluşur (bkz. Alternatif olarak, M-CSF yerine %20 L929 şartlandırılmış ortam kullanılabilir. - İki adet 15 cm'lik Petri kabına 15 mL BMDM kültür ortamı ekleyin. Her plakaya 5 mL tek hücreli çözelti ekleyin.
NOT: Doku kültürü ile muamele edilmiş plakalar kullanmayın. Doku kültürü ile tedavi edilen plakalar farklılaşmayı sınırlar. - Bulaşıkları 6 gün boyunca 37 °C, % 5 CO2'ye yerleştirin.
NOT: BMDM'ler 5-7 gün sonra hasat edilebilir. Farklılaşma için daha uzun inkübasyon süreleri, anti-apoptotik protein ekspresyonunun artmasına neden olur26.
2. Hücrelerin toplanması, tohumlanması ve işlenmesi
NOT: Bir doku kültürü laminer akış başlığındaki tüm adımları uygulayın ve steril aseptik teknikler kullanın. Tamamen farklılaşmış makrofajlar plakaya yapışır ve kolay ayrılmaya izin verirken, yüzen hücreler atılabilir. Fosfat tamponlu salin (PBS), Ca 2+ve Mg 2+ ile birlikte veya bunlar olmadan kullanılabilir.
- 6 günlük inkübasyondan sonra, yüzen hücreleri ve ortamı bir aspiratör kullanarak plakadan çıkarın.
- Her 15 cm'lik plakaya 5 mL PBS ekleyin. PBS'yi bir aspiratör kullanarak plakadan çıkarın.
- Her plakaya 2 mL tripsin ekleyin (bkz. Malzeme Tablosu). Plakanın hafifçe dokunulması hücreleri yerinden çıkarana kadar plakayı inkübe edin. 5 mL BMDM kültür ortamı alın ve hücreleri plakadan toplayın.
- İkinci 15 cm'lik plakaya aktarın ve hücreleri plakadan toplayın. Hücre süspansiyonunu plakadan 50 mL'lik bir tüpe çıkarın. Ek olarak 5 mL BMDM kültür ortamı alın ve tüm hücrelerin toplandığından emin olmak için her iki plakayı da yıkayın. Hücre süspansiyonunu aynı 50 mL tüpe yerleştirin.
- Hücre süspansiyonunun 10 μL'sini alın ve tripan mavisi ile 1: 1 seyreltme kullanarak bir hemasitometre kullanarak sayın.
NOT: Otomatik hücre sayaçları, makrofajların boyutuna göre kalibre edildiğinde de kullanılabilir. - Makrofajları 1 x 106 hücre / mL yoğunlukta tohumlayın. 6 kuyucuklu bir plakada 2 x 106 hücre / kuyucukta tohumlanan BMDM'ler yaklaşık 2 mg / mL toplam protein sağlar. Hücrelerin tedaviden önce plakaya en az 6 saat yapışmasına izin verin.
NOT: Diğer hücre tipleri için optimum konsantrasyon belirlenmelidir. - Makrofajları 250 nM'de Smac mimetik (Bileşik A, bakınız Malzeme Tablosu)22 ve 16 saat boyunca 500 nM ile tedavi edin.
NOT: Tahlilin çalıştığından emin olmak için apoptozu ve kaspaz-3 bölünmesini indüklemek için pozitif bir kontrol ekleyin. Yaygın apoptoz indükleyicileri arasında staurosporin ve etoposid bulunur. Birçok hücre hattının apoptoza uğraması için, 16 saatlik stimülasyon için 0.1-10 μM yeterlidir.
3. Tedavi edilen hücrelerden hücre lizatlarının hazırlanması
NOT: Bu adım buz üzerinde yapılmalı ve reaktifler ve malzemeler önceden soğutulmalıdır.
- İşlem görmüş hücreleri içeren plakaları buzun üzerine aktarın. Ortamı hücre kültüründen 1,5 mL'lik bir tüpe toplayın, 4 ° C'de 5 dakika boyunca 300 x g'de santrifüj yapın, ortamı aspire edin ve tüpü buz üzerine koyun. Bu, plakadan ayrılan hücrelerin toplanmasını sağlar.
- Hücreleri yıkamak için hücre kültürü plakasına 1 mL soğuk PBS ekleyin ve tüm PBS'yi aspire edin. Hücrelere 100 μL tripsin ekleyin (6 kuyucuklu bir tabakla çalışıyorsanız). Tripsinin hücreleri plakadan kaldırmasına izin verin ve bunları 1,5 mL tüpe toplayın. Tüm hücrelerin toplandığından emin olmak için 1 mL soğuk PBS kullanın.
NOT: Süspansiyon hücreleriyle çalışıyorsanız, ortamı ve hücreleri nazikçe 1,5 mL'lik bir tüpe aktarın. - Hücreleri 300 x g'de 4 ° C'de 5 dakika boyunca santrifüj edin. Süpernatanı çıkarın ve 100 μL DISC lizis tamponunda yeniden askıya alın (150 mM sodyum klorür, 2 mM EDTA,% 1 Triton X-100,% 10 gliserol, 20 mM Tris, pH 7.5, Malzeme Tablosuna bakınız).
- Örnekleri 20 dakika boyunca buz üzerinde inkübe edin.
- Çözünmeyen fraksiyonu pelet etmek için lizatları ~ 12.000 x g'de 4 ° C'de 10 dakika boyunca santrifüj edin.
- Lizatın 25 μL'sini, kaspaz-3 / kaspaz-7 aktivite testi için beyaz düz tabanlı 96 kuyucuklu bir plakaya aktarın (adım 5).
NOT: Pelet'i rahatsız etmeyin. Bu, hücre lizatının çözünmeyen fraksiyonudur. - Kalan lizatın 10 μL'sini, bisinkoninik asit (BCA) testi için şeffaf düz tabanlı 96 delikli bir plakaya aktarın (adım 4). Bu, numunelerin normalleştirilmesi için kullanılacaktır.
- Daha fazla işlem için her iki plakayı da buz üzerinde tutun.
NOT: Bu aşamada, plakalar yapışkan bir kapakla kapatılabilir ve yaklaşık 4 hafta boyunca -20 ° C'de saklanabilir.
4. BCA tahlili kullanılarak protein niceliği
NOT: Her numunedeki protein miktarını ölçmek için diğer reaktifler veya testler kullanılabilir. Popülasyon bazlı tahlilde, numuneler tahlilde kullanılan protein miktarını normalleştirerek karşılaştırılabilir.
- Sığır serum albümini (BSA) ile 0 μg/mL ile 2.000 μg/mL (0 μg/mL, 25 μg/mL, 125 μg/mL, 250 μg/mL, 500 μg/mL, 750 μg/mL, 100 μg/mL, 1.500 μg/mL, 2.000 μg/mL) arasında standart protein konsantrasyonları hazırlayın. Boşlukları sadece lizis tamponu ile hazırlayın.
- Adım 3.7'de belirtilen numuneleri içeren düz tabanlı 96 delikli plakaya her standardın 10 μL'sini ekleyin.
- BCA reaktifi 1 ile BCA reaktifi 2'yi 50:1 oranında karıştırın (bkz. Her numuneye ve standarda 200 μL karışık BCA reaktifi ekleyin.
- 30 dakika boyunca 37 ° C'de inkübe edin.
- Florometrik bir cihazda 562 nm'deki absorbansı ölçün ve protein konsantrasyonunu standart eğri ile ölçün.
5. Kaspaz-3/kaspaz-7 aktivitesi için popülasyona dayalı tahlil
NOT: Plakadaki hücre lizatlarının buz üzerinde 3 saatten fazla oturmasına izin vermeyin. Kaspaz aktivitesi varsa, numunenin buz üzerinde olmasına rağmen bu zamanla artar. Numuneler dondurulmuşsa, onları buz üzerinde çözün ve lizatlar çözüldükten hemen sonra devam edin.
- Florometrik cihazı çalıştırın ( bkz. Malzeme Tablosu) ve makineyi 37 °C'ye ısıtın. Senaryoyu belirtildiği gibi hazırlayın:
- Reaksiyonun kinetiğini belirlemek için 40 dakika boyunca her dakika bireysel okumalar yapın.
- Uyarımı 360 nm'ye ve emisyonu 465 nm'ye ayarlayın. Kuyu başına on flaş yeterlidir.
- Rekombinant kaspaz-3'ün pozitif kontrolünü hazırlayın (bakınız Malzeme Tablosu). Rekombinant kaspaz-3 enziminin 1 U'sunu 50 μL lizis tamponunda (tüp 1) karıştırın. Ek üç tüpe 25 μL lizis tamponu ekleyin. Tüp 1'den tüp 2'ye 25 μL aktarın. Pipetleme ile karıştırın.
- Tüp 3 ve tüp 4 için tekrarlayın. Tüp 5 sadece 50 μL lizis tamponu içerecektir. Adım 3.6'da belirtilen kaspaz-3 aktivite testi için beyaz düz tabanlı 96 delikli plakaya her standardın 25 μL'sini ekleyin.
- Buz üzerinde kaspaz aktivitesi testi için bir ana reaksiyon karışımı hazırlayın. Bir reaksiyon için, 50 μL 2x kaspaz bölünme tamponu (0.2M HEPES pH 7.5; % 20 sakkaroz veya PEG; % 0.2 CHAPS), 5 μL 1 mM DEVD-AMC (kaspaz-3 tetrapeptid substratı), 2 μL 500 mM DTT ve 18 μL deiyonize su karıştırın (bkz.
- Toplam 100 μL'lik bir reaksiyon hacmi elde etmek için her numuneye ve standarda 75 μL reaksiyon karışımı ekleyin.
- Adım 5.1'de ayarlanan florometrik cihazı kullanarak floresanı hemen ölçün.
- Her floresan ölçümü için, boşluğun floresan okumasını (yalnızca lizis tamponu) numunenin floresansından çıkarın. Numunenin protein konsantrasyonuna bölerek okumayı normalleştirin (adım 4.5'te hesaplanmıştır)27:
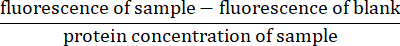
- Y eksenindeki normalleştirilmiş floresanın eğimini ve x eksenindeki zamanı belirleyerek kaspaz aktivitesinin oranını hesaplayın.
6. Kaspaz-3/kaspaz-7 aktivitesi için tek hücreli tahlil (akış sitometri analizi)
- Hücreleri bölüm 2'de açıklandığı gibi tohumlayın.
- Hücreleri 5 mL'lik bir polistiren tüpe toplayın. Yapışkan hücrelerle çalışıyorsanız, ortamı 5 mL tüpe toplayın. Hücre kültürü plakasına 1 mL soğuk PBS ekleyin ve PBS'yi 5 mL tüpe toplayın. Hücrelere tripsin ekleyin (6 kuyucuklu bulaşıklarla çalışıyorsanız 100 μL). Tripsinin hücreleri plakadan kaldırmasına izin verin ve 5 mL tüpe toplayın. Tüm hücrelerin toplandığından emin olmak için 1 mL soğuk PBS kullanın.
NOT: Süspansiyon hücreleriyle çalışıyorsanız, ortamı ve hücreleri yavaşça 5 mL'lik bir tüpe aktarın. - Numuneleri 5 dakika, 4 ° C boyunca 300 x g'de santrifüj yapın. Bir vakum aspiratörü kullanarak süpernatantı çıkarın.
- Boyama karışımını hazırlayın. Optimum boyama konsantrasyonu, 50 μL'de 1 x 106-2 x 106 hücredir. Florojenik substratı üreticinin talimatlarına göre seyreltin (bakınız Malzeme Tablosu, akış sitometrisi). Stok substratından 1 μL alın ve 150 μL PBS içinde seyreltin. Örnek başına 50 uL ekleyin.
- Numuneleri ışıktan korunarak 37 °C'de 30 dakika boyunca inkübe edin ve her 15 dakikada bir karıştırın.
- Bu çalışmada kullanılan akış sitometresi ile kırmızı lazeri 640 nm'de kullanın ve 675/25 nm kullanarak tespit edin. Önce lekesiz kontrol örneğini çalıştırın ve istenen popülasyondan en az 10.000 olay elde edin. FSC-A ve SSC-A nokta grafiğinde bir kapı (P1) kullanarak kalıntıları hariç tutun.
- P1 kapısındaki olayları görüntüleyen bir histogram kullanın ve medyan floresan yoğunluğunu (MFI) belirlemek için kaspaz substratı (y ekseni) için algılama kullanın.
NOT: Bu yöntemde açıklanan kaspaz substratı, 590 nm'de bir uyarma gerektirir ve 628 nm'de yayılır.
- P1 kapısındaki olayları görüntüleyen bir histogram kullanın ve medyan floresan yoğunluğunu (MFI) belirlemek için kaspaz substratı (y ekseni) için algılama kullanın.
Sonuçlar
Primer fare makrofajları 6 gün boyunca farklılaştı. 6 gün sonra, hücreler toplandı, sayıldı ve tohumlandı. Aşağıdaki tedaviler kullanıldı: tedavi yok ve 250 nM'de Smac mimetik (Bileşik A)22 ve 16 saat boyunca 500 nM (Şekil 1). Deney, kaspaz-3 / kaspaz-7 aktivasyonunun popülasyon tabanlı bir tahlil veya akış sitometrisi kullanılarak tek hücreli analiz ile değerlendirilmesine izin vermek için çift olarak gerçekleştirildi.
Hücre lizatlarının protein konsantrasyonu, BCA testi kullanılarak ölçüldü (Ek Tablo 1). Bu, kaspaz-3 / kaspaz-7 aktivite testinde kullanılan protein miktarının numuneler arasında aynı olmasını sağlamak için gereklidir. Bu popülasyon bazlı tahlilde, veriler iki şekilde sunulabilir. Birincisi, ayarlanan floresansı (y ekseni) zamana (x ekseni) karşı çizerek kinetiği göstermektir (Şekil 2A). Alternatif olarak, eğim numuneleri doğrudan karşılaştırmak için hesaplanabilir (Şekil 2B). 500 nM Smac mimetik tedavisine göre eğimdeki artış, çoklu karşılaştırmalara sahip sıradan bir tek yönlü ANOVA'ya dayanarak anlamlı değildi (Dunnett'in çoklu karşılaştırma testi28).
Akım sitometrisi kullanılarak kaspaz-3/kaspaz-7 aktivitesinin analizi için hücreler ve süpernatant toplandı. Lekesiz hücreler veya floresan eksi bir, tedavi edilmemiş hücrelerin yanı sıra negatif kontrol olarak kullanılmıştır. Akış sitometrisi ile toplanan hücrelerin histogramı, tedavi edilmemiş hücrelere kıyasla Smac mimetiği ile tedavi edilen hücreler için floresanda bir kayma gösterdi (Şekil 2C). Veriler medyan floresan yoğunluğu (Şekil 2D) veya tedavi edilmemiş hücreler üzerinde bir kıvrım değişimi (Şekil 2E) olarak gösterilebilir.

Şekil 1: Çalışmanın akış şeması . (A) Femurlar ve tibiaslar C57Bl/6 farelerden eksize edildi. Kemikler 6 gün boyunca 20 ng/mL M-CSF ile yıkandı ve farklılaştırıldı. (B) 6. günde, makrofajlar hasat edildi ve tedavi için yeniden tohumlandı. Bir hücre seti lizatlar için toplandı ve florojenik aktivite ile değerlendirilirken, diğer set toplandı, florojenik substrat ile inkübe edildi ve akış sitometrisi ile değerlendirildi. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
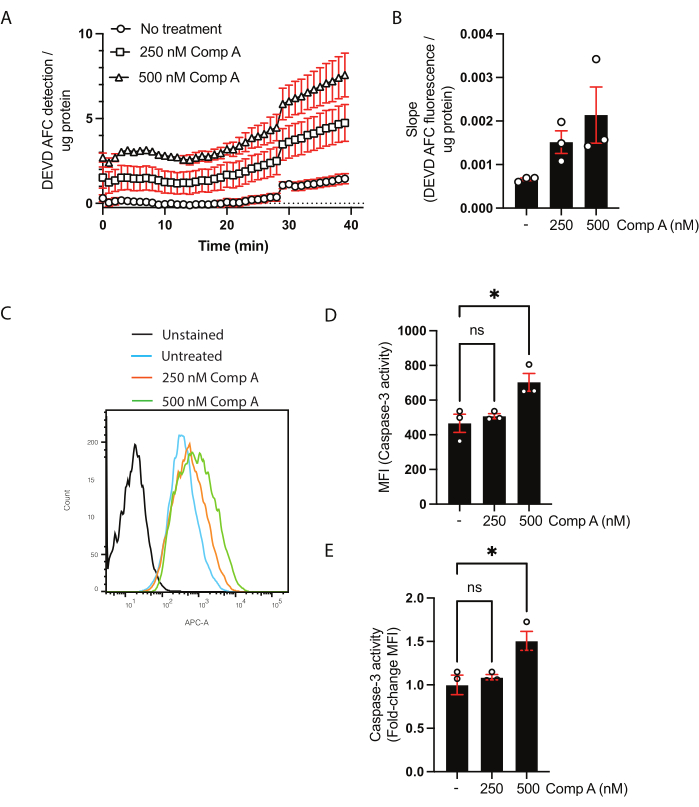
Şekil 2: Akım sitometrisi ile kaspaz-3/kaspaz-7 aktivitesi ve substrat bölünmesi için kinetik tahlil. (A,B) Kaspaz-3/kaspaz-7 aktivitesi (C-E) ve akım sitometrisi ile substrat bölünmesi için kinetik tahlilin temsili verileri. Makrofajlar, 16 saat boyunca iki konsantrasyonda Smac mimetik (Bileşik A; 250 nM ve 500 nM) ile muamele edildi. (A) Zamanla parçalanmış DEVD AFC substratının tespiti. Veriler, numunedeki protein konsantrasyonuna normalleştirildi. (B) Her numune için DEVD AFC'nin bölünme hızı (eğimi), işlenmemiş eğime normalleştirildi ve işlenmemiş hücreler üzerinde kıvrım değişimi olarak sunuldu. (C) Kaspaz-3 substratı ile inkübe edilen hücrelerin akış sitometrik histogramları. (D,E) İşlenmemiş numuneye kıyasla MFI karşılaştırması ve MFI'daki katlama değişimi. Her veri noktası bağımsız bir örneği temsil eder; ortalamanın standart hatası ± gösterilmiştir; *p < tek yönlü ANOVA ve çoklu karşılaştırma testleri (Dunnett'in çoklu karşılaştırma testi) kullanılarak 0.05'tir. Bu şeklin daha büyük bir versiyonunu görüntülemek için lütfen buraya tıklayın.
| Kaspaz | Tür | Substrat sırası | Protein alanları | ||
| Kaspaz-1 | Hs, Mm | (W/L) İHB | CARD, büyük etki alanı, küçük katalitik etki alanı | ||
| Kaspaz-2 | Hs, Mm | DEXD | CARD, büyük etki alanı, küçük katalitik etki alanı | ||
| Kaspaz-4 | Hs | (W/L) İHB | CARD, büyük etki alanı, küçük katalitik etki alanı | ||
| Kaspaz-5 | Hs | (W/L) İHB | CARD, büyük etki alanı, küçük katalitik etki alanı | ||
| Kaspaz-9 | Hs, Mm | (I/V/L) E(H/T)D | CARD, büyük etki alanı, küçük katalitik etki alanı | ||
| Kaspaz-11 | Mm | (W/L) İHB | CARD, büyük etki alanı, küçük katalitik etki alanı | ||
| Kaspaz-12 | Mm | ATAD | CARD, büyük etki alanı, küçük katalitik etki alanı | ||
| Kaspaz-8 | Hs, Mm | (I/V/L) E(H/T)D | DED, büyük alan, küçük katalitik etki alanı | ||
| Kaspaz-10 | Hs | (I/V/L) E(H/T)D | DED, büyük alan, küçük katalitik etki alanı | ||
| Kaspaz-3 | Hs, Mm | DEXD | büyük alan, küçük katalitik etki alanı | ||
| Kaspaz-6 | Hs, Mm | (I/V/L) E(H/T)D | büyük alan, küçük katalitik etki alanı | ||
| Kaspaz-7 | Hs, Mm | DEXD | büyük alan, küçük katalitik etki alanı | ||
| kaspaz-14 | hs, mm | (W/L) İHB | büyük alan, küçük katalitik etki alanı | ||
| KART | caspase aktivasyon ve işe alım domain | ||||
| DED | ölüm efektör alanı | ||||
| Hs | homo sapien | ||||
| Mm | mus musculus | ||||
Tablo 1: Substrat özgüllüğü ve kaspazların protein alanları. Tablo McStay ve ark.20'den uyarlanmıştır; Shalini ve ark.3; ve van Opdenbosch ve Lamkanfi4.
Ek Tablo 1: DEVD kinetik analizi. Bu tabloyu indirmek için lütfen tıklayınız.
Tartışmalar
Bu yöntemde, kaspaz-3 / kaspaz-7 aktivitesini ölçmek için popülasyon bazlı bir tahlilde veya tek hücreli analizde florojenik bir substrat kullanılır. Her iki yöntem de kaspaz aktivitesini bir substratın bölünmesine dayanan nicel bir şekilde ölçer. Bir avantaj, bu yöntemleri çok sayıda numune için kullanabilme yeteneğidir. Bu yöntemlerle, Smac mimetiği ile tedavi edilen primer makrofajlarda kaspaz-3/kaspaz-7 aktivitesi saptanır.
Popülasyon bazlı florometrik tahlilin kritik bir yönü, lizisten floresanı okumaya kadar geçen süredir. Numuneler, özellikle tahlil "okunmadan" önce, prosedür boyunca buz üzerinde tutulmalıdır. Bu, substratın erken bölünmesini ve floresansını önler. Popülasyon bazlı tahlil kullanılarak, daha az optimizasyon gerekebilir. Tahlilde kullanılan protein miktarı normalleştirilerek numunelerin doğrudan karşılaştırılmasına izin verilir. Bir uyarı, apoptotik hücre ölümünün geç bir aşamasında, toplam protein miktarının azalmasıdır; Bu nedenle, kaspaz aktivitesinin saptanması mümkün olmayabilir. Bu sorunu aşmak için farklı kinetik veya farklı tedavi dozları önerilir. Ayrıca kaspaz aktivitesinin oranını doğru bir şekilde değerlendirmek için bu yöntemde açıklanan yazılımların yanı sıra başka yazılımlar da kullanılabilir.
Akış sitometrik testi için, popülasyonları güvenle geçmek için yeterli olay veya hücre gereklidir. Ek olarak, substratın hücre sayısına optimal oranını elde etmek için akışa dayalı tahlilde daha fazla optimizasyon gerekebilir. Bununla birlikte, akış sitometrisi ile bu yöntem, hücre tipi tanımlaması için hücre yüzey belirteçleri gibi ek parametrelerin ölçülmesine katkıda bulunur.
Hem popülasyon hem de tek hücreli yöntemler diğer kaspazlar için kullanılabilir. Bununla birlikte, tanıma sekansının diğer kaspazlar için daha az ayırt edildiğini hatırlamak önemlidir. Bu nedenle, kaspaz aktivitesi için diğer yöntemler kullanılmalıdır. Bu, kaspaz aktivitesinin inhibisyonunu, CRISPR'yi veya spesifik kaspazların yıkılmasını ve bilinen substratların bölünmesini tespit etmek için batı lekelenmesini içerir.
Kaspaz aktivitesini saptamak için alternatif bir yöntem hızlandırılmış görüntülemedir. Aynı geçirgen kaspaz substratı, hücre ölümünün kinetiği hakkında bilgi sağlamak için ek V gibi diğer canlılık belirteçleri ile birlikte kullanılabilir. Görüntüleme ayrıca kaspaz aktivitesini ve hücre sağkalımını ayıracak ve bir hücre popülasyonunda subletal miktarlarda kaspaz aktivitesinin tespit edilmesine izin verecektir. Kaspaz-3 / kaspaz-7'nin ölümcül olmayan fonksiyonları, doğuştan gelen immün hücrelerde antiviral regülasyonile bağlantılıdır 29, özellikle mitokondriyal DNA salınımı yoluyla tip I IFN'nin aktivasyonu15,16. Bu nedenle, kaspaz aktivitesini ölçmek için yapılan bu testler, farklı hücre ölümü modlarını tanımlamak için kritik öneme sahiptir ve hücre dışı ölüm fonksiyonlarının değerlendirilmesinde yararlı olabilir.
Açıklamalar
Yazarların açıklayacağı bir çıkar çatışması yoktur.
Teşekkürler
W.W.W. Clöetta Medical Research Fellow hibesi, S.R. CanDoc UZH Forschungskredit ve J.T. Çin Burs Konseyi tarafından desteklenmektedir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| 1.5 mL microfuge tubes | Sarstedt | 72.706.400 | |
| 15 cm Petri plates | Sarstedt | 82.1184.500 | |
| 37 degree incubator shaker | IKA shaker KS 4000i | 97014-816 | distributed by VWR |
| 6-well cell culture dish | Sarstedt | 83.392 | |
| 96 well flat bottom, white polystyrene, non-sterile | Sigma | CLS3600 | |
| 96 well flat plate | Sarstedt | 82.1581 | |
| Ac-DEVD-AFC | Enzo Life Sciences | ALX-260-032-M005 | Caspase-3 substrate |
| BD Fortessa | BD | any flow cytometer with the appropriate excitation and emission detector will work | |
| b-glycerolphosphate | Sigma | G9422-10G | |
| caspase-3 recombinant | Enzo Life Sciences | ALX-201-059-U025 | |
| CHAPS | Sigma | 1.11662 | |
| DMEM, low glucose, pyruvate | Thermoscientific | 31885023 | |
| DMSO | Sigma | D8418-250ML | |
| EDTA | Sigma | 03685-1KG | |
| EGTA | Sigma | 324626-25GM | |
| Etoposide | MedChem Express | HY-13629 | |
| FBS | Thermoscientific | 26140 | |
| Flow cytometry tubes | Falcon | 352008 | |
| Flowjo | Flowjo | A license in required but any program that can analyze .fcs files will suffice | |
| Glycerol | Sigma | G5516-500ML | |
| HEPES | Sigma | H4034 | |
| Magic Red caspase-3/7 assay kit; flow cytometry or imaging | Immunochemistry Technologies | 935 | |
| M-CSF | ebioscience | 14-8983-80 | now a subsidiary of Thermoscientific |
| M-Plex | Tecan | any fluorometric reader will work with the appropriate excitation and emission detectors | |
| NaCl | Roth | 3957.1 | |
| PBS pH 7.4 | Thermoscientific | 10010023 | |
| Penicillin-Streptomycin-Glutamine (100X) | Thermoscientific | 10378016 | |
| Pierce BCA Protein Assay Kit | ThermoFisher Scientific | 23225 | protein concentration assay |
| protease inhibitors | Biomol | P9070.100 | |
| Smac mimetic, Compound A | Tetralogics | also known as 12911; structure shown in supplementary figures of Vince et al., Cell 2007 | |
| Sodium Fluoride | Sigma | S7920-100G | |
| sodium orthovanadate | Sigma | S6508-10G | |
| sodium pyrophosphate | Sigma | P8010-500G | |
| Staurosporine | MedChem Express | HY-15141 | |
| sucrose | Sigma | 1.07687 | |
| Tris Base | Sigma | T1503-1KG | |
| Triton X100 | Sigma | T8787-50ML | |
| TrypLE | Thermoscientific | A1285901 | In the protocol, it is listed as Trypsin |
Referanslar
- Ramirez, M. L. G., Salvesen, G. S. A primer on caspase mechanisms. Seminars in Cell and Developmental Biology. 82, 79-85 (2018).
- Nicholson, D. W., Thornberry, N. A. Caspases: Killer proteases. Trends in Biochemical Sciences. 22 (8), 299-306 (1997).
- Shalini, S., Dorstyn, L., Dawar, S., Kumar, S. Old, new and emerging functions of caspases. Cell Death and Differentiation. 22 (4), 526-539 (2014).
- Van Opdenbosch, N., Lamkanfi, M. Caspases in cell death, inflammation, and disease. Immunity. 50 (6), 1352-1364 (2019).
- Kesavardhana, S., Malireddi, R. K. S., Kanneganti, T. -. D. Caspases in cell death, inflammation, and pyroptosis. Annual Review of Immunology. 38, 567-595 (2020).
- Fu, T. -. M., et al. Cryo-EM structure of caspase-8 tandem DED filament reveals assembly and regulation mechanisms of the death-inducing signaling complex. Molecular Cell. 64 (2), 236-250 (2016).
- Jiang, X., Wang, X. Cytochrome c promotes caspase-9 activation by inducing nucleotide binding to Apaf-1. Journal of Biological Chemistry. 275 (40), 31199-31203 (2000).
- Christgen, S., Place, D. E., Kanneganti, T. -. D. Toward targeting inflammasomes: Insights into their regulation and activation. Cell Research. 30 (4), 315-327 (2020).
- Shi, J., et al. Cleavage of GSDMD by inflammatory caspases determines pyroptotic cell death. Nature. 526 (7575), 660-665 (2015).
- Sborgi, L., et al. GSDMD membrane pore formation constitutes the mechanism of pyroptotic cell death. EMBO Journal. 35 (16), 1766-1778 (2016).
- Rühl, S., et al. ESCRT-dependent membrane repair negatively regulates pyroptosis downstream of GSDMD activation. Science. 362 (6417), 956-960 (2018).
- Declercq, W., Takahashi, N., Vandenabeele, P. Dual face apoptotic machinery: From initiator of apoptosis to guardian of necroptosis. Immunity. 35 (4), 493-495 (2011).
- Newton, K., et al. Cleavage of RIPK1 by caspase-8 is crucial for limiting apoptosis and necroptosis. Nature. 574, 428-431 (2019).
- Fritsch, M., et al. Caspase-8 is the molecular switch for apoptosis, necroptosis and pyroptosis. Nature. 575, 683-687 (2019).
- White, M. J., et al. Apoptotic caspases suppress mtDNA-induced STING-mediated type I IFN production. Cell. 159 (7), 1549-1562 (2014).
- Rongvaux, A., et al. Apoptotic caspases prevent the induction of type I interferons by mitochondrial DNA. Cell. 159 (7), 1563-1577 (2014).
- Nakajima, Y. -. I., Kuranaga, E. Caspase-dependent non-apoptotic processes in development. Cell Death and Differentiation. 24, 1422-1430 (2017).
- Kumar, S., Dorstyn, L., Lim, Y. The role of caspases as executioners of apoptosis. Biochemical Society Transactions. 50 (1), 33-45 (2022).
- Agniswamy, J., Fang, B., Weber, I. T. Plasticity of S2-S4 specificity pockets of executioner caspase-7 revealed by structural and kinetic analysis. FEBS Journal. 274 (18), 4752-4765 (2007).
- McStay, G. P., Salvesen, G. S., Green, D. R. Overlapping cleavage motif selectivity of caspases: implications for analysis of apoptotic pathways. Cell Death and Differentiation. 15 (2), 322-331 (2008).
- Thornberry, N. A., et al. A combinatorial approach defines specificities of members of the caspase family and granzyme B. Functional relationships established for key mediators of apoptosis. Journal of Biological Chemistry. 272 (29), 17907-17911 (1997).
- Vince, J. E., et al. IAP antagonists target cIAP1 to induce TNFalpha-dependent apoptosis. Cell. 131 (4), 682-693 (2007).
- McComb, S., et al. cIAP1 and cIAP2 limit macrophage necroptosis by inhibiting Rip1 and Rip3 activation. Cell Death and Differentiation. 19 (11), 1791-1801 (2012).
- Wong, W. W. -. L., et al. cIAPs and XIAP regulate myelopoiesis through cytokine production in an RIPK1- and RIPK3-dependent manner. Blood. 123 (16), 2562-2572 (2014).
- Liu, X., Quan, N. Immune cell isolation from mouse femur bone marrow. Bio-Protocol. 5 (20), e1631 (2015).
- Lin, H., Chen, C., Chen, B. D. Resistance of bone marrow-derived macrophages to apoptosis is associated with the expression of X-linked inhibitor of apoptosis protein in primary cultures of bone marrow cells. Biochemical Journal. 353 (Pt 2), 299-306 (2001).
- . Caspase activity assay buffer. Cold Spring Harbor Protocols. , (2015).
- Mackridge, A., Rowe, P. One-way analysis of variance (ANOVA) - Including Dunnett's and Tukey's follow up tests. Practical Approach to Using Statistics in Health Research: From Planning to Reporting. , 93-103 (2018).
- Chen, H., Ning, X., Jiang, Z. Caspases control antiviral innate immunity. Cellular and Molecular Immunology. 14 (9), 736-747 (2017).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır