Bu içeriği görüntülemek için JoVE aboneliği gereklidir. Oturum açın veya ücretsiz deneme sürümünü başlatın.
Method Article
CDH1 Gen Mutasyonu Tedavisi için Robotik Vagus Koruyucu Total Gastrektomi
Bu Makalede
Özet
Bu makalede robotik vagus koruyucu total gastrektomi üzerinde durulmuştur. Vagus koruma, dikişli özofagojejunostomi, jejunal poş oluşumu ve zımba zımbalı jejunojejunostomi ile Roux-en-Y rekonstrüksiyonunun teknikleri ve tuzakları tartışılmıştır.
Özet
CDH1 gen mutasyonunun neden olduğu kalıtsal diffüz mide kanseri (HDGC), diffüz mide kanseri riskini artıran ve gastroskopi taraması ile tespit edilmesi neredeyse imkansız olan kalıtsal bir kanser sendromudur. Önerilen koruyucu tedavi total gastrektomidir. Robotik cerrahi, olumsuz fonksiyonel sonuçları potansiyel olarak azaltmak için anastomozlar ve posterior vagusun korunması için minimal invaziv cerrahi (MIS) tekniklerin kullanımını kolaylaştırır. Genetik testlerle kanıtlanmış CDH1 gen mutasyonu olan asemptomatik 24 yaşında erkek hasta ve ailesinde HDGC nedeniyle total gastrektomi geçiren bir erkek kardeş bu teknikle tedavi edildi. Bu video olgu sunumu, hasta pozisyonu ve port yerleşimi, posterior vagus koruyucu diseksiyon, dikişli özofagojejunostomi, jejunal poş oluşumu ve stapler zımbalı jejunojejunostomi ile Roux-en-Y rekonstrüksiyonu açısından robotik cerrahinin tekniklerini ve tuzaklarını göstermektedir. Bu teknikler profilaktik gastrektomi olgusunda gösterilmekle birlikte, birçoğu diğer benign ve bariatrik foregut ve genel cerrahi tiplerine uygulanabilir. Robotik cerrahi, bu vagus koruyucu total gastrektomi vakasında tarif edildiği gibi foregut MIS tekniğini kolaylaştırabilir.
Giriş
Kalıtsal diffüz mide kanseri (HDGC), otozomal dominant kalıtımpaterni 1 olan E-kaderin (CDH1) tümör baskılayıcı genindeki genetik bir mutasyon ile karakterizedir. Bu kalıtsal kanser sendromu, yaygın mide kanseri ve lobüler meme kanseri (LBC) riskini artırır. Mevcut kılavuzlar, ailesel HDGC ve LBC kümeleri olan hastalarda, özellikle erken başlangıçlı (40 yaşından önce) hastalarda CDH1 mutasyonlarının test edilmesini önermektedir2. Bildirilen en büyük CDH1 mutasyon taşıyıcıları serisine göre, mide kanserinin kümülatif yaşam boyu insidansı erkekler için %70 (%95 CI, %59-%80) ve bu mutasyona sahip kadınlar için %56 (%95 CI, %44-%69)'dur3. Bununla birlikte, son zamanlarda yapılan çalışmalar, bu mutasyon ile mide kanseri penetransının erkeklerde %37-42 ve kadınlarda %25-33 aralığında olduğunu tahmin etmiştir1.
Biyopsilerle endoskopik sürveyans, profilaktik gastrektomiyi geciktirmeyi seçenler için önerilen sürveyans türüdür; Bununla birlikte, bu kohortta tarama gastroskopisi2 kullanılarak erken mide kanserini tespit etmek neredeyse imkansızdır. Kapsamlı beyaz ışıklı endoskopik muayeneyi, midenin beş ayrı bölgesinden en az 30 hedeflenmemiş mide biyopsisi takip eder. Bununla birlikte, bu sürveyans yöntemi yüksek bir yanlış negatif oranına sahiptir ve gizli taşlı yüzük hücre odaklarının yalnızca %20-63'ünü tespit eder 4,5.
Profilaktik total gastrektomi (PTG), 20 yaşında başlayan herhangi bir patojenik veya olası patojenik CDH1 varyant taşıyıcısı için önerilen önleyici tedavidir, ancak 70 yaşından sonra önerilmez 1,2. Perigastrik lenf nodu metastazı, tipik olarak T1a veya in situ taşlı yüzük hücrelerine sahip asemptomatik hastalarda nadir görülen bir bulgudur. Perioperatif morbidite genellikle düşük, hasta memnuniyeti yüksektir6. Ameliyat sonrası genel yaşam kalitesi yüksek olmasına rağmen, total gastrektomide genellikle trunkal vagotomi yapılır 7,8. Vagus sinirinin çölyak ve hepatik dalların seviyesinin üzerine çıkarılması, hepatobiliyer ağacın ve ince ve kalın bağırsağın parasempatik denervasyonuna yol açar. Vagotomi sonrası ishal ve dumping sendromu PTG8'i takiben iyi bilinen uzun vadeli komplikasyonlardır.
Robotik cerrahi, cerraha cerrahi alanın 3 boyutlu, 10x büyütülmüş bir görünümünü sağlar ve eklemli cerrahi aletlerle yüksek derecede serbestlik sunar9. Bu tekniğin önceden uygulanmasının amacı, minimal invaziv cerrahi (MIS) tekniklerle kolaylaştırılan posterior vagusun korunması yoluyla olumsuz fonksiyonel sonuçları potansiyel olarak azaltmaktır.
Protokol
Hasta, kimliksizleştirilmiş bilgilerin, görüntülerin ve video belgelerinin yayınlanması için bilgilendirilmiş onam verdi. Doçent Dr. Michael Talbot (ortak yazar), kurumunda gastrektomi yapmak için akredite edilmiş bir üst gastrointestinal cerrahtır. Bu vaka raporunun ve protokolün ihmal edilebilir riski nedeniyle, yerel kurumsal inceleme kurulu yönergelerine göre etik incelemeden muaf tutulmuştur. Olgu sunumları için etik başvuru, yerel kurumsal inceleme kurulu yönergelerine göre muaftır.
1. Hasta konumlandırma
- Genel anestezi verildikten sonra hastayı ters Trendelenburg pozisyonuna getirin.
- Hastayı bir ayak plakası, dizlerin üzerine yerleştirilmiş bir vücut kayışı ve ayak bileği kayışları ile pozisyonda sabitleyin. Kolları (<90°) alın ve kol tahtalarına krep bandajlayın. Ameliyat masasına, kraniyal olarak sol kol tahtasına bir Nathanson karaciğer ekartör braketi yerleştirin.
2. Bağlantı noktası yerleşimi (Şekil 1)
- Göbek seviyesinde veya altında sağ orta klaviküler pozisyonda cerrahın tercih ettiği yaklaşımla 12 mm'lik bir cilt kesisi yapın. Bu kesiden 8 mm, 0° laparoskop dürbünü ve 12 mm port ile optik giriş yapın. Kamera bağlantı noktasının hedef anatomiden 10-20 cm uzakta olması gerektiğini unutmayın.
- Bağlantı noktasını 12-8 mm redüktörlü 12 mm'lik bir robotik (zımbalama) bağlantı noktasıyla değiştirin ve laparoskopu 8 mm, 30°'lik bir laparoskopla değiştirin. 45 mmHg akışla 15 mmHg CO2 pnömoperitoneum oluşturun.
- Transumbilikal düzlemde üç adet 8 mm'lik ek cilt kesisi yapın ve üç adet 8 mm'lik robotik port yerleştirin. Robotik portlardan birini göbek deliğine, diğer iki robotik portu ise onun yanına sol tarafa yerleştirin. Bağlantı noktaları arasında >8 cm ve bağlantı noktaları ile hedef anatomi arasında 10-20 cm mesafe olduğundan emin olun.
- Sağ üst çeyreğe başka bir 12 mm yardımcı bağlantı noktası (bağlantı noktası A) yerleştirin. 5 mm'lik bir kesiden epigastriuma bir Nathanson ekartörü yerleştirin ve karaciğerin sol lobunu geri çekin.
- Robotik hasta arabasını, karaciğer ekartörü ile çarpışmayı önlemek için hastanın sağ tarafından hastanın üzerine yerleştirin. Önce lazer kılavuzlu bağlantı noktası yerleşimini kullanarak kamera kolunu yerleştirin. Bağlantı noktası 3'ü kullanarak 8 mm, 30° robotik dürbün ile mideyi hedef alan bir insizürasyon gerçekleştirin.
- Kalan robotik bağlantı noktalarını alet kollarına yerleştirin ve geğirin ve ardından bir kuvvet bipolar 8 mm aleti (bağlantı noktası 1), bir kap kapatıcı uzatma (bağlantı noktası 2) ve bir devrilme fenestre kavrayıcı (kap 4) yerleştirin. Monopolar ve bipolar otomatik kesme ve zorlanmış pıhtılaşmayı efekt 3'te ayarlayın ve sistem kurulumunu kontrol edin.
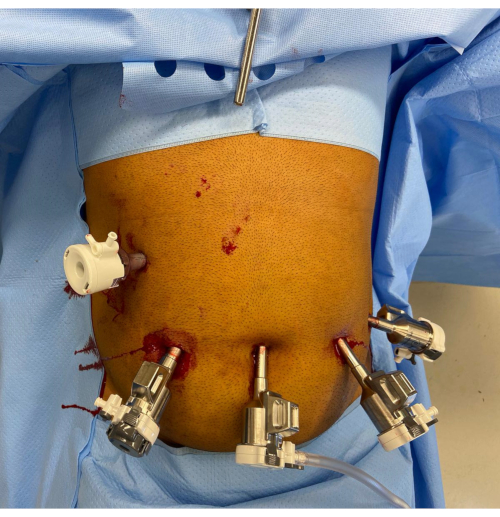
Şekil 1: Robotik port yerleşimi. Nathanson ekartör kolu epigastriumda görülür. Sağ üst kadranda 12 mm'lik bir yardımcı bağlantı noktası vardır. Görüntünün solundan sağına kalan bağlantı noktaları, redüktörlü 12 mm robotik bağlantı noktası, 8 mm kamera bağlantı noktası ve iki ek 8 mm robotik bağlantı noktasıdır. Bu rakamın daha büyük bir sürümünü görüntülemek için lütfen buraya tıklayın.
3. Vagus koruyucu diseksiyon
- Midenin daha büyük eğrisini antrumdan kardiyaya kadar gastrokolik ligament boyunca mobilize edin ve arcade damar kapatıcısının lateralinde beş ila yedi kısa mide damarına bölün, N1 düğümlerini içerecek şekilde uzanın. Ardından, özofagus boşluğunun sol tarafını harekete geçirin.
- Frenoözofageal ligamente girin ve distal özofagusun sol tarafını harekete geçirin. Damar kapatıcı ile distal diseksiyon yapın ve duodenumun ilk kısmının mobilizasyonuna kadar devam edin. Sağ taraflı özofagus mobilizasyonunu tamamlamak için pars flaccida'dan supraduodenal pencereyi takip edin ve diseksiyon düzlemi özofagusa bitişik hale getirin.
- Duodenumun ilk kısmını, bir payanda takviyesi ile 60 mm x 4,3 mm yeşil yeniden yükleme kullanarak robotik zımba ile kesin. Damar kapatıcıyı kullanarak sol mide damarlarını mide duvarına yakın bölün. Bu, posterior vagusun sol mide pedikülü etrafındaki mezenterde bölünmeden bırakılmasını sağlamak içindir.
- Yemek borusu ve mideyi süperolateral yönde geri çekin ve posterior vagus sinirini tanımlayın. Siniri arkaya doğru süpürün ve koruyun.
4. Özofagojejunostomi jejunal kese ile sütür
- Frenoözofageal ligament rekonstrüksiyonu
- Frenoözofageal ligament rekonstrüksiyonunu, 26 mm 1/2 daire konik uçlu bir iğne üzerinde 2-0 emilmeyen dikenli sütür kullanarak saat 5'ten saat 9'a kadar saat yönünün tersine sürekli olarak gerçekleştirin. 60 mm x 4,3 mm yeşil yeniden yükleme kullanarak intraabdominal yemek borusunu robotik zımba ile kesin. Ayrılan mideyi sağ üst kadrana taşıyın.
- Özofagojejunal anastomoz
- Duodenojejunal fleksurayı tanımlamak için büyük omentumu kraniyal olarak kaldırın ve yemek borusuna 50 cm'lik bir jejunal döngü getirin (jejunal kese oluşumundan sonra 40-60 cm'lik bir biliopankreatik uzuv oluşturun).
- 23 cm uzunluğunda 3-0 emilebilir dikenli sütür, 26 mm 1/2 daire konik uçlu iğne üzerine saat 3 yönünde lateral özofagojejunal peksi olarak dikiş. Kesilmemiş sütürü lateral olarak geri çekin. 18Fr nazogastrik tüp kılavuzu ile monopolar diatermi kancası kullanarak zımba hattının önünde bir özofagostomi oluşturun. Özofagostomi için yapılana eşit veya biraz daha küçük boyutta bir jejunostomi oluşturun.
- Özofagojejunostomi'nin arka duvarını dikenli sütür ile saat 3'ten saat 9'a kadar sürekli, saat yönünde, zımba hattını içerecek şekilde dikin. Özofagojejunal anastomoz için tam kalınlıkta tek katmanlı sütürü tamamlamak için aynı sütürden başka bir tane kullanarak ön kısmı dikin. Anastomozun ötesine medial peksi olarak birkaç medial sütür yerleştirin.
- Jejunal kese
- Proksimal jejunal halkayı 60 mm x 2,5 mm beyaz yeniden yükleme kullanarak robotik bir zımba ile anastomozdan 10 cm uzakta kesin. Özofagojejunal anastomozun 10 cm proksimal ve distalinde antimesenterik enterostomiler oluşturun.
- Jejunal torbayı oluşturmak için 60 mm x 2,5 mm beyaz yeniden yükleme kullanarak robotik zımbayı iki kez ateşleyin. Anastomozlara giden kan akışını korumak için ikinci ateşlemenin özofagojejunal anastomozu karşılamak için sonuna kadar gitmediğinden emin olun. Jejunal enterotomiyi 3-0 emilebilir dikenli sütür ile sürekli bir şekilde kapatın.
5. Zımbalanmış jejunojejunostomi
- 70 cm'lik bir sindirim uzvunu ölçün ve bu noktada 2-0 ipek kesintili bir sütür yerleştirin ve hem işaretleme hem de retraksiyon için distal biliopankreatik uzuv yerleştirin.
- Laparoskopik gastrik bypass için üçlü zımbalama tekniğinde açıklandığı gibi, yalnızca zımba tekniği kullanarak jejunojejunostomiyi oluşturun10,11. Anastomozu oluşturmak ve enterotomiyi kapatmak için 60 mm x 2,5 mm beyaz yeniden yükleme kullanın.
- İç fıtıklaşmaya bağlı komplikasyon riskini azaltmak için 2-0 emilmeyen dikenli sütürler kullanarak hem jejunal hem de retro-Roux mezenterik defektleri kapatın.
6. Numune çıkarma ve kapatma
- Aletleri, Nathanson ekartörünü ve bağlantı noktalarını robotik görüş altında çıkarın. Robotik hasta arabasını hastadan ayırın.
- Göbek portunun uzatılması yoluyla 5 cm'lik bir mini laparotomi oluşturun. Numuneyi küçük bir O-ring yara koruyucu ekartör ile teslim edin. Laparotomiyi her zamanki gibi, sürekli fasyal kapama ve 1:4 sütür / yara uzunluğu oranı ile kas koruyucu dikişler kullanarak kapatın.
Sonuçlar
Toplam ameliyat süresi 2 sa 50 dk idi ve hastanın ameliyat sonrası seyri hiç de dikkat çekmeyen bir seyir izledi. Hasta ameliyattan sonraki 1. günde serbest sıvı diyetine tabi tutuldu ve 4. günde hastaneden taburcu edildi. 1 aylık ve 3 aylık takiplerde hasta iyiydi ve ishal veya dökülme semptomu bildirmedi.
Örnek patolojik inceleme için gönderildi ve taşlı yüzük hücreli adenokarsinom tarafından lamina propria'nın yüzeysel invazyonunun b...
Tartışmalar
Genetik testlerle kanıtlanmış CDH1 gen mutasyonu olan ve ailesinde HDGC için total gastrektomi geçiren bir erkek kardeşin öyküsü olan asemptomatik 24 yaşında bir erkek hasta seçildi. Preoperatif endoskopide herhangi bir bulguya rastlanmadı. Dava, teknikleri ve temel yönlerinin tuzaklarını tartışmak için bir platform olarak kullanılıyor. Bu, protokolde tarif edildiği gibi hasta konumlandırma ve port yerleştirme, posterior vagus koruyucu diseksiyon, dikişli özofag...
Açıklamalar
Yazarların ifşa edecek hiçbir şeyi yok.
Teşekkürler
Yazarlar, dergi yayın ücretlerini finanse ettiği için Üst Gastrointestinal ve Metabolik Araştırma Vakfı'na teşekkür eder. Yazarlar ayrıca bu durumda hastaya, kimliksizleştirilmiş bilgi ve görüntülerinin yayınlanmasına rıza gösterdiğini kabul eder.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Laparoscopic instruments | |||
| 5 mm optical entry port | Applied Medical | CFF03 | Kii Fios First entry access system. |
| Laparoscopic 5mm 0° camera | Olympus | ENDOEYE HD II | 5 mm, 0° |
| Laparoscopic needle holder | KARL STORZ | Laparoscopic needle holder | |
| Nasogastric tube | Cardinal Health | 8888264960E | 16Fr |
| Nathanson liver retractor | COOK Medical | NLRS-1001/ NLRS-1002 | Large/ Extra-large |
| Robotic instruments | |||
| 12 mm port | Intuitive Surgical | 470375 | |
| 8 mm port | Intuitive Surgical | 470380 | |
| 8 mm reducer | Intuitive Surgical | 470381 | |
| Da Vinci Xi/X Endoscope with Camera, 8 mm, 0° | Intuitive Surgical | 470026 | |
| Da Vinci Xi/X Endoscope with Camera, 8 mm, 30° | Intuitive Surgical | 470027 | |
| Force Bipolar 8 mm | Intuitive Surgical | 470405 | |
| Mega SutureCut Needle Driver | Intuitive Surgical | 470309 | |
| Monopolar hook diathermy | Intuitive Surgical | 470183 | |
| SureForm 60mm stapler | Intuitive Surgical | 480460 | |
| Tip-up fenetrated grasper 8 mm | Intuitive Surgical | 470347 | |
| Vessel Sealer Extend 8 mm | Intuitive Surgical | 480422 | |
| Stapler reloads | |||
| Seamguard buttress 60 mm | GORE | 1BSGXI60GB/12BSGXI60GB | |
| SureForm 60 mm green reload | Intuitive Surgical | 48360G | |
| SureForm 60 mm white reload | Intuitive Surgical | 48360W | |
| Sutures | |||
| 2-0 nonabsorbable barbed suture | Medtronic | VLOCN0644 | 23 cm V-Loc on a 26 mm ½ circle taper point needle |
| 3-0 absorbable barbed suture | Medtronic/ Ethicon (J&J) | VLOCM0644 | 23 cm V-Loc on a 26 mm ½ circle taper point needle (preferred), STRATAFIX (alternate). Catalogue number |
| 2-0 monocryl suture | Ethicon (J&J) | JJW3463 | Cut to 15 cm, taper point needle |
| 2-0 silk suture | Ethicon (J&J) | JJ423H | Cut to 15 cm, taper point needle |
| 1 PDS suture | Ethicon (J&J) | JJ75414 | Fascial closure |
| 3-0 monocryl suture | Ethicon (J&J) | JJY227H | Skin closure |
| Topical Skin Adhesive | Ethicon (J&J) | JJ79025 | Skin closure/ wound dressing |
| Specimen extraction | |||
| Alexis O-ring wound retractor | Applied Medical | C8402 | Medium. For specimen extraction |
| Handheld diathermy | Covidien/ Valleylab | VLE2515 | For specimen extraction |
Referanslar
- Gamble, L. A., Heller, T., Davis, J. L. Hereditary diffuse gastric cancer syndrome and the role of CDH1: A review. JAMA Surgery. 156 (4), 387-392 (2021).
- Shenoy, S. CDH1 (E-cadherin) mutation and gastric cancer: Genetics, molecular mechanisms and guidelines for management. Cancer Management and Research. 11, 10477-10486 (2019).
- Hansford, S., et al. Hereditary diffuse gastric cancer syndrome: CDH1 mutations and beyond. JAMA Oncology. 1 (1), 23-32 (2015).
- Friedman, M., et al. Surveillance endoscopy in the management of hereditary diffuse gastric cancer syndrome. Clincal Gastroenterology and Hepatology. 19 (1), 189-191 (2021).
- van der Post, R. S., et al. Hereditary diffuse gastric cancer: updated clinical guidelines with an emphasis on germline CDH1 mutation carriers. Journal of Medical Genetics. 52 (6), 361-374 (2015).
- Kaurah, P., et al. Hereditary diffuse gastric cancer: Cancer risk and the personal cost of preventive surgery. Familal Cancer. 18 (4), 429-438 (2019).
- Hejazi, R. A., Patil, H., McCallum, R. W. Dumping syndrome: Establishing criteria for diagnosis and identifying new etiolo gies. Digestive Diseases and Sciences. 55 (1), 117-123 (2010).
- Johnston, D. Operative mortality and postoperative morbidity of highly selective vagotomy. British Medical Journal. 4 (5996), 545-547 (1975).
- Nakauchi, M., et al. Robotic surgery for the upper gastrointestinal tract: Current status and future perspectives. Asian Journal of Endoscopic Surgery. 10 (4), 354-363 (2017).
- Frantzides, C. T., et al. Laparoscopic Roux-en-Y gastric bypass utilizing the triple stapling technique. Journal of the Society of Laparoendoscopic Surgeons. 10 (2), 176-179 (2006).
- Madan, A. K., Frantzides, C. T. Triple-stapling technique for jejunojejunostomy in laparoscopic gastric bypass. Archives of Surgery. 138 (9), 1029-1032 (2003).
- Forrester, J. D., et al. Surgery for hereditary diffuse gastric cancer: Long-term outcomes. Cancers. 14 (3), 728 (2022).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır