E. coli'den Rekombinant Protein Dolu Veziküllerin Optimize Edilmiş Üretimi ve Analizi
Bu Makalede
Özet
Bu protokol, hücre dışı membrana bağlı veziküller içinde paketlenmiş, tipik olarak çözünmeyen veya disülfür bağı içeren proteinler de dahil olmak üzere rekombinant proteinlerin bakteriyel üretimi için ayrıntılı bir yöntem açıklamaktadır. Bu, uygulamalı biyoteknoloji ve tıp da dahil olmak üzere çok yönlü bilimsel araştırma alanlarına uygulanma potansiyeline sahiptir.
Özet
E. coli'den membrana bağlı veziküllerde çoklu rekombinant proteinleri ihraç eden kısa bir peptit etiketi kullanan bu yenilikçi sistem, bakteriyel rekombinant protein ekspresyonu ile ilişkili bir dizi soruna etkili bir çözüm sunar. Bu rekombinant veziküller, bakterilerden başka türlü zorlu, toksik, çözünmez veya disülfür bağı içeren proteinlerin üretimini kolaylaştıran mikro bir ortamda proteinleri bölümlere ayırır. Vezikül çekirdekli peptid etiketinin yokluğunda tipik bakteri ekspresyonuna kıyasla protein verimi önemli ölçüde artar. Vezikül paketlenmiş proteinlerin salınması, kültür ortamından izolasyonu destekler ve uzun süreli aktif protein depolanmasına izin verir. Bu teknoloji, uygulamalı biyoteknolojiden keşif bilimi ve tıbbına kadar çeşitli uygulamalar için basitleştirilmiş aşağı akış işleme için vezikül paketlenmiş, fonksiyonel proteinlerin veriminin artmasına neden olur. Bu makalede ve ilgili videoda, rekombinant protein dolu vezikül üretimini en üst düzeye çıkarmak için metodolojideki önemli adımları vurgulayan yöntemin ayrıntılı bir protokolü sağlanmıştır.
Giriş
Gram-negatif bakteri E. coli , hem endüstriyel hem de akademik ölçekte rekombinant protein üretimi için çekici bir sistemdir. Sadece yüksek yoğunluklu partiler halinde kültüre uygun maliyetli ve basit olmakla kalmaz, aynı zamanda E. coli1'de fonksiyonel proteinlerin üretimini teşvik etmek için geniş bir reaktifler, suşlar, aletler ve promotörler spektrumu kurulmuştur. Ek olarak, sentetik biyoloji teknikleri şimdi tipik olarak çeviri sonrası modifikasyonların uygulanması ve karmaşık proteinlerin katlanması ile ilgili engellerin üstesinden gelmektedir2. Rekombinant proteinlerin kültür ortamına salgılanmasını hedefleme yeteneği, verimi artırmak ve üretim maliyetlerini azaltmak için caziptir. Kullanıcı tanımlı proteinlerin membran veziküllerine kontrollü bir şekilde paketlenmesi, uygulanan biyoteknoloji ve tıp endüstrilerinde ürün ve teknolojilerin geliştirilmesine yardımcı olur. Şimdiye kadar, E. coli 3'ten rekombinant proteinleri salgılamak için yaygın olarak uygulanabilir yöntemlerin eksikliği vardı.
Eastwood ve ark. yakın zamanda E. coli1'den rekombinant protein içeren veziküllerin üretilmesi ve izole edilmesi için peptid etiketleme tabanlı bir yöntem geliştirmiştir. Bu Vezikül Çekirdeklendirici peptit (VNp), hedef proteinin saflaştırılmasını ve depolanmasını basitleştirmek için tercih edilen rekombinant proteinin hedeflenebileceği hücre dışı bakteriyel membran veziküllerinin üretimine izin verir ve şişe kültürlerinin sallanmasından normalde izin verilenden önemli ölçüde daha yüksek verim sağlar. Şişe kültürünün litresi başına 3 g'a yakın rekombinant protein verimi bildirilmiştir ve VNp etiketinden yoksun eşdeğer proteinlerle elde edilenlerden >100 kat daha yüksek verim elde edilmiştir. Bu rekombinant protein bakımından zenginleştirilmiş veziküller, kültür ortamından hızla saflaştırılabilir ve konsantre edilebilir ve depolama için kararlı bir ortam sağlar. Bu teknoloji, E. coli rekombinant protein üretiminde büyük bir atılımı temsil etmektedir. Veziküller, toksik ve disülfür bağı içeren proteinleri çözünür ve fonksiyonel bir biçimde bölümlere ayırır ve uzun süreli depolama veya doğrudan işleme için vezikül paketli, fonksiyonel proteinlerin basit, verimli ve hızlı saflaştırılmasını destekler1.
Bu teknolojinin mevcut tekniklere göre sunduğu başlıca avantajlar şunlardır: (1) çeşitli boyutlara (1 kDa ila >100 kDa) ve protein türlerine uygulanabilirlik; (2) proteinler arası ve protein içi disülfür bağ oluşumunu kolaylaştırmak; (3) multiprotein komplekslerine uygulanabilir; (4) bir dizi promotör ve standart laboratuvar E. coli suşları ile kullanılabilir; (5) Normalde sadece fermantasyon kültürlerinde görülen sallanan şişelerden protein veriminin üretilmesi; proteinler ihraç edilir ve membrana bağlı veziküllere paketlenir (6) aktif çözünür proteinin depolanması için kararlı bir ortam sağlar; ve (7) çıkış yönündeki işlemeyi ve protein saflaştırmayı basitleştirir. Bu basit ve uygun maliyetli rekombinant protein aracının, biyoteknoloji ve tıp endüstrilerinin yanı sıra keşif bilimi üzerinde de olumlu bir etkisi olması muhtemeldir.
Burada, birkaç yıl içinde geliştirilen ayrıntılı bir protokol, VNp teknolojisi ile bakterilerden rekombinant protein dolu veziküller üretmek için en uygun koşulları açıklamaktadır. Bu sistemin pratikte örnek görüntüleri, üretim, saflaştırma ve konsantrasyonun farklı aşamalarında veziküllerin varlığının görselleştirilmesine izin veren bir floresan proteini eksprese edilerek gösterilmiştir. Son olarak, bakterilerden VNp füzyon içeren veziküllerin üretimini doğrulamak için canlı hücre görüntülemenin nasıl kullanılacağı konusunda rehberlik sağlanmaktadır.
Protokol
Üstlenilen bakteri çalışması, her bir suşun belirli biyogüvenlik tehlike seviyesine uygun yerel, ulusal ve uluslararası biyogüvenlik koruma yönetmeliklerini takip eder.
1. Farklı VNp'lerin seçimi
- VNp dizilerini tanımlayın.
NOT: Bu çalışma için, bugüne kadar incelenen proteinlerin maksimum verimi ve veziküler ihracatı ilesonuçlanan üç VNp dizisi 1 tanımlanmıştır: VNp2, VNp6 ve VNp15. Bazı VNp varyantlarının neden bazı proteinlerle diğerlerinden daha verimli performans gösterdiği şu anda açık değildir; bu nedenle, füzyonların her VNp varyantı (yani, VNp2, 6 veya 15) ile ilgilenilen yeni bir protein arasında üretilmesi önerilir.
VNp2: MDVFMKGLSKAKEGVVAAAEKTQGVAEA
AGKTKEGVL
VNp6: MDVFKKGFSIADEGVVGAVEKTDQGVTEA
AEKTKEGVM
VNp15: MDVFKKGFSIADEGVVGAVE
İlgilenilen proteinin farklı VNp amino terminal füzyonları ile ekspresyonuna izin veren plazmidler ticari olarak kullanıma sunulmuştur (bakınız Malzeme Tablosu). - Bu yapılardan birinde VNp için kodlayan cDNA'nın 3' ucuna ilgili geni yerleştirmek için bir klonlama stratejisi tasarlayın veya ilgili protein için kodlayan genin ilk ATG kodonunun sentezlenmiş VNp cDNA yukarı akışını entegre ederek mevcut bir plazmidi uyarlayın. Yöntemleri 1'de açıklandığı gibi kullanın.
- Toksik proteinler için, bastırılabilir bir ekspresyon promotörüne sahip bir vektör veya minimum indüklenmemiş ekspresyon gürültüsüne sahip bir promotor kullanın.
- VNp dizi etiketini füzyon proteininin amino terminalinde klonlayın. Afinite etiketlerinin, proteaz bölünme dizilerinin vb. ve ilgilenilen proteinin VNp etiketinin karboksil tarafında bulunduğundan emin olun. VNp'nin aşağı akış peptidinden, bir -G-G-S-G- polipeptit dizisinin iki veya üç tekrarı gibi esnek bir bağlayıcı bölge ile ayrılması önerilir (Şekil 1).
NOT: Hücre yüzeyini zayıflatan ve vezikül verimini azaltan peptidoglikanı hedeflemeyen bir antibiyotik seçimi ile plazmidler kullanın. Kanamisin ve kloramfenikol (bakınız Malzeme Tablosu) bu çalışmada kullanılan tercih edilen antibiyotiklerdi.
2. Bakteriyel hücre kültürü ve protein indüksiyonu
NOT: Bu protokolde tipik olarak kullanılan bakteri suşları Escherichia coli BL21 (DE3) veya W3110'dur. E. coli hücreleri, lizojen suyu (LB) (10 g / L tripton; 10 g / L NaCl; 5 g / L maya ekstresi) veya müthiş et suyu (TB) (12 g / L tripton; 24 g / L maya ekstresi; 4 mL / L% 10 gliserol; 17 mM KH2PO 4; 72 mM K2HPO4, ayrı ayrı otoklavlanmış tuzlar) ortamında kültürlenir (bkz. Protein indüksiyonunun her adımını ve ardından izolasyon ve saflaştırma işlemini gösteren örnek görüntüler Şekil 2'de gösterilmiştir.
- Kültür 5 mL LB, 37 ° C'deki taze bakteri dönüşümlerinden doygunluğa kadar başlatır ve bunları 500 mL'lik bir konik şişede 25 mL TB'yi aşılamak için kullanır, hepsi de uygun antibiyotik seçimi ile.
- Yüzey alanı: hacim oranı, bu sistemin optimize edilmesinde önemli bir faktördür. Mümkün olduğunca büyük hacimli bir şişe kullanın (örneğin; 1 L kültür içeren 5 L şişe; optimizasyon çalışmaları için 500 mL'lik bir şişede 25 mL ortam kullanın).
- Daha büyük sallama şişesi kültürlerini 37 ° C'de bir inkübatörde inkübe edin ve 0.8-1.0'lık 600 nm optik yoğunluk değerine (OD 600) ulaşılana kadar200 rpm'de (≥25 mm yörünge atışı) sallayın.
NOT: Vezikülasyon, hücreler 37 ° C'de büyütüldüğünde en uygunudur. Bununla birlikte, bazı rekombinant proteinler daha düşük sıcaklıklarda ekspresyon gerektirir. İlgilenilen protein için durum buysa, VNp6 etiketi kullanılmalıdır, çünkü bu, 25 ° C'ye kadar olan sıcaklıklarda yüksek verimli vezikül ihracatına izin verir. - T7 promotöründen rekombinant protein ekspresyonunu indüklemek için, 20 μg / mL'ye (84 μM) kadar bir nihai konsantrasyona izopropil β-D-1-tiogalaktopiranosid (IPTG) ekleyin (bakınız Malzeme Tablosu). Rekombinant protein ekspresyonunun indüksiyonu, veziküllerin üretimi için geç log fazında (yani, 0.8-1.0'ın tipik OD600'ü ) gerçekleşmelidir.
NOT: İndüksiyon periyodunun uzunluğu proteinler arasında farklılık gösterebilir, bazıları 4 saatte ve diğerleri bir gecede (18 saat) maksimum üretime ulaşır. Bugüne kadar, gecelik kültürlerde maksimum vezikül ihracatı elde edilmiştir.
3. Rekombinant vezikül izolasyonu
- Hücreleri 20 dakika boyunca 3.000 x g'de (4 ° C) santrifüjleme ile pelet yapın.
- Vezikül içeren ortamları uzun süreli depolama amacıyla sterilize etmek için, temizlenmiş kültür ortamını steril ve deterjansız 0,45 μm polietersülfon (PES) filtreden geçirin ( bkz.
NOT: Canlı hücrelerin vezikül içeren filtrattan dışlanmasını test etmek için, LB agar üzerine plakalayın ve gece boyunca 37 ° C'de inkübe edin. - Vezikülleri daha küçük bir hacimde konsantre etmek için, steril vezikül içeren ortamı steril ve deterjansız 0,1 μm karışık selüloz esterleri (MCE) filtresinden geçirin (bkz.
- Vezikülleri membrandan dikkatlice çıkarmak için membranı bir hücre kazıyıcı veya plastik yayıcı kullanarak 0,5-1 mL steril PBS ile nazikçe yıkayın. Taze bir mikrofüj tüpüne aktarın.
NOT: Saflaştırılmış veziküller steril ortamda veya fosfat tamponlu salin (PBS) içinde 4 °C'de saklanabilir. Bu veziküllerde 6 ay boyunca saklanan rekombinant proteinlerin örnekleri vardır, bu şekilde enzimatik aktivitede kayıp olmaz.
4. İzole veziküllerden çözünür protein salınımı
- Protein içeren veziküller steril ortama / tampona izole edildikten sonra, veziküler lipit membranlarını cihaz için uygun bir program kullanarak sonikasyona maruz bırakın (örneğin, 6x 20 s açma ve kapama döngüleri) ve vezikül kalıntılarını gidermek için 20 dakika boyunca 39.000 x g'de (4 ° C) santrifüj.
NOT: Ozmotik şok veya deterjan işlemi, vezikülleri açmak için alternatif olarak kullanılabilir, ancak protein işlevselliği ve / veya aşağı akış uygulaması üzerindeki etkiye dikkat edilmelidir. - VNp füzyonu sitozolik kalırsa ve ortama salınmazsa, proteini standart protokoller kullanarak izole edin (örneğin, hücre peletlerini uygun bir ekstraksiyon tamponunun 5 mL'sinde (20 mM tris, 500 mM NaCl) yeniden askıya alın, sonikat yapın ve santrifüjleme ile hücre kalıntılarını çıkarın).
5. Protein konsantrasyonu tayini
- Üçlü numunelerin jel dansitometri analizi ile proteinlerin konsantrasyonunu belirleme1. Coomassie boyalı sodyum dodesil-sülfat poliakrilamid jel elektroforezi (SDS-PAGE) jelleri üzerinde sığır serum albümini (BSA) yükleme standartlarıyla birlikte çalıştırın. Uygun yazılımı kullanarak jelleri tarayın ve analiz edin (örneğin, Resim J; bkz.
6. Vezikül oluşumunun ve izole veziküllerin floresan mikroskobu ile görselleştirilmesi
NOT: Hücreler floresan olarak etiketlenmiş VNp füzyonu veya membran belirteçleri içeriyorsa, vezikül oluşumunu takip etmek için canlı hücre görüntüleme kullanılabilir. Alternatif olarak, floresan lipit boyaları, üretimi ve saflaştırmayı doğrulamak için vezikülleri görselleştirmek için kullanılabilir.
- Hücre montajı
- Kapak kapağına monte etmeden önce birkaç saat boyunca VNp füzyon ifadesini indükleyin.
- Agaroz ped yöntemi (Şekil 3A-C): Hücreleri, temiz bir cam slayt oluşturmasına ve ayarlamasına izin verilen ince (<1 mm), dairesel LB-agaroz (% 2) bir ped üzerine pipetleyin. Hücrelerin yerleşmesine ve dengelenmesine izin verin ve pedin ve hücrelerin üzerine 50 mm x 25 mm'lik bir örtü kayması yerleştirin. Kapak kapağını ara parçalar ve yapışkan bantla yerinde tutun.
- Polietilenimin (PEI) yöntemi (Şekil 3D-F): 20 μL% 0.05 PEI (dH2O cinsinden) pipet ucu ile bir kapak kapağına yayın ve kurumasına izin vermeden cama bağlanması için 3-5 dakika bekletin. 50 μL hücre kültürü ekleyin ve bakterilerin PEI kaplı yüzey4 ile ilişkili olduğundan emin olmak için 5-10 dakika bekletin. Kapak kapağını slayta yerleştirmeden önce 100 μL ortam ile yıkayın ve ara parçalar ve yapışkan bantla yerinde tutun.
- Montaj vezikülleri
- Pipet saflaştırılmış veziküller, temiz bir cam slayt oluşturmasına ve ayarlanmasına izin verilen ince (<1 mm), dairesel LB-agaroz (% 2) bir ped üzerine saflaştırılmıştır. Sıvı kuruduktan sonra, pedin ve veziküllerin üzerine 50 mm x 25 mm'lik bir kapak kayması yerleştirin. Kapak kapağını ara parçalar ve yapışkan bantla yerinde tutun.
- Floresan lipit boyası FM4-64, membranları5 ile boyayabilir ve bu nedenle vezikülleri görselleştirmek için kullanılabilir. FM4-64'ü saflaştırılmış veziküllere 2 μM'lik son konsantrasyonda (dimetil sülfoksit [DMSO] içinde çözünmüş 2 mM'lik bir stoktan) ve 10 dakikalık bir inkübasyondan sonra görüntü ekleyin. Bu, özellikle floresan olarak etiketlenmemiş yükler içeren vezikülleri tanımlamak için kullanışlıdır5.
- Kapakları, gözlemlenen hücreleri kültürlemek için kullanılan aynı ortamla durulayın.
NOT: Bazı karmaşık ortamlar (örneğin, TB) otofloresan sergileyebilir ve bu da aşırı arka plan sinyaline neden olabilir.
- Görüntüleme vezikülleri
NOT: VNp rekombinant veziküllerinin örnek mikroskopi görüntüleri Şekil 4'te görülebilir.- Sürgüyü bir yağ daldırma hedefi kullanarak ters çevrilmiş bir mikroskopa (bakınız Malzeme Tablosu) monte edin ve numunenin yerleşmesini ve sıcaklığın dengelenmesini sağlamak için 2-3 dakika bekletin.
NOT: Her numune için tüm canlı hücre görüntülemeleri, fototoksisitenin ve anaerobik stresin etkisini en aza indirmek için hücrelerin kapaklara monte edilmesinden sonraki 30 dakika içinde tamamlanmalıdır. Bu nedenle z-stack'lere göre tek düzlemli görüntüler tercih edilir. - Uygun ışık kaynaklarını kullanın (örneğin, ışık yayan diyot [LED] veya halojen ampul; bakınız Malzemeler Tablosu) ve kullanılan floresan protein(ler)/boya(lar)ı için filtre kombinasyonları6.
- Mikrobiyal hücreleri ve vezikülleri görüntülemek için yüksek büyütme (yani 100x veya 150x) ve yüksek sayısal diyafram açıklığına (yani, NA ≥1.4) lens kullanın.
- Hücrelerden ve / veya veziküllerden gelen floresan sinyallerini görselleştirmek için gereken minimum ışık yoğunluğunu belirleyin. Bu, kullanılan fotoğraf makinesi için pozlama ve kazanç ayarlarının bazı ayarlarının yapılmasını gerektirebilir.
NOT: Mevcut tamamlayıcı metal oksit yarı iletken (CMOS) kameralardan tipik pozlama süreleri, görüntüleme sistemine bağlı olarak 50-200 ms arasında değişmektedir. - Tek kareli görüntülerde, donanıma bağımlı rastgele arka plan gürültüsünü azaltmak için üç görüntü ortalaması kullanın.
- Hızlandırılmış görüntüleme için, tek tek kareler arasında 3-5 dakika bekleyin.
NOT: Mikroskop kurulumuna bağlı olarak, odağın daha uzun hızlandırılmış deneyler boyunca aralıklı olarak ayarlanması gerekebilir.
- Sürgüyü bir yağ daldırma hedefi kullanarak ters çevrilmiş bir mikroskopa (bakınız Malzeme Tablosu) monte edin ve numunenin yerleşmesini ve sıcaklığın dengelenmesini sağlamak için 2-3 dakika bekletin.
Temsili Sonuçlar
VNp6-mNeongreen ekspresyon yapısını içeren BL21 DE3 E. coli, geç log fazına kadar büyütüldü (Şekil 2A). VNp6-mNeongreen ekspresyonu, kültüre IPTG'nin eklenmesiyle (20 μg / mL veya 84 μM nihai konsantrasyon) indüklendi ve daha sonra kuvvetli sallanma (200 rpm, ≥25 mm yörünge atışı) ile 37 ° C'de gece boyunca büyümeye bırakıldı. Ertesi sabah, kültür, bakteri hücrelerinin santrifüjleme ile uzaklaştırılmasından sonra ortamda görünür kalan mNeongreen floresan7'yi (Şekil 2B) gösterdi (Şekil 2C). VNp-mNeongreen'in kültür ve temizlenmiş kültür medyasındaki varlığı SDS-PAGE tarafından doğrulanmıştır (Şekil 2D). mNeongreen içeren veziküller 0.1 μm MCE filtresi üzerine izole edildi (Şekil 2E) ve PBS'de yeniden askıya alındı (Şekil 2F). Saflaştırılmış veziküller daha sonra bir agaroz pedi üzerine monte edildi (Şekil 3A-C) ve geniş alan floresan mikroskobu kullanılarak görüntülendi (Şekil 4A). Vezikül membranlarının varlığı lipofilik floresan boya FM4-64 kullanılarak doğrulandı (Şekil 4B). mNeongreen (yeşil) ve VNp6-mCherry2 (macenta)8 ile kaynaşmış iç membran proteini CydB'yi eksprese eden E. coli hücreleri, canlı bakteri hücrelerinde vezikül üretimi ve kargo yerleştirme göstermektedir (Şekil 4C). Şekil 4A,B, geniş alan floresan mikroskobu kullanılarak yakalanırken, Şekil 4C, daha önce 9,10'da açıklanan yöntemler kullanılarak yapılandırılmış aydınlatma mikroskobu (SIM) kullanılarak elde edilmiştir.
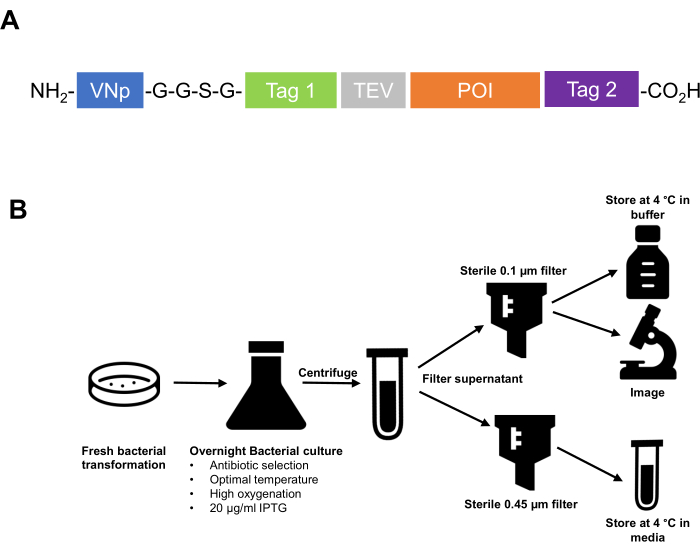
Şekil 1: Bir klonlama stratejisinin tasarlanmasından hücre dışı veziküllerin saflaştırılmasına ve depolanmasına kadar VNp teknolojisinin özeti. (A) Tipik bir VNp füzyon proteininin şeması. NH2 terminusunda VNp, ardından esnek bir bağlayıcı ve afinite ve floresan etiketlerinin uygun bir kombinasyonu (Tag1, Tag 2, proteaz bölünme bölgesi [örneğin, TEV]) ve ilgilenilen protein. (B) E. coli'den rekombinant protein dolu membran veziküllerinin ekspresyonu ve saflaştırılması için protokolü özetleyen şematik diyagram. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
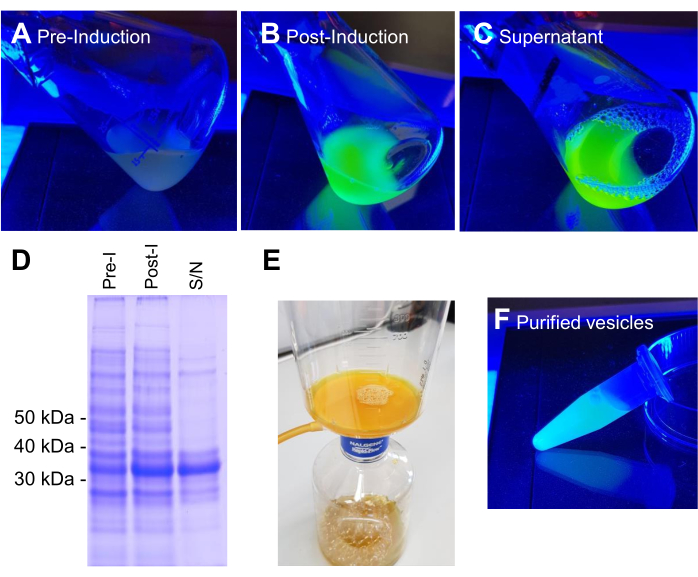
Şekil 2: VNp6-mNg veziküllerinin üretim ve saflaştırma aşamaları. VNp-mNeongreen ekspresyonunu içeren E. coli hücrelerinin kültürleri, füzyon proteininin IPTG kaynaklı ekspresyonundan önce (A) veya sonra (B) mavi ışıkta oluşur. (B)'den gelen hücreler santrifüjleme ile uzaklaştırıldı ve ortamdaki (C) VNp-mNeongreen dolu veziküller bırakıldı. (D) A, B ve C'den alınan eşdeğer örnekler SDS-PAGE ve coomassie boyama ile analiz edildi. Veziküller 0.1 μm'lik bir filtre (E) üzerinde izole edildi ve daha sonra uygun bir tampon hacmine (F) yıkandı. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
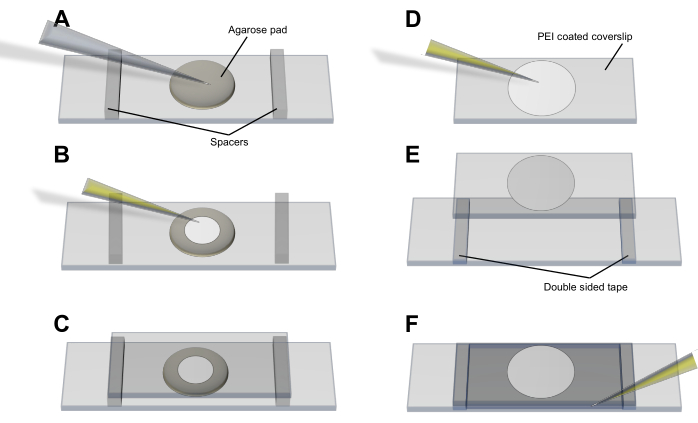
Şekil 3: Veziküllerin ve vezikül üretiminin görüntülenmesi için hücre montaj prosedürü. (A-C) Agaroz pedi yöntemi ve (D-F) E. coli hücrelerini kapak kaymasına monte etmek için PEI yöntemi. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
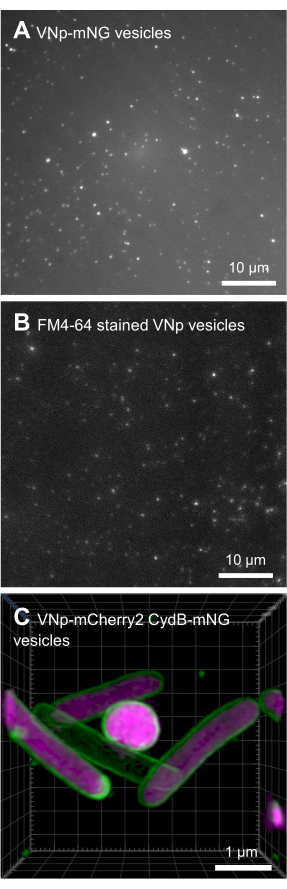
Şekil 4: VNp rekombinant veziküllerinin mikroskopi görüntüleri. Bir agaroz pedi üzerine monte edilmiş VNp6-mNeongreen içeren veziküllerin farklı alanlarından gelen yeşil (A) ve kırmızı (B) emisyon görüntüleri. (C) mNeongreen (yeşil) ve VNp6-mCherry2 (macenta) ile kaynaşmış iç zar proteini CydB'yi eksprese eden E. coli hücrelerinin görüntülenmesi, canlı bakteri hücrelerinde vezikül üretimini ve kargo yerleştirmeyi gösterir. (A,B) geniş alan floresan mikroskobu kullanılarak görüntülenirken, (C) yapılandırılmış aydınlatma mikroskobu (SIM) kullanılarak elde edildi. Ölçek çubukları: (A,B) = 10 μm; (C) = 1 μm. Bu şeklin daha büyük bir versiyonunu görmek için lütfen buraya tıklayın.
Tartışmalar
Yukarıda tarif edilen rekombinant proteinlerin üretimi için amino-terminal peptid etiketli yöntem, verimli bir şekilde izole edilebilen ve / veya aylarca saklanabilen büyük miktarlarda protein veren basit bir işlemdir.
Bu sistemin optimum kullanımı için gerekli olan protokoldeki temel adımları vurgulamak önemlidir. İlk olarak, VNp etiketi1 , N-terminus'ta bulunmalı, ardından ilgilenilen protein ve uygun etiketler bulunmalıdır. Ampisilin gibi peptidoglikan tabakasını hedef alan antibiyotiklerin kullanılmasından kaçınmak da önemlidir.
Büyüme koşulları açısından, vezikül üretimini en üst düzeye çıkarmak için zengin medya (örneğin, LB veya TB ortamı) ve yüksek bir yüzey alanı: hacim oranı gereklidir. Hücre dışı veziküllerin üretimi için en uygun sıcaklık 37 ° C'dir, ancak ilgilenilen proteinin ekspresyonu için tipik olarak gerekli koşullar da dikkate alınmalıdır. Daha düşük indüksiyon sıcaklıkları için VNp6 kullanılmalıdır. En önemlisi, T7 promotörünün indüksiyonu, hücreler 0.8-1.0'lık bir OD600'e ulaştığında 20 μg / mL (84 μM) IPTG'den daha büyük olmayan bir şekilde gerçekleştirilmelidir. Sistem kullanılarak eksprese edilen proteinler, 4 saatte veya gece boyunca indüksiyondan sonra maksimum vezikül üretimine ulaşır.
Bu protokolün basitliğine rağmen, optimizasyon gerektirir. VNp varyantı füzyonu, ekspresyon sıcaklıkları ve indüksiyon zaman periyotları, ilgilenilen proteine bağlı olarak farklılık gösterebilir. Ayrıca, ortamdan hücre dışı veziküllerin saflaştırılmasını ve müteakip konsantrasyonunu optimize etmeye ihtiyaç vardır. Geçerli yordam ölçeklenebilir değildir ve zaman alıcı olabilir. Bunlar bu metodolojinin sınırlamalarıdır.
VNp teknolojisinin geleneksel yöntemlere göre birçok avantajı vardır2. Çeşitli proteinlerin veziküler ihracatına izin verir, bugüne kadar başarıyla ifade edilen maksimum boyut, dahili kalan veziküller için 175 kDa ve ihraç edilenler için 85 kDa'dır. Ayrıca, bu teknoloji bir dizi fiziksel özellik ve aktiviteye sahip rekombinant proteinlerin verimini önemli ölçüde artırabilir. İlgili proteini içeren ihraç edilen veziküller, önceden temizlenmiş ortamdan basit filtreleme ile izole edilebilir ve daha sonra steril kültür ortamında veya tamponda, birkaç ay boyunca 4 ° C'de saklanabilir.
Bu sistemin uygulamaları, keşif biliminden uygulamalı biyoteknoloji ve tıbba (örneğin, fonksiyonel terapötiklerin üretimi yoluyla) kadar çeşitlidir3. Üretim kolaylığı, çıkış yönündeki işleme ve yüksek verim, bu alanlarda ve özellikle endüstride çekici niteliklerdir.
Açıklamalar
Yazarlar rakip finansal çıkarlar veya diğer çıkar çatışmaları olmadığını beyan ederler.
Teşekkürler
Yazarlar, VNp teknolojisini açıklayan makalede sunulan protokol hakkında sorular soran çeşitli Twitter kullanıcılarına teşekkür ediyor. Şekil 1A , flaticon.com'daki simgeler kullanılarak oluşturulmuştur. Bu çalışma Kent Üniversitesi tarafından desteklenmiş ve Biyoteknoloji ve Biyolojik Bilimler Araştırma Konseyi (BB / T008/768/1 ve BB / S005544/1) tarafından finanse edilmiştir.
Malzemeler
| Name | Company | Catalog Number | Comments |
| Ampicillin | Melford | 69-52-3 | |
| Chloramphenicol | Acros Organics (Thermofisher Scientific) | 56-75-7 | |
| E. coli BL21 (DE3) | Lab Stock | N/A | |
| E. coli DH10β | Lab Stock | N/A | |
| Filters for microscope | Chroma | ||
| FM4-64 | Molecular Probes (Invitrogen) | T-3166 | Dissolved in DMSO, stock concentration 2 mM |
| ImageJ | Open Source | Downloaded from: https://imagej.net/ij/index.html | |
| Inverted microscope | Olympus | ||
| Isopropyl β-D-1-thiogalactopyranoside (IPTG) | Melford | 367-93-1 | |
| Kanamycin sulphate | Gibco (Thermofisher Scientific) | 11815-024 | |
| LED light source for micrscope | Cairn Research Ltd | ||
| Lysogeny Broth (LB) / LB agar | Lab Stock | N/A | 10 g/L Tryptone; 10 g/L NaCl; 5 g/L Yeast Extract (1.5 g/L agar) |
| Metamorph imaging software | Molecular Devices | ||
| MF-Millipore Membrane filter (0.1 µm, MCE) | Merck | VCWP04700 | |
| Millipore Express PLUS membrane filter (0.45 µm, PES) | Merck | HPWP04700 | |
| Phosphate buffered saline (PBS) | Lab Stock | N/A | |
| Plasmids allowing expression of protein of interest with different VNp amino terminal fusions | Addgene | https://www.addgene.org/Dan_Mulvihill/ | |
| Terrific Broth (TB) | Lab Stock | N/A | 12 g/L Tryptone; 24 g/L Yeast Extract; 4 ml/L 10% glycerol; 17 mM KH2PO4 72 mM K2HPO4 |
Referanslar
- Eastwood, T. A., et al. High-yield vesicle-packaged recombinant protein production from E. coli. Cell Reports Methods. 3 (2), 100396 (2023).
- Makino, T., Skretas, G., Georgiou, G. Strain engineering for improved expression of recombinant proteins in bacteria. Microbial Cell Factories. 10, 32 (2011).
- Peng, C., et al. Factors influencing recombinant protein secretion efficiency in gram-positive bacteria: Signal peptide and beyond. Frontiers in Bioengineering and Biotechnology. 7, 139 (2019).
- Lewis, K., Klibanov, A. M. Surpassing nature: rational design of sterile-surface materials. Trends in Biotechnology. 23 (7), 343-348 (2005).
- Betz, W. J., Mao, F., Smith, C. B. Imaging exocytosis and endocytosis. Current Opinion in Neurobiology. 6 (3), 365-371 (1996).
- Mulvihill, D. P. Live cell imaging in fission yeast. Cold Spring Harbor Protocols. 2017 (10), (2017).
- Shaner, N. C., et al. A bright monomeric green fluorescent protein derived from Branchiostoma lanceolatum. Nature Methods. 10 (5), 407-409 (2013).
- Shen, Y., Chen, Y., Wu, J., Shaner, N. C., Campbell, R. E. Engineering of mCherry variants with long Stokes shift, red-shifted fluorescence, and low cytotoxicity. PloS One. 12 (2), e0171257 (2017).
- Periz, J., et al. A highly dynamic F-actin network regulates transport and recycling of micronemes in Toxoplasma gondii vacuoles. Nature Communications. 10 (1), 4183 (2019).
- Qiu, H., et al. Uniform patchy and hollow rectangular platelet micelles from crystallizable polymer blends. Science. 352 (6286), 697-701 (2016).
Yeniden Basımlar ve İzinler
Bu JoVE makalesinin metnini veya resimlerini yeniden kullanma izni talebi
Izin talebiThis article has been published
Video Coming Soon
JoVE Hakkında
Telif Hakkı © 2020 MyJove Corporation. Tüm hakları saklıdır