Method Article
تجميد التساهمية من البروتينات للتحليل الطيفي قوة جزيء واحد
* These authors contributed equally
In This Article
Summary
يصف هذا البروتوكول تجميد التساهمية من البروتينات مع سيلاني هيتيروبيفونكشونال اقتران وكيل للأسطح أكسيد السيليكون مصممة للتحليل الطيفي قوة جزيء واحد مجهرية على أساس القوة الذرية الذي يتجلى تفاعل ررجا (تلميح الهياكل-1 أدهيسين من الرئوية س) مع فيبرونيكتين.
Abstract
في السنوات الأخيرة، إلى مجهر القوة الذرية (AFM) جزيء واحد قوة التحليل الطيفي (SMFS) توسيع فهمنا للخصائص الجزيئية ووظائفها. فإنه أتاح لنا الفرصة لاستكشاف تعدد الآليات الفيزيائية، مثلاً، كيف البكتيرية أدهيسينس ربط المستقبلات السطحية المضيف بمزيد من التفصيل. من بين عوامل أخرى، يتوقف نجاح تجارب SMFS على التثبيت الوظيفية وأصلي من الجزيئات الحيوية للفائدة على السطوح الصلبة ونصائح فؤاد. هنا، يمكننا وصف بروتوكول بسيط لاقتران التساهمية من البروتينات للأسطح السيليكون باستخدام سيلاني-شماعة-كاربوكسيلس والكيمياء N-hydroxysuccinimid/1-ethyl-3-(3-dimethyl-aminopropyl)carbodiimid (مؤسسة/دائرة الصحة الوطنية) راسخة في النظام لاستكشاف التفاعل بين الهياكل-1 أدهيسين ررجا من بكتيريا إيجابية العقدية الرئوية (س. نيمونيا) مع فيبرونيكتين البروتين المصفوفة خارج الخلية (الجبهة الوطنية). النتائج التي توصلنا إليها تظهر أن الروغان السطحية يؤدي إلى توزيع الجبهة الوطنية بصورة متجانسة على سطح الزجاج بتركيز مناسب من ررجا على طرف ناتئ فؤاد، الظاهر بقيمة تصل إلى 20 في المائة أحداث التفاعل أثناء SMFS الهدف القياسات وكشفت عن أن ررجا تربط بين الجبهة الوطنية بقوة يعني 52 pN. ويمكن تعديل البروتوكول للزوجين عن طريق مجموعات المواقع ثيول الحرة محددة. هذه النتائج في اتجاه بروتين أو جزيء المعرفة مسبقاً وهو مناسبة للتطبيقات الأخرى الفيزيائية الأحيائية إلى جانب SMFS.
Introduction
بجوار ملاقط الضوئية والمغناطيسية، قد برز كأداة مفيدة لتحليل ومعالجة جزيئات القوة الذرية المجهر (فؤاد)1،2 والتحقيق خصائص ووظائف، بما في ذلك الرد على قوة خارجية3 ،4. في المقابل إلى أساليب مثل مقايسة الممتز مرتبط الإنزيم (إليزا)، السطح الرنين مأكل مثل الطحين (موارد البرنامج الخاصة) أو كريستال الكوارتز ميكروبالانسي (QCM) الأجهزة، فؤاد يسمح لقياس التفاعلات في جزيء واحد (SMFS)5 والمستوي خلية مفردة (سكفس)6 . هذه التكنولوجيات أسفرت عن نظرة متعمقة في آليات ملزمة مثل السندات الصيد التي وجدت للتفاعل بين البروتين الهياكل كولاي فيمه مع يطلق7، أو جنبا إلى جنب β-الزمام ويكرر شكلتها الجبهة الوطنية ملزم البروتينات من المذهبة س. عند الربط إلى الجبهة الوطنية8. وقد تمكنا مؤخرا تبين أن أدهيسين الهياكل-1 ررجا9،10 من بكتيريا إيجابية العقدية الرئوية (س. نيمونيا)11 قادرة على ربط فيبرونيكتين12 مع أن هذين المجالين المحطة الطرفية. وكشف هذا عن إليه ملزمة المجال الثاني جديد الذي يختلف عن β-الزمام جنبا إلى جنب، وقد تمكن بنيوموكوكسي بيلياتيد لتشكيل والحفاظ على سطوح مضيف اتصال باحتواء فيبرونيكتين عابر13.
نجاح تجارب SMFS نقديا يعتمد على تجميد وظيفي وأصلي الجزيئات الحيوية على السطوح الصلبة ونصائح فؤاد. كما قد يحدث قوات عالية خلال قياسات SMFS، البروتينات ينبغي أن يفضل أن تساهمي يقترن إلى السطح. وهناك عدد كبير من أساليب مختلفة من اقتران للتثبيت من البروتينات وغيرها من الجزيئات الحيوية، فضلا عن الخلايا كلها على السطوح الصلبة (غير العضوية)، جسيمات نانو وغيرها من الأجهزة المذكورة في الأدب14،15 ،16،17،،من1819،20،21،،من2223،24، 25،،من2627. غالباً ما تجعل هذه البروتوكولات تستخدم المواد الخطرة، ويصعب تنفيذ و/أو تتطلب معدات خاصة (مثلاً، البلازما أنظف). طريقة بسيطة للزوجين جزيئات الزجاج إرفاق طبقة بوليمر أكثر سمكا من كروسلينكيرس هيتيروبيفونكشونال مع مجموعة سيلاني--رد الفعل على جانب واحد وجماعة أمين-القائم على رد الفعل على الجانب الآخر. اعتماداً على التطبيق، يمكن أن تشمل العوامل اقتران سلاسل الكربون المائية مرنة متغيرة الطول، على سبيل المثال-، بوليثيلينجليكول (الربط). قمع التفاعلات غير محدد الأسطح تم التعديل (مثلاً، الماء، والكهرباء والتفاعلات فإن-دير-فالس)، وقد توفر حرية جزيء يزوج التناوب.
وهنا، يمكننا وصف بروتوكول عام لاقتران التساهمية من البروتينات التي تحتوي على واحد أو أكثر من المجموعات الأمينية الحرة (-NH2) الزجاج السطوح ونصائح نيتريد السيليكون فؤاد عبر هيتيروبيفونكشونال اثوكسي سيلاني-شماعة-الكربوكسيل (-COOH). يمكن استخدام هذا البروتوكول في تجارب SMFS، الذي يتمثل استناداً إلى التفاعل بين ررجا والبروتين المصفوفة خارج الخلية الجبهة الوطنية (انظر الشكل 1 لمحة عامة).
والخطوة الأولى هي سيلانيزيشن السطحية28،،من2930،31. أنها تنطوي على التحلل المائي لمجموعات اثوكسي عامل اقتران بغية تشكيل مجموعات سيوح عالي التفاعل. وهذه يمكن أن تتفاعل مع مجموعات سيوح على الركازة. في تكثيف الأولية خطوة، هذه السندات الهيدروجين النموذج سيلانولس وانتشرت على الركازة. في رد فعل تكثيف ثانوي (الذي عادة ما يتطلب الحرارة أو فراغ لإزالة الماء)، شكلت سندات siloxane. هذه النتائج في طبقة سيلاني organo تساهمي مرفقة.
والخطوة الثانية هي اقتران البروتينات للوظيفية (-COOH) المجموعات التي تمتد من البوليمر32. أولاً، يتم تحويل الحامض إلى رد الفعل N-هيدروكسيسوكسينيميد (NHS) إستر وسيطة، المكتسبة من خلال دائرة الصحة الوطنية الراسخة/تنمية الصادرات (1-إيثيل-3-(3-ديميثيلامينوبروبيل) كاربودييميد الكيمياء33 ويخضع لتفاعلات الاستبدال وأخيراً تشكيل في سندات أميد مع الأمينات الأولية على البروتينات.
وبهذه الطريقة، كان ررجا بالإضافة إلى نصائح فؤاد نيتريد السيليكون والجبهة الوطنية البشرية إلى ركائز زجاجية في اتجاه عشوائي وحللت قواتهما التفاعل على مستوى جزيء واحد. وتظهر النتائج التي توصلنا إليها أن وصف الكيمياء السطحية يؤدي إلى توزيع الجبهة الوطنية بصورة متجانسة على سطح الزجاج بتركيز مناسب من ررجا على الحافة، الظاهر بقيمة تصل إلى 20 في المائة أحداث التفاعل من خلال قياسات SMFS الهدف. هذا الكيمياء يقلل التفاعلات الخلفية غير محددة، ويخضع للتغيير قليلاً أثناء الحصول على البيانات وبالتالي ممتاز يناسب دقة SMFS التجارب.
Protocol
1-تجميد من البروتينات عن طريق وكلاء اقتران Silane الوظيفية
ملاحظة: يعطي الشكل 1 نظرة عامة على الكيمياء السطحية المطبقة في هذا البروتوكول.
تنبيه: في البروتوكول التالي، تستخدم مواد كيميائية مختلفة قابلة للتآكل والجلد المهيجة خصائص. ارتداء قفازات (مقاومة للأحماض) كافية، ونظارات واقية، ومعطف المختبر والعمل تحت غطاء الدخان أثناء إعداد الحلول لتجنب استنشاق الأبخرة.
- الروغان من الأسطح الزجاجية وناتئ نيتريد السيليكون مع سيلاني اقتران وكلاء
- إزالة الغبار الخشنة وتقضي على التلوث من الشرائح الزجاجية مع الايزوبروبانول والدقة خالية من الوبر وقص الشرائح في الحجم المطلوب (اختياري).
ملاحظة: بجانب الزجاج، يمكن سطح صلب السيليكا والكوارتز وأكاسيد الألومنيوم والنحاس والقصدير، والتيتانيوم، الحديد، الكروم، الزركونيوم، النيكل والزنك.
تنبيه: قطع الشرائح الزجاجية قد يسبب حواف حادة. - مكان الزجاج الشرائح في جرة المصبوغة مملوءة بحامض الهيدروكلوريك (33% HCl) المخفف بالماء المقطر مضاعف (ddH2س) إلى 3-5% (v/v)، أغلق الجرة مع غطاء مناسباً ووضعه في حمام الموجات فوق الصوتية لمدة 90 دقيقة في درجة حرارة الغرفة.
ملاحظة: قد جرة تستخدم قطره 6 سم وحجم تقريبي لمل 65-70. حجم مناسب من HCl المخفف للجرة 50 مل يحتوي على 5 مل 33% HCl و 45 مل ddH2o. HCl فعال يزيل الأيونات المعدنية غير ملزم، خاصة الصوديوم والبوتاسيوم والكالسيوم ويقلل من السيليكون من أجل إنتاج سطح زجاج مشبعة هيدروكسيل.
تنبيه: HCl هو التآكل وتهيّج الجلد. ارتداء قفازات مقاومة للأحماض كافية، ونظارات واقية، ومختبر معطف وتعمل تحت غطاء الدخان أثناء إعداد الحل لتجنب استنشاق الأبخرة. - ضع نيتريد السيليكون فؤاد تعزية المسابير على شريحة زجاجية نظيفة مع تلميح تواجه صعودا ويتهددها البنفسجية الخفيفة من أعلاه لمدة 90 دقيقة على الأقل.
ملاحظة: للتحليل الطيفي قوة جزيء واحد، كانتيليفيرس مع ثابت ربيع اسمي من 0.01 إلى 0.1 N m-1 مناسبة. سيتم إزالة الملوثات العضوية، أساسا من الدهون المواد، تشعيع السطح ناتئ مع الأشعة فوق البنفسجية وجعله ماء على جانب واحد. إذا كان الجانب الآخر هو تلوثاً-التي ينبغي أن لا تكون القضية، أو إذا تم استخدام المسابير ناتئ جديدة خارج مربع الموردين-قد تؤثر على القياس SMFS. تنظيف شامل للرقاقة ناتئ كله باستخدام حل البيرانا، التي استخدمت في العديد من الدراسات34، قد يساعد.
تنبيه: الأشعة فوق البنفسجية الضارة على العينين؛ ولذلك، ينبغي أن تنفذ تشعيع المسابير ناتئ في دائرة ضوء كتيمة للأشعة فوق البنفسجية. البيرانا الحل هو شدة رد الفعل، وقد حرق الجلد والورق والمواد العضوية الأخرى. يجب عدم استخدام الحاويات البلاستيكية. إذا وضعت في الأطباق أو الجرار حتى مع كميات صغيرة من الملوثات السطحية العضوية (مثلاً، من الاستخدام السابقة)، يمكن الرد بسرعة. - استبدال استبدال حمض الهيدروكلوريك في جرة المصبوغة مع ddH2س دون السماح لسطح الزجاج الجاف ووضع الجرة إلى الوراء في الحمام بالموجات فوق الصوتية لآخر دقيقة 10 المياه اثنين مرات أكثر عن 10 دقيقة على التوالي ليغسل بشكل صحيح الهيدروكلوريك حمض.
- وفي الوقت نفسه، يحل حمض البولي إثيلين غليكول سيلاني اثوكسي (أو ميثوكس) (Si (2ح5OC)3-ربط-COOH) في خليط من الإيثانول و ddH2س (v/v 95%/5%، الأس الهيدروجيني 4.6 تعديلها مع حمض الخليك) إلى تركيز نهائي لمل 0.1 مغ -1. تخزين الحل مغلقة تجنبا للتبخر الإيثانول.
ملاحظة: عملاء اقتران Silane حساسة للرطوبة ودرجات الحرارة. ولذلك ينبغي تخزينها تحت غاز خامل (N2)، في درجة حرارة منخفضة (-20 درجة مئوية) وظروف الجفاف. قبل فتح قارورة، تأكد من أن silanes قد وصلت إلى درجة حرارة الغرفة للتقليل من الماء ومن ثم التخميل الجماعات المتفاعلة. ربط هيتيروبيفونكشونال وكلاء اقتران متوفرة مع العديد من المجموعات الوظيفية المختلفة ومباعدة مختلفة الأطوال. لتجميد عشوائية من البروتينات عن طريق يجب مجموعاتهم الأمينية الحرة (NH2)، كما هو موضح في هذا البروتوكول، مجموعة وظيفية إضافية إلى سيلاني اثوكسي/ميثوكس إستر دائرة الصحة الوطنية. إلى جانب شراء عامل سيلاني مع إستر دائرة الصحة الوطنية، طريقة بسيطة لكسب هذه إستر دائرة الصحة الوطنية لتنشيط مجموعة الكربوكسيل (-COOH) مع 1-ethyl-3-(3-dimethylaminopropyl) كاربودييميد (EDC) ودائرة الصحة الوطنية (انظر 1.2.1. و 1.2.2.).
تنبيه: هو الإيثانول القابلة للاشتعال، وتهيّج الجلد. حمض الخليك قابل للاشتعال والتآكل. الحرص على عدم الحصول على رد الفعل silanes على الجلد أو في العيون. ارتداء القفازات الملائمة، ونظارات واقية ومعطف المختبر والعمل تحت غطاء الدخان لتفادي استنشاق الأبخرة. - من أجل حل سيلاني في أطباق بتري منفصلة اثنين، وضع المسابر ناتئ استعداد والشرائح الزجاجية في طبق بتري واحد على التوالي، وختم مغلقة بأحكام (بارافيلممثلاً ) تجنب تبخر الإيثانول واحتضان ثابتة لمدة 90 دقيقة في درجة حرارة الغرفة.
ملاحظة: الحجم الأمثل لطبق بيتري يعتمد على عدد المجسات ناتئ وحجم الشرائح الزجاجية التي يجب أن فونكتيوناليزيد. حجم قطر لمعالجة جيدة وحجم الكاشف المنخفضة 50-60 مم. ينبغي أن تعقد لتجنب ثني غير مرغوب فيه ناتئ حين اختراق من خلال واجهة المياه الجوية ناتئ بزاوية 90 درجة إلى واجهة الهواء والماء. يمكن القيام اختيارياً الحضانة من الشرائح الزجاجية (ولكن ليس المسابير ناتئ) على شاكر مداري. - شطف الشرائح ناتئ والزجاج في قنينة متتالية الثلاثة التي تحتوي على الإيثانول النقي يغسل تماما أن المركبات سيلاني غير منضم.
ملاحظة: لتجنب الانحناء غير مرغوب فيها ناتئ حين اختراق من خلال واجهة المياه الجوية، ينبغي أن تعقد ناتئ بزاوية 90 درجة. - ضع الشرائح الزجاجية فونكتيوناليزيد في جرة المصبوغة وناتئ على شريحة زجاجية نظيفة وعلاج عند 110 درجة مئوية لمدة 30 دقيقة.
ملاحظة: علاج بالحرارة الحث على تشكيل روابط siloxane التساهمية والتخلص من المياه. كما كانت فونكتيوناليزيد الشرائح الزجاجية فقط على جانب واحد، تأكد من بشكل صحيح يشير إلى الجانب المغلفة. - تخزين العينات الزجاجية سيلانيزيد ويَسْبِر ناتئ في مجفف فراغ لمدة تصل إلى أسبوع واحد.
ملاحظة: يمكن أن يكون مؤقتاً البروتوكول هنا.
- إزالة الغبار الخشنة وتقضي على التلوث من الشرائح الزجاجية مع الايزوبروبانول والدقة خالية من الوبر وقص الشرائح في الحجم المطلوب (اختياري).
- تجميد عشوائية من البروتينات على ناتئ نيتريد السيليكون والزجاج سيلانيزيد
ملاحظة: لتجنب الانحناء غير مرغوب فيه ناتئ، المسبار ناتئ ينبغي أن تعقد بزاوية 90° حين اختراق أي واجهات الهواء والماء.- تعد الحل التي تحتوي على 42 mg مل-1 لتنمية الصادرات وملغ 20 مل-1 دائرة الصحة الوطنية في الفوسفات القياسية مخزنة المالحة (برنامج تلفزيوني؛ 137 مم كلوريد الصوديوم، 2.7 مم بوكل، 10 مم نا2هبو41.8 مم خ2ص4، درجة الحموضة 7.4).
تنبيه: تنمية الصادرات قابلة للتآكل، وتهيّج الجلد ويمكن أن تسبب أضرارا خطيرة في عينة. ارتداء القفازات الملائمة، ونظارات واقية ومعطف المختبر. - تغطي الشرائح الزجاجية سيلاني المغلفة مع الحل ووضع المسابر ناتئ سيلانيزيد قطره من الحل تنمية الصادرات/دائرة الصحة الوطنية واحتضان لمدة 10 دقائق في درجة حرارة الغرفة.
ملاحظة: للحضانة لتحقيقات ناتئ، مربع ناتئ الأصلي مناسبة. لزوجين البروتينات عن طريق هذه المجموعات الأمينية الحرة إلى كاربوكسيلس (-COOH) وكلاء شماعة silane هيتيروبيفونكشونال، يتم تنشيط المجموعة-COOH مع الكيمياء تنمية الصادرات/دائرة الصحة الوطنية المستخدمة على نطاق واسع. تنمية الصادرات الأزواج دائرة الصحة الوطنية لحمض الكربوكسيلية، تشكيل إستر الصحي "مستقر" الذي يتيح للتصريف الفعال للأمينات الأولية في الأس الهيدروجيني الفسيولوجي في خطوة تالية. - شطف الشرائح ناتئ والزجاج تماما مع برنامج تلفزيوني في الأكواب الثلاثة على التوالي كي يغسل تماما في تنمية الصادرات المفرطة/دائرة الصحة الوطنية.
ملاحظة: هذه الخطوة الغسيل الحرجة كمؤسسة/دائرة الصحة الوطنية المتبقية يمكن أن التشعب البروتينات ومما يغير وظيفة كل منها. - احتضان الشرائح الزجاج المنشط مع ويَسْبِر ناتئ في معالجة تجميعية للحل البروتين المطلوب في دائرة رطب في درجة حرارة الغرفة. وقت تركيز وحضانة البروتين ينبغي تكييفها لتلبية الاحتياجات للتجربة. وبصفة عامة، تجمع بين 0.5 إلى 1 مغ مل-1 والحضانة مرة من 30 دقيقة إلى 2 حاء مناسبة لمعظم البروتينات. وفي حالة فيبرونيكتين (على الشريحة الزجاجية) والبروتين نصيحة الهياكل-1 ررجا (على ناتئ) تركيز مولى 1.5 µM و 3 ميكرومتر، على التوالي، وفترة حضانة من ح 2 تكفي.
- يغسل الشرائح الزجاجية ويَسْبِر ناتئ دقة مع برنامج تلفزيوني في الأكواب الثلاثة على التوالي كي يغسل البروتينات غير منضم.
- تشبع إستر دائرة الصحة الوطنية المتبقية مع تريس (هيدروكسيميثيل)-أمينوميثان بوضع التحقيقات في تريس مخزنة المالحة (TBS؛ 50 مم تريس، 150 مم كلوريد الصوديوم، درجة الحموضة 7.6) لمدة 20 دقيقة في درجة حرارة الغرفة.
ملاحظة: هذه الخطوة يقلل من اقتران التساهمية غير مرغوب فيها من البروتينات بين سطح نصيحة فؤاد فونكتيوناليزيد والزجاج، لأنه يمكن ربط المجموعات الأمينية في تريس المجموعات COOH المنشط المتبقية على السطح ناتئ والركيزة. - يغسل الشرائح الزجاجية وناتئ تحقيقات شاملة مع برنامج تلفزيوني ومخزن لهم في أطباق بتري منفصلة المشمولة في برنامج تلفزيوني حتى الاستخدام.
ملاحظة: العينات ينبغي أن تعد طازجة واستخدامها في نفس اليوم.
- تعد الحل التي تحتوي على 42 mg مل-1 لتنمية الصادرات وملغ 20 مل-1 دائرة الصحة الوطنية في الفوسفات القياسية مخزنة المالحة (برنامج تلفزيوني؛ 137 مم كلوريد الصوديوم، 2.7 مم بوكل، 10 مم نا2هبو41.8 مم خ2ص4، درجة الحموضة 7.4).
2-مجهر القوة الذرية أساس جزيء واحد قوة التحليل الطيفي
ملاحظة: في هذا العمل، مجهر قوة ذرية من "الصكوك جبك" استخدمت والمجموعة يو بي إس للحصول على منحنيات القوة--المسافة وعرف مع "رامبديسيجنير القوة".
- معايرة ناتئ مع أسلوب الضوضاء الحرارية35
ملاحظة: لمعايرة ناتئ، اتبع الخطوة في دليل الشركة المصنعة. تعزية معظم الموردين الدولة قيمة ثابتة ربيع تقريبي الذي يحسب عادة من الشكل ناتئ الاسمية (الطول، العرض، وسمك) ومن ثم لا يمكن الاعتماد عليها كثيرا. كثابت الربيع الصحيح أمر حاسم، فمن المستحسن القيام بمعايرة ناتئ المبينة أدناه في ثلاث نسخ واستخدام القيم الوسطية للحساسية الضوئية رافعة وربيع دائم. يمكن أن تكون مفيدة لتسجيل انحراف ناتئ في فولت (V) أثناء التجربة وتحويل القوة (pN) وبعد ذلك استخدام حساسية رافعة الضوئية وربيع دائم يعني القيم. ويمكن تحديد حساسية رافعة ثابتة والبصرية الربيع قبل و/أو بعد التجربة، طالما لم يتغير موقف الليزر على ناتئ (يمكن تعديل موقف الليزر المنعكس على الضوئي).- إصلاح شريحة زجاجية نظيفة، جديدة على صاحب العينة فؤاد وتغطية ذلك مع المخزن المؤقت لبرنامج تلفزيوني.
ملاحظة: المعايرة ينبغي أن يتم على سطح صلب (مثلاً، الزجاج)، وفي نفس المخزن المؤقت كالتجارب الفعلية. - إصلاح المسبار ناتئ المعدة في حامل ناتئ ووضعه على رأسه فؤاد والرطب ناتئ مع قطره من المخزن المؤقت لبرنامج تلفزيوني بعناية.
ملاحظة: التبول ناتئ يقلل التوتر السطحي التي تظهر أثناء الإيلاج في المخزن المؤقت لبرنامج تلفزيوني على الشريحة الزجاجية المعايرة والانحناء وبالتالي غير مرغوب فيه ناتئ. - تتحرك ببطء ناتئ نحو السطح المعايرة حتى هي مغمورة ناتئ تماما في المخزن المؤقت لبرنامج تلفزيوني، لكنه لا يزال بعيداً عن السطح المعايرة.
- استخدام المجهر الضوئي عرض أعلى لفؤاد أو (إذا كان متوفراً) المجهر المقلوب تحت فؤاد بموقف الليزر لفؤاد على المؤخرة ناتئ. ضع الليزر بقعة قرب نهاية ناتئ قريبة حيث يوجد التلميح.
ملاحظة: بقعة ليزر ينبغي أن يقع بالقرب من نهاية ناتئ، ولكن لا يزال ينبغي تماما على ناتئ. في حالة توفر لا مجهر ضوئي، استخدم قطعة من الورق للثنائيات الليزر مرئية أو بطاقة ليزر كاشف للأشعة تحت الحمراء ليزر الثنائيات ووضعه تحت رأسه فؤاد وتتحرك بقعة ليزر نحو حافة رقاقة ناتئ، حيث توجد كانتيليفيرس ، حتى تشاهد الفور على الورق أو للكشف عن البطاقة. ثم حرك الليزر موازية إلى الحافة. عندما يختفي الفور، على ذراع ناتئ. ل cantilevers الخطي، تتحرك بقعة نهاية ذراع رافعة حتى يظهر على بطاقة ورق/كاشف والتحرك مرة أخرى حتى يتم مرة أخرى على ذراع رافعة (يختفي من الورق/البطاقة). للثلاثي، وضع الفور في الوسط بين اثنين من الأسلحة ناتئ وتحريكه صوب نهاية ناتئ، حتى يختفي من الورق/البطاقة. تحقق من أن كنت في منتصف ناتئ بتحريك خط عمودي بقعة المحور الطويل ناتئ. - ضبط موضع الضوئي للكشف عن أربع رباعي لفؤاد في مثل هذه طريقة أن يتم وضع شعاع الليزر المنعكس في مركز الضوئي.
ملاحظة: المضي قدما على النحو التالي: استخدام مسامير ميكرومتر قرب صمام ثنائي كاشف للتحرك صمام ثنائي في أفقي وفي الاتجاه العمودي، حتى يتم تكبير إشارة مبلغ من جميع الأرباع الأربعة. ثم نقل صمام ثنائي في الاتجاه الرأسي، حتى إشارة الانحراف الرأسي هو صفر، ونقل صمام ثنائي في الاتجاه الأفقي، حتى إشارة الانحراف الأفقي هو صفر. Cantilevers نيتريد السيليكون عادة لها طلاء الذهب، وهي بالتالي ترمومترات مع اثنين من معاملات مختلفة للتمدد الحراري. هذا يؤدي انجراف حرارية (ظاهر في إشارة الانحراف الرأسي) خاصة في حل. لتقليل هذا الانجراف خلال قياسات، السماح للنظام بأكمله حجته لبضع دقائق قبل بدء المعايرة. - فتح إدارة المعايرة في البرنامج فؤاد ومعايرة حساسية ناتئ وربيع ثابت ناتئ مع أسلوب الضوضاء الحرارية كما يلي.
- نهج على سطح الركازة وتسجيل منحنى قوة--مسافة بعناية.
- تحديد حساسية رافعة البصرية في شمال البحر الأبيض المتوسط/V بتركيب خط مستقيم إلى الجزء أشد من منحنى القوة تراجع، حيث التلميح على اتصال بسطح الركيزة. الحساسية التي تمكن من تحويل ثابت ربيع ناتئ للسندات الإذنية/nm.
ملاحظة: هو ميل المنحنى تراجع بيزو السفر المسافة مقابل. التغير في الجهد الكهربي الضوئي (يتم قياسها في شمال البحر الأبيض المتوسط/V). - تسجيل عدة أطياف الضوضاء الحرارية ناتئ مع مكم ناتئ ما يقرب من 100 أو أكثر بعيداً عن السطح من أجل استبعاد أي التخميد السطحية.
- تحديد ثابت الربيع من ناتئ في السندات الإذنية/V بتقريب مذبذب التوافقي يقدمها البرنامج فؤاد إلى الأطياف الضوضاء الحرارية.
- ببطء تتراجع ناتئ وسحبها من الحل.
- بديل سطح الزجاج المستخدمة لمعايرة ناتئ مع سطح العينة التي تحتوي على بروتينات المعطل تداولها. تأكد من أن ناتئ وسطح العينة (وبالتالي البروتينات) لم تجف أثناء تغيير الشرائح الزجاجية.
- إصلاح شريحة زجاجية نظيفة، جديدة على صاحب العينة فؤاد وتغطية ذلك مع المخزن المؤقت لبرنامج تلفزيوني.
- قوة التفاعل تجارب على مستوى البروتين وحيد
- تتحرك ببطء ناتئ رطبة نحو سطح العينة حتى تغطي تماما ناتئ من المخزن المؤقت لبرنامج تلفزيوني ولكن لا يزال بعيداً عن سطح الركيزة.
ملاحظة: إلى تقليل الانجراف الحرارية خلال التجربة، اسمحوا النظام بأكمله لبضع دقائق قبل البدء في القياسات الطيفي القوة. - الاقتراب من السطح وتسجيل عدة منحنيات القوة--المسافة (≥ 500) في مواقع مختلفة من سطح العينة، مع قوة اتصال من 250 pN، وقت اتصال من 1 s وطول تراجع من 2 ميكرومتر وسرعة تراجع 1 ميكرومتر s-1.
ملاحظة: التعديلات التحليل الطيفي بالقوة العامة، اتبع الدليل الخاص بالشركة المصنعة. الاختلافات: سرعة تراجع يمكن أن تختلف بين 0.1 و 5 ميكرومتر s-1 لحساب البيانات كينيتيكال استناداً إلى تحميل القوة المتزايدة. يمكن أن تختلف الوقت التفاعل لتحليل تعزيز السندات تعتمد الوقت. بدلاً من الاحتفاظ بسرعة تراجع مستمر، واحد قد تبقى ثابت القوة (قوة المشبك الوضع).
- تتحرك ببطء ناتئ رطبة نحو سطح العينة حتى تغطي تماما ناتئ من المخزن المؤقت لبرنامج تلفزيوني ولكن لا يزال بعيداً عن سطح الركيزة.
- تحليل البيانات
ملاحظة: تم تحليل البيانات باستخدام برامج معالجة البيانات. منحنيات القوة--المسافة بالاعتماد البروتينات المعطل تداولها ووقت الاتصال أو سرعة تراجع، وإذا أدرج بصمة أم لا وأخرى معلمات متغير، يحتوي على معلومات مختلفة متعددة. تحليل البيانات وتفسيرها يمكن أن تختلف اختلافاً كبيرا بين مختلف التجارب SMFS و ولذلك لا يمكن وصفها بالتفصيل هنا. أما بالنسبة للتفاعل بين ررجا والجبهة الوطنية، البروتوكول التالية يمكن أن تكون خطوة أولى لتحليل البيانات SMFS.- فتح ملفات منحنى قياس القوة عن طريق تحديد رمز فتح دفعة من قوة المسح الضوئي وعملية منحنيات المسافة القوة على النحو التالي:
- تحويل انحراف ناتئ (V) إلى القوة طرديا مع (و) عن طريق تحديد الرمز (Re) معايرة الخامس-انحراف بضبط حساسية وربيع دائم .
ملاحظة: إذا تم إجراء المعايرة ناتئ قبل التجربة، القيم التي يتم حفظها في ملفات مسح القوة ويتم استخدامها تلقائياً أثناء معايرة الخامس-الانحراف. إذا تم إجراء المعايرة بعد التجربة، البرنامج يستخدم القيم الافتراضية التي يمكن تغييرها إلى القيم المقاسة. - طرح الخط الأساسي للقناة تراجع في منطقة منحنى القوة بعيداً عن السطح لتعيين مستوى القوة صفر عن طريق تحديد رمز الطرح خط الأساس.
ملاحظة: في بعض الحالات، هذا التراجع قد لا يكون بنفس قوة ثابتة القيمة، وقد عرض المنحنى ميل خطي، التي يمكن إزالتها عن طريق تحديد إزاحة + إمالة. - تعرف نقطة حيث يحصل الحافة اتصال مع العينة عن طريق تحديد رمز تحديد نقطة الاتصال .
- تحويل إشارة الارتفاع إلى فصل تلميح--نموذج عن طريق تحديد رمز الفصل عينة تلميح . بالإضافة إلى طرح موقف نقطة الاتصال، يطرح هذا الإجراء ناتئ الانحناء لحساب المسافة بين سطح الركيزة وفؤاد-تلميح.
ملاحظة: لتركيب نماذج مرنة البوليمر، مثل نموذج دودة-مثل-السلسلة القابلة للتوسيع، وتصميم التفاعل أطوال، مطلوب الفصل عينة تلميح، الذي هو تصحيح الانحناء ناتئ،. لتحديد قوة تحميل معدل من المنحدر من منحنى القوة والسرعة z-بيزو، ينبغي استخدام منحنيات القوة التي لم يتم تصحيحها. - الشاشة آثار القوة--المسافة لقمم القوة التي تحدث في أطوال تمزق 70 نيوتن متر (طول مباعدة شماعة ممدد)36 فرز التفاعلات غير محدد وتطبيق نموذج دودة-مثل-السلسلة القابلة للتوسيع إلى قمم المحدد عن طريق تحديد أعلاه رمز تناسب "نموذج سلسلة البوليمر" واختار Extensible "نموذج سلسلة" الشبيهة بالدودة. سوف تكون مزودة القمم في منحنى قوة سحب هذا النموذج والحصول القوات تمزق وأطوال، جنبا إلى جنب مع المعلمات مطاطا من البوليمر.
- عرض البيانات كرسوم بيانية تبين توزيع القوة والطول. استخدام الأحداث غير ملزم على الأقل 100 رسوم بيانية.
النتائج
وصف البروتوكول هنا النتائج في تجميد التساهمية من البروتينات عن طريق تلك الأمينات الأولية موجوداً مع اتجاه عشوائي (الشكل 1). الشكل 2 يوضح صورة فؤاد سطح الزجاج سيلانيزيد مع (يسار) وسجلت دون الجبهة الوطنية (يمين) معطلة، بعد جفاف العينات تحت تيار لطيف من النيتروجين. طبقة البوليمر سيلاني يوضح فقط الصغيرة كوروجاتيونس السطح بارتفاع حوالي 2-5 نيوتن متر (الشكل 2، حق)، بينما على سطح فونكتيوناليزيد مع الجبهة الوطنية، وهي حوالي 10 نانومتر عالية Fn جزيئات الظاهر (الشكل 2، يسار). في مقربة، يمكن التعرف على هيكل ديميريك من الجبهة الوطنية. يبدو أن الجزيئات Fn المدمجة مع ارتفاع 4-5 نانومتر أعلاه طلاء السطح شماعة وطول ~ 120 نانومتر (انظر إدراج).
للتحقيق في تفاعل قوي ررجا مع الجبهة الوطنية، التي وصفت بالتفصيل مؤخرا لدينا مجموعة13، اقترن ررجا إلى نصيحة فؤاد نيتريد السيليكون والجبهة الوطنية البشرية إلى الركيزة الزجاج (الشكل 3a). ويبين الشكل 3 نصيحة الممثل منحنيات فصل عينة من تفاعل ررجا مع الجبهة الوطنية المسجلة سرعة سحب من 1 ميكرومتر s-1. الكيمياء السطحية المستخدمة أدى إلى وجود تفاعل خلفية منخفضة وأحداث التفاعل جيدا على شكل واحد (أو مزدوج) (الشكل 3 أ)، التي كانت مزودة باستخدام دودة الموسعة مثل سلسلة (أولك) طراز (المنحنيات الحمراء). التآمر نتائج تناسب (تمزق القوة-والطول، انظر الشكل 4) يبين أن بعد التغلب على التفاعلات السطحية غير محددة بين نصيحة فؤاد والركيزة، وتمتد linkers شماعة (> 70 nm)، ما يصل إلى ~ 19% منحنيات القوة أظهرت تمزق الأحداث مع تمزق متوسط القوة ررجا-تفاعل Fn ~ pN 52 مسافات تلميح-عينة من حوالي 100 نانومتر. وفي المقابل، كيمياء سطحية غير قابل للتطبيق (هنا، تبريد مهملة مع تريس مخزنة المالحة الشكل 3b) سوف تحول دون إجراء تقييم واضح لإحداث تفاعل واحد بسبب التفاعلات غير محدد، متعددة البروتين ملزمة (تتبع 2 و 3) و/أو اقتران التساهمية البروتينات بين سطح العينة وطرف ناتئ فؤاد. هذا يؤدي إلى تمزق عالية قوات (تتبع 1) يرافقه ربما تتكشف نطاقات البروتين (الجبهة الوطنية) (تتبع 4 و 5).
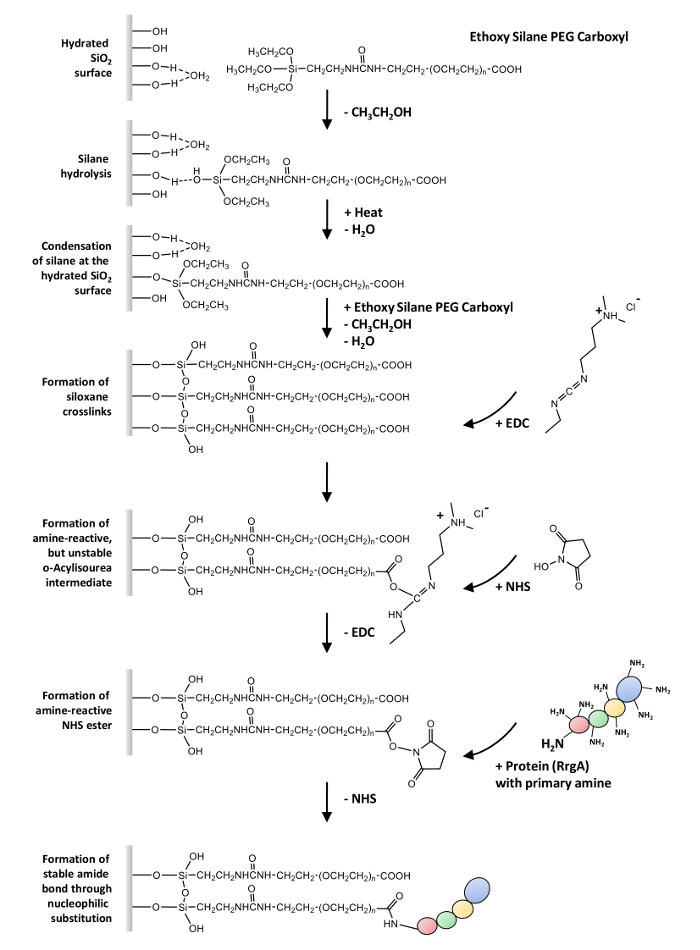
رقم 1: نظرة عامة على كيمياء السطح. أن التحلل من اثوكسي سيلاني-شماعة-الكربوكسيل متبوعاً التكثيف في سطح الزجاج رطب وتشكيل siloxane crosslinks. رد فعل لتنمية الصادرات مع مجموعات الكربوكسيل يؤدي رد الفعل س-أسيليسوريا، وسيط أمين المتفاعلة مع العمر النصفي له قصيرة للغاية في المحلول (التحلل المائي). واستقرت المتوسطة بتشكيل إستر الصحي الذي يخضع لتفاعلات الاستبدال وأخيراً تشكيل في سندات أميد مع الأمينات الأولية على البروتينات. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
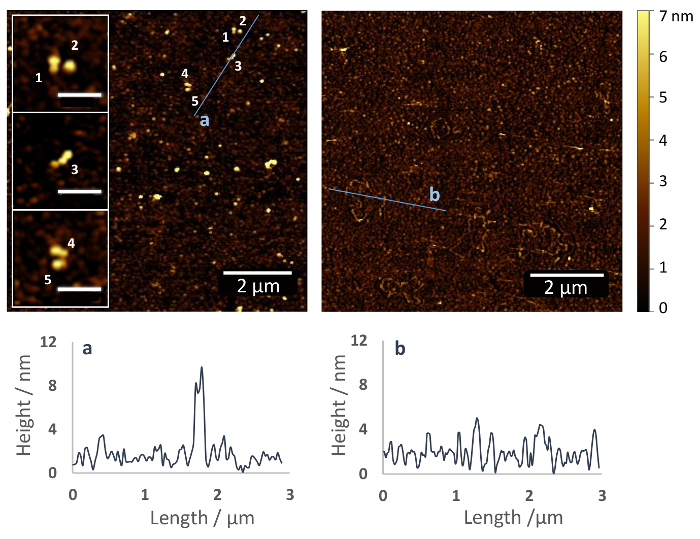
الشكل 2: التثبيت فيبرونيكتين على زجاج الركازة عبر هيتيروبيفونكشونال اثوكسي سيلاني شماعة عامل اقتران الكربوكسيل. صور فؤاد من الزجاج فونكتيوناليزيد السطوح مع (يسار) ودون (حق) تشير الأرقام Fn. إلى جزيئات الجبهة الوطنية الفردية، التي توزع البلوتينيوم على سطح الركازة (إدراج). الجزيئات اعتماد هيكل ديميريك والاتفاق مع ارتفاع من شمال البحر الأبيض المتوسط 4-5 أعلاه شماعة طلاء وطول > 100 نانومتر. وهذا يشبه هيكل الجبهة الوطنية في الحل ومتسقة مع البيانات السابقة فؤاد على الأسطح الأخرى، مثلاً، والميكا (شريط مقياس لتطعيم = 500 nm)37. فيما يلي صور فؤاد التشكيلات الجانبية للارتفاع على النحو المبين في الصور فؤاد. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
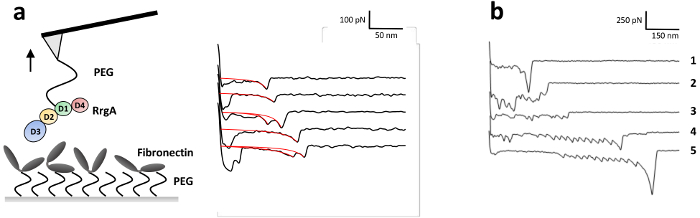
الشكل 3: توضيح لتجربة SMFS وممثل القوة منحنيات المسافة من ررجا-التفاعل Fn. (أ) ررجا والجبهة الوطنية كانت مرتبطة تساهميا عبر سيلاني اثوكسي هيتيروبيفونكشونال شماعة عامل اقتران الكربوكسيل إلى نيتريد سيليكون فؤاد تعزية نصيحة وسطح زجاج، على التوالي. SMFS ممثل القوة المسافة تظهر المنحنيات الحصول على ررجا--الجبهة الوطنية التفاعل سرعة تراجع من 1 ميكرومتر s-1 مع التثبيت وصف ررجا والجبهة الوطنية. تمثيل المنحنيات الحمراء يناسب الموسعة مثل دودة السلسلة تطبق على الحصول على قوات تمزق وأطوال. تم تعديل الرقم من بيك, et al., 2018 أكسنانو13. (ب (SMFS ممثل القوة منحنيات المسافة التي تم الحصول عليها ررجا--الجبهة الوطنية التفاعل دون تبريد مع تريس مخزنة المالحة. وفي هذه الحالة، أمين الأولية من تريس كان غائبا حتى أن تبقى نشطة استرات المستشفيات العامة تركت غير المشبعة أثناء التجربة. وادي ذلك إلى متعدد بروتين ملزمة (تتبع 2 و 3) ولقط البروتينات بين السطح ونصيحة فؤاد مما أدى إلى تمزق عالية القوات المجال مصحوبا (-الجبهة الوطنية) التي تتكشف (تتبع 1 و 4 و 5؛ ملاحظة مقاييس مختلفة). الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
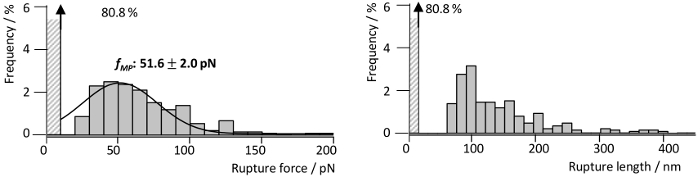
رقم 4: توزيع القوة وطول واحد ررجا-التفاعلات Fn. تمزق القوة ورسوم بيانية طول تمزق المقابلة التي تم الحصول عليها من ررجا-Fn SMFS التفاعل القياسات (n = 1400) سرعة تراجع من 1 ميكرومتر s-1. رسوم بيانية تكشف عن قوة تمزق الأكثر احتمالاً والنائب من 51.6 pN (تناسب غاوس، الخط الأسود) وتراكم تمزق أطوال حوالي 100 نانومتر. تم تعديل الرقم من بيك, et al., أكسنانو, 201813. الرجاء انقر هنا لمشاهدة نسخة أكبر من هذا الرقم-
Discussion
منذ إدخال فؤاد على أساس SMFS، تطورت تقنية تستخدم على نطاق واسع لمباشرة التحقيق البينية وقوات الجزيئات الفردية البروتينات والأحماض النووية وغيرها الجزيئات الحيوية3،،من4من5. للتجارب الناجحة التي SMFS، سطح مناسبة اقتران الاستراتيجية شرطا. للتحقيق أن القوات إينتراموليكولار في البوليمرات الطبيعية والاصطناعية، قد يقترن البوليمرات مباشرة على سطح الركازة وفؤاد نصيحة36،،من3839،،من4041. لتحقيق التفاعلات بين الجزيئات، مثل سندات الجزيئية، بيد أنه من المستحسن استخدام جزيئات رابط مرنة مثل هترو بيفونكشونال شماعة linkers، أو سلاسل ببتيد، تولي الشركاء التفاعل لنصيحة فؤاد سطح الركازة، بغية السماح للتوجه الصحيح للشركاء ملزمة، للتغلب على القوى السطحية قصيرة المدى وتجنب تمسخ وتتكشف من البروتينات21،،من2223، 24،،من2526،،من2742. ولذلك نحن وصف بروتوكول بسيطة ومباشرة إلى الأمام لتجميد التساهمية من البروتينات عن طريق الأمينات الأولية موجوداً استخدام الفواصل شماعة هترو-بيفونكشونال.
نحن أثبت قابليته للتطبيق مع التحقيق في التفاعل القوى بين أدهيسين ررجا من س. الرئوية والبروتين المصفوفة خارج الخلية الجبهة الوطنية، مؤخرا بالتفصيل في أماكن أخرى13.
كيمياء السطح بشكل جيد ونهج تم تحليلها ومماثلة قد استخدمت بنجاح في متعددة SMFS تجارب19،،من4243،،من4445. سيليليثير المستخدمة لاقتران البوليمر سيلاني إلى السطح، ويخضع للتحلل المائي. درجة التحلل المائي يعتمد على مقدار siloxane شكلت السندات التي يمكن السيطرة عليها أثناء عملية سيلانيزيشن. إذا كان من المتوقع خلال قياسات SMFS عالية التفاعل القوى (≥ 1000 السندات الإذنية)، ينبغي سيلانيزيشن المنجزة عن طريق المرحلة بخار ترسب30 الذي يؤدي إلى تشكيل طبقة مستمرة من السيلوكسانات. أما بالنسبة للعديد من التجارب (مثلاً، العديد من البروتين – تفاعلات البروتين)، قوي التفاعل في حدود بضع مئات من السندات الإذنية، ووصف الإجراء، في siloxane التي يضطلع بها ترسبات من مرحلة مائي تشكيل وغير منضم أورجانو-silanes يتم غسله مدروس مع الإيثانول (الخطوة 1.1.7) متبوعاً بالمعالجة بالحرارة (الخطوة 1.1.8)، وهو كاف.
خطوة حاسمة أخرى أن يغسل الصادرات المتبقية وجزيئات دائرة الصحة الوطنية قبالة السطح (الخطوة 1.2.3)، بقايا الطعام سوف يؤدي إلى تنشيط مجموعات الكربوكسيل في البروتينات. وهذا قد أما النتيجة في كروسلينكينج من البروتينات على السطح نفسه، والتي يمكن أن تغير من وظيفة كل منها أو تساهمي زوجين تنشيط البروتينات إلى غيرها من البروتينات على سطح المعاكس. قد يؤدي هذا إلى لقط البروتينات بين السطح ونصيحة فؤاد، الذي يؤدي إلى تمزق عالية القوات ربما مصحوبة بالمجال تتكشف (انظر الشكل 3b، تتبع 1 و 4 و 5، تتكشف من المجالات Fn)46. يمكن أن تحدث نفس المشكلة، إذا تركت استرات دائرة الصحة الوطنية النشطة من مباعدة شماعة غير المشبعة. ولذلك، الحضانة مع تريس مخزنة المالحة ينصح (الخطوة 1.2.6)، كما يروي أمين الأولية من تريس المجموعات المتفاعلة الأمينية المتبقية.
يتبع البروتوكول تدريجي يؤدي إلى توزيع متجانس للجبهة الوطنية على زجاج سيلانيزيد السطحية (انظر الشكل 2)، ترك نموذج ديميريك من البروتين. هذا يشبه هيكل Fn´s في الحل ومتسقة مع البيانات السابقة فؤاد على السطوح عينة أخرى37. وبالإضافة إلى ذلك، يتم الحصول عليها بتركيز مناسب من ررجا على نصيحة فؤاد، الذي يولد قيمة هدف ~ 20 ٪ من أحداث تفاعل محددة تحديداً جيدا خلال قياسات SMFS (رقم 3 و رقم 4). طريقة أنيقة أخرى للتحكم بكمية الجزيئات بالإضافة إلى نصيحة الركيزة وناتئ عينة إلى جانب متفاوتة الأوقات البروتين تركيز و/أو الحضانة، هو مزيج وكلاء سيلاني مع مختلف المجموعات الوظيفية الثانوية. عن طريق تغيير نسبة البروتين الجماعات المتفاعلة تمتد من شماعة-البوليمر، يمكن أن يكون عدد البروتينات المعطل تداولها التي تسيطر عليها15،16،،من1718.
يمكن أيضا استخدام البروتوكول الموصوفة هنا شل الجزيئات الأخرى التي تحتوي على2 -NH أو تعديلها للزوجين البروتينات على سطح أكسيد السيليكون الأخرى إلى جانب نيتريد السيليكون والزجاج. استناداً إلى تصميم البروتين، مجموعة الكربوكسيل رد الفعل أمين يمكن تغييرها إلى فريق رد الفعل سلفهيدريل (ثنائي كبريتيدمثلاًأو ماليميدي أو اورثو-بيرديدل) لزوجين البروتين عن طريق الحر-مجموعات SH. للجبهة الوطنية، وهذا يؤدي في اتجاه المعرفة مسبقاً13،17،20.
باختصار، هذا البروتوكول يمكن تعديلها لتلبية احتياجات مختلف وهو مناسبة للتطبيقات الفيزيائية الحيوية الأخرى إلى جانب تجارب التحليل الطيفي قوة جزيء واحد.
Disclosures
الكتاب ليس لها علاقة بالكشف عن.
Acknowledgements
السل وزئبق نعترف بالدعم المالي من خلال مجلس البحوث الأوروبية "سيلوفويل، متقدمة المنحة رقم 294438". HCS تسلم الدعم المالي من الوزارة الاتحادية للتعليم والبحث عن طريق Proteine تيتشنوفونكتيونالي إينوفاتيونساليانز (تيفوبروت)، يقر SS المالية دعم من وزارة الدولة البافارية للعلم والتعليم من خلال تركيز البحوث "هيرستيلونج und بيوفيسيكاليشي تشاراكتيريسيرونج دريديمينسيونالير جيويبي-كانتر". ونحن نشكر كريستوف هاسيلبيرج كوني ومارتينا Hörig للدعم الفني
Materials
| Name | Company | Catalog Number | Comments |
| Material | |||
| 2-Propanol | Carl Roth | 6752 | |
| 1-(3-dimethylaminopropyl)-3-ethylcarbodiimide | Sigma-Aldrich | 03450 | EDC |
| Acetic acid | Carl Roth | 3738 | 100 %; analytical purity |
| Doubly distilled water | |||
| Ethanol | Carl Roth | 9065 | ≥ 99.8 %; analytical purity |
| Ethoxy silane polyethylene glycol acid | Nanocs | PG2-CASL-5k | 5 kDa; COOH-PEG-Si(OC2H5)3 |
| Hydrochloric acid | Carl Roth | X896 | 32 % |
| N-Hydroxysuccinimid | Merck | 804518 | NHS; for synthesis |
| Phosphate Buffered Saline - Dulbecco | Biochrom | L1825 | PBS |
| Probe molecule e.g. Fibronectin, human plasma | Sigma-Aldrich | F1056 | |
| Probe molecule e.g. RrgA | Produced in laboratory | ||
| Sodiumchlorid | Carl Roth | 9265 | NaCl |
| Tris(hydroxymethyl)-aminomethan | Carl Roth | AE15 | ≥ 99,3 %; TRIS; Buffer Grade |
| Name | Company | Catalog Number | Comments |
| Equipment | |||
| Beakers | |||
| Glass cutter | |||
| Glass slides | Carl Roth | 0656 | |
| Inert gas desiccator | Sicco | ||
| Inverted Microscope - Zeiss Axiovert 200 | Zeiss | ||
| JPK NanoWizard 1 | JPK Instruments | ||
| JPK NanoWizard SPM and DP software | JPK Instruments | ||
| Laboratory oven | Binder | ||
| Magnetic stirrer | IKA | ||
| Micro spatula | |||
| Microcentrifuge tubes | |||
| Microsoft Excel | Microsoft | ||
| Parafilm M | Brand | 701606 | |
| Petri dishes | |||
| pH-meter | Knick | ||
| Pipettes | Starlab | 10-100 µl, 50-200 µl, 100-1000 µl | |
| Precision balance | Acculab | ||
| Silicon nitride cantilever - MLCT | Bruker AXS S.A.S | Spring constant ≤ 100 pN/nm | |
| Sonication bath | Bandelin | ||
| Staining jar | |||
| Stereo microscope - Zeiss Stemi | Zeiss | ||
| Stir bar | |||
| Kimtech science precision wipes | Kimberly-Clark | ||
| Twezzers | |||
| UV PenRay | UVP, LLC | 90-0012-01 | Mercury spectrum with the primary energy at 254 nm |
| Vacuum desiccator | |||
| Vacuum pump | |||
| Vortex mixer | VWR | ||
| Weighing paper | Carl Roth | TP64 |
References
- Binnig, G., Quate, C. F., Gerber, C. Atomic Force Microscope. Physical Review Letters. 56, 930-933 (1986).
- Neuman, K. C., Nagy, A. Single-Molecule Force Spectroscopy: Optical Tweezers, Magnetic Tweezers and Atomic Force Microscopy. Nature Methods. 5 (6), 491-505 (2008).
- Dufrene, Y. F. Atomic Force Microscopy, a Powerful Tool in Microbiology. Journal of Bacteriology. 184 (19), 5205-5213 (2002).
- Muller, D. J., Dufrene, Y. F. Atomic Force Microscopy as a Multifunctional Molecular Toolbox in Nanobiotechnology. Nature Nanotechnology. 3 (5), 261-269 (2008).
- Hinterdorfer, P., Dufrene, Y. F. Detection and Localization of Single Molecular Recognition Events Using Atomic Force Microscopy. Nature Methods. 3 (5), 347-355 (2006).
- Dufrene, Y. F. Sticky Microbes: Forces in Microbial Cell Adhesion. Trends in Microbiology. 23 (6), 376-382 (2015).
- Yakovenko, O., et al. FimH Forms Catch Bonds That Are Enhanced by Mechanical Force Due to Allosteric Regulation. The Journal of Biological Chemistry. 283 (17), 11596-11605 (2008).
- Casillas-Ituarte, N. N., et al. Amino Acid Polymorphisms in the Fibronectin-Binding Repeats of Fibronectin-Binding Protein A Affect Bond Strength and Fibronectin Conformation. The Journal of Biological Chemistry. 292 (21), 8797-8810 (2017).
- Hilleringmann, M., et al. Molecular Architecture of Streptococcus Pneumoniae TIGR4 Pili. The EMBO Journal. 28 (24), 3921-3930 (2009).
- Izore, T., et al. Structural Basis of Host Cell Recognition by the Pilus Adhesin from Streptococcus Pneumoniae. Structure. 18 (1), 106-115 (2010).
- Henriques-Normark, B., Tuomanen, E. I. The Pneumococcus: Epidemiology, Microbiology, and Pathogenesis. Cold Spring Harbor Perspectives in Medicine. 3 (7), a010215 (2013).
- Henderson, B., Nair, S., Pallas, J., Williams, M. A. Fibronectin: a Multidomain Host Adhesin Targeted by Bacterial Fibronectin-Binding Proteins. FEMS Microbiology Reviews. 35 (1), 147-200 (2011).
- Becke, T. D., et al. Single Molecule Force Spectroscopy Reveals Two-Domain Binding Mode of Pilus-1 Tip Protein RrgA of Streptococcus Pneumoniae to Fibronectin. ACS nano. 12 (1), 549-558 (2018).
- Herman-Bausier, P., Pietrocola, G., Foster, T. J., Speziale, P., Dufrene, Y. F. Fibrinogen Activates the Capture of Human Plasminogen by Staphylococcal Fibronectin-Binding Proteins. mBio. 8 (5), e01067 (2017).
- Vitry, P., Valotteau, C., Feuillie, C., Bernard, S., Alsteens, D., Geoghegan, J. A., Dufrene, Y. F. Force-Induced Strengthening of the Interaction between Staphylococcus aureus Clumping Factor B and Loricrin. mBio. 8 (6), e01748 (2017).
- Milles, L. F., Schulten, K., Gaub, H. E., Bernardi, R. C. Molecular Mechanism of Extreme Mechanostability in a Pathogen Adhesin. Science. 359 (6383), 1527-1533 (2018).
- Jobst, M. A., Schoeler, C., Malinowska, K., Nash, M. A. Investigating Receptor-Ligand Systems of the Cellulosome with AFM-Based Single-Molecule Force Spectroscopy. Journal of Visualized Experiments. (82), e50950 (2013).
- Stetter, F. W., Kienle, S., Krysiak, S., Hugel, T. Investigating Single Molecule Adhesion by Atomic Force Spectroscopy. Journal of Visualized Experiments. (96), e52456 (2015).
- Schmidt, S. W., Christ, T., Glockner, C., Beyer, M. K., Clausen-Schaumann, H. Simple Coupling Chemistry Linking Carboxyl-Containing Organic Molecules to Silicon Oxide Surfaces under Acidic Conditions. Langmuir: the ACS journal of surfaces and colloids. 26 (19), 15333-15338 (2010).
- Zimmermann, J. L., Nicolaus, T., Neuert, G., Blank, K. Thiol-Based, Site-Specific and Covalent Immobilization of Biomolecules for Single-Molecule Experiments. Nature Protocols. 5 (6), 975-985 (2010).
- Ott, W., Jobst, M. A., Schoeler, C., Gaub, H. E., Nash, M. A. Single-Molecule Force Spectroscopy on Polyproteins and Receptor-Ligand Complexes: The Current Toolbox. Journal of Structural Biology. 197 (1), 3-12 (2017).
- Ott, W., et al. Elastin-like Polypeptide Linkers for Single-Molecule Force Spectroscopy. ACS nano. 11 (6), 6346-6354 (2017).
- Ebner, A., et al. A New, Simple Method for Linking of Antibodies to Atomic Force Microscopy Tips. Bioconjugate Chemistry. 18 (4), 1176-1184 (2007).
- Kufer, S. K., et al. Covalent Immobilization of Recombinant Fusion Proteins with hAGT for Single Molecule Force Spectroscopy. European Biophysics Journal with Biophysics Letters. 35 (1), 72-78 (2005).
- Hinterdorfer, P., Baumgartner, W., Gruber, H. J., Schilcher, K., Schindler, H. Detection and Localization of Individual Antibody-Antigen Recognition Events by Atomic Force Microscopy. Proceedings of the National Academy of Sciences of the United States of America. 93 (8), 3477-3481 (1996).
- Hinterdorfer, P., Schilcher, K., Gruber, H. J., Schindler, H. Conjugation of Biomolecules to Tip and Probe Surfaces for Molecular Recognition in Atomic Force Microscopy. European Journal of Cell Biology. 74, 72 (1997).
- Riener, C. K., et al. Heterobifunctional Crosslinkers for Tethering Single Ligand Molecules to Scanning Probes. Analytica Chimica Acta. 497 (1-2), 101-114 (2003).
- Metwalli, E., Haines, D., Becker, O., Conzone, S., Pantano, C. G. Surface Characterizations of Mono-, Di-, and Tri-Aminosilane Treated Glass Substrates. Journal of Colloid and Interface Science. 298 (2), 825-831 (2006).
- Beyer, D., Knoll, W., Ringsdorf, H., Elender, G., Sackmann, E. Covalently Attached Polymer Mono- and Multilayers on Silanized Glass Substrates. Thin Solid Films. 284, 825-828 (1996).
- Hermanson, G. T. Chapter 13 - Silane Coupling Agents. Bioconjugate Techniques. 3, 535-548 (2013).
- Howarter, J. A., Youngblood, J. P. Optimization of Silica Silanization by 3-aminopropyltriethoxysilane. Langmuir: the ACS Journal of Surfaces and Colloids. 22 (26), 11142-11147 (2006).
- Hermanson, G. T. Chapter 6 - Heterobifunctional Crosslinkers. Bioconjugate Techniques. 3, 299-339 (2013).
- Sehgal, D., Vijay, I. K. A Method for the High Efficiency of Water-Soluble Carbodiimide-Mediated Amidation. Analytical Biochemistry. 218 (1), 87-91 (1994).
- Xue, Y., Li, X., Li, H., Zhang, W. Quantifying Thiol-Gold Interactions Towards the Efficient Strength Control. Nature Communications. 5, 4348 (2014).
- Butt, H. J., Jaschke, M. Calculation of Thermal Noise in Atomic Force Microscopy. Nanotechnology. 6, 1-7 (1995).
- Oesterhelt, F., Rief, M., Gaub, H. E. Single Molecule Force Spectroscopy by AFM Indicates Helical Structure of Poly(ethylene-glycol) in Water. New Journal of Physics. 1 (1), 6 (1999).
- Gugutkov, D., Gonzalez-Garcia, C., Rodriguez Hernandez, J. C., Altankov, G., Salmeron-Sanchez, M. Biological Activity of the Substrate-Induced Fibronectin Network: Insight Into the Third Dimension Through Electrospun Fibers. Langmuir: the ACS Journal of Surfaces and Colloids. 25 (18), 10893-10900 (2009).
- Rief, M., Oesterhelt, F., Heymann, B., Gaub, H. E. Single Molecule Force Spectroscopy on Polysaccharides by Atomic Force Microscopy. Science. 275 (5304), 1295-1297 (1997).
- Rief, M., Gautel, M., Oesterhelt, F., Fernandez, J. M., Gaub, H. E. Reversible Unfolding of Individual Titin Immunoglobulin Domains by AFM. Science. 276 (5315), 1109-1112 (1997).
- Marszalek, P. E., Oberhauser, A. F., Pang, Y. P., Fernandez, J. M. Polysaccharide Elasticity Governed by Chair-Boat Transitions of the Glucopyranose Ring. Nature. 396 (6712), 661-664 (1998).
- Clausen-Schaumann, H., Rief, M., Tolksdorf, C., Gaub, H. E. Mechanical Stability of Single DNA Molecules. Biophysical Journal. 78 (4), 1997-2007 (2000).
- Schmidt, S. W., Filippov, P., Kersch, A., Beyer, M. K., Clausen-Schaumann, H. Single-Molecule Force-Clamp Experiments Reveal Kinetics of Mechanically Activated Silyl Ester Hydrolysis. ACS nano. 6 (2), 1314-1321 (2012).
- Schmidt, S. W., Beyer, M. K., Clausen-Schaumann, H. Dynamic Strength of the Silicon-Carbon Bond Observed Over Three Decades of Force-Loading Rates. Journal of the American Chemical Society. 130 (11), 3664-3668 (2008).
- Schmidt, S. W., Kersch, A., Beyer, M. K., Clausen-Schaumann, H. Mechanically Activated Rupture of Single Covalent Bonds: Evidence of Force Induced Bond Hydrolysis. Physical Chemistry Chemical Physics. 13 (13), 5994-5999 (2011).
- Schmidt, S. W., Pill, M. F., Kersch, A., Clausen-Schaumann, H., Beyer, M. K. Mechanically Induced Silyl Ester Cleavage Under Acidic Conditions Investigated by AFM-Based Single-Molecule Force Spectroscopy in the Force-Ramp Mode. Faraday Discussions. 170, 357-367 (2014).
- Rief, M., Gautel, M., Gaub, H. E. Unfolding Forces of Titin and Fibronectin Domains Directly Measured by AFM. Advances in Experimental Medicine and Biology. 481, 129-136 (2000).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved