Method Article
تصنيع شبكة التقارب العقدي لإعداد عينة المجهر الإلكتروني بالتبريد
In This Article
Summary
يتم توفير بروتوكول خطوة بخطوة لتصنيع شبكات تقارب الستربتافيدين لاستخدامها في الدراسات الهيكلية لعينات الجزيئات الكبيرة الصعبة بواسطة المجهر الإلكتروني بالتبريد.
Abstract
توفر شبكات تقارب الستربتافيدين استراتيجيات للتغلب على العديد من تحديات تحضير العينات بالمجهر الإلكتروني بالتبريد (cryo-EM) الشائعة ، بما في ذلك تمسخ العينة والتوجهات التفضيلية التي يمكن أن تحدث بسبب واجهة الهواء والماء. ومع ذلك ، يتم استخدام شبكات تقارب الستربتافيدين حاليا من قبل عدد قليل من مختبرات cryo-EM لأنها غير متوفرة تجاريا وتتطلب عملية تصنيع دقيقة. تزرع بلورات الستربتافيدين ثنائية الأبعاد على طبقة أحادية من الدهون البيوتينيلية يتم تطبيقها مباشرة على شبكات cryo-EM القياسية ذات الكربون الهولي. يسمح التفاعل عالي التقارب بين الستربتافيدين والبيوتين بالربط اللاحق للعينات البيوتينيلاتية المحمية من واجهة الهواء والماء أثناء تحضير عينة cryo-EM. بالإضافة إلى ذلك ، توفر هذه الشبكات استراتيجية لتركيز العينات المتاحة بكميات محدودة وتنقية مجمعات البروتين ذات الأهمية مباشرة على الشبكات. هنا ، يتم توفير بروتوكول محسن خطوة بخطوة للتصنيع القوي لشبكات تقارب الستربتافيدين لاستخدامها في تجارب cryo-EM والبقع السلبية. بالإضافة إلى ذلك ، يتم تضمين دليل استكشاف الأخطاء وإصلاحها للتحديات الشائعة لجعل استخدام شبكات تقارب الستربتافيدين أكثر سهولة لمجتمع cryo-EM الأكبر.
Introduction
أحدث المجهر الإلكتروني بالتبريد (cryo-EM) ثورة في مجال البيولوجيا الهيكلية من خلال تمكين تحديد البنية الجزيئية الكبيرة والمرنة وغير المتجانسة التي لم يكن من الممكن الوصول إليها سابقا عن طريق علم البلورات بالأشعة السينية أو الرنين المغناطيسي النووي1. تعمل هذه الطريقة عن طريق تجميد الجزيئات الكبيرة في محلول لإنشاء طبقة رقيقة من الجليد الزجاجي يمكن تصويرها لاحقا باستخدام المجهر الإلكتروني. في السنوات الأخيرة ، أدت التطورات الكبيرة في كل من أجهزة المجهر وبرامج معالجة الصور إلى توسيع أنواع العينات المناسبة لتحديد الهيكل عالي الدقة بواسطة cryo-EM.
ومع ذلك ، يظل تحضير العينات الرقيقة والمزججة أحد أهم الخطوات في تحديد التركيب الجزيئي الكبير بواسطة cryo-EM. غالبا ما تكون العينات البيولوجية ديناميكية وهشة وعرضة للتمسخ ، وأحيانا لا تتوفر إلا بكميات صغيرة لدراسات cryo-EM. أثناء عملية النشاف ، تتفاعل هذه الجسيمات مع واجهة الهواء والماء الكارهة للماء ، والتي يمكن أن تؤدي إلى اتجاهات مفضلة للجسيمات ، وتفكيك المعقدات الهشة ، وتمسخ العينة الجزئي أو الكامل ، والتجميع2،3،4. يعد استخدام المنظفات أو المواد الخافضة للتوتر السطحي الأخرى ، والربط المتقاطع الكيميائي ، وامتصاص العينات لدعم الطبقات من الاستراتيجيات الشائعة للحفاظ على العينات البيولوجية أثناء عملية التجميد. تعمل طبقات الدعم مثل أكسيد الجرافين5،6،7 أو الكربون غير المتبلور8 أيضا على تركيز الجسيمات على الشبكة عن طريق الامتزاز عندما تكون العينة متاحة بكميات محدودة. ومع ذلك ، فإن هذه الطرق ليست عامة أو موثوقة ، ويمكن أن يستغرق تحسين إعداد الشبكة وقتا طويلا للغاية أو يفشل تماما.
تم تطوير شبكات تقارب Streptavidin 9,10 للتغلب على أوجه القصور هذه ولتوفير طريقة معتدلة وقابلة للتطبيق بشكل عام لعزل مجمع الاهتمام وحمايته من واجهة الهواء والماء. تستخدم هذه الشبكات شبكة بلورية ثنائية الأبعاد (2D) من الستربتافيدين تزرع على طبقة أحادية من الدهون البيوتينيلاتية على الشبكة. بعد أن يتم تكوين البيوتينيل في العينات نفسها (غالبا ما تكون قليلة وعشوائية ، مما يعني وجود بيوتين واحد لكل مركب في المتوسط) ، يمكن تطبيقها على الشبكة المغلفة بالستربتافيدين . نظرا لأن امتزاز العينة يعتمد على التقارب العالي للغاية بين الستربتافيدين والبيوتين ، يمكن استخدام تركيزات عينة منخفضة تصل إلى 10 نانومتر مع هذه الشبكات. مجموعات البيوتينيل المتاحة تجاريا للبروتينات وبادئات البيوتينيل للمجمعات المحتوية على الحمض النووي تجعل من السهل نسبيا إرفاق أجزاء البيوتين الضرورية بمعظم العينات ذات الأهمية. بالإضافة إلى تركيز العينة وإبقائها بعيدا عن واجهة الهواء والماء الضارة أثناء النشاف ، يمكن أن يؤدي البيوتينيل العشوائي لواحد أو عدد قليل من بقايا اللايسين إلى تحسين نطاق اتجاهات الجزيء محل الاهتمام على شبكة cryo-EM بشكل كبير ، كما هو موضح في عدد من الدراسات11. في حين أن الإشارة من بلورة الستربتافيدين الأساسية موجودة في الصور الخام ، يمكن إزالة مخططات معالجة البيانات التي تتضمن ترشيح فورييه لانعكاسات براغ الحادة من البلورة بسهولة أثناء معالجة البيانات المبكرة ، مما يتيح في النهاية إعادة بناء عالية الدقة للعينة محل الاهتمام11،12،13. هنا ، يتم توفير بروتوكول محسن خطوة بخطوة للإنتاج القوي لشبكات تقارب الستربتافيدين والاستخدام اللاحق في تجارب cryo-EM. من المتوقع أن يكتمل البروتوكول المقدم خلال فترة أسبوعين (الشكل 1أ). تصف الأجزاء الأولى من البروتوكول تحضير الكواشف ، والمعالجة المسبقة للشبكات ، وخطوات تبخر الكربون الأولى. بعد ذلك ، يتم وصف التعليمات لإعداد الطبقة الأحادية الدهنية ونمو بلورات الستربتافيدين على شبكات EM. بالإضافة إلى ذلك ، يتم توفير تعليمات لاستخدام شبكات تقارب الستربتافيدين في تجارب EM و cryo-EM للبقع السلبية. أخيرا ، يتم توفير إجراءات لإزالة إشارة الستربتافيدين من الصور المجهرية بمجرد الحصول على بيانات cryo-EM.
Protocol
1. إعداد الكواشف
- تمييع الستربتافيدين المشتراة تجاريا إلى تركيز نهائي قدره 0.5 ملغم / مل في محلول التبلور (50 ملي مول HEPES pH 7.5 ، 150 mM KCl ، 5 mM EDTA ، 10٪ تريهالوز). تأكد من أن تركيز تريهالوز النهائي هو 10٪. قسامات تجميد فلاش من 25-50 ميكرولتر في النيتروجين السائل وتخزينها في -80 درجة مئوية.
- قم بإذابة 1،2-dipalmitoyl-sn-glycero-3-phosphoethanolamine-N- (بيوتينيل) ملح الصوديوم في 65: 35: 8 v / v / v كلوروفورم / ميثانول / مذيب ماء لتركيز دهون نهائي يبلغ 1 مجم / مل. قم بتخزين القسوم ذات الاستخدام الواحد من 20-30 ميكرولتر عند -80 درجة مئوية في قوارير زجاجية.
ملاحظة: يكون تحضير المذيب أكثر دقة إذا تم بالوزن. أولا ، امزج 1.85 جم من الماء عالي النقاء مع 6.41 جم من الميثانول عالي الأداء من درجة الكروماتوغرافيا السائلة (HPLC) وأضف هذا إلى 22.42 جم من الكلوروفورم لتحضير المذيب.
تنبيه: يرجى قراءة وفهم صحائف بيانات السلامة الخاصة بالمصنعين والتعليمات الموصى بها للتعامل مع المذيبات العضوية للكلوروفورم والميثانول والتخلص منها قبل البدء في هذا البروتوكول. تجنب الاتصال المباشر للميثانول مع الجلد.
2. المعالجة المسبقة للشبكات
- اغسل ورق الكربون على شبكات شبكية ذهبية عن طريق غمسها مرتين في كلوروفورم 100٪ ومرة واحدة في إيثانول 100٪. ضع الشبكات على ورق ترشيح نظيف حتى يجف. كرر عملية الغسيل لمدة ثلاث دورات.
ملاحظة: تم تحقيق نجاح قابل للتكرار من خلال شبكات رقائق الكربون المتاحة تجاريا والتي تحتوي على فيلم كربون بسمك 10-12 نانومتر (انظر قائمة المواد) بأحجام ثقوب تتراوح من 0.6-2 ميكرومتر. كما تم بنجاح استخدام شبكات رقائق الذهب المتاحة تجاريا وشبكات الكربون المصنوعة منزليا والتي تم إعدادها وفقا لبروتوكول التصنيع النانوي14 لمختبر روبنشتاين. تم الحصول على نتائج أقل قابلية للتكرار من خلال الشبكات المتاحة تجاريا والتي تحتوي على أغشية كربون أرق. لا تستخدم الشبكات النحاسية ، حيث يتفاعل النحاس مع أي أمينات عضوية قد تكون في العينة. - بعد أن تجف الشبكات ، تبخر طبقة من الكربون بسمك 2.5-5 نانومتر على جانب الكربون من شبكات الكربون الثقيلة. يتم التحكم في سمك الكربون من خلال قياس سمك فيلم بلور الكوارتز المدمج في مبخر الكربون المقدم في ملف جدول المواد .
- السماح للكربون المتبخر حديثا بالعمر (أي يصبح أكثر كارها للماء) لمدة 1 أسبوع.
3. إعداد شعرية الستربتافيدين
ملاحظة: لزراعة بلورات الستربتافيدين ثنائية الأبعاد على شبكات EM الكربونية ، أولا ، يتم تطبيق طبقة أحادية من الدهون البيوتينيلية على ثقوب فيلم الكربون (الشكل 1 ب) عن طريق نقل Langmuir-Schaefer. تتشكل الطبقة الأحادية الدهنية باتباع الخطوات اللاحقة (الشكل 2). يخلق بودرة التلك حدا بين زيت الخروع وطبق بتري ، وتساعد طبقة رقيقة من زيت الخروع في الحفاظ على ضغط سطحي ثابت عند تكوين طبقة أحادية دهنية. يستخدم الجانب الذي يحتوي على الكربون المتبخر من الخطوة 2.2 لالتقاط الطبقة الأحادية ، ويتم غسل الدهون الزائدة بمحلول التبلور ، ويتم تحضين محلول الستربتافيدين على الشبكة للتبلور.
- نظف منطقة المقعد بنسبة 70٪ من الإيثانول.
- شطف حقنة زجاجية 5 ميكرولتر عدة مرات مع الكلوروفورم لتنظيف. اترك المحقنة تجف تماما قبل الاستخدام.
- اغسل الشبكات المتبخرة بالكربون مرة أخرى ، أي قبل الاستخدام مباشرة ، عن طريق غمسها في الإيثانول بنسبة 100٪. اترك الشبكات تجف على ورق ترشيح نظيف.
- أثناء تجفيف الشبكات ، اغسل كل ملقط مضاد للشعيرات الدموية بنسبة 100٪ كلوروفورم و 100٪ إيثانول. اترك الملقط حتى يجف تماما.
- على الجانب النظيف من parafilm ، قم بإعداد ثلاث قطرات 50 ميكرولتر من مخزن التبلور (50 mM HEPES pH 7.5 ، 150 mM KCl ، 5 mM EDTA ، 10٪ trehalose) لكل شبكة سيتم تصنيعها.
- املأ غطاء طبق بتري غير مطلي 35 مم بمحلول تبلور (50 مللي متر HEPES pH 7.5 ، 150 mM KCl ، 5 mM EDTA ، 10٪ trehalose). نظف السطح بورق العدسة.
- يرش بودرة التلك من الدرجة العلمية حول محيط طبق بتري. يعمل هذا لاحقا كمؤشر ، في الخطوة التالية ، على مدى انتشار زيت الخروع. أضف ما يكفي من بودرة التلك لإنشاء حاجز يحمي زيت الخروع من لمس حافة طبق بتري. إضافة الكثير من بودرة التلك يحد من المساحة المتاحة لجعل طبقة الدهون أحادية.
- اغمس طرف ماصة سعة 200 ميكرولتر في زيت الخروع للحصول على قطرة متوسطة الحجم (حوالي 20 ميكرولتر) تتدلى من طرف الماصة. المس هذا الانخفاض على سطح المخزن المؤقت في طبق بتري ، حيث سينتشر لتشكيل فيلم موحد. يعمل الفيلم الرقيق الناتج من الزيت كمكبس15 ، والذي يحافظ على ضغط سطحي ثابت عند تكوين طبقة أحادية دهنية (الخطوة 3.10).
ملاحظة: من المهم إضافة كمية كافية من زيت الخروع بدلا من القليل جدا ، ومن الأفضل إضافتها كقطرة واحدة. اترك زيت الخروع ينتشر تماما قبل عمل الطبقة الأحادية للدهون. - شطف حقنة زجاجية 5 ميكرولتر مرة أو مرتين مع الدهون المذابة قبل تناول القسمة للاستخدام. تجنب خلق فقاعات الهواء في الدهون التي تملأ المحقنة.
ملاحظة: يتم شطف المحقنة الزجاجية بالدهون المذابة في حالة بقاء أي كلوروفورم متبقي من الخطوة 3.2. يمكن أن يؤثر الكلوروفورم المتبقي على جودة الطبقة الأحادية الناتجة. - استغني عن أصغر حجم ممكن (~ 0.5 ميكرولتر) من الدهون من المحقنة والمس القطرة المعلقة برفق على سطح فيلم زيت الخروع. لاحظ أن محلول الدهون يخترق فيلم زيت الخروع عند نقطة التلامس وأن الطبقة الأحادية الدهنية الناتجة تشكل دائرة في وسط الطبقة الرقيقة من زيت الخروع.
- أضف عدة قطرات من الدهون بالتتابع أو أضف المزيد من الدهون بعد عمل بعض الشبكات ، ولكن إذا تمت إضافة الكثير ، فسوف ينتشر الليبيد خارج حدود زيت الخروع إلى المحيط حيث تم عزل بودرة التلك وأي خافض للتوتر السطحي ملوث. في حالة حدوث ذلك ، ستحتاج العملية إلى إعادة التشغيل.
- التقط شبكة بملقط مضاد للشعيرات الدموية بحيث يواجه كل من الذراع المستقيم للملقط والجانب المتبخر بالكربون من الشبكة الطبقة الأحادية.
- انقل جزءا من الطبقة الأحادية إلى الكربون المثقوب عن طريق لمس الجانب المتبخر بالكربون من الشبكة إلى الطبقة الأحادية لمدة 1-2 ثانية.
ملاحظة: يشار إلى النقل الناجح من خلال سطح الشبكة الذي يصبح محبا للماء ، مما يتسبب في غطاء كروي رفيع من المخزن المؤقت لتغطية الشبكة بأكملها بعد رفعه بعيدا عن طبق بتري. - المس الغطاء الكروي للمخزن المؤقت الذي يلتصق الآن بالشبكة ، بالتتابع لمدة 1 ثانية لكل منهما ، إلى ثلاث قطرات 50 ميكرولتر من مخزن التبلور الواقي الذي تم تحضيره على parafilm في الخطوة 3.5.
ملاحظة: تحاول هذه الخطوة إزالة أكبر قدر ممكن من الدهون الزائدة ، والتي تغطي سطح الغطاء الكروي (بدلا من فيلم الكربون الكارهة للماء سابقا) ، من أجل تجنب تكوين حويصلات دهنية عند عرض العينات في المجهر الإلكتروني. - أضف بعناية 4 ميكرولتر من 0.5 مجم / مل من الستربتافيدين إلى الغطاء الكروي المتبقي لمخزن التبلور على الشبكة.
- ضع الشبكة في غرفة الرطوبة. كرر الخطوات 3.11-3.14 لمجموعة الشبكات بأكملها.
- احتضان الشبكات في درجة حرارة الغرفة (RT) لمدة 2 ساعة داخل غرفة الرطوبة لتجنب التبخر.
ملاحظة: من المهم ألا يصبح الجانب الذهبي من الشبكة مبللا في أي وقت بعد تطبيق الطبقة الأحادية. - بعد الحضانة لمدة ساعتين ، قم بإعداد قطرة واحدة 300 ميكرولتر من محلول الشطف (10 mM HEPES ، درجة الحموضة 7.5 ، 50 mM KCl ، 5 mM EDTA ، 10٪ trehalose) لكل شبكة على الجانب النظيف من parafilm.
ملاحظة: يحتوي المخزن المؤقت للشطف على 50 مللي متر KCl بدلا من 150 مللي متر KCl ، وهو موجود في مخزن التبلور المؤقت المستخدم في الخطوات 3.5-3.6. - اغسل الستربتافيدين الزائد (غير المنضم) عن طريق وضع الشبكة على قطرة 300 ميكرولتر من محلول الشطف. قم بتنفيذ الخطوات 3.18-3.20 لشبكة واحدة في كل مرة. تجنب ترك الشبكات على قطرة عازلة للشطف سعة 300 ميكرولتر لفترات طويلة من الوقت.
ملاحظة: يتم إجراء غسلة واحدة فقط لأن بلورة / أحادية الطبقة من الستربتافيدين هشة في هذه المرحلة. في كل مرة يتم فيها رفع الشبكة بعيدا عن سطح قطرة من محلول الغسيل ، يتمزق الجسر السائل بين الشبكة وقطرة الغسيل. في وقت التمزق ، يتم تطبيق تدرج ضغط عابر (ضغط الشفط) على بلورات أحادية الطبقة ذاتية الدعم تمتد عبر الثقوب المفتوحة لفيلم الكربون. من المتوقع أن يتسبب ضغط الشفط هذا في هيمنة عابرة للبلورة أحادية الطبقة ، مصحوبة بتوسيع المنطقة التي تغطيها البلورات. إذا تجاوزت الزيادة في المنطقة الحد المرن للبلورة ، فقد تنكسر البلورة أو تصبح مضطربة. - جفف الملقط المضاد للشعيرات الدموية على الفور بمنديل خال من النسالة لتسهيل إطلاق الشبكة على ورق الترشيح في الخطوة التالية. التقط الشبكة العائمة على قطرة العازلة للشطف عن طريق لصق الذراع الملتوية للملقط المضاد للشعيرات الدموية في القطرة.
- امسح المخزن المؤقت الزائد برفق من الجانب باستخدام ورق الترشيح. ضع الشبكة على ورق الترشيح بحيث يكون الجانب الذهبي لأسفل ، وكرر الخطوات 3.18-3.20 لكل شبكة ، واترك الشبكات تجف لمدة 15-20 دقيقة.
- بعد أن تجف الشبكات ، اقلبها بحيث يكون الجانب الذهبي متجها الآن لأعلى. تبخر طبقة رقيقة من الكربون (حوالي 0.5-2 نانومتر) على الجانب الذهبي من الشبكات.
ملاحظة: قم بتخزين الشبكات في رطوبة ثابتة ، لا يبدو أن قيمتها مهمة ، مع ملاحظة أنه من المتوقع أن تؤدي التغييرات المتعددة في الرطوبة النسبية إلى دورات من التمدد والانكماش. السماح للشبكات بالعمر لمدة 1 أسبوع قبل استخدام cryo-EM للحصول على أفضل النتائج لأن الكارهة للماء في الجانب الخلفي من الشبكة قد تكون مهمة لاستقرار الطبقة الأحادية. الشبكات مستقرة لفترات طويلة من الزمن ، ولكن بعد 3 أشهر ، قد يصبح الكربون الخلفي أقل كارها للماء.
4. التحقق من جودة دفعة شبكة تقارب الستربتافيدين بواسطة وصمة عار سلبية
- قم بإعداد قطرتين من 50 ميكرولتر وقطرة واحدة من 100 ميكرولتر من المخزن المؤقت للعينة (50 mM HEPES pH 7.5 ، 50 mM KCl ، 0.5 mM TCEP) على الجانب النظيف من parafilm.
- قم بإزالة شبكات trehalose و rehydrate streptavidin عن طريق لمس قطرتين 50 ميكرولتر واترك الشبكة تطفو على قطرة 100 ميكرولتر من المخزن المؤقت للعينة لمدة 10 دقائق.
ملاحظة: من الأفضل تجنب استخدام المنظفات أثناء الإماهة وحضانات ربط العينات اللاحقة. سوف يتشتت المخزن المؤقت إلى الجانب الذهبي من الشبكات ويحد من كفاءة الغسيل لإزالة العينات الزائدة. - بعد إعادة الترطيب ، التقط الشبكة باستخدام ملقط مضاد للشعيرات الدموية بحيث يكون الذراع الملتوي للملقط المضاد للشعيرات الدموية في الانخفاض.
- امسح المخزن المؤقت الزائد برفق بعيدا عن الجانب وأعد تطبيق 4 ميكرولتر من عينة 75-100 نانومتر بسرعة (اختياري).
ملاحظة: تجنب ترك الشبكة تجف بعد الإماهة. - احتضان العينة في غرفة الرطوبة لمدة 1-5 دقائق.
ملاحظة: ستعتمد أوقات التركيز والحضانة على العينة ويجب تحسينها. يقترح تركيز العينة المقدمة ووقت الحضانة. - على الجانب النظيف من parafilm ، قم بإعداد أربع قطرات من 30 ميكرولتر لكل من المخزن المؤقت للعينة وبقعة فورمات اليورانيل (UF) بنسبة 1٪.
ملاحظة: يرجى قراءة وفهم صحائف بيانات السلامة الخاصة بالشركات المصنعة والتعليمات الموصى بها للتعامل مع فورمات اليورانيل والتخلص منها قبل تنفيذ هذه الخطوة. فورمات اليورانيل مركب سام ومشع. التأكد من الحصول على موافقة مؤسسية مسبقة لاستخدام المواد المشعة. - اغسل العينة غير المنضمة عن طريق لمس كل قطرة من القطرات الأربع من المخزن المؤقت للعينة.
- قم بتلطيخ العينة باستخدام إجراءات البقع السلبية القياسية مع UF. امسح بقعة UF برفق من الجانب ، تاركا طبقة سميكة جدا من البقع على الشبكة. يمكن وضع 0.5 ميكرولتر إضافية من البقعة على الشبكة بعد النشاف لجعل البقعة أكثر سمكا إذا لزم الأمر. اترك الشبكة تجف في الهواء.
ملاحظة: نظرا لأن شبكات الستربتافيدين محبة للماء للغاية ، تميل البقعة السلبية إلى تكوين طبقة موحدة للغاية في كل مكان ، على عكس ما هو شائع عند استخدام شبكات الكربون المستمرة المعالجة بالتوهج. نتيجة لذلك ، يوصى بترك طبقة سميكة من محلول البقع.
5. تجميد شبكات تقارب الستربتافيدين مع عينات البيوتينيل
ملاحظة: الإجراء التالي مخصص لمكبس آلي أحادي الجانب يحتوي على مستشعر نشاف داخلي (يمكن أيضا النشاف اليدوي من جانب واحد في جهاز الغمر الآلي الآخر)
- قم بإعداد قطرتين من 50 ميكرولتر وقطرة واحدة من 100 ميكرولتر من المخزن المؤقت للعينة (على سبيل المثال ، 50 mM HEPES pH 7.5 ، 50 mM KCl ، 0.5 mM TCEP) على الجانب النظيف من parafilm.
- أعد ترطيب شبكات الستربتافيدين عن طريق لمس قطرتين سعة 50 ميكرولتر واترك الشبكة تطفو على قطرة 100 ميكرولتر من المخزن المؤقت للعينة لمدة 10 دقائق.
- بعد إعادة الترطيب ، التقط الشبكة باستخدام ملقط مضاد للشعيرات الدموية بحيث يكون الذراع الملتوي للملقط المضاد للشعيرات الدموية في الانخفاض.
- امسح المخزن المؤقت الزائد برفق بعيدا عن الجانب وقم بتطبيق 4 ميكرولتر من عينة 75-100 نانومتر بسرعة.
- احتضان العينة في غرفة الرطوبة لمدة 1-5 دقائق.
ملاحظة: مرة أخرى ، ستعتمد أوقات التركيز والحضانة على العينة ويجب تحسينها. يقترح تركيز العينة المقدمة ووقت الحضانة. بالنسبة للعينات ذات التركيزات المنخفضة ، يمكن للمرء أن يحتضن لفترات زمنية أطول و / أو يربط العينة بالشبكات عدة مرات. - قم بإعداد قطرتين 10 ميكرولتر من المخزن المؤقت للتجميد (على سبيل المثال ، 50 mM HEPES pH 7.5 ، 50 mM KCl ، 0.5 mM TCEP ، 3٪ trehalose ، 0.01٪ NP40) على الجانب النظيف من parafilm. بعد الحضانة ، اغسل العينة غير المنضمة عن طريق لمس الشبكة بأول قطرة من المخزن المؤقت للتجميد. قم بإسقاط الشبكة على القطرة الثانية من المخزن المؤقت للتجميد.
- أمسك بسرعة بحافة الشبكة باستخدام الملقط المتصل بالمكبس الآلي أحادي الجانب. امسح المخزن المؤقت الزائد برفق وقم بتطبيق 4 ميكرولتر من المخزن المؤقت للتجميد بسرعة (50 مللي متر HEPES pH 7.5 ، 50 mM KCl ، 0.5 mM TCEP ، 3٪ trehalose ، 0.01٪ NP40) على الشبكة.
- قم بتوصيل الملقط بالمكبس الآلي أحادي الجانب. تم الحصول على أفضل النتائج باستخدام مستشعر البقع الذي يكتشف انخفاض السائل على الشبكة مع أوقات لطخة تتراوح بين 4-6 ثوان. ستختلف الظروف حسب العينة والمخزن المؤقت المستخدم.
6. معالجة البيانات من أفلام cryo-EM التي تم جمعها من شبكات تقارب الستربتافيدين
يمكن إجراء جمع البيانات على شبكات تقارب الستربتافيدين كما هو الحال مع الشبكات القياسية ، ولا يلزم إجراء تعديلات مجهرية خاصة. ومع ذلك ، فإن الإجراء المفصل هنا يزيل إشارة الستربتافيدين فقط بعد تصحيح حركة الصورة المجهرية. لذلك ، لا يمكن تنفيذ خطوات معالجة البيانات مثل تلميع الجسيمات التي تعتمد على إطارات الأفلام الأصلية بشكل موثوق. يتطلب طرح إشارة streptavidin (مطلوب لجميع عمليات المعالجة النهائية القياسية باستثناء تقدير CTF) هنا إصدار Matlab R2014b أو أحدث يعمل على بيئة Linux. يعتمد طرح الإشارة على الطبيعة البلورية لطبقة الستربتافيدين ، والتي تسمح بإخفاء الذروة ، وبالتالي إزالة الإشارة من تحويل فورييه لكل صورة مجهرية.
- إعداد البرامج النصية للمعالجة
- انسخ جميع الملفات من الملفات التكميلية إلى مجلد مخصص داخل دليل المشروع
- قم بإعداد دليل يسمى processing_scripts يتضمن الملفات التالية:
lsub.m (ملف الترميز التكميلي 1 ؛ نص الطرح)
process_subtration.sh (ملف الترميز التكميلي 2 ؛ برنامج نصي مغلف يتكرر فوق جميع الصور المجهرية المتاحة ، ويولد وظائف متوازية ، ويتتبع المدخلات والمخرجات)
process_subtraction.cfg (ملف الترميز التكميلي 3؛ ملف التكوين الذي يحتوي على معلمات مهمة الطرح، راجع 6.2) - قم بإعداد دليل يسمى support_scripts يتضمن الملفات التالية:
bg_drill_hole.m (ملف الترميز التكميلي 4)
bg_FastSubtract_standard.m (ملف الترميز التكميلي 5)
bg_Pick_Amp_masked_standard.m (ملف الترميز التكميلي 6)
bg_push_by_rot.m (ملف الترميز التكميلي 7)
ReadMRC.m (ملف الترميز التكميلي 8)
WriteMRC.m (ملف الترميز التكميلي 9)
WriteMRCHeader.m (ملف الترميز التكميلي 10)
- اضبط ملف التكوين حسب الحاجة (process_subtraction.cfg ، (راجع الشكل 3) حسب الحاجة:
- الإدخال: المسار إلى الدليل الذي يحتوي على الصور المجهرية المصححة للحركة بتنسيق mrc. استخدم إما دليلا أو نمطا يتضمن أحرف بدل (؟، *).
مثل:
الإدخال = "/ المسار / إلى / project_directory / الصور المجهرية /"
أو
الإدخال = "/ المسار / إلى / project_directory / الصور المجهرية / * .mrc" - output_dir: المسار إلى الدليل الذي يجب أن تكتب إليه الصور المجهرية المطروحة من الشبكة.
- only_do_unfinished: حدد (صواب|خطأ) ما إذا كان يجب الكتابة فوق الصور المجهرية المطروحة الموجودة مسبقا أو تخطيها. هذه المعلمة مفيدة لبدء البرنامج النصي للطرح الشبكي في منتصف جلسة المجهر (الافتراضي: صواب).
- num_parallel_jobs: حدد عدد الوظائف المتوازية. يعتمد هذا الرقم على مواصفات الأجهزة المستخدمة للمعالجة ويجب ألا يكون أعلى من عدد النوى المتاحة. في الأنظمة التي تحتوي على 32 مركزا ونظام ملفات الشبكة ، تم تحقيق الأداء الأمثل من خلال 14 مهمة متوازية. للحصول على أفضل أداء، قم بتحسين هذه القيمة باستخدام مجموعة فرعية من الصور المجهرية.
- Pad_Origin_X: 200 لكاشف K3 في الاتجاه الرأسي (عرض الصورة < ارتفاع الصورة) أو عند استخدام كاشف مربع (Falcon III ، Falcon IV ، K2) ، 1000 لكاشف K3 في الاتجاه الأفقي (عرض الصورة > ارتفاع الصورة). يتم تنفيذ FFT في صناديق مربعة والحشو مطلوب إذا كان الكاشف له أبعاد غير مربعة.
- Pad_Origin_Y: 1000 لكاشف K3 في الاتجاه الرأسي (عرض الصورة < ارتفاع الصورة) ، 200 عند استخدام كاشف مربع (Falcon III ، Falcon IV ، K2) أو في حالة استخدام كاشف K3 في الاتجاه الأفقي (عرض الصورة > ارتفاع الصورة).
- لا تقم بتغيير Inside_Radius_Ang (90) و Outside_Radius_Ang (3.0). يتم إجراء الطرح الشبكي بين قرارين (الوحدة في أنجستروم).
- Pixel_Ang: قم بتوفير حجم البكسل كقيمة فاصلة عائمة.
- العتبة: قيمة قطع عتبة الطرح لاستبدال الشبكة بالخلفية في مساحة فورييه. تتراوح القيم المستخدمة بنجاح بين 1.4-1.6. استخدم 1.42 كنقطة بداية.
- لا تقم بتغيير expand_pixel (10) و pad_out_opt (0). expand_pixel هي قيمة قطر تستخدم للإخفاء حول البيكسلات ذات القيم الأعلى من الحد الأدنى. pad_out_opt هو خيار يقرر ما إذا كانت منطقة مبطنة مضمنة في الإخراج.
- addpath_m: المسار إلى البرامج النصية للدعم.
- path_to_matlab_bin: المسار إلى دليل سلة تثبيت Matlab الخاص بالنظام.
- path_matlab_script: المسار إلى البرنامج النصي لطرح matlab (lsub.m) الذي تم نسخه أعلاه ضمن الخطوة 6.1.2.
- الإدخال: المسار إلى الدليل الذي يحتوي على الصور المجهرية المصححة للحركة بتنسيق mrc. استخدم إما دليلا أو نمطا يتضمن أحرف بدل (؟، *).
- بعد حفظ البرنامج النصي المعدل ، قم بتشغيل البرنامج النصي (bash ./process_subtraction.sh ) لطرح إشارة الستربتافيدين من الصور المجهرية للإدخال. يمكن مقاطعة البرنامج النصي و / أو إعادة تشغيله إذا تم تعيين only_do_unfinished المعلمة إلى true (انظر في الخطوة 6.2.3). في حالة حدوث خطأ ، راجع المعلمات المحددة في البرنامج النصي bash. تأكد من عدم وجود مسافات غير مقصودة بين متغيرات المعلمات والقيم المخصصة لها ، لأن هذا مصدر شائع للأخطاء.
- استخدم الصور المطروحة الشبكية لمعالجة الصور القياسية cryo-EM.
النتائج
بعد تبخر الكربون في الخطوة 3.21 (عادة بعد أسبوع واحد) ، يمكن استخدام شبكات تقارب الستربتافيدين لتحضير عينة cryo-EM أو البقع السالبة باتباع الإجراءات الموضحة في الخطوتين 4 و 5. يظهر في الشكل 4 أ صورة مجهرية تمثيلية تم التقاطها باستخدام كاشف K3 على عملاق Krios عند تكبير 81000X بحجم بكسل 1.05 Å لعينة بيوتينيل مجمدة بشبكات تقارب الستربتافيدين. لوحظ تكوين شعرية ناجح من خلال نمط الشبكة المستمر الذي يظهر في خلفية الصورة. يمكن ملاحظة ذلك بسهولة أكبر من خلال نمط الحيود الذي يظهر في تحويل فورييه السريع (FFT) الموضح في الشكل 4A (يمين). بعد جمع البيانات ، باتباع الإجراء الموضح في الخطوة 6 من هذا البروتوكول ، يمكن إخفاء الإشارة التي تساهم بها شبكة الستربتافيدين في الصورة حسابيا لإنتاج صورة مجهرية مطروحة (الشكل 4 ب) يمكن استخدامها لخطوات معالجة البيانات اللاحقة. يوضح FFT في الشكل 4B (يمين) أن نمط الحيود الملاحظ في الشكل 4A (يمين) قد تمت إزالته بنجاح من الصورة الأصلية.
يوضح الشكل 4C مثالا على صورة مجهرية مأخوذة على مجهر Tecnai 12 بتكبير 49000x بحجم بكسل 1.6 Å لعينة بيوتينيل مرتبطة بشبكات تقارب الستربتافيدين وملطخة سلبا باستخدام فورمات اليورانيل. تم إعداد الشبكات باتباع الإجراء الموضح في الخطوة 4 من هذا البروتوكول ، تاركة طبقة سميكة من البقع.
هناك العديد من الملاحظات الشائعة عندما يكون إجراء تصنيع شبكة الستربتافيدين غير ناجح والتي تم وصفها بمزيد من التفصيل في قسم المناقشة والجدول 1. الشكل 5 عدة أمثلة على هذه الملاحظات. يوضح الشكل 5 أ صورة مجهرية لشبكة تقارب ستربتافيدين ملطخة سالبا مستخدمة من دفعة عمرها أكثر من ستة أشهر. تم تعبئة الطبقة الأحادية من الثقوب الموجودة في رقائق الكربون لشبكات quantifoil ولوحظ بأبعاد مماثلة للثقوب الموجودة في الشبكة. يوضح الشكل 5B مثالا على بلورات الستربتافيدين ذات الفسيفساء العالية التي تصبح مضطربة بسهولة أثناء إجراءات تحضير العينة. يوضح الشكل 5 ج صورة مجهرية تمثيلية من شبكة تقارب الستربتافيدين يكون فيها تبخر الكربون في الخطوة 3.21 رقيقا جدا أو محذوفا. أصبحت شبكة الستربتافيدين مجزأة أثناء عملية تحضير عينة cryo-EM. يوضح الشكل 5D شبكة تقارب الستربتافيدين الملطخة سلبا والتي تحتوي على تلوث من الحويصلات الدهنية ، ويرجع ذلك على الأرجح إلى عدم كفاية عمليات الغسيل خلال الخطوة 3.13 أو أن الجانب الذهبي من الشبكة يصبح رطبا خلال الخطوات 3.13-3.20. يرجى الرجوع إلى قسم المناقشة والجدول 1 للاطلاع على استراتيجيات التغلب على هذه المشكلات الشائعة.
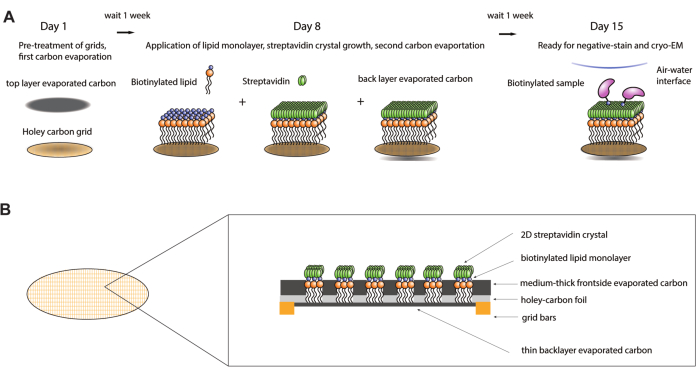
الشكل 1: رسم تخطيطي لإجراء تصنيع شبكة تقارب الستربتافيدين. (أ) نظرة عامة على الجدول الزمني لإجراء تصنيع شبكة تقارب الستربتافدين. يمكن إكمال الإجراء بأكمله على مدار أسبوعين يتطلب خطوتين لتبخر الكربون وأسبوع واحد بعد كل منهما للسماح للكربون بالتقدم في العمر بشكل كاف. (B) تم تكبيره في عرض مربع شبكي لشبكة تقارب ستربتافيدين تظهر الطبقات التي تشكل الشبكة بعد الانتهاء من عملية التصنيع ، بما في ذلك شبكة cryo-EM القياسية مع قضبان ذهبية وفيلم كربون هولي ، وأول طبقة كربون متبخرة ، وطبقة أحادية دهنية ، وبلورة 2D-streptavidin ، وطبقة دعم الكربون المتبخر الخلفية. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 2: بلورة الليبيدات أحادية الطبقة والستربتافيدين (A) صور توضح كيفية تكوين الطبقة الأحادية للدهون بنجاح داخل طبق بتري الصغير باستخدام بودرة التلك لإنشاء حدود لزيت الخروع الذي يخلق ضغطا سطحيا ثابتا أثناء تكوين الطبقة الأحادية لليبيدات. (ب) صور توضح كيفية نمو بلورات الستربتافيدين على شبكات cryo-EM. أولا ، يتم لمس جانب الكربون من الشبكات إلى الطبقة الأحادية الدهنية ويتبعه ثلاث غسلات متتالية في المخزن المؤقت للتبلور. يضاف الستربتافيدين ، ويتم تحضين الشبكات في غرفة الرطوبة لمدة 2 ساعة. الرجاء الضغط هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 3: مثال على معلمات ملف process_subtraction.cfg لإجراء طرح شبكة الستربتافيدين من الصور المجهرية (الخطوة 6). يرجى النقر هنا لعرض نسخة أكبر من هذا الشكل.

الشكل 4: النتائج التمثيلية لتصنيع شبكة تقارب الستربتافيدين الناجحة. (أ) صورة مجهرية بالتبريد EM لمجمعات البروتين / النيوكليوسوم البيوتينيل المحضرة بشبكات تقارب الستربتافيدين محلية الصنع. يظهر FFT على اليمين ويظهر نمط حيود بلورة الستربتافيدين. (B) تظهر نفس الصورة المجهرية الموجودة في اللوحة A بعد إجراء الطرح الشبكي لإزالة الإشارة من بلورة الستربتافيدين 2D من الصورة الأصلية. (ج) مثال على صورة مجهرية تم الحصول عليها من تلطيخ سلبي لعينة بيوتينيل مرتبطة بشبكات ميل الستربتافيدين . يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.

الشكل 5: النتائج التمثيلية لتصنيع شبكة تقارب الستربتافيدين غير الناجحة. (أ) صورة مجهرية توضح تعبئة الطبقة الأحادية للستربتافيدين من ثقوب الشبكة عندما يكون عمر الشبكات أكثر من ستة أشهر. (B) صورة مجهرية توضح شبكات الستربتافيدين ذات الفسيفساء العالية التي تتلف بسهولة أثناء إجراءات تحضير العينات بالتبريد EM والبقع السالبة. (ج) صورة مجهرية توضح تجزئة شبكة الستربتافيدين أثناء تحضير عينة cryo-EM عندما تكون طبقة تبخر الكربون في الخطوة 3.21 رقيقة جدا أو محذوفة. (د) صورة مجهرية تمثيلية ملوثة بحويصلات دهنية على الأرجح بسبب عدم كفاية الغسيل أثناء الخطوة 3.13 أو تبلل الجانب الذهبي من الشبكة خلال الخطوات 3.13-3.20. يرجى النقر هنا لعرض نسخة أكبر من هذا الرقم.
الجدول 1: دليل استكشاف الأخطاء وإصلاحها للتغلب على التحديات الشائعة التي تتم مواجهتها أثناء تصنيع شبكة تقارب الستربتافيدين غير الناجح. الرجاء الضغط هنا لتنزيل هذا الجدول.
ملف الترميز التكميلي 1: lsub.m الرجاء النقر هنا لتنزيل هذا الملف.
ملف الترميز التكميلي 2: process_subtration.sh الرجاء النقر هنا لتنزيل هذا الملف.
ملف الترميز التكميلي 3: process_subtraction.cfg الرجاء الضغط هنا لتنزيل هذا الملف.
ملف الترميز التكميلي 4: bg_drill_hole يرجى النقر هنا لتنزيل هذا الملف.
ملف الترميز التكميلي 5: bg_FastSubtract_standard.m الرجاء النقر هنا لتنزيل هذا الملف.
ملف الترميز التكميلي 6: bg_Pick_Amp_masked_standard صباحا الرجاء النقر هنا لتنزيل هذا الملف.
ملف الترميز التكميلي 7: bg_push_by_rot.m الرجاء النقر هنا لتنزيل هذا الملف.
ملف الترميز التكميلي 8: ReadMRC.m الرجاء النقر هنا لتنزيل هذا الملف.
ملف الترميز التكميلي 9: WriteMRC.m الرجاء الضغط هنا لتنزيل هذا الملف.
ملف الترميز التكميلي 10: WriteMRCHeader.m الرجاء النقر هنا لتنزيل هذا الملف.
Discussion
يصف بروتوكولنا كيفية صنع واستخدام شبكات تقارب الستربتافيدين وكيفية معالجة البيانات التي تحتوي على إشارة حيود الستربتافيدين. هناك العديد من الخطوات الحاسمة في البروتوكول التي تتطلب اهتماما خاصا.
يمكن إرجاع دفعات الشبكة غير الناجحة إلى العديد من الأخطاء الشائعة. المصدر الأكثر شيوعا للخطأ يأتي من استخدام الكواشف القديمة أو ذات الجودة الرديئة. من المهم بشكل خاص تحضير محلول الدهون البيوتينيلية تماما كما هو موضح في البروتوكول. علاوة على ذلك ، يمكن أن تؤثر أي شوائب ، مثل بقايا المنظفات على أدوات المختبر أو الزيوت الموجودة بشكل طبيعي على الجلد ، على جودة بلورات الستربتافيدين ، وبالتالي جودة الصور الناتجة. لذلك يوصى بإجراء ثلاث دورات غسيل للشبكات قبل تبخر الكربون الأول لإزالة التلوث المحتمل بالسطح من الشركة المصنعة للشبكة (الخطوة 2.1). بالإضافة إلى ذلك ، لوحظ تلوث أو شوائب زيت الخروع لإعاقة تكوين البلورات على الشبكة.
يعد صنع الطبقة الأحادية الدهنية والتقاطها مهمة يجب ممارستها عدة مرات للتعرف على أحجام الدهون الصغيرة. ليس من غير المعتاد أن تفشل هذه الخطوة في أول مرتين أو ثلاث مرات قبل أن يتم إنتاج طبقة أحادية دهنية كافية ، كما ينعكس في النهاية في جودة بلورات الستربتافيدين التي تظهر في شبكات ملطخة سلبا (الشكل 4C).
من المهم ألا تدع الجانب الخلفي (الجانب الذهبي ، الجانب الدهني) من الشبكة يبلل أثناء عملية تصنيع الشبكة (الخطوات 3.12-3.20). في حالة تبلل المؤخر ، يوصى بتجاهل الشبكة. يمكن أن يؤدي ذلك إلى ظهور حويصلات دهنية كبيرة تعطل جودة الصورة (الشكل 5D) (الصف 3 ، الجدول 1). يمكن أيضا ملاحظة الحويصلات الدهنية بسبب عدم كفاية الغسيل بعد تطبيق الطبقة الأحادية الدهنية (الخطوة 3.13). يوصى بثلاث غسلات لاحقة باستخدام محلول التبلور بعد لمس الطبقة الأحادية الدهنية قبل إضافة الستربتافيدين.
بعد تبخير طبقة رقيقة من الكربون على شبكات مدمجة في الترهالوز ، يمكن أن يكون الجانب الخلفي من الشبكة رطبا دون الإضرار بجودة الشبكة. على سبيل المثال ، يتم ملاحظة ترطيب المؤخر بشكل متكرر عندما يحتوي المخزن المؤقت للعينة على كميات قليلة من المنظفات. يمكن أن يؤدي ترطيب المؤخرة بواسطة العينة إلى ارتباط غير محدد للعينات بطبقة الكربون الرقيقة على الجانب الخلفي ، مما يقلل من فعالية منع الجسيمات من الانتشار إلى واجهة الهواء والماء أو استخدام ربط التقارب لاستراتيجيات التنقية على الشبكة. إذا أمكن ، أضف العينة إلى الشبكة في حالة عدم وجود منظف. يمكن إضافة المنظفات والمواد المضافة الأخرى لاحقا أثناء خطوات غسل الشبكة أو إضافتها في خطوة أخيرة قبل التزجيج. هذا هو أحد القيود على استخدام شبكات تقارب الستربتافيدين ؛ ومع ذلك ، إذا كان الهدف هو تحسين التوجه التفضيلي ، فقد تم إجراء تحضير العينة باستخدام المخازن المؤقتة ، بما في ذلك المنظفات ، بنجاح11.
يمكن تتبع مصدر الخطأ الشائع إلى عمر الشبكات بالنسبة إلى كل من خطوات تبخر الكربون (الخطوة 2.3 والخطوة 3.21). في هذا البروتوكول ، تكون فترة الانتظار الموصى بها هي 5-7 أيام بعد تبخر الكربون الخلفي قبل استخدام شبكات الستربتافيدين ل cryo-EM. عندما يتم استخدام الشبكات في وقت مبكر جدا بعد التصنيع ، لوحظ أن الطبقة الأحادية الشبكية والدهون تحشد خارج ثقوب الشبكة. يمكن إجراء ملاحظة مماثلة عندما تكون الشبكات قديمة جدا وتستخدم بعد ستة أشهر (الشكل 5 أ) (الصف 1 ، الجدول 1). نفترض أن هذه الملاحظة تفسر بالتغيرات في الكارهة للماء لدعامة الكربون التي يتم تطبيقها لتثبيت بلورات الدهون أحادية الطبقة والستربتافيدين. بالإضافة إلى ذلك ، قد تظهر شبكات الستربتافيدين فسيفساء (الشكل 5 ب) (الصف 3 ، الجدول 1) ومكسورة في كل من البقع السالبة و cryo-EM إذا تم تطبيق الطبقة الأحادية على الشبكات حيث لم تتقدم طبقة تبخر الكربون الأولى (الخطوة 2.3) بما فيه الكفاية.
يمكن إرجاع مصدر شائع إضافي للخطأ إلى هشاشة الطبقة الأحادية البلورية للستربتافيدين (الطبقة الأحادية الدهنية هي نفسها سائلة ويمكن أن تتوسع أو تضغط بشكل عكسي). يوفر تبخر الكربون الخلفي (الخطوة 3.21) ثباتا حرجا لكل من الشبكة أحادية الطبقة والستربتافيدين أثناء عملية امتصاص العينة والغسيل ونشاف cryo-EM. في حالة عدم وجود تبخر كاف للكربون إلى الجانب الخلفي من الشبكة ، غالبا ما تظهر شبكات الستربتافيدين مجزأة بعد النشاف / التجميد (الشكل 5C) (الصف 2 ، الجدول 1). في هذا البروتوكول ، نقترح استخدام فريزر غطس أوتوماتيكي من جانب واحد للنشاف من جانب واحد. تنتج هذه الطريقة ظروف نشاف قابلة للتكرار بدرجة عالية تحافظ على شبكة الستربتافيدين أثناء عملية التجميد وتسمح بالتحسين المبسط لتطبيق العينة ومعلمات النشاف. بدلا من ذلك ، تم استخدام أجهزة التجميد الآلي الأخرى مع النشاف اليدوي. للقيام بذلك ، يتم تعطيل وظيفة النشاف الفعلية في إعدادات الجهاز ، ويتم مسح الشبكة بدلا من ذلك عن طريق الوصول إلى زوج من الملقط يحمل الورق النشاف من خلال المدخل الجانبي. يمكن أن تحقق هذه الطريقة نتائج عالية الجودة للمختبرات بدون جهاز نشاف وتجميد من جانب واحد ؛ ومع ذلك ، فإن قابلية التكاثر من شبكة إلى شبكة تمثل تحديا.
في حين أن استخدام شبكات تقارب الستربتافيدين له العديد من المزايا ، يجب مراعاة بعض قيود هذه الطريقة. نظرا لطبيعة الإجراء ، لا يمكن عادة تقييم جودة شبكة الستربتافيدين حتى تكتمل العملية بأكملها. يقترح فحص جودة كل دفعة بسرعة عن طريق البقعة السلبية قبل تجميد العينات. نظرا للإشارة التي تساهم بها شبكة الستربتافيدين في الصور الخام ، قد يكون من الصعب في بعض الحالات تقييم ، من الصور وحدها ، ما إذا كان هناك عدد كاف من الجسيمات السليمة والمشتتة. للسبب نفسه ، لا يمكن معالجة بيانات cryo-EM أثناء الحصول على البيانات أثناء الحصول على البيانات ما لم يتم تضمين إجراء طرح إشارة الستربتافيدين في خط أنابيب المعالجة المسبقة للبيانات. نظرا لأن إشارة الستربتافيدين عادة ما يتم طرحها من الصور المصححة للحركة وليس الإطارات نفسها ، فقد يفشل تلميع Bayesian ، كما هو مطبق في مجموعات البرامج الشائعة ، عند استخدام إجراءات الطرح كما هو موضح. لذلك يوصى بإجراء تصحيح الحركة في بقع متعددة لتقليل حركة الجسيمات من بداية معالجة البيانات16.
على الرغم من هذه القيود ، توفر شبكات تقارب الستربتافيدين العديد من المزايا. هناك ميزتان رئيسيتان توفرهما شبكات تقارب الستربتافيدين على شبكات cryo-EM القياسية ذات الفتحة المفتوحة وهما وسيلة لحماية العينات من واجهة الهواء والماء وتركيز العينات ذات الوفرة المنخفضة (10-100 نانومتر) على الشبكة. يمكن أيضا استخدام طبقات الدعم الأخرى ، مثل أكسيد الكربون والجرافين ، كاستراتيجيات للتغلب على اختناقات تحضير العينات. في أحد الأمثلة ، كانت شبكات تقارب الستربتافيدين هي الحل الوحيد للحصول على إعادة بناء سليمة لتفاعل البروتين والحمض النووي الذي كان غير متوافق مع نهج الربط المتقاطع. 12
ميزة رئيسية أخرى توفرها شبكات تقارب الستربتافيدين هي حل للعينات التي تمتز لطبقات الدعم الأخرى ، مثل أكسيد الكربون أو الجرافين ، مع الاتجاهات المفضلة التي تعيق القدرة على الحصول على إعادة بناء 3D للعينة ذات الاهتمام. يسمح البيوتينيل العشوائي للعينات باستخدام مجموعات متاحة تجاريا بالتعلق العشوائي للعينة ذات الأهمية بطبقة الستربتافيدين الأحادية للحصول على المزيد من المشاهدات المحتملة للتغلب على هذا التحدي.
بالإضافة إلى ذلك ، توفر شبكات تقارب الستربتافيدين مزايا فريدة للشبكات القائمة على التقارب. يسمح التقارب العالي وخصوصية تفاعل الستربتافيدين والبيوتين باقتران شبكات تقارب الستربتافيدين مع تدفقات العمل الأخرى التي تتضمن البيوتين لتنقية المجمعات ذات الأهمية. في أحد الأمثلة المنشورة ، قام المؤلفون بشل حركة مجمع على شبكات تقارب الستربتافيدين واحتضان شريكا ملزما للقياس المتكافئ غير المعروف بفائض كبير. بعد غسل أي بروتين غير منضم ، تم الحصول على المركب الفائق الذي تم تجميعه بشكل صحيح ويمكن تحليله على الفور باستخدام cryo-EM11. قد يكون أحد التطبيقات المستقبلية المحتملة هو الجمع بين علامات البروتين المرتبطة بالستربتافيدين ، أو نظام Avi-tag ، أو نهج وضع العلامات القريبة مع شبكات تقارب الستربتافيدين لاستخراج البروتينات المفردة و / أو مجمعات البروتين مباشرة من المصادر المؤتلفة أو الداخلية دون مخططات تنقية قياسية مفصلة.
من خلال توفير هذا البروتوكول ، يجب أن تكون المختبرات قادرة على إعادة إنتاج تصنيع شبكات تقارب الستربتافيدين بسهولة وتأسيسها كأداة أكثر استخداما للتحليل الهيكلي لمجمعات البروتين بواسطة cryo-EM.
Disclosures
اي.
Acknowledgements
تم دعم T.C. من قبل المعهد الوطني للعلوم الطبية العامة منحة التدريب على الفيزياء الحيوية الجزيئية GM-08295 وزمالة أبحاث الدراسات العليا لمؤسسة العلوم الوطنية بموجب رقم المنحة DGE 2146752. تم دعم R.G. و B.H. من خلال منحة المعهد الوطني للصحة R21-GM135666 الممنوحة ل R.G. و B.H. تم تمويل هذا العمل جزئيا من خلال منحة المعهد الوطني للعلوم الطبية العامة R35-GM127018 الممنوحة ل E.N. E.N. هو محقق في معهد هوارد هيوز الطبي.
Materials
| Name | Company | Catalog Number | Comments |
| 1,2-dipalmitoyl-sn-glycero-3- phosphoethanolamine-N-(biotinyl) sodium salt | Avanti Polar Lipids | 870285P | Comes as a powder. Dissolve at concentration of 1–10 mg/mL in chloroform/methanol/water solvent, 65:35:8 v/v and store in single use aliquots at -80 °C |
| 200 proof pure ethanol | Fisher Scientific | 07-678-005 | |
| 5 μL Hamilton Syringe | Hamilton | 87930 | 5 µL Microliter Syringe Model 75 RN, Small Removable Needle, 26 G, 2 in, point style 2 |
| Castor Oil | Sigma Adrich | 259853 | |
| Cell culture dishes untreated (35 mm) | Bio Basic | SP22146 | |
| Chloroform | Sigma Aldrich | 650471 | |
| D-(+)-Trehalose dihydrate,from starch, ≥99% | Sigma Aldrich | T9449 | |
| DUMONT Anti-Capillary Reverse (self-closing) Tweezers Biology Grade | Ted Pella | 510-5NM | |
| HPLC Grade Methanol | Fisher Scientific | A452-4 | |
| Leica EM ACE600 High Vacuum Sputter Coater | Leica | ||
| Leica EM GP2 Automatic Plunge Freezer | Leica | ||
| Quantifoil R 2/1 Au300 | Quantifoil | Q84994 | |
| Steptavidin | New England Bioscience | N7021S | Comes as 1 mg/mL solution. Dilute to final concentration of 0.5 mg /mL in crystallization bufferwith a final trehalose concentration of 10%. Can be flash frozen in 25–50 μL aliquots |
| Talcum powder | Carolina | 896060 | |
| Whatman Grade 1 filter paper | Cytiva | 1001-085 |
References
- Glaeser, R. M., Nogales, E., Chiu, W. . Single-particle Cryo-EM of Biological Macromolecules. IOP Publishing. , (2021).
- Carragher, B., et al. Current outcomes when optimizing 'standard' sample preparation for single-particle cryo-EM. Journal of Microscopy. 276 (1), 39-45 (2019).
- Drulyte, I., et al. Approaches to altering particle distributions in cryo-electron microscopy sample preparation. Acta Crystallographica Section D-Structural Biology. 74, 560-571 (2018).
- Noble, A. J., et al. Routine single particle cryoEM sample and grid characterization by tomography. eLife. 7, e34257 (2018).
- Patel, A., Toso, D., Litvak, A., Nogales, E. Efficient graphene oxide coating improves cryo-EM sample preparation and data collection from tilted grids. bioRxiv. , (2021).
- Wang, F., et al. General and robust covalently linked graphene oxide affinity grids for high-resolution cryo-EM. Proceedings of the National Academy of Sciences. 117 (39), 24269-24273 (2020).
- Pantelic, R. S., Meyer, J. C., Kaiser, U., Baumeister, W., Plitzko, J. M. Graphene oxide: A substrate for optimizing preparations of frozen-hydrated samples. Journal of Structural Biology. 170 (1), 152-156 (2010).
- Williams, R. C., Glaeser, R. M. Ultrathin carbon support films for electron microscopy. Science. 175 (4025), 1000-1001 (1972).
- Han, B. -. G., et al. Long shelf-life streptavidin support-films suitable for electron microscopy of biological macromolecules. Journal of Structural Biology. 195 (2), 238-244 (2016).
- Han, B. -. G., et al. Electron microscopy of biotinylated protein complexes bound to streptavidin monolayer crystals. Journal of Structural Biology. 180 (1), 249-253 (2012).
- Domínguez-Martín, M. A., et al. Structures of a phycobilisome in light-harvesting and photoprotected states. Nature. 609 (7928), 835-845 (2022).
- Kasinath, V., et al. JARID2 and AEBP2 regulate PRC2 in the presence of H2AK119ub1 and other histone modifications. Science. 371 (6527), eabc3393 (2021).
- Lahiri, I., et al. 3.1 structure of yeast RNA polymerase II elongation complex stalled at a cyclobutane pyrimidine dimer lesion solved using streptavidin affinity grids. Journal of Structural Biology. 207 (3), 270-278 (2019).
- Marr, C. R., Benlekbir, S., Rubinstein, J. L. Fabrication of carbon films with ~ 500nm holes for cryo-EM with a direct detector device. Journal of Structural Biology. 185 (1), 42-47 (2014).
- Levine, M. J., Schwarz, J. A. Experimental guidelines for producing molecular assemblies by Langmuir-Blodgett techniques. Journal of Chemical Education. 65 (7), 638 (1988).
- Zheng, S. Q., et al. MotionCor2: anisotropic correction of beam-induced motion for improved cryo-electron microscopy. Nature Methods. 14 (4), 331-332 (2017).
Reprints and Permissions
Request permission to reuse the text or figures of this JoVE article
Request PermissionExplore More Articles
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. All rights reserved