3.9 : 化学式的实验确定
化合物的元素组成定义其化学特征,化学式是表示该元素组成的最简洁的方法。当未知某个化合物的公式时,测量其组成元素的质量通常是通过实验确定该公式的第一步。
经验公式的确定
确定化合物化学式的最常见方法是首先测量其组成元素的质量。但是,化学式表示的是物质中原子的相对数,而不是原子的质量。因此,必须使用任何涉及质量的实验数据来获得化合物中相应的原子数。这是通过使用摩尔质量将每个元素的质量转换为其摩尔数来实现的。这些摩尔量用于计算可用于得出物质经验公式的整数比。
考虑一种化合物样品,确定其含有1.71克碳和0.287克氢。相应的原子数是0.142摩尔的碳和0.284摩尔的氢。因此,该化合物可以由式C 0.142 H 0.284 表示。按照惯例,公式包含整数下标,可以通过将每个下标除以最小的下标(0.142)来实现。因此,该化合物的经验公式为CH 2 。下标" 1"如果没有其他数字,则不写,而是假设。这可以是化合物的分子式,也可以不是。但是,需要额外的信息来进行该确定。
作为第二实例,确定化合物样品含有5.31克氯和8.40克氧。用同样的方法得出ClO 3.5 的实验经验公式。在这种情况下,除以最小下标仍会在经验公式中保留小数点。要将其转换为整数,请将每个下标乘以2,保持相同的原子比,并得出Cl 2 O 7 作为最终的经验公式。
在化合物的百分比组成可用的情况下,它用于计算化合物中存在的元素的质量。由于百分比刻度为100,因此可以方便地计算重量为100克的样品中存在的元素的质量。获得的质量可用于得出经验公式。
例如,假设一种气体化合物包含27.29%的C和72.71%的O。因此,质量百分比用分数表示:
确定组成一个共价化合物的单个分子的原子的绝对数量需要了解其经验式以及其分子质量或摩尔质量。这些量可以通过各种测量技术实验确定。例如,分子质量通常来自化合物的质谱图。
通过将化合物的摩尔质量或分子质量与其经验式质量进行比较,得出分子式。顾名思义,经验公式质量是经验公式中表示的所有原子的平均原子质量的总和。如果将物质的已知摩尔质量除以经验公式质量,则得出每个分子的经验公式单位数( n )。
然后通过将经验公式中的每个下标乘以 n 来获得分子式,如通用经验公式A x B y :
例如,将共价化合物的经验式确定为CH 2 O,并且其经验式质量约为30 amu。 如果确定该化合物的分子量为180 amu,则表明该化合物的分子中所含原子数是经验式中表示的原子数的六倍。
该化合物的分子由一个分子式表示,其下标比经验式大6倍:(CH 2 O) 6 = C 6 H 12 O 6 。
从组成百分比导出经验公式

 碳的质量27.29 g对应于2.272摩尔的碳,氧的质量72.71 g对应于4.544摩尔的氧。因此,代表性的公式是C 2.272 O 4.544 。将每个下标除以2.272可提供经验公式:CO 2 。
碳的质量27.29 g对应于2.272摩尔的碳,氧的质量72.71 g对应于4.544摩尔的氧。因此,代表性的公式是C 2.272 O 4.544 。将每个下标除以2.272可提供经验公式:CO 2 。
分子式的推导
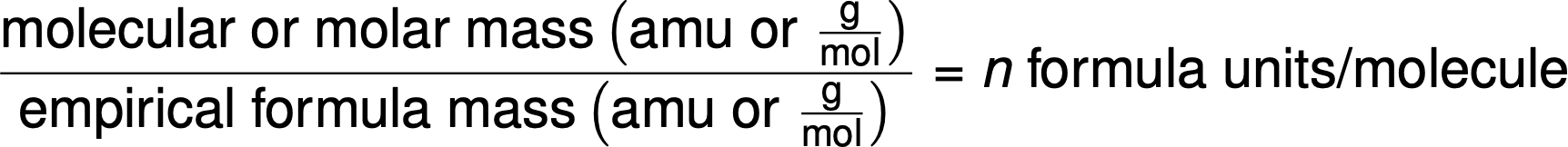
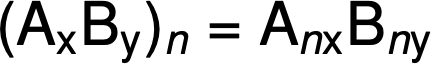
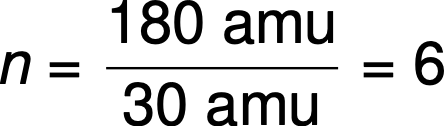
来自章节 3:

Now Playing
3.9 : 化学式的实验确定
化学量和水溶液反应
37.3K Views

3.1 : 分子和化合物
化学量和水溶液反应
53.3K Views

3.2 : 化学配方
化学量和水溶液反应
48.7K Views

3.3 : 分子模型
化学量和水溶液反应
37.6K Views

3.4 : 元素和化合物的分类
化学量和水溶液反应
65.1K Views

3.5 : 离子化合物:分子式和术语
化学量和水溶液反应
66.1K Views

3.6 : 分子化合物:分子式和名称
化学量和水溶液反应
42.6K Views

3.7 : 有机化合物
化学量和水溶液反应
50.8K Views

3.8 : 化合物的分子质量和摩尔概念
化学量和水溶液反应
64.2K Views

3.10 : 化学方程式
化学量和水溶液反应
62.2K Views
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。