需要订阅 JoVE 才能查看此. 登录或开始免费试用。
Method Article
这些模型在体外间皮间隙检测卵巢癌转移的早期步骤
摘要
这里描述的皮间隙检测,利用荧光标记的细胞和延时视频显微镜,可视化和定量测量卵巢癌多细胞球体和间皮细胞单层的相互作用。此法模拟卵巢癌转移的早期步骤。
摘要
卵巢癌是第五次在美国癌症相关死亡的首要原因。尽管积极的初步反应治疗,70%至90%的卵巢癌的妇女开发新的转移,复发往往是致命的2。因此,有必要的,它是了解出现二次转移,以发展中间和晚期卵巢癌的更好的治疗。卵巢癌转移发生恶性细胞脱离原发肿瘤部位和传播整个腹腔。传播的细胞可以形成多细胞集群,或球体,将保持独立,或者植入到机关内的腹腔(图1,电影1)。
腹腔内的器官全部一字排开用一个单一的,连续的,一层4-6间皮细胞(图2)。然而,间皮细胞是从下面缺席腹膜肿块,切除人体肿瘤组织切片3,5-7(图2)的电子显微镜研究发现。这表明,由一个未知的过程中,间皮细胞排除从下面的肿块。
以前在体外实验表明,原发性卵巢癌的细胞更有效地附加比8间皮细胞外基质,最近的研究表明,原发性腹膜间皮细胞,实际上提供了一个屏障,卵巢癌的细胞粘附和侵袭(相比,黏附和侵袭不包括与间皮细胞)9,10基板上。这表明,间皮细胞对卵巢癌转移的障碍行动。卵巢癌细胞突破这一障碍,排除间皮有细胞和分子机制,直到最近,仍然不明。
在这里,我们描述日e为在体外试验方法,模型与卵巢癌的细胞球体和间皮细胞在体内的相互作用(图3,电影2)。我们的协议是改编自先前所描述的方法,分析卵巢肿瘤细胞的相互作用与8-16皮单层,并首次在报告中显示,卵巢肿瘤细胞利用整合依赖激活的肌球蛋白和牵引力,以促进排除描述从下间皮细胞肿瘤球体17。这种模式需要时间推移荧光显微镜的优势,在实时监控的两个细胞群,提供了空间和时间上的互动信息。卵巢癌的细胞表达红色荧光蛋白(RFP),而间皮细胞表达绿色荧光蛋白(GFP)。 RFP的表达卵巢癌的细胞球体连接到表达GFP的皮单层。球体的蔓延,侵入,迫使除了创造一个洞单层间皮细胞。这个洞是在GFP图像为负空间(黑)的可视化。洞的面积,然后可以测量,控制和卵巢癌和/或间皮细胞的实验种群之间的间隙活动的差异定量分析。此法只需要一个小数目,卵巢癌的细胞(100细胞每球体X 20-30%条件下球体),所以它是可行的,执行此法,采用珍贵的原发肿瘤细胞样本。此外,该法可以很容易地适应高通量筛选。
研究方案
1。卵巢癌的细胞球体的形成
- RFP的表达卵巢癌的细胞培养在10%的基础培养基(自定义的细胞培养液中含有199和一个MCDB105 50:50的混合物,10%的灭活胎牛血清和1%笔链球菌)。来表达RFP的未标记卵巢癌的细胞,转染质粒含有利福平的细胞和细胞表达RFP的选择。另外,病毒载体可用于瞬时表达荧光蛋白或细胞可以预孵育与红色荧光的细胞追踪染料(Invitrogen公司)。
- 对卵巢癌的球体形成之前,有必要准备低96附着力以及圆底培养皿。要产生低附着力文化的板,聚HEMA30μL溶液(1毫升95%乙醇为6mg羟乙酯)被添加到每个井的96康宁细胞培养皿。在37°C非湿润的孵化器,蒸发乙醇,L孵育96孔板eaving对每口井的聚甲基丙烯酸羟乙酯的电影。这种聚甲基丙烯酸羟乙酯的电影阻止细胞附着到井底,迫使18悬浮液中的细胞生长。 [另外,超低的附件培养皿(康宁)可以用聚甲基丙烯酸羟乙酯涂层菜,来代替。]
- 低粘附培养皿准备后,一盘卵巢癌的细胞,颗粒细胞,在3分钟,在900离心力台式离心机(贺利氏)吸上清,重新暂停在10%,相应的中等trypsinize。
- 使用血球细胞计数。
- 调整细胞等有50μl的100个细胞的10%,相应的中等浓度。
- 以及每96聚甲基丙烯酸羟乙酯涂层培养皿均匀悬浮稀释细胞悬液50μL。
- 在37℃16小时细胞培养孵化器(这段时间内应增加或减少所花费的时间取决于孵育96孔板一个特定的细胞株,形成多细胞球体所需的实验条件下),使卵巢癌细胞聚集在一起,形成一个单一的每口井的多细胞球体。在此期间可以接受一些肿瘤细胞凋亡,所以重要的是要选择一个时间,诱导细胞凋亡前。
2。间皮细胞单层形成
- 在细胞培养罩,预涂层井6以及玻璃底部MatTek菜与纤维连接蛋白,加入2mL的每个菜以及一个5μg纤维连接蛋白/毫升PBS溶液,在室温下孵育30分钟。允许高分辨率的显微成像的光学质量的玻璃裤MatTek菜。
- 间皮细胞表达GFP的10%的基础培养基中培养。板皮细胞Trypsinize,旋转,在台式离心机(Heraeus公司)在900RPM 3分钟,吸出上清液,并在10%,相应的中等重新挂起。 “这里所用的皮细胞表达GFP时,他们得到的,但可以通过质粒含有绿色荧光蛋白基因转染,或在绿色荧光的细胞追踪染料(Invitrogen公司)preincubating细胞产生的未标记的间皮细胞。
- 经过30分钟的纤维连接蛋白孵化(步骤2.1),与2毫升PBS洗的水井的MatTek培养皿。
- 吸干PBS和板6×10 5%以及在每个6以及MatTek菜的井间皮细胞。在37℃的细胞培养孵化器一夜之间让皮细胞菜的重视,并形成了单层孵育MatTek菜。
3。间皮细胞间隙分析
- 用吸管收集96以及聚甲基丙烯酸羟乙酯涂层板卵巢癌的球体。
- 从6井MatTek菜含有间皮细胞单层吸介质。用2毫升PBS洗一次。新增的96个以及带够所有的球体迟到的MatTek菜(〜3倍的球体,球体降落成像帐户上的不能成像菜,部分)。
- 放置在一个倒置的宽视场荧光显微镜能够执行持续时间至少8小时的时间推移成像阶段MatTek菜。使用机动的舞台形象在菜的多个位置,多个球体插事件,在一个单一的实验。我们用完美的对焦系统集成和低[20X-0.75数值孔径(NA)的]放大倍率/无微分干涉对比(DIC)光学尼康钛 - E倒置电动广角荧光显微镜的时间推移,与0.52不适用尼康卤素灯透射长工作距离(LWD)冷凝器,尼康快(<100毫秒切换时间)激发和发射滤波器(GFP的前480/40,EM 525/50,RFP-mCherry EX EM 575/50 640/50),萨特快速传播和萤光光路智能关机TERS,尼康线性编码机动阶段,滨松ORCA的银冷却电荷耦合器件(CCD)摄像头,一个定制的显微镜,孵化室温度和CO 2控制,尼康NIS元素AR软件版本,并TMC隔振表。
- 卵巢癌的细胞球体将落户盘底部和重视的间皮细胞单层。 GFP,RFP和相位图20 +球体/单层相互作用,每次10分钟,收集8小时。
- RFP的表达卵巢癌的细胞球体表达GFP创建一个洞单层间皮细胞的单层侵入。 8小时后,测量孔的大小,使用元素的软件(或其他合适的软件,如图像J)在GFP图像跟踪黑洞。孔的大小正常化最初的球体大小,孔的大小,由相应的RFP的图像在时间为零球体的大小除以8小时。在这个前充足的,孔的大小只测一次,但它可以测量整个8小时的实验多次,以便更好地了解动态插。
4。代表结果
在这个例子中,我们比较皮OVCA433卵巢癌的细胞球体,有塔林-1的减毒表达控制OVCA433球体的通关能力。从各组OVCA433球体添加到MatTek菜含有征途间皮细胞单层。从每组六个球体成像八个小时,每10分钟(图4 3,电影,电影4)。单层制作传播球体的孔进行测量和平均从每个组6个职位。图4表明,大林1击倒球体创造的平均清关区显着高于控制球体创造的平均面积小,这表明,大林皮间隙由OVCA433卵巢癌的球体。
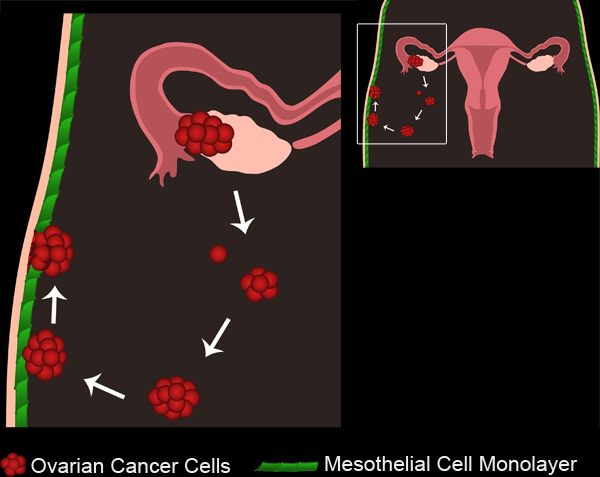
图1。卵巢癌转移。原发性卵巢肿瘤的发展无论是从卵巢表面上皮或输卵管。肿瘤细胞/集群断绝从原发肿瘤和收集在腹腔。肿瘤细胞可以聚集形成多细胞球体。球体然后附加到腹腔间皮细胞单层衬砌。皮细胞被排除从下面所附的卵巢癌的球体,使球体获得底层基底膜。
电影1。卵巢癌转移。 点击这里观看电影 。
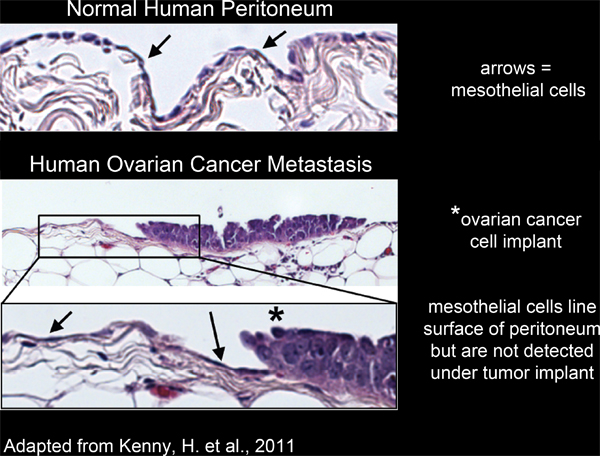
图2。 行间皮细胞表面人腹膜组织,并从下方卵巢癌的细胞植入排除。
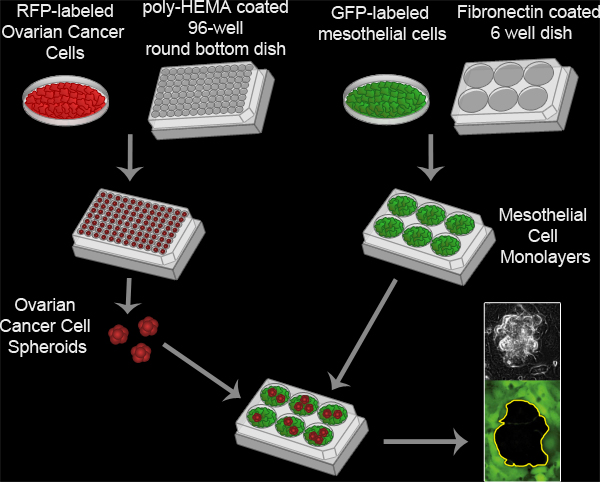
图3。间皮间隙检测。卵巢癌的球体形成孵化100 RFP的表达卵巢癌的细胞每孔聚甲基丙烯酸羟乙酯涂层96底部以及轮在37°C培养16小时菜。聚甲基丙烯酸羟乙酯防止附着到培养皿中的细胞,使细胞保持悬浮,并坚持到另一个,每口井,形成一个单一集群。镀1纤维连接蛋白涂层以及MatTek菜6X10每口井的5间皮细胞,并在37°C孵育16小时的板皮细胞单层准备。的球体,然后转移到MatTek菜皮单层和两个细胞群成像为8小时,每10分钟使用尼康钛 - E我电动nverted广角荧光显微镜的时间推移和元素的软件。
电影2。间皮间隙检测。 点击这里观看电影 。
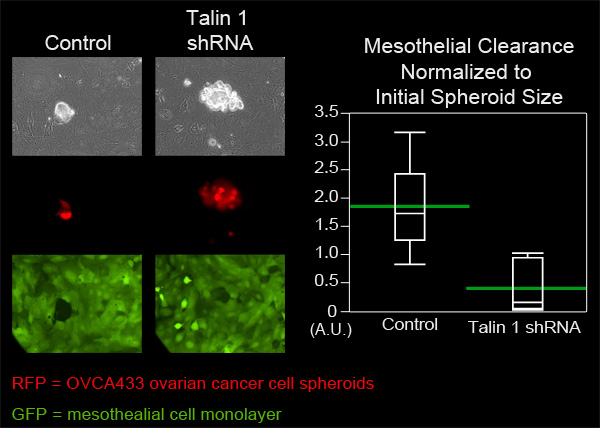
图4。大林1 OVCA433球体表达的衰减,降低皮的清除能力。大林1减毒表达与不OVCA433球体(红色)被允许附加到并侵入到征途皮单层(绿色)。两个细胞群成像为8小时,每10分钟使用尼康钛 - E倒置电动广角荧光显微镜的时间推移和元素的软件。图表显示,1大林衰减显着降低间皮细胞间隙(位数情节与手段的绿色酒吧)。
电影3。控制OVCA433球体(红色),侵犯到皮单层(绿色)。 点击这里观看电影 。
电影4。大林1 OVCA433球体表达(红色)的衰减降低皮(绿色),通关能力。 点击这里观看电影 。
讨论
“间皮间隙检测”这里使用的时间推移显微镜监测卵巢癌多细胞球体和间皮细胞单层的相互作用,在很大的空间和时间上的细节。此前,几组8-14端点检测表明,卵巢癌的细胞附着和侵入皮细胞单层。此法是独一无二的,它使用荧光标记的细胞来区分间皮细胞的肿瘤细胞,使这两个细胞群的动态,可以监测整个实验。插的过程中可以实时可视化,并随着时间的推移,皮清除率可以定量测定...
披露声明
我们什么都没有透露。
致谢
我们要感谢哈佛医学院的尼康影像中心,尤其是珍妮弗水域,拉拉Petrak和温迪三文鱼,培训和使用他们的RSS 2.0订阅显微镜。我们也想感谢罗莎·吴和阿希姆·贝瑟有价值的讨论。这项工作是由NIH资助5695837(M. Iwanicki)GM064346来JSB的支持;由授予博士仪和Sheldon G.阿德尔森医学研究基金会(JSB的)。
材料
| Name | Company | Catalog Number | Comments |
| 试剂 | 公司 | 目录编号 | 评论 |
| OVCA433卵巢癌细胞 | 礼品从Slamon医师谭维义 | ||
| ZT间皮细胞 | 从谭智因斯的礼物 | ||
| 中等199 | Gibco公司 | 19950 | |
| MCDB105 | 细胞应用公司 | 117-500 | |
| 胎牛血清的热灭活 | Gibco公司 | 10082 | |
| 本 - 链球菌 | Gibco公司 | 15070 | |
| 96孔板 | 康宁COSTAR | 3799 | |
| 羟乙酯(聚甲基丙烯酸羟乙酯) | Sigma Aldrich公司 | 192066-25G | 为聚甲基丙烯酸羟乙酯的解决方案,为6mg溶于95%乙醇1毫升聚甲基丙烯酸羟乙酯粉 |
| 乙醇 | pharmco-aaper | 111ACS200 | 稀释至95%,在卫生署2 0 |
| 细胞培养罩 | nuaire | NU-425-300 | |
| 组织文化的孵化器 | Thermo Scientific的 | 3110 | |
| 孵化器聚黑马板块 | labline仪器 | 帝国三305 | |
| 台式离心机 | 贺利氏 | 75003429/01 | |
| 6以及玻璃底菜 | MatTek公司。 | P06G-1.5的20-F | |
| 纤维连接蛋白 | 西格玛 | F1141-1MG | |
| PBS | cellgro | 21-040-CV | |
| RSS 2.0订阅显微镜: | |||
| 显微镜 | 尼康 | 钛 - E倒立时间推移电动荧光显微镜完美的对焦系统综合 | |
| 镜片 | 尼康 | 20X-0.75数值apeture | |
| 卤素灯透射 | 尼康 | 0.52不适用长工作距离聚光镜 | |
| 激发和发射滤波器 | 色度在尼康住房单通滤波器 | GFP的前480/40,EM 525/50 RFP-mCherry前575/50 EM 640/50 | |
| 传输和Epifluoresce光路 | 萨特 | 智能百叶窗 | |
| 线性编码机动阶段 | 尼康 | ||
| 冷却电荷耦合器件摄像机的 | 滨松 | ORCA的-AG | |
| 显微镜孵化室温度和CO 2控制 | 定制 | ||
| 隔振表 | 丰田汽车公司 | ||
| NIS元素软件 | 尼康 | 第3版 |
参考文献
- Jemal, A. . CA Cancer J. Clin. 59, 225-249 (2009).
- Ries, L. G., Melbert, D., Krapcho, M., Stinchcomb, D. G., Howlader, N., Horner, M. J., Mariotto, A., Miller, B. A. . SEER Cancer Statistics Review, 1975-2005. , (2007).
- Burleson, K. M. Ovarian carcinoma ascites spheroids adhere to extracellular matrix components and mesothelial cell monolayers. Gynecol. Oncol. 93, 170-181 (2004).
- Birbeck, M. S., Wheatley, D. N. An Electron Microscopic Study of the Invasion of Ascites Tumor Cells into the Abdominal Wall. Cancer Res. 25, 490-497 (1965).
- Witz, C. A., Monotoya-Rodriguez, I. A., Schenken, R. S. Whole explants of peritoneum and endometrium: a novel model of the early endometriosis lesion. Fertil. Steril. 71, 56-60 (1999).
- Zhang, X. Y. Characteristics and growth patterns of human peritoneal mesothelial cells: comparison between advanced epithelial ovarian cancer and non-ovarian cancer sources. J. Soc. Gynecol. Investig. 6, 333-340 (1999).
- Kenny, H. A., Nieman, K. M., Mitra, A. K., Lengyel, E. The First Line of Intra-abdominal Metastatic Attack: Breaching the Mesothelial Cell Layer. Cancer Discovery. 1, 100-102 (2011).
- Niedbala, M. J., Crickard, K., Bernacki, R. J. Interactions of human ovarian tumor cells with human mesothelial cells grown on extracellular matrix. An in vitro model system for studying tumor cell adhesion and invasion. Exp. Cell. Res. 160, 499-513 (1985).
- Kenny, H. A., Krausz, T., Yamada, S. D., Lengyel, E. Use of a novel 3D culture model to elucidate the role of mesothelial cells, fibroblasts and extra-cellular matrices on adhesion and invasion of ovarian cancer cells to the omentum. Int. J. Cancer. 121, 1463-1472 (2007).
- Ksiazek, K. Senescent peritoneal mesothelial cells promote ovarian cancer cell adhesion: the role of oxidative stress-induced fibronectin. Am. J. Pathol. 174, 1230-1240 (2009).
- Burleson, K. M., Boente, M. P., Pambuccian, S. E., Skubitz, A. P. Disaggregation and invasion of ovarian carcinoma ascites spheroids. J. Transl. Med. 4, 6-6 (2006).
- Heyman, L. Vitronectin and its receptors partly mediate adhesion of ovarian cancer cells to peritoneal mesothelium in vitro. Tumour. Biol. 29, 231-244 (2008).
- Heyman, L. Mesothelial vitronectin stimulates migration of ovarian cancer cells. Cell. Biol. Int. 34, 493-502 .
- Lessan, K., Aguiar, D. J., Oegema, T., Siebenson, L., Skubitz, A. P. CD44 and beta1 integrin mediate ovarian carcinoma cell adhesion to peritoneal mesothelial cells. Am. J. Pathol. 154, 1525-1537 (1999).
- Leroy-Dudal, J., Heyman, L., Gauduchon, P., Carreiras, F. Adhesion of human ovarian adenocarcinoma IGROV1 cells to endothelial cells is partly mediated by the alphav integrins-vitronectin adhesive system and induces an alteration of endothelial integrity. Cell. Biol. Int. 29, 482-488 (2005).
- Leroy-Dudal, J. Transmigration of human ovarian adenocarcinoma cells through endothelial extracellular matrix involves alphav integrins and the participation of MMP2. Int. J. Cancer. 114, 531-543 (2005).
- Iwanicki, M. Ovarian cancer spheroids use myosin-generated force to clear the mesothelium. Cancer Discovery. 1, 144-157 (2011).
- Folkman, J., Moscona, A. Role of cell shape in growth control. Nature. 273, 345-349 (1978).
- Gregoire, L., Munkarah, A., Rabah, R., Morris, R. T., Lancaster, W. D. Organotypic culture of human ovarian surface epithelial cells: a potential model for ovarian carcinogenesis. In Vitro Cell Dev. Biol. Anim. 34, 636-639 (1998).
- Roberts, P. C. Sequential molecular and cellular events during neoplastic progression: a mouse syngeneic ovarian cancer model. Neoplasia. 7, 944-956 (2005).
- Okada, T., Okuno, H., Mitsui, Y. A novel in vitro assay system for transendothelial tumor cell invasion: significance of E-selectin and alpha 3 integrin in the transendothelial invasion by HT1080 fibrosarcoma cells. Clin. Exp. Metastasis. 12, 305-314 (1994).
- Zervantonakis, I. K., Kothapalli, C. R., Chung, S., Sudo, R., Kamm, R. D. Microfluidic devices for studying heterotypic cell-cell interactions and tissue specimen cultures under controlled microenvironments. Biomicrofluidics. 5, 13406-1310 (2011).
- Brandt, B. 3D-extravasation model -- selection of highly motile and metastatic cancer cells. Semin. Cancer Biol. 15, 387-395 (2005).
- Condeelis, J., Segall, J. E. Intravital imaging of cell movement in tumours. Nat. Rev. Cancer. 3, 921-930 (2003).
- Dai, J., Ting-Beall, H. P., Hochmuth, R. M., Sheetz, M. P., Titus, M. A. Myosin I contributes to the generation of resting cortical tension. Biophys. J. 77, 1168-1176 (1999).
- Laferriere, J., Houle, F., Taher, M. M., Valerie, K., Huot, J. Transendothelial migration of colon carcinoma cells requires expression of E-selectin by endothelial cells and activation of stress-activated protein kinase-2 (SAPK2/p38) in the tumor cells. J. Biol. Chem. 276, 33762-33772 (2001).
- Dong, C., Slattery, M. J., Rank, B. M., You, J. In vitro characterization and micromechanics of tumor cell chemotactic protrusion, locomotion, and extravasation. Ann. Biomed. Eng. 30, 344-355 (2002).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。