基于图像的高通量表型分析用于确定马铃薯对单一胁迫和联合胁迫的形态和生理响应
摘要
我们设计了一种基于图像的表型分析方案,以确定对单一和联合高温、干旱和内涝处理的形态和生理反应。这种方法能够在整个工厂级别(尤其是地上部件)识别早期、晚期和恢复响应,并强调了使用多个成像传感器的必要性。
摘要
高通量基于图像的表型分析是一种强大的工具,可以非侵入性地确定植物在特定条件下随时间推移的发育和性能。通过使用多个成像传感器,可以评估许多感兴趣的性状,包括植物生物量、光合效率、树冠温度和叶片反射率指数。在严重的热浪、洪水和干旱事件严重威胁作物生产力的田间条件下,植物经常暴露在多重压力下。当胁迫重合时,由于协同或拮抗相互作用,对植物产生的影响可能是不同的。为了阐明马铃薯植株如何应对类似于自然发生的胁迫情景的单一和综合胁迫,在块茎化开始时对选定的马铃薯品种(Solanum tuberosum L., cv. Lady Rosetta)实施了五种不同的处理,即控制、干旱、高温、内涝以及高温、干旱和涝渍胁迫的组合。我们的分析表明,涝渍胁迫对植物性能的不利影响最大,导致与气孔闭合相关的快速而剧烈的生理反应,包括光系统II的量子产量和效率降低以及冠层温度和水指数的增加。在热处理和联合胁迫处理下,胁迫初期相对生长速率降低。在干旱和共同胁迫下,随着温度的升高和胁迫后期气孔的闭合,植株体积和光合性能下降。在规定的环境条件下,优化的应激处理与选定的表型分析方案相结合,可以揭示对单一和组合应激的形态和生理反应的动态。在这里,为植物研究人员提供了一个有用的工具,他们希望确定表明对几种气候变化相关压力具有复原力的植物性状。
引言
气候变化的潜在影响,包括热浪、洪水和干旱事件的强度和频率的增加,对作物生长产生负面影响1.了解气候变化对作物变异性的影响以及随之而来的作物年产量波动非常重要2.随着人口和粮食需求的增加,保持农作物的产量是一项挑战,因此,迫切需要找到具有气候适应性的作物进行育种 3,4.马铃薯(Solanum tuberosum L.)是促进全球粮食安全的重要粮食作物之一,因为它具有高营养价值和更高的用水效率。然而,在不利条件下生长和产量下降是一个主要问题,特别是在易感品种中 5,6.许多研究强调了调查维持马铃薯作物生产力的替代方法的重要性,包括农业实践,找到耐受的基因型,以及了解压力对发育和产量的影响7,8,9,这也是欧洲马铃薯种植者(或农民)的高度要求10。
自动化表型分析平台,包括基于图像的表型分析,能够对植物结构和功能进行定量分析,这对于选择感兴趣的相关性状至关重要11,12。高通量表型分析是一种先进的非侵入性技术,可以可重复和快速的方式确定感兴趣的各种形态和生理特征 13.尽管表型反映了与环境影响相关的基因型差异,但比较在胁迫受控条件下的植物可以将广泛的表型信息与特定(胁迫)条件联系起来14.基于图像的表型分析在描述表型变异性方面至关重要,并且它还能够筛选植物发育中的一组性状,而不管群体规模如何15。例如,使用红-绿-蓝 (RGB) 成像传感器测量形态性状,包括叶子的形状、大小和颜色指数,用于确定植物的生长和发育。此外,生理性状的测量,包括光合性能、树冠温度和叶片反射率,使用多种类型的传感器进行量化,例如叶绿素荧光、热红外 (IR) 和高光谱成像16。最近在受控环境中的研究表明,使用基于图像的表型分析在评估植物在非生物胁迫下的不同机制和生理反应的潜力,例如马铃薯的热量17、大麦18、水稻的干旱19 以及小麦的干旱和热处理20。尽管研究植物对多种胁迫相互作用的反应很复杂,但这些发现揭示了理解植物应对气候条件快速变化的机制的新见解21。
植物的生理和形态响应直接受到非生物胁迫条件(高温、缺水和洪水)的影响,导致产量下降22.尽管与其他作物相比,马铃薯具有较高的水分利用效率,但由于根系结构较浅,缺水对产量和质量产生负面影响5.根据干旱程度的强度和持续时间,叶面积指数降低,在胁迫后期阶段,树冠生长迟缓和新叶形成受到抑制,导致光合速率降低23。水分过多或干旱期延长时,水的阈值水平至关重要,由于氧气限制、根系水力传导率降低和气体交换限制,对植物生长和块茎发育产生负面影响24,25.此外,马铃薯对高温很敏感,温度高于最佳水平会导致块茎萌发、生长和同化率延迟26.当胁迫组合出现时,生化规律和生理反应与个体胁迫反应不同,凸显了研究植物对胁迫组合反应的必要性27.综合胁迫可导致(甚至更多)植物生长严重减少,并对生殖相关性状产生决定性影响28.胁迫组合的影响取决于每个胁迫相对于其他胁迫的优势,导致植物反应增强或抑制(例如,干旱通常导致气孔关闭,而气孔打开以允许在热胁迫下冷却叶片表面)。然而,联合胁迫研究仍在兴起,需要进一步的研究,以更好地理解在这些条件下介导植物反应的复杂调控29.因此,本研究旨在强调和推荐一种使用多个成像传感器的表型分析方案,该方案适用于评估形态生理反应并了解单一和联合胁迫处理下马铃薯整体性能的潜在机制。正如假设的那样,结合多个成像传感器被证明是表征植物胁迫响应期间早期和后期策略的宝贵工具。优化基于图像的表型分析协议将成为植物研究人员和育种者寻找非生物胁迫耐受性感兴趣的性状的交互式工具。
研究方案
1.植物材料制备和生长条件
- 将体外马铃薯(Solanum tuberosum L., cv. Lady Rosetta)插条从组织培养物移植到250mL盆中。
- 用完全饱和的Klasmman Substrate 2填充罐,并将它们在弱光条件下保持在生长室中1周。
- 使用照度计将冠层的光照条件调整为 160 μmol·m-2·s-1 ,结合 25% 白光和 35% 红外线。
- 在土壤中生长10天后,将体 外 插条移植到3L盆中(直径15.5厘米,高20.5厘米)。
- 用 1850 克 3:1 克拉斯曼底物 2:沙子填充 3 升罐。
- 将植物置于320μmol·m - 2·s - 1 的光照条件下,用55%白光和81%红外线的组合在生长室中,并将其设置为长日照状态(16小时光周期)。
- 将生长室中的温度设置为白天/黑夜的22°C / 19°C,将整个实验的相对湿度(RH)设置为55%。
- 将盆重保持在土壤相对含水量(SRWC)的60%作为适宜的控制水平,以维持生长和产量30,31。
注:根据以前的试验,保持体积含水量高于60%可以促进土壤表面的苔藓生长,并增加植物病害的风险。此外,苔藓的存在可能会从叶绿素荧光成像中产生误导性的阳性信号,而叶绿素荧光成像很难过滤掉。使用以下公式:SRWC% = (FW-DW)/(TW-DW) × 100,其中 FW 是土壤鲜重,TW 是膨胀重,DW 是干重32。- 从三个不同的Klasmman Substrate 2混合袋中选择土壤样品(100g)作为重复样品,并称量土壤的鲜重。
- 用水浸透土壤,直到花盆保持水而不滴落,并称量土壤膨胀重量。
- 将样品置于80°C的烘箱中3天,直到土壤样品完全干燥,称取土壤干重33。
- 将蓝色垫子放在锅表面以减少蒸发。
注意:在图像分割中,蓝色对于从植物像素中减去土壤背景是必要的。 - 每种处理选择10个生物学重复。
- 在灌溉过程中随机分配花盆(总共 50 个花盆)。
- 添加蓝色支架以支撑植物,并避免在将它们放入表型系统中时造成机械损坏。
2. 压力施加
- 在早期块茎化阶段(移植 体外 插条后28天),将植物分为五个处理组,每个处理表型为10株植物(图1)。
- 将单一压力和组合压力诱导到不会造成损害的水平,如下所示:
- 在生长室中,保持植物在22°C / 19°C的昼夜(步骤1.7)下控制,干旱和涝渍处理,SRWC的百分比不同:
对照(C)用60%SRWC进行整个实验。
干旱 (D) 用 20% SRWC 逐渐持续 7 天,然后恢复 1 天。
内涝 (W) 用 160% SRWC 持续 5 天,然后恢复 10 天。 - 为了在涝处理中保持水位高于土壤表面,将塑料袋插入空盆中,然后将装有土壤的主盆放入准备好的第二个盆中。
- 将植物置于30/28°C的生长胶囊中,昼夜和55%RH进行热处理。施加单一热应力和组合热应力,如下所示:
- 对于加热 (H),使用 60% 的 SRWC 保持温度 30-28 °C 15 天。
- 对于热 + 干旱 + 涝 (HDW) 三重胁迫,将植物暴露在前 7 天 30 °C/28 °C 昼/夜温度下进行热处理(保持 60% SRWC),然后进行其余 7 天的干旱 + 热联合处理(20% SRWC 和 30 °C/28 °C),最后将植物暴露在涝渍胁迫下 1 天。对于后者,将植物放回生长室中(条件见步骤1.7),并诱导涝水至160%SRWC 1天。
注:选定的诱导胁迫持续时间基于一项试点实验,该实验显示了胁迫效应,而处理过的植物存活率为100%,没有不利影响。在生长室环境中,环境条件的变化在温度±0.2 °C,湿度变化±3%。
- 在生长室中,保持植物在22°C / 19°C的昼夜(步骤1.7)下控制,干旱和涝渍处理,SRWC的百分比不同:
3. 用于表型分析的植物准备
- 在生长室中于上午6:00打开灯后,让植物在恒定的生长光照条件(320μmol·m-2·s-1)下适应环境至少2-3小时,然后再进行表型分型方案。这确保了光合作用和气孔调节处于稳定状态34.
- 在测量之前,将植物从其培养位置转移到表型系统的生长缓冲区,用于将植物手动加载到系统中,同时自动评分处于待机模式并放置在温室内(补充图1,补充图2和 补充图3)。
注意:在持续3.5小时的表型分析期间,植物保持在生长缓冲区中。温室环境条件变化幅度为±温度为2 °C±,湿度变化幅度为5%,光照强度波动幅度为20%。因此,考虑到测量应该立即开始并且时间短,以避免温室条件对植物的影响。 - 在表型分析平台中,将罐子放入圆盘中,这些圆盘根据第 4 节中指定的测量协议,在传送带上以给定的间隔自动移动到成像传感器。
- 用唯一的 ID 标记每个植物/托盘,以确保在整个实验过程中将测量数据分配给正确的植物。
4. 表型分析方案
- 使用多个成像传感器(叶绿素荧光、热红外、RGB和高光谱成像)优化表型分析方案,从而可以同时测量植物的生理和形态参数(图2)。
注意:由于植物的反应反映了环境条件和昼夜效应,因此重要的是要考虑盆栽的随机化和在一天中的同一时间段内进行表型分析。 - 在表型分析平台中,确保植物通过适应隧道(图2A)进入系统,首先捕获植物的高度,然后根据固定的工作距离调整每个传感器的高度。
- 按照测量协议中的合理性,使用软件分两轮进行测量。
- 在第一轮中,包括使用叶绿素荧光和热成像测量量化为“快速反应”的生理反应。
- 首先测量热应激处理下的生理参数,然后测量其余的处理。
- 在第二轮中,继续进行其他测量以评估较慢的反应,包括结构RGB和高光谱成像,然后进行体重评估和浇水。
- 在称重和浇水步骤中,定义每株植物的参考重量,以便能够自动浇水和称重到给定的处理。
- 确保总参考重量包括位于传送带上的圆盘、插入物、支撑蓝色支架、蓝色垫子、盆栽、土壤和定义协议中植物生物量的重量。
- 为了准确测量称重和浇水步骤中的蒸散量,请准备空罐作为参考。此外,准备额外的花盆以校正植物生物量重量。
- 要测量 50 株植物,整个表型分析方案持续时间需要 215 分钟(第 1 轮为 85 分钟,第2 轮为 130 分钟)。
- 在对照条件下(处理前1天)每天对所有植物进行表型分析,然后诱导胁迫处理以监测动态响应并评估诱导胁迫的早期和后期阶段。
5. 调整每个成像传感器的设置
- 动力学叶绿素荧光成像
注:动力学叶绿素荧光用于研究植物响应不同环境条件(包括非生物胁迫)的光合作用能力,并提供有关光化学和散热(非光化学过程)的量子效率的宝贵信息。- 使用短光协议对光适应植物进行叶绿素荧光测量,以区分不同处理下植物的反应。
- 在配备冷白光LED(6500K)的适应隧道中,在500μmol·m-2·s-1的光照下驯化35种植物5分钟。
注:叶绿素荧光成像是光适应后用于监测植物光合能力变化的第一次测量。 - 根据植物规模和所需的光强度选择并优化预定义的方案。
- 优化测量设置,包括相机和光强度设置,以确保以最佳信噪比采集强信号。
- 调整相机设置,例如快门(曝光时间、测量闪光灯的持续时间)和灵敏度(相机的电增益)。使用快门的快门时间为 2 ms,灵敏度为 12%。
注意:这些值是根据叶子的大小和形状以及树冠顶部与成像传感器之间定义的距离进行调整的。 - 将光化光强度调整为500 μmol·m-2·s-1 ,将饱和脉冲设置为3200 μmol·m-2·s-1,至少是光化光的6-7倍。
- 调整相机设置,例如快门(曝光时间、测量闪光灯的持续时间)和灵敏度(相机的电增益)。使用快门的快门时间为 2 ms,灵敏度为 12%。
- 为了测量光稳态 (Lss) (如下所述) 的参数,在光适应隧道中测量之前,将光适应植物 5 分钟。
- 为了估计光适应植物的稳态光系统II(PSII)量子产率,选择短光协议(图3)并按如下方式设置协议。
注意:协议持续时间为每株植物 10 秒。- 打开500 μmol·m-2·s-1 的冷白光化光3 s开始测量,以测量光中的稳态荧光(Ft_Lss又名。Ft')
- 施加3200μmol·m-2·s-1 的饱和脉冲800 ms,以测量光(Fm_Lss的稳态最大荧光。Fm')
- 关闭光化灯,然后打开远红光 (735 nm),使 PSII 在黑暗中松弛 800 毫秒,并测量光中的稳态最小荧光 (Fo_Lss 又名。Fo')。
- 要计算相对参数,请使用数据分析器软件,该软件减去背景并提取相关参数。
注:从所使用的协议中提取的参数是:光适应样品在光稳态下的PSII光化学的最大效率,确定为Fv / Fm_Lss又名。Fv'/Fm',光系统II的量子产率或光系统II在光稳态下的运行效率定义为QY_Lss又名。φPSII = Fq'/Fm',PSII中开放反应中心的分数(氧化QA)测定为qL_Lss = (Fq'/Fv') x (F0'/Ft')。
- 热红外 (IR) 成像
注意:热红外成像用于非侵入性测量实际树冠温度,从而确定不同的气孔规定。在热红外成像单元中,热像仪横向安装在机械臂上,用于从侧面测量树冠温度。- 为了在图像处理过程中增加背景温度相对于成像物体温度的对比度,请在热像仪的另一侧使用自动控制的加热墙来增加对比度。在成像单元中将壁温调节在高于空气温度 8 °C 处。
注意:热图像是在黑暗中使用线扫描模式35 采集的。 - 图像采集后, 基于RGB侧视数据生成植物掩模, 并利用它与图像分析中的热数据共同配准.这确保了对扫描物体的精确识别,同时消除了背景干扰,如植物支架。
- 为防止波动的环境条件在整个实验过程中产生影响,请计算参数温差(delta T 或 ΔT)。
注意:Delta T (ΔT) 定义为叶片表面的测量温度(植物整个检测到的表面的所有像素的平均值)与成像盒内的环境空气温度之间的差值。
- 为了在图像处理过程中增加背景温度相对于成像物体温度的对比度,请在热像仪的另一侧使用自动控制的加热墙来增加对比度。在成像单元中将壁温调节在高于空气温度 8 °C 处。
- RGB成像
注意:RGB 成像基于视觉惯性系统 (VIS) 相机,可检测 400-700 nm 可见光范围内的光,用于深入分析植物形态、结构和颜色指数特征的提取。- 成像单元包含一个旋转台,用于托盘的精确定位,同时允许对侧面视图进行多角度成像。
- 设置基于侧视成像的RGB成像,从三个角度(0°、120°和240°)捕获植物,在线扫描模式(RGB1)和俯视图像在快照模式(RGB2)下拍摄。
- 两台相机都具有基于 LED 的光源,可确保成像植物的均匀照明,从而准确确定形态和颜色特征。
- 使用数据分析器软件提取计算参数。
- 有关基于侧视图和俯视图的其他参数,请计算植物体积(数字生物量)36:
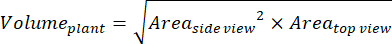
- 计算相对增长率 (RGR)37:
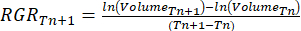
其中 Tn 和 Tn+1 表示时间间隔(天)。
- 高光谱成像
注意:高光谱成像用于植物光谱反射率的可视化。叶片反射率的变化是给定植物不同生理状态的指标.- 使用高光谱成像传感器量化光谱可见光部分的冠层反射率,使用范围为 380-900 nm 的可见光近红外 (VNIR) 高光谱相机和 900-1700 nm 范围内的短波红外相机 (SWIR)。
- 相机安装在带有卤素灯管光源 (600 W) 的机械臂上,用于在穿过 XZ 区域移动的图像采集过程中实现均匀且光谱适当的样品照明。
- 两台相机均以线扫描模式运行,并放置在光绝缘成像盒中。
- 在每轮测量之前,执行两次校准测量(自动):暗电流校准和使用光谱反射聚四氟乙烯标准的辐射校准。
- 从原始和白色校准图像中减去暗校准图像,以消除暗电流噪声。然后,通过将减去后的原始图像除以白色校准图像来生成最终的高光谱。
6. 导出数据和图像分析
- 使用数据分析器软件对图像处理管道进行自动提取、背景减去和 植物掩膜 分割(图2B)。
- 该软件执行全自动分析,其中掩模应用、背景减去(其中植物与其背景隔离)以及参数计算按照 RGB 成像38 和热成像20 的描述进行处理。
- 从 RGB 图像生成的 植物蒙版 和 托盘蒙版定义的植物特定像素中提取测量和计算的参数。
- 如果未完全选择图像(这可能是由于后期发育阶段植被绿度的变化或胁迫处理的影响而发生的),请在软件中打开本地数据分析部分,并在数据分析器软件中根据每个传感器重新调整 植物掩模 设置。
- 在叶绿素荧光图像处理中,调整叶绿素荧光 植物掩膜 设置分析参数(补充图4)。
- 将阈值设置为 True,这意味着将自动执行植物分割。
- 将 Mask Frame Index 设置为 False,这意味着对于 Plant Mask 检测,将按照叶绿素荧光协议中的定义使用 Time-Visual 帧。
- 在热图像处理中, 设置 植物掩模 分析的参数 (补充图 5).
- 将 对象蒙版生成的 自动阈值设置为 False。
- 将 RGB侧图像 中的蒙版设置为 True 以用于分析。
- 在RGB图像处理中,根据物种和发育阶段调整 植物掩膜 设置分析参数(补充图6 和 补充图7)。
- 选择公式 4*G-3*B-R,这是对象蒙版生成的定义,并定义了使用的颜色分量(红色、绿色、蓝色分量)。
注意:此标准公式和其他设置可能会根据所使用的相机类型(顶部或尺寸视图)、应用的处理和不同的品种而更改。 - 调整用于将具有增强绿色通道的灰度图像转换为二值图像的 阈值 - 确定植物覆盖的表面。
- 调整用于减少噪点和无效像素的 中值滤镜大小 ,并填充缺失的像素。
- 调整要包含在分析中的 对象的最小大小 (以像素为单位)。
- 以像素为单位调整蒙版对象中 孔的最小大小 ,通常为数十像素。小于此值的孔被闭合并放入对象像素中。
- 将 Use Reflection Reduction 设置为 True ,以对每个像素中的 RGB 值进行归一化。
- 将 Skip Bad Exposed Points 设置为 True ,以裁剪植物蒙版中曝光像素的上方/下方(例如,省略表面反射或噪声大于信号的暗像素)。
- 选择公式 4*G-3*B-R,这是对象蒙版生成的定义,并定义了使用的颜色分量(红色、绿色、蓝色分量)。
- 使用数据分析器软件对从 RGB 分析的分割设置进行着色,以提供有关与胁迫响应和植物衰老相关的颜色变化的信息。
注意:绿色是使用代表植物发育所有阶段的预定义颜色范围来估计的。对植物表面对应的所有像素的颜色通道中的强度进行分组和聚类,作为颜色分割的源颜色图。- 提供处理过的RGB图像(去除背景),颜色图-用于特定分析的色调列表,作为软件的输入。
- 为了获得公正的结果,请使用“训练”数据集进行色调选择,并选择不同的发育阶段和治疗方法。
注意:分析会保存此训练数据集中每个图像的每个像素的 R、G 和 B 值。 - 使用软件定义颜色定义输出的色调数量(选择 6 种色调),每个通道的范围为 0-255。
- 提供数据分析器软件中生成的色调列表(颜色)。
- 在高光谱图像处理中,使用高光谱分析仪软件中实现的逐像素分析处理获取的高光谱数据,具有辐射和暗噪声校准、背景减去和植物掩模分割等功能。使用平均光谱和植被指数进行进一步分析。
- 创建掩码,以便从 VNIR 高光谱相机拍摄的 VNIR 图像中提取高光谱图像中提取数据。对于SWIR高光谱扫描,基于SWIR分析生成植物掩模。
- 在 VNIR植物掩模中,使用公式 1.2*(2.5*(R740-R672)-1.3*(R740-R556)) 来可视化图像,其中R代表特定波长的反射率值(补充图8)。
- 在 SWIR植物掩膜中,在图像处理中使用公式 (R960-R1450)-(R960-R1200) 来可视化图像(补充图9)。
7. 称重和浇水
- 在称重和浇水过程中储存重量(浇水前)。然后浇水,浇水后也要保持重量。
- 在参考模式下给托盘浇水 - 每个托盘都有一个参考值存储在数据库中,它总是被浇水到该数据库中。根据处理情况确定参考。
8. 数据分析
- 使用方差分析和夏皮罗检验分析数据。
- 在 R 工作室(版本 4.2.3)中使用 (dplyr)、(tidyverse)、(rstatix) 和 (ggpubr) 包通过 Pairwise Wilcox 测试对不同处理进行成对比较。
注意:图像分析是使用数据分析器软件自动完成的。为了进一步分析图像采集,请使用传感器专用的数据分析器软件。
结果
本研究采用基于自动图像的表型分析方法研究了马铃薯(Lady Rosetta)在单一胁迫和联合胁迫下的形态和生理响应。应用方法显示了在块茎萌发阶段诱导胁迫时植物在高时空分辨率下的动态响应。为了评估压力的早期和晚期阶段,结果以 3 个时间段([0-5 天表型 (DOP)]、[6-10 DOP] 和 [11-15 DOP])(图 1)。在0 DOP之前,所有植物都在控制条件(C)下生长,然后从1-5 DOP开始,其中应用涝胁迫(W)和热胁迫(H)。因此,观察到的响应如下:(i)在0-5 DOP中,表示初始热量和内涝;(ii)在6-10 DOP中,反映了早期干旱(D)和热旱联合(HD),(iii)在11-15 DOP中,表现出晚热、干旱和联合热+干旱+内涝(HDW)胁迫。在6-10 DOP和11-15 DOP中观察到内涝恢复。
形态学特征
采用RGB成像技术测定了不同胁迫和组合对地上植物生长的影响。 图 4 中的结果表明,与对照组相比,热处理和涝渍应力 (0-5 DOP) 已经导致植物体积和 RGR 减少。在6-10 DOP期间,对照植物的植株体积和RGR持续增加,而在高温、热合、干旱和涝渍下,植物体积的增加明显减少(图4A)。由于植物非常容易受到涝灾胁迫的影响,因此RGR明显下降(图4B)。在干旱胁迫后期(11-15 DOP),SRWC保持在20%,与对照组相比,RGR明显降低。然而,在联合HDW的后期,应用涝处理导致胁迫最后一天RGR增加。
生理特征
应用结构和生理表型的结合来揭示对压力的进一步反应。使用多个成像传感器可以确定压力早期阶段的生理反应。对叶绿素荧光数据的进一步分析表明,涝渍对光合效率产生负面影响,其中Fv'/Fm' (Fv/Fm_Lss)在0-5 DOP和6-10 DOP中急剧下降,但在11-15 DOP中观察到恢复响应,其中Fv'/Fm'略有增加(图5A)。在胁迫后期(11-15 DOP),干旱和热旱联合期间,Fv'/Fm'有所减少。在涝渍植物中,与其他处理相比,0-5 DOP和6-10 DOP的植物(QY_Lss又名φ PSII)的运行效率显着降低,但在11-15 DOP时略有增加,因此表明植物恢复(图5B)。此外,通过计算轻稳态(qL_Lss)下PSII中开放反应中心的比例,确定了调节有助于保护PSII的效率的不同机制(图5C)。只有在干旱的情况下,才观察到 qL 的增加,可能是由于光抑制。
这些发现与反映应力下不同潜在机制的 IR 数据一致(图 6)。在内涝中观察到 deltaT (ΔT) 增加,降低了天然气交换率。在晚旱和热旱共同胁迫下,ΔT的增加是由于气孔闭合造成的,气孔被认为是避免水分流失过多的主要反应之一。另一方面,在热处理下,随着气孔打开,ΔT降低,以提高蒸腾效率并冷却叶片表面。
通过对高光谱数据的分析,从高光谱VNIR数据中选取2个参数来评估叶片反射率指数,其中NDVI作为叶绿素含量的指标,PRI作为光合作用效率的指标。结果表明,仅在涝渍条件下,NDVI和PRI的降低与形态性状的减少有关(图7A,B)。此外,从用于评估植物中含水量的SWIR高光谱数据来看,在0-5 DOP期间观察到内涝中的水指数增加(图7C)。然而,在热处理下,当水指数低于对照时,观察到相反的响应。这些发现与RGB顶视图颜色分割对植被的检查一致。色调比例的变化表明了应力反应随时间的变化(图8)。绿化指数表现为干旱和混合HDW在胁迫后期色素含量降低,涝渍处理逐渐恢复。因此,使用多个成像传感器反映了形态生理性状的相关性,并能够评估植物在非生物胁迫下的整体性能。
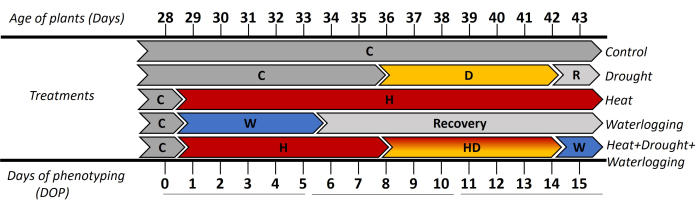
图 1:应用不同处理的时间表,包括移植 体外 插条后几天内的植物年龄。 在对照(C)条件下测量表型(DOP)第0天,然后诱导不同持续时间的不同胁迫。在1-5 DOP时施加涝渍应力(W)和热处理的初始响应(H)。接下来的6-10 DOP,其中提出了干旱胁迫(D)和热旱胁迫(HD)的初始阶段。在11-15 DOP期间,植物对干旱和热处理后期的响应以及1 d的HD(HDW)涝涝应用均有反映。 请点击这里查看此图的较大版本.
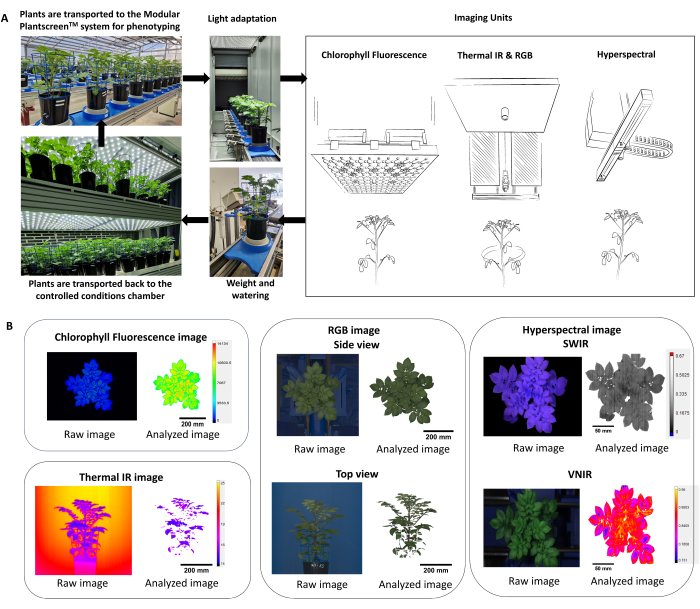
图 2:总结表型分析方案和数据分析的方案。 (A) 表型分析方案概述。植物从FS-WI生长室(PSI)的受控条件运输到表型系统。在测量前,植物在光适应室中以 500 μmol.m-2.s-1 进行光适应 5 min。使用多个成像传感器确定形态和生理特征,然后确定加权和浇水站。根据处理的不同,将植物放回受控条件下,温度为22°C / 19°C或30°C / 28°C。 (B) 从每个成像传感器自动提取和分割图像处理管道。请点击这里查看此图的较大版本.
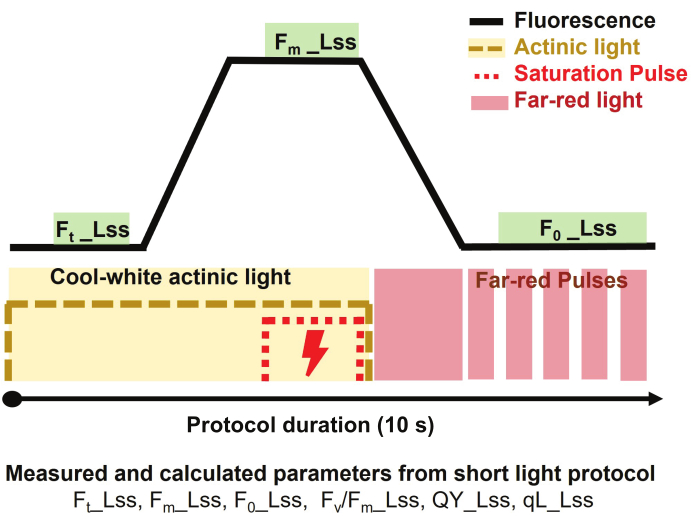
图 3:叶绿素荧光成像的短光协议概述。 测量方案首先打开冷白光化光以测量光中的稳态荧光 (Ft_Lss),然后应用饱和脉冲以测量光中的稳态最大荧光 (Fm_Lss)。关闭光化灯,打开远红光灯以确定光中的稳态最小荧光 (Fo_Lss)。协议的持续时间为每株植物 10 秒。 请点击这里查看此图的较大版本.
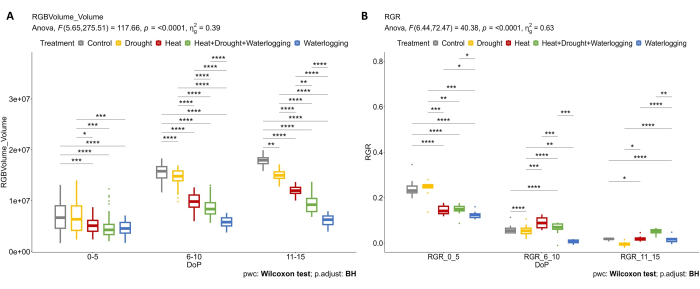
图 4:用于形态学评估的 RGB 成像。 (A) 根据 RGB 顶视图和侧视图区域计算的植物体积。(B) 块茎萌发期的相对生长率(RGR)。数据表示平均值±标准差 (n = 10)。 请点击这里查看此图的较大版本.
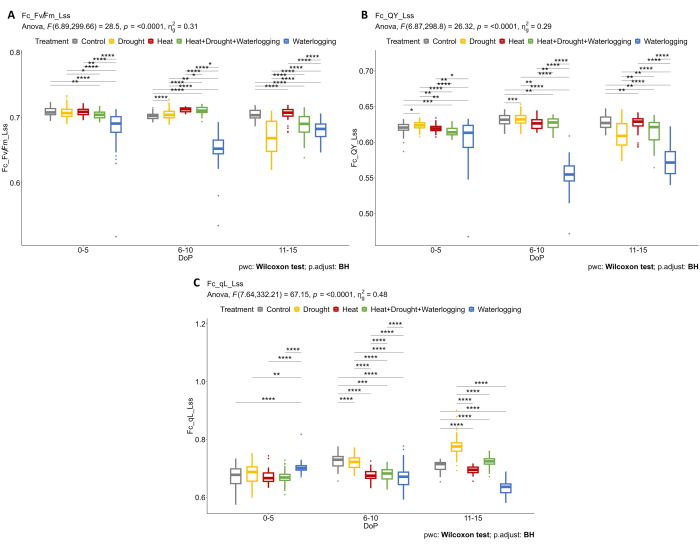
图5:光适应植物的叶绿素荧光成像。 (A) 光适应样品在光稳态下PSII光化学的最大效率(Fv / Fm_Lss)。(B) 光系统II的量子产率或光系统II在光稳态(QY_Lss)下的运行效率。(C) PSII中轻稳态(氧化QA)中开放反应中心的分数(qL_Lss)。数据表示平均值±标准差 (n = 10)。 请点击这里查看此图的较大版本.
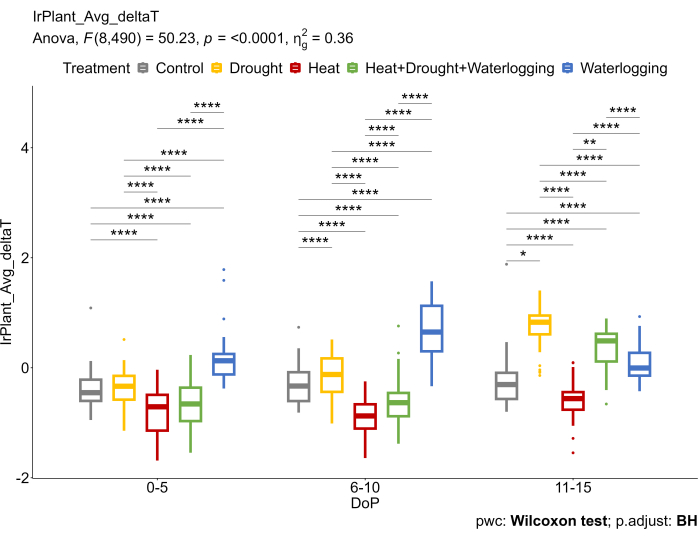
图 6:热红外成像用于计算从热红外图像中提取的树冠平均温度与空气温度 (ΔT) 之间的差异。 数据表示平均值±标准差 (n = 10)。 请点击这里查看此图的较大版本.
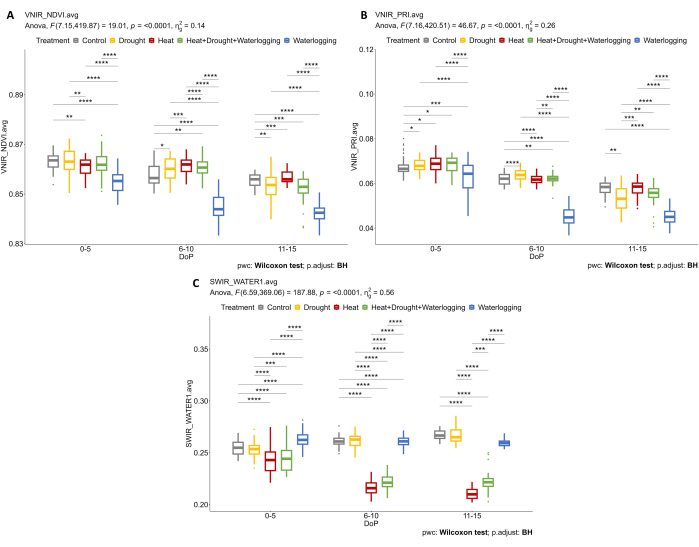
图7:用于确定植被指数和含水量的高光谱成像。 (A) 归一化差值植被指数(NDVI)。(B)由VNIR成像计算的光化学反射指数(PRI)。(C)根据短波红外成像计算出的水量指数。数据表示平均值±标准差 (n = 10)。 请点击这里查看此图的较大版本.
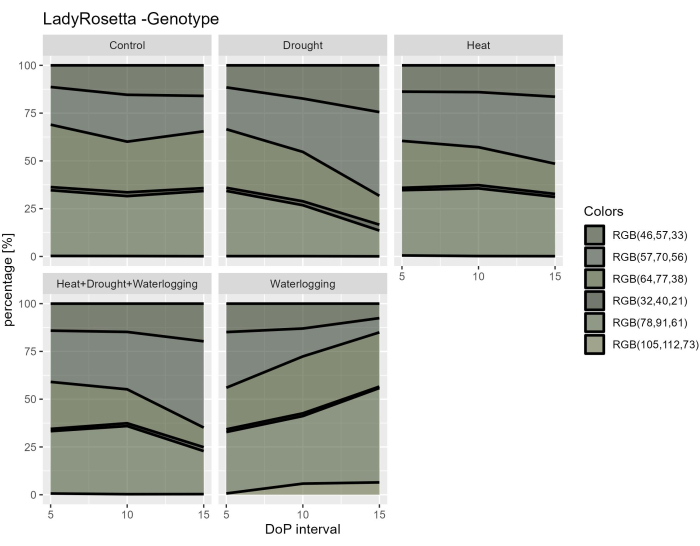
图8:不同处理下植物的绿化指数。 图像处理基于原始 RGB 图像在由 6 种定义色调组成的颜色映射图中的转换。数据表示平均值±标准差 (n = 10)。 请点击这里查看此图的较大版本.
补充图 1:在表型 (DOP) 期间测量的光强度。 从上午 9:00 到中午 12:35 的测量持续时间。 LI_Buff是指分布在温室中的 5 个光传感器的中值数据。 请点击这里下载此文件。
补充图 2:在表型 (DOP) 期间测量的相对湿度 (RH)。 从上午 9:00 到中午 12:35 的测量持续时间。 RH_Buff是指分布在温室内的 5 个湿度传感器的中位数数据。RH2是指适应室中的相对湿度。 请点击这里下载此文件。
补充图 3:在表型分析 (DOP) 期间测量的温度。 从上午 9:00 到中午 12:35 的测量持续时间。 T_Buff是指分布在温室内的 5 个温度传感器的中位数数据。T2是指适应室中的温度。T3是指加热壁的温度。T4 是指热红外成像单元中的温度。 请点击这里下载此文件。
补充图4:数据分析器软件的屏幕截图,显示了叶绿素荧光成像传感器中为植物掩膜分析调整的参数。请点击这里下载此文件。
补充图5: 数据分析器软件的屏幕截图显示了在热红外成像传感器中为植物掩膜分析调整的参数。 请点击这里下载此文件。
补充图6: 数据分析器软件的屏幕截图显示了在 RGB 1 侧视图成像传感器中为植物掩膜分析调整的参数。 请点击这里下载此文件。
补充图7: 数据分析器软件的屏幕截图显示了在 RGB2 顶视图成像传感器中为植物掩模分析调整的参数。 请点击这里下载此文件。
补充图8: 数据分析器软件的屏幕截图显示了在VNIR成像传感器中为植物掩膜分析调整的参数。 请点击这里下载此文件。
补充图9: 数据分析器软件的屏幕截图显示了在SWIR成像传感器中为植物掩膜分析调整的参数。 请点击这里下载此文件。
讨论
改进的先进高分辨率成像工具和计算机视觉技术使植物表型分析的快速发展成为可能,以可重复的方式从大量植物图像中获取定量数据39.本研究旨在采用和优化基于高通量图像的方法,使用一系列目前可用的成像传感器来监测植物在单一和联合非生物胁迫下的动态响应。应用方法的几个关键步骤需要调整,包括施加压力和为测量选择合适的成像协议。使用多个传感器进行图像采集可以量化关键表型性状(如植物生长、光合效率、气孔调节、叶片反射率等)。此外,还提高了对马铃薯植物如何应对不同非生物胁迫的理解。这是加快植物育种项目以开发耐气候基因型的关键先决条件40.对诱导应力的形态响应取决于发育阶段。例如,在匍匐茎或块茎萌发阶段诱导胁迫会抑制叶片和植物的发育,并限制匍匐茎的数量,从而降低最终产量41。然而,在不利的条件下,植物利用应激反应作为适应性反应来预防和修复应激诱导的细胞损伤42.植物具有适应性机制,可以避免和忍受压力条件,具体取决于严重程度43。
为了了解植物的机制,诱导适当的胁迫持续时间和强度,并使用成像传感器确定植物对胁迫的反应被认为是关键步骤之一。当几个应力重合时,一个应力的强度可以抵消其他应力的影响,具体取决于应力的组合、强度和持续时间。因此,压力效应可以加起来,或者相反的反应可以(部分)相互抵消,最终导致对植物的积极或消极影响。本研究中选择的方案基于以前的经验,以确保应用足够的压力水平。例如,与之前的实验一样,将干旱胁迫的应用调整到适度水平,根据叶绿素荧光成像,响应与胁迫早期阶段的对照处理没有差异。这是由于光呼吸的发生,光呼吸充当类囊体膜中电子的替代接收器和光系统 II 的保护机制II 44,45。在综合胁迫响应下,植物暴露于轻度初级胁迫源可以增强对后续胁迫源的耐受性,这可能产生有益或有害的影响46.在这项研究中,与单个干旱胁迫相比,在联合胁迫下观察到更强的响应。通过研究其他生理反应,结果表明,在干旱的情况下,气孔接近以避免过多的水分流失,ΔT(deltaT)增加。相比之下,在热胁迫下观察到相反的响应,与对照组相比,ΔT 较低,反映了气孔张开以增强叶片冷却,这与小麦在高温和干旱胁迫下的发现不同20。在内涝期间,由于气孔闭合导致的 ΔT 增加是由于土壤中的缺氧和根系水稳态的破坏造成的,从而降低了蒸腾流,增加了 ABA,这是水胁迫反应中的关键激素47.
在植物胁迫研究中,胁迫的持续时间和随后的恢复处理与胁迫强度成正比。例如,中度干旱胁迫,例如将土壤水分保持在 20% 的田间容量 (FC),会引起可逆的表型变化,这些变化通常在重新灌溉一天后恢复。相比之下,严重的压力条件(如内涝)会导致广泛的表型损伤,因此需要更长的恢复期。尽管标准化治疗持续时间是理想的,但在实验设计中必须考虑应力强度的固有可变性。
第二个关键步骤是选择合适的协议并优化每个传感器的设置。叶绿素荧光是确定光合装置在胁迫下性能的有力工具48.根据研究问题和实验设计,可以选择不同的叶绿素荧光测量方案,适用于光适应或适应黑暗的植物49.在这项研究中,选定的方案(短光响应)能够确定各种性状,包括 Fv'/Fm'、φPSII 和 qL,它们表明了不同条件下的光合作用性能50。先前的研究表明,在高通量表型分析中使用的方案可有效研究植物在不同胁迫处理下的光合效率,并区分健康和胁迫植物14,20。根据实验设计,在具有高植物群的高通量系统中进行测量时,考虑所选协议的持续时间非常关键。因此,选择使用短时协议对光适应植物进行叶绿素荧光测量,以区分不同处理下的响应。基因型-环境相互作用可以影响许多表型性状,这在测量过程中至关重要12.必须考虑到,测量的持续时间应在短时间内完成,以尽量减少对光合限制的昼夜效应51.
热红外成像用于确定树冠温度并了解不同处理下的气孔调节52。值得一提的是,在加热墙位于摄像机的另一侧,并且加热墙的温度是动态控制和可编程的,从而采用了技术优化。因此,使用集成环境传感器调整背景加热壁是必要的,以便通过增加背景温度与成像物体温度的对比度来正确选择背景中的植物。
尽管图像分析是自动化的,但仍需要调整RGB阈值指数,以便在RGB成像中获得适当的二进制掩码,以精确选择植物53。此外,选择多个角度对于适当估计定量参数(包括数字生物量和生长速率)非常重要。在这项研究中,选择RGB侧视图上的三个角度(0°、120°和240°)并进行平均,以准确计算植物体积和相对生长速率。
根据光谱范围的不同,可以使用高光谱成像54 来研究许多生理特征。有必要确定哪些反射率指数提供了必要的信息,并显示了植物在不同条件下的反应14.在筛选耐性品种和植物表型时,非常需要确定高光谱指数与其他生理性状之间的相关性55。本研究采用涝渍处理的植物在叶绿素含量和VNIR成像的光合效率上表现出明显的响应。此外,由于气孔规律和叶片含水量的不同,在热处理和涝渍下,SWIR成像计算的水分指数观察到不同的响应。
因此,这些发现突出了这种方法在优化设置后的实用性,以及使用多个传感器来找到与气候耐受性相关的压力特征的潜力。使用多个成像传感器评估反应的动态可以用作改进育种计划的有力工具之一。
披露声明
作者声明,他们没有已知的相互竞争的经济利益或个人关系,这些利益或个人关系可能会影响本文所报告的工作。
致谢
该ADAPT项目(耐多重胁迫马铃薯的加速开发)已获得欧盟地平线2020研究和创新计划的资助,资助协议编号为GA 2020 862-858。这项工作得到了捷克共和国教育、青年和体育部的部分支持,得到了欧洲区域发展基金“SINGING PLANT”项目的部分支持。CZ.02.1.01/0.0/0.0/16_026/0008446)。CEITEC MU的核心设施植物科学因其栽培设施支持而受到认可。我们感谢 Meijer BV 提供本研究中使用的体外插条。我们感谢 Lenka Sochurkova 协助图 2 的图形设计,感谢 Pavla Homolová 在 Photon Systems Instruments (PSI) 研究中心(捷克共和国德拉索夫)的实验中帮助准备植物材料。
材料
| Name | Company | Catalog Number | Comments |
| 1.1” CMOS Sensor with RGB camera | PSI, Drásov, Czech Republic | https://psi.cz/ | The sensor delivers a resolution of 4112 × 4168 pixels for side view and 2560 × 1920 pixels for top view. The sensor is extremely sensitive and is a real megapixel CCD replacement and produces sharp, low-noise images |
| FluorCam | PSI, Drásov, Czech Republic | FC1300/8080-15 | Pulse amplitude modulated (PAM) chlorophyll fluorometer |
| Fluorcam 10 software | PSI, Drásov, Czech Republic | Version 1.0.0.18106 | For Chlorophyll fluorescence images visualization and analysis |
| GigE PSI RGB – 12.36 Megapixels Camera | PSI, Drásov, Czech Republic | https://psi.cz/ | For the side view projections, line scan mode was used with a resolution of 4112 px/line, 200 lines per second. The imaged area from the side view was 1205 × 1005 mm (height × width), while the imaged area from the top view position was 800 × 800 mm. |
| Hyperspectral Analyzer software | PSI, Drásov, Czech Republic | Version 1.0.0.14 | For hyperspectral images visualization and analysis |
| Hyperspectral camera HC-900 Series | PSI, Drásov, Czech Republic | https://hyperspec.org/products/ | Visible-near-infrared (VNIR) camera 380-900 nm with a spectral resolution of 0.8 nm FWHM |
| Hyperspectral camera SWIR1700 | PSI, Drásov, Czech Republic | https://hyperspec.org/products/ | Short-wavelength infrared camera (SWIR) camera 900 - 1700 nm with a spectral resolution of 2 nm FWHM |
| InfraTec thermal camera (VarioCam HEAD 820(800)) | Flir, United States | https://www.infratec.eu/thermography/infrared-camera/variocam-hd-head-800/ | Resolution of 1024 × 768 pixels, thermal sensitivity of < 20 mK and thermal emissivity value set default to 0.95. with a scanning speed of 30 Hz and each line consisting of 768 pixels. The imaged area was 1205 × 1005 mm (height × width). |
| LED panel | PSI, Drásov, Czech Republic | https://led-growing-lights.com/products/ | Equipped with 4 × 240 red-orange (618 nm), 120 cool-white LEDs (6500 K) and 240 far-red LEDs (735 nm) distributed equally over an imaging area of 80 × 80 cm |
| Light, temperature and relative humidity sensors | PSI, Drásov, Czech Republic | https://psi.cz/ | Sensors used to monitor controlled conditions in greenhouse |
| MEGASTOP Blue mats | Friedola | 75831 | To cover soil surface |
| Morphoanalyzer software | PSI, Drásov, Czech Republic | Version 1.0.9.8 | For RGB images visualization and analysis and color segmentation analysis |
| PlantScreen Data Analyzer software (Version 3.3.17.0) | PSI, Drásov, Czech Republic | https://plantphenotyping.com/products/plantscreen-modular-system/ | To visualize and analyze the data from all imaging sensors, watering-weighing unit and environmental conditions in greenhouse |
| PlantScreen Modular system | PSI, Drásov, Czech Republic | https://plantphenotyping.com/products/plantscreen-modular-system/ | Type of phenotyping platform |
| Plantscreen Scheduler software | PSI, Drásov, Czech Republic | Version 2.6.8368.25987 | To plan the experiment and set the measuring protocol |
| SpectraPen MINI | PSI, Drásov, Czech Republic | https://handheld.psi.cz/products/spectrapen-mini/#details | Light meter to adjust light level on a canopy level |
| TOMI-2 high-resolution camera | PSI, Drásov, Czech Republic | https://fluorcams.psi.cz/products/handy-fluorcam/ | Resolution of 1360 × 1024 pixels, frame rate 20 fps and 16-bit depth) with a 7-position filter wheel is mounted on a robotic arm positioned in the middle of the multi-color LED light panel with dimensions of 1326 x 1586 mm. |
| Walk-in FytoScope growth chamber | PSI, Drásov, Czech Republic | https://growth-chambers.com/products/walk-in-fytoscope-fs-wi/ | Type of chambers used to grow the plant |
参考文献
- Climate Change 2021: The Physical Science Basis. IPCC Available from: https://www.ipcc.ch/report/ar6/wg1/ (2021)
- Ray, D. K., Gerber, J. S., Macdonald, G. K., West, P. C. Climate variation explains a third of global crop yield variability. Nat Commun. 6, 5989 (2015).
- Acevedo, M., et al. A scoping review of adoption of climate-resilient crops by small-scale producers in low- and middle-income countries. Nat Plants. 6 (10), 1231-1241 (2020).
- van Dijk, M., Morley, T., Rau, M. L., Saghai, Y. A meta-analysis of projected global food demand and population at risk of hunger for the period 2010-2050. Nat Food. 2 (7), 494-501 (2021).
- Handayani, T., Gilani, S. A., Watanabe, K. N. Climatic changes and potatoes: How can we cope with the abiotic stresses. Breed Sci. 69 (4), 545-563 (2019).
- Devaux, A., Goffart, J. P., Kromann, P., Andrade-Piedra, J., Polar, V., Hareau, G. The potato of the future: Opportunities and challenges in sustainable agri-food systems. Potato Res. 64 (4), 681-720 (2021).
- Dahal, K., Li, X. Q., Tai, H., Creelman, A., Bizimungu, B. Improving potato stress tolerance and tuber yield under a climate change scenario - a current overview. Front Plant Sci. 10, 563 (2019).
- Ahmad, U., Sharma, L. A review of best management practices for potato crop using precision agricultural technologies. Smart Agricultural Technology. 4, 100220 (2023).
- Cabello, R., Monneveux, P., De Mendiburu, F., Bonierbale, M. Comparison of yield based drought tolerance indices in improved varieties, genetic stocks and landraces of potato (Solanum tuberosum L). Euphytica. 193 (2), 147-156 (2013).
- von Gehren, P., et al. Farmers feel the climate change: Variety choice as an adaptation strategy of European potato farmers. Climate. 11 (9), 189 (2023).
- Fiorani, F., Schurr, U. Future scenarios for plant phenotyping. Annu Rev Plant Biol. 64, 267-291 (2013).
- Poorter, H., et al. Pitfalls and potential of high-throughput plant phenotyping platforms. Front Plant Sci. 14, 1233794 (2023).
- Berger, B., de Regt, B., Tester, M. High-throughput phenotyping of plant shoots. Methods Mol Biol. 918, 9-20 (2012).
- Humplík, J. F., Lazár, D., Husičková, A., Spíchal, L. Automated phenotyping of plant shoots using imaging methods for analysis of plant stress responses - a review. Plant Methods. 11, 29 (2015).
- Danilevicz, M. F., Bayer, P. E., Nestor, B. J., Bennamoun, M., Edwards, D. Resources for image-based high-throughput phenotyping in crops and data sharing challenges. Plant Physiol. 187 (2), 699-715 (2021).
- Abebe, A. M., Kim, Y., Kim, J., Kim, S. L., Baek, J. Image-based high-throughput phenotyping in horticultural crops. Plants. 12 (10), 2061 (2023).
- Lazarević, B., Carović-Stanko, K., Safner, T., Poljak, M. Study of high-temperature-induced morphological and physiological changes in potato using nondestructive plant phenotyping. Plants. 11 (24), 3534 (2022).
- Marchetti, C. F., et al. A novel image-based screening method to study water-deficit response and recovery of barley populations using canopy dynamics phenotyping and simple metabolite profiling. Front Plant Sci. 10, 1252 (2019).
- Kim, S. L., et al. High-throughput phenotyping platform for analyzing drought tolerance in rice. Planta. 252 (3), 38 (2020).
- Abdelhakim, L. O. A., Rosenqvist, E., Wollenweber, B., Spyroglou, I., Ottosen, C. O., Panzarová, K. Investigating combined drought- and heat stress effects in wheat under controlled conditions by dynamic image-based phenotyping. Agronomy. 11 (2), 364 (2021).
- Zandalinas, S. I., Sengupta, S., Fritschi, F. B., Azad, R. K., Nechushtai, R., Mittler, R. The impact of multifactorial stress combination on plant growth and survival. New Phytologist. 230 (3), 1034-1048 (2021).
- Raza, A., et al. Impact of climate change on crops adaptation and strategies to tackle its outcome: A review. Plants. 8 (2), 34 (2019).
- Nasir, M. W., Toth, Z. Effect of drought stress on potato production: A review. Agronomy. 12 (3), 635 (2022).
- Wagg, C., Hann, S., Kupriyanovich, Y., Li, S. Timing of short period water stress determines potato plant growth, yield and tuber quality. Agric Water Manag. 247, 106731 (2021).
- Yamauchi, T., Colmer, T. D., Pedersen, O., Nakazono, M. Regulation of root traits for internal aeration and tolerance to soil waterlogging-flooding stress. Plant Physiol. 176 (2), 1118-1130 (2018).
- Aien, A., Chaturvedi, A. K., Bahuguna, R. N., Pal, M. Phenological sensitivity to high temperature stress determines dry matter partitioning and yield in potato. Indian J Plant Physiol. 22 (1), 63-69 (2017).
- Zandalinas, S. I., Mittler, R., Balfagón, D., Arbona, V., Gómez-Cadenas, A. Plant adaptations to the combination of drought and high temperatures. Physiol Plant. 162 (1), 2-12 (2018).
- Suzuki, N., Rivero, R. M., Shulaev, V., Blumwald, E., Mittler, R. Abiotic and biotic stress combinations. New Phytologist. 203 (1), 32-43 (2014).
- Atkinson, N. J., Jain, R., Urwin, P. E. The Response of Plants to Simultaneous Biotic and Abiotic Stress. Combined Stresses in Plants. , (2015).
- Harris, P. M., Harris, P. M. . The Potato Crop. 2nd ed. , (1992).
- Weisz, R., Kaminski, J., Smilowitz, Z. Water deficit effects on potato leaf growth and transpiration: Utilizing fraction extractable soil water for comparison with other crops. Am Potato J. 71 (12), 829-840 (1994).
- Wang, X., Vignjevic, M., Jiang, D., Jacobsen, S., Wollenweber, B. Improved tolerance to drought stress after anthesis due to priming before anthesis in wheat (Triticum aestivum L.) var. Vinjett. J Exp Bot. 65 (22), 6441-6456 (2014).
- Junker, A., et al. Optimizing experimental procedures for quantitative evaluation of crop plant performance in high throughput phenotyping systems. Front Plant Sci. 5, 770 (2015).
- Smith, S. M., et al. Diurnal changes in the transcriptome encoding enzymes of starch metabolism provide evidence for both transcriptional and posttranscriptional regulation of starch metabolism in arabidopsis leaves. Plant Physiol. 136 (1), 2687-2699 (2004).
- Findurová, H., Veselá, B., Panzarová, K., Pytela, J., Trtílek, M., Klem, K. Phenotyping drought tolerance and yield performance of barley using a combination of imaging methods. Environ Exp Bot. 209, 105314 (2023).
- Klukas, C., Chen, D., Pape, J. M. Integrated analysis platform: an open-source information system for high-throughput plant phenotyping. Plant Physiol. 165 (2), 506-518 (2014).
- Paul, K., et al. Understanding the biostimulant action of vegetal-derived protein hydrolysates by high-throughput plant phenotyping and metabolomics: A case study on tomato. Front Plant Sci. 10, 47 (2019).
- Awlia, M., et al. High-throughput non-destructive phenotyping of traits that contribute to salinity tolerance in Arabidopsis thaliana. Front Plant Sci. 7, 1414 (2016).
- Li, Z., Guo, R., Li, M., Chen, Y., Li, G. A review of computer vision technologies for plant phenotyping. Comput Electron Agric. 176, 105672 (2020).
- Li, L., Zhang, Q., Huang, D. A review of imaging techniques for plant phenotyping. Sensors (Switzerland). 14 (11), 20078-20111 (2014).
- Obidiegwu, J. E., Bryan, G. J., Jones, H. G., Prashar, A. Coping with drought: Stress and adaptive responses in potato and perspectives for improvement. Front Plant Sci. 6, 542 (2015).
- Zhang, H., Zhao, Y., Zhu, J. K. Thriving under stress: How plants balance growth and the stress response. Dev Cell. 55 (5), 529-543 (2020).
- Bandurska, H. Drought stress responses: Coping strategy and resistance. Plants. 11 (7), 922 (2022).
- Wingler, A., Lea, P. J., Quick, W. P., Leegood, R. C. Photorespiration: metabolic pathways and their role in stress protection. Philos Trans R Soc Lond B Biol Sci. 355 (1402), 1517-1529 (2000).
- Baker, N. R., Rosenqvist, E. Applications of chlorophyll fluorescence can improve crop production strategies: an examination of future possibilities. J Exp Bot. 55 (403), 1607-1621 (2004).
- Georgieva, M., Vassileva, V. Stress management in plants: Examining Provisional and Unique Dose-Dependent Responses. Int J Mol Sci. 24 (6), 5105 (2023).
- Leeggangers, H. A. C. F., Rodriguez-Granados, N. Y., Macias-Honti, M. G., Sasidharan, R. A helping hand when drowning: The versatile role of ethylene in root flooding resilience. Environ Exp Bot. 213, 105422 (2023).
- Baker, N. R. Chlorophyll fluorescence: a probe of photosynthesis in vivo. Annu Rev Plant Biol. 59 (1), 89-113 (2008).
- Murchie, E. H., Lawson, T. Chlorophyll fluorescence analysis: a guide to good practice and understanding some new applications. J Exp Bot. 64 (13), 3983-3998 (2013).
- Maxwell, K., Johnson, G. N. Chlorophyll fluorescence-a practical guide. J Exp Bot. 51 (345), 659-668 (2000).
- Yokoyama, G., Ono, S., Yasutake, D., Hidaka, K., Hirota, T. Diurnal changes in the stomatal, mesophyll, and biochemical limitations of photosynthesis in well-watered greenhouse-grown strawberries. Photosynthetica. 61 (1), 1-12 (2023).
- Jones, H. G. Application of thermal imaging and infrared sensing in plant physiology and ecophysiology. Advances in Botanical Research. 41, 107-163 (2004).
- Brainard, S. H., Bustamante, J. A., Dawson, J. C., Spalding, E. P., Goldman, I. L. A digital image-based phenotyping platform for analyzing root shape attributes in carrot. Front Plant Sci. 12, 690031 (2021).
- Huber, S., Tagesson, T., Fensholt, R. An automated field spectrometer system for studying VIS, NIR and SWIR anisotropy for semi-arid savanna. Remote Sens Environ. 152, 547-556 (2014).
- Mertens, S., et al. Proximal hyperspectral imaging detects diurnal and drought-induced changes in maize physiology. Front Plant Sci. 12, 640914 (2021).
转载和许可
请求许可使用此 JoVE 文章的文本或图形
请求许可探索更多文章
This article has been published
Video Coming Soon
版权所属 © 2025 MyJoVE 公司版权所有,本公司不涉及任何医疗业务和医疗服务。