Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
In vitro Uncoating von HIV-1-Kerne
In diesem Artikel
Zusammenfassung
Uncoating ist ein wesentlicher Schritt in der frühen Phase der HIV-1 Lebenszyklus und wird als der Demontage der Kapsid-Shell und die Freisetzung des viralen Ribonukleoproteinkomplex (vRNP) definiert. Hier zeigen wir Techniken zur Isolierung von intakten Kernen aus HIV-1 Virionen und zur Quantifizierung ihrer uncoating In-vitro-.
Zusammenfassung
Das Genom der Retroviren ist verpackt in einem Kapsid von einer Lipid-Hülle umgeben. Für Lentiviren wie HIV-1, ist die konische Kapsid Schale CA-Protein als ein Gitter aus Sechseck angeordnet sind. Das Kapsid ist um 7 Pentamere auf das breite Ende und 5 am schmalen Ende des Konus 1, 2 geschlossen. Eingeschlossen in diese Kapsid-Shell ist die virale Ribonukleoproteinkomplex, und zusammen umfassen sie den Kern.
Nach der Fusion der Virushülle mit der Zellmembran Ziel ist die HIV-1 in das Zytoplasma freigesetzt. Das Capsid dann zerlegt veröffentlicht kostenlose CA in die lösliche Form 3 in einem Prozess genannt uncoating. Die intrazelluläre Ort und Zeitpunkt des HIV-1 uncoating sind weitgehend unverstanden. Einzel-Aminosäure-Substitutionen in CA, dass die Stabilität des Kapsid verändern ebenfalls beeinträchtigen die Fähigkeit des HIV-1 auf Zellen 4 zu infizieren. Dies deutet darauf hin, dass die Stabilität des Kapsid von entscheidender Bedeutung für HIV-1 Infektion ist. HIV-1 uncoating wurde schwer Studie aufgrund mangelnder Verfügbarkeit von sensitiven und zuverlässigen Tests für diesen Prozess. Hier beschreiben wir eine quantitative Methode zur Untersuchung uncoating in vitro mit Kernen von infektiösen HIV-1 Partikel isoliert. Der Ansatz beinhaltet Isolierung der Kerne durch Sedimentation von konzentrierten Virionen durch eine Schicht von Wasch-und in eine lineare Saccharose-Gradienten, in der Kälte. Zur Quantifizierung uncoating werden die isolierten Kerne bei 37 ° C für verschiedene Zeitintervalle und anschließend pelletiert durch Ultrazentrifugation. Das Ausmaß der uncoating wird durch die Quantifizierung der Anteil der CA in den Überstand analysiert. Dieser Ansatz wurde eingesetzt, um Effekte von viralen Mutationen auf HIV-1 Capsid Stabilität 4, 5, 6 zu analysieren. Es sollte auch für die Untersuchung der Rolle zellulärer Faktoren in HIV-1 uncoating.
Protokoll
1. Produktion von HIV-1 Partikel
Bevor Sie fortfahren, müssen Sie eine Genehmigung erhalten und befolgen Sie die Anweisungen aus dem Biosafety Büro Ihrer Institution in einem Biosafety-Anlage für infektiöse HIV genehmigten Arbeitsprogramms. Sie müssen sicherstellen, dass die richtige Pflege und Sicherheitshinweise sind während der Arbeitszeit in der Biosicherheit Labor.
Produktion von HIV-1 Partikel ist in der Regel durch transiente Transfektion von 293T-Zellen mit HIV-1 Provirus-DNA mit Hilfe eines Calciumphosphat-Transfektion Methode 7, 8 durchgeführt. Hohe Titer Virusstocks durch Kultur von infizierten T-Zellen gezüchtet sind ebenfalls geeignet.
- Kultur 293T-Zellen in Dulbecco Modified Eagle Medium (DMEM) mit 10% fötalem Rinderserum (FBS) und ergänzt mit Antibiotika [Penicillin (100 IU / ml) und Streptomycin (100 ug / ml)] bei 37 ° C, 5% CO 2 .
- Lösen Zellen aus nahezu konfluenten Gerichte mit 0,25% Trypsin-EDTA und Saatgut 2x10 6 Zellen in 9 ml pro 100 mm Kulturschale einen Tag vor der Transfektion. Seed sechs 100 mm Kulturschalen für die Produktion von Virionen. Wenn konzentrierte Vorbereitung von Kernen benötigt wird, könnte mehr Gerichte für die Transfektion ausgesät werden.
- Am nächsten Tag sollte der Zellrasen werden etwa 25% konfluent und bereit für die Transfektion. Seit sechs Gerichte der Zellen transfiziert werden, bringen 120 pg Provirus-DNA bis zu einem Volumen von 2,7 ml mit sterilem Wasser. Zu dieser Mischung hinzu 0,3 ml von 2,5 M CaCl 2 und 3 ml 2XBBS, und mischen Sie richtig durch und Abpipettieren mehrmals. Lassen Sie die Mischung bei Raumtemperatur für 10-20 Minuten stehen lassen.
- 1 ml der resultierenden Mischung tropfenweise in die Mitte von jedem Gericht, während vorsichtiges Schwenken mischen. Die Schalen werden über Nacht (~ 16 Stunden) in einem Inkubator eingestellt bei 35 ° C und 3% CO 2.
- Absaugen des Kulturmediums und sanft mit 5 ml PBS.
- Absaugen PBS und 5 ml frisches Medium. Kultur der Zellen im Brutschrank bei 37 ° C und 5% CO 2 für zusätzliche 24-48 Stunden.
- Sammeln Sie die Kulturüberstand mit viralen Partikeln, die Übertragung auf einen 50 ml konischen Zentrifugenröhrchen. Kombinieren Sie die Überstände von allen Gerichten und Zentrifuge bei 1.500 xg für 5 min auf Pellet-Zellen und Trümmer. Den Überstand mit 0,45 um Porengröße Spritzenvorsatzfilter. Es sollten Vorkehrungen getroffen, um die Bildung von Aerosolen zu minimieren und gleichzeitig die Zusammenarbeit mit der Live-Virus sein. Dies beinhaltet die Nutzung des konischen Röhrchen mit O-Ringen oder Rotor Eimer deckt während der Zentrifugationsschritt. Wenn dies nicht möglich ist, sollten die Verschlusskappen der Tuben mit Parafilm umwickelt werden.
2. Die Konzentration von HIV-1 Virionen durch Ultrazentrifugation
- Setzen Sie den Kulturüberstand (30 ml) in einem 38,5 ml Polyallomer Zentrifugenröhrchen (für Beckman SW32Ti Rotor oder gleichwertig). Gently Unterlage das Virus enthaltende Überstand mit 5 ml Lösung von 20% Saccharose in PBS mit einer 5 ml Pipette.
- Zentrifuge für 3 Stunden bei32.000 rpm bei 4 ° C (175.000 xg und r max) zu Pellets Viruspartikel.
- Entfernen Überstände durch Absaugen, dabei nicht auf die Pellet am Boden des Röhrchens zu stören. 0,5 ml 1XSTE Puffer (10 mM Tris-HCl [pH 7,4], 100 mM NaCl, 1 mM EDTA) auf die Tube und bei 4 ° C für 1 Stunde, um das Pellet zu lösen. Mit einer breit Bohrung 1 ml Pipettenspitze vorsichtig pipet nach oben und unten ein paar Mal, um das Pellet aus dem Boden des Röhrchens zu lösen. Als nächstes übertragen Sie die gelösten Pellets in ein 1,5 ml Mikrozentrifugenröhrchen, kümmert Schaumbildung zu vermeiden. Inkubation bei 4 ° C für weitere 1-3 Stunden, damit der kleine Klumpen von Viren zu zerstreuen. Während dieser Zeit bereiten die Saccharose-Gradienten wie in Schritt 3.1 beschrieben.
- Vorsichtig pipet die Virussuspension nach oben und unten mehrere Male, und Zentrifuge bei 8.000 Umdrehungen pro Minute (6.000 xg) bei 4 ° C in einem gekühlten Mikrozentrifuge für 1 min zu entfernen verbleibende Klumpen. Halten Sie die Probe kalt während dieses Prozesses.
3. Saccharose-GradientenZentrifugation, um Kerne zu isolieren
HIV-1-Kerne werden getrennt mit einem "spin-thru"-Methode 9, die eine Änderung der zuvor beschriebenen Verfahren zur Reinigung von HIV-2-Kerne 10 ist.
- Bereiten Sie eine 12 ml linear um 30% auf 70% Saccharose-Gradienten in 1XSTE Puffer in einem 14,5 ml Polyallomer Zentrifugenröhrchen für SW32.1Ti Rotor. Zur Vorbereitung Gradienten, verwenden Sie eine 20 ml Gradienten ehemaligen, Platz 6 ml 70% Saccharose-Lösung auf der uns zugewandten Seite (in der Nähe der Austrittsöffnung) und 6 ml 30% Saccharose-Lösung auf der anderen Seite. Stellen Sie sicher, dass keine Luftblasen in den Kanal zwischen den beiden Kammern eingeschlossen. Verwenden Sie das Auto Densi-Flow Gradientenformer zu den Gradienten von unten nach oben in der Röhre mit 1 ml 85% Saccharose-Lösung am Boden zu pumpen. Sanft statt dem Gradienten bei 4 ° C abgekühlt, bis (2-4 Stunden).
- Mit einer breit Bohrung 1 ml Pipettenspitze vorsichtig Overlay die Steigung mit 0,25 ml 15% Saccharose-Lösung in STE mit 1% Triton X-100.
- Gently Overlay mit 0,25 ml 7,5% Saccharose-Lösung in STE mit einem breiten Bohrung 1 ml Pipettenspitze. Achten Sie darauf, um die Schichten zu mischen.
- Gently Overlay mit 0,5 ml Virussuspension von Schritt 2.4. Dieser Schritt sollte sorgfältig durchgeführt werden, um jede Störung in der Steigung und Mischen des unterlegten Saccharose Schichten zu vermeiden.
- Legen Sie die Rohre in die vorgekühlte SW32.1Ti Eimer und Zentrifuge auf 32.000 rpm (187.000 xg und r max) über Nacht (16-20 Stunden) bei 4 ° C. Um zu vermeiden, Pausieren der Zentrifuge nicht starten Zentrifugieren, bis das Vakuum in der Zentrifuge erreicht 250 pm
- Sammeln Sie 1 ml Fraktionen von oben nach unten von der Steigung mit dem Auto-Densi-Flow Gradient Fraktionator. Die Röhrchen auf Eis sofort bei der Abholung. Mischen Sie den Inhalt der Rohre durch Invertieren paar Mal, und ziehen Sie 50 ul jeder Fraktion für die Quantifizierung durch ELISA oder Reverse-Transkriptase-Aktivitäts-Assay.
4. Lokalisierung von HIV-1-Kerneund Lagerung der Kerne
- Vor der Durchführung uncoating Assays, ist es wichtig zu bestimmen, welche Fraktionen erhalten HIV-1-Kerne enthalten. Dies kann durch p24 ELISA oder Reverse-Transkriptase-Aktivitäts-Assay unter Verwendung der 50 ul Aliquots aus Schritt 3.6 bestimmt werden.
- Die Rückgewinnung von CA mit den Kernen lässt sich oft um die Stabilität der Kerne zusammen. Messen Sie den Kern verbunden CA von p24 ELISA 9 mit einer Probe aus jeder Fraktion. Alternativ messen Sie die Reverse-Transkriptase-Aktivität der einzelnen Fraktionen. Mit beiden Methoden der Spitze sollte etwa Fraktion 10 werden.
- Pool der Fraktionen, die Kerne. Wenn die Kerne sind nicht für uncoating Assay sofort Aliquot der gepoolten Kerne in 0,2 bis 0,3 ml Aliquots, flash-freeze in flüssigem N2 und bei -80 ° C eingesetzt werden Cores auf diese Weise eingefroren eignen sich für die uncoating Assay. Die Ausbeute der Kern-assoziierten CA ist in der Regel 1-2 ug von p24 pro Milliliter oder etwa 15% der gesamten Virion-assoziiertenp24.
5. Kinetic Assay von HIV-1 uncoating
- Die Höhe der HIV-1-Kerne je uncoating Reaktion erforderlich ist, etwa 50 ng. Zur Durchführung der in vitro-Assay uncoating, vorzuverdünnen der Aliquot-Kerne mit dem gleichen Volumen kalten 1XSTE Puffer, um die Viskosität der Suspension zu reduzieren und Pipettieren Fehler zu minimieren.
- Weitere verdünnten 100 ul der Kerne in 0,15 ml kaltem 1XSTE Puffer mit 10 pg / ml BSA in einem 1,5 ml Reaktionsgefäß. Wir ergänzen die STE-Puffer mit BSA (10 pg / ml) zur Adsorption von CA an die Wände der Röhre zu minimieren. Mix durch Invertieren des Röhrchens mehrmals. Nicht vortexen der Proben. Die Röhrchen in ein Wasserbad bei 37 ° C für Zeitintervallen (15, 30, 60 und 120 min). Die Rohre sollten in das Wasser getaucht mindestens bis auf die Ebene der internen Stichprobe sein, um auch Erwärmung zu gewährleisten.
- Während der Inkubation vorsichtig mischen Sie den Inhalt des Röhrchens in regelmäßigen Abständen (in der Regel 5 -10 min) durch blätterte die Röhre. Für eine Null-Minuten-Steuerung, verdünnte 100 ul der Kerne in 0,15 ml kaltem 1XSTE Puffer und Inkubation auf Eis für die gesamte Länge des Experiments (120 min). Die Null-Minuten-Steuerung gibt dem basalen uncoating Wert und wird verwendet, um Erhöhung der uncoating von Kernen bei 37 ° C für verschiedene Zeitintervalle inkubiert bestimmen.
- Am Ende der Inkubationszeit, stoppen Sie den uncoating Prozess, indem die Rohre in Eis für 10 Minuten.
- Zentrifugieren bei 45.000 rpm (TLA-55 Rotor, 125.000 xg und r max) für 20 Minuten bei 4 ° C. Dies wird Pellet intakten Kernen und den freien CA als Folge der uncoating der Kerne freigesetzt wird im Überstand verbleiben. Der Rotor bei 4 ° C vorgekühlt werden vor dem Laden der Proben.
- Übertragen Sie den Überstand auf neue vorgekühlt Mikrozentrifugenröhrchen vorzugsweise unter Verwendung von Gel-loading Tipps bei Raumtemperatur gelagert. Bitte beachten Sie, dass die Pellets nicht sichtbar für das bloße Auge, so wenden äußerste Sorgfalt an während Pipettieren aus dem Überstand. Resuspendieren der Pellets in 250 ul ELISA Probenverdünner (0,5% Triton X-100 und 5% Donor Kälberserum in PBS). Um eine effiziente Auflösung der Pellet-, Wirbel nach der Zugabe der ELISA Probenverdünner gewährleisten. Quantifizierung der CA Inhalt der Pellet und Überstand mit p24 ELISA wie im folgenden Abschnitt beschrieben.
- Das Ausmaß der uncoating wird durch die Berechnung des Anteils der CA im Überstand erhalten.
6. Assay für CA von p24 ELISA
- Viele kommerzielle ELISA-Kits sind verfügbar und können verwendet werden, um CA zu quantifizieren. Verwenden Sie einen kommerziellen oder "in-house" ELISA und beinhalten p24-Standards, um die Linearität des Tests zu bestimmen. Verdünnungen der Proben sollte getestet werden, um die Genauigkeit zu gewährleisten.
- Wir haben eine hausgemachte ELISA, die wir routinemäßig Assay für CA Einsatz entwickelt. Das Verfahren ist aus einem früheren Bericht 11 angepasst und wird mit Erfassung und Detektor-Antikörper erhältlich NIH-HILFES Forschung und Reference Reagent Program.
7. Repräsentative Ergebnisse:
Ein Beispiel für ein Ergebnis aus ELISA zur Bestimmung von Fraktionen, die Kern ist in Abbildung 1 dargestellt. Nach dem Sammeln von Fraktionen (1 ml) wurden 50 ul Probe von jeder Fraktion zur seriellen Verdünnungen machen und mittels ELISA. Die gesamte p24, indem die Werte für zwölf Fraktionen betrug 14,5 pg. Wie in der Abbildung Fraktionen 8 bis 10 enthaltenen Kerne gezeigt. Die p24-Wert für die Kern-Fraktionen war 2,17 pg. Der Anteil der Kern-assoziierten p24 (14,97%) wurde durch Bildung des Verhältnisses von p24-Wert für den Kern Fraktionen (2,17 pg) zu den gesamten p24-Wert (14,5 pg) ermittelt. Fraction 1 oder 2 enthält immer höchste Menge an p24, das entspricht freie CA, die nicht mit den Kernen verbunden ist. Dies wird durch eine schrittweise Verringerung der p24-Werte mit jedem weiteren Teil, dann einen starken Anstieg und schließlich ein starker Abfall der p24 gefolgtWerte. Wenn die richtige Pflege genommen wird beim Laden der Gradient dann den Gipfel des Kern-assoziierten CA ist um Fraktion 10 gefunden.
Ein typisches Ergebnis durch Testen der Kinetik der uncoating von HIV-1 gewonnenen Bohrkerne wird in Abbildung 2 dargestellt. Die Grafik zeigt eine zeitabhängige Zunahme uncoating von Wildtyp-HIV-1-Kerne. Der prozentuale uncoating Wert wurde durch die Berechnung des Anteils der CA im Überstand erhalten. Mit etwas Übung, ist der Test in hohem Maße reproduzierbar und ist nützlich für die Bestimmung der Stabilität von viralen Cores in vitro. Bitte beachten Sie, dass die Reproduzierbarkeit des Tests stark abhängig von der richtigen Handhabung der Proben während des Verfahrens ist. Da die Kerne hitzelabil sind, sollten die Proben bei 4 ° C während des Tests nur während der Inkubationszeit gehalten werden.
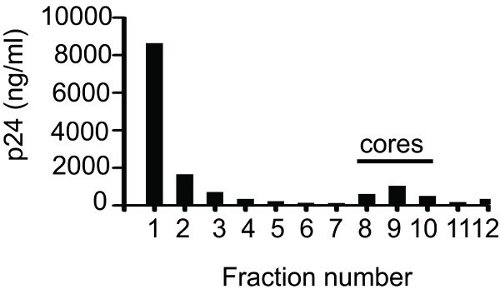
Abbildung 1 Equilibrium Dichtegradientenzentrifugation vonHIV-1-Kerne. Eine konzentrierte Virussuspension wurde an die Spitze einer 30 bis 70% linear Sucrosegradienten mit 1% Triton-X-100 überlagert angewendet. Nach über Nacht Zentrifugation bei 187.000 xg und 4 ° C, 1 ml Fraktionen wurden von oben (Fraktion 1) nach unten (Fraktion 12) gesammelt und p24 wurde mittels ELISA quantifiziert.
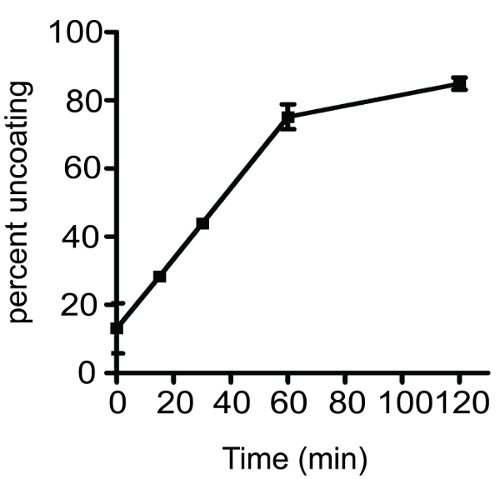
Abbildung 2 Zeitlicher Verlauf der HIV-1 uncoating in vitro. Gereinigte HIV-1-Kerne wurden verdünnt und bei 37 ° C für die angegebenen Zeitintervalle. Die Null-min-Probe wurde auf Eis für die gesamte Dauer des Experiments inkubiert. Nach der Inkubation wurden die Proben auf 125.000 xg für 20 Minuten bei 4 ° C ultrazentrifugiert Überstand und Pellets wurden getrennt und von p24 ELISA analysiert. Das Ausmaß der uncoating wurde bestimmt, wie im Protokoll Text beschrieben. Jeder uncoating Reaktion wurde doppelt durchgeführt; Fehlerbalken span Bereich der beiden Werte.
Diskussion
Die hier beschriebene Methode zur HIV-1-Kerne zu reinigen, um studieren uncoating in vitro ist für das Studium dieser Phase der HIV-1 Lebenszyklus, vor allem aufgrund der Nichtverfügbarkeit eine validierte Methode zur HIV-1 uncoating in Zielzellen zu analysieren nützlich. Obwohl diese Methode verwendet Gleichgewicht Ultrazentrifugation zu Kernen zu reinigen, andere haben direkte Pelletierung nach kurzer Lyse verwendet mit 1% Triton-X-100 12, 13 oder Pelletierung durch eine Saccharose-Kissen mit 0,1% Triton...
Offenlegungen
Keine Interessenskonflikte erklärt.
Danksagungen
HIV-1 uncoating Studien in den Aiken Labor wurden von NIH gewährt AI40364, AI50423 und AI076121 unterstützt. Mehrere wichtige Materialien, einschließlich Reagenzien in der p24 ELISA verwendet wurden, wurden durch die NIH AIDS Research and Reference Program, Division of AIDS, NIAID, NIH zur Verfügung gestellt.
Materialien
| Name | Company | Catalog Number | Comments |
| Name des Reagenzes | Firma | Katalog-Nummer | Kommentare (optional) |
| DMEM | CellGro | 10 bis 013-CV | |
| PBS | CellGro | 21 bis 031-CV | |
| Triton-X-100 | Mallinckrodt Baker Inc | 9002-93-1 | |
| Tween 20 | Acros | 9005-64-5 | |
| 0,25% Trypsin-EDTA | CellGro | 25 bis 053-CI | |
| 2XBBS | Zusammensetzung: 50 mM BES [p H 6.95], 280 mM NaCl und 1,5 mM Na 2 HPO 4. Der pH-Wert auf 6,95bei Raumtemperatur. Filter sterilisieren und lagern in Aliquots bei -20 ° C. | ||
| Coating-Antikörper: Monoklonale Antikörper gegen p24 (183-H12-5C) | NIH AIDS Research and Reference Reagent Programm | 3537 | |
| Primärer Antikörper: HIV-Ig (hyperimmune menschlichen Patienten Serum) | NIH AIDS Research and Reference Reagent Programm | 3957 | |
Sekundäre Antikörper: Anti-Human-IgG, Peroxidase-konjugierten | Durchstechen | 31130 | |
| HRP-Substrat | KPL Inc | 50-76-11 | |
| Immulon 2HB 96-Well-Platten | Thermo Scientific | 3455 | |
| SW32Ti und SW32.1 Ti Rotoren und kompatibel Ultrazentrifuge | Beckman Coulter | ||
| TLA-55 Rotor-und Tabletop-Ultrazentrifuge | Beckman Coulter | ||
| High speed Mikrozentrifugenröhrchen | Beckman Coulter | 326823, 358123, 357448 | |
| Auto-Densi Flow-Dichtegradienten Fraktionator | Labconco Corp | 4517000 | |
| Gradient Ehemalige | CBS Scientific Co. Inc. | GM-20 |
Referenzen
- Ganser, B. K., Li, S., Klishko, V. Y., Finch, J. T., Sundquist, W. I. Assembly and analysis of conical models for the HIV-1 core. Science. 283, 80-83 (1999).
- Li, S., Hill, C. P., Sundquist, W. I., Finch, J. T. Image reconstructions of helical assemblies of the HIV-1 CA protein. Nature. 407, 409-413 (2000).
- Aiken, C. Viral and cellular factors that regulate HIV-1 uncoating. Curr. Opin. HIV. AIDS. 1, 194-199 (2006).
- Forshey, B. M., Schwedler, U. v. o. n., Sundquist, W. I., Aiken, C. Formation of a human immunodeficiency virus type 1 core of optimal stability is crucial for viral replication. J. Virol. 76, 5667-5677 (2002).
- Forshey, B. M., Aiken, C. Disassembly of human immunodeficiency virus type 1 cores in vitro reveals association of Nef with the subviral ribonucleoprotein complex. J. Virol. 77, 4409-4414 (2003).
- Wacharapornin, P., Lauhakirti, D., Auewarakul, P. The effect of capsid mutations on HIV-1 uncoating. Virology. 358, 48-54 (2007).
- Chen, C., Okayama, H. High-efficiency transformation of mammalian cells by plasmid DNA. Mol Cell Biol. 7, 2745-2752 (1987).
- Aiken, C., Prasad, V. R., Ganjam, K. V. . Methods in Molecular Biology. 485, 41-53 (2009).
- Kotov, A., Zhou, J., Flicker, P., Aiken, C. Association of Nef with the human immunodeficiency virus type 1 core. J. Virol. 73, 8824-8830 (1999).
- Kewalramani, V. N., Emerman, M. Vpx association with mature core structures of HIV-2. Virology. 218, 159-168 (1996).
- Wehrly, K., Chesebro, B. p24 antigen capture assay for quantification of human immunodeficiency virus using readily available inexpensive reagents. Methods. 12, 288-293 (1997).
- Welker, R., Hohenberg, H., Tessmer, U., Huckhagel, C., Kräusslich, H. G. Biochemical and structural analysis of isolated mature cores of human immunodeficiency virus type 1. J. Virol. 74, 1168-1177 (2000).
- Briggs, J. A., Wilk, T., Welker, R., Kräusslich, H. G., Fuller, S. D. Structural organization of authentic, mature HIV-1 virions and cores. EMBO J. 22, 1707-1715 (2003).
- Auewarakul, P., Wacharapornin, P., Srichatrapimuk, S., Chutipongtanate, S., Puthavathana, P. Uncoating of HIV-1 requires cellular activation. Virology. 337, 93-101 (2005).
- Accola, M. A., Ohagen, A., Göttlinger, H. G. Isolation of human immunodeficiency virus type 1 cores: retention of Vpr in the absence of p6(gag. J. Virol. 74, 6198-6202 (2000).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten