Method Article
Erzeugung eines Immortalisierte Murine Gehirn mikrovaskulären Endothelzellen Zelllinie als
In diesem Artikel
Zusammenfassung
Diese Methode beschreibt, wie zu isolieren und zu verewigen mikrovaskulären Endothelzellen von der Maus Gehirn. Wir beschreiben ein Schritt-für-Schritt-Protokoll ausgehend von der Homogenisierung von Hirngewebe, Verdauungsschritten, Aussaat und Immortalisierung der Zellen. Normalerweise dauert es etwa fünf Wochen, um eine homogene, verewigt mikrovaskuläre Endothelzellen Zelllinie zu erhalten.
Zusammenfassung
Epithel-und Endothelzellen (EC) bauen parazellulären Barrieren, die das Gewebe aus der externen und internen Umwelt zu schützen. Die Blut-Hirn-Schranke (BHS), bestehend aus EG, Astrozyten end-Füße, Perizyten und die Basalmembran ist verantwortlich für den Schutz und die Homöostase des Hirnparenchym. In vitro BBB Modelle sind gemeinsame Instrumente, um die Struktur und Funktion des BBB studieren auf zellulärer Ebene. Eine beträchtliche Anzahl von verschiedenen in vitro BBB Modelle wurden für Forschung in verschiedenen Labors auf dem neuesten Stand eingerichtet. Normalerweise werden die Zellen von Rindern, Schweinen, Ratte oder Maus Hirngewebe (ausführlich im Aufsatz von Wilhelm et al. 1). Menschlichen Gewebeproben sind nur in einer begrenzten Anzahl von Labors oder Unternehmen 2,3. Während primäre Zellpräparationen zeitaufwendig sind und die EC-Kulturen können von Charge zu Charge unterschiedlich, verewigt die Gründung der EG-lines steht im Mittelpunkt des wissenschaftlichen Interesses.
Hier präsentieren wir eine Methode zur Festlegung einer immortalisierten Gehirn mikrovaskulären EC Linie von neonatalen Maus Gehirn. Wir beschreiben das Verfahren Schritt für Schritt verwalten die Reagenzien und Lösungen verwendet. Die Methode, mit unserem Labor etablierten ermöglicht die Isolierung eines homogenen verewigt Endothelzelllinie innerhalb von vier bis fünf Wochen. Das Gehirn mikrovaskulären endothelialen Zelllinien bezeichnet CEND 4 (aus Großhirnrinde) und cerebEND 5 (aus Kleinhirnrinde), wurden nach diesem Verfahren in der Förster Labor isoliert und sind effektiv zur Erläuterung der verschiedenen physiologischen und pathologischen Prozessen an der BHS verwendet. Verwendung CEND und cerebEND haben wir gezeigt, dass diese Zellen zu Glucocorticoid 4,6-9 reagieren und Östrogen-Behandlung 10 sowie pro-infammatory Mediatoren wie TNFalpha 5,8. Darüber hinaus haben wir die Pathologie Multiple sc studiertlerosis 11 und Hypoxie 12,13 auf der EG-Ebene. Die CEND und cerebEND Linien können als ein gutes Werkzeug zur Untersuchung der Struktur und Funktion der BBB, zellulärer Reaktionen von ECs auf verschiedene Reize oder die Interaktion der EG mit Lymphozyten oder Krebszellen in Betracht gezogen werden.
Protokoll
Ein. Isolierung von Hirnkapillaren
- Für jedes Präparat verwenden, fünf Minuten vor zehn neugeborenen Mäusen beiderlei Geschlechts (3-5 Tage alt).
- Euthanize eine Maus nach den örtlichen IACUC / Tierarzt Empfehlungen, entfernen Sie das Gehirn sofort, und der Transfer in eine Petrischale mit folgender Lösung: 15 mM Hepes (pH 7,4), 153 mM NaCl, 5,6 mM KCl, 2,3 mM CaCl 2 x 2H 2 O, 2,6 mM MgCl 2 x 6 H 2 O, 1% (w / v) BSA (im folgenden bezeichnet als Puffer A).
- Sofern nicht anders angegeben, sollten alle Isolierungsverfahren bei Raumtemperatur (RT) (22-24 ° C) unter der Sterilbank durchgeführt werden. Schneiden Sie die Gehirne (Großhirn, ohne Kleinhirn und Hirnstamm), nach dem Entfernen der Hirnhäute und Kapillar-Fragmente, in Puffer A mit einem sterilen Skalpell. Pipettieren Die Gewebestücke nach oben und unten mit einer 10 ml Pipette, bis keine Klumpen erscheinen. Man führt die Suspension in einen 50 ml-Falcon-Röhrchen und Zentrifuge bei 250 × g für 5 min bei RT.
Anmerkung: Meninges können als dünne, transparente Membranen an der Oberfläche des Hirngewebes identifiziert werden. Sie können vorsichtig mit sterilen Pinzetten entfernt werden.
- Überstand verwerfen.
- Das Pellet in 4,5 ml Puffer A mit 1,5 ml 0,75% (w / v) Collagenase / Dispase (Roche) und Inkubation für 45 min bei 37 ° C in einem Wasserbad (gelegentlich Schütteln).
- Inzwischen bereitet die 12-Well-Platten durch Beschichten vier Vertiefungen mit Kollagen IV (0,1 mg / ml in 50 mM Essigsäure gelöst). Lassen Sie für 1 Stunde halten.
- Stoppen Sie die Verdauung durch Zugabe von 15 ml eiskaltem Puffer A. das Pellet gründlich.
- Die Suspension bei 250 x g für 10 min bei RT.
- Überstand verwerfen.
- An Myelin zu entfernen, 10 ml 25% (w / v) BSA (Sigma, Reinheit> 98%) und Zentrifuge bei 1000 × g für 20 min bei 4 ° C. 25% BSA sollte in 1x PBS (PAA Laboratories) aufgelöst werden und durch 0,2 um filter).
- Vorsichtig den Überstand verwerfen, das Pellet in 10 ml Puffer A und übertragen auf ein neues Falcon-Röhrchen.
- Die Suspension bei 250 x g für 5 min bei RT. Das resultierende Pellet enthält die Endothelzellen.
- Zweimal waschen das Kollagen IV-beschichteten 12-Well-Platte mit PBS.
- Das Pellet in 4 ml Wachstumsmedium (DMEM mit 10% FCS, 50U/ml Penicillin / Streptomycin 1% L-Glutamin) und Platte die Zellsuspension in zwei Vertiefungen, 2 ml zu jeder Vertiefung. Hinzufügen des Puromycin zu einer Endkonzentration von 4 pg / ml und Inkubation für 45 min bei 37 ° C in einem Zellkulturbrutschrank. Dieser Schritt ermöglicht die Entfernung von schnell anhaftenden Zellen. Hinweis: Puromycin wird für 24 h zugegeben. Nur Gehirn ECs metabolisieren kann es für andere Zelltypen Puromycin toxischen 14 ist.
- Übertragen Sie die 2 ml Medium mit nicht verklebten Zellen aus Schritt 1,14 in zwei frische Brunnen (diese Vertiefungen enthalten die EG-Fraktion). Füllen Sie die Vertiefungen mit anhaftenden Zellen aus step 1,14 mit 2 ml frischem Medium (diese Vertiefungen enthalten anderen Zelltypen, wie Fibroblasten, Astrocyten und können parallel gezüchtet werden und für Vergleiche der Morphologie).
- Ändern Sie das Medium des folgenden Tages.
2. Immortalisierung der Gehirn mikrovaskulären Endothelzellen
- Kultivieren die GP + E-86 Neo (GPENeo) 15 Fibroblasten, sekretieren ein replikationsdefizienter Virus mit Polyoma mittleren T-Onkogen in DMEM Medium mit 10% hitzeinaktiviertem FCS, 50U/ml Penicillin / Streptomycin und 2 mg / ml G418 ( . PAA Laboratories) in Gelatine beschichteten Kolben Anmerkung: Polyoma mittleren T-Onkogen Transfektion bewirkt Wachstumsvorteil ECs über nicht ECs, die zu einer homogenen Monoschicht von Zellen mit endothelialen Morphologie 4 bis 6 Wochen der Kultur. GPENeo sind nicht im Handel erhältlich und können als gemeinsame öffentliche Material erhalten werden (siehe Originalarbeiten 4,16).
- Um das Virus enthaltende Medium für verwenden Immortalisierung kultivieren die GPENeo Zellen in G418-freiem Medium für 24 h.
- Entfernen 10 ml des Überstandes und GPEneo hinzuzufügen Polybrene (Hexadimethrinbromid) (Sigma) auf eine Endkonzentration von 8 ug / ml, durch 0,45 um Filter zu sterilisieren, um die zellulären Bruchstücke zu entfernen.
- Entfernen Sie das Wachstumsmedium von den EC-Kulturen in Teil 1 hergestellt und 2 ml GPEneo Überstand / Polybrene Mischung in die Vertiefungen. Wiederholen es am nächsten Tag mit einer frischen GPEneo Überstand / Polybrene Mischung Anmerkung:. Polybrene verwendet wird, um Poren in der Zellwand zu machen, um die Infektion mit den viralen Partikeln) zu erleichtern.
- Entfernen Sie die GPEneo Überstand / Polybrene Mischung am folgenden Tag, waschen Sie die Zellen zweimal mit PBS und pflegen die Zellen im Wachstumsmedium ändern Sie es alle 3 Tage. Bei Konfluenz spaltete die Zellen 1:2 auf Kollagen IV-beschichteten Platten.
- Normalerweise sollten stabile zerebralen Endothelzellen (CEND) Zelllinien 4-5 Wochen später erhalten werden.
- Tauen Sie die Zellen aus cryoaliquot im Wasserbad und Übertragung in 15 ml-Falcon mit 10 ml vorgewärmten Medium.
- Die Suspension bei 250 x g für 5 min bei RT.
- Entfernen Medium, übertragen die Pellets in der Kollagen IV beschichteten T 25 cm 2 Zellkulturflasche mit vorgewärmten Wachstumsmedium (Zelldichte für die Beschichtung sollte mindestens 1x 10 4 Zellen / ml).
- Ändern Medium am nächsten Tag und nachdem die Zellen erreicht Zusammenfluss (in der Regel nach 5 Tagen) spalten die Zellen.
4. Splitting der CEND-Zellen (Hinweis: Splitting nur einmal pro Woche getan werden sollte, vermeiden Splitting Höher als 1:4).
- Entfernen Medium, waschen Sie die Zellen mit PBS.
- 3 ml warmem Trypsin-EDTA-Lösung (PAA Laboratories) (T 75 cm 2-Kolben), bei 37 ° C und warten Sie, bis die Zellen Schicht verteilt ist (in der Regel innerhalb von 5 bis 15 min).
- 5 ml of Wachstumsmedium und Abpipettieren und Transfer zu einem neuen Kollagen IV-beschichteten Kolben.
5. Einfrieren von CEND-Zellen
- Besorgen Sie sich die Zellsuspension wie in Schritt 4 beschrieben
- Die Suspension bei 250 x g für 5 min bei RT.
- Zellpellet (aus 1 T 75 cm 2-Kolben) in 6 ml Einfriermedium (95% Wachstumsmedium, 5% DMSO).
- Teilen Sie die Zellsuspension in vier 1,5 ml Kryo-Aliquots. Hinweis: Ein Kryo-Aliquot auf T 25 cm 2 ausgesät werden.
- Bewahren Sie die Kryo-Aliquots in flüssigem Stickstoff Dampftemperatur.
CEND Wachstumsmedium: 450 ml DMEM, 10% FCS, 10 ml L-Glutamin, 2% MEM-Kit, 2% NEAA, 10 ml Natrium-Pyruvat, 50 U / ml Penicillin / Streptomycin
6. Repräsentative Ergebnisse
Die CEND und cerebEND Zellen wurden durch Immunfärbungen der endothelialen a gekennzeichnetnd BBB Markern sowie durch Messungen der transendotheliale elektrischen Widerstand (TEER) und Durchlässigkeit. Die CEND und cerebEND hatte eine ähnliche Morphologie der primären Kulturen des Gehirns ECs, mit Monoschichten aus dicht gepackten länglichen Zellen, die Wachstumshemmung bei Konfluenz ausgestellt. Die Zellen exprimiert gut nachweisbaren Konzentrationen von Claudin-5, Occludin und VE-Cadherin Proteine, die an den Zell-Zell-Verbindungen lokalisiert wurden, wie durch Immunfluoreszenz (Abbildung 3) 4,5 gezeigt. Kultivieren CEND Zellen in Serum-reduziertem Medium zu einer Erhöhung der TEER (ab 150 Qcm 2 in Gegenwart von 10% Serum und 500 Qcm 2 in Gegenwart von 2% Serum), die durch die Zugabe von Hydrocortison potenziert wurde (800 Qcm führten 2) oder Insulin (1.000 Qcm 2) 4. Monoschichten von CEND in Serum-reduziertem Medium für 21 Tage kultiviert hatten TEER von 900 Qcm 2 (Abbildung 4). TEER wurde gemessen unter Verwendung einer Anordnungenthaltenden Strom-und Spannungs-ziehende Meßelektroden (World Precision Instruments). Zum Vergleich wurde der primäre mikrovaskuläre Gehirn ECs wurde berichtet, TEER-Werte von 200-600 haben Qcm 2 und eine handelsübliche Maus-Zelllinie bEnd.3 hatten TEER-Werte von 100-140 Qcm 2 (für Übersichtsartikel siehe Abt 2005 und Toth et al., 2011 17,18). Darüber hinaus wurde der Durchgang von Makromolekülen, wie nicht geladene FITC-Dextrane Molekularmassen 4, 10, 70 und 500 kDa oder Fluorescein (300 Da) durch die Monoschicht von CEND in 2% FCS Differenzierungsmedium über 4 h verringerte verglichen mit Kontrollzellen in Wachstumsmedium mit 10% FCS gehalten: parazellulären Flussmittel wurde zu 30% der Kontrollzellen für Fluorescein verringert, auf 26% für FITC-Dextran 10 und 70 kDa, und Flussmittel wurde zu 4,5% der Kontroll-Zellen für FITC reduziert -dextrtan 500 kDa. TEER-Werte ähnlich war die Durchlässigkeit auf der untersten Ebene in den Zellen in Gegenwart von gluc kultiviertocorticoids (GC) 4. In weiteren Studien identifizierten wir die Glucocorticoid Zielgene, Occludin, Claudin-5 und VE-Cadherin in Gehirn Gefäßendothel 4,7,9. GC Behandlung führte zu einer Erhöhung der Expression dieser Proteine und auf die Umlagerung von VE-Cadherin mit dem Zytoskelett. Die direkte GC-vermittelten Regulation von Tight junction-Proteine und Claudin Occludin-5 erscheint durch GC Response-Elemente in ihren Promotorregionen 4,7,19. Zusätzlich Claudin-5 wurde als neuartiges Östrogen Ziel im Gefäßendothel 10 identifiziert.
Endotheliale Dysfunktion liegt vielen verschiedenen Krankheiten. Wir kultiviert Die CEND unter Sauerstoff / Glukose Deprivation (OGD) Bedingungen. OGD führte zur Unterbrechung der BBB-Funktion, die nach der kombinierten Behandlung mit GC und Proteasom-Inhibitor Bortezomib 12 rekonstituiert werden konnte. OGD Bedingungen führten zu einem starken Anstieg der Glucose-Aufnahme und in der Expression von Glucose transporsitz in cerebEND, denen durch die Zugabe von MK801, ein nicht-kompetitiver Inhibitor der NMDA-Rezeptor-13 könnte.
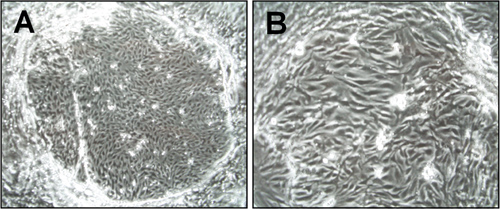
Abbildung 1. Morphologie Gehirn mikrovaskuläre Endothelzellen (CEND) eine Woche nach der Isolierung. Lichtmikroskopie Bilder wurden unter dem 6x (A) und 15x (B) Vergrößerung. Die inselartigen gebildeten Kolonien von Endothelzellen sind sichtbar.
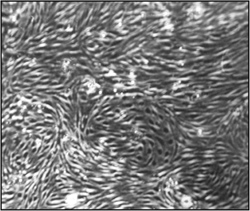
Abbildung 2. Morphologie des Gehirns mikrovaskulären Endothelzellen (CEND) 1 Monat nach der Isolierung und Immortalisierung. Lichtmikroskopie Bilder wurden unter 15x Vergrößerung. Ein konfluenten, homogene Endothelzelle Monoschicht beobachtet werden kann.
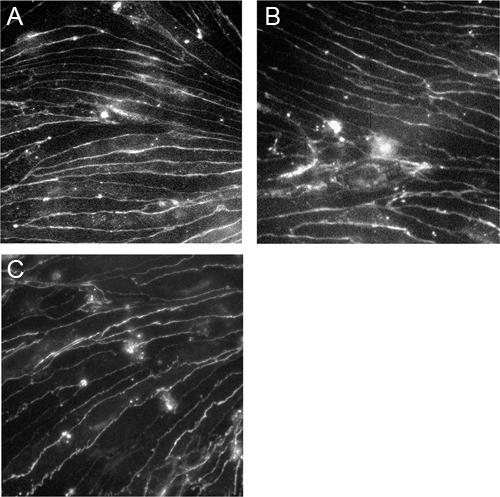
Abbildung 3. Verewigt Gehirn microvascular endothelialen Zellen exprimieren Claudin-5, Occludin und VE-Cadherin. CEND Zellen wurden auf Kollagen IV-beschichteten Deckgläsern gezüchtet und angefärbt mit Antikörpern gegen Claudin-5 (A), Occludin (B) und VE-Cadherin (C). Die Aufnahmen wurden mit einem Zeiss-Mikroskop Axioscop2 unter 40-facher Vergrößerung.
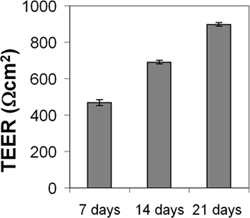
Abbildung 4. Messung transendotheliale elektrischen Widerstand (TEER) von CEND Monoschicht. CEND wurden auf Kollagen IV-beschichteten Transwell-Filter (Porengröße 0,4 um) gezüchtet. Nach Erreichen der Konfluenz wurden die Zellen in Medium mit 2% FCS gehalten. TEER wurde nach 7, 14 und 21 Tagen unter Verwendung einer Anordnung, die Strom-und Spannungs-ziehende Messelektroden gemessen.
Diskussion
Das beschriebene Verfahren kann zur Isolierung von mikrovaskulären ECs verwendet werden aus verschiedenen Mausstämmen sowie aus verschiedenen Knock-out-Maus-Stämme, die spezifischen Änderungen im vaskulären Endothel-Funktion zu studieren. Als ein Verfahren zur Immortalisierung verwendeten wir die Transformation mit Onkoproteins von murinem Polyomavirus, Polyoma mittleren T-Antigen. Es wandelt sich rasch unreifen Endothelzellen in vivo und in vitro 20,21,22. Andere Verfahren zur Immortalisierung von ECs in der Literatur beschrieben sind beispielsweise die Immortalisierung mit SV40 large T-Antigens von Simian Virus 40 vakuolisierenden 23, Adenovirus E1A Genprodukt 24 oder Überexpression der katalytischen Untereinheit der humanen Telomerase 3. Die Immortalisierung mit PYMT ist spezifisch für den murinen unreifen ECs, die Gewinnung eines homogenen EG Kultur aus neugeborenen Mäusen in einer kurzen Zeit ermöglicht. Immortalisierung verändert die Eigenschaften der Zellen und the Ergebnisse mit immortalisierten Zelllinien erhalten sollten entweder mit primären Zellen oder mit Experimenten in vivo an Mäusen verglichen werden. PYMT immortalisierten EG beschrieben worden, um eine hohe fibrinolytische Aktivität, die aus einer erhöhten Produktion von Urokinase-Plasminogen-Aktivator exprimieren und eine verminderte Produktion von Plasminogenaktivator-Inhibitoren 25. Direkter Vergleich von PYMT verewigt bEND5 Zelllinie mit primären ECs ergab, dass sowohl in vitro als BBB Modelle sind bekannt für T-Zell-Adhäsion Studien 26 geeignet.
Die Zelllinien etabliert nach dem beschriebenen Verfahren kann bei niedrigen Passage-Nummer verwendet werden, um Barriereeigenschaften durch hohe Expression von BBB und EC junctional Proteine zu erhalten, da die Zellen diese Eigenschaften verlieren, während des Alterns. Somit nach Verlust der Barriereeigenschaften, sollte die Herstellung einer neuen Zellinie betrachtet werden. Zelle Plattierungsdichte sollte für ECs hoch, da diese entscheidend für die Zellproliferation. Dies muss bei der Isolierung als auch Wartung des verewigt ECs werden. Jede neue Zelllinie sollte ihre Sperreigenschaften und für eventuelle Verunreinigungen mit anderen Zelltypen getestet werden. EC Monoschichten kann mit anti-Galactocerebrosid, Anti-glial fibrillary acidic protein-und anti-glatte Muskulatur-Antigen als primäre Antikörper angefärbt werden, um die Kontamination mit Oligodendrozyten, Astrozyten und Perizyten 4,27 auszuschließen. Um eine Kontamination durch meningal Gefäßsystem kann die Expression von Thrombomodulin getestet werden, was sich in allen Gefäßbetten mit Ausnahme des Gehirns 28 exprimiert.
Interessanterweise unterscheiden sich die immortalisierten mikrovaskulären Endothelzellen Zelllinien aus verschiedenen Hirnregionen isoliert in ihrer Barriere-Eigenschaften und die Anfälligkeit für proinflammatorische Stimuli. Als ein Beispiel können die zerebrale CEND und zerebelläre cerebEND Zelllinien genannten 4,5 sein. CerebEND zeigten im Vergleichum CEND, geringere Expression von großen tight junction Komponenten Claudin-1 und Occludin. Jedoch waren die Ebenen der Claudin-3 und -12 höher cerebEND. Die Barrierefunktion cerebEND Zellen erlitten wesentlich unter einer Behandlung mit dem Entzündungsmediator, TNFa als die Barriereeigenschaften CEND Zellen tat 5. Höhere Kleinhirn Anfälligkeit für entzündliche Stimuli können in vivo in Patienten mit Multipler Sklerose und in seiner Tiermodell der experimentellen autoimmunen Enzephalomyelitis 29 beobachtet werden. Diese interessanten Ergebnisse zeigen die Notwendigkeit der Erzeugung und Charakterisierung von einzelnen in vitro Modelle für unterschiedliche Hirnregionen, um die Zukunft Drug Targeting in das Gehirn zu verbessern.
Offenlegungen
Keine Interessenskonflikte erklärt.
Danksagungen
Diese Arbeit wurde von der Deutschen Forschungsgemeinschaft DFG unter Grantnummer FO 315/4-1 und DFG SFB 688 unterstützt.
Materialien
| Name | Company | Catalog Number | Comments |
| Name des Reagenzes | Firma | Katalog-Nummer | Kommentare |
| Rinderserumalbumin (BSA) | Sigma-Aldrich | A7906 | Reinheit> 98% |
| Kollagen IV | Sigma-Aldrich | C5533 | 50 ug / ml in 50 mM Essigsäure |
| Collagenase / Dispase | Roche | 10269638001 | |
| Dulbecco modifiziertem Eagle-Medium (DMEM) | Sigma-Aldrich | D5796 | |
| Dimethylsulfoxid (DMSO) | Sigma-Aldrich | D2650 | |
| Fötalem Kälberserum (FCS) | PAA Laboratories | A15110-1333 | Endkonzentration 10%, hitzeinaktiviertes (30 min bei 56 ° C) |
| L-Glutamin | Biochrom AG | K0282 | Lagerung: ≤ -15 ° C |
| MEM Vitamine | Biochrom AG | K0373 | Lagerung: ≤ -15 ° C |
| Na-Pyruvat | Biochrom AG | L0473 | |
| Neomycin (G418) | PAA Laboratories | P11-012 | |
| Nicht essentielle Aminosäuren (NEA) | Biochrom AG | K0293 | Lagerung bei 4 ° C |
| Penicilin / Streptomycin | Biochrom AG | A2212 | Lagerung: ≤ -15 ° C |
| Phosphatgepufferte Kochsalzlösung (PBS) | Biochrom AG | L1825 | |
| Polybrene (Hexadimethrinbromid) | Sigma-Aldrich | 107689 | 0,8 mg / ml in PBS, Lagerung bei -20 ° C |
| Puromycin | Sigma-Aldrich | P8833 | |
| Trypsin / EDTA | Biochrom AG | L1825 | 0,05%, 0,02% EDTA in PBS |
Referenzen
- Wilhelm, I., Fazakas, C., Krizbai, I. A. In vitro models of the blood-brain barrier. Acta Neurobiol. Exp (Wars). 71, 113 (2011).
- Forster, C. Differential effects of hydrocortisone and TNFalpha on tight junction proteins in an in vitro model of the human blood-brain barrier. J. Physiol. 586, 1937 (2008).
- Weksler, B. B. Blood-brain barrier-specific properties of a human adult brain endothelial cell line. FASEB. J. 19, 1872 (2005).
- Forster, C. Occludin as direct target for glucocorticoid-induced improvement of blood-brain barrier properties in a murine in vitro system. J. Physiol. 565 (Pt 2), 475 (2005).
- Silwedel, C., Forster, C. Differential susceptibility of cerebral and cerebellar murine brain microvascular endothelial cells to loss of barrier properties in response to inflammatory stimuli. J. Neuroimmunol. 179, 37 (2006).
- Forster, C. Glucocorticoid effects on mouse microvascular endothelial barrier permeability are brain specific. J. Physiol. 573 (Pt 2), 413 (2006).
- Burek, M., Forster, C. Y. Cloning and characterization of the murine claudin-5 promoter. Mol. Cell Endocrinol. 298, 19 (2009).
- Forster, C., Kahles, T., Kietz, S., Drenckhahn, D. Dexamethasone induces the expression of metalloproteinase inhibitor TIMP-1 in the murine cerebral vascular endothelial cell line cEND. J. Physiol. 580 (Pt.3), 937 (2007).
- Blecharz, K. G., Drenckhahn, D., Forster, C. Y. Glucocorticoids increase VE-cadherin expression and cause cytoskeletal rearrangements in murine brain endothelial cEND cells. J. Cereb. Blood Flow Metab. 28, 1139 (2008).
- Burek, M., Arias-Loza, P. A., Roewer, N., Forster, C. Y. Claudin-5 as a novel estrogen target in vascular endothelium. Arterioscler. Thromb Vasc. Biol. 30, 298 (2010).
- Blecharz, K. G. Glucocorticoid effects on endothelial barrier function in the murine brain endothelial cell line cEND incubated with sera from patients with multiple sclerosis. Mult. Scler. 16, 293 (2010).
- Kleinschnitz, C. Glucocorticoid insensitivity at the hypoxic blood-brain barrier can be reversed by inhibition of the proteasome. Stroke. 42, 1081 (2011).
- Neuhaus, W. Addition of NMDA-receptor antagonist MK801 during oxygen/glucose deprivation moderately attenuates the upregulation of glucose uptake after subsequent reoxygenation in brain endothelial cells. Neurosci. Lett. 506, 44 (2012).
- Perriere, N. Puromycin-based purification of rat brain capillary endothelial cell cultures. Effect on the expression of blood-brain barrier-specific properties. J. Neurochem. 93, 279 (2005).
- Golenhofen, N., Ness, W., Wawrousek, E. F., Drenckhahn, D. Expression and induction of the stress protein alpha-B-crystallin in vascular endothelial cells. Histochem Cell Biol. 117, 203 (2002).
- Risau, W., Engelhardt, B., Wekerle, H. Immune function of the blood-brain barrier: incomplete presentation of protein (auto-)antigens by rat brain microvascular endothelium in vitro. J. Cell Biol. 110, 1757 (1990).
- Abbott, N. J. Dynamics of CNS barriers: evolution, differentiation, and modulation. Cell Mol. Neurobiol. 25, 5 (2005).
- Toth, A. Patented in vitro blood-brain barrier models in CNS drug discovery. Recent Pat. CNS Drug Discov. 6, 107 (2011).
- Harke, N. Glucocorticoids regulate the human occludin gene through a single imperfect palindromic glucocorticoid response element. Mol. Cell Endocrinol. 295, 39 (2008).
- Kiefer, F., Courtneidge, S. A., Wagner, E. F. Oncogenic properties of the middle T antigens of polyomaviruses. Adv. Cancer Res. 64, 125 (1994).
- Kiefer, F. Endothelial cell transformation by polyomavirus middle T antigen in mice lacking Src-related kinases. Curr. Biol. 4, 100 (1994).
- Ong, S. H. ShcA and Grb2 mediate polyoma middle T antigen-induced endothelial transformation and Gab1 tyrosine phosphorylation. EMBO J. 20, 6327 (2001).
- O'Connell, K. A., Edidin, M. A mouse lymphoid endothelial cell line immortalized by simian virus 40 binds lymphocytes and retains functional characteristics of normal endothelial cells. J. Immunol. 144, 521 (1990).
- Roux, F. Regulation of gamma-glutamyl transpeptidase and alkaline phosphatase activities in immortalized rat brain microvessel endothelial cells. J. Cell Physiol. 159, 101 (1994).
- Montesano, R. Increased proteolytic activity is responsible for the aberrant morphogenetic behavior of endothelial cells expressing the middle T oncogene. Cell. 62, 435 (1990).
- Steiner, O., Coisne, C., Engelhardt, B., Lyck, R. Comparison of immortalized bEnd5 and primary mouse brain microvascular endothelial cells as in vitro blood-brain barrier models for the study of T cell extravasation. J. Cereb. Blood Flow Metab. 31, 315 (2010).
- Skaper, S. D., Conn, M. . Methods in Neurosciences. 2, 1303 (1990).
- Ishii, H. Thrombomodulin, an endothelial anticoagulant protein, is absent from the human brain. Blood. 67, 362 (1986).
- Minagar, A., Alexander, J. S. Blood-brain barrier disruption in multiple sclerosis. Mult. Scler. 9, 540 (2003).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten