Method Article
Massenspektrometrische Analyse Glycosphingolipid Antigene
In diesem Artikel
Zusammenfassung
Eine spezifische und sensitive Methode, um Einblick in die Expression von Glykosphingolipid Antigene Immunsystem Organe und Zellen zu gewinnen beschrieben. Das Verfahren nutzt die Ionenfallenmassenspektrometer ermöglicht stufenweise Fragmentierung Glycosphingolipid Moleküle zur Strukturanalyse gegenüber chemisch synthetisierten Standard.
Zusammenfassung
Glykosphingolipide (GSL die) gehören zur Klasse der Biomakromoleküle Glycokonjugat, das strukturelle Informationen für signifikante biologische Prozesse wie bei der Embryonalentwicklung, Signaltransduktion, und Immun Rezeptorerkennung 1-2 ertragen. Sie enthalten komplexe Zuckerreste in Form von Isomeren, und Lipidgruppierungen mit Variationen einschließlich Fettacyl Kettenlänge, Ungesättigtheit und Hydroxylierung. Beide Kohlenhydrat-und Ceramid Abschnitte können aufgrund der biologischen Bedeutung sein. Zum Beispiel schließen Tri-hexosylceramides Globotriaosylceramid (Galα4Galβ4Glcβ1Cer) und isoglobotriaosylceramide (Galα3Galβ4Glcβ1Cer), die gleich, aber unterschiedliche Molmassen Zucker-Verknüpfungen der Kohlenhydratanteil, verantwortlich für völlig unterschiedliche biologische Funktionen haben 3-4. In einem anderen Beispiel wurde gezeigt, dass eine Modifikation des Ceramid Teil alpha-Galactosylceramid, ein potenter Ligand-Agonist für Invariantenant NKT-Zellen, Änderungen ihrer Zytokinsekretion Profilen und Funktion in Tiermodellen von Krebs und Autoimmunerkrankungen 5. Die Schwierigkeit bei der Durchführung einer Strukturanalyse von Isomeren in Immun Organen und Zellen dienen als Barriere zur Bestimmung viele biologische Funktionen 6.
Hier präsentieren wir eine visualisierte Version einer Methode für relativ einfache, schnelle und sensitive Analyse von Glykosphingolipid Profile in Immunzellen 7-9. Dieses Verfahren basiert auf Extraktion und chemischen Modifikation (Permethylierung, siehe unten 5A, alle OH-Gruppen der Hexose wurden durch MeO nach Permethylierung Reaktion ersetzt) von Glycosphingolipiden 10-15, durch anschließende Analyse mittels Matrix-Assisted Laser Desorption / Ionisation Time-Basis verfolgt of-Flight Massenspektrometrie (MALDI-TOF/MS) und Ionenfallenmassenspektrometer. Diese Methode erfordert 50 Millionen Immunzellen für eine vollständige Analyse. Die Experimente können innerhalb einer Woche abgeschlossen sein. Die relative Häufigkeit der verschiedenen Glycosphingolipiden kann durch Vergleich mit synthetischen Standards abgegrenzt werden. Diese Methode hat eine Empfindlichkeit der Messung 1% iGb3 unter Gb3 Isomere, wenn 2 fmol des gesamten iGb3/Gb3 Gemisch vorhanden ist 9.
Ionenfallenmassenspektrometer Isomeren kann verwendet werden, um zu analysieren. Zum Beispiel, um das Vorhandensein von Globotriaosylceramid und isoglobtriaosylceramide in der gleichen Probe zu analysieren, kann man die Fragmentierung der Glykosphingolipid Moleküle strukturell zwischen den beiden (siehe unten Abbildung 5) zu unterscheiden. Weiterhin verbessert die chemische Modifikation der Zuckergruppierungen (durch eine Permethylierung Reaktion) die Ionisierung und Fragmentierung Wirkungsgrade für höhere Empfindlichkeit und Spezifität, und erhöht die Stabilität der Sialinsäurereste. Die Extraktion und chemische Modifikation von Glykosphingolipiden kann in einem klassischen chemischen zertifizierten Abzug durchgeführt werden, und das kann durch Massenspektrometrie Kern durchgeführt werdenEinrichtungen mit Ionenfalle MS Instrumente.
Protokoll
Ein. Lab Sicherheitsbedenken
- Alle organischen Lösungsmittel müssen in bestimmten Bereichen durch klare Kennzeichnung gespeichert werden. Siehe Etiketten fertigt für Arten von Feuerlöschern erforderlich.
- Mehrere verwendeten Reagenzien sind potentiell krebserregend und kann Depressionen verursachen. Diese Reagenzien müssen in einer chemischen Kapuze mit Belüftung (siehe Tabelle der spezifischen Reagenzien und Geräte für Einzelheiten) behandelt werden.
- Es wird empfohlen, dass beim Arbeiten mit organischen Lösungsmitteln und Zellen, persönliche Schutzausrüstung wie Handschuhe, Kittel und Schutzbrille zu allen Zeiten genutzt werden.
2. Extraktion von Glycosphingolipide vom Rat Leukemia Cells
- Shop RBL rat Leukämiezellen 8 (10.000.000 bis 100.000.000) in 16x100 mm Glasröhrchen unter -80 ° C Bedingungen. Zellen sind von einer Zählkammer nach Trypanblaufärbung gezählt. Lebensfähigkeit von Zellen sollte höher als 95%.
- Entpacken Sie die Lipide mit umfangreichen sonicatIonen viermal für 1-2 Stunden mit jeweils gemischten polaren Lösungsmitteln. Verwenden 6 ml Chloroform-Methanol 1:1 (v / v) als das erste und das letzte Lösungsmittel. Sechs Milliliter Isopropanol: Hexan: H 2 O 55:25:20 (v / v / v, zu entfernen Oberphase durch Absaugen vor Gebrauch) kann dann als zweite und dritte Lösungsmittel verwendet werden. Das Lösungsmittel wird durch Mischen von Isopropanol: Hexan: H 2 O in einem 55:25:20-Verhältnis, schüttelte sie heftig, und ermöglicht eine obere Phase zu erscheinen, welche entfernt werden. Halten Sie die untere Phase zum Einsatz.
- Folgen Beschallung mit Zentrifugieren zu Pellets das unlösliche Material. Bündeln die Überstände. Trocknen Sie sie in einem Speedvac für 4 Stunden. Stickstoffstrom Rotationsverdampfer oder kann verwendet werden, wenn Speedvac nicht verfügbar ist. Verwenden Sie eine gute Kühlfalle zu verdampfenden organischen Lösungsmitteln zu halten. Verunreinigung von organischen Lösungsmittels in Vakuumpumpenöl verschlechtern die Effizienz der Vakuumpumpe.
- Führen Sie eine vorläufige Analyse unter Verwendung von Hochleistungs-Dünnschichtchromatographie (HPTLC). Um Glykolipide quantifizieren, Bereiten eine 0,2% Orcinol in 50% iger Schwefelsäure-Lösung (100 mg in 50 ml) und einem Galactose-Standard (40 mg in 100 ml Stammlösung). Bereiten Sie in 30 ul Reaktionsvolumen eine Reihe von Verdünnungen als Standardkurve (von 0 g / L bis 20 g / L) zu verwenden. Fügen Sie 20 ul Methanol jeder Verdünnungsreihe Probe. Lösen Sie jedes Glykolipid Probe in 200 ul Methanol, beschallen, und verwenden Sie 20 ul für Glykolipid Mengenmessung. In 1,5 ml Eppendorf-Röhrchen mit verschraubten Kappen (Sarstedt, 72.692.005), 0,4 ml von 0,2% Orcinol in 50% iger Schwefelsäure-Lösung zu jeder Probe, mit einer Reihe von Galactose-H 2 O-Methanol-Lösungen, die für die Standardkurve dienen . Kochen für 5 min in Heizblock bei 100 ° C. Lesen optische Dichte der Farbreaktion bei 440 nm mit Sonnenaufgang Tecan Mikroplatten-Reader. Zur Durchführung HPTLC, verwenden Chloroform: Methanol: H 2 O 60:35:8 (v / v / v) als Lösungsmittel für die neutralen Lipide mit Chloroform-Methanol 1:1 (v / v) behandelt. Verwendung von Isopropanol: Hexan: H 2 O 55:25:20 (v / v / v) alsdas Lösungsmittel für die Säure Lipide (Ganglioside). Die isolierten neutralen GSL wurde in 200 ul Lösungsmittel Chloroform: Methanol 1:1 (v / v) geladen und auf Merck Silicagel Dünnschichtchromatographieplatte von Drummond Microcaps. Die Platten wurden im Lösungsmittel Chloroform ausgeführt: Methanol: H 2 O 60:35:8 (v / v / v) gewaschen und getrocknet. Die Glykosphingolipide wurden durch Orcinol-Schwefelsäure bei 300 ° C.
- Um die Abscheidung von neutralen Lipiden aus den sauren Lipiden, Fraktion aus den neutralen und sauren Lipiden durch Anionenaustauschchromatographie auf einer kleinen Säule aus DEAE-Sephadex A-25 [der DEAE Sephadex A25 Harz kann durch Einweichen Sephadex A-25-Harz hergestellt werden Pulver in Chloroform: Methanol: H 2 O 30:60:8 (v / v / v) über Nacht. Überstand bis die Sephadex A25 Harz wird alles, was übrig ist. Add frischen Chloroform: Methanol: H 2 O 30:60:8 (v / v / v), um das Harz zu waschen. Wiederholen Sie dreimal, um die negativ geladenen Reste aus Sephadex A25 Harz] entfernen.
- Auflösen, Beschallen (nicht länger als 10 min) und resuspendiert die Lipide aus Schritt 2.1 in Chloroform: Methanol: H 2 O 30:60:8 (v / v / v), wenn nötig.
- Bereiten Sie eine kleine DEAE Sephadex A25 (Cl Form) Spalte mit Glaswolle und einen 9 "Pasteurpipette. Packen Sie die Glaswolle sorgfältig, so dass Harzpulver nicht durch die Säule nicht passieren. Hinzufügen DEAE Sephadex A25 (Cl Form) Harz auf die" Hals "des 9" Pasteurpipette, ohne dass die Spalte trocken. Stellen Sie sicher, dass Sie sehen keinen Harz in Eluent. Die Proben in Chloroform: Methanol: H 2 O 30:60:8 (v / v / v) gelöst. Die neutrale Lipidfraktion ist die Strömung durch Bruch.
- Eluieren der sauren Lipidfraktion (gebunden an den Harzen) mit 8 ml Natriumacetat in Methanol. Trocknen Sie sowohl die neutrale und saure Fraktionen, entsalzen sie durch Dialyse, trocknen sie durch Speedvac und analysieren sie durch HPTLC.
Die saure Fraktion enthält Ganglioside, die für den Schritt 3 Reaktion direkt dialysiert werden können.Die neutrale Fraktion enthält neben neutralen Glycosphingolipiden, sondern auch Phospholipide (Phosphatidylcholin und Sphingomyelin), die durch eine Acetylierungsreaktion entfernt werden müssen.
Nach unserer Erfahrung, wobei das Verfahren eines Dialyse-Kassette, ist effizienter und bequemer als ein Dialyserohr oder Umkehrphasen-C18-Säule gereinigt.
- Der nächste Schritt ist das Entfernen von Phospholipiden aus neutralen Glycosphingolipiden durch eine Acetylierung und Peracetylierung Reaktion. Trocknen des DEAE Sephadex A-25-Pass-Through-Fraktion in der Speedvac (mit Kühlung) für 4 Stunden. Nachdem die Proben trocken sind, setzen Sie sie zurück in die Speedvac und trocken für weitere 4 Stunden. Stellen Sie sicher, dass diese Proben vollständig trocken sind, wie der restliche Wasser wird die Peracetylierung Reaktion zu verhindern.
- Peracetylate die Proben mit 1 ml Pyridin und 0,5 ml Essigsäureanhydrid in der Dunkelheit bei Raumtemperatur oder 37 ° C über Nacht. Diese Menge an Pyridin und Essigsäureanhydrid für bis ordnungsgemäßebis 200 ug von Glykosphingolipiden. Diese Reaktion kann bei 37 ° C durchgeführt werden, da die GSLs bessere Löslichkeit haben.
- Trocknen des Materials durch peracetylierten Speedvac für 3 Stunden, unter Zusatz von 1 ml Toluol 3x (Koevaporation) nach vollständiger Verdampfung gewährleisten. Wenn die Proben sind noch nicht ganz trocken, Speedvac bis trocken.
- Bereiten Sie eine Florisil (Sigma-Aldrich) Spalte (30-60 mesh, 10 × 80 mm) in einer Pasteurpipette mit Glaswolle, mit Florisil Perlen. Florisil Kügelchen sollten vor Gebrauch vollständig getrocknet werden, durch Inkubation in einem 110 ° C Ofen. Füllen der Kügelchen in die Pasteurpipette bis zum Hals, und äquilibrieren in 1,2-Dichlorethan-Hexan 4:1 (v / v).
Elution aus der Florisil Säule ist sehr schnell. Schnelle Volatilität der Lösungsmittel können die Spalte Trocknung führen. Damit sind alle Lösungsmittelgemische sollte vor dem Ausführen der Säule, da es nicht möglich ist, um die Säule während der Elution stoppen hergestellt werden.
- Übernehmen Sie die Peracetylated Probe in 1 ml 1,2-Dichlorethan-Hexan 4:1 (V / V), und die Säule mit 6 ml des gleichen Lösungsmittels, gefolgt von 10 ml 1,2-Dichlorethan, gefolgt. Eluieren neutralen peracetylierten GSLs mit 6 ml 1,2-Dichlorethan-Aceton 1:1 (v / v). Dieser Schritt entfernt die peracetylierten Phospholipide aus Glykosphingolipide, weil die peracetylierten Glykosphingolipide der Florisil Säule binden, während peracetylierten Phospholipide nicht tun.
- Trocknen der Fraktionen durch Speedvac für 2 Stunden und desacetylieren mit 2 ml 0,5 M Natriummethylat [Sigma-Aldrich, 403.067] in 2 ml Methanol für 3 Stunden bei Raumtemperatur.
- Neutralisieren die Mischung mit 3 ml methanolischer Essigsäure [Essigsäure / Methanol 15/85 v / v], trocken Speedvac, desalt durch Dialyse [Lösen Sie die getrockneten Produkte in 3 ml Wasser und spritzen in die Slide-A-Lyzer Dialyse Cassette, gegen Wasser dialysiert für 24 Std. Wechseln Sie das Wasser mindestens zweimal]. Trocknen Sie die dialysierten GSLs (in wässriger Lösung) durch Speedvac, bis die Proben vollständig trocken sind.
3. Chemische Modifizierung (Permethylierung) von Glykosphingolipiden 13
- Einführen GSLs (1-20 ug) in ein Glasröhrchen mit einem Schraubdeckel und Teflonseele und fügen Dimethylsulfoxid (150 ul) ohne Verwendung von speziellen Trocknungsbedingungen oder Inertgasatmosphäre.
- Planen pulverförmiges Natriumhydroxid (40-60 mg) aus Natriumhydroxid Teilchen durch Mahlen in einer chemischen Mörser mit einem Pistill. Achten Sie darauf, die Pulver in einer sehr trockenen Umgebung lagern und darauf achten, dass die Schleifen in der chemischen Haube tun, um das Einatmen der Pulver.
- Weiter fügen Natriumhydroxidpulver zu der Probenlösung mit einem Spatel. Hinzufügen Iodmethan (80 ul) mit 100 Mikroliter Halmilton Spritze, [oder einer 100-Mikroliter-Pipette VWR kalibrierten Verbindung mit einer Spritze durch Gummischlauch verwendet werden kann], und schüttelt das Gemisch bei Raumtemperatur für 1 Stunde.
- Quench die Methylierungsreaktion mit Wasser (2 ml). Entpacken Sie die permethylierte Produkte 3 mal durchdie Zugabe von Dichlormethan (2 ml) [Glykolipide sind in der Dichlormethan-Phase, die die untere Phase, so dass die obere Phase kann auf eine neue Glasröhrchen transferiert werden, und extrahiert nochmals mit Dichlormethan ist].
- Die vereinigten Dichlormethan extrahiert 3 mal mit 2 ml Wasser [die obere Phase, die das Wasser ist, kann anschließend entsorgt werden]. Nach dem letzten Waschen übertragen die Proben in ein neues Röhrchen, und unter Verwendung der Speedvac trocknen.
- Proben können dann in 100 bis 200 ul Methanol ESI-MS-Analyse gelöst werden.
4. MALDI-TOF-Analyse der permethylierten Gycosphingolipids
- Führen MALDI-TOF-MS und MALDI-TOF/TOF-MS/MS Experimente auf einem MALDI-TOF-TOF-Massenspektrometer (Applied Biosystems 4700, Foster City, CA). Bereiten Sie die Matrix durch Mischen von 50% Volumen von 10 mg / ml Dihydroxybenzoesäure (DHB) in Acetonitril und 50% Volumen von 0,1% Trifluoressigsäure (TFA) in Wasser.
- Der DHB-Matrix kann auf der MALDI targe entdeckt werdent (1 ul), durch eine 1 ul (enthaltend 100 ng GSL) Spot der Probe in Methanol gelöst gefolgt. Übernehmen langsam und lassen Sie es vor der Analyse zu trocknen.
5. Ion Trap MS-Analyse von permethylierten Glycosphingolipide
- Führen Sie Massenspektrometrie auf einem linearen Ionenfallen-Massenspektrometer (LTQ, ThermoScientific, San Jose, CA) mit einem Nanoelektrospray Quelle, 0,30 ul / min bei 230 ° C Kapillartemperatur in positive Ionen-Modus mit 30-50% Kollisionsenergie. Set Kollisionsenergien eine minimal residual Fülle von Vorläufer-Ion verlassen. Erkennen alle Ionen wie Natrium-Addukte.
- Identifizieren Sie die iGb3 (Galα3Galβ4Glcβ1Cer) in einer isobaren Mischung aus Gb3 (Galα4Galβ4Glcβ1Cer) und iGb3 (Galα3Galβ4Glcβ1Cer) Standards durch den Vergleich der unterschiedlichen Muster der MS 4 Produkt-Ionen aus dem sodiated Molekülion über die Glykan-Fragment m / z 667 und dem Terminal Disaccharid 1 - ene Ionen m / z 445 (dhX → 667 → 445 →, X bedeutet die Molekülion bei MS 1) aus reinem permethylierten iGb3 (Galα3Galβ4Glcβ1Cer) Standards über ESI-LIT-MS nachgewiesen mit denen der permethylierten Gb3 (Galα3Galβ4Glcβ1Cer).
Ergebnisse
Ein Beispiel für eine MALDI-MS-Analyse der Glycosphingolipide aus Ratten-Leukämie-Zelllinie RBL (ein Antigen präsentierenden Zelle Typ, Glycosphingolipid Antigene präsentiert NKT-Zellen), ist in 3 gezeigt. Die Ionen können bestimmten Glycosphingolipid Strukturen (3A) zugeordnet werden. In RBL-Zellen durch NB-DGJ 16, ein Medikament, das Glycosphingolipid Synthese signifikante Reduktion aller Glycosphingolipiden wurde beobachtet (Abbildung 3B) hemmt behandelt. Strukturisomeren kann nicht unterschieden werden. Die MS / MS-Kapazität des Applied Biosystems 4700 ermöglicht Fragmentierung von Ionen MS1, MS 2-Fragmente, die eine begrenzte strukturelle Information generiert. Jedoch ist MS2 Analyse oft nicht ausreicht, um Oligosaccharid Isomeren diskriminieren.
Das Ionenfallen-MS-Analyse Glycosphingolipide ermöglicht die Untersuchung Isomere, wie iGb3 (Galα3Galβ4Glcβ1Cer) und Gb3 (Galα4Galβ4Glcβ1Cer), die als die trihexosylceramide Ionen in 3A detektiert existieren können. Um solche Isomere nachzuweisen, wurden Standard iGb3 und Gb3 durch mehrere Runden von Fragmentierung analysiert, bis Unterschiede gefunden wurden (4A und 4B). In dem hier vorgestellten Beispiel (Abbildung 5C) iGb3 und Gb3 konnte durch Vergleich mit Standard-iGb3 und Gb3 diskriminiert werden.
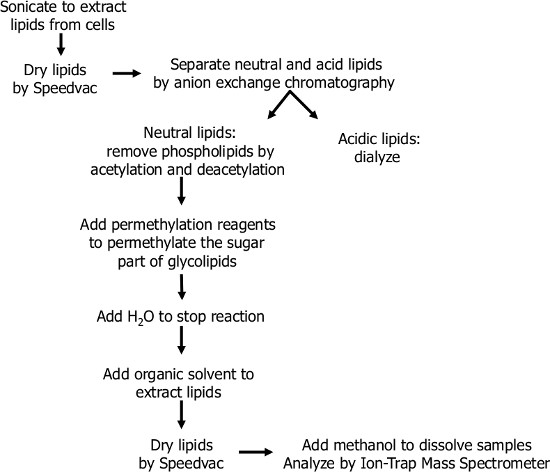
Abbildung 1. Flußdiagramm des Glycosphingolipid Extraktionsverfahren und chemische Modifikation von Glykosphingolipiden (Permethylierung). Glycosphingolipide wurden aus Zellen, die durch organische Lösungsmittel extrahiert. Um nicht Glykosphingolipide entfernen, können Lipide peracetylierten und deacetyliert. Zweitens Glycosphingolipiden chemisch wurden durch eine Permethylierung Reaktion modifiziert, verbessert die Empfindlichkeit und Spezifität der MS detection. Schließlich wurden die Glykosphingolipid Profile ermittelt mittels MALDI-TOF-Massenspektrometrie und Ionenfallenmassenspektrometer.
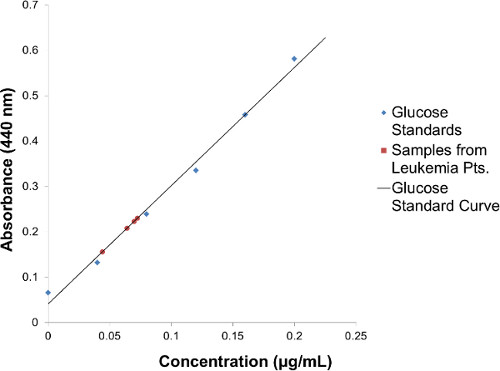
Abbildung 2. Glycosphingolipid Quantifizierung durch Orcinol Schwefelsäure-Verfahren: Quantifizierung von Glykosphingolipiden mittels eines 0,2% Orcinol in 50% igen Schwefelsäure und einem Glukose-Eichkurve.

Abbildung 3. Glycosphingolipidomics von Ratten-Leukämiezellen A. Repräsentative MALDI Massenspektrum;. Jedes Ion repräsentiert eine bestimmte Glycosphingolipid Struktur kann Strukturisomeren nicht unterschieden werden B. NB-DGJ, ein Medikament, das Glycosphingolipid Synthese, s hemmt.ignificantly reduziert alle Glykosphingolipide in RBL-Zellen produziert.

Abbildung 4. Tandem-Massenspektrometrie von Isomeren Glycosphingolipide. A. Charakteristische Abbauwege für positive mode Ionenfallenmassenspektrometer der permethylierte GSLs Gb 3 Cer und IGB 3 Cer. Gb 3 und IGB 3 sind eindeutig durch ihre Fragmentierungsmuster getrennt. Die Unterschiede in der Verknüpfung in den MS 4 Produkt-Ionen, die mit den isobaren m / z 445 Vorläufern wider. B. Repräsentative Ergebnisse zeigt iGb3 kann in einer Mischung aus Isomeren iGb3/Gb3 gemessen werden. Sterne bedeuten diagnostischen Ionen für iGb3 nur. Klicken Sie hier, umeine größere Abbildung.
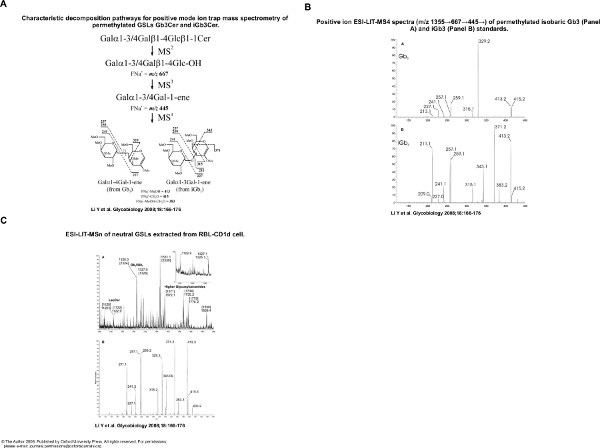
Abbildung 5. Ion Trap MS ermöglicht die Analyse von Isomeren Glykosphingolipide. A. Standard iGb3 und Gb3 Show Differenz von Fragmentierung Profil nach 4 Runden Fragmentierung in einer Ionenfalle LTQ Massenspektrometer. B. Charakteristisch MS 4 Profil von Ionen aus iGb3 oder Gb3. C. abgeleitet Trihexosyleramides sind Mischungen aus iGb3 und Gb3 Isomere, die durch die Ionenfalle MS-Methode (Abbildung von Dapeng Zhou) identifiziert werden können. Klicken Sie hier für eine größere Abbildung zu sehen .
Diskussion
Die Glykoms, ein Begriff in Analogie zu dem Genom und Proteom geprägt, bezieht sich auf alle Saccharid-Strukturen eines Organismus. Um vollständig zu verstehen, die vielfältigen Funktionen der Glykosylierung ist ein integrierter Ansatz, der sowohl funktionelle und strukturelle Glykomik Studien. Beide werden von der nicht-angetriebenen Schablone Art Glycan-Biosynthese, die resultierende Komplexität und Vielfalt der Glycanstrukturen, die häufige Beteiligung Aglykon Struktur in Modulieren Glycan Ligand-Rezeptor-Wechselwirkungen auf molekularer Ebene, und die funktionelle Bedeutung von geringer Häufigkeit Liganden kompliziert.
Es ist allgemein anerkannt, dass Massenspektrometrie (MS) ein unverzichtbares Verfahren zur strukturellen Glykomik Studien, insbesondere zur Identifizierung und Charakterisierung niedriger Häufigkeit Liganden ist. Um Glycane oder Glycokonjugate als molekulare Spezies beobachten, wir verwenden häufig eine hocheffiziente, niedrige Energie Ionisation Methode, genannt Elektrospray-Ionisation (ESI). Für weitere detfehlte Charakterisierung Glykanstruktur, ist es wichtig, einzelne molekulare Spezies auszuwählen und brechen die Glykane in kleinere Stücke. Dies wird normalerweise durch Kollision-induzierte Dissoziation, die Aktivierung der Glycane durch Kollision mit inerten Gasmolekülen beinhaltet getan. Die erhöhte Energie induziert Bindungsbruch und systematische Analyse der resultierenden Fragmente liefert Informationen über die molekulare Struktur des Glycan. Oft können "Signatur"-Fragmente erzeugt werden, die für bestimmte Glykan strukturelle Merkmale diagnostischen werden. Zusammen mit der Molekularmasse können diese Fragmente manchmal ausreichend zum Identifizieren Glycane, aber in der Vergangenheit viel mehr Informationen verlangt worden, um sie vollständig zu charakterisieren, besonders wenn die Struktur neu ist. Diese Verfahren umfassen Zuckerzusammensetzung Analyse, Gaschromatographie-Massenspektrometrie-Analyse von teilweise methylierten Alditolacetate für Kopplungsanalyse und spezifischen Glykosidase Verdauung 17.
Wie im vergangenen Jahrzehnt 18-19 gezeigt, mehrere Runden von Niedrigenergiehäusern Fragmentierung, die effektiv durchgeführt werden kann in einem Ionenfallen-Massenspektrometer (IT-MS), verbessert die Informationen Ausbeute von Glykan massenspektrometrische Analyse . Mit vier oder fünf Runden der Fragmentierung (das kann nicht mit anderen MS-Geräten durchgeführt werden), ist es möglich, isomeren Glykane, die die gleichen Zucker-Komponenten in verschiedenen Zucker-Verknüpfungen angeordnet enthalten unterscheiden, selbst wenn diese vorhanden sind zusammen in Mischungen von Komponenten mit der gleichen Molmasse (Isobaren). Für diese Analyse wurden die Glykane derivatisiert, ersetzt alle freien Hydroxylgruppen mit Methylgruppen mit Permethylierung. Während strukturelle Zuordnung der Glykane ohne Permethylierung möglich, erhöht sich die Permethylierung Empfindlichkeit 17.
Levery und Zhou, haben alle potenziellen Vorteile von IT-MS Methodik, einschließlich der Ermittlung der isomeren stru kombiniertctures Verwendung Signatur diagnostische Ionen, 4 nur im MS und MS-Spektren 5 beobachtbar ist, zum hochempfindlichen Identifizierung und Quantifizierung von Glycosphingolipiden in Form mehrerer isobaren Mischungen 7-9. In der Theorie können wir in der Lage sein, jeden bestehenden Glykolipid Struktur zu identifizieren, bis die Verfügbarkeit von Standard-Glykolipide, die chemisch synthetisiert werden können.
Die kritischen Schritte dieser Analyse sind die Recovery Rate von GSL aus biologischen Proben. Typischerweise 80 ug GSL kann von 100 Millionen Tumorzellen wie RBL zurückgewonnen werden. Um eine ausreichende molekulare Ionen für mehrere Runden der Fragmentierung in Ionenfallen-Massenspektrometer zu erzeugen, werden mindestens 10 Mikrogramm des Tumors GSLs erforderlich. Geringe Ausbeute von GSL während der Reinigung wird auf niedriger Häufigkeit von Ionen, die nicht zu einer weiteren Fragmentierung unterworfen werden könnten. Der Erfolg der Analyse ist abhängig von der Menge von GSL welche wiedergewonnen werden. Typischerweise Endkonz.entration der permethylierten GSLs erreichen sollte 1 mg / ml, in Methanol gelöst, bevor sie auf einem Nano-Elektrospray-Quelle analysiert. Der Grenzwert für eine gründliche Analyse MS n ist abhängig von der Häufigkeit des spezifischen Ions in MS 1 Profil. Eine typische e 7 Ionenhäufigkeit ist für eine gründliche MS 5 Analyse erforderlich. Die geringe Ausbeute von GSL während der Reinigung kann durch den Verlust von GSL während Peracetylierung Schritt (die entfernt die Phospholipide), wenn die pro-acetylierten GSLs um Florisil Harz Chromatographiesäule muss gebunden werden, gewaschen und anschließend eluiert verursacht werden. Um die Bindung von Pro-acetylierten GSLs an Silicagel zu gewährleisten, sollten die Proben zweimal in die Chromatographiesäule geladen werden nach Durchströmen.
Offenlegungen
DZ ist ein Berater für Biotex, Houston, TX, und einem Erfinder in Patenten im Zusammenhang mit Technologien in diesem Artikel erwähnt, ausgegeben oder in Anwendung eingebunden.
Danksagungen
DZ wird von MD Anderson Cancer Center und NIH Zuschüsse AI079232 unterstützt. MD Anderson Cancer Center wird zum Teil durch NIH CA16672 unterstützt.
Materialien
| Name | Company | Catalog Number | Comments |
| 1,2 Dichlor–thane | Sigma-Aldrich | 34872 | Carcinogenic |
| Acetic acid | VMR | JT9524-0 | |
| Acetic anhydride | Fluka | 45830 | |
| Acetone | Fischer | A18P-4 | |
| Chloroform | Fischer | C606-1 | Carcinogenic |
| DEAE Sephadex A25 (Cl Form) | GE Healthcare Biosciences | AB 17—170-01 | 100 gram |
| Decane (anhydrous): | Sigma-Aldrich | 457116 | 100 ml |
| Dichloroacetic acid | Sigma | D54702 | Carcinogenic |
| Dialysis cassette | Fischer(Pierce) | 66110 | Slide-A-Lyzer, 3500 MWCO, 3-12 ml |
| DMSO | Thermo Scientific | 20684 | |
| Ethyl acetate | Fischer | UN1173 | |
| Florisil | Fluka | 46384 | for packing chromatography column |
| Hexanes | EMD | HX0290-6 | |
| Iodomethane | Riedel de Haen, Germany | 03810 | stabilized with silver foil Carcinogenic |
| Methanol | VWR/EMD | MXO475-1 | |
| Neutral glycosphingolipid Qualmix | Matreya | 1505 | |
| Monosialganglioside mixture | Matreya | 1508 | |
| Disialoganglioside mixture | Matreya | 1509 | |
| Lactosyl ceramide and sialosylderivatives | Matreya | 1510 | |
| Gangliotetraosyl ceramide and sialosyl derivatives | Matreya | 1511 | |
| Pasteur pipettes | Fischer | 13-678-6A | 9"'' |
| Pyridine: | Sigma | 270407 | |
| Sodium Hydroxide: | BDH | 0292 | 500 gram |
| Sodium methoxide | Sigma | 404367 | 0.5 M solution in methanol |
| Toluene | J.T. Baker | 9351-03 | 4 L |
| Pasteur pipettes | Fischer | 13-678-6A | 9"'' |
| Fiber glass (glass wool) | Corning Incorporated | 3950 | Pyrex 9989 glass |
| 12x75 mm glass tubes | Fischer | 14-962-10B | |
| Calibrated pipettes (100 microlitter) | VMR | 53432-921 | |
| 16x100 mm disposible borosilicate tubes x1,000 | Fischer | 14-961-29 | With screw caps |
| Caps for glass tubes | Kimble | 40566C | size/13-415 |
| Merck TLC plates | Sigma | Z 29, 301-6 | |
| Glass tank for TLC | Sigma | Z 12,619-5 | |
| Drummond Microcaps | Drummond scientific company | 1-000-0100 | 10 μl, for loading of TLC samples |
| Sunrise Microplate Absorbance Reader | Tecan | A-5082 | |
| Whatman Chromatography Paper | Fischer | 05-716-3E | 18 cm x 34 cm For TLC Tank |
| Orcinol ferric chloride spray reagent | Sigma | O7875 | For detecting glycosphingolipids on TLC plates |
| Prevel Spray Unit | Sigma | Z 36,555-6 | |
| Sonicator | Fischer | FS20 | |
| Centrifuge | Sorvall | Legend RT | |
| Speedvac | Savant | AS160 | With chemical trap for organic solvants |
| MALDI TOF-TOF Mass spectrometer | Applied Biosystems | Proteomics 4700 | |
| Ion Trap Mass spectrometer | Thermo | LTQ |
Referenzen
- Schnaar, R. L., Suzuki, A., Stanley, P. Chapter 10 Glycosphingolipids. Essentials of Glycobiology. Varki, A., Cummings, R. D., Esko, J. D., Freeze, H. H., Stanley, P., Bertozzi, C. R., Hart, G. W., Etzler, M. E. , 2nd edition, Cold Spring Harbor Laboratory Press. Cold Spring Harbor, N.Y. (2009).
- Bendelac, A. Chapter 17 NKT cells and other Innate-like T and B lineages. Fundamental Immunology. Paul, W. E. , 6th edition, Lippincott Williams & Wilkins. (2011).
- Jacewicz, M., Clausen, H., Nudelman, E., Donohue-Rolfe, A., Keusch, G. T. Pathogenesis of shigella diarrhea. XI. Isolation of a shigella toxin-binding glycolipid from rabbit jejunum and HeLa cells and its identification as globotriaosylceramide. J. Exp. Med. 163 (6), 1391-1404 (1986).
- Zhou, D. The immunological function of iGb3. Curr. Protein Pept. Sci. 7 (4), 325-333 (2006).
- Miyamoto, K., Miyake, S., Yamamura, T. A synthetic glycolipid prevents autoimmune encephalomyelitis by inducing TH2 bias of natural killer T cells. Nature. 413 (6855), 531-534 (2001).
- Zhou, D., Levery, S. B., Hsu, F. F., Wang, P. G., Teneberg, S., Almeida, I. C., Li, Y., Xu, H., Wang, L. X., Xia, C., Ibrahim, N. K., Michael, K. Immunologic mapping of glycomes: implications for cancer diagnosis and therapy. Frontiers in Bioscience. S3, 1520-1532 (2011).
- Li, Y., Thapa, P., Hawke, D., Kondo, Y., Furukawa, K., Furukawa, K., Hsu, F. F., Adlercreutz, D., Weadge, J., Palcic, M. M., Wang, P. G., Levery, S. B., Zhou, D. Immunologic glycosphingolipidomics and NKT cell development in mouse thymus. J. Proteome Res. 8 (6), 2740-2751 (2009).
- Li, Y., Zhou, D., Xia, C., Wang, P. G., Levery, S. B. Sensitive quantitation of isoglobotriaosylceramide in the presence of isobaric components using electrospray ionization-ion trap mass spectrometry. Glycobiology. 18 (2), 166-176 (2008).
- Li, Y., Teneberg, S., Thapa, P., Bendelac, A., Levery, S. B., Zhou, D. Sensitive detection of isoglobo and globo series tetraglycosylceramides in human thymus by ion trap mass spectrometry. Glycobiology. 18 (2), 158-165 (2008).
- Hakomori, S. I. A rapid permethylation of glycolipid, and polysaccharide catalyzed by methylsulfonyl carbanion in dimethyl sulfoxide. J. Biochem. (Tokyo). 55, 205(1964).
- Ciucanu, I., Kerek, F. Rapid and simultaneous methylation of fatty and hydroxy fatty acids for gas-liquid chromatographic analysis. Carbohydr. Res. 131, 209(1984).
- Kang, P., Mechref, Y., Klouckova, I., Novotny, M. V. Rapid Commun Mass Spectrom. 19 (23), 3421-3428 (2005).
- Levery, S. B., Hakomori, S. Microscale methylation analysis of glycolipids using capillary gas chromatography-chemical ionization mass fragmentography with selected ion monitoring. Methods Enzymol. 138, 13-25 (1987).
- Spooncer, E., Fukuda, M., Klock, J. C., Oates, J. E., Dell, A. Isolation and characterization of polyfucosylated lactosaminoglycan from human granulocytes. J. Biol. Chem. 259 (8), 4792-4801 (1984).
- Ciucanu, I., Costello, C. E. Elimination of oxidative degradation during the per-O-methylation of carbohydrates. J. Am. Chem. Soc. 125, 16213(2003).
- Platt, F. M., Neises, G. R., Karlsson, G. B., Dwek, R. A., Butters, T. D. N-butyldeoxygalactonojirimycin inhibits glycolipid biosynthesis but does not affect N-linked oligosaccharide processing. J. Biol. Chem. 269 (43), 27108-27114 (1994).
- Mulloy, B., Hart, G. W., Stanley, P. Chapter 47 Structural Analysis of Glycans. Essentials of Glycobiology. Varki, A., Cummings, R. D., Esko, J. D., Freeze, H. H., Stanley, P., Bertozzi, C. R., Hart, G. W., Etzler, M. E. , 2nd edition, Cold Spring Harbor Laboratory Press. Cold Spring Harbor, N.Y. (2009).
- Ashline, D., Singh, S., Hanneman, A., Reinhold, V. Congruent strategies for carbohydrate sequencing. 1. Mining structural details by MSn. Anal. Chem. 77 (19), 6250-6262 (2005).
- Zhang, H., Singh, S., Reinhold, V. N. Congruent strategies for carbohydrate sequencing. 2. FragLib: an MSn spectral library. Anal. Chem. 77 (19), 6263-6270 (2005).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenWeitere Artikel entdecken
This article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten