Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Beobachtung und Analyse der Oberfläche-enhanced Raman-Streuung zu blinken
In diesem Artikel
Zusammenfassung
Dieses Protokoll beschreibt die Analyse der blinkende Oberfläche-enhanced Raman Streuung durch die Irrfahrt eines einzelnen Moleküls auf einer silbernen Oberfläche mittels macht Gesetze.
Zusammenfassung
Aus einem einzigen Molekül an eine silberne Nanoaggregate-Kreuzung wird blinkend Oberfläche-enhanced Raman-Streuung (SERS) beobachtet. Hier ist ein Protokoll zum Vorbereiten der SERS-Active präsentiert Silber Nanoaggregate, eine Video von bestimmten blinkenden Stellen im mikroskopischen Bild aufzeichnen und analysieren die blinkenden Statistiken. In dieser Analyse reproduziert ein Potenzgesetz Wahrscheinlichkeitsverteilungen für helle Veranstaltungen im Verhältnis zu ihrer Dauer. Die Wahrscheinlichkeitsverteilungen für dunklen Ereignisse sind durch ein Potenzgesetz mit einer Exponentialfunktion ausgestattet. Die Parameter des Kraft Gesetzes darstellen molekulare Verhalten in hellen und dunklen Staaten. Die Random-Walk-Modell und die Geschwindigkeit des Moleküls über die gesamte Silberoberfläche können geschätzt werden. Es ist schwer zu schätzen, auch bei Verwendung von Durchschnittswerten, Autokorrelation Funktionen und Höchstauflösung SERS Imaging. In Zukunft sollte Kraft Gesetz Analysen mit spectral imaging, kombiniert werden, da die Ursprünge des blinken von dieser Analysemethode allein nicht bestätigt werden können.
Einleitung
Oberfläche-enhanced Raman-Streuung (SERS) ist hochsensiblen Raman-Spektroskopie von einer edlen Metall-Oberfläche. Da das Raman-Spektrum detaillierte Informationen über molekulare Struktur basierend auf den scharfen Peak-Positionen durch die Schwingungs-Modi von funktionellen Gruppen in den Molekülen liefert kann die Informationen eines einzelnen Moleküls auf einer Metalloberfläche untersucht werden Verwendung von SERS1,2,3. Aus einem silbernen Nanoaggregate mit einem adsorptiv Einzelmolekül-Ebene wird ein Blinksignal1,2,3,4,5,6, beobachtet. 7 , 8 , 9 , 10 , 11 , 12 , 13 , 14 , 15 , 16und das Spektrum schwankt1,2,3,4,5,6,7,8, 9,10,11,12,13,14. Blinken kann durch ein einzelnes Molekül induziert werden, die nach dem Zufallsprinzip innerhalb und außerhalb eine verbesserte elektromagnetischen (EM) Feld an einer Kreuzung nanometergroßen Silber Nanoaggregate bewegt. Daher gilt das Blinken einfache Beweise für die Einzelmolekül-Erkennung, verglichen mit einer Technik, die mit einer Poisson-Verteilung von SERS Intensität und eine Bi-Analyt2,3,17. Die detaillierten Mechanismen des blinkenden und schwankenden Spektrums, das molekulare Verhalten auf der Ag-Oberfläche stark abhängen kann, sind jedoch nach wie vor umstritten.
In früheren Studien wurde blinken SERS analysiert mithilfe der Autokorrelationsfunktion, die die Diffusionskoeffizienten und Konzentration der Moleküle, die eine verbesserte EM Feld12,13,14 zunehmenden berechnen können . Darüber hinaus hat der zeitliche Verlauf der Signal-15eine normalisierte Standardabweichung Punktzahl, die Instabilität in die Gesamtintensität darstellt, abgeleitet. Jedoch können diese analytische Ansätze auf das Verhalten von wenigen Molekülen beruhen. Im Gegensatz dazu kann in eine super-Resolution Imaging blinkender SERS, Einzelmolekül-Verhalten in einem erweiterten EM-Feld identifizierten16sein. Allerdings können diese Techniken solche Parameter nur in einer erweiterten EM-Feld erhalten. Das zufällige Verhalten eines einzelnen Moleküls in einem weiten Bereich (z. B. in SERS blinkt) kann als ein Potenzgesetz, anstatt eine durchschnittliche4,5,6,7,8 dargestellt werden ,9,10,11, ähnlich wie blinkende Fluoreszenz aus einem einzigen Halbleiter Quantum Dot (QD)18,19. Durch den Einsatz einer Kraft Gesetz Analyse4,5,6,7,8,9,10,11, molekulare Verhalten kann im hellen Zustand (in der erweiterten EM-Feld) und dunklen Zustand10geschätzt werden; Das heißt, kann das Verhalten des Moleküls Silber vollflächig geschätzt werden.
Für diese Technik sind Silber kolloidales Nanoaggregates verwendeten4,5,6,7,8,9,10,11. Diese Nanoaggregates zeigen verschiedene lokalisierte Oberflächen Plasmon-Resonanz (LSPR)-Bands, die stark verbesserte elektromagnetische Felder beeinflussen, wenn sie aufgeregt bei bestimmten Wellenlängen sind. So erhalten Sie sofort SERS-Active Silber Nanopartikel in kolloidalen Suspension und einige Daten vorhanden sind. Bei einfachen Nanostrukturen, die bestimmte Größen, Formen und Arrangements haben, kann die LSPR Abhängigkeit des SERS blinken andere Abhängigkeiten7verbergen; nämlich, wenn das gut oder schlecht Nanostruktur, LSPR verwendet wird, werden die Parameter konstant, und die anderen Abhängigkeiten werden daher ausgeblendet werden. Kraft Gesetzes Analyse wurde verwendet, um verschiedene Abhängigkeiten von der blinkenden SERS aus Silber kolloidales Nanoaggregates4,5,6,7,8, zu entdecken 9 , 10 , 11.
Access restricted. Please log in or start a trial to view this content.
Protokoll
1. die Probenvorbereitung
-
Vorbereitung von kolloidalem Silber-Nanopartikeln 20
- Um kolloidales Silber-Nanopartikeln zu fabrizieren, lösen Sie 0,030 g Silbernitrat und 0,030 g Trinatrium Citrat Dihydrat in 150 mL Wasser in einen 200-mL Rundboden-Kolben.
- Kombinieren Sie die Flasche mit einem Reflux (Dimroth) Kondensator.
- Rühren Sie die Lösung in die Flasche mit einem magnetischen Rührer und rühren. Dann Hitze rühren Lösung in die Küvette in einem Ölbad bei 150 ° C für 60 min.
Hinweis: Die Lösung leuchtet gelb, dann milchig grau. - Kühlen Sie die Federung bei Raumtemperatur ab, und halten Sie die Aufhängung in die Küvette mit Alu-Folie im Kühlschrank abgedeckt.
Hinweis: Das Protokoll kann an dieser Stelle angehalten werden. Verwenden Sie die kolloidale Nanopartikel nach Lagerung im Kühlschrank, innerhalb eines Monats.
-
Vorbereitung der Probe für mehrfarbige blinkende emission 11
- Um einen Objektträger bereit, eine Glasplatte mit Seife per hand waschen und mit Wasser abspülen.
- Die Glasplatte 0,1 % Poly-L-Lysin wässriger Lösung hinzu, und entfernen Sie die Lösung mit einem Gebläse.
- Die Glasplatte Silber kolloidalen Suspension hinzu, und entfernen Sie die Aufhängung mit einem Gebläse.
- Fügen Sie einen Dropdown-Bereich auf der Glasplatte mit einem flüssigen Blocker Stift.
- Tropfen Sie destilliertes Wasser auf der Glasplatte, und bedecken Sie es mit einem anderen Glasplatte auf einen Objektträger zu schaffen und verhindern, dass Wasser verdunstet.
-
Vorbereitung der Probe für monotone farbigen blinkenden SERS 7 , 8 , 9 , 10
- Um einen Objektträger bereit, eine Glasplatte mit Seife per hand waschen und mit Wasser abspülen.
- Mischen Sie silberne kolloidale Suspension mit Thiacyanine oder Thiacarbocyanine Farbstoff (25 oder 4 µM, beziehungsweise) und eine wässrige Lösung von NaCl (10 mM) in einem Volumenverhältnis von 2:1:1.
- Fallen Sie die Probe-Suspension auf der Glasplatte, und entfernen Sie die Aufhängung mit einem Gebläse.
- Fügen Sie einen Dropdown-Bereich auf der Glasplatte mit einem flüssigen Blocker Stift.
- Legen Sie eine wässrige Lösung von NaCl (1 M) auf der Glasplatte, die Silber-Nanopartikel zu immobilisieren, und bedecken Sie es mit einem anderen Glasplatte zum Erstellen einer Mikroskop-Gleitplatte und verhindern, dass die Lösung verdunstet.
2. Beobachtung von Silber-Nanopartikeln zu blinken
-
Beleuchtung der Probe
- Legen Sie die Probe Glasplatte mit Protokoll 1,2 oder 1,3 auf der Bühne von einem inversen Mikroskop zubereitet.
- Beleuchten Sie die Probe Glasplatte mit weißem Licht durch ein Dunkelfeld Kondensor und Fokus auf verschiedenen farbigen Flecken (blau, grün, gelb und rot) auf der Glasplatte mit einem Objektiv (60 X).
- Beleuchten Sie die Probe Glasplatte mit eine abgeschwächte Strahl, geliefert in einem Winkel von 30° im Verhältnis zu der Oberfläche der Probe aus einem Diodenlaser gepumpten Festkörperlaser (DPSS) Dauerstrich-(cw) durch ein Interferenzfilter.
- Laser-Beleuchtung verwenden, um die silberne Nanoaggregates als eintönig farbige Flecken in einer gleichfarbigen Umgebung zu beobachten, verschieben Sie der Laserbereich Beleuchtung in den Mittelpunkt der Ansicht, und konzentrieren Sie sich auf die Flecken auf der Glasplatte durch Anpassen der Bühne in Z-Richtung.
-
Beobachtung von blinken
- Fügen Sie einen lang-Pass-Filter nach der Objektivlinse und beleuchten Sie die Probe Glasplatte mit einem DPSS cw-Laserstrahl in einem Winkel von 30° gegenüber der Probenoberfläche durch ein Interferenzfilter geliefert.
- Finden Sie das Blinken Flecken, wie in Abbildung 1 dargestellt (siehe auch Abbildung S1 in das ergänzende Material) von der Bühne in x- und y-Richtung verschieben.
- Videoaufnahme der blinkenden Spots mit der inversen Mikroskop, gekoppelt mit einer gekühlten kostenlos – Coupled Digitalgerät (CCD) Kamera, die eine zeitlichen Auflösung von 61-120 ms hat, für 20 Minuten.
3. Analyse der SERS blinkt
-
Ableitung der zeitliche Verlauf von video
- In der Software steuert, dass die CCD-Kamera, die video-Datei zu öffnen.
- Wenn die blinkende Flecken und dunklen Bereich auswählen möchten, ziehen Sie Bereiche, die separat Regionen mit und ohne Flecken im Videobild zu decken.
- Um die blinkende Flecken und dunkle Bereiche im Video Signal Intensität Zeitprofile abgeleitet, wählen Sie Zeitliche Analyse Analyse, und klicken Sie auf berechnen im Fenster Zeitliche Analyse .
- Speichern Sie die Daten als Textdatei.
-
Analyse der das Zeitprofil
- Glätten Sie einen Überblick über den zeitlichen Verlauf durch Subtraktion der zeitliche Verlauf von den dunklen Bereich und/oder Armatur mit eine Polynomfunktion, wie in den Abbildungen 2A und 2 bdargestellt.
- Bewerten Sie eine gemittelte Baseline-Intensität, die besteht aus ca. 2000 Punkte ichbaseund einer Standardabweichung von Baseline Intensitäten, σ, wie in den Figuren 2 und 2Ddargestellt.
- Dunklen Ereignissen mit größerer Intensität als ein Schwellenwert von ichbase + 3σ unterscheiden Sie hellen Ereignisse, und notieren Sie die Dauer der jeweiligen Veranstaltung. In Abbildung 3, z. B. Aufzeichnen der Veranstaltung von 0 bis 3.5476 s als das dunkle Ereignis (mit einer Laufzeit von t = 3.5476 s), und notieren Sie das Event vom 3.5476 bis 4.0981 s als helles Ereignis (mit einer Laufzeit von t = 0.5505 s). Wiederholen Sie Vorgang, wie in Tabelle 1dargestellt.
- Die Anzahl der hellen und dunklen Ereignisse für jede Dauer ausgedrückt in die erste und zweite Zeile der Tabelle 2.
- Addieren Sie die Anzahl der Ereignisse für jede Dauer, außer bei Veranstaltungen kürzer als Dauer t. Ausgedrückt in den zweiten und dritten Zeilen der Tabelle 2Summe zum Beispiel die Anzahl der Ereignisse für jede Dauer (außer bei Veranstaltungen für t = 0.0612 s) als 41 + 18 + 9 +...; Das Ergebnis ist gleich die Summe für t = 0.1223 s, d. h. 103.
- Unterteilen Sie die Summierungen von jeder Dauer und normalisieren sie. Wie in Tabelle 2angegeben, z. B. Teilen Sie die Summe für die Dauer t = 0.0612 s durch die Dauer 0.0612 s. Das Ergebnis ist 3,351.5791. Teilen Sie das Ergebnis dann durch die Summe der Ergebnisse in die vierte Zeile in Tabelle 2. Die Wahrscheinlichkeitsverteilung wird abgeleitet, um 0.64494 zu sein.
- Die Wahrscheinlichkeitsverteilungen für die hellen Ereignisse Pauf(t) gegen ihre Dauer t in einem Logarithmus-Logarithmus Graphen Plotten, und Log10Ppassenauf(t) durch Log10 (
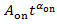 ), die Kraft Gesetz Exponent αauf für eine bestimmte Stelle blinkt abzuleiten. Wenn Pauf(t), durch ausgestattet ist
), die Kraft Gesetz Exponent αauf für eine bestimmte Stelle blinkt abzuleiten. Wenn Pauf(t), durch ausgestattet ist 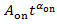 , der Anpassungslinie weicht von den Parzellen bei kleinen Werten von Pauf(t), wie gezeigt durch die gestrichelte Linie in Abbildung 4A.
, der Anpassungslinie weicht von den Parzellen bei kleinen Werten von Pauf(t), wie gezeigt durch die gestrichelte Linie in Abbildung 4A. - Die Wahrscheinlichkeitsverteilungen für dunklen Ereignisse Paus(t) gegen ihre Dauer t in einem Logarithmus-Logarithmus Graphen Plotten, und Log10Paus(t) von Log10(passen
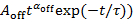 , die Kraft Gesetzes Exponent αaus und die Trunkierung Zeit τ aus der gleichen blinken vor Ort abzuleiten. Wenn Paus(t), durch ausgestattet ist
, die Kraft Gesetzes Exponent αaus und die Trunkierung Zeit τ aus der gleichen blinken vor Ort abzuleiten. Wenn Paus(t), durch ausgestattet ist 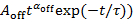 , die angepasste Kurve weicht von den Parzellen bei kleinen Werten von Paus(t).
, die angepasste Kurve weicht von den Parzellen bei kleinen Werten von Paus(t). - Wiederholen Sie 3.2.1 zu 3.2.8 für die anderen blinkende Punkte im Video.
Access restricted. Please log in or start a trial to view this content.
Ergebnisse
Aus der silbernen Nanoaggregates mit Poly-L-Lysin ausgearbeiteten Protokoll 1.2 sind mehrfarbige blinkende Spots von SERS und Oberfläche verbessert Fluoreszenz beobachtet, wie in Abbildung 111gezeigt. Im Gegensatz dazu wurden eintönige farbige blinkende Flecken von SERS mit der Farbstoffmoleküle ausgearbeiteten Protokoll 1.37,8,9,
Access restricted. Please log in or start a trial to view this content.
Diskussion
Von der Kreuzung Silber Nanoaggregate wird SERS ausgegeben. Wir müssen also bereiten Sie Nanoaggregates anstatt kolloidale Nanopartikel, die mit Citrat Anionen bedeckt sind. Silber Aggregate werden durch das Einsalzen, Effekt, der durch die Zugabe von Poly-L-Lysin, die NH -3+ und ist der Ursprung der SERS, geformt oder Na+ Kationen aus NaCl, wie in Abbildung S2 des zusätzlichen Materials dargestellt. Darüber hinaus wird zur Beleuchtung der vielen Stellen in den weiten ...
Access restricted. Please log in or start a trial to view this content.
Offenlegungen
Der Autor hat nichts preisgeben.
Danksagungen
Der Autor dankt Prof. Y. Ozaki (Kwansei Gakuin University) und Dr. T. Itoh (National Institute of Advanced Industrial Science and Technology) für ihre fruchtbare Diskussionen dieser Arbeit. Diese Arbeit wurde vom Ministerium für Bildung, Kultur, Sport, Wissenschaft und Technologie (Nr. 16 K 05671) von KAKENHI (Beihilfe für wissenschaftliche Forschung C) unterstützt.
Access restricted. Please log in or start a trial to view this content.
Materialien
| Name | Company | Catalog Number | Comments |
| Silver nitrate, 99.8% | Wako | 194-00832 | |
| Trisodium citrate dihydrate, 99. % | Wako | 191-01785 | |
| Poly-L-lysine aqueous solution, 0.1% | Sigma-Aldrich | P8920 | |
| 3,3'-disulfopropylthiacyanine triethylamine | Hayashibara Biochemical Laboratories | NK-2703 | a kind of thiacyanine dyes |
| 3,3'-diethyl-5,5'-dichloro-9-methylthiacarbocyanine iodine salt | Hayashibara Biochemical Laboratories | SMP-9 | a kind of thiacarobocyanine dyes |
| Sodium chloride, 99.5% | Wako | 191-01665 | |
| Dimroth condenser | Iwaki | 61-9722-22 | perchased from AS ONE |
| Magnetic stirrer | Corning | DC-420D | |
| Oil bath | Advantech | OS-220 | |
| Glass plate | Matsunami | S-1112 | Microscope slide |
| Blower | Hozan | Z-288 | Air duster |
| Liquid blocker pen | Daido Sangyo | LIQUID BLOCKER (Super Pap Pen). Ready-to-use hydrophobic barrier pen designed for immunohistochemistry applications | |
| Inverted microscope | Olympus | IX-70 | |
| Objective lens | Olympus | LCPlanFl 60× | NA 0.7 |
| Dark field condenser | Olympus | U-DCD | NA 0.8–0.92 |
| Cooled digital CCD camera | Hamamatsu | ORCA-AG | controlled by software Aqua Cosmos |
| Software for the cooled digital CCD camera | Hamamatsu | AquaCosmos | used for also derivation of the time-profiles from the blinking spots in the video |
| Color CCD camera | ELMO | TNC-C920 | not used for analysis |
| DPSS laser | RGB laser system | NovaPro532-75 | λ = 532 nm; 60 mW (corresponds to a power density of 600 W/cm2) |
| Interference filter | Semrock | LL01-532-12.5 | |
| Long pass filter | Semrock | BLP01-532R-25 | |
| Software for the distinguishment and counting of the bright/dark events | home-maid | programmed by C++ | |
| Software for the fitting by a power law | LightStone | Origin6.1 |
Referenzen
- Qian, X. M., Nie, S. M. Single-molecule and single-nanoparticle SERS: from fundamental mechanisms to biomedical applications. Chem. Soc. Rev. 37, 912-920 (2008).
- Pieczonka, N. P. W., Aroca, R. F. Single molecule analysis by surfaced-enhanced Raman scattering. Chem. Soc. Rev. 37, 946-954 (2008).
- Kneipp, J., Kneipp, H., Kneipp, K. SERS -a single-molecule and nanoscale tool for bioanalytics. Chem. Soc. Rev. 37, 1052-1060 (2008).
- Kitahama, Y., Ozaki, Y. Analysis of blinking SERS by a power law with an exponential function. Frontiers of Surface-Enhanced Raman Scattering: Single-Nanoparticles and Single Cells. , Wiley. Chichester. Chapter 6 (2014).
- Kitahama, Y. Truncated Power Law Analysis of Blinking SERS. Frontiers of Plasmon Enhanced Spectroscopy Volume 1 (ACS Symposium series Vol. 1245). , American Chemical Society. Washington DC. Chapter 4 (2016).
- Bizzarri, A. R., Cannistraro, S. Lévy Statistics of Vibrational Mode Fluctuations of Single Molecules from Surface-Enhanced Raman Scattering. Phys. Rev. Lett. 94, 068303(2005).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Power-law analysis of surface-plasmon-enhanced electromagnetic field dependence of blinking SERS of thiacyanine or thiacarbocyanine adsorbed on single silver nanoaggregates. Phys. Chem. Chem. Phys. 13, 7439-7448 (2011).
- Kitahama, Y., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of excitation laser intensity dependence of blinking SERRS of thiacarbocyanine adsorbed on single silver nanoaggregates by using a power law with an exponential function. Chem. Commun. 47, 3888-3890 (2011).
- Kitahama, Y., Enogaki, A., Tanaka, Y., Itoh, T., Ozaki, Y. Truncated power law analysis of blinking SERS of thiacyanine molecules adsorbed on single silver nanoaggregates by excitation at various wavelengths. J. Phys. Chem. C. 117, 9397-9403 (2013).
- Kitahama, Y., Araki, D., Yamamoto, Y. S., Itoh, T., Ozaki, Y. Different behaviour of molecules in dark SERS state on colloidal Ag nanoparticles estimated by truncated power law analysis of blinking SERS. Phys. Chem. Chem. Phys. 17, 21204-21210 (2015).
- Kitahama, Y., Nagahiro, T., Tanaka, Y., Itoh, T., Ozaki, Y. Analysis of blinking from multicoloured SERS-active Ag colloidal nanoaggregates with poly-L-lysine via truncated power law. J. Raman. Spectrosc. 48, 570-577 (2017).
- Habuchi, S., et al. Single-Molecule Surface Enhanced Resonance Raman Spectroscopy of the Enhanced Green Fluorescent Protein. J. Am. Chem. Soc. 125, 8446-8447 (2003).
- Weiss, A., Haran, G. Time-Dependent Single-Molecule Raman Scattering as a Probe of Surface Dynamics. J. Phys. Chem. B. 105, 12348-12354 (2001).
- Emory, S. R., Jensen, R. A., Wenda, T., Han, M., Nie, S. Re-examining the origins of spectral blinking in single-molecule and single-nanoparticle SERS. Faraday Discuss. 132, 249-259 (2006).
- Itoh, T., Iga, M., Tamaru, H., Yoshida, K., Biju, V., Ishikawa, M. Quantitative evaluation of blinking in surface enhanced resonance Raman scattering and fluorescence by electromagnetic mechanism. J. Chem. Phys. 136, 024703(2012).
- Willets, K. A. Super-resolution imaging of SERS hot spots. Chem. Soc. Rev. 43, 3854-3864 (2014).
- Dieringer, J. A., Lettan, R. B., Scheidt, K. A., Van Duyne, R. P. A Frequency Domain Existence Proof of Single-Molecule Surface-Enhanced Raman Spectroscopy. J. Am. Chem. Soc. 129, 16249-16256 (2007).
- Cichos, F., von Borczyskowski, C., Orrit, M. Power-law intermittency of single emitters. Curr. Opin. Colloid Interface Sci. 12, 272-284 (2007).
- Tang, J., Marcus, R. A. Mechanisms of fluorescence blinking in semiconductor nanocrystal quantum dots. J. Chem. Phys. 123, 054704(2005).
- Lee, P. C., Meisel, D. Adsorption and surface-enhanced Raman of dyes on silver and gold sols. J. Phys. Chem. 86, 3391-3395 (1982).
- Krichevsky, O., Bonnet, G. Fluorescence correlation spectroscopy: the technique and its applications. Rep. Prog. Phys. 65, 251-297 (2002).
- Hess, S. T., Huang, S., Heikal, A. A., Webb, W. W. Biological and Chemical Applications of Fluorescence Correlation Spectroscopy: A Review. Biochemistry. 41, 697-705 (2002).
Access restricted. Please log in or start a trial to view this content.
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten