Method Article
Mikroskopische Visualisierung von porösen Nanographenen, die durch eine Kombination aus Lösungs- und Oberflächenchemie synthetisiert werden
In diesem Artikel
Zusammenfassung
Eine Kombination aus lösungs- und oberflächengestützter Synthese eröffnet neue Wege in der atomar präzisen Synthese von Nanostrukturen. Die Rastertunnelmikroskopie (STM), ergänzt durch die berührungslose Rasterkraftmikroskopie (nc-AFM), ermöglicht eine detaillierte Charakterisierung von neu entworfenen und erzeugten kohlenstoffbasierten Nanoobjekten.
Zusammenfassung
Die On-Surface-Synthese gilt in jüngster Zeit als vielversprechender Ansatz für die Erzeugung neuer molekularer Strukturen. Besonders erfolgreich war es bei der Synthese von Graphen-Nanobändern, Nanographenen und intrinsisch reaktiven und instabilen, aber dennoch attraktiven Spezies. Es basiert auf der Kombination von Lösungschemie mit dem Ziel, geeignete molekulare Vorläufer für weitere oberflächengestützte Umwandlungen im Ultrahochvakuum herzustellen. Dieser Ansatz verdankt seinen Erfolg auch einer unglaublichen Entwicklung von Charakterisierungstechniken, wie z.B. dem Rastertunneln/Rasterkraftmikroskopie und verwandten Methoden, die eine detaillierte, lokale Charakterisierung auf atomarer Skala ermöglichen. Während die oberflächengestützte Synthese molekulare Nanostrukturen mit hervorragender Präzision bis hin zu einzelnen Atomen liefern kann, leidet sie unter der Basis auf metallischen Oberflächen und der oft begrenzten Ausbeute. Daher scheinen die Ausweitung des Ansatzes weg von Metallen und der Kampf um Produktivitätssteigerung eine große Herausforderung für breitere Anwendungen zu sein. Darin demonstrieren wir den Ansatz der On-Surface-Synthese zur Erzeugung von nicht-planaren Nanographenen, die durch eine Kombination aus Lösungschemie und sequentiellen oberflächengestützten Prozessen synthetisiert werden, zusammen mit der detaillierten Charakterisierung durch Rastersondenmikroskopie-Methoden.
Einleitung
In den letzten Jahren wurden präzise Fragmente einer Graphenschicht, nämlich Nanographene, erzeugt1,2,3,4,5 und Graphen-Nanobänder6,7 gewinnen wachsende Aufmerksamkeit aufgrund von Perspektiven für weitreichende Anwendungen in Bereichen wie Sequenzierung, Gassensorik, Siebung, (Opto-)Elektronik und Photovoltaik. Die größenbegrenzten Nanostrukturen, die die Graphen-Atomstruktur duplizieren, behalten ihre hervorragenden Eigenschaften wie hohe Beweglichkeit der Ladungsträger oder mechanische Festigkeit. Um jedoch ein hohes Maß an Kontrolle über die gewünschten einstellbaren Eigenschaften zu erreichen, sind Präzision und Wiederholbarkeit bis hin zu einzelnen Atomen in der chemischen Synthese erforderlich. Während die traditionelle Lösungschemie einen unglaublich hohen Entwicklungsstand erreicht hat und die Synthese eines extrem breiten Spektrums von Molekülen mit der notwendigen Präzision und Wiederholgenauigkeit ermöglicht und zusätzlich eine hervorragende Effizienz erreicht, bleibt die Synthese von atomar reinen und präzisen ausgedehnten Nanostrukturen nach wie vor eine Herausforderung. Eine der größten Schwierigkeiten scheint die abnehmende Löslichkeit von immer größeren Nanostrukturen zu sein. Unter den verschiedenen Ansätzen, die als vielversprechend zur Überwindung dieser Schwierigkeiten angesehen werden, hat sich in den letzten Jahren die Kombination von Nass- und Oberflächenansatz in großem Umfang entwickelt8,9,10,11,12,13,14. Diese Strategie basiert auf der Herstellung stabiler, löslicher und gut strukturierter molekularer Vorläufer, die durch Lösungschemie erzeugt werden. Des Weiteren werden die Vorläufer auf den atomar sauberen kristallinen Oberflächen abgeschieden, in der Regel unter Ultrahochvakuumbedingungen (UHV). In der Folge werden Prozesse an der Oberfläche ausgelöst, oft unterstützt durch die katalytische Aktivität der Oberfläche10,15. Ein solcher Ansatz hat sich bei der Herstellung von Graphen-Nanobändern als besonders leistungsfähig erwiesen6,7, die häufig durch die Kombination von Polymerisation15 und Zyklodehydrierung6,7,16 Abläufe14. Zweifellos führen die am weitesten verbreiteten Protokolle zu kovalenten Bindungen molekularer Vorläufer und internen Umwandlungen, die eine Planarisierung durch die Bildung neuer Benzolringe ermöglichen14. Der Wunsch, ein höheres Maß an Kontrolle über die Eigenschaften der auf diese Weise erzeugten molekularen Nanostrukturen zu erlangen, zwingt die Suche nach Wegen, die es ermöglichen, über die sechseckigen Ringe hinauszugehen und gleichzeitig die atomare Präzision zu erhalten. Dies könnte durch gezieltes Design und Synthese von molekularen Vorläufern erreicht werden, die sich in sequentiellen Umwandlungen durch Zwischenstrukturen entwickeln könnten17,18. Ein solcher Ansatz hat sich als effizient erwiesen (z. B. bei der Erzeugung von porösen Nanostrukturen wie nanoporösem Graphen19 oder Nanographene mit eingebetteten Ringen8,17,18). Der Erfolg des Ansatzes der Oberflächensynthese ist dank der Einführung neuer Forschungsmethoden in den letzten Jahrzehnten möglich, die einen Einblick in die lokale atomare Struktur von Molekülen mit bisher unerreichter Präzision ermöglichen. Dies könnte mit der Rastertunnelmikroskopie (STM) erreicht werden20,21,22 und in jüngster Zeit sogar mit höherer Auflösung mit berührungsloser Rasterkraftmikroskopie (AFM) mit funktionalisierten Spitzen, die bindungsaufgelöste Bilder liefern23. Hier stellen wir die Synthese von trigonalen porösen Nanographenen vor, die durch die Kombination von Lösungschemie mit oberflächengestützten Prozessen erzeugt werden17. Des Weiteren demonstrieren wir die atomar präzise Visualisierung der erzeugten Nanoobjekte auf Basis der STM-, STS- (Rastertunnelspektroskopie) und nc-AFM (berührungslose Rasterkraftmikroskopie) Techniken17.
In diesem Bericht werden in Abschnitt 1 die Verfahren zur Herstellung des speziell entwickelten molekularen Vorläufers (d. h. Dodecaphenyl[7]starphen) beschrieben. Des Weiteren wird in Abschnitt 2 ein Verfahren zur sauberen Au(111)-UHV-Aufbereitung beschrieben. Darauf folgt die Darstellung des Verfahrens, das zur Abscheidung von Vorläufern auf der Au(111)-Oberfläche führt, die unter UHV-Bedingungen gehalten wird. Diese Vorgehensweisen werden in Abschnitt 3 ausführlich beschrieben. Anschließend stellen wir in Abschnitt 4 ein detailliertes Protokoll vor, das zur Oberflächensynthese von trigonalen porösen Nanographenen durch absichtliches Glühen führt, das sequentielle Zyklodehydrierungsprozesse auslöst. Die STM-Messungen und die dI/dV-Kartierung der elektronischen Wolken sind in Abschnitt 5 beschrieben. In Abschnitt 6 schließlich wird gezeigt, wie die nc-AFM-Spitze funktionalisiert und bindungsaufgelöste Messungen durchgeführt werden können, um zweifellos die Struktur der auf der Oberfläche erzeugten Nanographene zu entschlüsseln.
Protokoll
HINWEIS: Die Reaktion zur Gewinnung von Dodecaphenyl[7]starphen (Abbildung 1) wurde in Lösung unter Argon unter Verwendung von ofengetrockneten Glaswaren durchgeführt. Alle experimentellen Verfahren im Zusammenhang mit der Synthese und Reinigung dieser Verbindung wurden in einem Abzug durchgeführt. Das Oberflächenexperiment wurde unter Verwendung eines Niedertemperatur-STM/AFM-Systems (LT) unter Anwendung des Au(111)-Kristalls und molekularer Vorläufer durchgeführt, die unter den UHV-Bedingungen verdampft und anschließend geglüht wurden (Abbildung 2).
1. Synthese von Dodecaphenyl[7]starphen (Abbildung 1)
- 95 mg handelsübliches 5,6,7,8-Tetraphenyl-2-(trimethylsilyl)-3-naphthyltriflat, 16,5 mg Pd(PPh3)4 und ein teflonbeschichtetes magnetisches Rührstäbchen werden in einen Schlenk-Kolben gegeben.
- Der Schlenk-Kolben wird mit einem Vakuum versehen, um das atmosphärische Gas zu evakuieren. Mit Argon auffüllen.
- 12 ml einer Mischung aus wasserfreiem CH3CN/THF (5:1) werden in den Kolben gegeben.
- Fügen Sie 65 mg wasserfreies und fein pulverisiertes CsF hinzu.
- Erhitzen (60 °C) und das Reaktionsgemisch unter Argon 16 Stunden lang umrühren.
- Das Reaktionsgemisch wird über einen Filtertrichter (Borosilikatglas, Porengröße: 10-20 μm) filtriert. Waschen Sie den Feststoff nacheinander mit 10 mL CH3CN (zweimal) und 10 mL Et2O (zweimal). Entsorgen Sie die Lösungsmittel.
- Der resultierende Feststoff wird in einem Soxhlet-Gerät 16 Stunden lang mit 50 mlCHCl 3 extrahiert.
- Entfernen SieCHCl 3 unter reduziertem Druck, um 23 mg Docecaphenyl[7]starphen als weißen Feststoff zu erhalten, der als Nanographen-Vorläufer verwendet wird.
2. Vorbereitung der atomar sauberen Au(111)-Oberfläche
- Verwenden Sie Nitrilhandschuhe, um die Probe vor Kontamination zu schützen. Waschen Sie die Handschuhe vor dem Gebrauch mit Alkohol.
- Der Au-Kristall (Au(111)-monokristallin) wird in dem Ultraschallwäscher gespült, der mit Aceton und anschließend mit Isopropanol gefüllt ist. Lassen Sie die Probe 5 Minuten lang vollständig in jedes der Lösungsmittel eintauchen.
- Montieren Sie den Au(111)-Monokristall auf dem Probenhalter, der mit dem LT-STM-Transfersystem kompatibel ist, indem Sie zwei dünne Tantal-Metallstreifen verwenden, die fest mit dem Probenhalter verschweißt sind.
- Übertragen Sie die Probe in das UHV-System und erhitzen Sie sie etwa eine Stunde lang auf über 100 °C, um die Verschmutzung von der Oberfläche, insbesondere vom Wasser, zu entfernen. Anschließend wird die Probe in die Vorbereitungskammer überführt und mit dem in der Vorbereitungskammer montierten Widerstandsheizer auf 450 °C geglüht. Regelung der Temperatur durch das Thermoelement (Typ K); Die Prozessdauer wird auf 15 min geschätzt.
- Kalibrieren Sie die Pistole vor dem Sputtern mit Luminophor. Stellen Sie den Abstand zwischen der Pistole und der Probe auf ~50 mm ein.
- Während des Glühens wird die Probe mit Ar+ -Ionen gesät, die von der Ionenkanone mit einem Gasdruck von 5 x 10-7 mbar bereitgestellt werden, wobei die Pistole in einem Winkel von 45° zur Probenoberfläche ausgerichtet ist.
- Wiederholen Sie den Glüh- und Sputtervorgang mindestens dreimal. Nach drei Zyklen überprüfen Sie die Qualität der Probe durch STM-Messungen. Die entsprechend präparierte Au(111)-Oberfläche muss das bekannte Fischgrätenmuster ohne meldepflichtige Verunreinigungen aufweisen (Ergänzende Abbildung 2). Wenn die Probe immer noch nicht atomar rein ist, wiederholen Sie den Reinigungsvorgang.
3. Abscheidung des Nanographen-Vorläufers (Docecaphenyl[7]starphen) auf dem Au(111)-Kristall
HINWEIS: Die Knudsen-Zelle muss mit einem separaten Ventil in der Vorbereitungskammer montiert werden, um eine einfache Entlüftungsoption zu ermöglichen (z. B. für den Austausch von Vorläufern ohne Systementlüftung).
- Schließen Sie das Ventil zwischen der Knudsen-Zelle und der Präparationskammer.
- Entlüften Sie die Knudsen-Zelle und nehmen Sie sie aus der Präparationskammer.
- Füllen Sie den speziellen Quarztiegel mit Molekülen. Verwenden Sie ~1 mg des Molekularpulvers.
- Platzieren Sie den Tiegel richtig in der Knudsen-Zelle.
- Montieren Sie die Knudsen-Zelle auf das Ventil an der Präparationskammer und pumpen Sie sie mit der externen Vakuumpumpe nach unten. Öffnen Sie nicht das Ventil zwischen der Präparationskammer und der Knudsen-Zelle, um eine Kontamination der Präparationskammer zu vermeiden.
- Gasen Sie die Knudsen-Zelle mindestens 12 Stunden lang bei 120 °C aus, um Verunreinigungen zu entfernen. Während des Ausgasens kühlen Sie die Tiegel in der Knudsen-Zelle auf Raumtemperatur (oder niedriger) ab, um die Moleküle im Tiegel vor Überhitzung und unkontrollierter Verdampfung zu schützen.
HINWEIS: Das Verfahren ist auf den molekularen Vorläufer anwendbar, der bei Raumtemperatur unter UHV-Bedingungen einen vernachlässigbaren Dampfdruck aufweist. - Wenn das Vakuumniveau in der Knudsen-Zelle im niedrigen Bereich von 10-10 mbar liegt, öffnen Sie das Ventil zwischen der Zelle und der Vorbereitungskammer. Schließen Sie anschließend das Ventil zwischen der Knudsen-Zelle und der externen Pumpe. Schalten Sie außerdem die externe Pumpe aus.
- Um den molekularen Fluss zu kalibrieren, verwenden Sie eine Quarz-Mikrowaage. Erhöhen Sie die Temperatur in der Knudsen-Zelle 10 Minuten lang vorsichtig um 5 °C (durch Einstellen des entsprechenden Temperaturwerts am Knudsen-Zellencontroller) und überwachen Sie die Variation des molekularen Flusses, indem Sie die Anzeige der Quarz-Mikrowaage überprüfen.
HINWEIS: Der adäquate Flussmittel für Dodecaphenyl[7]starphen-Moleküle beträgt ca. 1 Hz/5 min. Wenn das Flussmittel für 5x5 min = 25 min stabil ist, ist der Kalibriervorgang abgeschlossen.
4. Präparation der Nanographene auf der Oberfläche
- Die saubere Au(111)-Probe wird aus der Mikroskopkammer in die Präparationskammer überführt. Anschließend wird die saubere Au(111)-Probe direkt auf eine Linie mit der Knudsen-Fassung gebracht (hier beträgt der Winkel zwischen Probenoberfläche und Verdampfer 85°) und der Abstand zwischen der Probe und dem Verdampfer auf 50-100 mm eingestellt. Halten Sie die Probe von der Knudsen-Zelle abgewandt, um eine unkontrollierte Ablagerung des molekularen Materials zu vermeiden.
- Mit der Knudsen-Zelle scheiden Sie die Moleküle ab, indem Sie die Probe so drehen, dass sie der Knudsen-Zelle zugewandt ist, und die Probe für t=4 min in einer solchen Position halten (dies entspricht ca. ~0,8 Hz Auslesung der Quarzmikrowaage, was einer Unterschichtbedeckung entspricht, die für weitere Schritte der intramolekularen Bindungsbildungsprozesse entscheidend ist). Drehen Sie anschließend die Probe so, dass sie von der Knudsen-Zelle weg zeigt. Schalten Sie die Knudsen-Zelle aus, um die Verdunstung zu stoppen.
- Glühen Sie die Probe mit den Molekülen auf vordefinierte Temperaturen: (1) 320 °C für 15 Minuten; (2) 370 °C für 15 min.
- Messen Sie die Probe nach jedem Glühschritt mit LT-STM/AFM, um das aktuelle Stadium des Experiments zu untersuchen und das Vorhandensein und die Art der erzeugten Objekte zu überprüfen.
- Während der STM-Messungen ist die Probenvorspannung auf -1,0 V und der Tunnelstrom-Sollwert auf 100 pA einzustellen, um eine Unterscheidung zwischen unterschiedlich reagierenden Molekülen zu ermöglichen (Abbildung 5).
5. dI/dV-Messungen
- Schließen Sie den Lock-in-Verstärker an die Mikroskopelektronik an: Verbinden Sie It mit dem Eingang des Lock-in, Vext mit dem Ausgang des Lock-in-Verstärkers. Verbinden Sie den AUX-Ausgang des Lock-ins mit dem AUX-Eingang in der Mikroskopelektronik.
- Stellen Sie die Lock-in-Parameter ein: Frequenz (560-720 Hz), Amplitude (~10 mV) und Zeitkonstante (10 ms).
- Nähern Sie sich der Oberfläche vorsichtig mit der STM-Spitze, wenn die Verriegelung ausgeschaltet ist. Ziehen Sie sich 2-3 Schritte von der Oberfläche zurück. Schalten Sie den Lock-in ein und überwachen Siedas IT-Signal . Durch Ändern der Phase des Lock-in-Verstärkers minimieren Siedas IT-Signal um den Nullpunkt.
- Annäherung an die Oberfläche; Jetzt ist der Lock-in bereit für die Messungen.
- Kalibrieren Sie dI/dV auf einer sauberen Au(111)-Oberfläche, indem Sie nach der Position und Form des Shockley-Oberflächenzustands 24,25,27 suchen.
- Stellen Sie für das dI/dV-Mapping den niedrigen Wert der Scangeschwindigkeit ein. Verwenden Sie die Rasterzeit in der Größenordnung von 4 ms pro Punkt.
6. Funktionalisierung des NC-AFM-Sensors
HINWEIS: Die Gasleitung mit CO muss in der Mikroskopkammer montiert werden, da CO-Moleküle bei T > 40 K aus der Probe desorbieren, so dass die CO-Moleküle direkt auf gekühlten Proben abgelagert werden, die im Kryostaten gelagert werden. Montieren Sie den CO-Melder aus Sicherheitsgründen in der Nähe der UHV-Anlage.
- Kühlen Sie die Probe im Mikroskop auf 5 K ab.
- Öffnen Sie das Leckageventil mit CO für t=1:30 min und stellen Sie den Druck des CO auf den Wert von pCO=5x10-8 mbar ein.
- Überprüfen Sie die Probe unter STM. Wenn die Spitze metallisch ist (ohne CO), weisen die CO-Moleküle auf der Au-Oberfläche einen spezifischen Kontrast in STM auf, der in der ergänzenden Abbildung 3c22 dargestellt ist.
- Um das einzelne CO-Molekül aufzunehmen, führen Sie den Vorgang entweder manuell durch oder versetzen Sie den Controller in den Spektroskopiemodus mit vordefinierten Parametern, einschließlich der folgenden Schritte.
- Platzieren Sie die Spitze über dem CO-Molekül, das für die Aufnahme bei +0,5 V und 15 pA vorgesehen ist.
- Ziehen Sie die Spitze um mindestens 0,3 nm zurück.
- Erhöhen Sie die Spannung auf +3 V.
- Bringen Sie die Fläche in die zuvor vordefinierte Position (vor dem Einfahren) zurück.
- Stellen Sie die Spektroskopiezeit auf etwa 5 s ein und überwachen Sie die I(t)-Kurve, deren abrupte Änderung des I-Wertes auf den Manipulationsprozess der CO-Aufnahme hinweist. Die oben erwähnte Spektroskopiedauer von 5 s wurde gewählt, um die Auslösezeit des Aufnehmers lange genug dauern zu lassen, um ein angemessenes Gleichgewicht zwischen dem Wirkungsgrad des Aufnehmers und der Umkehrabsetzung des CO zu erreichen.
- Prüfen Sie, ob sich der STM-Kontrast des CO-Moleküls verändert hat. Das typische Erscheinungsbild, das bei +0,5 V, 15 pA aufgezeichnet wurde, ist in der ergänzenden Abbildung 3b dargestellt.
- Die Spitze wird durch das CO-Molekül funktionalisiert. Wenn das CO-Molekül verloren geht, wiederholen Sie den Vorgang bis zur erfolgreichen Funktionalisierung.
7. Nc-AFM mit CO-Messungen
- Nähern Sie sich der Oberfläche im STM-Modus.
- Führen Sie das STM-Imaging durch. Wählen Sie aus dem STM-Scan das getrennte Einzelmolekül für nc-AFM-Messungen aus.
- Suchen Sie im STM-Modus eine geeignete z-Ebene, die parallel zur Molekülebene verläuft.
- Ziehen Sie die Spitze um ca. 0,7 nm von der Oberfläche zurück und schalten Sie die STM-Schlaufe aus.
- Finden Sie eine Q-plus-Sensorfrequenz, stellen Sie die Parameter für die Amplitude (~100 pm) und die AFM-Schleife (~3% P-I) ein.
- Starten Sie den Scanvorgang mit niedriger Scangeschwindigkeit.
- Während des Scannens nähern Sie sich der Oberfläche Schritt für Schritt mit einem exemplarischen Schritt bis zu 0,01 nm und beobachten Sie den Scan, bis das bindungsaufgelöste Bild aufgenommen wurde.
Ergebnisse
Abbildung 2 zeigt schematisch die UHV-STM/nc-AFM-Experimente. Zuerst wird der Au(111)-Einkristall durch Zyklen des Glühens und gleichzeitigen Sputterns mit Ar+-Ionen gereinigt. Die saubere Au-Oberfläche weist das bekannte Fischgräten-Rekonstruktionsmuster auf, das in STM-Aufnahmen als helle Kämme entsteht, die durch einen dunkleren Bereich getrennt sind. Dies ist bereits in Abbildung 2 gut visualisiert, wo die Au(111)-Probe als topografisches 3D-STM-Bild dargestellt ist. Die Kämme der Oberflächenrekonstruktion trennen die fcc- und hcp-Bereiche, wie in der Einschub der ergänzenden Abbildung 2a angedeutet. Abbildung 2 zeigt auch relativ schmale und hoch isolierte Entitäten. Dabei handelt es sich um Vorläufermoleküle, die durch Glühen umgewandelt werden. Das Verfahren wird im Folgenden in den folgenden Absätzen beschrieben und die Molekültrennung ist recht typisch für Kohlenwasserstoffspezies auf Au(111)28,29,30. An dieser Stelle ist es wichtig zu beachten, dass die Vorbereitung einer sauberen Oberfläche bei vielen Experimenten von entscheidender Bedeutung ist, bei denen Verunreinigungen das Verhalten der interessierenden Adsorbate stark beeinflussen können. Die Sauberkeit der Au(111)-Oberfläche konnte in der STM-Bildgebung überwacht werden, indem das Fischgrätmuster visualisiert und die meisten reaktiven Stellen (d.h. die Ellbogen der Rekonstruktionstopographie, wo die Rippen ihre Richtung ändern) untersucht wurden. In der sauberen Probe sind die Ecken wie in der ergänzenden Abbildung 2a darzustellen, ohne dass zusätzliche Unebenheiten auftreten, die auf Verunreinigungen hinweisen könnten.
Es ist auch wichtig, dass vor der Charakterisierung der elektronischen Eigenschaften durch dI/dV-Einzelpunkt- und laterale Mapping-Spektroskopie die Spitze auf der Au(111)-Oberfläche kalibriert werden muss, um eine weitestgehende Entkopplung der Spitzenzustände von den Oberflächen- und Adsorbateigenschaften zu ermöglichen. Dies ist ein wichtiger Schritt, da sonst die erhaltenen Spektroskopiedaten stark von den Eigenschaften der Spitzenspitze beeinflusst werden könnten und die erfassten STS-Resonanzen sowie räumliche Bilder die komplexe Faltung sowohl der Spitzen- als auch der Probeneigenschaften darstellen könnten. Um die Spitze zu kalibrieren, wird ein zweistufiges Verfahren empfohlen. Zunächst müssen die hochauflösenden STM-Bilder des Fischgrätmusters aufgenommen werden. Zweitens müssen die Einzelpunkt-STS-Spektren der blanken Oberfläche das bekannte Merkmal darstellen, das dem Au-Shockley-Oberflächenzustand entspricht (d. h. der Kurvenverlauf von STS dI/dV(V) muss relativ flach sein, mit einem deutlich erkennbaren Beginn des Oberflächenzustands bei etwa -0,5 V und ohne weitere übertriebene Schwankungen des dI/dV-Signals, wie in der ergänzenden Abbildung 2b24 dargestellt, 25,26,27). Wenn die aufgezeichneten Daten die oben genannten Anforderungen nicht erfüllen, muss die Spitze gereinigt werden; Dies geschieht häufig durch sanftes Aufprallen der Spitze in die Probenoberfläche, bis das Fischgrätenmuster eindeutig aufgezeichnet und das entsprechende dI/dV-Signal über Au(111) erreicht ist.
Um bindungsaufgelöste nc-AFM-Messungen zu ermöglichen, muss die Mikroskopspitze mit dem CO-Molekül23 funktionalisiert werden. Bei der Funktionalisierung konzentriert sich der erste Schritt auf die Abscheidung von CO-Molekülen auf der Au(111)-Oberfläche, die bei kryogenen Temperaturen gehalten wird. Für die CO-Aufnahme haben wir das Verfahren angewendet, das im Spektroskopiemodus durchgeführt wird, der den Ansatz über die für die Manipulation des CO-Moleküls vorgesehene Spannungsrampe und die weitere Überwachung des Strom-Zeit-Signals enthält. Die schematische Darstellung des Prozesses ist in der ergänzenden Abbildung 3a dargestellt. Des Weiteren verifizieren wir die erfolgreiche Funktionalisierung der Spitze, indem wir das Erscheinungsbild der an der Oberfläche adsorbierten CO-Moleküle aufzeichnen22. Die ergänzende Abbildung 3a,b zeigt das typische Erscheinungsbild des CO-Moleküls auf Au(111), das unter spezifischen Tunnelbedingungen mit (ergänzende Abbildung 3b, deutlich sichtbare Beule in der Mitte des CO-Bildes) und ohne das CO-Molekül aufgenommen wurde (ergänzende Abbildung 3c, keine Anzeichen der charakteristischen Beule in der Mitte).
Abbildung 3 zeigt schematisch die Idee hinter der sequentiellen Zyklodehydrierung auf der Oberfläche. Wir gehen von den flexiblen Vorläufern aus (gekennzeichnet durch ein schwarzes Rechteck), die mit dem lösungschemischen Ansatz hergestellt werden. Des Weiteren führen wir das zweistufige oberflächengestützte Cyclodehdrogenierungsverfahren durch, das das molekulare Propeller-Zwischenprodukt (markiert durch ein blaues Rechteck) mit bereits intern verschmolzenen Schaufeln und schließlich die nicht-planaren Nanographene mit eingebetteten [14]annulenen Poren liefert. Die Zielmoleküle sind in Abbildung 3 durch ein rotes Rechteck dargestellt.
Der erste Schritt der Cyclodehydrierung wird erreicht, wenn die Au(111)-Probe mit molekularen Vorläufern bei 320 °C geglüht wird, wodurch isolierte molekulare Propeller entstehen, die durch STM deutlich sichtbar gemacht werden, wie in Abbildung 4 gezeigt. Die nicht-planare Konformation der Moleküle konnte aus ihrem STM-Aussehen abgeleitet werden, wobei in Abbildung 4b,c drei helle Lappen deutlich erkennbar waren, die durch blaue Kreise markiert sind.
Die abschließende Zyklodehydrierung, die [14]annulene Poren ergibt, wird erreicht, wenn die Probe auf 370 °C erhitzt wird. Abbildung 5 zeigt das STM-Erscheinungsbild isolierter Moleküle, das hochauflösende Bild in Abbildung 5b zeigt das Vorhandensein eines molekularen Gemisches mit einzelnen Einheiten, die ein, zwei drei eingebettete Poren enthalten.
Schließlich wird die detaillierte strukturelle Charakterisierung durch bindungsaufgelöste nc-AFM-Messungen (siehe Abbildung 6 ) und die anschließende Charakterisierung der elektronischen Zustände (siehe Abbildung 7) erreicht.
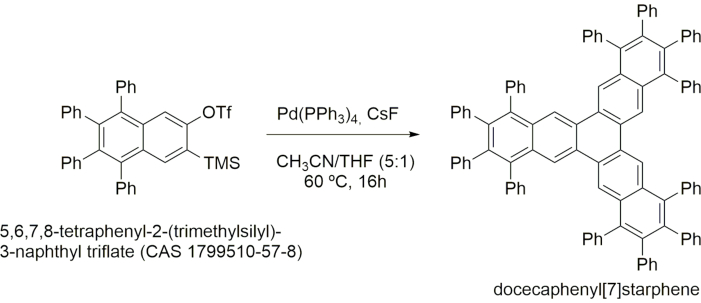
Abbildung 1. Synthetisches Verfahren zur Gewinnung des Nanographen-Vorläufers (d. h. Dodecaphenyl[7]starphen) durch Lösungschemie. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
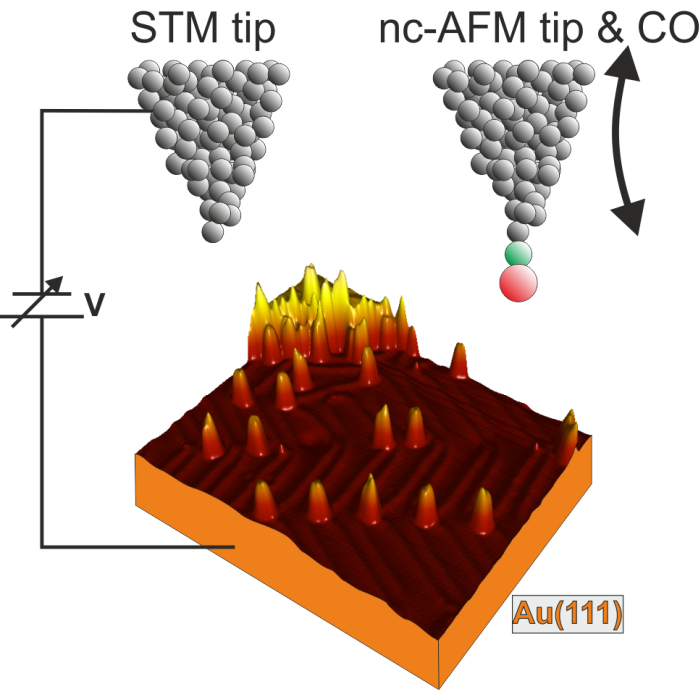
Abbildung 2. Schema des UHV STM/nc-AFM-Experiments. Das CO-Molekül wird an der Spitze der AFM-Spitze mit der Farbcodierung grün - C, rot - O angezeigt. Der Pfeil mit zwei Spitzen zeigt die Oszillationsbewegung der AFM-Spitze an. Unten ist das 3D-STM-Bild der Au(111) mit transformierten Vorläufern zu sehen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
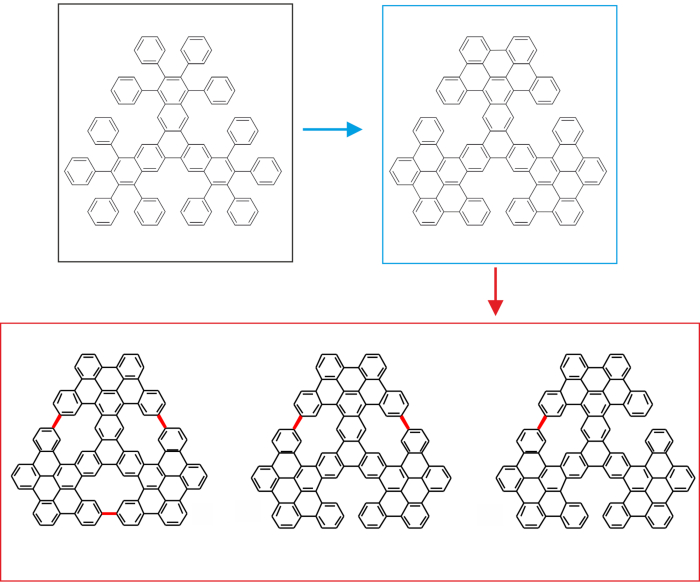
Abbildung 3. Schema, das die Idee des sequentiellen Synthesewegs der Zyklodehydrierung zeigt. Der Vorläufer ist durch ein schwarzes Rechteck gekennzeichnet. Der molekulare Zwischenpropeller ist durch das blaue Rechteck gekennzeichnet. Die Zielmoleküle, die mit eingebetteten [14]Anulenringen ausgestattet sind, sind durch ein rotes Rechteck hervorgehoben. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
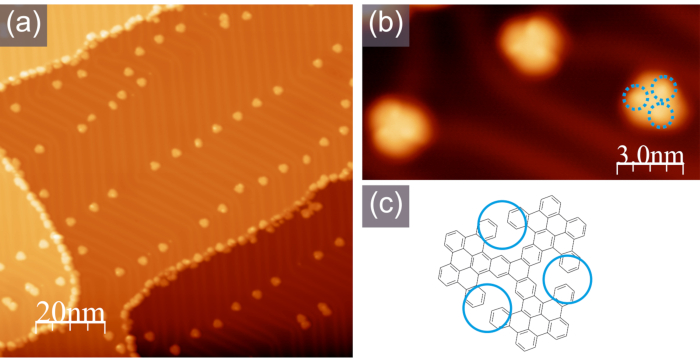
Abbildung 4. Typisches STM-Erscheinungsbild des Zwischenpropellers. a) ein großformatiges STM-Bild; b) ein hochauflösendes STM-Bild mit deutlich erkennbaren hellen Lappen, die den nicht-planaren Anteilen der Moleküle entsprechen, wie in dem in Buchstabe c) gezeigten Schema angegeben, -1,0 V, 100 pA. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
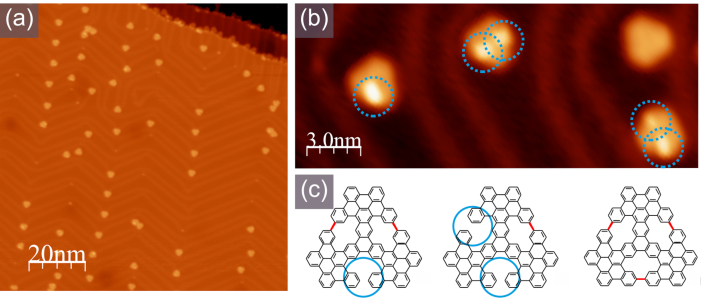
Abbildung 5. Typisches STM-Erscheinungsbild der Moleküle mit eingebetteten [14]Anulenringen. a) ein großformatiges STM-Bild; b) ein hochauflösendes STM-Bild mit deutlich erkennbaren hellen Lappen, die den nicht-planaren Teilen der Moleküle entsprechen, wie in dem in (c) gezeigten Schema -1,0 V, 100 pA angegeben. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
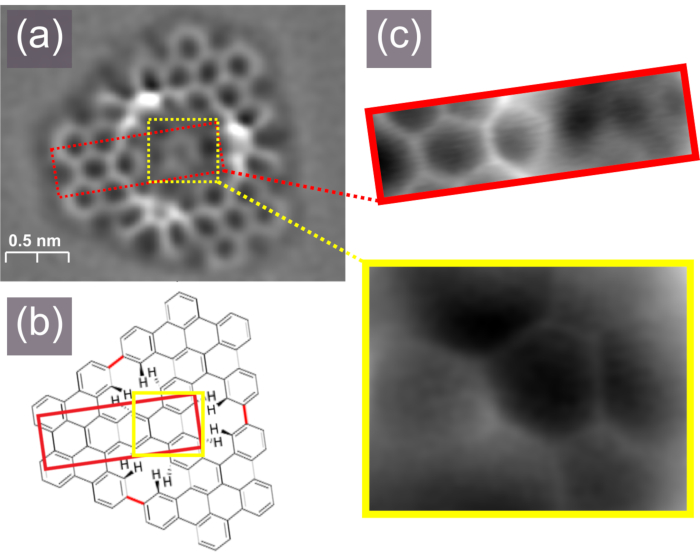
Abbildung 6. Bindungsaufgelöstes nc-AFM-Bild der Frequenzverschiebung des trigonalen porösen Nanographens (a) mit seinem in (b) gezeigten Schema, kleinere nc-AFM-Bilder zeigen Teile des Moleküls (c). Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
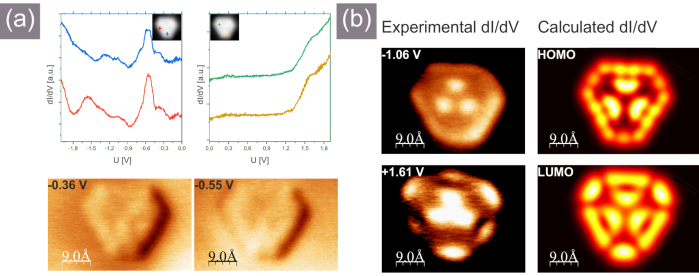
Abbildung 7. Rastertunnelspektroskopie-Daten, die für das trigonale poröse Nanographen gewonnen wurden. (a) Einzelpunkt-STS-Spektren (oben), dI/dV-Karten, die bei Spannungen aufgenommen wurden, die dem Beginn des Au-Oberflächenzustands entsprechen (Einschübe in den dI/dV-Diagrammen zeigen die laterale Lage der Spitze während der Spektroskopiemessungen); (b) linkes Feld - dI/dV-Raumbilder, die über das Nanographen bei Spannungen aufgenommen wurden, die den Resonanzen entsprechen, die bei Einzelpunkt-STS-Messungen aufgezeichnet wurden, wie in (a) gezeigt, rechtes Feld - berechnete dI/dV-Bilder bei den Spannungen, die den HOMO- und LUMO-Zuständen entsprechen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
Ergänzende Abbildung 1. Spektroskopische Charakterisierung von Docecaphenyl[7]starphen Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Abbildung 2. Au(111)-Oberfläche. (a) Hochauflösendes STM-Bild im gefüllten Zustand mit deutlich erkennbarem Fischgrätmuster, der Einschub zeigt ein vergrößertes Bild mit markierten fcc- und hcp-Bereichen, -1,0 V, 100 pA, (b) typische Einzelpunkt-STS-Daten, die mit einer gut geformten metallischen Spitze aufgenommen wurden und den Beginn des Au-Oberflächenzustands bei etwa -0,5 V darstellen. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Ergänzende Abbildung 3. Funktionalisierung der nc-AFM-Spitze mit einem CO-Molekül. a) eine schematische Zeichnung des Verfahrens; (b) ein typisches STM-Bild von Au(111) mit CO-Molekülen, das mit einer CO-funktionalisierten Spitze abgebildet wurde, das CO-Molekül wird als dunkle Vertiefung visualisiert, die von einem hellen Halo und einem charakteristischen hellen Lappen in der Mitte umgeben ist; c) ein typisches STM-Bild von Au(111) mit CO-Molekülen, das mit einer metallischen Spitze abgebildet ist; Das CO-Molekül wird als dunkle Vertiefung dargestellt, die von einem hellen Halo umgeben ist, ohne den charakteristischen hellen Lappen in der Mitte, beispielhafte CO-Moleküle sind durch weiße gestrichelte Kreise in (b,c), +0,5 V, 15 pA hervorgehoben. Bitte klicken Sie hier, um diese Datei herunterzuladen.
Diskussion
Für eine erfolgreiche oberflächengestützte Synthese und eine weitere detaillierte Charakterisierung umfassen die kritischen Schritte: (1) Lösungssynthese einer reinen Vorläuferprobe, die im Bereich von mindestens 1 mg liegen muss, um eine problemlose UHV-Abscheidung zu ermöglichen, (2) Erzeugung großer und atomar sauberer Terrassen der Au(111)-Oberfläche, (3) Abscheidung der entsprechenden Menge der molekularen Vorläufer auf der Probenoberfläche, (4) Vorbereitung und Anwendung der wohlgeformten STM-Spitze für dI/dV-Messungen und Spitzenfunktionalisierung für die bindungsaufgelöste nc-AFM-Bildgebung, (5) gezielte Erwärmung der Probe mit detaillierter Charakterisierung des Annealing-Ergebnisses in Bezug auf intramolekulare Transformationen.
Das erste Ziel wird durch das Design, die Synthese und die Reinigung des Nanographen-Vorläufers (Docecaphenyl[7]starphene) bestimmt. Die Synthese erfolgt in Lösung, in einem Schritt aus kommerziell erhältlichen Reagenzien, wie in Abbildung 1 gezeigt. Die Reinigung wird durch die Unlöslichkeit des Nanographen-Vorläufers in den meisten organischen Lösungsmitteln erleichtert. Daher fällt die Verbindung aus dem Reaktionsgemisch aus und wird dann durch Waschen und anschließende kontinuierliche Extraktion mit heißem Chloroform gereinigt.
Das zweite Ziel wird durch sich wiederholende Reinigungszyklen mit angemessener Überwachung der Probentemperatur erreicht, die 450 °C nicht überschreiten darf. Eine Überhitzung kann zu einer Beschädigung der Probe und zum Schmelzen führen. Die Oberflächenqualität muss durch STM-Messungen und die Aufzeichnung des Fischgrätmusters ohne erkennbare Verunreinigungen überprüft werden.
Um Ziel drei zu erreichen, muss man den Fluss der Vorläufermoleküle aus dem Pulver, das sich im Inneren des Verdampfers befindet, schonend kalibrieren. Die Experimente werden häufig mit molekularen Vorläufern durchgeführt, bei denen die Abscheidungstemperatur überhaupt nicht bekannt ist und vor dem Versuch schwer abzuschätzen sein kann und zusätzlich die Vorläufer fragil sein können. Daher wird empfohlen, die Kalibrierung langsam mit kleinen Schritten durchzuführen, um die Verdampfertemperatur zu erhöhen und die Anzeige der Quarzmikrowaage genau zu beobachten. Es ist sinnvoll, den Molekülfluss im Bereich von etwa 1 Hz pro 5 Minuten einzustellen, was je nach dem jeweiligen Vorläufer in etwa der Bildung einer geschlossenen Monoschicht innerhalb von mehr als 15 Minuten nach der Verdampfung entspricht. Solche Einstellungen ermöglichen eine präzise Abscheidung einer beträchtlichen Unterschichtmenge des Ausgangsmaterials, die für die Beobachtung von intramolekularen oberflächengestützten Umwandlungen am besten geeignet ist.
Das vierte Ziel wird durch das geeignete Verfahren der Spitzenbildung bestimmt. Bei der Vorbereitung der STM-Spitze ist es von größter Bedeutung, die beschriebenen Kalibrierprotokolle auf dem sauberen Au(111) zu befolgen, um irreführende STM- und STS-Ergebnisse zu vermeiden, die von einer schlecht geformten Spitze herrühren, die sich stark mit den Eigenschaften des interessierenden Objekts verflechtet. Daher müssen die dI/dV-Referenzspektren auf der Au(111)-Oberfläche jedes Mal erfasst und analysiert werden, wenn die Spitzenspitze während der Messungen verändert wird oder wenn die aufgenommenen STM-Bilder oder STS-Daten Verdacht erregen. Generell ist die STM- und insbesondere die STS-Bildgebung anfällig für Fehlinterpretationen, da die aufgezeichneten Daten nicht einfach mit dem topographischen Muster oder der elektronischen Struktur in Verbindung gebracht werden können, sondern die Faltung widerspiegeln. In diesem Zusammenhang scheint es entscheidend zu sein, dass der Einfluss der Spitze minimiert wird. Auf der anderen Seite bieten das Single-Point-STS- und das räumliche STS-Mapping einen noch nie dagewesenen Einblick in die Eigenschaften der nanoskaligen Objekte mit submolekularer Auflösung. Hier präsentieren wir ein Beispiel für die dI/dV-Einzelpunktspektroskopie und das planare dI/dV-Mapping, die für das trigonale poröse Zielnanographen durchgeführt wurden. Die Ergebnisse sind in Abbildung 7 dargestellt. Abbildung 7a zeigt die Einzelpunkt-STS-Daten, die immer über verschiedene Bereiche des Moleküls erfasst werden, um die Intensitätsschwankungen der STS-Resonanzen zu überwachen. Dies ist ein wichtiger Schritt, um eine Positionierung der Spitze über der molekularorbitalen Knotenebene zu vermeiden, die zu einer signifikanten Unterdrückung des STS-Signals beitragen und in der Folge zum Weglassen der speziellen Resonanz führen könnte. Die oberen Felder von Abbildung 7a zeigen ausgewählte Einzelpunkt-STS-Daten, die innerhalb der gefüllten und leeren staatlichen Regime aufgezeichnet wurden. Um die Übereinstimmung der aufgezeichneten Resonanzen mit den mit dem Molekül assoziierten Zuständen zu bestätigen, muss anschließend das räumliche dI/dV-Mapping durchgeführt werden. Die Bilder sind in Abbildung 7b dargestellt, die linke Spalte zeigt die experimentellen Daten, während die berechneten Bilder auf der rechten Seite dargestellt sind. Die vernünftige Übereinstimmung lässt den Schluss zu, dass die experimentell gemessene Resonanz bei -1,06 V mit dem dominanten Beitrag von HOMO in Verbindung gebracht werden könnte, während die bei +1,63 V erfasste Resonanz von LUMO dominiert wird. Wichtig ist, dass wir beachten müssen, dass es im gefüllten Zustand der Spektren, die über dem Molekül aufgezeichnet und in Abbildung 7a gezeigt sind, auch zwei weitere Resonanzen gibt, die näher am Fermi-Niveau liegen: bei -0,36 V und -0,55 V. Diese Resonanzen liegen jedoch im Bereich des bekannten Schockley-Oberflächenzustands und können von der Oberfläche statt vom Molekül selbst stammen. Darauf deutet auch das zusätzliche laterale dI/dV-Mapping hin, das bei den oben genannten Spannungswerten durchgeführt wird. Die Bilder sind am unteren Rand von Abbildung 7a zu sehen und wir können feststellen, dass wir innerhalb der Bilder nur die Erinnerung an die Molekülform ohne weitere Merkmale bemerken können, was es erlaubt, die beobachteten Resonanzen mit dem Oberflächenzustand in Verbindung zu bringen. Die obige Beschreibung weist deutlich auf die Bedeutung des Vergleichs zwischen den experimentell aufgezeichneten Daten und den Berechnungen bei der Zuordnung der Einzelpunkt-STS-Resonanzen und räumlichen dI/dV-Karten hin.
Die CO-Funktionalisierung erfordert einen patientenorientierten Ansatz; Daher wird die erfolgreiche Realisierung durch die Aufnahme von bindungsaufgelösten Bildern, die die Struktur des Molekülrückgrats zeigen, deutlich visualisiert. Die Annäherung an die NC-AFM-Bildgebung sollte Schritt für Schritt und mit dem Bewusstsein durchgeführt werden, dass die AFM-Verfahren in der Regel viel langsamer angewendet werden müssen als typische STM-Messungen. An dieser Stelle ist anzumerken, dass im vorgestellten Experiment die erwartete Zielstruktur, das trigonale poröse Nanographen, flach genug sein soll, um bindungsaufgelöste nc-AFM-Messungen zu ermöglichen. Dies wird in der Tat in Abbildung 5a bewiesen, wo das Bild der Frequenzverschiebung nc-AFM dargestellt ist. Das Aussehen des Nanographens deutet darauf hin, dass die Struktur aufgrund der sterischen Wechselwirkungen zwischen Wasserstoffatomen, die sich in den [14]annulenen Poren befinden, eine nicht-planare Konformation annimmt, wie in Abbildung 5b schematisch dargestellt. Das nc-AFM-Bild liefert auch zusätzliche Informationen über die Details der Nanographen-Konfiguration, ein kurzer Blick in Abb.5a lässt den Schluss zu, dass der zentrale Teil näher an der Au(111)-Oberfläche liegt als an den Rändern der Nanostruktur. Um die atomare Struktur des Nanographens besser sichtbar zu machen, insbesondere um das Vorhandensein des zentralen Phenylrings und der drei daran befestigten Arme zu zeigen, könnten zusätzliche kleinere nc-AFM-Bilder aufgenommen werden, bei denen die Scanhöhe an verschiedene Teile der Moleküle angepasst ist. Die Ergebnisse sind in Abbildung 5c dargestellt, wo der zentrale Phenylring mit drei angehängten Armen innerhalb des durch das gelbe Rechteck hervorgehobenen Bildes deutlich erkennbar ist und ein Arm im Detail durch das durch das rote längliche Rechteck markierte Bild sichtbar ist. Dies beweist, dass die verschiedenen Teile nicht-planarer Moleküle durch unabhängige Scans, die mit der an den zu visualisierenden Teil der Struktur angepassten Abtastebene durchgeführt wurden, getrennt dargestellt werden konnten31. Dennoch ist es wichtig zu beachten, dass die eher nicht-planaren Objekte, in unserem Fall die Zwischenprodukte als Beispiele dienen können, in der Regel zu wenig flach sind, um bondaufgelöste nc-AFM-Messungen zu ermöglichen, und die Identifizierung auf der Grundlage von STM-Bildgebung erfolgen muss. In einigen Fällen kann das nc-AFM jedoch auch durch Messungen angewendet werden, die nur über einen ausgewählten Bereich des Moleküls durchgeführt werden, der eine planare Konformation aufweist, wie am Beispiel des Zwischenprodukts mit zwei eingebetteten [14]annulenen Poren in Ref. 18 ausführlich beschrieben.
Die fünfte Zielerreichung basiert auf den mehrfachen Wiederholungen des On-Surface-Experiments während der Suche nach den geeigneten Bedingungen, um die oberflächengestützten intramolekularen Transformationen auszulösen. In diesem Zusammenhang muss jeder Schritt des Versuchs durch STM-Messungen verifiziert werden, die Hinweise auf die möglichen Prozesse geben; Schließlich ist es von Vorteil, wenn bindungsaufgelöste NC-AFM-Messungen angewendet werden, um das Ergebnis der Prozesse an der Oberfläche zu überprüfen.
Kombinierte STM/nc-AFM-Untersuchungen neu erzeugter molekularer Strukturen ermöglichen eine detaillierte Charakterisierung sowohl der strukturellen Anordnung als auch der elektronischen Zustände mit submolekularer Präzision. Daher scheinen die Rastersondenmikroskope bei der atomaren Charakterisierung von schwer fassbaren und neuen molekularen Gerüsten unersetzlich zu sein. Die Kombination von Lösungschemie, die wohlgeformte und reine molekulare Vorläufer mit oberflächengestützten Umwandlungen liefert, ist ein leistungsfähiger Ansatz für die präzise Synthese von Molekülen und hat sich insbesondere bei der Erzeugung neuer Nanographene und Graphen-Nanobänder als sehr erfolgreich erwiesen. Dies eröffnet neue Perspektiven für die Weiterentwicklung von Synthesestrategien, um die neuen Generationen von abstimmbaren Nanostrukturen mit den gewünschten Eigenschaften herzustellen. Dennoch ist das auf der oberflächengestützten Synthese basierende Verfahren auf die Reaktionsschemata beschränkt, die auf Oberflächen angewendet werden könnten, und die Anzahl der bereits etablierten Reaktionen ist recht begrenzt. Dies bedeutet, dass der Ansatz als eine Erweiterung bereits bestehender, gut entwickelter Protokolle der Lösungschemie angesehen werden könnte. Es sollte erwähnt werden, dass in einigen Fällen die bei der Oberflächensynthese beobachteten Reaktionen anders ablaufen als in Lösung, so dass sich die Endprodukte erheblich unterscheiden. Dies eröffnet Perspektiven für die Synthese neuer Verbindungen, die auf der Grundlage bestehender nasschemischer Wege nicht erzeugt werden können. Eine der großen Einschränkungen des Ansatzes ergibt sich auch aus der sehr begrenzten Menge der Produkte, die erzeugt werden können, sowie aus der manchmal beobachteten geringen Effizienz. Die mikroskopische Charakterisierung auf Basis von Rastersondentechniken mit funktionalisierten Spitzen bietet einen noch nie dagewesenen Einblick in die atomare Struktur neu geschaffener Verbindungen, ist aber andererseits sehr zeitaufwändig und auf die lokale Charakterisierung beschränkt. Mit anderen Worten, es bietet keine globale, makroskopische Sicht auf die synthetisierten Verbindungen, es sei denn, die Prozesse sind sehr homogen. Dies soll jedoch auch durch andere, stärker gemittelte Techniken bestimmt und bestätigt werden.
Offenlegungen
Die Autoren haben nichts offenzulegen.
Danksagungen
Wir danken für die finanzielle Unterstützung durch das Nationale Wissenschaftszentrum, Polen (2017/26/E/ST3/00855), die Agencia Estatal de Investigación (MAT2016-78293-C6-3-R und CTQ2016-78157-R), Xunta de Galicia (Centro singular de investigación de Galicia, Akkreditierung 2019-2022, ED431G 2019/03) und den Fondo Europeo de Desarrollo Regional (FEDER). IP dankt Xunta de Galicia und der Europäischen Union (Europäischer Sozialfonds, ESF) für die Vergabe eines Stipendiums für die Doktorandenausbildung.
Materialien
| Name | Company | Catalog Number | Comments |
| Au(111) monocrystal | SPL | Au (111) diameter 8 mm and 2 mm thick aligned to ~ 0.1 degree and one side polished make into model 12 | single monocrystal of Au |
| 5,6,7,8-tetraphenyl-2-(trimethylsilyl)-3-naphthyl triflate (CAS 1799510-57-8) | ABCR | AB357101 | |
| Argon gas (0.99% purity) | LindeGas | Argon 5.0 Ar 12 l 1 4950 001 | for ion sputtering |
| CH3CN | Sigma-Aldrich | 271004 | anhydrous |
| CHCl3 | vwr | 8,36,27,320 | |
| CO gas (0.99% purity) | LindeGas | Carbon monoxide 3.7 CO 12 l 1 4950 029 | for tip functionalization |
| CsF | Sigma-Aldrich | 289345 | anhydrous, finely podered, weigh in a glove box |
| Et2O | Sigma-Aldrich | 309966 | |
| Pd(PPh3)4 | Sigma-Aldrich | 216666 | Store cold under inert atmoshere, weigh in a glove box |
| PtIr wire 0.15mm | Mint of Poland | wire used for tip etching | |
| sample holder | ScientaOmicron | ||
| THF | Sigma-Aldrich | 186562 | anhydrous, 250 ppm BHT as inhibitor |
| tip holder | ScientaOmicron | tip holder LT-STM S2701-S |
Referenzen
- Ostroverkhova, O. Organic optoelectronic materials: mechanisms and applications. Chemical Reviews. 116, 13279(2016).
- Beser, U., et al. A C216-nanographene molecule with defined cavity as extended coronoid. Journal of the American Chemical Society. 138, 4322-4325 (2016).
- Ikemoto, K., Kobayashi, R., Sato, S., Isobe, H. Synthesis and bowl-in-bowl assembly of a geodesic phenylene bowl. Angewandte Chemie: International Edition. 56 (23), 6511-6514 (2016).
- He, L., et al. Trefoil-shaped porous nanographenes bearing a tribenzotriquinacene core by three-fold Scholl macrocyclization. Angewandte Chemie: International Edition. 57, 13635-13639 (2018).
- Buttrick, J. C., King, B. T. Kekulenes, cycloarenes, and heterocycloarenes: addressing electronic structure and aromaticity through experiments and calculations. Chemical Society Reviews. 46, 7-20 (2017).
- Cai, J., et al. Atomically precise bottom-up fabrication of graphene nanoribbons. Nature. 466, 470-473 (2010).
- Ruffieux, P., et al. On-surface synthesis of graphene nanoribbons with zigzag edge topology. Nature. 531, 489-492 (2016).
- Hieulle, J., et al. On-surface route for producing planar nanographenes with azulene moieties. Nano Letters. 18, 418-423 (2018).
- Ammon, M., Sander, T., Maier, S. On-Surface Synthesis of Porous Carbon Nanoribbons from Polymer Chains. Journal of the American Chemical Society. 139 (37), 12976-12984 (2017).
- Bieri, M., et al. Two-dimensional polymer formation on surfaces: insight into the roles of precursor mobility and reactivity. Journal of the American Chemical Society. 132 (46), 16669-16676 (2010).
- Bieri, M., et al. Porous graphenes: two-dimensional polymer synthesis with atomic precision. Chemical Communications. , 6919-6921 (2009).
- Mishra, S., et al. Topological frustration induces unconventional magnetism in a nanographene. Nature Nanotechnology. 15, 22-28 (2020).
- Pavliček, N. Synthesis and characterization of triangulene. Nature Nanotechnology. 542, 284-285 (2017).
- Clair, S., De Oteyza, D. G. Controlling a chemical coupling reaction on a surface: tools and strategies for on-surface synthesis. Chemical Reviews. 119 (7), 4717-4776 (2019).
- Grill, L., et al. Nano-architectures by covalent assembly of molecular building blocks. Nature Nanotechnology. 2, 687-691 (2007).
- Zuzak, R., et al. Building a 22-ring nanographene by combining in-solution and on-surface syntheses. Chemical Communications. 54, 10256-10259 (2018).
- Xu, K., et al. On-surface synthesis of a nonplanar porous nanographene. Journal of the American Chemical Society. 141 (19), 7726-7730 (2019).
- Zuzak, R., et al. Synthesis and reactivity of a trigonal porous nanographene on a gold surface. Chemical Science. 10, 10143-10148 (2019).
- Moreno, C. Bottom-up synthesis of multifunctional nanoporous graphene. Science. 360, 199-203 (2018).
- Soe, W. -H., Manzano, C., De Sarkar, A., Chandrasekhar, N., Joachim, C. Direct observation of molecular orbitals of pentacene physisorbed on Au(111) by scanning tunneling microscope. Physical Review Letters. 102, 176102(2009).
- Repp, J., Meyer, G., Stojković, S. M., Gourdon, A., Joachim, C. Molecules on insulating films: scanning-tunneling microscopy imaging of individual molecular orbitals. Physical Review Letters. 94, 026803(2005).
- Gross, L., Mohn, F., Moll, N., Liljeroth, P., Meyer, G. The chemical structure of a molecule resolved by atomic force microscopy. Science. 325 (5944), 1110-1114 (2009).
- Kichin, G., Weiss, C., Wagner, C., Tautz, F. S., Temirov, R. Single molecule and single atom sensors for atomic resolution imaging of chemically complex surfaces. Journal of the American Chemical Society. 133 (42), 16847-16851 (2011).
- Andreev, T., Barke, I., Hövel, H. Adsorbed rare-gas layers on Au(111): of the Shockley surface state studied with ultraviolet photoelectron spectroscopy and scanning tunneling spectroscopy. Physical Review B. 70, 205426(2004).
- Jung, H. S., et al. Fabrication of gate-tunable graphene devices for scanning tunneling microscopy studies with Coulomb impurities. Journal of Visualized Experiments. (101), e52711(2015).
- Kim, J. -H., et al. Direct observation of adsorption geometry for the van der Waals adsorption of a single π-conjugated hydrocarbon molecule on Au(111). Journal of Chemical Physics. 140, 074709(2014).
- Chen, W., Madhavan, V., Jamneala, T., Crommie, M. F. Scanning tunneling microscopy observation of an electronic superlattice at the surface of clean gold. Physical Review Letters. 80, 1469(1998).
- Zuzak, R., et al. Nonacene generated by on-surface dehydrogenation. ACS Nano. 11, 9321-9329 (2017).
- Zuzak, R., et al. Higher acenes by on-surface dehydrogenation: from heptacene to undecacene. Angewandte Chemie: International Edition. 57 (33), 10500-10505 (2018).
- Krüger, J., et al. Decacene: On-surface generation. Angewandte Chemie: International Edition. 56 (39), 11945-11948 (2017).
- Jelínek, P. High resolution SPM imaging of organic molecules with functionalized tips. Journal of Physics: Condensed Matter. 29, 343002(2017).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten