Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Method Article
Optimierung der Verarbeitung von Tiebangchui mit Hochlandgerstenwein auf der Grundlage des Box-Behnken-Designs in Kombination mit der Entropiemethode
In diesem Artikel
Zusammenfassung
Das vorliegende Protokoll beschreibt eine effiziente Methode zur Optimierung der Verarbeitungstechnologie von Tiebangchui, die mit Hochlandgerstenwein verarbeitet wird, basierend auf einer Box-Behnken-Design-Response-Oberfläche in Kombination mit der Entropiemethode.
Zusammenfassung
Die Verarbeitung toxischer Ethnoarzneimittel ist für deren sichere klinische Anwendung von großer Bedeutung. Daher sollten die Grenzen der traditionellen Verarbeitung angegangen und die Verarbeitungsmethode von Ethnoarzneimitteln mit modernen Forschungsmethoden standardisiert werden. In dieser Studie wurde die Verarbeitungstechnologie eines häufig verwendeten tibetischen Medikaments Tiebangchui (TBC), der getrockneten Wurzel von Aconitum pendulum Busch, die mit Hochlandgerstenwein verarbeitet wird, optimiert. Als Bewertungsindikatoren wurden Diester-Diterpenoid-Alkaloid (DDA) (Aconitin, 3-Desoxyaconitin, 3-Acetylaconitin) und Monoester-Diterpenoid-Alkaloid (MDA) (Benzoylaconine) verwendet, und der Gewichtskoeffizient jedes Bewertungsindex wurde durch die Entropiemethode bestimmt.
Der Ein-Faktor-Test und das Box-Behnken-Design wurden verwendet, um den Einfluss des Verhältnisses zwischen Hochlandgerstenwein und TBC, der Scheibendicke von TBC und der Verarbeitungszeit zu untersuchen. Ein umfassendes Scoring wurde anhand der objektiven Gewichtung jedes Index durchgeführt, die durch die Entropiemethode bestimmt wurde. Die optimalen Verarbeitungsbedingungen von TBC mit Hochlandgerstenwein waren wie folgt: Die Menge an Hochlandgerstenwein ist fünfmal so hoch wie die von TBC, eine Einweichzeit von 24 h und eine TBC-Dicke von 1,5 cm. Die Ergebnisse zeigten, dass die relative Standardabweichung zwischen dem Verifizierungstest und dem prognostizierten Wert weniger als 2,55 % betrug und die optimierte Verarbeitungstechnologie von TBC, die mit Hochlandgerstenwein verarbeitet wird, einfach, machbar und stabil ist und daher eine Referenz für die industrielle Produktion darstellen kann.
Einleitung
Tiebangchui (TBC), die getrocknete Wurzel von Aconitum pendulum Busch, ist eine bekannte tibetische Medizin und wurde erstmals in dem klassischen tibetischen medizinischen Buch "Vier medizinische Tantra"1,2 aufgezeichnet. Gemäß den "Arzneimittelstandards des Gesundheitsministeriums der Volksrepublik China (Tibetische Medizin)" ist TBC wirksam bei der Vertreibung von Kälte, der Linderung von Schmerzen, der Vertreibung von Wind und der Beruhigung von Schocks und wird häufig zur Behandlung von rheumatoider Arthritis in Kliniken eingesetzt 3,4,5.
TBC enthält hauptsächlich Alkaloide, darunter hochtoxische Diester-Diterpenoid-Alkaloide (DDAs) und die mäßig toxischen Monoester-Diterpenoid-Alkaloide (MDAs)6,7,8. Bei diesen chemischen Bestandteilen handelt es sich um Wirkstoffe mit medizinischer Wirkung, die jedoch toxisch sind. Einer der bekanntesten aktiven und giftigen Inhaltsstoffe, Aconitin, verursacht Vergiftungen, wenn er 1 mg9 überschreitet. Daher kann eine unsachgemäße oder übermäßige Anwendung von TBC zu Vergiftungen und sogar zum Tod führen, und die Toxizitätsabschwächung und der Wirksamkeitsvorbehalt von TBC sind entscheidend für seine sichere klinische Anwendung10,11.
Die Verarbeitung ist eine effektive Methode zur Entgiftung von TBC. Laut alten tibetischen Medizinbüchern ist die Verarbeitung mit Hochlandgerstenwein ein effizienter Weg, um die Toxizität zu verringern und die Wirksamkeit von TBC zu erhalten. TBC wird in Hochlandgerstenwein eingeweicht, eine Nacht gelagert, getrocknet und den Medikamenten12 zugesetzt. Über die spezifische Verarbeitungstechnologie und mögliche Einflussfaktoren wird jedoch selten berichtet, und der traditionelle Verarbeitungsprozess beruht oft auf Erfahrung und es fehlen standardisierte Methoden. Daher werden moderne wissenschaftliche und technologische Methoden zur Optimierung und Standardisierung des Verarbeitungsprozesses benötigt.
Die Box-Behnken-Entwurfsmethode wird verwendet, um Wechselwirkungen zwischen verschiedenen Faktoren und deren Einfluss auf das umfassende Scoring durch quadratische Polynomanpassung zu untersuchen. Dieses Design ermöglicht die intuitive Beobachtung optimaler Bedingungen und ist im Bereich der Pharmazieweit verbreitet 13. So hat beispielsweise die auf der Entropiemethode basierende Box-Behnken-Auslegungsmethode die Verarbeitungstechnologie des Pfannenrührens mit Essig von Curcuma Longa Radix14 erfolgreich optimiert. In dieser Studie wurde das experimentelle Design der Box-Behnken-Antwortfläche in Kombination mit der Entropiemethode verwendet, um die Verarbeitungstechnologie von TBC zu optimieren, die mit Hochlandgerstenwein verarbeitet wurde. Die optimierte Verarbeitungstechnologie soll die Qualitätskontrolle und den sicheren klinischen Einsatz gewährleisten.
Protokoll
In dieser Studie wurde die Verarbeitungstechnologie von TBC, die mit Hochlandgerstenwein verarbeitet wurde, mit einem Box-Behnken-Design in Kombination mit der Entropiemethode optimiert. DDA- und MDA-Gehalt wurden als Bewertungsindikatoren verwendet, und der Gewichtskoeffizient jedes Bewertungsindex wurde durch die Entropiemethode bestimmt.
1. Experimentelle Vorbereitung
- Hochlandgerstenwein zubereiten15.
- Man nehme 500,00 g schwarzen Hochlandgerstenreis und füge die fünffache Menge Wasser hinzu. Den Reis kochen, bis das restliche Wasser aufgesogen ist (~2 h). Gießen Sie es aus, warten Sie, bis die Temperatur auf 37 °C fällt, fügen Sie 4 g Jiuqu hinzu (siehe Materialtabelle), mischen Sie es gut, verschließen Sie die Dose, wickeln Sie den Behälter mit Watte ein und lassen Sie es 7 Tage lang schmoren.
- Fügen Sie am 7. Tag 300 ml Wasser hinzu und verschließen Sie erneut. Beginnen Sie am 8. Tag mit der Entfernung des Weins und ersetzen Sie ihn anschließend durch 300 ml Wasser. Verschließen und 1 Tag lang gären, den Wein nehmen und erneut 300 ml Wasser hinzufügen. Wiederholen Sie diesen Vorgang dreimal und kombinieren Sie die Spirituosen.
- Zum Kochen bringen, dann die Hitze auf ein Köcheln reduzieren und weiterkochen, bis das restliche Wasser absorbiert ist.
- Um verarbeitete Produkte zuzubereiten, wiegen Sie den TBC in einem Behälter genau ab, fügen Sie Hochlandgerstenwein hinzu und lassen Sie ihn 1 Tag einweichen. Anschließend in einem elektrischen Trockenofen mit konstanter Temperatur trocknen.
Anmerkungen: Die Trocknungstemperatur sollte unter 40 °C liegen, um Veränderungen in der Alkaloidzusammensetzung zu vermeiden. - Bereiten Sie die Testprobenlösung vor.
- TBC-verarbeitetes Produktpulver (2 g) in einem Erlenmeyerkolben genau einwiegen, 40%ige Ammoniaklösung hinzufügen und eine ultraschallgestützte Extraktion mit Isopropanol-Ethylacetat (1:1) gemischten Lösungsmitteln (50 ml) (Leistung: 200 W; Frequenz: 40 kHz; Temperatur: 40 °C) für 30 min durchführen.
Anmerkungen: Zur Herstellung einer 40%igen Ammoniaklösung werden 40 ml Ammoniak in einen 100-ml-Messkolben überführt und dann mit reinem Wasser verdünnt. - Stellen Sie die extrahierte Lösung durch Zugabe eines Isopropanol-Ethylacetat-Gemischs (1:1 v/v) auf das ursprüngliche Gewicht ein.
- Die extrahierte Lösung (25 ml) wird genau in einen Rundkolben überführt, um das Lösungsmittel unter reduziertem Druck bis zum Trocknen zurückzugewinnen.
- Schließlich wird eine 0,05%ige Salzsäure-Methanol-Lösung zur Lösung des Rückstandes aus Schritt 1.3.3 in einen 5-ml-Messkolben überführt und mit 0,05%iger Methanolhydrochloridlösung verdünnt. Filtrieren Sie die Lösung durch einen mikroporösen 0,22-μm-Membranfilter, bevor Sie sie in die Hochleistungsflüssigkeitschromatographiesysteme (HPLC) einspritzen.
Anmerkungen: 0,05%ige Methanolhydrochloridsäure herstellen, indem 0,05 ml Salzsäure in einen 100-ml-Messkolben gegeben und dann mit Methanol verdünnt werden.
- TBC-verarbeitetes Produktpulver (2 g) in einem Erlenmeyerkolben genau einwiegen, 40%ige Ammoniaklösung hinzufügen und eine ultraschallgestützte Extraktion mit Isopropanol-Ethylacetat (1:1) gemischten Lösungsmitteln (50 ml) (Leistung: 200 W; Frequenz: 40 kHz; Temperatur: 40 °C) für 30 min durchführen.
- Bereiten Sie eine Standardlösung vor, indem Sie 5,18 mg Benzoylaconin, 13,13 mg Aconitin, 10,05 mg 3-Desoxyaconitin und 10,09 mg 3-Acetylaconitin genau wiegen und dann die Feststoffe einzeln in einen 5-ml-Messkolben geben. Mit 0,05%iger Methanolhydrochloridlösung verdünnen.
2. Chromatographischer Zustand
- Richten Sie die chromatographischen Bedingungen wie in Tabelle 1 für HPLC gezeigt ein. Details zu den verwendeten Instrumenten finden Sie in der Materialtabelle.
3. Prüfung der Anpassungsfähigkeit des Systems
- Bereich der Linearität
HINWEIS: Zuerst haben wir die HPLC verwendet, um die Peakbereiche von Benzoylaconiten, Aconitin, 3-Desoxyaconitin und 3-Acetylaconitin in der Probe zu bestimmen, und dann nach dem Zufallsprinzip die Peakfläche einer bekannten Konzentration der Standardlösung bestimmt. Als nächstes verglichen wir die Differenz zwischen zwei Peakbereichen (Probenlösung und Standardlösung), um die Konzentration von Benzoylaconitin, Aconitin, 3-Desoxyaconitin und 3-Acetylaconitin in verschiedenen Proben abzuschätzen, und passten dann die Standardlösung in einen linearen Bereich an, um die Konzentration der Probe in der Kurve einzubeziehen. Die Konzentrationen der Standardkurve sind in Tabelle 2 dargestellt.- Benzoylaconitin-Referenzlösungen mit 1,036 mg/ml, 0,518 mg/ml, 0,2072 mg/ml, 0,1036 mg/ml und 0,0518 mg/ml herstellen.
- Aconitin-Referenzlösungen mit 1,313 mg/ml, 0,5252 mg/ml, 0,2626 mg/ml, 0,1313 mg/ml und 0,05252 mg/ml herstellen.
- Bereiten Sie 3-Desoxyaconitin-Referenzlösungen mit 1,005 mg/ml, 0,5025 mg/ml, 0,201 mg/ml, 0,1005 mg/ml und 0,402 mg/ml vor.
- 3-Acetylaconitin-Referenzlösungen mit 0,2018 mg/ml, 0,1009 mg/ml, 0,04036 mg/ml, 0,02018 mg/ml und 0,01009 mg/ml herstellen.
- Untersuchen Sie die Linearität jeder Verbindung, indem Sie die Peakfläche im Vergleich zur Injektionskonzentration darstellen.
- Um den Präzisionstest durchzuführen, injizieren Sie sechsmal täglich 10 μl jeder Referenzlösung in das HPLC-System und verwenden Sie die gleichen HPLC-Bedingungen, die in Schritt 2.1 beschrieben sind, um die Proben auszuführen Zeichnen Sie den Peakbereich jeder Komponente auf.
- Führen Sie einen Intraday-Stabilitätstest durch, indem Sie 10 μl der vorbereiteten Probenlösung über Schritt 1.3 injizieren, und bestimmen Sie die Peakbereiche nach 0 h, 2 h, 4 h, 8 h, 14 h, 12 h und 24 h16.
- Führen Sie einen Reproduzierbarkeitstest durch, indem Sie sechs Proben derselben TBC-Charge entnehmen, um die Testprobenlösung gemäß Schritt 1.3 herzustellen. Injizieren Sie 10 μl jeder Probe in das HPLC-System und führen Sie die Proben wie in Schritt 2.1 beschrieben aus.
- Führen Sie den Wiederherstellungstest durch, um die Genauigkeit der Methode zu bewerten. Fügen Sie 100 % der Standardlösung jeder Indexkomponente (Benzoylaconitein, Aconitin, 3-Desoxyaconitin und 3-Acetylaconitin) in die Testlösung hinzu, um die Wiederfindungsrate zu berechnen. Da beispielsweise der Gehalt an Benzoylaconitin in der TBC-Probe 0,1524 mg/ml beträgt, werden 0,1524 mg Benzoylaconitin-Standards genau abgewogen und der TBC-Probe hinzugefügt, dann die Testprobenlösung gemäß Schritt 1.3 hergestellt. Führen Sie diese Proben mit den gleichen HPLC-Bedingungen aus, die in Schritt 2.1 beschrieben wurden. Berechnen Sie die Rückgewinnungsrate mit Gleichung (1):
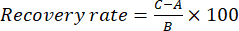 (1)
(1)
Dabei ist A die Menge der Komponente (Benzoylaconitein, Aconitin, 3-Desoxyaconitin oder 3-Acetylaconitin), die in der Probenlösung gemessen werden soll, B ist die Menge des zugesetzten Standards (Benzoylaconiten, Aconitin, 3-Desoxyaconitin oder 3-Acetylaconitin) und C ist der Messwert der Lösung, die die Standardlösung und die Probenlösung enthält (siehe Tabelle 3). In Schritt 2.1 finden Sie die chromatographischen Bedingungen, um die oben genannten Schritte auszuführen. Die Wiederfindungsrate spiegelt den Grad des Verlusts der Zielkomponente (Benzoylaconitin, Aconitin, 3-Desoxyaconitin oder 3-Acetylaconitin) während der Probenanalyse wider. Je höher die Wiederherstellungsrate, desto geringer der Verlust der Zielkomponente.
4. Ein-Faktor-Test von TBC, verarbeitet mit Hochlandgerstenwein
HINWEIS: Das Verhältnis zwischen Hochlandgerstenwein und TBC, die Scheibendicke von TBC und die Einweichzeit beeinflussen die Auflösung von toxischeren Komponenten (Aconitin, 3-Desoxyaconitin und 3-Acetylaconitin) in TBC während der TBC, die mit Hochlandgerstenwein17 verarbeitet wird. Der Einfaktortest und das Box-Behnken-Design wurden verwendet, um den Einfluss des Verhältnisses von Hochlandgerstenwein zu TBC, der Scheibendicke von TBC und der Einweichzeit zu untersuchen.
- Führen Sie den Zusatztest für Hochlandgerstenwein (A) durch, indem Sie fünf Gruppen von Tests mit jeweils 30 g TBC einrichten, wobei die Menge an Hochlandgerstenwein das Zwei-, Drei-, Vier-, Fünf- und Sechsfache der Menge an TBC im Rezept beträgt. Die Einweichzeit beträgt 12 h und die Scheiben sind 1,0 cm dick18.
HINWEIS: Jede Gruppe desselben Zustandstests sollte in drei parallelen Gruppen verarbeitet werden. - Führen Sie den Einweichzeittest (B) durch, indem Sie fünf Testgruppen mit jeweils 30 g TBC einrichten. Die Einweichzeiten betragen 12 h, 24 h, 36 h und 48 h. Die Menge an Hochlandgerstenwein ist fünfmal so hoch wie die von TBC, und die Scheiben sind1,0 cm dick 19.
HINWEIS: Jede Gruppe desselben Bedingungsexperiments sollte in drei parallelen Gruppen verarbeitet werden. - Führen Sie den Schneiddickentest (C) durch, indem Sie fünf Testgruppen mit jeweils 30 g TBC einrichten. Die Scheiben sind 0,5, 1,0, 1,5, 2,0 und 2,5 cm dick, die Einweichzeit beträgt 24 h und die Menge an Hochlandgerstenwein ist fünfmal so hoch wie die von TBC20.
HINWEIS: Jede Gruppe desselben Bedingungsexperiments sollte in drei parallelen Gruppen verarbeitet werden. - Wiegen Sie die verarbeiteten Produkte für jede Testgruppe genau, um die Testprobenlösung gemäß Schritt 1.3 herzustellen. Bestimmen Sie die Peakfläche jeder Probe mittels HPLC und verwenden Sie die Standardkurve, um die Mengen an MDAs und DDAs abzuschätzen. In der Standardkurve ist y die Peakfläche und x der Inhalt. Der Gehalt an MDAs ist Benzoylaconitin, und der Gehalt an DDAs ist die Summe aus Aconitin, 3-Desoxyaconitin und 3-Acetylaconiten.
- Verwenden Sie den Gesamtgehalt von DDAs und den Inhalt von MDAs als Bewertungsindikatoren und bestimmen Sie den Gewichtskoeffizienten jedes Bewertungsindex und das umfassende Scoring mit Hilfe der Entropiemethode (Abschnitt 5).
ACHTUNG: TBC ist giftig und daher sollten während der Verarbeitung Schutzmaßnahmen ergriffen werden.
5. Entropiemethode zur Berechnung des umfassenden Scorings
HINWEIS: Wir verwenden die experimentellen Daten des Messerdickentests im Einfaktortest als Beispiel, um den Berechnungsprozess im Detail zu veranschaulichen. Wir verwenden die Peakfläche der Komponenten in jeder Probe in der Ergänzungstabelle S1 und die Standardkurve in Tabelle 2, um den Gehalt an MDAs und DDAs zu berechnen (siehe Ergänzungstabelle S2). In der linearen Gleichung ist y die Peakfläche und x der Inhalt. In dieser Studie wurde das mäßig toxische MDA (Benzoylaconiten) als positiver Indikator und der Gesamtgehalt an DDAs (Aconitin, 3-Desoxyaconitin und 3-Acetylaconitin) mit hoher Toxizität als negativer Indikator verwendet. Der Gehalt an MDAs ist Benzoylaconitin, und der Gehalt an DDAs ist die Summe aus Aconitin, 3-Desoxyaconitin und 3-Acetylaconiten. Jede Stichprobe hat zwei Auswertungsindikatoren: i = 1,2,...,n und j = 1,2,... M21.
- Verwenden Sie Gleichung (2), um den Inhalt von MDAs22 zu standardisieren.
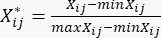 (2)
(2)
So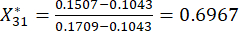
HINWEIS: Xij ist der Wert des j-ten Indikators der i-ten Stichprobe. Xij* ist der standardisierte Wert von Xij. Beispielsweise ist i = 3 und j = 1, X31 stellt den Wert des ersten Indikators der dritten Stichprobe dar und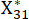 ist der standardisierte Wert des ersten Indikators in der dritten Stichprobe. sind in der ergänzenden Tabelle S3 dargestellt.
ist der standardisierte Wert des ersten Indikators in der dritten Stichprobe. sind in der ergänzenden Tabelle S3 dargestellt. 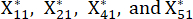
- Verwenden Sie Gleichung (3), um den Gesamtinhalt der DDAs23 zu standardisieren.
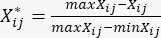 (3)
(3)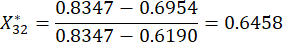
HINWEIS: Hier stellt i = 3, j = 2 den zweiten Indikator der dritten Stichprobe dar.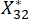 ist der standardisierte Wert des zweiten Indikators in der dritten Stichprobe.
ist der standardisierte Wert des zweiten Indikators in der dritten Stichprobe. 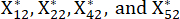 sind in der Ergänzungstabelle S3 aufgeführt.
sind in der Ergänzungstabelle S3 aufgeführt. - Verwenden Sie die Gleichungen (4) und (5), um den Entropiewert (Hj) jedes Indikators23 zu definieren.
- Berechnen Sie die Wahrscheinlichkeit des j-ten Versuchs unter dem i-ten Bewertungsindikator Pij unter Verwendung von Gleichung (4).
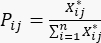 (4)
(4)
Für Nummer 3,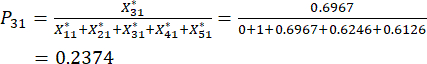
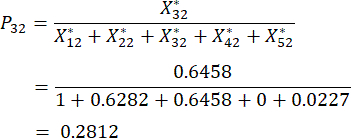
HINWEIS: Die Wahrscheinlichkeitswerte für den ersten Indikator und den zweiten Indikator der dritten Stichprobe betragen 0,2374 bzw. 0,2812.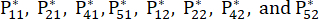 sind in der Ergänzungstabelle S3 aufgeführt.
sind in der Ergänzungstabelle S3 aufgeführt. - Berechnen Sie die Informationsentropie Hj.
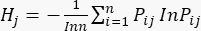 (5)
(5)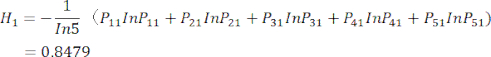
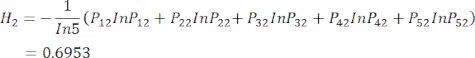
HINWEIS: H 1 ist die Entropie des ersten Indikators (MDAs) und H2 ist die Entropie des zweiten Indikators (DDAs) im Schnittdickentest.
- Berechnen Sie die Wahrscheinlichkeit des j-ten Versuchs unter dem i-ten Bewertungsindikator Pij unter Verwendung von Gleichung (4).
- Verwenden Sie Gleichung (6), um die Indikatorgewichte (Wj)23 zu berechnen.
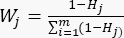 (6)
(6)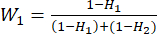 = 33,3 %
= 33,3 % = 66,7 %
= 66,7 %
HINWEIS: Wjist der Gewichtskoeffizient jedes Indikators. Beim Schneiddickentest beträgt der Gewichtskoeffizient des positiven Indikators (MDAs) und des negativen Indikators (DDAs) 33,3 % bzw. 66,7 %. - Verwenden Sie Gleichung (7), um die umfassende Bewertung der Indikatoren23 zu berechnen.
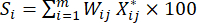 (7)
(7)
Für Nummer 3,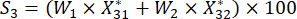
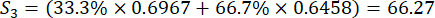
HINWEIS: Si ist die umfassende Bewertung jeder Probe. Wir müssen die höchste Punktzahl als zentralen Punkt im Box-Behnken-Design erhalten. S 1, S 2, S 3, S 4 und S5 sind in der Ergänzungstabelle S3 dargestellt.
6. Box-Behnken-Design
- Verwenden Sie beim Ein-Faktor-Test die Bedingung mit der höchsten umfassenden Bewertung (siehe Tabelle 4, Tabelle 5, Tabelle 6 und Abbildung 2) als Mittelpunkt der Antwortfläche. Verwenden Sie die Menge an Hochlandgerstenwein (A), die Einweichzeit (B) und die Scheibendicke von TBC (C) als Einflussfaktoren und das umfassende Scoring als Antwortwert24.
HINWEIS: Basierend auf den Einzelfaktordaten in Tabelle 4, Tabelle 5 und Tabelle 6 wird die höchste umfassende Bewertung durch die Gleichungen (2), (3), (4), (5), (6) und (7) in Abschnitt 5 berechnet, und die beste Punktzahl wird erhalten. Die Menge an Hochlandgerstenwein war fünfmal so hoch wie die von TBC, die Einweichzeit betrug 36 h und die Schnittdicke betrug 1,0 cm.
7. Arbeitsschritte der Box-Behnken-Designsoftware
- Öffnen Sie die Software (siehe Materialtabelle) und wählen Sie Neues Design | Box-Behnken Design (siehe Schritt 5.1; Ergänzungsdatei 1).
- Geben Sie die Anzahl der Einflussfaktoren ein und geben Sie die Niveauinformationen ein (dreistufig-dreifaktorig; siehe Tabelle 7). Das Box-Behnken-Design setzt sich aus 17 Experimenten in dieser Studie zusammen. Klicken Sie abschließend auf Weiter (siehe Schritt 5.2; Ergänzungsdatei 1).
- Legen Sie die umfassende Bewertung (Y) durch die Gleichungen (2), (3), (4), (5), (6) und (7) in Abschnitt 5 als Antwort fest. Geben Sie die Anzahl der Werte der Antwortvariablen ein (Abbildung zeigt nur einen Wert der Antwortvariablen) und klicken Sie auf Fertig stellen (siehe Schritt 5.3; Ergänzungsdatei 1).
- Verarbeiten Sie die TBC mit Hochlandgerstenwein gemäß den Entwurfsergebnissen und führen Sie das Experiment auf der Grundlage der 17 Szenarien durch, die für die Antwortfläche entworfen wurden.
- Bereiten Sie die Probenlösungen vor, indem Sie Schritt 1.3 befolgen, und berechnen Sie den Gesamtgehalt der MDAs und DDAs durch das HPLC-System.
- Berechnen Sie die umfassende Bewertung für jede Gruppe anhand der Gleichungen (2), (3), (4), (5), (6) und (7) in Schritt 5 und geben Sie die Ergebnisse ein (siehe Schritt 5.4; Ergänzungsdatei 1).
- Klicken Sie auf Analysieren , um die Datums- und Modellinformationen zu analysieren (siehe Schritt 5.4.1; Ergänzungsdatei 1).
- Führen Sie eine statistische Validierung von Polynomgleichungen und eine Analyse der Antwortfläche durch, die in 3D-Modelldiagrammen dargestellt werden, die von der Software erhalten wurden.
- Klicken Sie im oberen Menü auf ANOVA und sehen Sie sich die Ergebnistabelle an.
- Klicken Sie auf Optimierung , um die prognostizierten optimalen Prozessbedingungen anzuzeigen (siehe Schritt 5.4.2; Ergänzungsdatei 1).
8. Validierungstest
- Anhand der Ergebnisse, die aus dem Box-Behnken-Response-Surface-Design vorhergesagt wurden, ist in Schritt 7.3 die optimale Verarbeitungsbedingung von TBC zu identifizieren. Hier ist es wie folgt: TBC wird 24 Stunden lang in der fünffachen Menge Hochlandgerstenwein eingeweicht, und die Dicke des TBC beträgt 1,5 cm. Nehmen Sie das optimale Maß an Einflussfaktoren als Verarbeitungsbedingungen und bauen Sie drei parallele Versuchsreihen auf, um die Stabilität der Verarbeitungstechnologie zu überprüfen.
Ergebnisse
In dieser Studie zeigten die Präzision, Stabilität, Wiederholbarkeit und Probenrückgewinnung von TBC, dass die Methode durchführbar ist. Die vier Indexkomponenten in TBC wiesen eine gute lineare Beziehung innerhalb eines bestimmten Konzentrationsbereichs auf. Typische Chromatogramme sind in Abbildung 1 dargestellt. Die Präzisionstestergebnisse (Tabelle 8) zeigten, dass die relative Standardabweichung (RSD) der Peakbereiche 2,56 %, 1,49 % bzw. 2,03 % für Benzoylaconine,...
Diskussion
Da es sich um ein häufig verwendetes tibetisches Arzneimittel mit toxischer Wirkung handelt, ist die toxizitätsmindernde Wirkung der Verarbeitung für die klinische Anwendung von TBC äußerst wichtig25. In dieser Studie wurde die Verarbeitungstechnologie von TBC, die mit Hochlandgerstenwein verarbeitet wurde, optimiert. Durch die Überprüfung der Hauptwirkstoffe und die Beziehung zu den pharmakologischen Wirkungen von TBC haben wir herausgefunden, dass TBC-Alkaloide entzündungshemmende und sc...
Offenlegungen
Die Autoren haben keine Interessenkonflikte offenzulegen.
Danksagungen
Diese Arbeit wurde finanziell unterstützt von der National Natural Science Foundation of China (Nr. 82130113), der China Postdoctoral Science Foundation (Nr. 2021MD703800), der Science Foundation for Youths of Science & Technology Department der Provinz Sichuan (Nr. 2022NSFSC1449) und dem Forschungsförderungsprogramm "Xinglin Scholars" der Chengdu University of Traditional Chinese Medicine (Nr. 2022NSFSC1449) BSH2021009).
Materialien
| Name | Company | Catalog Number | Comments |
| Aconitine | Chengdu Push Biotechnology Co.,Ltd | PS000905 | |
| 3-Acetylaconitine | Chengdu Push Biotechnology Co.,Ltd | PS010552 | |
| 3-Deoxyaconitine | Chengdu Push Biotechnology Co.,Ltd | PS011258 | |
| Benzoylaconine | Chengdu Push Biotechnology Co.,Ltd | PS010300 | |
| Circulating water vacuum pump | Gongyi City Yuhua Instrument Co., Ltd | SHZ-DIII | |
| Design-Expert | State-East Corporation | 8.0.6 | |
| Electric constant temperature drying oven | Shanghai Yuejin Medical Equipment Co., Ltd | 101-3-BS | |
| Electronic analytical balance | Shanghai Liangping Instruments Co., Ltd. | FA1004 | |
| High performance liquid chromatography | Shimadzu Enterprise Management (China) Co., Ltd | shimadzu 2030 | |
| Highland barley rice | Kangding City, Ganzi Tibetan Autonomous Prefecture, Sichuan Province | 20221015 | |
| Millipore filter | Tianjin Jinteng Experimental Equipment Co., Ltd | φ13 0.22 Nylon66 | |
| Rotary evaporator | Shanghai Yarong Biochemical Instrument Factory | RE-2000A | |
| Starter of liquor-making | Angel Yeast CO., Ltd | BJ22-104 | |
| Ultra pure water systemic | Merck Millipore Ltd. | Milli-Q | |
| Ultrasonic cleansing machine | Ningbo Xinyi Ultrasonic Equipment Co., Ltd | SB-8200 DTS |
Referenzen
- Zhang, J., et al. Study of quality standards for Aconitum pendulum Busch. Chinese Traditional Patent Medicine. 40 (9), 2100-2103 (2018).
- Liu, X. F., et al. Study on toxicity reduction and effect preservation of the compatibility of Tibetan medicine Aconitum pendulum Busch and Terminalia chebula Retz. Pharmacy and Clinics of Chinese Materia Medica. 13 (3), 69-72 (2022).
- Luo, D. S. . Chinese Tibetan herbs. 63, (2007).
- Li, C. Y., et al. Aconitum pendulum Busch and A. flavum Hand-Mazz: A narrative review on traditional uses, phytochemistry, bioactivities and processing methods. Journal of Ethnopharmacology. 292, 115216 (2022).
- Yu, L. Q., et al. Traditional Tibetan medicine: therapeutic potential in rheumatoid arthritis. Frontiers in Pharmacology. 13, 938915 (2022).
- Zhang, Y., Fu, X. Y. UPLC Simultaneous determination of six esteric alkaloids components in Aconitum pendulum Busch. Asia-pacific Traditional Medicine. 16 (5), 62-65 (2020).
- Wang, Y. J., et al. Determination of alkaloid content in different medicinal parts of the folk medicine. Aconitum pendulum Busch. Chinese Traditional Patent Medicine. 32 (8), 1390-1393 (2010).
- Shao, C. L., Fu, J. L., Fu, S. X., Ma, H. W., Sun, X. D. Toxicity research and processing methods of Aconitum pendulum Busch. Asia-pacific Traditional Medicine. 10 (2), 32-34 (2014).
- Chan, T. Y. K. Aconite poisoning. Clinical Toxicology. 47 (4), 279-285 (2009).
- Li, S. L., et al. An insight into current advances on pharmacology, pharmacokinetics, toxicity and detoxification of aconitine. Biomedicine & Pharmacotherapy. 151, 113115 (2022).
- Zhao, M. Y. Study on identification and processing attenuation of Tibetan drug Bangna. Southwest Jiaotong University. , (2018).
- Tibet Autonomous Region Food and Drug Administration. . Tibetan herbal medicine concoction specification. , 135 (2008).
- Abd-El-Aziz, N. M., Hifnawy, M. S., El-Ashmawy, A. A., Lotfy, R. A., Younis, I. Y. Application of Box-Behnken design for optimization of phenolics extraction from Leontodon hispidulus in relation to its antioxidant, anti-inflammatory and cytotoxic activities. Scientific Reports. 12 (1), 8829 (2022).
- Quan, L., et al. Optimization of processing technology of stir-frying with vinegar of Curcuma Longa Radix by orthogonal design and Box-Behnken design-response surface based on entropy method. Chinese Traditional and Herbal Drugs. 49 (8), 1823-1828 (2018).
- Jia, F. C., et al. Research on the brewing technology of Tibetan traditional barley liquor based on response surface method. Food and Fermentation Industries. 45 (22), 171-178 (2019).
- Zhao, X. H., et al. Determination of osthol in different traditional Chinese medicines by HPLC. Chinese Journal of Pharmaceutics. 19 (5), 154-158 (2021).
- Feng, Z. G., et al. Processing methods and the underlying detoxification mechanisms for toxic medicinal materials used by ethnic minorities in China: A review. Journal of Ethnopharmacology. 305, 116126 (2023).
- Wang, D. M., Lu, Z. J., Wang, Y. H., Zhang, C. S. Applying grading methods of synthesizing multiple guidelines to optimizing alcohol-steam processing technology from Ploygonatum odordatum. Journal of Zhejiang A & F University. 30 (1), 100-106 (2013).
- He, N. L., Bao, M. L., Ba, G. N. Study on the best processing technology of Terminalia Decoction soaking iron. Journal of Medicine & Pharmacy of Chinese Minorities. 20 (9), 36-38 (2014).
- Liu, C., et al. Optimization of processing technology for Saposhnikoviae Radix by Box-Behnken design-response surface methodology. Chinese Journal of Experimental Traditional Medical Formulae. 20 (5), 18-21 (2014).
- Ferreira, S. L. C., et al. Box-Behnken design: an alternative for the optimization of analytical methods. Analytica Chimica Acta. 597 (2), 179-186 (2007).
- Dong, R., Lu, Y., Wang, P. The process optimization of vinegar roasting of Bupleurum chinense by entropy weight method combined with Box-Behnken response surface method and its protective effect on mice liver injury. Science and Technology of Food Industry. 42 (23), 209-217 (2021).
- Li, W. J., et al. Analysis on the times of Polygonati Rhizoma steamed by multiple times based on entropy weight and gray relative analysis method. China Journal of Traditional Chinese Medicine and Pharmacy. 36 (11), 6764-6769 (2021).
- Huang, B. J., Liu, X. T., Mao, Y. M., Qi, B., Liu, L. Response surface methodology combined with analytic hierarchy process to optimize the processing technology of Custutae semen with wine. Lishizhen Medicine and Materia Medica Research. 33 (8), 1890-1894 (2022).
- Wang, J., Meng, X. H., Chai, T., Yang, J. L., Shi, Y. P. Diterpenoid alkaloids and one lignan from the roots of Aconitum pendulum Busch. Natural Products and Bioprospecting. 9 (6), 419-423 (2019).
- Xie, H. H., et al. Metabolomics study of aconitine and benzoylaconine induced reproductive toxicity in Be Wo cell. Chinese Journal of Analytical Chemistry. 43 (12), 1808-1813 (2015).
- Han, Y. F., et al. Optimization of extraction process for Yangyin Runmu granules by Box-Behnken design based on entropy weight method-analytic hierarchy process method. Chinese Journal of Modern Applied Pharmacy. 39 (7), 896-903 (2022).
- Chen, F. G., et al. Optimization of the baked drying technology of Clinamomi Ramulus based on CRITIC combined with Box-Behnken response surface method. Journal of Chinese Medicinal Materials. 2022 (8), 1838-1842 (2022).
- Pan, Y. L. Optimization of stir-baking process of Coix lacryma-Jobi Var.Mayuen Kernel by Box-Behnken response surface methodology. Shandong Chemical Industry. 51 (14), 73-75 (2022).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten