Operationstechnik des 3-dimensional gedruckten personalisierten Hüftimplantats zur Behandlung der Hüftdysplasie bei Hunden
In diesem Artikel
Zusammenfassung
Diese Arbeit beschreibt eine neuartige Operationstechnik zur extrakapsulären Implantation eines personalisierten, 3-dimensional gedruckten, gelenkerhaltenden Implantats. Diese neuartige Behandlung zielt darauf ab, die Hüftstabilität bei jungen erwachsenen Hunden wiederherzustellen, die an Hüftdysplasie mit Laxität leiden, indem sie die anatomische Form des Hüftpfannenrandes des Hüftgelenks auf einzigartige Weise reproduziert.
Zusammenfassung
Hüftdysplasie führt bei Hunden zu schweren Behinderungen. Die Behandlungsmöglichkeiten beschränken sich auf palliative Behandlungen (z. B. Schmerzlinderung, körperliche Bewegung, Änderungen des Lebensstils und Gewichtskontrolle) oder invasive Operationen wie Beckenosteotomien und Hüfttotalendoprothetik. Daher besteht ein großer ungedeckter Bedarf an einer effektiven und hundefreundlichen Lösung, die die Lebensqualität des besten Freundes des Menschen verbessert. Wir schließen diese Behandlungslücke, indem wir ein minimal traumatisches und extraartikuläres, hundespezifisches, 3-dimensional gedrucktes Hüftimplantat (3DHIP) anbieten, das die Stabilität des Hüftgelenks wiederherstellt. Die chirurgische Behandlung mit einem 3DHIP-Implantat ist weniger invasiv als Osteotomien und kann beidseitig in einer chirurgischen Sitzung durchgeführt werden. Das 3DHIP-Implantat verlängert den dorsalen Hüftpfannenrand des dysplastischen Hüftgelenks, wodurch die Abdeckung des Hüftkopfes erhöht und die Subluxation des Gelenks mit schneller Genesung gehemmt wird. Ein ausreichender Zugang zum dorsalen Hüftpfannenrand und ventralen Rand des Beckenkörpers sowie die optimale Anpassung und Fixierung des Implantats sind wichtige Schritte für eine erfolgreiche 3DHIP-Implantation und implizieren die Notwendigkeit eines spezifischen Ansatzes. Der vorliegende Artikel zielt darauf ab, diese innovative Operationstechnik mit Tipps und Tricks als chirurgisches Handbuch für die Implantation des 3DHIP-Implantats bei Hunden mit Hüftdysplasie vorzustellen.
Einleitung
Hüftdysplasie (HD) bei Hunden manifestiert sich aufgrund einer schlechten Passform zwischen der Hüftpfanne (Acetabulum) und dem Hüftkopf, was zu einer Subluxation des Hüftgelenks führt. Sie betrifft vor allem junge Hunde mittlerer bis großer Rassen, was zu einer Verschlechterung des Gelenkknorpels und schließlich zu schwerer Osteoarthritis (OA) führt, die zu chronischen Schmerzen und geringer Lebensqualität führt 1,2. Die Gesamtprävalenz der Hüftdysplasie bei Hunden beträgt 15,56 %, was je nach Rasse und Klassifikationssystem stark variiert 3,4.
Abgesehen von Änderungen des Lebensstils werden hüftdysplastische Hundepatienten mit entzündungshemmenden und schmerzstillenden Medikamenten behandelt, um die Schmerzen zu kontrollieren und die Beweglichkeit zu erhalten4. Im Falle einer Hüftlaxität bei jungen erwachsenen Hunden ist der einzige chirurgische Ausweg die doppelte (DPO) oder dreifache Beckenosteotomie (TPO), ein Verfahren, bei dem zwei oder drei vollständige Schnitte der Beckenknochen durchgeführt werden, um die Abdeckung des Hüftkopfes zu erweitern. Komplikationen nach Osteotomien sind jedoch häufig und das Fortschreiten der Arthrose wird immer noch beobachtet 5,6,7,8,9. Sobald sich schwere Arthrose und chronische Schmerzen entwickelt haben, bleiben nur noch komplexe Operationen mit hoher Belastung wie der Hüfttotalersatz (THR) oder die Salvage-Femur-Kopf-Hals-Ostektomie (FHO) übrig10. FHO zeigt jedoch bei Hunden großer Rassen weniger günstige Ergebnisse und erfordert eine längere Physiotherapie zur Wiederherstellung der Gliedmaßenfunktion11. Darüber hinaus ist THR technisch anspruchsvoll und von Natur aus mit schweren Komplikationen verbunden 12,13,14. Daher ist eine wirksame Hüftdysplasie-Therapie erforderlich, die nur eine schonende Operation und ein geringeres Komplikationsrisiko erfordert, bevor dieses Endstadium erreicht wird.
Das 3-dimensionale (3D)-gedruckte personalisierte Hüftimplantat (3DHIP) ist eine einzigartige Behandlung für Hüftdysplasie bei Hunden, die mit der Absicht entwickelt wurde, ein minimales traumatisches hundespezifisches Implantat anzubieten, das die Stabilität des Hüftgelenks wiederherstellt. Bei der Technik handelt es sich um ein Titanimplantat zur Behandlung von hauptsächlich jungen erwachsenen Hundepatienten (6 Monate bis 2 Jahre alt) mit einem dysfunktionalen Hüftgelenk, das laut der Fédération Cynologique Internationale (FCI)15 eine Hüftlaxität der Grade B (Borderline) bis D (moderat) aufweist. Nach der Computertomographie (CT) des dysplastischen Gelenks wird ein Implantat nach der spezifischen Anatomie des Hüftgelenks auf personalisierte Weise entworfen, um den dorsalen Hüftpfannenrand zu verlängern und so eine Subluxation des Hüftgelenks zu verhindern und die Stabilität des Hüftgelenks wiederherzustellen.
Eine frühere Studie an Hundeleichen zeigte, dass das Implantat die Abdeckung des Hüftkopfes verbesserte und bei einer Aufprallkraft von 1.330 ± 320 Newton ein Versagen zeigte16. Anschließend zeigte eine Pilotstudie mit Versuchshunden eine verbesserte Femurkopfabdeckung, eine reduzierte Hüftlaxität und eine erhöhte Gewichtsbelastung durch Kraftmessplattenanalyse. Darüber hinaus zeigte die Untersuchung der intervenierten Hüften 6 Monate nach der Implantation ein normales Volumen und eine glatte Oberfläche sowohl des Hüftkopfes als auch des Hüftpfannenknorpels, begleitet von einer Gelenkkapselhypertrophie auf der Grundlage grober und histologischer Befunde17. Nach Bestätigung der Wirksamkeit und Sicherheit des Implantats und des Behandlungskonzepts wurde eine klinische Untersuchung an kundeneigenen Hunden mit Hüftdysplasie durchgeführt. Die Kurzzeitstudie ergab, dass die Vorteile des 3D-gedruckten Implantats zur Verlängerung des Hüftpfannenkranzes eine individuelle, gute Anpassung des Implantats an die Hüftpfanne, die Wiederherstellung der Stabilität des Hüftgelenks, eine Verringerung schmerzbedingter Aktivitäten und ein chirurgisches Verfahren mit geringen Auswirkungen sind18. Die Anwendung des Implantats erfordert einen Zugang zum ventrocaudalen Aspekt des Beckenkörpers und zum kraniodorsalen Aspekt des Hüftgelenks. In dieser Arbeit beschreiben wir unsere Operationsplanung und unser Operationsvorgehen mit einem modifizierten kraniodorsalen Zugang zum Hüftgelenk als Handbuch für die Implantation des 3DHIP bei Hunden, die von Hüftdysplasie betroffen sind.
Protokoll
Diese Studie wurde als nicht-experimentelle klinische Tierarztpraxis im Sinne von Artikel 1 bis 5 Buchstabe b der Richtlinie 2010/63/EU eingestuft und von den Ausschüssen für veterinärmedizinische klinische Studien (VCSC) der Universität Utrecht, Utrecht, Niederlande, genehmigt. Diese Studie umfasste die Behandlung von Hunden im Besitz von Kunden, wobei alle Hunde weiterhin in der Obhut ihrer jeweiligen Besitzer blieben. Alle Hundebesitzer erhielten ein Informationsschreiben, in dem das Studienprotokoll, alle möglichen Komplikationen (z. B. Infektionen, Implantatversagen, neurologische Defizite und andere) und alternative Behandlungen wie Beckenosteotomie aufgeführt waren. Des Weiteren wurden in dieser Form Datenschutzaspekte und das inhärente Datenmanagement erläutert. Alle Kunden unterschrieben eine Einverständniserklärung. Das gesamte Protokoll dieser Studie ist in die folgenden Hauptschritte unterteilt: Patientenauswahl, 3DHIP-Implantatdesign und -herstellung, präoperatives Management und Anästhesie, chirurgischer Eingriff und postoperatives Management.
1. Auswahl des Patienten
- Identifizierung von Hunden im Besitz von Klienten im Alter von > 6 Monaten mit klinischen Symptomen im Zusammenhang mit der Huntington-Krankheit, die ein positives Ortolani-Subluxationszeichen aufweisen (Abbildung 1) und röntgenologische Hinweise auf die Huntington-Krankheit mit FCI-Grad B bis D (Abbildung 2).
HINWEIS: Der Ortolani-Subluxationstest ist ein diagnostisches Manöver, das in der Veterinärmedizin zur Beurteilung der Stabilität des Hüftgelenks bei Hunden verwendet wird. Beim Ortolani-Test beim Hund positioniert der Untersucher das Tier auf dem Rücken und beugt die Hüfte um 90°, während er das Becken stabilisiert. Jede hintere Gliedmaße wird sanft abduziert, mit dem Ziel, den Hüftkopf aus der Hüftpfanne zu verlagern, um die Stabilität des Hüftgelenks zu beurteilen. Ein positives Ortolani-Zeichen, das durch ein charakteristisches "Klirren" oder eine Bewegung angezeigt wird, deutet auf eine Hüftdysplasie und das Potenzial für eine Instabilität des Hüftgelenks hin. - Schließen Sie Hunde mit einer offenen Hüftpfanne, luxoiden Hüften oder einer früheren Hüftoperation aus.
- Führen Sie eine CT-Untersuchung der Hüften durch, um Hunde mit mittelschweren bis schweren osteoarthritischen Veränderungen der Hüften auszuschließen und für das Implantatdesign.
HINWEIS: Hunde mit Osteophyten am Oberschenkelhals und/oder kranialen und kaudalen Acetabulumrand-Osteophyten > 2 mm sind ausgeschlossen (Abbildung 3).
2. Design und Produktion von 3DHIP-Implantaten
- Entwerfen Sie das 3DHIP-Implantat (Patentnummer EP3463198B119) aus präoperativen CT-DICOM-Bildern des gesamten Beckens, wie von Willemsen et al.16 und Kwananocha et al.18 im Labor beschrieben (siehe Materialtabelle).
- Segmentieren Sie den Beckenknochen und die Oberschenkelknochen jedes Kandidatenhundes aus dem präoperativen CT und erstellen Sie ein 3D-Modell mit spezieller Software (siehe Materialtabelle und Abbildung 4A).
- Erstellen Sie ein lokales Koordinatensystem für das Becken, basierend auf der geneigten hinteren Beckenebene.
- Messen Sie den nativen Norberg-Winkel (NA) der Hüften jedes Hundekandidaten auf dem 3D-Modell (Abbildung 4B).
- Verwenden Sie die spezielle Software (siehe Materialtabelle), um das 3DHIP-Implantat auf dem 3D-Modell des Beckens zu entwerfen. Verwenden Sie die native NA, um den Umfang der erforderlichen Ausdehnung des dorsalen Hüftpfannenrandes zu bestimmen. das 3DHIP-Implantat erhöht die NA um 25-35 Grad (Abbildung 4C und Abbildung 4D).
- Stellen Sie sicher, dass das 3DHIP-Implantat aus zwei Unterteilen besteht: dem Befestigungsteil und dem Randverlängerungsteil. Entwerfen Sie das Befestigungsteil so, dass es aus einer porösen Innenschale besteht und vier Verriegelungsschraubenlöcher und einen zusätzlichen ventralen Darmbeinflansch enthält, um eine einfache und präzise Positionierung zu ermöglichen. Entwerfen Sie das Felgenverlängerungsteil so, dass der dorsale Hüftpfannenkranz mit einem internen Versatz von 1,5 mm verlängert wird, was eine ungehinderte Befestigung der Gelenkkapsel ermöglicht (Abbildung 5A und Abbildung 5B).
- Drucken Sie das erstellte 3DHIP-Implantat (Abbildung 5C) aus einer medizinischen Titanlegierung (Ti6AI4V ELI Grad 23) unter Verwendung der selektiven Laserschmelztechnologie mit einer direkten Metalldruckmaschine, die vom Implantathersteller betrieben wird (siehe Materialtabelle).
- Nachbearbeitung des gedruckten 3DHIP-Implantats, einschließlich Spannungsentspannung (Vakuumglühen), manuelles Spiegelpolieren und Ultraschallreinigung, durchgeführt vom Implantathersteller (siehe Materialtabelle).
- Führen Sie die Endreinigung in der Sterilisationseinheit des Krankenhauses durch, um alle Reste von Metallstaub aus dem Herstellungsprozess zu entfernen.
- Waschen Sie das 3DHIP-Implantat manuell mit Povidon-Jod-Shampoo (siehe Materialtabelle) und sterilem Wasser.
- Reinigen Sie das 3DHIP-Implantat mit der hygienischen Waschmaschine (siehe Materialtabelle) bei einer Temperatur von 94 °C für 90 min.
- Umschließen Sie das 3DHIP-Implantat mit doppelt transparenten Sterilisationslaminaten (siehe Materialtabelle) und versiegeln Sie jedes Laminat separat.
- Sterilisieren Sie das Implantat durch Dampfautoklavieren (siehe Materialtabelle) bei einer Temperatur von 134 °C für 80 min.
3. Präoperatives Management und Anästhesie
- Führen Sie vor der Anästhesie eine allgemeine Untersuchung des Hundes des Kunden durch und kategorisieren Sie das Anästhesierisiko anhand der Patientenskala der American Society of Anesthesiologists (ASA) (Skala 1-5)20.
HINWEIS: Die Patientenskala der American Society of Anesthesiologists (ASA) wird verwendet, um das Anästhesierisiko von Hunden zu kategorisieren, und unterstützt Tierärzte bei der Bestimmung geeigneter Anästhesieprotokolle für jeden Hund. Es klassifiziert Hunde basierend auf ihrem Gesundheitszustand in verschiedene Klassen, die von Klasse I für gesunde Hunde bis Klasse V für Hunde in kritischem Zustand reichen, von denen nicht erwartet wird, dass sie eine Operation überleben. Hunde, die in die Kategorien ASA 1 (normaler gesunder Hund) und ASA 2 (Hunde mit leichter systemischer Erkrankung) eingeordnet sind, gelten als geeignete Kandidaten für diese chirurgische Behandlung. Diese Hunde haben in der Regel keine oder nur leichte systemische Grunderkrankungen, sind bei guter allgemeiner Gesundheit und weisen normale physiologische Funktionen auf. Sie gelten als risikoarme Kandidaten für Operationen und Anästhesie. Das Tier muss mindestens 6 Stunden vor der geplanten Einführungszeit nüchtern sein. - Betäuben Sie den Hund nach ASA-Kategorisierung nach den individuellen Bedürfnissen des Patienten.
- Intravenös Dexmedetomidin in einer Dosis von 2 μg/kg und Methadonhydrochlorid in einer Dosis von 0,3 mg/kg zur Prämedikation beim Hund verabreichen. (siehe Werkstofftabelle).
HINWEIS: Die Auswahl der Prämedikation und der Verabreichungsweg können je nach Vorliebe des Anästhesisten und dem Gesundheitszustand und Verhalten des Hundes unterschiedlich sein. - Verabreichen Sie intravenös Propofol in einer Dosierung von 2-4 mg/kg (siehe Materialtabelle) zur Anästhesieeinleitung.
- Intubieren Sie den Hund und halten Sie die Narkose mit inhalativem Isofluran (siehe Materialtabelle) und Sauerstoff aufrecht.
- Intravenös Dexmedetomidin in einer Dosis von 2 μg/kg und Methadonhydrochlorid in einer Dosis von 0,3 mg/kg zur Prämedikation beim Hund verabreichen. (siehe Werkstofftabelle).
- Kontinuierliche Überwachung und Sicherstellung der Stabilität der Vitalparameter, einschließlich Herzfrequenz, Atemfrequenz, endexspiratorischer Kohlendioxidspiegel, perkutane arterielle Sauerstoffsättigung, nicht-invasiver arterieller Blutdruck, Ösophagustemperatur und Elektrokardiographie.
- Führen Sie eine epidurale Analgesie mit einer sterilen Technik durch.
- Positionieren Sie den Hund in Brustbeinlage und beugen Sie die Hintergliedmaßen sanft nach vorne, um mehr Platz zwischen dem letzten Lendenwirbel und dem Kreuzbein zu schaffen.
- Identifizieren Sie die Injektionsstelle, die sich direkt kaudal des 7. dorsalen Wirbelsäulenfortsatzes befindet, wo ein "Grübchen" abgetastet werden kann.
- Führen Sie ein steriles Peeling durch und ziehen Sie sterile Handschuhe mit aseptischen Techniken an.
- Führen Sie die Spitze der Spinalnadel in den Epiduralraum ein und überprüfen Sie die korrekte Platzierung mit der Technik des "hängenden Tropfens". Geben Sie kurz einen Tropfen Kochsalzlösung in die Nadelnabe der Wirbelsäule. Wenn die spinale Nadelspitze in das Ligamentum flavum eindringt und in den Epiduralraum eintritt, wandert die Kochsalzlösung innerhalb der Nabe von der Nabe in die Nadel21.
- Injizieren Sie die Arzneimittel (Morphin 0,1 mg/kg verdünnt mit Levobupavacain 1 ml/5 kg) (siehe Materialtabelle) mit einer langsamen, konstanten Rate, um eine gleichmäßige Verteilung des Arzneimittels zu gewährleisten, wenn die korrekte Platzierung bestätigt wird.
- Legen Sie einen Foley-Verweilkatheter (siehe Materialtabelle) mit einer sterilen Technik in die Blase und lassen Sie ihn 12-24 Stunden lang an Ort und Stelle.
- Gewährleistung einer sauberen und sterilen Umgebung für das Katheterisierungsverfahren; Schneiden Sie die Haare an der Vorhaut bei Rüden und das umgebende ventrale Scheidengewölbe bei Hündinnen.
- Reinigen Sie den Bereich mit Povidon-Jod-Lösung (siehe Materialtabelle) und spülen Sie das Vorhaut-/Vaginalgewölbe mit 2-12 ml verdünnter Povidon-Jod-Lösung (das Volumen variiert je nach Größe des Hundes).
- Waschen Sie sich gründlich die Hände und tragen Sie sterile Handschuhe, um das Risiko einer Kontamination zu minimieren.
- Tragen Sie steriles Gleitgel auf das distale Ende des Foley-Katheters auf und wenden Sie während des Einführens des Foley-Katheters eine aseptische Technik an.
- Sobald der Katheter richtig in der Blase sitzt, blasen Sie den Ballon mit sterilem Wasser entsprechend dem auf der Packung angegebenen Volumen auf. Dadurch wird der Katheter an Ort und Stelle fixiert und ein versehentliches Lösen verhindert.
- Verbinden Sie die Drainageöffnung am Foley-Katheter mit der Aufnahmeöffnung an einem Urinauffangbeutel.
- Schneiden Sie die gesamte Extremität umlaufend von der Wirbelsäule bis knapp distal des Sprunggelenks ab. Bei einer einstufigen bilateralen 3DHIP-Implantation wird die andere Extremität auf ähnliche Weise abgeschnitten und die linke und rechte Seite am lumbosakralen Rücken verbunden.
- Wickeln Sie den distalen Teil der Extremität mit einem unsterilen kohäsiven Verband ein. Wählen Sie eine geeignete Breite und Länge des unsterilen kohäsiven Verbandes, der etwas unterhalb der Operationsstelle beginnt und ihn spiralförmig über die Extremität wickelt und die Pfote und die Nägel bedeckt.
- Verabreichen Sie Cefazolin zur Injektion in einer Dosis von 20 mg/kg (siehe Materialtabelle) intravenös 30 Minuten vor dem Hautschnitt und wiederholen Sie dies alle 90 Minuten bis zum Ende der Operation.
- Positionieren Sie den Hund in seitlicher Liege auf einem handelsüblichen Operationstisch und bringen Sie das betroffene Glied in eine hängende Position. Sichern Sie den Patienten in dieser Position mit einem Vakuum-Sitzsackpositionierer
- Führen Sie das abschließende sterile chirurgische Peeling an der Extremität zur Vorbereitung der Operation durch. Schrubben Sie die Haut 2x mit 4 % Chlorhexidingluconat und beenden Sie mit zwei Anwendungen von 70 % (v/v) Ethanolspray (siehe Materialtabelle).
- Positionieren Sie vier wasserdichte OP-Abdeckungen um die Operationsstelle. Weisen Sie einen Assistenten an, die distale Extremität aus ihrer schwebenden Position zu lösen, während der Chirurg die distale Extremität mit einer sterilen, wasserdichten Socke sichert und abdeckt. Fügen Sie eine Schicht steriler, kohäsiver Folie für zusätzlichen Schutz hinzu.
- Decken Sie die freiliegende Haut des gesamten Operationsgebietes mit einem jodimprägnierten Tuch ab (siehe Materialtabelle) und befestigen Sie sie anschließend mit Handtuchklammern.
4. Chirurgischer Eingriff
- Identifizieren Sie die Spitze des Trochanters major, den kranialen Rand des proximalen Femurs und den Beckenflügel durch Palpation, um die Orientierung zu ermitteln.
- Schneiden Sie die Haut mit einem chirurgischen Messer scharf von der kranialen dorsalen Beckenwirbelsäule beginnend 6-10 cm kranial bis zum Trochanter major ein. Drehen Sie sich dann leicht nach ventral entlang der kranialen Grenze des proximalen Femurs. Stoppen Sie die Inzision 2-5 cm distal des Trochanters major. Die Schnittlänge beträgt ca. 8-15 cm (abhängig von der Größe des Hundes; Abbildung 6A).
HINWEIS: Dieser chirurgische Ansatz wurde gegenüber dem kraniodorsalen Zugang des Hüftgelenks modifiziert, über den Johnson22 berichtet hatte. - Machen Sie einen Schnitt durch das Unterhautfett bis hinunter zur Faszie, um eine anatomische Dissektion entlang der anatomischen Ebenen zu etablieren (Abbildung 6B).
- Trennen und schneiden Sie das oberflächliche Blatt des Musculus fascia latae entlang des Schädelrandes des Musculus biceps femoris scharf ab. Ziehen Sie den Musculus biceps femoris nach kaudal zurück.
- Identifiziere das Fettdreieck, das vom Musculus tensor fascia latea, dem Musculus glutealis und dem Musculus biceps femoris begrenzt wird. Trennen Sie das Fettdreieck mit einer Präparierschere und einem Zeigefinger mit stumpfer Spitze, um Zugang zu den tieferen Schichten zu erhalten.
- Mit einem chirurgischen Messer wird das intermuskuläre Septum zwischen dem oberflächlichen Gesäßmuskel, dem mittleren Gesäßmuskel und dem Musculus tensor fascia latae eingeschnitten (Abbildung 7A und Abbildung 7E).
- Verwenden Sie einen Handretraktor, um die oberflächlichen und mittleren Gesäßmuskeln nach dorsal zu trennen und zurückzuziehen, wodurch der Ansatz des tiefen Gesäßmuskels freigelegt wird.
- Untergraben Sie den tiefen Gesäßmuskel in der Nähe des Trochanters major mit einer Präparierschere mit stumpfer Spitze.
- Legen Sie eine Haltenaht auf die tiefe Gesäßsehne etwa 1-1,5 cm proximal von ihrem Ansatz am Trochanter major an.
- Führen Sie mit einem chirurgischen Messer eine vollständige tiefe Gesäßtenotomie in der Nähe des Knochens (ca. 0,5-1 cm vom Ansatz entfernt) durch (Abbildung 7B und Abbildung 7F).
- Führen Sie eine stumpfe Dissektion mit einer stumpfen Dissektionsschere durch, um den tiefen Gesäßmuskel von der darunter liegenden Gelenkkapsel zu befreien, wonach er mit einem Periostlift und Zeigefinger subperiostal vom Darmbein angehoben werden kann.
- Verwenden Sie den bipolaren Elektrokauter zur Blutstillung kleiner Gefäße zwischen dem tiefen Gesäßmuskel und der Gelenkkapsel. Ziehen Sie dann den tiefen Gesäßmuskel dorsal zurück, indem Sie die Amry Navy-Retraktoren ersetzen.
- Befreien Sie den Musculus iliacus mit Hilfe eines Periostlifts teilweise von der kaudoventralen Grenze des Beckenschafts und identifizieren Sie den Ansatz des Musculus rectus femoris (Abbildung 7C und Abbildung 7G).
- Verwenden Sie einen Periostlifter, um das gesamte verbleibende Weichgewebe aus dem freiliegenden Beckenschaft zu entfernen, um eine genaue Positionierung des 3DHIP-Implantats vorzubereiten, und kratzen Sie das Periost, um das Einwachsen von Knochen für die sekundäre Fixation des Implantats zu stimulieren.
- Identifizieren Sie den Musculus articularis coxae kaudal zum Musculus rectus femoris, der über der Gelenkkapsel liegt.
HINWEIS: Der Musculus articularis coxae kann von seinem Ansatz befreit werden, wenn er die Positionierung des Implantats beeinträchtigt. - Setzen Sie das 3DHIP-Implantat in die vorgesehene Position ein, wobei der Flansch des Implantats des Befestigungsteils unter dem ventralen Rand des freiliegenden kaudoventralen Beckenschafts gerade kranial zu dem knöchernen Vorsprung eingehakt wird, der den Ansatz des Musculus rectus femoris markiert (Abbildung 7D und Abbildung 7H).
- Vergewissern Sie sich, dass der Randverlängerungsteil des Implantats den kraniodorsalen Teil der Hüftgelenkskapsel überlagert, ohne die Befestigung der Gelenkkapsel am Hüftpfannenrand zu beeinträchtigen, und dass kein tiefer Gesäßmuskel unter dem Streckteil erfasst wird.
HINWEIS: Eine adäquate Belichtung für die Implantatpositionierung und das Einsetzen von Schrauben kann durch kontinuierliche Abduktion, Außenrotation und Beugung des Hüftgelenks durch einen Assistenten erreicht werden, um die Spannung auf den Gesäßmuskelkomplex zu lösen und die chirurgische Exposition zu erleichtern. - Überprüfen Sie das Implantat auf ideale Positionierung, indem Sie mit der Absaugkanüle den perfekten Knochenbestand in allen vier freiliegenden Schraubenlöchern visualisieren und sondieren und auf das Fehlen von Platz zwischen dem Beckenflansch und dem kaudoventralen Beckenschaft sondieren.
- Fixieren Sie das Implantat vorübergehend in der gewünschten Position mit einer selbstschneidenden Feststellschraube aus Titan (2,4 mm, 2,7 mm oder 3,5 mm) (siehe Materialtabelle), die nicht vollständig angezogen ist, um beim Einsetzen der zweiten Schraube minimale Rotationsanpassungen am Implantat zu ermöglichen.
HINWEIS: Die Reihenfolge der Platzierung der vier Schrauben kann entsprechend ihrer bequemen Zugänglichkeit angepasst werden (Abbildung 5C). - Führen Sie eine intraoperative Fluoroskopie (siehe Materialtabelle) in lateraler (Abbildung 8A) und latero-schräger (Abbildung 8B) Ansicht durch, um die Position und Ausrichtung des Implantats umfassend zu beurteilen. Vergleichen Sie die erhaltenen fluoroskopischen Bilder mit der präoperativen Planung, um sicherzustellen, dass das Implantat gemäß dem Operationsplan positioniert wird.
- Prüfen Sie, ob die Krümmung des Randverlängerungsteils des Implantats genau deckungsgleich mit der Krümmung des Hüftkopfes und des sichtbaren kaudalen und kranialen Hüftpfannenrandes ist, die nicht vom Implantat bedeckt sind.
HINWEIS: Bei Bedarf können Anpassungen vorgenommen werden. Die erste Schraube wird entfernt, das Implantat ersetzt und provisorisch mit einer Schraube in neuem Knochenbestand fixiert, und die Durchleuchtung wird wiederholt. - Setzen Sie drei selbstschneidende Feststellschrauben aus Titan (2,4 mm, 2,7 mm oder 3,5 mm) in die verbleibenden Schraubenlöcher ein, um das Implantat am Beckenschaft zu befestigen. Nachdem die zweite Schraube platziert wurde, ziehen Sie die erste Schraube vollständig fest.
- Führen Sie eine letzte Überprüfung durch, ob alle Schrauben von Hand mit dem Verriegelungsmechanismus angezogen sind.
- Führen Sie die Beugung, Streckung und Abduktion des Hüftgelenks sowie den Ortolani-Subluxationstest durch, um ein Femurkopf-/Halsimpingement auszuschließen und sicherzustellen, dass die Hüftlaxität rückgängig gemacht wird.
- Befestigen Sie die abgeschnittenen Enden der Ansatzsehne des tiefen Gesäßmuskels wieder mit einem Verriegelungsschlaufen-Nahtmuster und 1-2 Matratzennähten mit synthetischem, resorbierbarem monofilem Nahtmaterial (siehe Materialtabelle), die für die Annäherung des Gewebes über längere Zeiträume bestimmt sind. Strecken Sie das Hüftgelenk und drehen Sie es nach innen, um die Spannung auf die Ansatzsehne des tiefen Gesäßmuskels während des Nähens zu verringern.
- Reparieren Sie die Gesäßfaszie und die Tensorfaszie mit synthetischem, monofilem, resorbierbarem Nahtmaterial in einem einfachen, unterbrochenen Muster.
- Verschließen Sie das Unterhautgewebe mit einer resorbierbaren Naht aus synthetischem Monofilament in einem einfachen unterbrochenen Muster und verschließen Sie die Haut mit einer nicht resorbierbaren Naht aus synthetischem Monofilament in einem einfachen unterbrochenen Muster (siehe Materialtabelle).
HINWEIS: Wenn ein einstufiger bilateraler Eingriff geplant ist, drehen Sie den Hund auf die andere Seite, während sich die unbehandelte Gliedmaße in hängender Position befindet. Nach der aseptischen Vorbereitung werden die chirurgischen Eingriffsschritte 3.10-4.27 in ähnlicher Weise durchgeführt. - Führen Sie eine postoperative Bildgebung durch, die entweder aus einem CT-Scan der Hüfte oder orthogonalen Röntgenaufnahmen der Hüfte in latero-oblysalen und ventrodorsalen Ansichten besteht, um die endgültige Beurteilung der Implantatpositionierung und der Schraubenplatzierung zu ermöglichen (Abbildung 9).
5. Postoperatives Management
- Stationäre Versorgung und Schmerzbehandlung über Nacht (z. B. mit kontinuierlichen Infusionen [CRI] von Ketamin HCl 2-10 μg∙kg-1∙min-1 oder Sufentanilcitrat 0,1 μg∙kg-1∙h-1 mit Methadon (i.v., 0,2 mg/kg alle 6 h), Carprofen (i.v., 4 mg/kg einmal täglich) und Gabapentin (PO, 10 mg/kg alle 8 h) (siehe Materialtabelle).
- Erlauben Sie bei Bedarf ein direktes postoperatives Gehen an der kurzen Leine, um am Folgetag auf den rutschfesten Boden zu urinieren und zu koten (siehe Ergänzendes Video S1).
HINWEIS: Bei Instabilität der Hintergliedmaßen oder Problemen beim Aufstehen verwenden Sie eine Stützschlinge oder ein Handtuch unter dem Bauch, um die Hintergliedmaßen zu stützen. - Lassen Sie am Tag nach der Operation nach der Entfernung des Foley-Katheters und wenn freiwilliges Wasserlassen beobachtet wird, die Entlassung zu Hause zu.
- Verschreiben Sie Medikamente zur Schmerzbehandlung zu Hause (z. B. orale Medikamente wie Carprofen 2 mg/kg BID und Gabapentin 10 mg/kg alle 8 Stunden für 14 Tage) (siehe Materialtabelle).
HINWEIS: Bei hyperaktiven Hunden kann Trazodonhydrochlorid 2-5 mg/kg BID (siehe Materialtabelle), oral verabreicht werden. Dies kann 1-2 Wochen postoperativ fortgesetzt werden, um eine sichere Rehabilitation ohne belastende Aktivitäten zu gewährleisten. - Verbieten Sie Aktivitäten mit hoher Belastung (z. B. Springen, Laufen, Treppensteigen, Laufen mit anderen Haustieren oder "raue Haltung") für 6 Wochen nach der Operation. Gehen Sie zu Hause langsam mit den Hunden spazieren und ermutigen Sie sie, die operierte(n) Hintergliedmaße(n) nach einem wöchentlichen Übungsschema zu benutzen. Lassen Sie den Hundepatienten innerhalb von 6 Wochen postoperativ 4-6 Mal täglich mit Leinengurt laufen, zunächst jeweils 5-10 Minuten in den ersten 2 Wochen, und verlängern Sie dann die Dauer alle 2 Wochen um 5 Minuten.
- Raten Sie ab der zweiten Woche nach der Operation zu einer professionellen Physiotherapie und/oder Hydrotherapie, wenn die Wundheilung der Haut abgeschlossen ist.
Repräsentative Ergebnisse
Kurzfristige Ergebnisse der Hüftpfannenrandverlängerung wurden bereits veröffentlicht, die aus einer laufenden Beobachtungsstudie am Department of Clinical Sciences der Universität Utrecht hervorgegangensind 18. Von Dezember 2019 bis März 2022 wurden insgesamt 61 Hüften von 34 Hunden in die Studie eingeschlossen. Die Kohorte bestand aus 24 Männern und 10 Frauen mit einem mittleren Alter von 12 Monaten (von 7 bis 38 Monaten) und einem mittleren Körpergewicht von 27,3 kg (von 12 bis 86 kg). Sieben Hunde wurden an einer einseitigen Hüfte operiert, während zwanzig Hunde in einer einzigen Sitzung beidseitig an der Hüfte operiert wurden. Darüber hinaus wurden sieben Hunde an beiden Hüften operiert, die in zwei separaten Sitzungen durchgeführt wurden.
Die vorherige Studie fand einen signifikanten Anstieg des Norberg-Winkels (NA), des linearen Prozentsatzes der Femurkopfabdeckung (LFO) und des Prozentsatzes der Femurkopfabdeckung (PC) unmittelbar nach der Implantation (Tabelle 1). Darüber hinaus war das postoperative Ortolani-Subluxationszeichen bei 96,7 % der operierten Gliedmaßen negativ, was darauf hindeutet, dass das Acetabulumrandstreckungsimplantat die Hüftkongruenz wiederherstellte und die Laxheit der dysplastischen Hüften verringerte18. Insbesondere die Möglichkeit, die Abdeckung des Hüftkopfes zu erhöhen, ohne eine redirektionale Osteotomie durchzuführen, ermöglichte die physiologische Beibehaltung der Beckengeometrie. Die minimal-invasive Technik führte kurzfristig zu einer geringen Inzidenz von Komplikationen (4,9 %), förderte eine frühe Mobilisation und verringerte die Schmerzen im Zusammenhang mit der Aktivität (Tabelle 1).
Darüber hinaus ermöglichte diese Technik die einstufige bilaterale 3DHIP-Implantatplatzierung. Die behandelte(n) Gliedmaße(n) wurden innerhalb von 12 bis 24 Stunden nach der Operation ohne Beckenstütze belastet. Während des 12-monatigen Überwachungszeitraums mussten 3 Hunde aufgrund eines Implantatversagens (2 Hunde) oder eines signifikanten Fortschreitens der Arthrose (1 Hund) einer Revisionsoperation unterzogen werden. Bei gleichzeitiger Anwendung des vorgestellten chirurgischen Ansatzes mit den vorgeschlagenen Hüftgelenksbewegungen (Abduktion, Flexion und Außenrotation) wurde eine bessere Freilegung des ventrocaudalen Aspekts des Beckenschafts und des kraniodorsalen Aspekts des Hüftgelenks erreicht, was die Positionierung des 3DHIP-Implantats erleichterte. Darüber hinaus erhöhte die intraoperative Durchleuchtung die Genauigkeit der Implantatpositionierung.
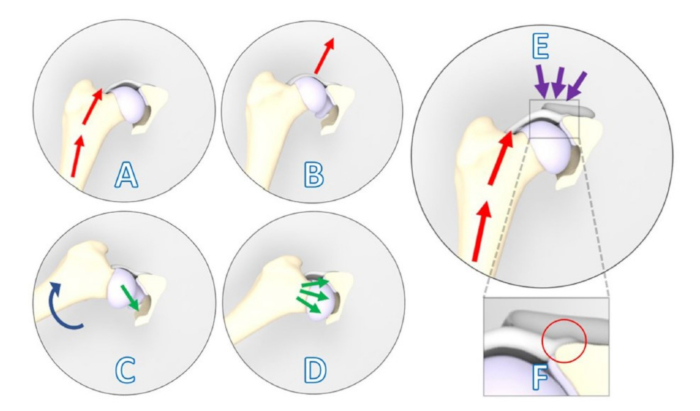
Abbildung 1: Schematische Darstellungen, die ein positives Ortolani-Subluxationszeichen zeigen, das durch das 3DHIP-Implantat entgegenwirkt. (A-D) Positives Ortolani-Subluxationszeichen. (A) Die Gliedmaße des Hundes wird in neutraler Beugung und Adduktion positioniert, und es wird eine Kraft (rote Pfeile) in Richtung des Rückens des Hundes entlang der Femurachse ausgeübt, die (B) eine dorsale Subluxation des dysplastischen Hüftgelenks verursacht. (C) Die allmähliche Abduktion der Gliedmaßen (blauer Pfeil) wird unter Aufrechterhaltung des Drucks auf den Femur durchgeführt. (D) Abhängig von der Fehlfunktion des Hüftpfannenrandes fällt der subluxierte Hüftkopf in die Pfanne zurück (grüne Pfeile). (E) Das 3DHIP-Implantat wird eingeführt, um die Stabilität des dysplastischen Hüftgelenks zu erhöhen, indem es die Hüftkapsel und das Labrum verstärkt, die als tragende und stabilisierende Flächen dienen (violette Pfeile). (F) Bei der Vergrößerung des rechteckigen Bereichs ist der innere Versatz des Implantats von 1,5 mm im roten Kreis sichtbar, wodurch sichergestellt wird, dass der Kapselansatz nicht beeinträchtigt wird. Diese Abbildung wurde von Willemsen et al.17 modifiziert. Abkürzung: 3DHIP = 3-dimensional gedrucktes, Hüftimplantat. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
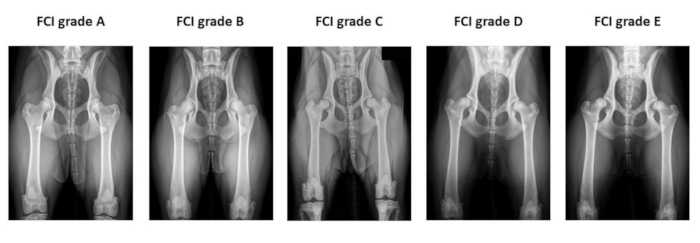
Abbildung 2: Beispiel für die präoperativen Röntgenaufnahmen der Hüfte, die für die Klassifikation der Hüftdysplasie der Fédération Cynologique Internationale verwendet werden . Die Röntgenaufnahmen werden in ventro-dorsaler Hüftstrecke angefertigt. Von links nach rechts klassifiziert die FCI die Hüftdysplasie in fünf verschiedene Kategorien: A (normal), B (Borderline), C (leichte Hüftdysplasie), D (mittelschwere Hüftdysplasie) und E (schwere Hüftdysplasie). Abkürzung: FCI = Fédération Cynologique Internationale. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
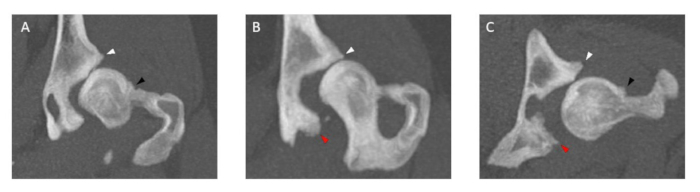
Abbildung 3: Bilder von CT-Untersuchungen des Hüftgelenks, die Osteophyten unterschiedlicher Größe zeigen. Die Mächtigkeit aller Osteophyten wird sowohl in der (A, B) koronalen Ebene als auch in der (C) Transversalebene am kranialen (weiße Pfeilspitze) und kaudalen (rote Pfeilspitze) Hüftpfannenrand und am Oberschenkelhals (schwarze Pfeilspitze) gemessen. Hunde mit Osteophyten am Hüfthals und/oder an einem kranialen und kaudalen Hüftpfannenrand > 2 mm sind ausgeschlossen. Die Dicke der CT-Untersuchungsscheibe beträgt 5 mm. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
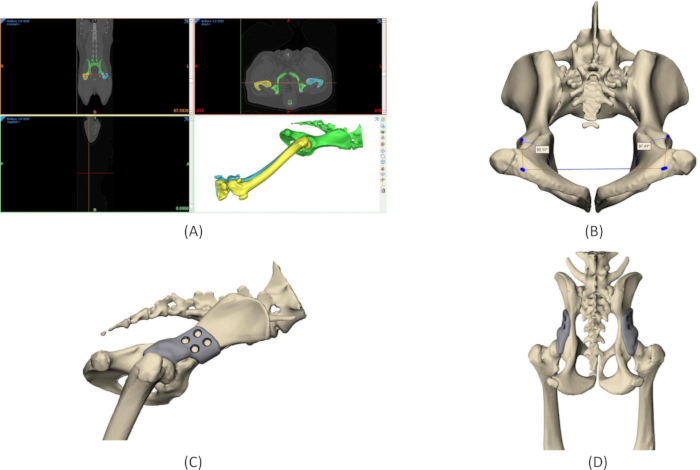
Abbildung 4: Designprozess des 3DHIP-Implantats. (A) Segmentierung der Region of Interest aus CT-DICOM-Daten. (B) Messungen der nativen Norberg-Winkel auf dem 3D-Modell des Beckens. (C) Rendering eines 3DHIP-Implantats an der rechten Hüfte, Seitenansicht. (D) Rendering von bilateralen 3DHIP-Implantaten, dorsal-ventrale Ansicht. Abkürzung: 3DHIP = 3-dimensional gedrucktes, Hüftimplantat. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
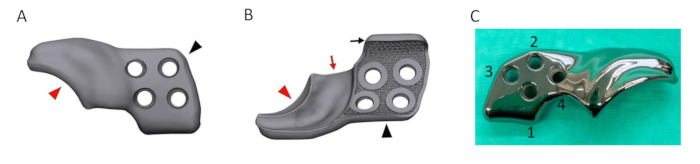
Abbildung 5: Rendering eines entworfenen 3DHIP-Implantats. (A) Gerendertes Bild der lateralen/äußeren Seite des 3DHIP-Implantats. (B) Gerendertes Bild der inneren Implantatoberfläche, das die poröse Oberfläche zeigt, die das Einwachsen von Knochen für die Osseointegration ermöglicht. Das Knochenbefestigungsteil (schwarze Pfeilspitze) des gerenderten Implantats mit 4 Verriegelungsschraubenlöchern und dem ventralen Darmbeinflansch (schwarzer Pfeil) zur Unterstützung der korrekten Positionierung und Stabilisierung des Implantats. Das Randverlängerungsteil (rote Pfeilspitze) des gerenderten Implantats mit dem internen Versatz von 1,5 mm (roter Pfeil) ermöglicht eine ungehinderte Befestigung der Gelenkkapsel. (C) Foto eines 3DHIP-Implantats aus Titan mit 4 Schraubenlöchern, die in der Reihenfolge für das Einsetzen der Schrauben angeordnet sind. Abkürzung: 3DHIP = 3-dimensional gedrucktes, Hüftimplantat. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
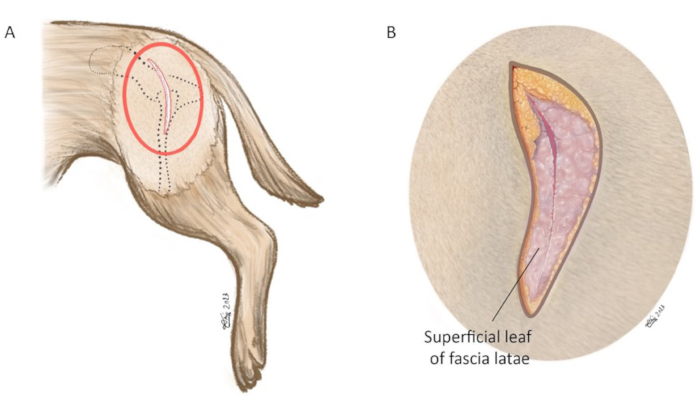
Abbildung 6: Schematische Darstellung des Hautschnitts. (A) Das rote Oval markiert den Bereich, in dem der Hautschnitt vorgenommen wird. (B) Vergrößerung des roten Kreises in (A). Der Hautschnitt wird mit einer #10-Klinge durchgeführt, die zentriert auf der Spitze des Trochanters major liegt und auf die kraniale dorsale Beckenwirbelsäule abzielt. Die Schnittlänge beträgt ca. 8-15 cm. In der vergrößerten Abbildung ist das oberflächliche Blatt der Fascia latae entlang der kranialen Muskelgrenze des Musculus biceps femoris eingeschnitten. Ausrichtung: links ist kranial, oben ist dorsal. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
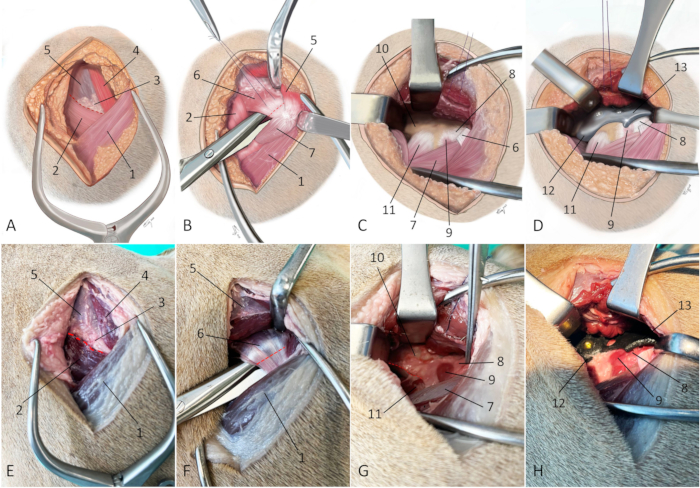
Abbildung 7: Schematische Illustrationen und Fotografien eines einbalsamierten Leichnams, die den chirurgischen Ansatz für die 3DHIP-Implantation darstellen. (A-D) Schematische Illustrationen und (E-H) Fotografien eines einbalsamierten Leichnams zeigen den chirurgischen Ansatz für die 3DHIP-Implantation. (A und E) Die rot gestrichelte Linie markiert die Linie des Schnitts durch das intermuskuläre Septum zwischen dem oberflächlichen Gesäßmuskel, dem mittleren Gesäßmuskel und dem Musculus tensor fascia latae. (B und F) Die rote gestrichelte Linie markiert die Tenotomiestelle. Die oberflächliche und mittlere Gesäßmuskulatur werden nach dorsal zurückgezogen, um den tiefen Gesäßmuskel freizulegen. Eine Präparierschere wird verwendet, um den tiefen Gesäßmuskel in der Nähe seines Ansatzes am Trochanter major zu untergraben. Die Tenotomie wird in der Nähe (bei 0,5-1 cm) des Ansatzes am Knochen durchgeführt. (C und G) Eine adäquate Belichtung für die 3DHIP-Implantatinsertion erfordert die Befreiung des tiefen Gesäßmuskels von der Gelenkkapsel und der lateralen Oberfläche des Beckenkörpers und die teilweise Befreiung des Musculus iliacus und des Musculus rectus femoris von der kaudoventralen Grenze des Beckenschafts (rote gestrichelte Linie). (D und H) Das 3DHIP-Implantat wird außerhalb der Kapsel des Hüftgelenks platziert. Aus Gründen der Genauigkeit und einfachen Positionierung wird der Darmfellflansch des Befestigungsteils des Implantats unter dem ventralen Rand des freiliegenden kaudoventralen Beckenschafts platziert. Ausrichtung: links ist kranial, oben ist dorsal. 1) Musculus biceps femoris, 2) Musculus tensor fascia latae, 3) Fettdreieck, 4) oberflächlicher Gesäßmuskel, 5) mittlerer Gesäßmuskel, 6) tiefer Gesäßmuskel/Sehne, 7) Musculus vastus lateralis, 8) Musculus boucularis coxae, 10) kaudaler Teil des Beckenkörpers, 11) Musculus rectus femoris, 12) iliumflansch des Implantats und 13) Randverlängerungsteil des Implantats. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
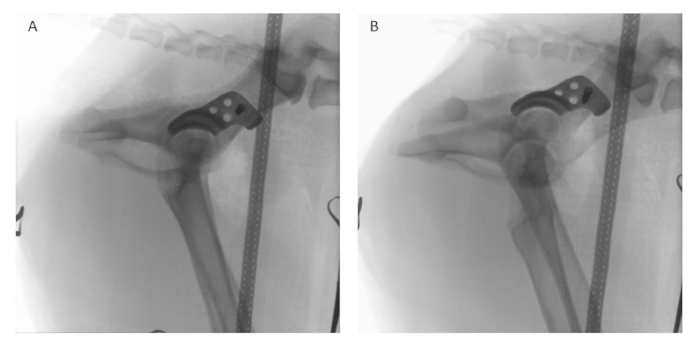
Abbildung 8: Intraoperative Fluoroskopie. Nach der Implantatpositionierung und der temporären Fixierung mit einer Feststellschraube erfolgt die intraoperative Durchleuchtung in (A) lateraler und (B) latero-obliner Ansicht mit einem digitalen Bildverstärker, um die Positionierung des Implantats zu beurteilen und mit der präoperativen Planung zu vergleichen. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.

Abbildung 9: Beispiele für postoperative Röntgenaufnahmen in drei Ebenen und postoperative CT-Scans nach einstufiger bilateraler 3DHIP-Implantatoperation bei einem Hund. (A) Röntgenaufnahme ventrodorsal Ansicht; (B) Röntgenaufnahme rechts latero-schräge Ansicht; (C) Röntgenaufnahme links latero-schräge Ansicht. 3D-Rekonstruktion aus dem postoperativen CT in lateraler Ansicht, die die rechte Hüfte (D) und (E) die dorso-ventrale Ansicht zeigt. (F) Postoperative CT beider Hüften in der Querebene mit einer Schnittdicke von 5 mm. Die 3DHIP-Implantate wurden mit vier Feststellschrauben auf jeder Seite fixiert. Bitte klicken Sie hier, um eine größere Version dieser Abbildung anzuzeigen.
| Messung der Ergebnisse | Präoperativ | Unmittelbar postoperativ | 1,5 Monate | 3 Monate | p-Wert |
| NA (◦) | 87 ± 13A | 134 ± 19b | - | 131 ± 20b | 0,001 <* |
| LFO (%) | 22 ± 15A | 81 ± 16b | - | 76 ± 19b | 0,001 <* |
| PC (%) | 33 ± 17A | 79 ± 21b | - | 77 ± 20b | 0.002* |
| HCPI (%) | 31,44 ± 11,9A | - | 20.39 ± 10.09B | 17,69 ± 10,8Mrd. | 0,001 <** |
Tabelle 1: Kurzfristige Ergebnisse (Mean ± SD) von Röntgenmessungen mittels koronaler CT und schmerzbezogenem Besitzerfragebogen unter Verwendung des Helsinki Chronic Pain Index bei Hunden mit Hüftdysplasie, die sich einer 3DHIP-Implantation unterzogen haben. Diese Tabelle wurde von Kwananocha et al.18 modifiziert. HCPI (%) = 100% × Gesamtindexpunktzahl/maximal möglicher Indexwert der beantworteten Fragen. a,bp-Wert < 0,05 aus Bonferroni, p-Wert* aus der Analyse wiederholter Messungen, p-Wert** aus einem verallgemeinerten linearen gemischten Modell. Abkürzungen: NA = Norberg-Winkel; LFO = linearer Prozentsatz der Überlappung des Hüftkopfes; PC = Prozentsatz der Oberschenkelkopfbedeckung; SD = Standardabweichung; HCPI = Helsinki Chronischer Schmerzindex.
Ergänzendes Video S1: Direkte postoperative Belastung mit nur kurzen Leinengängen auf rutschfestem Boden ab dem Tag nach der Operation erlaubt. Bitte klicken Sie hier, um dieses Video herunterzuladen.
Diskussion
Die Verlängerung des Hüftpfannenrandes mit dem 3DHIP-Implantat bietet Vorteile gegenüber herkömmlichen chirurgischen Therapien bei Hüftdysplasie bei Hunden und hat in der kurzfristigen Nachbeobachtung vielversprechende Ergebnisse gezeigt, um die Abdeckung des dysplastischen Hüftgelenks zu erhöhen und die Hüftlaxität umzukehren17,18. Ziel dieser Veröffentlichung war es, die Operationstechnik mit Tipps und Tricks als chirurgisches Handbuch für die Implantation des 3DHIP-Implantats bei Hunden mit Hüftdysplasie vorzustellen.
Auswahl der Kandidaten für die 3DHIP-Implantatinsertion - junge Hunde im Alter zwischen 6 und 24 Monaten mit klinischer Hüftdysplasie, die durch Hüftlaxität gekennzeichnet ist (FCI-Grad B-D) mit einem positiven Ortolani-Subluxationstest, sind geeignete Kandidaten. Die triradiate acetabuläre Wachstumsfuge muss verschlossen werden und vorzugsweise liegt in der CT-Bildgebung keine Osteoarthritis vor, obwohl kleinere Osteophyten bis zu 2 mm akzeptiert werden. Hunde mit luxoiden Hüften mit nahezu vollständiger Luxation des Hüftkopfes werden aufgrund des raschen Fortschreitens der Arthrose, der Unfähigkeit des Hüftkopfes, in die Hüftpfanne zu wandern, und der erwarteten frühen Umstellung auf einen Hüfttotalersatz nicht für die 3DHIP-Implantatinsertion akzeptiert.
Es gibt einige kritische Schritte innerhalb der Operationstechnik.
Implantat-Design
Aufgrund des individuellen Designs der 3DHIP-Implantate ist eine präoperative Beurteilung des dysplastischen Hüftgelenks mittels CT zwingend erforderlich. Neben der Bestimmung der korrekten Implantatgröße und -lage des ventralen ilialen Flansches kann insbesondere die Menge an Hüftpfannenrandverlängerung bestimmt werden, die für eine ausreichende Abdeckung des Femurkopfes erforderlich ist.
Chirurgischer Ansatz
Ein kritischer Schritt während der Operation ist die ausreichende Freilegung des dorsalen Hüftpfannenrandes und der ventralen Grenze des kaudalen Beckenkörpers für die Implantation. Der chirurgische Zugang zum Beckenkörper und zu den kraniodorsalen Aspekten des Hüftgelenks bei der 3DHIP-Implantation unterscheidet sich von herkömmlichen Ansätzen22. Bei der vorgestellten Technik wurde auf eine trochantäre Osteotomie verzichtet und eine tiefe Gesäß-Tenotomie durchgeführt, wobei die oberflächliche und mittlere Gesäßmuskulatur erhalten blieben. Dadurch wurde das Risiko von Komplikationen im Zusammenhang mit Trochanterosteotomien 23,24,25 wie verzögerter oder fehlender Pseudarthrose vermieden und der Genesungsprozess beschleunigt. Darüber hinaus kann dieser modifizierte kraniodorsale Ansatz bei einer Vielzahl von Altersgruppen, Rassen und Größen von Hunden ohne notwendige Modifikationen angewendet werden. Bemerkenswert ist, dass keine Komplikationen im Zusammenhang mit dem vorgestellten chirurgischen Ansatz berichtet wurden.
Korrekte Implantatinsertion
Obwohl das maßgeschneiderte 3D-gedruckte Hüftimplantat so konzipiert ist, dass es perfekt an die einzigartige Hüftpfannenanatomie jedes Hundes angepasst ist, wurde in der ersten Kohorte von Hunden immer noch eine unvollkommene Implantatinsertion mit 4-5 mm kraniokaudaler Abweichung zur geplanten Zielposition beobachtet18. Der ventrale iliale Flansch des Knochenansatzteils des 3DHIP-Implantats ermöglicht eine genauere Positionierung, insbesondere in dorsoventraler Richtung. Aufgrund der extrakapsulären Lage des Implantats ist es jedoch immer noch schwierig, eine perfekte Implantatpositionierung zu erreichen. Der innere Rand der Hüftpfanne wird durch die Synovialmembran verdeckt. Darüber hinaus kann die Osteophytenbildung während der Vorlaufzeit der Implantatherstellung die korrekte Positionierung des Implantats beeinflussen. Um eine genaue Positionierung des Implantats gemäß dem präoperativen Plan zu gewährleisten, ist derzeit eine Überprüfung mittels intraoperativer Fluoroskopie erforderlich. Es wird auch erwartet, dass mit zunehmender Erfahrung die Präzision der Implantatpositionierung weiter auf unter 1-2 mm genaue Platzierung abnimmt. In Zukunft könnte die schablonengeführte Chirurgie mit 3D-gedruckten Bohrschablonen die Notwendigkeit einer Durchleuchtung überflüssig machen.
Diese Technik hat auch einige Einschränkungen. Bisherige Kurzzeitergebnisse deuten auf eine große Bandbreite unterschiedlicher Hüftanatomien hin, die mit 3DHIP-Implantaten behandelt werden können. Obwohl die Ergebnisse der Langzeitstudie noch nicht vorliegen, wird empfohlen, eine 3DHIP-Implantation bei Hunden in Betracht zu ziehen, die keine Anzeichen von Osteoarthritis (OA) zeigen oder nur einen leichten Grad an OA in ihren Hüftgelenken haben. Die 3DHIP-Implantatinsertion zielt darauf ab, das Fortschreiten der Verschlechterung des Hüftgelenks effektiv zu verlangsamen. Hunde mit luxoiden Hüften und mittelschwerer bis schwerer Hüftdegeneration, wie in der präoperativen Bewertung festgestellt, sollten ausgeschlossen werden.
Im Vergleich zur 3DHIP-Implantation stellen konventionelle Operationen zur Behandlung von Hüftdysplasie bei Hunden wie DPO/TPO größere Herausforderungen dar, insbesondere bei einem einstufigen bilateralen Eingriff und/oder bei Riesenhunden aufgrund ihres invasiven Charakters, der zwei oder drei Beckenosteotomien umfasst 5,6,7,26. Daher können Hunde mit beidseitiger Huntington-Krankheit von einer Hüftpfannenrandverlängerung mit einem 3DHIP-Implantat profitieren; Es bietet ein effektives und schonendes invasives einstufiges bilaterales Verfahren. Darüber hinaus hilft die 3DHIP-Implantation, wertvolle Zeit zu sparen und kann die weitere Entwicklung von OA verhindern, wie sie bei zweistufigen bilateralen Eingriffen auftreten kann.
Zusammenfassend lässt sich sagen, dass die Verwendung des vorgestellten 3DHIP-Implantats zur Verlängerung des dorsalen Hüftpfannenrand als vielversprechende alternative chirurgische Behandlung von Hüftdysplasie bei Hunden vielversprechend ist. Insbesondere die Möglichkeit, ein effektives und schonend invasives einstufiges bilaterales Verfahren für Hunde mit beidseitiger Hüftdysplasie und Laxität anzubieten, ist ein enormer Vorteil gegenüber den bisherigen alternativen Behandlungen. Eine weitere Überwachung dieser neuen Technik in der mittel- und langfristigen Nachbeobachtung ist obligatorisch.
Offenlegungen
Die Autoren haben keine Interessenkonflikte anzugeben. BM ist einer der fünf Erfinder des Verfahrens zur Herstellung eines Implantats zur Verlängerung des dorsalen Hüftpfannenrandes (2021), dessen Patent (EP3463198B1) an Rita Leibinger lizenziert wurde.
Danksagungen
Die vorliegende Studie wurde hauptsächlich von der Stiftung Vrienden Diergeneeskunde Universiteit Utrecht finanziell unterstützt; MT hat eine langfristige Finanzierung von der Dutch Arthritis Society (LLP22) erhalten; FV und JM werden durch Eurostars Project E115515 - 3DHIP finanziert. IK ist Stipendiat der Fakultät für Veterinärmedizin der Kasetsart University, Thailand.
Materialien
| Name | Company | Catalog Number | Comments |
| The laborotory for implant design | |||
| 3D Lab | University Medical Center Utrecht 3D, Utrecht, Netherlands | The laboratory responsible for designing the 3DHIP implant. [https://www.umcutrecht.nl/nl/3d-lab/] | |
| Software | |||
| 3-Matic software version 17 | Materialise, Leuven, Belgium | CT DICOM data processing | |
| Materialise Mimics software version 25.1 | Materialise, Leuven, Belgium | Software to design the 3DHIP implant on the 3D model of the pelvis | |
| Implant manufacturer | |||
| Amnovis | Amnovis, Aarschot, Belgium | Printing and postprocessing of the 3DHIP implant. [https://www.amnovis.com/] | |
| Instrument and machine | |||
| 2.4 LeiLOX locking screw titanium | Rita Leibinger, BW, Germany | 242-224 | Titanium self tapping locking screw 2.4 mm. |
| 2.7 LeiLOX locking screw titanium | Rita Leibinger, BW, Germany | 242-227 | Titanium self tapping locking screw 2.7 mm. |
| 3.5 LeiLOX locking screw titanium | Rita Leibinger, BW, Germany | 242-235 | Titanium self tapping locking screw 3.5 mm. |
| BLUE SEAL 100 x 360 mm | Interster, Wormerveer, Netherlands | 3FKFB210819 | The transparent sterilization laminate size 100 x 360 mm |
| ETHILON 3-0 with FS-1 needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | 669H | Polyamide 6 3-0 (non-absorbable suture material) with 24 mm 3/8c reverse cutting needle using for skin closure |
| Fluoroscopy model NZS 229 | Philips, Eindhoven, Netherlands | Fluoroscopy | |
| Foley Catheter 10 fr x 90 cm (36") with 3 cc Balloon | MILA international inc., Kentucky, USA | MLIUC1036 | Foley urine catheter size 10 fr |
| Foley Catheter 6 fr x 60 cm (24") with 3 cc Balloon | MILA international inc., Kentucky, USA | MLIUC624 | Foley urine catheter size 6 fr |
| Foley Catheter 8 fr x 90 cm (36") with 3 cc Balloon | MILA international inc., Kentucky, USA | MLIUC836 | Foley urine catheter size 8 fr |
| Ioban 2 | 3M, MN, USA | 6640EU | Iodine-impregnated surgical drape |
| Miele professional G 7826 | Miele Nederland B.V., Vianen, Netherlands | The hygienic washing machine | |
| MMM sterilizer OB10643 | MMM Group, Planegg, Germany | Steam autoclave | |
| MONOCRYL 2-0 with SH Plus needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | MCP3170H | Poliglecaprone 25 plus antibacterial 2-0 (absorbable suture material) with 26 mm 1/2c taperpoint needle using for subcutaneous tissue closure |
| MONOCRYL 3-0 with SH Plus needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | MCP3160H | Poliglecaprone 25 plus antibacterial 3-0 (absorbable suture material) with 26 mm 1/2c taperpoint needle using for subcutaneous tissue closure |
| PDS 0 with CP needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | PDP485H | Polydioxanone plus antibacterial 0 (absorbable suture material) with 40 mm 1/2c reverse cutting needle using for muscle fascia and tendon closure |
| PDS 2-0 with CP-1 needle | Johnson & Johnson Medical GmbH, Norderstedt, Germany | PDP466H | Polydioxanone plus antibacterial 2-0 (absorbable suture material) with 36 mm 1/2c reverse cutting needle using for muscle fascia and tendon closure |
| ProX DMP320 | 3D systems, South Carolina, USA | Direct metal printing machine using selective laser melting technology | |
| Medications | |||
| Betadine oplossing | Mylan B.V., Amstelveen, Netherlands | RVG 01331 | Povidone-iodine solution 100 mg/mL (500 mL) |
| Betadine shampoo | Mylan B.V., Amstelveen, Netherlands | RVG 08943 | Povidone-iodine 75 mg/mL (120 mL) |
| Carporal 20 mg | AST Farma B.V. Oudewater, Netherlands | REG NL 101766 | Carprofen 20 mg/tablet |
| Carporal 40 mg | AST Farma B.V. Oudewater, Netherlands | REG NL 115715 | Carprofen 40 mg/tablet |
| Carporal 50 mg | AST Farma B.V. Oudewater, Netherlands | REG NL 101767 | Carprofen 50 mg/tablet |
| Cefazolin Mylan 1 g | Mylan B.V., Amstelveen, Netherlands | RVG 16532 | Cefazolin powder 1 g for injection |
| Chlorhexidine 0.5% in alcohol 70% spray | Orphi Farma BV, Lage Zwaluwe, Netherlands | 8711407672906 | Chlorhexidine 0.5% in alcohol 70% spray (250 mL) |
| Dexdomitor 0.5 mg/mL | Orion Corporation, Espoo, Finland | EU/2/02/033/001-002 | Dexmedetomidine hydrochloride 0.5 mg/mL for injection (20 mL) |
| Gabapentin Sandoz 300 mg | Sandoz B.V., Almere, Netherlands | RVG 33681 | Gabapentin 300 mg/capsule |
| GABAPENTINE TEVA 100 mg | Teva B.V., Haarlem, Netherlands | RVG 31980 | Gabapentin 100 mg/capsule |
| HiBiScrub | Mölnlycke Health Care AB., Utrecht, Netherlands | RVG 10156 | Chlorhexidine digluconate 40 mg/mL (500 mL) |
| Insistor 10 mg/mL | Richter pharma AG, Oostenrijk, Netherlands | REG NL 121166 | Methadone hydrochloride 10 mg/mL for injection (10 mL) |
| Isoflutek 1000 mg/g | Laboratorios Karizoo S.A., Barcelona, Spain | REG NL 118938 | Isoflurane 1000 mg/g (250 mL) |
| Levobupivacaine Fresenius Kabi 2.5 mg/mL | Fresenius Kabi Nederland b.v., Huis ter Heide, Netherlands | AWA 0611 | Levobupivacaine 2.5 mg/mL solution for injection (10 mL) |
| Morfine HCI CF 10 mg/mL | Centrafarm B.V., Breda, Netherlands | RVG 50836 | Morphine hydrochloride 10 mg/mL (1 mL) |
| Narketan 10 | Vetoquinol B.V., Breda, Netherlands | vm08007/4090 | Ketamine 10 mg/mL (10 mL) |
| Propofol 10 mg/mL | Fresenius Kabi Nederland b.v., Huis ter Heide, Netherlands | RVG 110627 | Propofol 10 mg/mL emulsion for injection or infusion (50 mL) |
| Rimadyl | Zoetis B.V., Capelle a/d Ijssel, Netherlands | REG NL 10101 | Carprofen 50 mL/mL for injection (20 mL) |
| Sufentanil-hameln 50 mcg/mL | Hameln pharma gmbh, Hameln, Germany | 4260016653249 | Sufentanil citrate 50 mcg/mL for injection |
| Trazadone EG 100 mg | EG (Eurogenerics) NV Heizel, Brussel, Belgium | BE439607 | Trazadone hydrochloride 100 mg/tablet |
Referenzen
- King, M. D. Etiopathogenesis of canine hip dysplasia, prevalence, and genetics. Vet Clin North Am Small Anim Pract. 47 (4), 753-767 (2017).
- Akis, I., et al. The association of genetic polymorphisms of bone formation genes with canine hip dysplasia. Iran J Vet Res. 21 (1), 40-45 (2020).
- Loder, R. T., Todhunter, R. J. The demographics of canine hip dysplasia in the United States and Canada. J Vet Med. 2017, 1-15 (2017).
- Schachner, E. R., Lopez, M. J. Diagnosis, prevention, and management of canine hip dysplasia: a review. Vet Med (Auck)l. 6, 181-192 (2015).
- Vezzoni, A., Boiocchi, S., Vezzoni, L., Vanelli, A. B., Bronzo, V. Double pelvic osteotomy for the treatment of hip dysplasia in young dogs). Vet Comp Orthop Traumatol. 23 (6), 444-452 (2010).
- Tavola, F., Drudi, D., Vezzoni, L., Vezzoni, A. Postoperative complications of double pelvic osteotomy using specific plates in 305 dogs. Vet Comp Orthop Traumatol. 35 (1), 47-56 (2022).
- Koch, D. A., Hazewinkel, H. A. W., Nap, R. C., Meij, B. P., Wolvekamp, W. T. C. Radiographic evaluation and comparison of plate fixation after triple pelvic osteotomy in 32 dogs with hip dysplasia. Vet Comp Orthop Traumatol. 06 (01), 09-15 (1993).
- Rose, S. A., Bruecker, K. A., Petersen, S. W., Uddin, N. Use of locking plate and screws for triple pelvic osteotomy. Vet Surg. 41 (1), 114-120 (2012).
- Remedios, A. M., Fries, C. L. Implant complications in 20 triple pelvic osteotomies. Vet Comp Orthop Traumatol. 06 (04), 202-207 (1993).
- Moses, P. A. Alternative surgical methods for treating juvenile canine hip dysplasia. Aust Vet J. 78 (12), 822-824 (2000).
- Harper, T. A. M. Femoral head and neck excision. Vet Clin North Am Small Anim Pract. 47 (4), 885-897 (2017).
- Forster, K. E., et al. Complications and owner assessment of canine total hip replacement: a multicenter internet based survey. Vet Surg. 41 (5), 545-550 (2012).
- Volstad, N. J., Schaefer, S. L., Snyder, L. A., Meinen, J. B., Sample, S. J. Metallosis with pseudotumour formation: Long-term complication following cementless total hip replacement in a dog. Vet Comp Orthop Traumatol. 29 (4), 283-289 (2016).
- Nesser, V. E., Kowaleski, M. P., Boudrieau, R. J. Severe polyethylene wear requiring revision total hip arthroplasty in three dogs. Vet Surg. 45 (5), 664-671 (2016).
- Verhoeven, G., Fortrie, R., Van Ryssen, B., Coopman, F. Worldwide screening for canine hip dysplasia: where are we now. Vet Surg. 41 (1), 10-19 (2012).
- Willemsen, K., et al. Patient-specific 3D-printed shelf implant for the treatment of hip dysplasia: Anatomical and biomechanical outcomes in a canine model. J Orthop Res. 40 (5), 1154-1162 (2021).
- Willemsen, K., et al. Patient-specific 3D-printed shelf implant for the treatment of hip dysplasia tested in an experimental animal pilot in canines. Sci Rep. 12 (1), 3032 (2022).
- Kwananocha, I., et al. Acetabular rim extension using a personalized titanium implant for treatment of hip dysplasia in dogs: short-term results. Front Vet Sci. 10, 1160177 (2023).
- Van Der Wal, B. C. H., Sakkers, R. J. B., Meij, B. P., Evers, L. A. M., Weinans, H. H. . Method of manufacturing an implant. EP3463198B1. , (2021).
- Brainard, B. M., Hofmeister, E. H. Anesthesia principles and monitoring. Small Animal Surgery. , (2012).
- Martinez-Taboada, F., Redondo, J. I. Comparison of the hanging-drop technique and running-drip method for identifying the epidural space in dogs. Vet Anaesth Analg. 44 (2), 329-336 (2017).
- Johnson, K. A. Approach to the craniodorsal aspect of the hip joint through a craniolateral incision in the dog. Piermattei's Atlas of Surgical Approaches to the Bones and Joints of the dog and cat. , (2014).
- Whitelock, R. G., Dyce, J., Houlton, J. E. Repair of femoral trochanteric osteotomy in the dog. J Small Anim Pract. 38 (5), 195-199 (1997).
- Silveira, C. J., Saunders, W. B. Greater trochanter osteotomy as a component of cementless total hip replacement: Five cases in four dogs. Vet Surg. 51 (2), 303-310 (2022).
- Archibeck, M. J., Rosenberg, A. G., Berger, R. A., Silverton, C. D. Trochanteric osteotomy and fixation during total hip arthroplasty. J Am Acad Orthop Surg. 11 (3), 163-173 (2003).
- Vezzoni, A. Complications of double and triple pelvic osteotomies. Complications in Small Animal Surgery. , (2016).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten