Zum Anzeigen dieser Inhalte ist ein JoVE-Abonnement erforderlich. Melden Sie sich an oder starten Sie Ihre kostenlose Testversion.
Light-Sheet-Bildgebung zur Aufdeckung der Herzstruktur in Nagetierherzen
In diesem Artikel
Zusammenfassung
Das Protokoll nutzt fortschrittliche Lichtblattmikroskopie zusammen mit angepassten Gewebereinigungsmethoden, um komplizierte kardiale Strukturen in Nagetierherzen zu untersuchen, was ein großes Potenzial für das Verständnis der kardialen Morphogenese und des Umbaus birgt.
Zusammenfassung
Die Lichtblattmikroskopie (LSM) spielt eine entscheidende Rolle beim Verständnis der komplizierten dreidimensionalen (3D) Struktur des Herzens und liefert entscheidende Einblicke in die grundlegende Herzphysiologie und pathologische Reaktionen. Wir befassen uns mit der Entwicklung und Implementierung der LSM-Technik, um die Mikroarchitektur des Herzens in Mausmodellen aufzuklären. Die Methodik integriert ein maßgeschneidertes LSM-System mit Gewebereinigungstechniken, um die Lichtstreuung im Herzgewebe für die volumetrische Bildgebung zu verringern. Die Kombination von konventionellem LSM mit Image Stitching und Multiview-Dekonvolutionsansätzen ermöglicht die Erfassung des gesamten Herzens. Um den inhärenten Kompromiss zwischen axialer Auflösung und Sichtfeld (FOV) zu adressieren, führen wir außerdem eine axial gesweepte Lichtblattmikroskopie (ASLM) Methode ein, um unscharfes Licht zu minimieren und das Herz gleichmäßig über die Ausbreitungsrichtung zu beleuchten. In der Zwischenzeit verbessern Gewebereinigungsmethoden wie iDISCO die Lichtdurchdringung, erleichtern die Visualisierung tiefer Strukturen und gewährleisten eine umfassende Untersuchung des Myokards im gesamten Herzen. Die Kombination der vorgeschlagenen LSM- und Gewebereinigungsmethoden stellt eine vielversprechende Plattform für Forscher bei der Aufklärung kardialer Strukturen in Nagetierherzen dar, die ein großes Potenzial für das Verständnis der kardialen Morphogenese und des Umbaus birgt.
Einleitung
Herzinsuffizienz ist nach wie vor die häufigste Todesursache weltweit, was vor allem auf die mangelnde Regenerationsfähigkeit reifer Kardiomyozytenzurückzuführen ist 1. Die komplizierte Architektur des Herzens spielt eine entscheidende Rolle für seine Funktion und gibt Einblicke in Entwicklungsprozesse. Ein tiefgreifendes Verständnis der kardialen Struktur ist unerlässlich, um die grundlegenden Prozesse der kardialen Morphogenese und des Umbaus als Reaktion auf einen Myokardinfarkt aufzuklären. Jüngste Fortschritte haben gezeigt, dass neugeborene Mäuse die Herzfunktion nach einer Verletzung wiederherstellen können, während erwachsenen Mäusen eine solche Regenerationsfähigkeit fehlt2. Dies schafft eine Grundlage für die Untersuchung von Hinweisen, die mit strukturellen und funktionellen Anomalien in Mausmodellen verbunden sind. Herkömmliche bildgebende Verfahren wie die konfokale Mikroskopie weisen technische Einschränkungen auf, darunter eine begrenzte Eindringtiefe, ein langsames Punktabtastschema und Lichtschäden durch längere Exposition gegenüber Laserlicht. Diese behindern eine umfassende dreidimensionale (3D) Darstellung des intakten Herzens. In diesem Zusammenhang erweist sich die Lichtblattmikroskopie (LSM) als leistungsstarke Lösung, die die Vorteile einer Hochgeschwindigkeitsbildgebung, reduzierter Lichtschäden und außergewöhnlicher optischer Schnittmöglichkeiten bietet 3,4,5. Die einzigartigen Eigenschaften der LSM machen sie zu einer vielversprechenden Methode, um die Grenzen konventioneller Techniken zu überwinden und beispiellose Einblicke in die kardialen Entwicklungs- und Umbauprozesse zu bieten 6,7,8.
In diesem Protokoll stellen wir eine Bildgebungsstrategie vor, die fortschrittliches LSM mit angepassten Gewebereinigungsansätzen9 kombiniert und die Bildgebung ganzer Mausherzen ermöglicht, ohne dass eine spezifische Markierung und mechanische Schnitte erforderlich sind. Wir schlagen ferner vor, dass die konventionelle LSM-Bildgebung durch Multiview-Dekonvolution10 oder axial gesweepte Lichtblattmikroskopie (ASLM) Techniken 11,12,13,14,15 verbessert werden kann, um die axiale Auflösung zu verbessern. Darüber hinaus kann die Integration von Image Stitching mit einer dieser Methoden den Kompromiss zwischen räumlicher Auflösung und Sichtfeld (FOV) effektiv überwinden und so die Bildgebung von adulten Mausherzen verbessern. Die Einbeziehung zahlreicher Gewebereinigungsansätze, einschließlich hydrophober, hydrophiler und hydrogelbasierter Methoden, ermöglicht eine tiefere Lichteindringung zur Erfassung der Morphologie des gesamten Herzens 16,17,18,19.
Während mehrere Clearing-Methoden mit aktuellen LSM-Systemen kompatibel sind, besteht das Ziel darin, die Photonenstreuung zu minimieren und die Lichtdurchdringung in Geweben wie dem Herzen zu verbessern, indem Lipide durch ein Medium ersetzt werden, das seinem Brechungsindex sehr nahe kommt. iDISCO wurde als Vertreter20,21 ausgewählt und aufgrund seiner schnellen Verarbeitung und hohen Transparenz für die Autofluoreszenzbildgebung in diesem Protokoll angepasst (Abbildung 1A). Insgesamt bietet die Integration des fortschrittlichen LSM-Ansatzes mit Gewebereinigungstechniken einen vielversprechenden Rahmen, um die komplizierte Herzanatomie in Nagetierherzen zu entschlüsseln, was ein erhebliches Potenzial für die Verbesserung unseres Verständnisses der kardialen Morphogenese und Pathogenese birgt.
Protokoll
Tierversuche und -versuche wurden genehmigt und unter der Aufsicht des Institutional Animal Care and Use Committee der University of Texas in Dallas (IACUC #21-03) durchgeführt. In dieser Studie wurden C57BL6-Mäuse, einschließlich Neugeborene am postnatalen Tag 1 (P1) und 8 Wochen alte Erwachsene, verwendet. Es wurde kein Unterschied zwischen Männchen und Weibchen beobachtet. Die gesamte Datenerfassung und Bildnachbearbeitung erfolgte mit Open-Source-Software oder Plattformen mit Forschungs- oder Bildungslizenzen. Die Ressourcen sind auf begründete Anfrage bei den Autoren erhältlich.
1. Probenvorbereitung und Gewebereinigung (6 - 10 Tage)
- Bereiten Sie alle chemischen Lösungen in der Materialtabelle vor, die für die Gewebereinigungsmethode erforderlich sind, bevor Sie mit der Gewebereinigung beginnen.
HINWEIS: Führen Sie alle Verfahren in einem Abzug mit geeigneter persönlicher Schutzausrüstung durch, insbesondere beim Umgang mit giftigen Chemikalien. - Tiere mit CO2 einschläfern, indem sie zu den gewünschten Zeitpunkten, wie P1 und 8 Wochen, in eine CO2 -Kammer gelegt werden, um das ganze Herz zu entnehmen, und das frisch isolierte Herz bei Raumtemperatur (RT) in 0,2 M KCl tauchen, um es in Diastole16 zu verhaften.
- Fixieren Sie das Herz, indem Sie über Nacht in 4% Paraformaldehyd (PFA) in 1x phosphatgepufferte Kochsalzlösung (PBS) unter leichtem Rühren auf einer Wippe eintauchen, um die Herzanatomie bei 4 °C zu erhalten, siehe Tabelle 1.
ACHTUNG: PFA ist eine giftige Chemikalie und sollte unter einem Abzug durchgeführt werden. - Waschen Sie das Herz mit 1x PBS bei RT für 30 min, 3x.
HINWEIS: Optional: Betten Sie das Herz in Agarosegel ein, um eine Herzanordnung für das individuell angefertigte LSM-System in Schritt 2 zu erstellen, wie unten beschrieben.- Bereiten Sie die 1%ige Agaroselösung vor, indem Sie Agarose in PBS auflösen und die Mischung in der Mikrowelle erhitzen, bis sie vollständig aufgelöst ist. Gießen Sie die Lösung in eine Form, um eine untere Schicht zu bilden, bis die Lösung auf 40 °C abgekühlt ist.
- Lege das Herz in die Form und fülle die Form mit Agarosegel, bis es fest wird. Beseitigen Sie alle Blasen im Agarose-Gel, um Artefakte in der Bildgebung zu minimieren.
HINWEIS: Das Einbetten der Probe verringert das Risiko einer möglichen Schädigung der Herzanatomie während der Montage.
VORSICHT: Verwenden Sie Agarose mit niedrigem Schmelzpunkt und vermeiden Sie es, das Herz direkt in erhitzte Agarose zu legen, um das Risiko zu verringern, dass die Probe erhöhten Temperaturen ausgesetzt wird.
- Dehydrieren Sie das Herz mit Gradienten von Methanol, gemischt mit deionisiertem Wasser (Abbildung 1B), und verarbeiten Sie es durch sequenzielle Konzentrationen von 20 %, 40 %, 60 %, 80 % und 100 %, wie in Tabelle 1 beschrieben. Wiederholen Sie den Vorgang 1x mit frischem 100% Methanol, um eine vollständige Dehydrierung zu gewährleisten. Dehydrieren Sie die Herzen von neugeborenen Mäusen für 1 h in jeder Methanolmischung unter Schütteln. Stellen Sie die Inkubationszeit für 8 Wochen alte Mäuseherzen und Rattenherzen auf 2 Stunden ein.
ACHTUNG: Methanol ist eine flüchtige, reizende und brennbare Chemikalie. - Das Herz durch frisches 100%iges Methanol ersetzen und 10 min bei 4 °C kalt stellen.
- Ersetzen Sie die Lösung und bleichen Sie das Herz mit 5 % Wasserstoffperoxid (H2O2) in Methanol in einem Volumenverhältnis von 1:5 (30 % H2O2 bis 100 % Methanol) über Nacht bei 4 °C, um die Pigmente zu entfernen.
HINWEIS: Die Entfernung von Pigmenten ermöglicht eine Minimierung der Photonenabsorption, was zu einer verbesserten Bildqualität mit weniger Artefakten führt. - Ersetzen Sie die Lösung und inkubieren Sie das Herz 1 h lang in 100% Methanol bei RT.
- Entfetten Sie das Herz mit der Lösung, die 66 % Dichlormethan (DCM) und 33 % Methanol enthält, für 3 h unter Schütteln. Stellen Sie sicher, dass das Herz am Ende dieses Schritts auf den Boden der Durchstechflasche sinkt. Wenn nicht, erneuern Sie die Lösung (66 % DCM / 33 % Methanol) und verlängern Sie die Inkubationszeit (z. B. 1 weitere Stunde), um eine vollständige Entfettung zu erreichen. Übertragen Sie das Herz schnell in eine frische Lösung, um ein Austrocknen zu verhindern, da DCM sehr flüchtig ist.
ACHTUNG: Verwenden Sie für das Experiment Polypropylen oder Glaswaren, da DCM nicht mit Polystyrol kompatibel ist. - Verwendung von Dibenzylether (DBE) für die Anpassung des Brechungsindex (RI = 1,56). Bei neugeborenen Mäuseherzen dauert der Prozess des Brechungsindexabgleichs 2 Tage, während er bei 8 Wochen alten Mäuseherzen 5 Tage bei leichtem Schütteln dauert. Ersetzen Sie es durch frisches DBE und verlängern Sie die Inkubationszeit, bis das Herz vollständige Transparenz erreicht.
ACHTUNG: DBE ist gefährlich. Vermeiden Sie jeglichen Kontakt mit der Haut.
2. Montage der Probe (1 Tag)
HINWEIS: Falls ein kommerzielles LSM-System verwendet wird, befolgen Sie das vom Unternehmen bereitgestellte spezifische Protokoll, um das Herz zu reparieren, und überspringen Sie die Schritte 2.1 - 2.9.
- Passen Sie eine Kammer und einen Halter an, die gegen die Brechungsindex-Anpassungslösung (z. B. DBE im angepassten iDISCO-Ansatz) resistent sind, indem Sie einen 3D-Drucker und Onyx-Materialien verwenden (Abbildung 2A)16.
- Befestigen Sie einen Magneten am Boden der Kammer, um eine schnelle Verbindung und genaue Lokalisierung unter dem LSM-System zu ermöglichen (Abbildung 2B).
- Befestigen Sie 25 mm x 50 mm x 0,17 mm große Deckgläser mit transparentem Silikonkleber an der Kammer und überprüfen Sie die Wasserdichtigkeit der Kammer, indem Sie sie mit DBE füllen und nach 1 Tag auf Undichtigkeiten prüfen.
- Passen Sie einen Klemmhalter mit einem 3D-Drucker an und befestigen Sie einen Magneten zur Befestigung der Herzbaugruppe in der Kammer (Abbildung 2C) oder führen Sie eine Nadel in das Agarosegel ein, um die Herzbaugruppe zu befestigen.
- Durchführung der Entwicklung eines hauseigenen LSM-Systems unter Verwendung einer zylindrischen Linse und diodengepumpter Festkörperlaser (DPSS) mit kontinuierlicher Welle, wie bereits berichtet16,22. Verwenden Sie die Anregungswellenlänge von 532 nm, um die Autofluoreszenz aus dem Myokard einzufangen (Abbildung 2D).
- Montieren Sie die Kammer auf einem 6-dimensionalen Tisch und lokalisieren Sie die optimale Position, an der die Kammer senkrecht zur Richtung der Laserausbreitung steht.
- Verwenden Sie einen magnetischen Klemmhalter, um die Probe in der Mitte der Kammer zu positionieren, und verbinden Sie den Halter mit einem 4-dimensionalen motorisierten Tisch (X, Y, Z und Gier; Abbildung 2D).
- Tauchen Sie die Herzbaugruppe mit Hilfe des motorisierten Tisches in die mit DBE gefüllte Kammer ein und bestimmen Sie den Scanbereich entlang der Erfassungsachse (Z-Richtung).
- Bestimmen Sie die Abtastgeschwindigkeit (Vz) des Motors entlang der Z-Richtung basierend auf der Schrittweite (S) und der Erfassungszeit eines Bildes (T) mit der folgenden Gleichung:
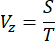
HINWEIS: Die Beziehung zwischen der Schrittweite und der axialen Auflösung des Bildgebungssystems entspricht dem Nyquist-Shannon-Abtasttheorem. So wurde beispielsweise die Schrittweite auf 1 μm festgelegt, da die axiale Auflösung 2,91 μm betrug, wie im vorherigen Bericht16 angegeben. - Um die räumliche Auflösung zu überprüfen und potenzielle Opazitätsprobleme in verschiedenen Tiefen zu minimieren, messen Sie die Punktspreizfunktion (PSF) des Systems, indem Sie fluoreszierende Kügelchen mit einem Durchmesser von 0,53 μm abbilden, die in 1 % Agarosegel mit niedrigem Schmelzpunkt mit einer Konzentration von 1:1,5 x 105 verdünnt sind. Berechnen Sie den PSF über die gesamte Probe, indem Sie die volle Breite bei halbem Maximum (FWHM)16 messen.
3. Bild-Stitching (4-8 h)
- Berechnen Sie die Anzahl der Kacheln, die erforderlich sind, um das gesamte Mausherz unter Berücksichtigung des begrenzten Sichtfelds zu bedecken. Für jede Fliese entsprechen die Abmessungen dem Sichtfeld des LSM-Systems. Für ein neonatales Mausherz mit einem Querschnittsmaß von 3 x 3,6 mm2 sind beispielsweise 2 x 2 Kacheln für die Abdeckung im personalisierten LSM erforderlich (Abbildung 3A). Im Gegensatz dazu benötigt ein 8 Wochen altes Mausherz mit den Maßen 5 x 8 mm2 3 x 4 Kacheln, um die gesamte Herzstruktur abzudecken (Abbildung 3B).
HINWEIS: Ein Bild-Stitching ist erforderlich, wenn das herkömmliche LSM ein begrenztes Sichtfeld für die Abbildung des gesamten Herzens hat. - Nehmen Sie Bilder des Herzens auf, beginnend mit Kachel 1, d. h. der Kachel in der oberen linken Ecke des Herzens (Abbildung 3A-B).
- Erfassen Sie sequenziell Bilder der verbleibenden Kacheln mit einer Überlappung von 10 % zwischen aufeinanderfolgenden Kacheln, bis das gesamte Herz bedeckt ist, wie in Abbildung 3C dargestellt.
- Laden Sie die Open-Source-Software Fiji23 herunter und installieren Sie sie. Laden Sie das Fidschi-Plugin BigStitcher24 herunter und installieren Sie es.
- Navigieren Sie zum Menü Hilfe, wählen Sie Update, wählen Sie Manage update site (Update-Site verwalten) und entscheiden Sie sich für BigStitcher. Klicken Sie anschließend auf Schließen, gefolgt von Änderungen übernehmen. Nachdem Sie den Plugin-Download abgeschlossen haben, starten Sie die Fiji-Software neu.
- Öffnen Sie das BigStitcher-Plugin und importieren Sie alle erforderlichen Kacheln über das Bilddateiverzeichnis. Speichern Sie das Dataset als HDF5-Datei.
- Organisieren Sie Kacheln, indem Sie Kachel nach regulärem Raster verschieben auswählen, wählen Sie das Muster aus, das zum Verschieben des Herzens verwendet wird, und wählen Sie eine Überlappung von 10 % zwischen den einzelnen Kacheln aus. Fügen Sie die Kacheln mit der Option Stickassistent zusammen.
- Exportieren Sie die zusammengefügten Daten mit Image Fusion, um eine TIFF-Datei zu generieren.
4. Multiview-Dekonvolution (5 Tage)
- Verwenden Sie fluoreszierende Kügelchen für die Bildregistrierung von Multiview-Rekonstruktionen entlang des Herzens (Abbildung 3D).
- Das Harz25 wird durch Mischen von Bisphenol-A-Diglycidylether (D.E.R. 332), Isophorondiamin, 5-Amino-1,3,3-trimethylcyclohexanmethylamin (IPDA) und Polypropylenglykoldiglycidylether (D.E.R. 736) in einem Volumenverhältnis von 4:1:1 hergestellt.
- Zentrifugieren Sie 10 μl Fluoreszenzkügelchen bei 161 x g für 5 min und fügen Sie 20 μl Methanol hinzu, um die Lagerlösung der Kügelchen zu ersetzen. Wiederholen Sie es 3x.
- Bereiten Sie eine 10 mL Lösung mit einer Konzentration von 1:1 x 105 Kügelchen vor, indem Sie die Bead-Lösung auf Methanolbasis in das in Schritt 4.1.1 hergestellte Harz mischen.
- Entgasen Sie die Lösung 3 h lang in einer Vakuumkammer, um Lufteinschlüsse und Blasen zu entfernen.
- Gießen Sie die Lösung in eine Silikonform oder einen Plastiktrinkhalm und warten Sie 2 bis 3 Tage, bis sie sich verfestigt hat. Nach 1 Tag, bevor das Harz fest wird, legen Sie das Glasrohr in die Form und warten Sie, bis das Rohr am Harz befestigt ist. Entfernen Sie das Harz mit dem Glasrohr aus der Form (Abbildung 3D).
- Lege das Herz in das Glasrohr, fülle es mit DBE und setze das Glasrohr in die mit DBE gefüllte Kammer ein.
- Erfassen Sie sequenzielle Bilder des Mausherzens zusammen mit den Kügelchen aus dem beleuchteten Bereich, indem Sie die Herzanordnung über die Erkennungsachse (Z-Achse; Abbildung 3E-F).
HINWEIS: Implementieren Sie das Bild-Stitching in Schritt 3, um einzelne Bildstapel zu generieren, wenn die Herzgröße das Sichtfeld überschreitet. - Drehen Sie das Mausherz um 60° entlang der Y-Achse, um nachfolgende Stapel aus mehreren Winkeln zu erfassen, z. B. 0°, 60°, 120°, 180°, 240° und 300° (Abbildung 3E-F).
- Öffnen Sie das BigStitcher-Plugin und importieren Sie alle Bilder über das Bilddateiverzeichnis. Speichern Sie das Dataset als HDF5-Datei.
- Wählen Sie Detect Interest Points (Interessenpunkte erkennen) und wählen Sie manuell die für die Registrierung interessanten Perlen aus.
- Wählen Sie Affines Transformationsmodell für die Registrierung aus. Wählen Sie Punktspreizungsfunktion und ordnen Sie PSF allen Ansichten zu.
- Klicken Sie auf Multiview-Dekonvolution und wählen Sie den Iterationstyp als Effizient Bayesian. Definieren Sie die Anzahl der Iterationen als 10 und führen Sie sie26 aus.
- Klicken Sie auf Image Fusion , um eine TIFF-Datei zu exportieren.
HINWEIS: Detailliertere Informationen zur Multiview-Dekonvolution finden Sie in anderen Berichten oder Protokollen 24,27,28.
5. Axial gesweepte Light-Sheet-Systemhardware (1 Tag)
- Installieren Sie eine elektrisch abstimmbare Linse (ETL) auf der Fourierebene der Zylinderlinse (CL)27 (Abbildung 2D), um den Laserstrahl axial abzutasten14. Stellen Sie sicher, dass die Flüssigkeitsgrenzfläche in ETL horizontal ist, um eine durch die Schwerkraft verursachte Wellenfrontverzerrung zu vermeiden. Richten Sie ETL präzise aus, um die Dezentrierung des Strahls und optische Aberrationen höherer Ordnungzu minimieren 30.
- Installieren Sie eine Datenerfassungskarte in der Workstation und schließen Sie ein BNC-Kabel an die Datenerfassungskarte an, um die Kamerabelichtung und das ETL-Scannen zu synchronisieren.
- Öffnen Sie das Gehäuse des ETL-Treibers, und entfernen Sie die Abdeckung (Abbildung 4).
- Löten Sie das Signalkabel des BNC-Kabels an den Analog-In-B-Pin, wie auf der Unterseite der Leiterplatte beschriftet (Abbildung 4).
- Löten Sie das Erdungskabel des BNC-Kabels an den GND-Pin; Verbinden Sie anschließend das andere Ende des BNC-Kabels mit dem AO (Analogausgang) in der Datenerfassungskarte (Abbildung 4).
- Schließen Sie den ETL-Treiber an den USB-Anschluss der Workstation an, verbinden Sie den Treiber über ein Hirose-Kabel mit dem ETL und installieren Sie die Lens Driver Controller Software.
- Ändern Sie den Betriebsmodus in der Lens Driver Controller-Software auf Analog, um das ETL mit einem von der Datenerfassungskarte generierten Trigger zu steuern.
- Schalten Sie in der Software der sCMOS-Kamera den Aufnahmemodus auf Extern (Lightsheet). Stellen Sie sicher, dass die aktive Pixelscanrichtung senkrecht zur Laserscanrichtung verläuft, um die Synchronisierung zu unterstützen.
- Verbinden Sie den externen Trigger-Port auf der Rückseite der sCMOS-Kamera über ein BNC-Kabel mit dem AO der Messkarte (Abbildung 4).
6. Synchronisierung des axial gesweepten Lichtblattsystems (7 Tage)
- Definieren Sie die Expositionszeit auf der Grundlage des akzeptablen Signal-Hintergrund-Verhältnisses (SBR), das für die vorgeschlagene Studie mindestens 10 beträgt. Erhöhen Sie die Belichtungszeit, wenn die SBR kleiner als 10 ist.
HINWEIS: Die Belichtungszeit von 10 bis 50 ms bietet in diesem Projekt einen akzeptablen SBR. - Definieren Sie die Erfassungszeit eines Bildes (T) und das Zeilenintervall (L) basierend auf der Belichtungszeit (E) für die Kamera und der ETL-Frequenz (f) mit den folgenden Gleichungen:
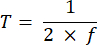
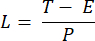
Dabei gibt P die Anzahl der Pixelspalten auf dem Kamerasensor an. Die repräsentativen Parameter für die Referenz sind f = 1 Hz, P = 2048, E = 10 ms bzw. L = 243 μs. - Im LabVIEW-Programm generiert Trigger Generator.vi sowohl quadratische als auch dreieckige Trigger für die Synchronisation (Abbildung 5).
HINWEIS: Das angepasste LabVIEW-Programm ist auf Anfrage bei den Autoren erhältlich. - Montieren Sie fluoreszierende Kügelchen, die in 1 % Agarosegel16 mit einem niedrigen Schmelzpunkt verdünnt sind, mit einer Konzentration von 1:1 x 103 , um die Position der Strahltaille im Bild zu lokalisieren (Abbildung 6A).
- Identifizieren Sie im Programm den Start- und Endpunkt des Laserstrahls unter dem Sichtfeld, indem Sie die Spannung entlang der Abtastrichtung ändern.
- Um die sCMOS-Kamera und ETL zu synchronisieren, scannen Sie den Laserstrahl entlang der X-Achse und die aktiven Pixel entlang der Y-Achse, um ein 2D-Bild zu erzeugen (Abbildung 6B). Die helleren und schärferen Perlen entlang der Diagonale im Bild zeigen die genaue Synchronisation zwischen sCMOS und ETL an.
HINWEIS: Die Synchronisierung der Scangeschwindigkeit von ETL- und sCMOS-Pixelaktivierung ist entscheidend für die Bildqualität. Verschiedene häufige asynchrone Fehler sind in Abbildung 6C-F zusammengefasst. - Nachdem Sie die optimalen Synchronisationsparameter für die Synchronisation bestimmt haben, drehen Sie die sCMOS-Kamera um 90° um die Z-Achse, um die aktive Pixelrichtung an der Laserscanrichtung auszurichten.
- Wiederholen Sie Schritt 2.10, und messen Sie den FWHM der PSF. Es ist die gleiche Methode wie im vorherigen Bericht16 anzugeben, wobei die gemittelte laterale und axiale Auflösung von ASLM 2,18 μm bzw. 2,88 μm beträgt (Abbildung 7).
HINWEIS: Eine gleichmäßige Beleuchtung und Auflösung über das gesamte Sichtfeld sind unter idealen Bedingungen möglich (Abbildung 7A-B). Der asynchrone Betrieb des ETL mit der sCMOS-Kamera sowie eine Fehlausrichtung der Beleuchtung und Detektion können zu einer ungleichmäßigen räumlichen Auflösung führen (Abbildung 7C-D). - Für die kardiale Bildgebung fahren Sie nach dem Ausrichten des Systems und der Bestimmung der optimalen Parameter für die Systemsynchronisation mit den Schritten 2.6 bis 2.9 fort.
Ergebnisse
Es wurde gezeigt, dass LSM im Gegensatz zu anderen optischen Bildgebungsverfahren wie Hellfeld- und Punktscantechniken kardiale Studien fördert 31,32,33,34,35,36,37 aufgrund des minimalen Risikos von Lichtschäden, der hohen räumlichen Auflösung und der optischen Schnittbildung
Diskussion
Die Weiterentwicklung von Bildgebungs-, Berechnungs- und Gewebereinigungsmethoden hat eine beispiellose Gelegenheit geboten, die Struktur und Funktion des Herzens umfassend zu untersuchen. Dies birgt ein großes Potenzial für die Vertiefung unseres Verständnisses der kardialen Morphogenese und Pathogenese anhand eines intakten Nagetierherzmodells. Im Gegensatz zu In-vivo-Studien an Zebrafischherzen mit einem ähnlichen Ansatz 40,41,42,43 ermöglicht uns die Integration fortschrittlicher LSM-Techniken und Geweb...
Offenlegungen
Die Autoren haben keinen Interessenkonflikt offenzulegen.
Danksagungen
Wir danken der Gruppe von Dr. Eric Olson am UT Southwestern Medical Center für die großzügige Bereitstellung der Tiermodelle. Wir schätzen alle konstruktiven Kommentare von D-Inkubator-Mitgliedern an der UT Dallas. Diese Arbeit wurde von NIH R00HL148493 (Y.D.), R01HL162635 (Y.D.) und dem UT Dallas STARS-Programm (Y.D.) unterstützt.
Materialien
| Name | Company | Catalog Number | Comments |
| 1% Agarose | |||
| Low melting point agarose | Thermo Fisher | 16520050 | |
| Deionized water | - | - | |
| Chemicals for tissue clearing | |||
| 5-Amino-1,3,3-trimethylcyclohexanemethylamine, mixture of cis and trans | Sigma-Aldrich | 118184 | |
| D.E.R.™ 332 | Sigma-Aldrich | 31185 | |
| D.E.R.™ 736 | Sigma-Aldrich | 31191 | |
| Dibenzyl ether (DBE) | Sigma-Aldrich | 33630 | |
| Dichloromethane (DCM) | Sigma-Aldrich | 270997 | |
| Fluorescent beads | Spherotech | FP-0556-2 | |
| Hydrogen peroxide (H2O2) | Sigma-Aldrich | 216736 | |
| Methanol | Sigma-Aldrich | 439193 | |
| Paraformaldehyde (PFA) | Thermo Fisher | 47392 | |
| Phosphate Buffered Saline (PBS) | Sigma-Aldrich | 79383 | |
| Potassium Chloride (KCl) | Sigma-Aldrich | P3911 | |
| Software and algorithms | |||
| Amira | Thermo Fisher Scientific | 2021.2 | |
| BigStitcher | Hörl et al.22 | ||
| Fiji-ImageJ | Schindelin et al.20 | 1.54f | |
| HCImage Live | Hamamatsu Photonics | 4.6.1.2 | |
| LabVIEW | National Instruments Corporation | 2017 SP1 | |
| Key components of the customized light-sheet system | |||
| 0.63 - 6.3X Zoom body | Olympus | MVX-ZB10 | |
| 10X Illumination objective | Nikon | MRH00105 | |
| 1X detection objective | Olympus | MV PLAPO 1X/0.25 | |
| 473nm DPSS Laser | Laserglow Technologies | LRS-0473-PFM-00100-05 | |
| 532nm DPSS laser | Laserglow Technologies | LRS-0532-PFM-00100-05 | |
| 589 nm DPSS laser | Laserglow Technologies | LRS-0589-GFF-00100-05 | |
| BNC connector | National Instrument | BNC-2110 | |
| Cylindrical lens | Thorlabs | ACY254-050-A | |
| DC-Motor Controller, 4 axes | Physik Instrumente | C-884.4DC | |
| ETL | Optotune | EL-16-40-TC-VIS-5D-1-C | |
| ETL Cable | Optotune | CAB-6-300 | |
| ETL Lens Driver | Optotune | EL-E-4i | |
| Filter | Chroma | ET525/30 | |
| Filter | Chroma | ET585-40 | |
| Filter | Chroma | ET645-75 | |
| Filter wheel | Shutter Instrument | LAMBDA 10-B | |
| Motorized translation stage | Physik Instrumente | L-406.20DG10 | |
| Motorized translation stage | Physik Instrumente | L-406.40DG10 | |
| Motorized translation stage | Physik Instrumente | M-403.4PD | |
| NI multifunction I/O | National Instrument | PCIe-6363 | |
| sCMOS camera | Hamamatsu | C13440-20CU | |
| Stepper motor | Pololu | 1474 | |
| Tube lens | Olympus | MVX-TLU |
Referenzen
- Sadek, H., Olson, E. N. Toward the goal of human heart regeneration. Cell Stem Cell. 26, 7-16 (2020).
- Porrello, E. R., et al. Transient regenerative potential of the neonatal mouse heart. Science. 331, 1078-1080 (2011).
- Stelzer, E. H. K. K., et al. Light sheet fluorescence microscopy. Nat Rev Methods Prim. 1, 73 (2021).
- Girkin, J. M., Carvalho, M. T. The light-sheet microscopy revolution. J Opt. 20, 053002 (2018).
- Power, R. M., Huisken, J. A guide to light-sheet fluorescence microscopy for multiscale imaging. Nat Methods. 14, 360-373 (2017).
- Ding, Y., et al. Multiscale light-sheet for rapid imaging of cardiopulmonary system. JCI Insight. 3, e121396 (2018).
- Ding, Y., et al. Light-sheet fluorescence imaging to localize cardiac lineage and protein distribution. Sci Rep. 7, 42209 (2017).
- Fei, P., et al. Cardiac light-sheet fluorescent microscopy for multi-scale and rapid imaging of architecture and function. Sci Rep. 6, 1-12 (2016).
- Richardson, D. S., Lichtman, J. W. Clarifying tissue clearing. Cell. 162, 246-257 (2015).
- Stelzer, E. H. K., Huisken, J., Swoger, J., Greger, K., Verveer, P. Multi-view image fusion improves resolution in three-dimensional microscopy. Opt Express. 15 (13), 8029-8042 (2007).
- Dean, K. M., Roudot, P., Welf, E. S., Danuser, G., Fiolka, R. Deconvolution-free subcellular imaging with axially swept light sheet microscopy. Biophys J. 108, 2807-2815 (2015).
- Dean, K. M., et al. Isotropic imaging across spatial scales with axially swept light-sheet microscopy. Nat Protoc. 17, 2025-2053 (2022).
- Hedde, P. N., Gratton, E. Selective plane illumination microscopy with a light sheet of uniform thickness formed by an electrically tunable lens. Microsc Res Tech. 81, 924 (2018).
- Voigt, F. F., et al. The mesoSPIM initiative: open-source light-sheet microscopes for imaging cleared tissue. Nat Meth. 16, 1105-1108 (2019).
- Giardini, F., et al. Mesoscopic optical imaging of whole mouse heart. J Vis Exp. (176), e62795 (2021).
- Sodimu, O., et al. Light sheet imaging and interactive analysis of the cardiac structure in neonatal mice. J Biophotonics. 16, e202200278 (2023).
- Ariel, P. A beginner's guide to tissue clearing. Int J Biochem Cell Biol. 84, 35-39 (2017).
- Richardson, D. S., et al. Tissue clearing. Nat Rev Methods Prim. 1, 1-24 (2021).
- Ueda, H. R., et al. Tissue clearing and its applications in neuroscience. Nat Rev Neurosci. 21, 61-79 (2020).
- Renier, N., et al. iDISCO: a simple, rapid method to immunolabel large tissue samples for volume imaging. Cell. 159, 896-910 (2014).
- Kirchner, K. N., et al. A hydrophobic tissue clearing method for rat brain tissue. J Vis Exp. (166), e61821 (2020).
- Ding, Y., et al. Light-sheet fluorescence microscopy for the study of the murine heart. J Vis Exp. (139), e57769 (2018).
- Schindelin, J., Rueden, C. T., Hiner, M. C., Eliceiri, K. W. The ImageJ ecosystem: An open platform for biomedical image analysis. Mol Reprod Dev. 82, 518-529 (2015).
- Hörl, D., et al. BigStitcher: reconstructing high-resolution image datasets of cleared and expanded samples. Nat Methods. 16, 870-874 (2019).
- Becker, K., et al. Reduction of Photo Bleaching and Long Term Archiving of Chemically Cleared GFP-Expressing Mouse Brains. PLoS One. 9, e114149 (2014).
- Preibisch, S., et al. Efficient Bayesian-based multiview deconvolution. Nat. Methods. 11, 645-648 (2014).
- Guo, M., et al. Rapid image deconvolution and multiview fusion for optical microscopy. Nat. Biotechnol. 38, 1337-1346 (2020).
- Tomer, R., Khairy, K., Amat, F., Keller, P. J. Quantitative high-speed imaging of entire developing embryos with simultaneous multiview light-sheet microscopy. Nat Methods. 9, 755-763 (2012).
- Fahrbach, F. O., Voigt, F. F., Schmid, B., Helmchen, F., Huisken, J. Rapid 3D light-sheet microscopy with a tunable lens. Opt Express. 21, 21010-21026 (2013).
- Liu, Y., Rollins, A. M., Jenkins, M. W. CompassLSM: axially swept light-sheet microscopy made simple. Biomed Opt Express. 12, 6571-6589 (2021).
- Kolesová, H., Olejníčková, V., Kvasilová, A., Gregorovičová, M., Sedmera, D. Tissue clearing and imaging methods for cardiovascular development. iScience. 24 (4), 102387 (2021).
- Sands, G. B., et al. It's clearly the heart! Optical transparency, cardiac tissue imaging, and computer modelling. Prog Biophys Mol Biol. 168, 18-32 (2022).
- Wilson, A. J., Sands, G. B., LeGrice, I. J., Young, A. A., Ennis, D. B. Muscle mechanics and ventricular function: Myocardial mesostructure and mesofunction. Am J Physiol - Hear Circ Physiol. 323, H257 (2022).
- Lee, S. E., et al. Three-dimensional cardiomyocytes structure revealed by diffusion tensor imaging and its validation using a tissue-clearing technique. Sci. Reports. 8, 1-11 (2018).
- Sereti, K. I., et al. Analysis of cardiomyocyte clonal expansion during mouse heart development and injury. Nat Commun. 9, 754 (2018).
- Olianti, C., et al. 3D imaging and morphometry of the heart capillary system in spontaneously hypertensive rats and normotensive controls. Sci. Reports. 10, 1-9 (2020).
- Olianti, C., et al. Optical clearing in cardiac imaging: A comparative study. Prog Biophys Mol Biol. 168, 10-17 (2022).
- Baek, K. I., et al. Advanced microscopy to elucidate cardiovascular injury and regeneration: 4D light-sheet imaging. Prog Biophys Mol Biol. 138, 105-115 (2018).
- Merz, S. F., et al. Contemporaneous 3D characterization of acute and chronic myocardial I/R injury and response. Nat Commun. 10, 1-14 (2019).
- Zhang, X., et al. 4D Light-sheet imaging and interactive analysis of cardiac contractility in zebrafish larvae. APL Bioeng. 7, 26112 (2023).
- Lee, J., et al. 4-Dimensional light-sheet microscopy to elucidate shear stress modulation of cardiac trabeculation. J Clin Invest. 126, 1679-1690 (2016).
- Zhang, X., Alexander, R. V., Yuan, J., Ding, Y. Computational Analysis of Cardiac Contractile Function. Curr Cardiol Rep. 24, 1983-1994 (2022).
- Zhang, X., et al. 4D Light-sheet Imaging of Zebrafish Cardiac Contraction. J Vis Exp. (203), e66263 (2024).
- Huisken, J., Swoger, J., Del Bene, F., Wittbrodt, J., Stelzer, E. H. K. K. Optical sectioning deep inside live embryos by selective plane illumination microscopy. Science. 305, 1007-1009 (2004).
- Molbay, M., Kolabas, Z. I., Todorov, M. I., Ohn, T., Ertürk, A. A guidebook for DISCO tissue clearing. Mol Syst Biol. 17, 9807 (2021).
- Chi, J., Crane, A., Wu, Z., Cohen, P. Adipo-clear: a tissue clearing method for three-dimensional imaging of adipose tissue. J Vis Exp. (137), e58271 (2018).
- Wan, Y., McDole, K., Keller, P. J. Light-sheet microscopy and its potential for understanding developmental processes. Ann Rev Cell Dev Biol. 35, 655-681 (2019).
- Yuan, J., et al. Extended reality for biomedicine. Nat Rev Methods Prim. 3, 1-1 (2023).
- Ding, Y., et al. Saak transform-based machine learning for light-sheet imaging of cardiac trabeculation. IEEE Trans Biomed Eng. 68, 225-235 (2020).
- Buffinton, C. M., Benjamin, A. K., Firment, A. N., Moon, A. M. Myocardial wall stiffening in a mouse model of persistent truncus arteriosus. PLoS One. 12 (9), e0184678 (2017).
- Trincot, C. E., et al. Adrenomedullin induces cardiac lymphangiogenesis after myocardial infarction and regulates cardiac edema via Cx43. Circ Res. 124, 101 (2019).
- Yokoyama, T., et al. Quantification of sympathetic hyperinnervation and denervation after myocardial infarction by three-dimensional assessment of the cardiac sympathetic network in cleared transparent murine hearts. PLoS One. 12, e0182072 (2017).
- Coram, R. J., et al. Muscleblind-like 1 is required for normal heart valve development in vivo. BMC Dev Biol. 15, 36 (2015).
Nachdrucke und Genehmigungen
Genehmigung beantragen, um den Text oder die Abbildungen dieses JoVE-Artikels zu verwenden
Genehmigung beantragenThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Alle Rechte vorbehalten