Method Article
Dimensionamiento electroquímico preciso de partículas electroinactivas individuales
En este artículo
Resumen
Como técnica analítica, la electroquímica de nanoimpacto, un enfoque cada vez más importante para contar y caracterizar partículas electroinactivas a escala nanométrica, adolece de poca precisión debido a las distribuciones de corriente heterogéneas que surgen de su uso de ultramicroelectrodos. Aquí se describe un enfoque generalizado, denominado "interrupción electrocatalítica", que mejora la precisión en tales mediciones.
Resumen
La electroquímica de nanoimpacto permite la caracterización in situ resuelta en el tiempo (por ejemplo, tamaño, actividad catalítica) de unidades individuales de nanomateriales, proporcionando un medio para dilucidar heterogeneidades que se enmascararían en estudios de conjuntos. Para implementar esta técnica con partículas inactivas redox, se utiliza una reacción redox en fase de solución para producir una corriente de fondo en estado estacionario en un ultramicroelectrodo de disco. Cuando una partícula se adsorbe en el electrodo, produce una reducción gradual en el área expuesta del electrodo, lo que produce, a su vez, una disminución gradual en la corriente proporcional al tamaño de la especie adsorbente. Históricamente, sin embargo, la electroquímica de nanoimpacto ha sufrido de "efectos de borde", en los que la capa de difusión radial formada en la circunferencia de los ultramicroelectrodos hace que el tamaño del paso dependa no solo del tamaño de la partícula, sino también de dónde aterriza en el electrodo. Sin embargo, la introducción de la generación de corriente electrocatalítica mitiga la heterogeneidad causada por los efectos de borde, mejorando así la precisión de la medición. En este enfoque, denominado "interrupción electrocatalítica", se introduce un sustrato que regenera la sonda redox en la capa de difusión. Esto cambia el paso limitante de velocidad de la generación actual de difusión a la constante homogénea de velocidad de reacción, reduciendo así la heterogeneidad del flujo y aumentando la precisión del tamaño de las partículas en un orden de magnitud. El protocolo descrito aquí explica la configuración y la recopilación de datos empleados en los experimentos de nanoimpacto que implementan este efecto para mejorar la precisión en el dimensionamiento de materiales redox inactivos.
Introducción
La electroquímica de nanoimpacto es una técnica electroquímica que permite la detección de partículas individuales in situ resueltas en el tiempo en una muestra 1,2,3,4,5,6,7. Las partículas individuales que se pueden caracterizar mediante este enfoque abarcan una amplia gama de materiales 6,8,9,10,11,12,13 y abarcan dimensiones desde átomos individuales hasta células enteras 7,8,14,15,16 . Para dar cabida a la detección y caracterización de materiales tan pequeños, la técnica utiliza ultramicroelectrodos de disco a escala micrométrica y submicrónica. El impacto de una nanopartícula electroactiva en un electrodo de este tipo produce un cambio de corriente fácilmente cuantificable a medida que la nanopartícula se somete a una reacción redox. Para ampliar esto a la detección de materiales activos electro-in, se utiliza una reacción electroquímica de fondo para producir una corriente de estado estacionario que se reduce de manera escalonada a medida que la adsorción de las nanopartículas cambia el área de superficie del electrodo17. En este esquema, se emplean ultramicroelectrodos para aumentar el cambio relativo producido por cada nanoimpacto. Sin embargo, la capa de difusión radial que producen estos microelectrodos reduce la precisión de la medición debido a los "efectos de borde"18. Esto ocurre porque el flujo de las especies redox al electrodo es mayor en los bordes del electrodo que en su centro19. Por lo tanto, cuando una sola nanopartícula aterriza en el borde de la superficie del electrodo, el evento de corriente resultante es mayor que el observado para una partícula idéntica que aterriza en el centro del electrodo19, y este efecto es más significativo para los ultramicroelectrodos debido a su pequeña relación área-circunferencia. Estos efectos de borde restan valor significativamente a la precisión de la electroquímica de nanoimpacto; Debido a su presencia, las distribuciones estimadas del tamaño de partícula producidas por el dimensionamiento por nanoimpacto son 20 veces más amplias que las obtenidas mediante técnicas de microscopía "gold standard"20. Esta precisión reducida resta valor al uso de la electroquímica de nanoimpacto como técnica analítica para evaluar la heterogeneidad de materiales inactivos redox a nanoescala 4,17,19,21,22,23,24,25,26.
Recientemente hemos introducido un método (Figura 1) que mitiga los efectos de borde en los enfoques de nanoimpacto20. En este método, la introducción de un sustrato regenera las especies redox cerca de la superficie del ultramicroelectrodo. Esto desplaza el paso limitante de la velocidad en la generación de corriente de la difusión a la velocidad de la reacción química homogénea de las especies redox en la solución27,28, reduciendo así el grado en que el campo de difusión radial contribuye a las corrientes heterogéneas. Específicamente, la oxidación de 2,2,6,6-tetrametilpiperidina 1-oxilo (TEMPO) proporciona la reacción redox de fondo en el ultramicroelectrodo29. La adición de maltosa a esto regenera la forma reducida de TEMPO30,31. Esta regeneración es rápida32, y comprime la capa de difusión y reduce la heterogeneidad actual asociada con el aterrizaje espacial20. Como resultado, el enfoque de "interrupción electrocatalítica" mejora la precisión del tamaño de las partículas de nanoimpacto en un orden de magnitud.
Protocolo
1. Establecimiento de un sistema de bajo nivel de ruido
NOTA: Los experimentos relevantes requieren un potenciostato capaz de lograr la medición de corrientes bajas con alta resolución de tiempo. Para lograr esto, emplee un potenciostato comercial de grado de investigación capaz de una resolución de tiempo de 1 μs que pueda cuantificar las corrientes a nivel de femtoamperios. Para reducir aún más la interferencia electrónica del entorno, realice experimentos dentro de dos jaulas de Faraday que anidan. Asegúrese de que la configuración sea capaz de una desviación cuadrática media de menos de 100 fA para un experimento de cronoamperometría muestreado a 10 Hz en cloruro de potasio 0,1 M.
- Obtener y montar el equipo, incluyendo las jaulas de potenciostato y Faraday.
NOTA: Las jaulas de Faraday pueden obtenerse comercialmente o fabricarse a medida utilizando metales conductores (por ejemplo, cobre o aluminio). Para el estudio descrito aquí se utilizaron jaulas de Faraday de aluminio fabricadas a medida (véase la Tabla de Materiales).
2. Preparación experimental
- Utilice perlas de poliestireno modificado con carboxilato de 2 μm de diámetro disponibles en el mercado (consulte la Tabla de materiales).
NOTA: Si bien este sistema puede generalizarse a otras especies electro-inactivas23,33, es fundamental recordar que los impactos dependen de la migración electroforética además del movimiento browniano. De esta manera, se aplica un atractivo potencial a las especies de interés, y se mantienen bajas concentraciones de sal17. - Prepare las siguientes soluciones, que se pueden almacenar a temperatura ambiente durante al menos 1 mes.
- Prepare una solución de carbonato de 50 mM y valore a pH 12.0 usando NaOH 1 M. Controle el pH semanalmente.
- Prepare una solución de perclorato de sodio 1 M.
- Prepare las siguientes soluciones frescas cada día, desechándolas al final del día.
- Preparar un TEMPO de 10 mM en una solución de carbonato de 50 mM, pH 12,0.
- Preparar una caldo de maltosa de 500 mM en una solución de carbonato de 50 mM, pH 12,0.
- Seleccione el electrodo de trabajo. Para obtener resultados consistentes, seleccione un ultramicroelectrodo (consulte la Tabla de materiales) de modo que el radio de la especie que se va a caracterizar no sea inferior al 10%-15% del radio del electrodo 17,21,23,33,34.
NOTA: Esta relación puede minimizarse después de determinar la magnitud de los pasos actuales asociados al impacto para la detección óptima de una especie particular de interés. El material del electrodo seleccionado debe catalizar la reacción redox de fondo. - Prepare dos celdas electroquímicas de 5 mL cada una.
- Prepare una celda de control que contenga 1 mM de TEMPO y 5 mM de perclorato de sodio (ver Tabla de Materiales) en tampón de carbonato a pH 12.0.
- Prepare una celda de prueba que contenga una solución de 1 mM de TEMPO, 5 mM de perclorato de sodio y 120 mM de maltosa en tampón de carbonato a pH 12,0.
NOTA: La relación entre el mediador redox y el sustrato (en este caso, TEMPO y maltosa) puede variarse para explorar los efectos de la velocidad de reacción20. Este valor proporciona información sobre la reacción química homogénea. - Después de preparar estas celdas, déjelas a un lado para mediciones electroquímicas posteriores.
3. Pulido de electrodos
- Antes de cada ejecución experimental, pula el electrodo secuencialmente durante 2 minutos cada uno con una suspensión de alúmina de 1 μm, 0,3 μm y 0,5 μm (consulte la Tabla de materiales) en las almohadillas de pulido.
- Mueva el electrodo en un patrón de "figura 8" para asegurar un pulido uniforme35,36. Enjuague generosamente con agua desionizada y seque con una toallita de laboratorio.
NOTA: No sonique los ultramicroelectrodos, ya que esto puede dañarlos.
4. Mediciones electroquímicas
NOTA: Consulte la Figura 2 para ver los resultados.
- Utilice una configuración de tres electrodos para las mediciones electroquímicas. Para los experimentos descritos aquí, emplee un ultramicroelectrodo de fibra de carbono de 11 μm, un contraelectrodo de alambre de platino y un electrodo de referencia de calomel saturado (SCE) (consulte la Tabla de materiales).
NOTA: Las ventanas de potencial electroquímico para los experimentos se indican a continuación; como referencia, TEMPO tiene un potencial formal de 0,49 V frente a SCE, y la maltosa no es electroactiva en la ventana de potencial utilizada en estos experimentos. Cualquier fuga del electrodo de referencia puede afectar a la concentración total de sal37, reduciendo así la conducción electroforética de las partículas al ultramicroelectrodo y reduciendo la eficiencia de recuento17. Si los experimentos arrojan una frecuencia de impacto baja, considere cambiar a un electrodo de referencia sin fugas38,39. - Coloque la celda de control en las jaulas de Faraday y conecte los electrodos a los cables apropiados. Recopile el primer conjunto de mediciones electroquímicas para cada celda. Esto consistirá en un experimento de voltamperometría cíclica y un experimento de cronoamperometría, como se detalla a continuación.
- Recopile los datos de voltamperometría cíclica utilizando una ventana de potencial de 0,2 V a 0,8 V en comparación con SCE a velocidades de exploración de 10 mV·s−1, 20 mV·s−1, 30 mV·s−1, 40 mV·s−1 y 50 mV·s−1.
- Recopile los datos de cronoamperometría aplicando 0,8 V en comparación con SCE durante 10 minutos y registre a una frecuencia de muestreo de 10 Hz.
NOTA: Se recomienda un período de muestreo de 10 minutos para los experimentos de cronoamperometría para obtener de 10 a 15 impactos individuales en pasos posteriores. No se esperan impactos en esta coyuntura.
- A continuación, agregue una solución diluida de perlas de poliestireno a una concentración final de 0,66 pM17 en cada una de las celdas electroquímicas. Después de la adición de las perlas de poliestireno, recoja el segundo conjunto de mediciones electroquímicas para cada celda.
NOTA: La frecuencia de impacto será una función de esta concentración y requiere optimización para recopilar datos suficientes para el análisis estadístico sin saturar el cronoamperograma con impactos superpuestos40,41,42,43.- Recopile datos de cronoamperometría aplicando 0,8 V en comparación con SCE durante 10 minutos y grabe a una frecuencia de muestreo de 10 Hz.
- Repita las mediciones cronoamperométricas hasta que se hayan recopilado suficientes puntos de datos para el análisis estadístico. Para detectar diferencias entre los métodos de dimensionamiento múltiple con un nivel de confianza del 95 % y una potencia del 80 %, seleccione un tamaño de muestra de aproximadamente 200 eventos de impacto individuales.
5. Microscopía electrónica de barrido (SEM)
NOTA: Utilice la microscopía electrónica de barrido como técnica de "estándar de oro" para confirmar el tamaño de las nanopartículas y la heterogeneidad de la muestra19,44.
- Preparación de la muestra
- Para preparar una muestra para la obtención de imágenes, diluya una suspensión de perlas de látex carboxilo (consulte la Tabla de materiales) 1:20 en agua. Coloque 10 μL en un portaobjetos de vidrio, séquelo bajo una corriente de nitrógeno y cúbrala con una capa conductora de oro-paladio bajo argón.
- Imagenológico
- Utilizando una tensión de haz de aceleración de 5 kV y una corriente de 0,4 nA, recopile imágenes según corresponda para el análisis estadístico. Utilice ImageJ45,46 o un software de análisis de imágenes equivalente para determinar el tamaño de las partículas.
6. Análisis electroquímico de datos
- Registre los datos electroquímicos utilizando el software del potenciostato y analice estos resultados utilizando un script escrito 20 que pueda extraer las magnitudes de corrientede los cambios detectados en la corriente de estado estacionario (pasos de corriente) resultantes de eventos de nanoimpacto20.
NOTA: Este guión se incluye como parte de la información complementaria de nuestro informe publicado anteriormente20. - Convierta las amplitudes de los pasos actuales en radios de cordón utilizando la siguiente ecuación:
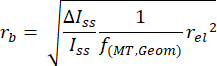
NOTA: Aquí, rb es el radio del cordón, rel es el radio del electrodo, Δ I ss/I ss es la relación entre el cambio en la corriente producida por la adsorción de una partícula y la corriente inicial en estado estacionario observada antes de la adsorción de esa partícula, y f(MT,Geom) = 0.067 es un factor de escala empírico que depende de consideraciones geométricas y de transporte de masa20, Artículo 25. - Grafique la frecuencia de detección de un radio de cordón determinado en comparación con el radio (Figura 3) para cuantificar las métricas de distribución.
7. Modelado
NOTA: Si se desea, el mecanismo por el cual funciona la interrupción electrocatalítica se puede validar confirmando el cambio de la generación de corriente limitada por difusión a la generación de corriente limitada por velocidad de reacción. Para describir y visualizar, utilice dos programas de simulación numérica diferentes: un software de ajuste de voltagrama, como DigiSim, para determinar la constante de velocidad homogénea, y una plataforma de modelado multifísico, como COMSOL Multiphysics, para visualizar los cambios locales en el perfil de difusión en la superficie del ultramicroelectrodo (ver Tabla de Materiales).
- Adaptación de voltagrama
NOTA: Utilice el software de ajuste del voltagrama para determinar la constante de velocidad homogénea (Figura 4).- Recoja voltamogramas cíclicos en una solución que contenga 1 mM de TEMPO (solamente) y 1 mM de TEMPO más 120 mM de maltosa. Para cada condición, recopile datos a varias velocidades de escaneo y utilice estos datos para ajustes numéricos de estos conjuntos de datos experimentales.
- Ajuste los voltammogramas recogidos del experimento TEMPO utilizando un mecanismo E, que describe un proceso de reacción impulsado únicamente por el electrodo47,48. Esto producirá los parámetros del electrodo.
- Utilizando los parámetros del electrodo obtenidos en el paso 7.1.1.1, ajuste los voltammogramas resultantes de la solución de maltosa TEMPO 1 mM más 120 a un mecanismo EC'47,48, que describe un proceso de electrodo seguido de una reacción química homogénea que regenera el mediador redox. Esto producirá la constante de velocidad homogénea.
- Recoja voltamogramas cíclicos en una solución que contenga 1 mM de TEMPO (solamente) y 1 mM de TEMPO más 120 mM de maltosa. Para cada condición, recopile datos a varias velocidades de escaneo y utilice estos datos para ajustes numéricos de estos conjuntos de datos experimentales.
- Modelado multifísico
- Utilice una plataforma de modelado multifísico para visualizar los cambios en los perfiles de difusión en la superficie del ultramicroelectrodo para los sistemas de control e interrupción electrocatalítica 20,49,50,51,52 (Figura 5). Utilice los parámetros del electrodo y la constante de velocidad homogénea obtenida del ajuste del voltammograma como condiciones iniciales. A continuación se ofrece una amplia descripción general del flujo de trabajo, que se puede adaptar a diferentes programas.
- Introduzca los parámetros globales. Estos consisten en valores fijos como (pero no limitados a) los valores de concentración, los coeficientes de difusión, el radio del electrodo y la temperatura.
- Construya el espacio de simulación. Se trata de un conjunto de geometrías que incluyen el electrodo, la vaina aislante, el espacio de solución circundante que representa la región de interés y un dominio de elemento infinito que representa el entorno a granel.
- Introducir paquetes de física para definir la simulación.
- Asocie el espacio del electrodo con un estudio de electroanálisis. Defina aquí los valores iniciales y la reacción del electrodo de interés.
- Asocie el espacio de solución circundante con un estudio químico. Defina aquí la reacción química homogénea que sigue a la reacción del electrodo.
- Introduzca una malla en todo el espacio de simulación. Esto define cómo se divide la geometría para resolver el modelo. Para lograr resultados de alta calidad, use una malla más fina cerca del electrodo.
- Para observar los cambios como resultado de la constante de velocidad homogénea, varíe el valor de este parámetro utilizando un estudio paramétrico para resolver el modelo.
- Para observar los cambios en función del tiempo, varíe el valor de este parámetro utilizando un estudio dependiente del tiempo para resolver el modelo.
Resultados
La interrupción electrocatalítica mitiga los efectos de borde al cambiar el mecanismo de generación de corriente primaria de difusión limitada (es decir, limitada por el transporte de una sonda redox al electrodo) a cinéticamente limitada (es decir, limitada por una reacción rápida en fase de solución)20. Este método es modular, lo que significa que permite un enfoque de mezcla y combinación para elegir el material del electrodo, la sonda redox y el sustrato, y esto hace que la interrupción electrocatalítica sea susceptible de la detección de muchos nano y biomateriales 6,7,8,9,10,11,12,13,14,15,22 . La implementación de esta técnica en un electrodo de fibra de carbono de 5,5 μm de radio produjo una mejora de 10 veces en la precisión asociada con el dimensionamiento electroquímico de un sistema modelo (perlas de poliestireno) en una solución que contenía TEMPO como sonda redox y maltosa como sustrato.
Siguiendo este protocolo, se pueden obtener los conjuntos de datos necesarios para validar este mecanismo y su capacidad para restaurar la precisión analítica a la hora de dimensionar nanopartículas electroinactivas. En primer lugar, los datos del voltamograma cíclico recogidos en ausencia de perlas de poliestireno mostraron un evento redox reversible en experimentos de control con TEMPO solo. A partir de aquí, la adición de maltosa dio como resultado un aumento en el pico oxidativo y una pérdida concurrente en el pico reductivo a medida que el TEMPO oxidado fue regenerado por maltosa. En segundo lugar, los cronoamperogramas recolectados en estas condiciones demostraron que las corrientes en estado estacionario a un potencial oxidativo eran más altas, lo que es consistente con la amplificación catalítica observada en los resultados de voltamperometría cíclica. Este paso también sugiere que la reacción química a granel se mantiene mediante la reacción del electrodo; Por lo tanto, cualquier mejora con respecto al método de control durará durante la duración de la medición. Sin embargo, esto por sí solo no es suficiente para evaluar cualquier mejora en la precisión de la medición; Para ello, los datos de cronoamperometría deben recogerse en presencia de perlas de poliestireno.
Para evaluar la precisión del dimensionamiento, los datos del cronoamperograma se recogieron utilizando perlas de poliestireno carboxilado de 2 μm. Tras su adición, se observaron cambios graduales en la corriente del cronoamperograma a medida que las partículas individuales impactaban y absorbían (control de la Figura 2A, interrupción electrocatalítica de la Figura 2B). Cada cambio escalonado en la magnitud de la corriente en estado estacionario se convirtió en radios de partículas, y los datos se visualizaron como histogramas para comparar la distribución de estas técnicas electroquímicas con la de una técnica estándar de oro, como la microscopía electrónica de barrido (Figura 3). Esta comparación permitió la caracterización de las métricas de precisión asociadas a cada enfoque de dimensionamiento.
Se utilizaron modelos para respaldar estas observaciones experimentales. Específicamente, el ajuste de los voltampogramas cíclicos de antes arrojó parámetros que caracterizaron tanto la reacción del electrodo como la reacción química en fase de solución (Figura 4). A partir de la solución control, algunos parámetros muestrales obtenidos fueron Efθ = 0.49 V, k 0 =0.02 cm·s-1 y ν = 10 mV·s-1 a T = 25° C. A partir de la solución de prueba, se pudieron obtener los parámetros cinéticos que limitaban la generación de corriente; específicamente, a medidaque K eq se acerca a infinito, kobs = 2.200 M-1·s-1. Las simulaciones numéricas podrían utilizar estos valores como condiciones iniciales para generar un perfil de concentración de la sonda redox (Figura 5). En ausencia de maltosa, el perfil de difusión resultante era radial, lo que daba lugar a un flujo heterogéneo del material; Específicamente, más material se difundió hacia el electrodo en los bordes. La introducción de maltosa comprimió el perfil de difusión, produciendo, a su vez, corrientes más homogéneas a través de la superficie del electrodo.
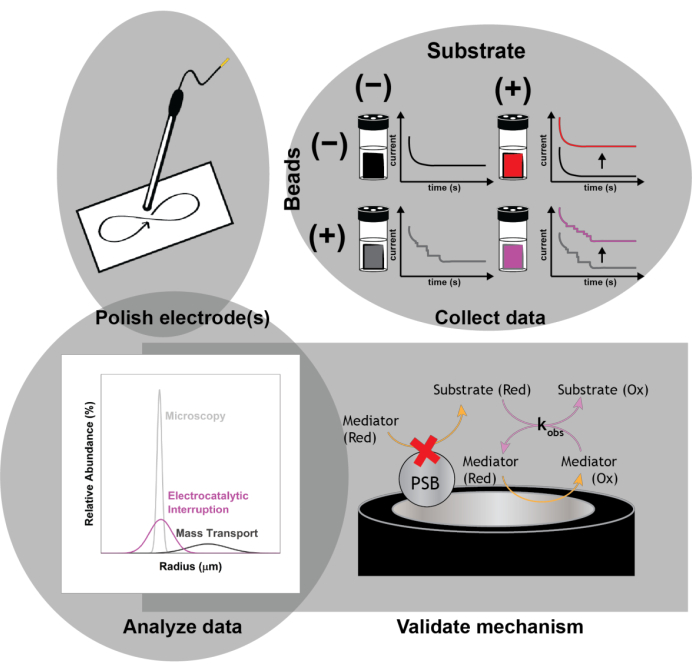
Figura 1: Esquema del protocolo experimental. Pula los electrodos antes de cada ejecución experimental. Recopile un conjunto de referencia de mediciones electroquímicas (voltamperometría cíclica y cronoamperometría) en ausencia de perlas con y sin la implementación de interrupción electrocatalítica para observar la mejora de corriente con la adición del sustrato. Pinche las perlas y recopile un segundo conjunto de mediciones electroquímicas para la determinación del tamaño de las nanopartículas que impactan. Validar el mecanismo de acción mediante simulaciones numéricas. Haga clic aquí para ver una versión más grande de esta figura.
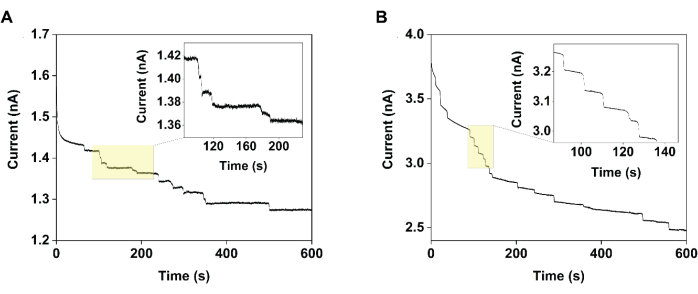
Figura 2: Cronoamperogramas recogidos con un ultramicroelectrodo de fibra de carbono de 11 μm de diámetro que demuestra la mejora en la precisión de la medición lograda mediante la interrupción electrocatalítica. Específicamente, al medir la corriente versus el tiempo en una solución de 1 mM TEMPO en la (A) ausencia (control) y (B) presencia de maltosa de 120 mM (interrupción electrocatalítica), los pasos observados en este último caso fueron más homogéneos. Reimpreso con permiso de Chung et al.20. Haga clic aquí para ver una versión más grande de esta figura.
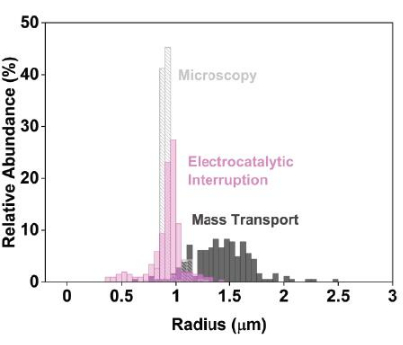
Figura 3: Datos de dimensionamiento electroquímico precisos cuando se utiliza la interrupción electrocatalítica en comparación con el enfoque electroquímico convencional de difusión limitada. Para representar estos datos, prepare histogramas comparando las distribuciones de tamaño determinadas mediante microscopía electrónica de barrido (gris claro) y electroquímica (interrupción electrocatalítica, rosa; control, gris oscuro). Los estudios convencionales de nanoimpacto, en los que la corriente está limitada por el transporte de masa del mediador, producen distribuciones de tamaño estimadas artificialmente amplias (gris oscuro). Por el contrario, la implementación de la interrupción electrocatalítica conduce a estimaciones de tamaño más estrechas y precisas (rosa). Reimpreso con permiso de Chung et al.20. Haga clic aquí para ver una versión más grande de esta figura.
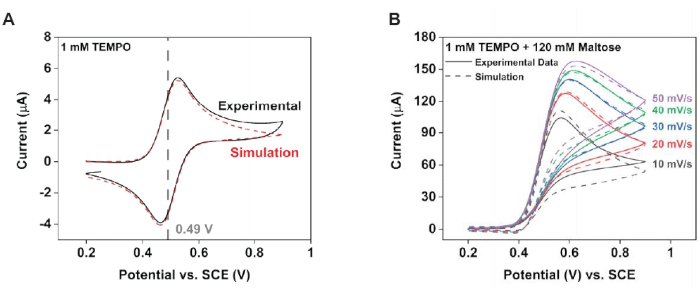
Figura 4: Modelado de la cinética del electrodo para caracterizar el nuevo esquema de reacción. Utilizando un software de ajuste de voltamografía cíclica, extraiga los parámetros de reacción del electrodo de los datos experimentales. (A) Datos con TEMPO de 1 mM. (B) Datos con 1 mM de TEMPO más 120 mM de maltosa. Reimpreso con permiso de Chung et al.20. Haga clic aquí para ver una versión más grande de esta figura.
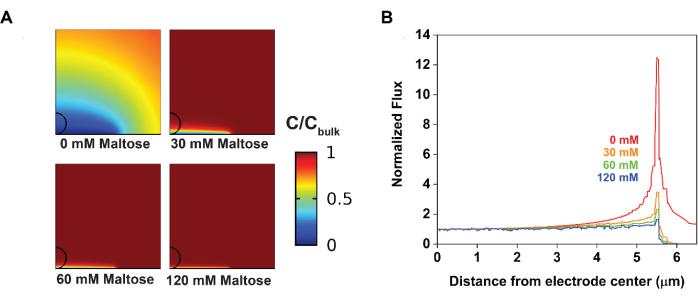
Figura 5: Cambios en el flujo de material en la superficie del electrodo al introducir la interrupción electrocatalítica visualizados mediante simulaciones numéricas . (A) La adición de maltosa comprime la capa de difusión de una manera dependiente de la concentración. (B) La adición de maltosa deprime el flujo heterogéneo en los bordes de los electrodos. Reimpreso con permiso de Chung et al.20. Haga clic aquí para ver una versión más grande de esta figura.
Discusión
La interrupción electrocatalítica es fácil de implementar y reduce la imprecisión asociada con la electroquímica de nanoimpacto en un orden de magnitud. Esta precisión mejorada permite directamente a los investigadores discriminar entre partículas de diferentes tamaños en una solución mixta20. También mejora la capacidad de detectar de manera confiable partículas inactivas redox más pequeñas que el límite históricamente reportado de 15%-20% del radio del electrodo 17,21,23,34.
Si bien la interrupción electroquímica puede dar cabida a varios sistemas redox para la detección de nanopartículas de diversos materiales electroinactivos, la identificación de dichos sistemas redox ha seguido siendo un desafío importante. La principal barrera para implementar la interrupción electroquímica es identificar una reacción química que sea lo suficientemente rápida como para reducir significativamente las contribuciones confusas de los efectos de borde. Específicamente, mientras que algunos ejemplos de reacciones EC', en las que una reacción del electrodo es seguida por una reacción química que regenera el reactivo del electrodo, están bien caracterizados en la literatura 29,32,53,54,55, pocos son lo suficientemente rápidos como para mejorar la precisión de la medición. En este estudio, de aquellas reacciones que son suficientemente rápidas, se eligió un sistema TEMPO-maltosa, y esto arrojó una constante de velocidad observada de 2.200 M-1·s-1. Esto, junto con las simulaciones multifísicas que demuestran que las velocidades de reacción más rápidas conducen a un flujo más homogéneo en el borde del electrodo, apoya la conclusión de que solo las reacciones químicas rápidas producen mejoras de corriente varias veces en los ultramicroelectrodos.
La interrupción catalítica no requiere manipulación de datos ni modificaciones en los ultramicroelectrodos disponibles en el mercado. Para explicar las magnitudes de corriente heterogéneas características de los datos de nanoimpacto, Bonezzi y Boika introdujeron un modelo teórico que relaciona la magnitud del paso actual con el tamaño de partícula25. Este análisis, sin embargo, se basa en gran medida en el promedio de las magnitudes actuales en función de la frecuencia de colisión. Esto no solo impide conocer las propiedades de las partículas individuales, sino que esta técnica también depende del flujo del reportero redox al electrodo y no elimina el problema de los efectos de borde, lo que resulta en una precisión reducida. Deng et al. introdujeron el primer enfoque experimental para abordar los efectos de borde, utilizando un ultramicroelectrodo hemisférico fabricado a partir de mercurio51. Sin embargo, los electrodos de gotas de mercurio son tóxicos, mecánicamente inestables y estables solo durante una ventana de potencial limitada56. Además, la fabricación (y el mantenimiento) de microelectrodos perfectamente hemisféricos utilizando otros materiales sigue siendo un reto51,52. Más recientemente, Moazzenzade et al. propusieron ultramicroelectrodos de anillo para la caracterización de nanoimpactos52. Esta geometría es prometedora, pero requiere capacidades de nanofabricación. Por el contrario, la interrupción catalítica permite experimentos de nanoimpacto con materiales que se encuentran universalmente en un laboratorio de electroquímica.
Divulgaciones
Los autores no tienen nada que revelar.
Agradecimientos
Este trabajo fue financiado por el R35GM142920 de subvenciones de los Institutos Nacionales de Salud (NIH, por sus siglas en inglés). La investigación aquí reportada hizo uso de instalaciones compartidas de UCSB MRSEC (NSF DMR 1720256), miembro de la Red de Instalaciones de Investigación de Materiales (www.mrfn.org). Agradecemos a Phoebe Hertler por contribuir al artículo original al que hace referencia este trabajo. Agradecemos a la Dra. Claire Chisholm por ayudar en la adquisición de las imágenes de microscopía electrónica de barrido.
Materiales
| Name | Company | Catalog Number | Comments |
| 0.05 µm microalumina polish | Buehler | 4010075 | |
| 0.3 µm microalumina polish | Buehler | 4010077 | |
| 1 µm microalumina polish | Buehler | 4010079 | |
| 20 mL scintillation vials | Fisher Sci | 03-339-26C | |
| Analytical balance | Ohaus | ||
| Apreo C LoVac FEG SEM | Thermo Fisher | ||
| Carbon fiber microelectrode | ALS | 002007 | Working electrode; purchased from CH Instruments |
| Carboxyl Latex Beads, 4% w/v, 2 µm | ThermoFisher Scientific | C37278 | |
| COMSOL Multiphysics | COMSOL Multiphysics | v6.0 | |
| D-(+)-Maltose monohydrate | Sigma Aldrich | M5885 | |
| DigiSim | Bioanalytical Systems, Inc. | v3.03b | Discontinued; comparable software is available commercially through the same vendor |
| EC-Lab | BioLogic | v11.27 | |
| Faraday cages | Custom; analogous equipment can be commercially purchased or fabriated of conductive sheet metals (e.g., copper or aluminum) | ||
| Hummer Sputter Coater | Anatech USA | ||
| OriginPro | OriginLab | v2022b | |
| P1000 micropipette | Fisher Scientific | ||
| P2 micropipette | Fisher Scientific | ||
| P20 micropipette | Fisher Scientific | ||
| P200 micropipette | Fisher Scientific | ||
| Platinum Wire Electrode | CH Instruments | CHI115 | Counter electrode |
| Potassium chloride | Sigma Aldrich | P3911 | |
| PSA-backed MicroCloth | Buehler | 407218 | |
| Saturated Calomel Electrode | CH Instruments | CHI150 | Reference electrode |
| Sodium carbonate | Fisher Chemical | S263 | |
| Sodium hydroxide | Sigma Aldrich | S8045 | |
| Sodium perchlorate | EM Science | SX0692 | |
| SP-300 | BioLogic | ||
| TEMPO | Oakwood Chemical | 013714 | |
| Ultra Low Current module | BioLogic |
Referencias
- Heyrovsky, M., Jirkovsky, J. Polarography and voltammetry of ultrasmall colloids: Introduction to a new field. Langmuir. 11 (11), 4288-4292 (1995).
- Kleijn, S. E. F., et al. Landing and catalytic characterization of individual nanoparticles on electrode surfaces. Journal of the American Chemical Society. 134 (45), 18558-18561 (2012).
- Hill, C. M., Clayton, D. A., Pan, S. Combined optical and electrochemical methods for studying electrochemistry at the single molecule and single particle level: Recent progress and perspectives. Physical Chemistry Chemical Physics. 15 (48), 20797-20807 (2013).
- Dick, J. E., Hilterbrand, A. T., Boika, A., Upton, J. W., Bard, A. J. Electrochemical detection of a single cytomegalovirus at an ultramicroelectrode and its antibody anchoring. Proceedings of the National Academy of Sciences of the United States of America. 112 (17), 5303-5308 (2015).
- Mirkin, M. V., Sun, T., Yu, Y., Zhou, M. Electrochemistry at one nanoparticle. Accounts of Chemical Research. 49 (10), 2328-2335 (2016).
- Sokolov, S. V., Eloul, S., Kätelhön, E., Batchelor-McAuley, C., Compton, R. G. Electrode-particle impacts: A users guide. Physical Chemistry Chemical Physics. 19 (1), 28-43 (2017).
- Stevenson, K. J., Tschulik, K. A materials driven approach for understanding single entity nano impact electrochemistry. Current Opinion in Electrochemistry. 6 (1), 38-45 (2017).
- Baker, L. A. Perspective and prospectus on single-entity electrochemistry. Journal of the American Chemical Society. 140 (46), 15549-15559 (2018).
- Cheng, W., Compton, R. G. Electrochemical detection of nanoparticles by 'nano-impact' methods. TrAC Trends in Analytical Chemistry. 58, 79-89 (2014).
- Bard, A. J., Fan, F. -. R. F. Electrochemical detection of single molecules. Accounts of Chemical Research. 29 (12), 572-578 (1996).
- Xiao, X., Bard, A. J. Observing single nanoparticle collisions at an ultramicroelectrode by electrocatalytic amplification. Journal of the American Chemical Society. 129 (31), 9610-9612 (2007).
- Anderson, T. J., Zhang, B. Single-nanoparticle electrochemistry through immobilization and collision. Accounts of Chemical Research. 49 (11), 2625-2631 (2016).
- Goines, S., Dick, J. E. Review-Electrochemistry's potential to reach the ultimate sensitivity in measurement science. Journal of the Electrochemical Society. 167 (3), 037505 (2020).
- Kai, T., Zhou, M., Johnson, S., Ahn, H. S., Bard, A. J. Direct observation of C2O4•- and CO2•- by oxidation of oxalate within nanogap of scanning electrochemical microscope. Journal of the American Chemical Society. 140 (47), 16178-16183 (2018).
- Dick, J. E. Electrochemical detection of single cancer and healthy cell collisions on a microelectrode. Chemical Communications. 52 (72), 10906-10909 (2016).
- Sepunaru, L., Sokolov, S. V., Holter, J., Young, N. P., Compton, R. G. Electrochemical red blood cell counting: One at a time. Angewandte Chemie International Edition. 55 (33), 9768-9771 (2016).
- Quinn, B. M., van't Hof, P. G., Lemay, S. G. Time-resolved electrochemical detection of discrete adsorption events. Journal of the American Chemical Society. 126 (27), 8360-8361 (2004).
- Oldham, K. B. Edge effects in semiinfinite diffusion. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 122, 1-17 (1981).
- Fosdick, S. E., Anderson, M. J., Nettleton, E. G., Crooks, R. M. Correlated electrochemical and optical tracking of discrete collision events. Journal of the American Chemical Society. 135 (16), 5994-5997 (2013).
- Chung, J., Hertler, P., Plaxco, K. W., Sepunaru, L. Catalytic interruption mitigates edge effects in the characterization of heterogeneous, insulating nanoparticles. Journal of the American Chemical Society. 143 (45), 18888-18898 (2021).
- Boika, A., Thorgaard, S. N., Bard, A. J. Monitoring the electrophoretic migration and adsorption of single insulating nanoparticles at ultramicroelectrodes. The Journal of Physical Chemistry B. 117 (16), 4371-4380 (2013).
- Kim, B. -. K., Boika, A., Kim, J., Dick, J. E., Bard, A. J. Characterizing emulsions by observation of single droplet collisions-Attoliter electrochemical reactors. Journal of the American Chemical Society. 136 (13), 4849-4852 (2014).
- Dick, J. E., Renault, C., Bard, A. J. Observation of single-protein and DNA macromolecule collisions on ultramicroelectrodes. Journal of the American Chemical Society. 137 (26), 8376-8379 (2015).
- Lee, J. Y., Kim, B. -. K., Kang, M., Park, J. H. Label-free detection of single living bacteria via electrochemical collision event. Scientific Reports. 6 (1), 30022 (2016).
- Bonezzi, J., Boika, A. Deciphering the magnitude of current steps in electrochemical blocking collision experiments and its implications. Electrochimica Acta. 236, 252-259 (2017).
- Ellison, J., Batchelor-McAuley, C., Tschulik, K., Compton, R. G. The use of cylindrical micro-wire electrodes for nano-impact experiments; Facilitating the sub-picomolar detection of single nanoparticles. Sensors and Actuators B: Chemical. 200, 47-52 (2014).
- Denuault, G., Fleischmann, M., Pletcher, D., Tutty, O. R. Development of the theory for the interpretation of steady state limiting currents at a microelectrode: EC' processes: First and second order reactions. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry. 280 (2), 243-254 (1990).
- Francke, R., Little, R. D. Redox catalysis in organic electrosynthesis: Basic principles and recent developments. Chemical Society Reviews. 43 (8), 2492-2521 (2014).
- Nutting, J. E., Rafiee, M., Stahl, S. S. Tetramethylpiperidine N-Oxyl (TEMPO), phthalimide N-oxyl (PINO), and related N-Oxyl species: Electrochemical properties and their use in electrocatalytic reactions. Chemical Reviews. 118 (9), 4834 (2018).
- Pierre, G., et al. TEMPO-mediated oxidation of polysaccharides: An ongoing story. Carbohydrate Polymers. 165, 71-85 (2017).
- Liaigre, D., Breton, T., Belgsir, E. M. Kinetic and selectivity control of TEMPO electro-mediated oxidation of alcohols. Electrochemistry Communications. 7 (3), 312-316 (2005).
- Rafiee, M., Karimi, B., Alizadeh, S. Mechanistic study of the electrocatalytic oxidation of alcohols by TEMPO and MHPI. ChemElectroChem. 1 (2), 455-462 (2014).
- Deng, Z., Renault, C. Detection of individual insulating entities by electrochemical blocking. Current Opinion in Electrochemistry. 25, 100619 (2021).
- Laborda, E., Molina, A., Batchelor-McAuley, C., Compton, R. G. Individual detection and characterization of non-electrocatalytic, redox-inactive particles in solution by using electrochemistry. ChemElectroChem. 5 (3), 410-417 (2018).
- Elgrishi, N., et al. A practical beginner's guide to cyclic voltammetry. Journal of Chemical Education. 95 (2), 197-206 (2018).
- Cardwell, T. J., Mocak, J., Santos, J. H., Bond, A. M. Preparation of microelectrodes: comparison of polishing procedures by statistical analysis of voltammetric data. Analyst. 121 (3), 357-362 (1996).
- Lämmel, C., Heubner, C., Liebmann, T., Schneider, M. Critical impact of chloride containing reference electrodes on electrochemical measurements. Electroanalysis. 29 (12), 2752-2756 (2017).
- Walker, N. L., Dick, J. E. Leakless, bipolar reference electrodes: Fabrication, performance, and miniaturization. Analytical Chemistry. 93 (29), 10065-10074 (2021).
- Troudt, B. K., Rousseau, C. R., Dong, X. I. N., Anderson, E. L., Bühlmann, P. Recent progress in the development of improved reference electrodes for electrochemistry. Analytical Sciences. 38 (1), 71-83 (2022).
- Stuart, E. J. E., Zhou, Y. -. G., Rees, N. V., Compton, R. G. Particle-impact nanoelectrochemistry: A Fickian model for nanoparticle transport. RSC Advances. 2 (33), 12702-12705 (2012).
- Boika, A., Bard, A. J. Time of first arrival in electrochemical collision experiments as a measure of ultralow concentrations of analytes in solution. Analytical Chemistry. 87 (8), 4341-4346 (2015).
- Robinson, D. A., et al. Collision dynamics during the electrooxidation of individual silver nanoparticles. Journal of the American Chemical Society. 139 (46), 16923-16931 (2017).
- Lemay, S. G., Moazzenzade, T. Single-entity electrochemistry for digital biosensing at ultralow concentrations. Analytical Chemistry. 93 (26), 9023-9031 (2021).
- Vernon-Parry, K. D. Scanning electron microscopy: An introduction. III-Vs Review. 13 (4), 40-44 (2000).
- Abramoff, M. D., Magalhães, P. J., Ram, S. J. Image processing with ImageJ. Biophotonics International. 11 (7), 36-42 (2004).
- Collins, T. J. ImageJ for microscopy. BioTechniques. 43, S25-S30 (2007).
- Bard, A. J., Faulkner, L. R. . Electrochemical Methods: Fundamentals and Applications. , (2001).
- Compton, R. G., Banks, C. E. . Understanding Voltammetry (Third Edition). , (2018).
- Cutress, I. J., Dickinson, E. J. F., Compton, R. G. Analysis of commercial general engineering finite element software in electrochemical simulations. Journal of Electroanalytical Chemistry. 638 (1), 76-83 (2010).
- Dickinson, E. J. F., Ekström, H., Fontes, E. COMSOL Multiphysics®: Finite element software for electrochemical analysis. A mini-review. Electrochemistry Communications. 40, 71-74 (2014).
- Deng, Z., Elattar, R., Maroun, F., Renault, C. In situ measurement of the size distribution and concentration of insulating particles by electrochemical collision on hemispherical ultramicroelectrodes. Analytical Chemistry. 90 (21), 12923-12929 (2018).
- Moazzenzade, T., Walstra, T., Yang, X., Huskens, J., Lemay, S. G. Ring ultramicroelectrodes for current-blockade particle-impact electrochemistry. Analytical Chemistry. 94 (28), 10168-101747 (2022).
- Nekrassova, O., et al. The oxidation of cysteine by aqueous ferricyanide: A kinetic study using boron doped diamond electrode voltammetry. Electroanalysis. 14 (21), 1464-1469 (2002).
- Kuss, S., Compton, R. G. Electrocatalytic detection of ascorbic acid using N,N,N',N'-tetramethyl-para-phenylene-diamine (TMPD) mediated oxidation at unmodified gold electrodes; Reaction mechanism and analytical application. Electrochimica Acta. 242, 19-24 (2017).
- Shayani-Jam, H., Nematollahi, D. Electrochemically mediated oxidation of glutathione and N-acetylcysteine with 4,4′-biphenol. Electrochimica Acta. 56 (25), 9311-9316 (2011).
- Vyskočil, V., Barek, J. Mercury electrodes-Possibilities and limitations in environmental electroanalysis. Critical Reviews in Analytical Chemistry. 39 (3), 173-188 (2009).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados