Se requiere una suscripción a JoVE para ver este contenido. Inicie sesión o comience su prueba gratuita.
Fabricación de nanocompuestos antibacterianos de óxido de grafeno/cobre
En este artículo
Resumen
En este trabajo, presentamos nanocompuestos de óxido de grafeno/cobre (GO/Cu) como nanomaterial antibacteriano. Se evaluó la eficacia antibacteriana de los nanocompuestos GO/Cu frente a bacterias grampositivas y gramnegativas resistentes a los antibióticos.
Resumen
Los antibióticos son actualmente el tratamiento antibacteriano más utilizado para matar las bacterias. Sin embargo, las bacterias desarrollan resistencia cuando se sobreexponen continuamente a los antibióticos. El desarrollo de agentes antimicrobianos que puedan reemplazar a los antibióticos existentes es esencial porque las bacterias resistentes a los antibióticos tienen mecanismos de resistencia a todos los antibióticos actuales y pueden promover infecciones nosocomiales. Para abordar este reto, en este estudio proponemos nanocompuestos de óxido de grafeno/cobre (GO/Cu) como materiales antibacterianos que pueden sustituir a los antibióticos existentes. Los nanocompuestos GO/Cu se caracterizan por microscopía electrónica de transmisión y microscopía electrónica de barrido. Muestran que las nanopartículas de cobre (Cu) están bien desarrolladas en las láminas de óxido de grafeno. Además, se utiliza un método de caldo de microdilución para confirmar la eficacia de la sustancia antimicrobiana contra Staphylococcus aureus (SARM) y Pseudomonas aeruginosa (P. aeruginosa) resistentes a la meticilina, que frecuentemente están implicadas en infecciones nosocomiales. En concreto, el 99,8% de MRSA y el 84,7% de P. aeruginosa son eliminados por 500 μg/mL de nanocomposites GO/Cu. Los nanocompuestos metálicos pueden erradicar las bacterias resistentes a los antibióticos mediante la liberación de iones, la formación de especies reactivas de oxígeno y el daño físico de las bacterias. Este estudio demuestra el potencial de los nanocompuestos antibacterianos GO/Cu en la erradicación de bacterias resistentes a los antibióticos.
Introducción
Las infecciones bacterianas tienen un impacto significativo en la salud pública. Las bacterias patógenas, en particular, pueden evadir los mecanismos protectores del cuerpo ycausar enfermedades. Los antibióticos se usan ampliamente para tratar infecciones bacterianas. Sin embargo, el uso inadecuado de antibióticos ha precipitado la aparición de bacterias resistentes a los antibióticos. En la actualidad, las infecciones nosocomiales atribuibles a bacterias resistentes a los antibióticos han causado complicaciones notables en los establecimientos de salud2. Desafortunadamente, las bacterias tienen mecanismos de resistencia para todos los antibióticos actuales3. Por lo tanto, el desarrollo de nuevos antibióticos es esencial, aunque también existe una alta probabilidad de que surjan mecanismos de resistencia.
Las nanopartículas metálicas se han convertido en agentes prometedores para combatir las bacterias resistentes a los antibióticos debido a sus eficaces propiedades antibacterianas 4,5,6. Es difícil que las bacterias desarrollen mecanismos de resistencia contra las nanopartículas metálicas porque no se unen a ningún receptor bacteriano específico7. En particular, las nanopartículas de óxido de plata, cobre y zinc son objeto de una amplia investigación debido a su notable eficacia antibacteriana 8,9,10,11,12,13. La toxicidad de las nanopartículas metálicas hacia las bacterias se atribuye a tres mecanismos principales: 1) la liberación de iones metálicos, 2) la generación de especies reactivas de oxígeno (ROS), como •OH y •O2−, y 3) la interacción física y la unión 4,14.
En este estudio, se desarrollaron nanocompuestos de óxido de grafeno/cobre (GO/Cu) como agente antimicrobiano. El cobre (Cu) mata eficazmente los patógenos que encuentran su superficie e interfiere con la replicación de genes bacterianos. Sin embargo, es un microelemento esencial en el cuerpo humano, y es menos tóxico para las células de mamíferos porque tiene mecanismos homeostáticos que regulan las concentraciones de Cu dentro de las células4. Cuando las nanopartículas de Cu se oxidan, generan iones de Cu, que tienen una afinidad relativamente alta por las bacterias cargadas negativamente15,16. Los iones Cu se unen a las estructuras celulares (por ejemplo, proteínas, membranas y ADN), alterando las funciones celulares17. Al sintetizar nanopartículas de Cu en la superficie del óxido de grafeno (GO), se puede controlar la tasa de liberación de iones metálicos 18,19,20. El GO también muestra un efecto antibacteriano al evitar la adhesión bacteriana con una superficie rugosa a través del estrés oxidativo o mediante la formación de ROS21,22. Además, los nanocompuestos GO/Cu liberan más ROS que GO a través de la acción química del Cu2+, que daña las proteínas bacterianas y el ADN, lo que provoca la muerte de las bacterias23,24.
Este artículo describe el protocolo para sintetizar nanocompuestos GO/Cu e introduce un enfoque de pruebas antimicrobianas contra las bacterias clínicas MRSA y P. aeruginosa, las cepas de bacterias multirresistentes más comunes que causan infecciones nosocomiales25. Este protocolo tiene como objetivo introducir un método de reducción química fácil para sintetizar nanocompuestos GO/Cu que pueden impedir el crecimiento de bacterias resistentes a los antibióticos. Utilizamos cloruro de cobre (II) (CuCl2) y borohidruro de sodio (NaBH4) como precursor y agente reductor, respectivamente. El protocolo también describe los detalles de la aplicación de estos nanocompuestos a las bacterias utilizando el método de caldo de microdilución. Para excluir errores debidos a la interferencia de absorción de nanopartículas metálicas y realizar evaluaciones precisas, la capacidad antibacteriana se evalúa utilizando el método de recuento de colonias.
Protocolo
1. Preparación de los nanocompuestos GO/Cu
NOTA: El tamaño y la morfología de las nanopartículas de Cu que crecen en las nanohojas de GO están determinados por el grado de oxidación de GO, la concentración del precursor de Cu y la concentración del agente reductor26.
- Prepare 10 mL de suspensión de GO de 1 mg/mL en un frasco de vidrio. Sonicar la suspensión de GO durante 1 h hasta que el GO esté bien disperso en agua destilada (DI).
- Prepare una solución de 20 mM de CuCl2 en un vial de vidrio. Sonicar la solución de CuCl2 hasta que el CuCl2 esté bien disperso en el agua desionizada.
- Añadir 10 mL de la solución de 20 mM de CuCl2 a la solución GO y sonicar la mezcla a 70 °C durante 1 h.
- Prepare una solución de NaBH4 de 20 mM.
PRECAUCIÓN: Este procedimiento debe realizarse en una campana de gases químicos. Se produce una reacción redox tan pronto como el agente reductor NaBH4 se introduce en el agua. Prepare la solución de NaBH4 inmediatamente antes del experimento. - Preparación de la mezcla de NaBH4, GO y CuCl2
- Agregue 20 mL de la solución de NaBH4 de 20 mM a la mezcla de GO y CuCl2 mientras agita con una barra magnética a 200 rpm. Después de agregar la solución de NaBH4 , revuelva continuamente durante 30 min.
PRECAUCIÓN: Este procedimiento debe realizarse en una campana de gases químicos.
- Agregue 20 mL de la solución de NaBH4 de 20 mM a la mezcla de GO y CuCl2 mientras agita con una barra magnética a 200 rpm. Después de agregar la solución de NaBH4 , revuelva continuamente durante 30 min.
- Centrifugación de la mezcla
- Transfiera la mezcla del paso 1.5.1 a un tubo de centrífuga. Centrifugar la solución a 23.000 × g durante 10 min a temperatura ambiente. Deseche el sobrenadante.
PRECAUCIÓN: Cuando opere la centrífuga, mantenga siempre el equilibrio colocando tubos de igual peso.
- Transfiera la mezcla del paso 1.5.1 a un tubo de centrífuga. Centrifugar la solución a 23.000 × g durante 10 min a temperatura ambiente. Deseche el sobrenadante.
- Vuelva a suspender la mezcla de nanocompuestos GO/Cu con 10 mL de agua desionizada y soniquelos para permitir que el precipitado se disperse uniformemente por toda la solución.
- Centrifugar la solución a 23.000 × g durante 10 min a temperatura ambiente; A continuación, retire el sobrenadante.
- Repita los pasos 1.7-1.8 una vez más para eliminar los productos químicos no reaccionados.
- Añadir 1 mL de agua destilada a los nanocompuestos GO/Cu y sonicar la mezcla para dispersar el sedimento de manera uniforme por toda la fase líquida.
NOTA: Recoja todas las soluciones de nanocompuestos GO/Cu en un tubo cónico. - Liofilizar la solución a -60 °C al vacío durante la noche hasta que los nanocompuestos GO/Cu se sequen por completo y se obtenga el polvo de nanocompuestos GO/Cu.
- Guarde el polvo nanocompuesto GO/Cu a -20 °C hasta su uso.
2. Preparación de bacterias para la prueba antibacteriana
PRECAUCIÓN: Este procedimiento debe realizarse en una cabina de seguridad biológica con una lámpara de alcohol. Los residuos bacterianos deben esterilizarse en autoclave antes de su eliminación. Al manipular bacterias resistentes a los antibióticos, se deben usar guantes, batas y mascarillas, y se deben lavar las manos con jabón o desinfectante para manos después del experimento. Desinfectar siempre a fondo; Si se produce contaminación en el área experimental, desinfectarla inmediatamente con etanol al 70%.
- Preparación de medios de cultivo bacteriano
- Mezclar 20 g de agar tríptico de soja y 500 mL de agua destilada en un matraz. Esterilizar la mezcla en autoclave a 121 °C durante 15 min.
- Prepare la placa de agar vertiendo 15 ml de la solución de agar en una placa de Petri antes de que el agar se endurezca. Guarde la placa de agar a 4 °C hasta su uso.
NOTA: Esto debe hacerse rápidamente antes de que la solución de agar se endurezca. Para evitar la contaminación, esterilice la placa de agar con UV durante 15 minutos durante el endurecimiento. - Mezclar 15 g de caldo de soja tríptico (TSB) y 500 mL de agua destilada en un matraz. Esterilizar la mezcla en autoclave a 121 °C durante 15 min.
- Alícuota 40-50 mL de la solución de caldo en un tubo cónico de 50 mL. Conservar el caldo a 4 °C hasta su uso.
NOTA: Para evitar la contaminación, esterilice el caldo alícuota con UV durante 15 min.
- Cultivo bacteriano
- Inocular la solución madre de MSRA o P. aeruginosa en la placa de agar mediante un asa. Incubar la placa de agar a 37 °C utilizando una incubadora agitadora durante 24 h.
- Inocular una colonia de bacterias en 10 ml de caldo usando un asa. Incubar el caldo a 37 °C utilizando una incubadora agitadora a 200 rpm durante 24 h.
- Repita los pasos 2.2.1-2.2.2 una vez más para obtener bacterias con las mismas características.
- Después de 24 h, diluir en serie la solución bacteriana diez veces con agua destilada estéril. Inocular 100 μL de la suspensión bacteriana diluida en la placa de agar y extenderla con un esparcidor. Incubar la placa de agar a 37 °C utilizando una incubadora agitadora durante 24 h.
NOTA: El nivel de dilución depende de las bacterias. Trate de preparar menos de 100 colonias en una placa de agar. - Cuente las colonias bacterianas después de la incubación de 24 h para determinar la unidad formadora de colonias (UFC) utilizando la ecuación (1).
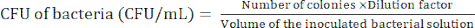 (1)
(1) - Repita los pasos 2.2.4-2.2.5 al menos 3 veces para confirmar si la UFC de las bacterias es relativamente constante.
3. Prueba antibacteriana mediante el método de caldo de microdilución
- Día 1) Inocular una colonia de las bacterias de la placa de agar en 10 mL del caldo usando un asa. Incubar el caldo a 37 °C utilizando una incubadora agitadora a 200 rpm durante 24 h.
- Día 2) Prepare la mezcla de nanocompuestos GO/Cu en al menos tres concentraciones utilizando la solución salina tamponada con fosfato (DPBS) de Dulbecco. Sonicar la suspensión de nanocompuestos GO/Cu hasta que los nanocompuestos GO/Cu estén bien dispersos en DPBS.
NOTA: En este protocolo, se probaron 500, 250, 125 y 62,5 μg/mL de la mezcla de nanocompuestos GO/Cu. - Preparar las soluciones de control. El control negativo es DPBS, y el control positivo es el 1% de una solución de penicilina/estreptomicina en DPBS que matará las bacterias.
- Agregue 100 μL de la suspensión de nanocompuesto GO/Cu y las soluciones de control en placas de 96 pocillos. Agregue todas las muestras por triplicado.
NOTA: Esterilice las muestras con UV durante 15 minutos antes de aplicarlas a las bacterias. - Sobre la base de la UFC después de 24 h de incubación, diluya la suspensión bacteriana con TSB a 1 × 106 UFC/mL.
NOTA: Las concentraciones iniciales de suspensión de cultivo de SARM y P. aeruginosa en nuestro estudio, de acuerdo con el paso 2.2.5, son 4,5 × 109 UFC/mL y 3 × 109 UFC/mL, respectivamente. Las concentraciones bacterianas de 1 × 106 UFC/mL se obtienen diluyendo los cultivos 4.500x y 3.000x, respectivamente. - Inocular 100 μL de la suspensión bacteriana diluida de 1 × 106 UFC/mL en los pocillos de muestra de las placas de 96 pocillos. Incubar las placas de 96 pocillos a 37 °C utilizando una incubadora agitadora a 200 rpm durante 24 h.
NOTA: La concentración final de bacterias es de 5 × 105 UFC/mL después de mezclar con 100 μL de muestra. - Día 3) Mezcle enérgicamente la muestra y las suspensiones bacterianas con una punta de micropipeta de 200 μL. Diluir en serie la mezcla de muestra y bacterias diez veces con agua destilada estéril.
NOTA: El nivel de dilución depende de las bacterias. Trate de preparar menos de 100 colonias en una placa de agar. - Inocular 100 μL de la suspensión bacteriana diluida en la placa de agar y extenderla con un esparcidor. Incubar la placa de agar a 37 °C utilizando una incubadora agitadora durante 24 h.
- Día 4) Contar las colonias bacterianas y determinar los valores de UFC para confirmar la actividad antibacteriana de los nanocompuestos GO/Cu utilizando la ecuación (2).
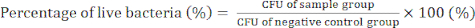 (2)
(2)
Resultados
Se realizaron análisis de microscopía electrónica de transmisión (TEM), microscopía electrónica de barrido (SEM) y espectroscopia de rayos X de dispersión de energía (EDS) para confirmar la formación de nanocompuestos GO/Cu. La Figura 1A, B muestra que se cultivaron nanopartículas heterogéneas de Cu en las láminas de GO. Como se muestra en la Figura 1C, el mapeo EDS confirmó que las partículas en l...
Discusión
En este trabajo se presenta un método sencillo y de bajo costo para la preparación de nanohojas de GO depositadas con nanopartículas de Cu, que sería un método potencialmente eficiente para erradicar bacterias resistentes a antibióticos. El paso crítico en la síntesis de nanocompuestos GO/Cu es dispersar completamente GO y CuCl2 en la solución y mantener una temperatura elevada mientras se mezclan. Además, el paso redox debe realizarse rápidamente porque el agente r...
Divulgaciones
El Dr. Jonghoon Choi es el director ejecutivo y fundador, y el Dr. Yonghyun Choi es el director de tecnología del Instituto de Tecnología Feynman de Nanomedicine Corporation.
Agradecimientos
Esta investigación fue apoyada por la beca de investigación de la Universidad Chung-Ang en 2022 (durante el año sabático del profesor Jonghoon Choi). Esta investigación también fue apoyada por el Programa de Investigación en Ciencias Básicas a través de la Fundación Nacional de Investigación de Corea (NRF), financiado por el Ministerio de Educación (No. RS-2023-00275006), y la subvención del Instituto de Industria y Tecnología del Medio Ambiente de Corea (KEITI) financiada por el Ministerio de Medio Ambiente de Corea (MOE) (No. 2022002980003). El SARM clínico y P. aeruginosa se obtuvieron del Hospital Universitario de Chung-Ang.
Materiales
| Name | Company | Catalog Number | Comments |
| Antibiotic-Antimycotic | Gibco | 15240062 | |
| Clinical MDR bacterial strains | Chung-Ang University Hospital (Seoul, South Korea) | ||
| Copper(II) chloride dihydrate | Duksan | 10125-13-0 | |
| Field Emission Scanning Electron Microscope (FE-SEM) | Carl Zeiss | SIGMA | |
| Graphene oxide | Sigma | 796034 | |
| Sodium Borohydride | Sigma | 71320 | |
| Transmission Electron Microscopy (TEM) | JEOL | JEM-2100 | |
| Tryptic Soy Agar | BD difco | 236950 | |
| Tryptic Soy Broth | BD difco | 211825 |
Referencias
- Doron, S., Gorbach, S. L. Bacterial infections: Overview. International Encyclopedia of Public Health. , 273-282 (2008).
- Van Duin, D., Paterson, D. L. Multidrug-resistant bacteria in the community: An update. Infect Dis Clin North Am. 34 (4), 709-722 (2020).
- Blair, J. M. A., Webber, M. A., Baylay, A. J., Ogbolu, D. O., Piddock, L. J. V. Molecular mechanisms of antibiotic resistance. Nat Rev Microbiol. 13 (1), 42-51 (2015).
- Sánchez-López, E., et al. Metal-based nanoparticles as antimicrobial agents: An overview. Nanomaterials (Basel). 10 (2), 292 (2020).
- Makabenta, J. M. V., et al. Nanomaterial-based therapeutics for antibiotic-resistant bacterial infections. Nat Rev Microbiol. 19 (1), 23-36 (2021).
- Liang, X., Govindaraju, S., Yun, K. Dual applicability of polyaniline coated gold nanorods: A study of antibacterial and redox activity. BioChip J. 12 (2), 137-145 (2018).
- Niño-Martínez, N., Salas Orozco, M. F., Martínez-Castañón, G. A., Torres Méndez, F., Ruiz, F. Molecular mechanisms of bacterial resistance to metal and metal oxide nanoparticles. Int J Mol Sci. 20 (11), 2808 (2019).
- Kim, J., Choi, Y., Park, J., Choi, J. Gelatin-gallic acid microcomplexes release go/cu nanomaterials to eradicate antibiotic-resistant microbes and their biofilm. ACS Infect Dis. 9 (2), 296-307 (2023).
- Jang, J., et al. Development of antibiofilm nanocomposites: Ag/cu bimetallic nanoparticles synthesized on the surface of graphene oxide nanosheets. ACS Appl Mater Interfaces. 12 (32), 35826-35834 (2020).
- Jang, J., Choi, Y., Tanaka, M., Choi, J. Development of silver/graphene oxide nanocomposites for antibacterial and antibiofilm applications. J Ind Eng Chem. 83, 46-52 (2020).
- Bankier, C., et al. Synergistic antibacterial effects of metallic nanoparticle combinations. Sci Rep. 9 (1), 16074 (2019).
- Mendes, C. R., et al. Antibacterial action and target mechanisms of zinc oxide nanoparticles against bacterial pathogens. Sci Rep. 12 (1), 2658 (2022).
- Yoon, S., et al. Biologically benign multi-functional mesoporous silica encapsulated gold/silver nanorods for anti-bacterial applications by on-demand release of silver ions. BioChip J. 13 (4), 362-369 (2019).
- Slavin, Y. N., Asnis, J., Häfeli, U. O., Bach, H. Metal nanoparticles: Understanding the mechanisms behind antibacterial activity. J Nanobiotechnology. 15 (1), 65 (2017).
- Ismail, N. A., et al. Sonochemical synthesis of a copper reduced graphene oxide nanocomposite using honey and evaluation of its antibacterial and cytotoxic activities. Front Mol Biosci. 9, 995853 (2022).
- Tu, Y., et al. Remarkable antibacterial activity of reduced graphene oxide functionalized by copper ions. Adv Funct Mater. 31 (13), 2008018 (2021).
- Li, M., et al. Toward a molecular understanding of the antibacterial mechanism of copper-bearing titanium alloys against staphylococcus aureus. Adv Healthc Mater. 5 (5), 557-566 (2016).
- Yang, Z., et al. Long-term antibacterial stable reduced graphene oxide nanocomposites loaded with cuprous oxide nanoparticles. J Colloid Interface Sci. 533, 13-23 (2019).
- Yang, Y., et al. Graphene oxide/copper nanoderivatives-modified chitosan/hyaluronic acid dressings for facilitating wound healing in infected full-thickness skin defects. Int J Nanomedicine. 15, 8231-8247 (2020).
- Mao, M., et al. Graphene oxide-copper nanocomposites suppress cariogenic streptococcus mutans biofilm formation. Int J Nanomedicine. 16, 7727-7739 (2021).
- Ravikumar, V., Mijakovic, I., Pandit, S. Antimicrobial activity of graphene oxide contributes to alteration of key stress-related and membrane bound proteins. Int J Nanomedicine. 17, 6707-6721 (2022).
- Afreen, G., Shoeb, M., Upadhyayula, S. Effectiveness of reactive oxygen species generated from rgo/cds qd heterostructure for photodegradation and disinfection of pollutants in waste water. Mater Sci Eng C. 108, 110372 (2020).
- Yang, F., et al. Fabrication of graphene oxide/copper synergistic antibacterial coating for medical titanium substrate. J Colloid Interface Sci. 638, 1-13 (2023).
- Rajapaksha, P., et al. Antibacterial properties of graphene oxide-copper oxide nanoparticle nanocomposites. ACS Appl Bio Mater. 2 (12), 5687-5696 (2019).
- Sachdeva, C., Satyamoorthy, K., Murali, T. S. Microbial interplay in skin and chronic wounds. Curr Clin Microbiol Rep. 9 (3), 21-31 (2022).
- Ramos, M. K., Zarbin, A. J. G. Graphene/copper oxide nanoparticles thin films as precursor for graphene/copper hexacyanoferrate nanocomposites. Appl Surf Sci. 515, 146000 (2020).
- Fivenson, E. M., et al. A role for the gram-negative outer membrane in bacterial shape determination. PNAS. 120 (35), e2301987120 (2023).
- Wu, C., et al. Copper-containing mesoporous bioactive glass scaffolds with multifunctional properties of angiogenesis capacity, osteostimulation and antibacterial activity. Biomater. 34 (2), 422-433 (2013).
- Zhang, W., et al. Graphene oxide-copper nanocomposite-coated porous cap scaffold for vascularized bone regeneration via activation of hif-1α. Adv Healthc Mater. 5 (11), 1299-1309 (2016).
- Labauve, A. E., Wargo, M. J. Growth and laboratory maintenance of pseudomonas aeruginosa. Curr Protoc Microbiol. 25 (1), 6E.1.1-6E.1.8 (2012).
- Lin, J., et al. The icmf3 locus is involved in multiple adaptation- and virulence-related characteristics in pseudomonas aeruginosa pao1. Front Cell Infect Microbiol. 5, 70 (2015).
Reimpresiones y Permisos
Solicitar permiso para reutilizar el texto o las figuras de este JoVE artículos
Solicitar permisoExplorar más artículos
This article has been published
Video Coming Soon
ACERCA DE JoVE
Copyright © 2025 MyJoVE Corporation. Todos los derechos reservados