Method Article
Irritation des yeux Test (IET) pour l'identification des dangers des produits chimiques irritants oculaires utilisant épithélial (RHCE) Tissue modèle reconstruit humain Cornea-like
Dans cet article
Résumé
Nous avons développé un test d'irritation des yeux qui utilise un modèle de tissu tridimensionnel épithéliale reconstruit cornée comme humaine (RHCE). Le test est capable de discriminer entre irritation oculaire et des matériaux corrosifs (SGH Catégories 1 et 2 combinés) et ceux qui ne nécessitent pas d'étiquetage (SGH sans catégorie).
Résumé
Pour se conformer à la septième amendement à la législation de l'UE Directive Cosmétique et de l'UE REACH, validées méthodes alternatives non animales pour l'évaluation fiable et précise de la toxicité oculaire chez l'homme sont nécessaires. Pour répondre à ce besoin, nous avons développé un test d'irritation des yeux (IET), qui utilise un modèle tridimensionnel reconstruit humaine cornée comme épithéliale (RHCE) tissu qui est basée sur des cellules humaines normales. L'IET est capable de séparer les irritants et corrosifs oculaires (SGH catégories 1 et 2 combinés) et ceux qui ne nécessitent pas d'étiquetage (SGH sans catégorie). Le test utilise deux protocoles séparés, l'un conçu pour des produits chimiques liquides et un deuxième protocole similaire pour les articles d'essai solides. Le modèle de prédiction IET utilise une seule période d'exposition (30 min pour les liquides, 6 heures pour les solides) et un seul la viabilité des tissus coupure (60,0% tel que déterminé par le test MTT). Basé sur les résultats de 83 produits chimiques (44 liquides et 39 solides) EIT atteint 95,5 / 68,2 / 81,8% et Sensibilité / spécificité et la précision (SS & A) pour les liquides, 100,0 / 68,4 / 84,6% et de SS & A pour les matières solides, et 97,6 / 68,3 / 83,1% et pour l'ensemble SS & A. L'IET contribuera de manière significative à classer le potentiel d'irritation oculaire d'un large éventail de produits chimiques liquides et solides, sans l'utilisation d'animaux pour satisfaire aux exigences d'essais réglementaires. La méthode EpiOcular IET a été réalisé en 2015 dans les directives de l'OCDE que TG 492.
Introduction
Les produits de consommation tels que les cosmétiques, les détergents et produits de nettoyage domestiques comprennent une variété de produits chimiques qui peuvent provoquer des lésions graves si elles en contact avec les yeux. Par conséquent, les tests de ces agents pour irritation des yeux est requis par les organismes de réglementation des États-Unis et de l'UE pour assurer la sécurité des consommateurs 1. Une évaluation du potentiel d'irritation oculaire de mélanges et formulations est aussi une exigence de se conformer à REACH (enregistrement, évaluation, autorisation et restriction des produits chimiques) de la législation sur l'étiquetage des ingrédients cosmétiques en vertu de la directive européenne sur les cosmétiques pour le transport de produits chimiques, et pour l'étiquetage des pesticides et des produits ménagers 2. Actuellement, les organismes de réglementation exigent une évaluation de risque oculaire à l'aide du Système général harmonisé de classification et d'étiquetage des produits chimiques (SGH) 3. SGH est principalement basée sur le test d'irritation oculaire de Draize, test d'irritation des yeux le plus largement utilisé dans lequel les substances étrangères et mixtures sont introduits directement dans le sac conjonctival de l'oeil de lapin 4. Selon la classification SGH, SGH Catégorie 1 (corrosives pour l'œil) se réfère à tester les produits chimiques qui causent la blessure initiale sévère pour les tissus oculaires ou de graves dommages à l'œil et de la vision qui est pas totalement réversibles dans les 21 jours suivant l'exposition 3,5. SGH Catégorie 2 se réfère à tester les produits chimiques qui produisent des changements importants dans l'œil qui sont totalement réversibles dans les 21 jours d'exposition. Produits chimiques de test qui ne sont pas corrosifs ou irritants sont appelés SGH Non Catégorie.
Depuis plus de 40 ans, le test de Draize lapin a été critiqué pour son manque de reproductibilité, surestimation des réactions humaines, et l'utilisation d'animaux vivants 5-8. Ces préoccupations ont encouragé de nombreuses propositions pour le raffinement, la réduction et le remplacement de l'essai in vivo 9. La nécessité d'alternatives validées non animales a été renforcéepar l'adoption de la septième amendement à la directive sur les cosmétiques, qui interdit l'utilisation d'animaux dans l'évaluation de la sécurité des produits cosmétiques (en 2005) et des ingrédients (en 2009) 2.
Depuis 1996, le modèle de tissu de la cornée comme reconstruite a été largement utilisé par l'industrie cosmétique pour évaluer le potentiel d'irritation des matières premières, des formulations à base de tensioactifs, et les mélanges qui sont conçus pour une utilisation dans aggravée, ou dans le voisinage de l'oeil 10-13. L'utilisation du modèle de tissu RHCE permet une application topique directe du matériau d'essai sur la surface du tissu dans sa forme non diluée natif. De cette manière, des formulations solubles dans l'eau non peuvent être testées sans les diluer avec des solvants. En réponse à des EURL ECVAM (Union européenne Laboratoire de référence Centre européen pour le validation des méthodes alternatives) demande d'une méthode largement applicable, simple, économique et du test d'irritation des yeux (IET), qui utilise un single temps d'exposition et est en mesure de séparer les irritants et corrosifs oculaires à partir de matériaux qui ne nécessitent pas d'étiquetage a été développé (figure 1) 14. Basé sur les résultats de 83 produits chimiques (44 liquides et 39 solides), l'IET atteint 95,5 / 68,2 / 81,8% de sensibilité / spécificité et la précision (SS & A) pour les liquides, 100,0 / 68,4 / 84,6% de SS & A pour les matières solides, et 97,6 / 68,3 / 83,1% et pour l'ensemble SS & A.
En 2007, une étude de pré-validation multi-laboratoire parrainé par Cosmetics Europe (anciennement Colipa) sous les auspices de l'ECVAM EURL évalué la pertinence et la fiabilité de l'IET dans le but de l'amener à une validation formelle 15. Dans cette étude, 298 essais indépendants ont été effectués dans sept des laboratoires indépendants. Résultats de l'étude ont démontré un accord de 99,7% dans la prédiction avec de faibles coefficients de variation dans tous les laboratoires participants 15. En conséquence, en 2010, le protocole est entré dans une IET formelle EURL ECVAMprogramme de validation. L'étude de validation utilisé 104 produits chimiques d'essai codés, y compris les substances individuelles et les mélanges de produits chimiques, pour lesquels des données de référence in vivo (Draize de données d'irritation oculaire) étaient disponibles. Basé sur le succès de ce travail, un projet d'orientation test OCDE a été présenté en 2014. Il est prévu que l'IET contribuera de manière significative à la classification du potentiel d'irritation oculaire d'un large éventail de matériaux en fonction de la classification et de l'étiquetage SGH des Nations unies.
Protocole
1. Préparation des tissus pour le traitement RHCE - Jour 0
- Dès réception du kit épithéliale commerciale de la cornée comme humaine (RHCE), vérifiez tous les composants du kit pour l'intégrité (pour les détails de Kit Voir standard Assay Kit Composants (tableau 1) et de l'équipement et des matériaux nécessaires pour réaliser le dosage IET (tableau 2). Sur le jour de la réception, équilibrer les tissus (dans son récipient de 24 puits expédition) à la température ambiante pendant 15 min.
| Montant | Réactif | Conditions | Source | Description | Date d'expiration |
| 1 | Sealed plaque de 24 puits de tissus EpiOcular (OCL-200) | 8.2 ° C | MatTek | Contient 24 tissUES de culture cellulaire inserts, paquet sur agarose | 72 h |
| 1 bouteille, 200 ml | EpiOcular milieu de dosage (OCL-200-ASY) | 8.2 ° C | MatTek | Milieu à base de DMEM | 21 jours |
| 1 bouteille, 100 ml | Mg ++ Ca ++ -Livraison Dulbecco-PBS (DPBS) | RT | Sigma-Aldrich, D5652, ou équivalent. | Utilisée pour le rinçage des inserts | 1 an |
| 4 | 6 puits Plaques | RT | Faucon | Utilisé pour le maintien des tissus lors de protocole de dosage | N / A |
| 2 | 12 puits Plaques | RT | Faucon | Utilisé pendant protocole de dosage | N / A |
| 2 | 24 puits Plaques | RT | Faucon | Utilisé pour effectuer un test MTT | N / A |
| 1 flacon, 0,5 ml | Acétate de méthyle (CAS 79-20-9 #) | RT | Sigma-Aldrich, Cat # 186325 | Utilisé comme PC dans le test | 1 mois |
Tableau 1: Etalon Dosage des composants du kit.
| / Matériel | Nécessaire pour: |
| Incubateur humidifié (37 ± 1 ° C, 5 ± 1% de CO2, 90% d'humidité 10 ±) | Incubation des tissus avant et pendant les essais |
| Hotte à flux laminaire | Sécurité au travail dans des conditions stériles |
| Pompe à vide (facultatif) | Aspiration des solutions à moyen et |
| Plate-lecteur photomètre (pour les plaques à 96 puits) | Lecture OD |
| Agitateur de plaque | Extraition de formazan |
| Forceps, émoussées tranchant stériles | Manipulation des inserts de tissu |
| Chronomètres | La période d'application du matériel de test et d'autres étapes chronométrées dans le protocole |
| Bain-marie (37 ± 1 ° C) | Le réchauffement et les médias solution MTT |
| Mortier et un pilon | Grincement solides granulaires |
| Volumétriques pipette (50 ul) | Application des matériaux et des suspensions visqueuses ou semi-solides |
| Pipettes réglables (200 pi-2 ml) | Application de matériaux liquides, milieu de dosage et MTT |
| Pré-stérilisé conseils (200 pi et 20 pi), Rainin Cat # HR-200F et HR-20F (ou équivalent) | Application de matériaux liquides, milieu de dosage et MTT |
| Conseils large orifice de pré-stérilisés (250 pi), Rainin Cat # HR-250WS (ou équivalentalent) | Application des matériaux et des suspensions visqueuses ou semi-solides |
| 8 oz / 220 ml conteneurs spécimen, Falcon Cat # 3540200 (ou équivalent) | Rinçage tissus |
| Stériles seringues à usage unique (par exemple 1 ml tuberkulin seringue Omnifix-F, B. Braun AG, cat. N ° 9161406V) | Livraison de ~ 50 mg matériaux solides (facultatif) |
| Ted Pella micro spatule / cuillère, Ted Pella Inc., Cat # 13504 (ou équivalent, une cuillère ou d'os forte curette, par exemple, Aesculap, No: FK 623) | Livraison de ~ 50 mg matériaux solides |
| Ca ++ et Mg ++ phosphate solution saline tamponnée de libre Dulbecco (Ca ++ Mg ++ Free-DPBS): Sigma-Aldrich, Cat # D5652 (ou équivalent) | Tissus rinçage lors dosage |
| Stérile l'eau déminéralisée, tissus qualité culture (qualité biologique ou équivalent) | Utiliser comme NC |
| Plaques de 96 puits à fond plat, Falcon (ou équivalent) | Pour lire OD |
| Swaps de coton-tige (stérile) | Pour le séchage de la surface du tissu (facultatif) |
| Ruban adhésif ou Parafilm | Couvrant plaques lors de l'extraction de formazan |
| Kit de dosage MTT-100 | Contient réactif MTT-bleu de thiazolyle Tetrazolium bromure (Sigma # M-5655) et de l'isopropanol extrait. |
Tableau 2: Equipement et matériaux nécessaires pour effectuer l'IET.
- Dans des conditions stériles, ouvrir le sac en plastique contenant la plaque de 24 puits avec les tissus RHCE et retirer la gaze stérile. Inspectez tous les tissus de bulles d'air entre le gel d'agarose et insérer. Ne pas utiliser les cultures avec des bulles d'air sous la couverture d'insertion> 50% de la zone d'insertion, tissus défectueux, ou des tissus WHI ch sont entièrement recouvert de liquide.
- Étiqueter les plaques de 6 puits avec l'article d'essai ou des codes de contrôle et de temps d'exposition. Aliquotes de 1,0 ml de milieu de dosage (fournies avec le kit), préchauffée à environ 37 ° C, dans les puits de plaques de 6 puits pré-étiquetés.
- Utilisez des pinces stériles pour supprimer chaque insert contenant le tissu RHCE et placer l'insert dans la plaque de 6 puits marqué. Lors de cette étape, enlever toute agarose d'expédition restant qui adhère aux côtés extérieurs de l'insert par blot douce sur du papier filtre stérile. Libérer les bulles d'air piégées sous les inserts.
- Pré-incuber les tissus RHCE dans les plaques de 6 puits à des conditions standard de culture (CSC, atmosphère humidifiée avec 5 ± 1% de CO 2 à 37 ± 1 ° C) pendant 1 heure.
- Après 1 h, remplacer le milieu de dosage avec 1,0 ml de milieu de dosage frais préchauffé à 37 ° C et incuber les tissus RHCE à des conditions de SCC (nuit = O / N) (16-24 h).
- Après le O / N incubation, 20 ul d'appliquer Ca2 + Mg2 + Phosphate Buffered Saline exempt de-Dulbecco (DPBS, à condition) en utilisant un dispositif de pipetage appropriées. Si le DPBS ne se propage pas à travers les tissus, tapotez doucement l'insert sur la plaque pour assurer que les DPBS mouille la surface du tissu ensemble.
- Incuber les tissus RHCE au CCN pour 30 ± 2 min.
Remarque: Cette étape est nécessaire pour l'hydratation des tissus et de mimer les conditions in vivo.
3. Procédures de l'exposition Test matériel
- Appliquer chaque article et les contrôles test pour reproduire tissus RHCE (n = 2). La procédure article d'essai de dosage est différent pour liquides et solides. Appliquer localement 50 pi d'articles liquides de test à l'aide d'une pipette. Le temps d'exposition pour les liquides est de 30 min. Appliquer 50 mg d'articles de test solides en utilisant une cuillerée nivelé (calibrée pour contenir 50 mg de chlorure de sodium). L'extemps de exposi- pour les matières solides est de 6 h.
Note: Les liquides sont définies comme des substances fluides (par exemple, des liquides, des gels, des crèmes) et qui peuvent être appliquées en utilisant un dispositif de pipetage. Les solides sont définies comme des substances non-liquide (par exemple, des poudres, des matières résineuses ou cireux) qui ne peuvent pas être appliqués à l'aide d'une pipette.- Si l'état physique des articles d'essai ne sont pas facile à déterminer, placer les flacons de l'article d'essai dans un bain-marie pendant 15 min (37 ° C). Suivre le protocole IET pour les liquides pour ces articles de test qui se liquéfient à 37 ° C.
- Utiliser une pipette volumétrique pour matériaux particulièrement visqueux.
- Doser le contrôle négatif et de contrôles positifs d'abord et ensuite doser les articles de test.
- Appliquer 50 pi du contrôle négatif (NC) et le contrôle positif (PC) pour les tissus RHCE aide d'une pipette standard. Le NC est de l'eau déminéralisée stérile; le PC est l'acétate de méthyle (CAS # 79-20-9). Appliquer le NC et PC pendant 30 minutes lorsque le testtion des articles liquides de test et pendant 6 heures lors de l'essai des articles de test solides.
4. Testez l'article Exposition - Jour 1
- Pour le traitement des articles liquides de test, suivre le calendrier de synchronisation donnée dans le tableau 3. Donner des intervalles de 1 min entre les applications de chaque article de test pour assurer une exposition égale pour tous les tissus.
- Après 30 ± 2 min dPBS de pré-traitement, appliquer localement 50 pi de NC et PC, et chaque article d'essai liquide topique sur les tissus RHCE en utilisant un dispositif de pipetage approprié.
- Appliquer 50 pi de l'article d'essai liquide directement sur le tissu pour couvrir la surface supérieure. Coupez la pointe de la pointe de la pipette étroite pour élargir l'orifice pour les matériaux visqueux. Pour les matériaux très visqueux, appliquer l'article de test à un dispositif de dosage (un cylindre à tête plate de diamètre légèrement inférieur au diamètre intérieur de l'insert de tissu ou une punaise de plastique), inverser le dosage dériphérique et le placer sur le tissu de sorte que l'article à tester uniformément contact avec la surface des tissus.
- Si l'article de test ne se propage pas à travers le tissu, tapotez doucement la pièce pour vous assurer qu'il se répand sur la surface du tissu ensemble. Épandage mécanique des articles de test (par exemple, avec une pointe de pipette) est déconseillée car elle peut endommager les tissus.
- Incuber les tissus au CCN pour 30 ± 2 min.
- Pour le traitement des articles de test solides - Jour 1, suivre le calendrier de synchronisation donnée dans le tableau 4 Donner des intervalles de 2 min entre les applications de chaque article de test pour assurer une exposition égale pour tous les tissus..
- Après 30 ± 2 min dPBS de pré-traitement, appliquer 50 pi de NC et PC topique sur les tissus RHCE en utilisant un dispositif de pipetage approprié.
- Pour solide demande d'article de test, retirer les inserts (n = 2) du puits et de les placer sur une surface stérile (par exemple, le couvercle de hplaque ultiwell) pour éviter un article de test répandre dans le milieu.
- Avec une cuillère nivelée, appliquer localement environ 50 mg de l'article d'essai sur la surface du tissu; faire en sorte que la surface du tissu est entièrement recouverte par l'article d'essai. Si l'article d'essai ne se propage pas à travers le tissu, secouez l'insert doucement de gauche à droite pour s'assurer que le tissu est complètement recouvert par l'article d'essai. Épandage mécanique des articles de test (par exemple, avec une pointe de pipette) est déconseillée car elle peut endommager les tissus.
- Si nécessaire, rectifier poudres cristallines avec un mortier et un pilon pour garantir un meilleur contact entre l'article d'essai et le tissu.
- Sinon, placez poudres directement sur la culture de tissus à l'intérieur de l'insert en utilisant une seringue de 1 ml avec sa tête coupée. Poudres de fourrer dans la seringue lorsque le piston est tiré en arrière et puis appliquent en appuyant sur le piston vers le bas.
- Si la paroi extérieure de l'insert est contaminated par exemple, par des poudres, essuyez les particules avec une gaze stérile.
- Après le dosage, retourner les tissus à des plaques de 6 puits contenant du milieu de culture et incuber à CSC pendant 6 h ± 15 min.
5. Rinçage
- Préparer une série de trois béchers propres (150 ml de capacité) par article de test et de remplir chacun d'eux avec 100 ml de DPBS. Pour chaque article de test, utiliser un ensemble différent de trois béchers.
- À la fin de l'exposition de ± 2 min 30 pour les matières liquides ou 6 h ± 15 min exposition pour les matières solides, retirez et jetez le dispositif de dosage si elle a été utilisée.
- Soulever les inserts contenant le tissu RHCE sur le moyen de préhension par le bord supérieur de la "collerette" plastique avec une pince fine. Utilisez une pince incurvées pour faciliter la manipulation et la décantation. Rincer les tissus deux à la fois en tenant les inserts en double ensemble par leurs colliers à l'aide de forceps. Soyez prudent nOT endommager les tissus avec la pince.
- Décanter les articles d'essai ou de contrôle de la surface du tissu sur un matériau absorbant propre (serviettes en papier, gaze, etc.)
- Tremper les inserts dans le premier bécher de DPBS, tourbillonner dans un mouvement circulaire dans le DPBS environ 2 secondes, lever les inserts de sorte qu'ils sont souvent remplis avec du DPBS, et décanter le liquide dans le bécher. Répétez ce processus à trois reprises dans le premier bécher.
- Rincer les inserts dans les deuxième et troisième béchers de DPBS trois fois chacun de la même manière.
- Décanter le liquide restant dans l'insert sur le matériau absorbant. Tournez l'insert à un angle de 45 ° (extrémité ouverte vers le bas) approximatives et toucher la lèvre supérieure de la matière absorbante.
Remarque: Si il est pas possible d'enlever tout le matériel de test visible, aucune autre rinçage doit être fait pour éviter d'endommager des tissus due à une manipulation excessive.
6. post-trempage
- Après rinçage,immerger immédiatement les tissus dans 5 ml de milieu de dosage précédemment chauffé à la température ambiante dans une plaque à 12 puits pré-marqué.
- Incuber les tissus de 12 ± 2 min pour les matières liquides ou 25 ± 2 min pour les matières solides immergés à la température ambiante pour faciliter l'élimination de n'importe quel article d'essai résiduel.
7. post-incubation
- À la fin de l'après-tremper période d'immersion, décanter le milieu de dosage à partir des tissus et épongez les inserts sur un matériau absorbant.
- Transférer les inserts dans la plaque de 6 puits pré-étiquetés contenant 1 ml de milieu de dosage chaude.
- Incuber les tissus pour 120 ± 15 min au CSC pour les matières liquides de test.
- Incuber les tissus pour 18 ± 0,25 h à SCC pour le matériel de test solides.
8. MTT dosage de viabilité - Jour 1 (Protocole pour les liquides) et le Jour 2 (Protocole pour les solides)
- Effectuez le test MTT après la post-incubation de 12077; 15 min pour les liquides et de 18 ± 0,25 h pour les matières solides, respectivement.
- Préparer 1,0 mg / ml de solution MTT et aliquote de 0,3 ml de la solution dans chaque puits d'une plaque de 24 puits pré-étiquetés.
- Utilisez le kit de MTT commerciale (tableau 5):
- 2 heures avant utilisation, décongeler le concentré de MTT à TA. Moissonneuse 2 ml du concentré de MTT et 8 ml de diluant pour produire MTT 1,0 mg / ml de solution MTT.
- Conserver la solution MTT à 4 ° C dans l'obscurité jusqu'à utilisation. Ne pas conserver la solution MTT pour plus de 1 jour.
- À la fin de la Poste incubation, retirez chaque insert de la plaque de 6 puits et éponger doucement sur un matériau absorbant.
- Placez les inserts dans la plaque de 24 puits contenant 0,3 ml de solution de MTT. Libérer les bulles d'air piégées sous les inserts. Incuber la plaque de 180 ± 10 min au CSC.
- Extraction MTT
- Après 180 ± 10 min d'incubation dans la solution de MTT, retirez chaque insertà partir de la plaque à 24 puits et efface le fond de l'insert sur un matériau absorbant.
- Pour les articles d'essai de liquide non colorantes (extraction) immergée: transférer les inserts dans une plaque à 24 puits pré-marqué contenant 2,0 ml d'une solution d'extraction (isopropanol) de sorte qu'elle submerge l'insert.
- Pour les solides et colorants liquides (non-immergé extraction pour éviter la contamination de la solution d'extraction): Transférer les insertions dans une plaque à 6 puits pré-étiquetés contenant 1,0 ml de la solution d'extraction (isopropanol) de sorte qu'il ne submerge pas l'insert.
Remarque: Effectuez la même extraction non-immergée pour les contrôles positifs et négatifs correspondants.
- Sceller les plaques (par exemple, avec du parafilm entre le couvercle de la plaque et le bord supérieur des puits ou avec un scellant pour plaques standard). Placez les plaques sur une plaque agitation et agiter pendant 2 à 3 heures à température ambiante pour extraire le MTT.
- Sinon, effectuer l'extraction O / N à 2-876; C dans l'obscurité sans agitation.
- Pour les articles de test de liquide non colorantes (extraction immergée): A la fin de la période d'extraction, décanter le liquide de chaque insérer dans le puits et jeter les inserts avec les tissus RHCE.
- Mélanger la solution d'extrait et transférer deux aliquotes de 200 ul dans les puits appropriés d'une plaque de 96 puits pré-étiquetés conformément à la configuration de la plaque (figure 2).
- Pour les solides et colorants liquides (extraction non-immergée): A la fin de la période d'extraction, jeter les tissus (assurez-vous de ne pas percer les tissus).
- Ajouter 1,0 ml de la solution d'extraction dans chaque puits de la plaque à 24 puits contenant la solution extraite à partir des tissus. Mélanger la solution d'extraction et le transfert de deux aliquotes de 200 dans les puits appropriés d'une plaque à 96 puits pré-marqué selon la configuration de la plaque (figure 2).
- Déterminer til densité optique (DO) des échantillons extraits à une seule longueur d'onde entre 550 et 590 nm (doit être cohérente au sein d'un laboratoire) sur un lecteur de plaque ou d'un spectrophotomètre.
- Dans le cas de solutions d'extrait troubles causés par des matières solides insolubles, centrifuger les solutions antérieures à mesure de la DO (refroidir la centrifugeuse à 4 ° C pour éviter l'évaporation). En cas de rinçage ne supprime pas l'article d'essai (TA) et le TA interfère avec réduction du MTT, des contrôles supplémentaires doivent être utilisés. S'il vous plaît se référer à une SOP détaillée pour corriger pour la réduction MTT 16.
- Dans le cas d'un TA est indiqué d'avoir ou de développer la couleur qui peut interagir avec la mesure de MTT, un test supplémentaire doit être effectuée afin de déterminer la quantité de couleur lié à, puis extraite à partir des tissus. S'il vous plaît se référer à une SOP détaillée pour corriger les articles d'essai colorées 16.
9. Les calculs pour la viabilité des tissus d'essai (tableau 6 et figure 3) & #160;
- Calculs généraux
- Calculer la valeur moyenne de la DO des puits témoins à blanc (OD noir) pour chaque expérience.
- Soustraire OD Blk de chaque valeur de DO de la même expérience (noir données corrigées).
- Calculer la valeur moyenne des deux fractions aliquotes de chaque tissu (DO = corrigé).
- Calculer la viabilité pour cent de chacun des deux tissus réplicats pour chaque commande et de l'article d'essai par rapport au témoin négatif moyenne (contrôle à 100%).
Viabilité (%) = [OD tissus traités / OD corrigée contrôle négatif corrigé] x 100% - Calculer la différence de la viabilité (la différence de viabilité entre deux tissus réplicats).
- Calculer l'article à tester la viabilité moyenne (TA de viabilité) et classer l'article d'essai en fonction du modèle de prédiction.
10. Modèle de prévision (figure 3)
- Si la viabilité du tissu TA-traitée est> 60,0 par rapport à NC-traitée tissus vESPONSABILITE, étiquette sur l'article de test non irritant (NI) (SGH Pas de catégorie).
- Si la viabilité du tissu TA-traitée est ≤ 60,0 par rapport à la viabilité des tissus NC-traitée, étiquette sur l'article de test comme irritant (I) (SGH Catégories 1 et 2).
Remarque: Les résultats des tests de l'IET sont considérées qualifié si:- l'OD IET NC> 0,8 et <2,5;
- la viabilité du tissu IET PC (%, par rapport à NC) est ≤50.0%;
- la différence entre les deux tissus identiques (NC, PC, et de l'article d'essai) est <20,0%.
Résultats
Résultats transition représentatifs effectués avec 10 des articles de test (TA) et des témoins négatifs et positifs sont présentés dans le tableau 6 et la Figure 3. La DO moyenne = 1,31 pour le NC correspond à 100% la viabilité des tissus, par conséquent, l'ordinateur (DO moyenne = 0,41) avaient la viabilité des tissus relative de 31,2%. Lorsque le protocole EIT a été réalisée dans 15 expériences indépendantes valides dans 7 laboratoires en utilisant le protocole d'exposition liquide et à 8 expériences valides indépendants dans 4 laboratoires, en utilisant le protocole d'exposition solide, la viabilité des tissus moyen de l'ordinateur en utilisant le protocole de liquide était de 36,4 ± 4,0 % et 32,3 ± 6,4% pour le protocole de solides. Dans tous les cas, les résultats de contrôle positifs étaient en dessous de la valeur de coupure de 60,0% 15.
Comme le montre la figure 3, TA1, TA2, TA4, TA7 et TA8 eu viabilités des tissus> 60,0% et ont donc été classés comme «NI». TA3, TA5, TA6, TA9, TA10 et avait viabilités de tissus X04; 60,0% et ont donc été classés comme "I". La différence de la viabilité des tissus entre les tissus en double était <20,0% pour l'ensemble des PS avec une exception de TA2. Par conséquent, les résultats de tous les articles de test, avec une exception de TA2, ont été considérés comme «qualifié», car ils répondaient à tous les critères d'acceptation de l'IET (article 10.2). En raison de la grande variabilité entre les tissus en double pour TA2 dans l'expérience initiale, une deuxième expérience était nécessaire pour obtenir des résultats qualifiés de l'IET.
La méthode d'essai IET comme décrit ici en utilisant le modèle de tissu RHCE a été utilisé pour l'évaluation de l'irritation oculaire dans plusieurs études de validation multilaboratoires, y compris la validation formelle par EURL ECVAM / Cosmetics Europe 15,17-19. Dans toutes les études, l'IET a été montré pour être reproductible et a été en mesure d'identifier correctement les produits chimiques (substances et mélanges) ne nécessitant pas de classification et d'étiquetage de l'irritation oculaire ou des lésions oculaires graves acCording au SGH des Nations unies 15,17-19. La méthode d'essai IET remplissait les critères d'acceptation du Groupe de gestion de la validation (VMG) pour irritation des yeux pour la sensibilité, la spécificité et la précision globale et il est actuellement en instance mise en œuvre formelle comme un remplacement partiel pour le lapin in vivo test de Draize 19.
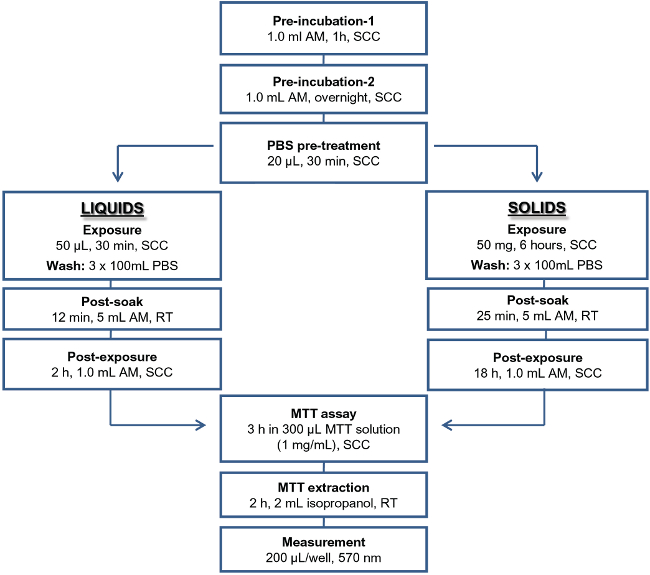
Figure 1: Schéma du protocole IET pour liquides et solides des articles de test abréviations utilisées: AM, milieu de dosage;. CSC, conditions de culture standard; PBS, saline tamponnée au phosphate de Dulbecco; RT température ambiante.
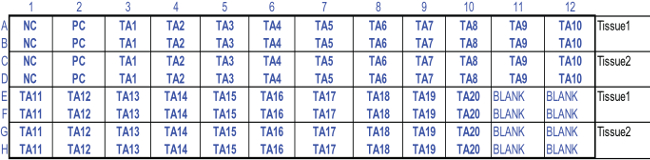
Figure 2:. La configuration de la plaque de 96 puits normalisé pour le test MTT de la viabilité des tissus 200 Deux aliquotes sont transferred dans les puits appropriés d'une plaque pré-marquée de 96 puits. Les abréviations utilisées: NC, contrôle négatif; PC, contrôle positif; TA1-TA20, articles de test 1-20; Blank, solution d'extraction. 96- configuration de plaque de MTT est utilisé avec Excel conçu pour calculer RHCE la viabilité des tissus et des résultats de l'IET.
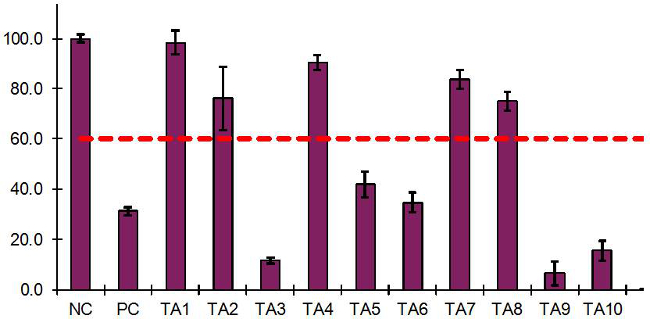
Figure 3: les résultats obtenus pour l'IET articles 10 de test, NC et les contrôles de PC en utilisant le modèle de tissu RHCE Le graphique est générée à partir d'une feuille de calcul Excel conçu pour présenter les résultats de l'IET.. Produits chimiques d'essai qui réduit la viabilité des tissus ≤ 60,0% par rapport à NC sont classés comme irritants ("I", TA3, TA5, TA6, TA9 et TA10) et les produits chimiques de test qui avait la viabilité des tissus> 60,0% sont classés comme non-irritants (" NI ", TA1, TA2, TA4, TA7 et TA8).
| Heure de départ pour les étapes de travail du protocole IET (le d'une journée de travail pour un opérateur) | |||||||
| Chaque ligne correspond à une paire de tissus | |||||||
| Ordre des étapes: | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Liquides: | PBS | TA Exposition | Post- Faire tremper | Post- Incub. | MTT Réaction | MTT Extraction | Mesure |
| 30 min | 30 min | 12 min | 120 min | 180 min | 120 min | OD | |
| Caroline du Nord | 09h00 | 09:30 | 10h00 | 10h12 | 12h12 | 15h12 | après |
| Ordinateur personnel | 09h01 | 09h31 | 10h01 | 10h13 | 12h13 | 15h13 | 17h30 |
| TA-1 | 09h02 | 09h32 | 10h02 | 10h14 | 12h14 | 15h14 | |
| TA-2 </ strong> | 09h03 | 09h33 | 10h03 | 10h15 | 12h15 | 15h15 | |
| TA-3 | 09h04 | 09h34 | 10h04 | 10h16 | 12h16 | 15h16 | |
| TA-4 | 09h05 | 09h35 | 10h05 | 10h17 | 12h17 | 15h17 | |
| TA-5 | 09h06 | 09h36 | 10h06 | 10h18 | 12h18 | 15h18 | |
| TA-6 | 09h07 | 09h37 | 10h07 | 10h19 | 12h19 | 15h19 | |
| TA-7 | 09h08 | 09h38 | 10h08 | 10h20 | 12h20 | 15h20 | |
| ng> TA-8 | 09h09 | 09h39 | 10h09 | 10h21 | 12h21 | 15h21 | |
| TA-9 | 09h10 | 9h40 | 10h10 | 10h22 | 12h22 | 15h22 | |
| TA-10 | 09h11 | 09h41 | 10h11 | 10h23 | 12h23 | 15h23 | |
Tableau 3:. Calendrier Exemple de l'essai des articles liquides de test étapes de Protocole, notamment en pré-mouiller les tissus avec DPBS, l'application des articles de test (AT), au rinçage et post-trempage, la période post-incubation, test MTT, Extraction de MTT, et évaluation de MTT OD sont présentés dans des colonnes. Fois pour les tissus doubles sont organisées en rangées. Les entières tests de dosage 10 PS et les contrôles peuvent être finis en une seule journée.
e_content ">| Heure de départ pour les étapes du protocole de l'IET (2 jours de travail pour un opérateur) | |||||||
| Chaque ligne correspond à une paire de tissus | |||||||
| Jour 1 | Jour 2 (le lendemain) | ||||||
| Ordre des étapes: | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| Solides: | PBS | TA Exposition | Post- Faire tremper | Post- IncubAction | MTT Réaction | MTT Extraction | Mesure |
| 30 min | 6 heures | 26 min | 18 h | 180 min | 120 min | OD | |
| Caroline du Nord | 09h00 | 09:30 | 15h30 | 15h56 | 09h56 | 12h56 | après |
| Ordinateur personnel | 09h02 | 09h32 | 15h32 | 15h58 | 09h58 | 12h58 | 15h30 |
| TA-1 | 09h04 | 09h34 | 15h34 | 16h00 | 10h00 | 13h00 | |
| TA-2 | 09h06 | 09h36 | 15h36 | 16h02 | 10h02 | 13h02 | |
| TA-3 | 09h08 | 09h38 | 15h38 | 16h04 | 10h04 | 13h04 | |
| TA-4 | 09h10 | 9h40 | 15h40 | 16h06 | 10h06 | 13h06 | |
| TA-5 | 09h12 | 09h42 | 15h42 | 16h08 | 10:08 | 13h08 | |
| TA-6 | 09h14 | 09h44 | 15h44 | 16h10 | 10h10 | 13h10 | |
| TA-7 | 09h16 | 09h46 | 15h46 | 16h12 | 10h12 | 13h12 | |
| TA-8 | 09h18 | 09h48 | 15h48 | 16h14 | 10h14 | 13h14 | |
| TA-9 | 09h20 | 09h50 | 15h50 | 16h16 | 10h16 | 13h16 | |
| TA-10 | 09h22 | 09h52 | 15h52 | 16h18 | 10h18 | 13h18 | |
Tableau 4: calendrier Exemple pour les tests d'articles de test solides. Étapes de Protocole, notamment en pré-mouiller les tissus avec DPBS, Application des articles d'essai, de rinçage et de post-trempage, la période post-incubation, test MTT, Extraction de MTT, et évaluation de MTT OD sont présentés dans des colonnes. Fois pour les tissus doubles sont organisées en rangées. L'ensemble du test de tester 10 AT et des contrôles est effectuée sur une période de deux jours.
| Montant | Réactif | Conditions de stockage | Source | Description | Date d'expiration |
| 1 flacon, 2 ml | Concentré MTT (MTT-100-CON) | Protégé de la lumière (-20ºC) | MatTek | Frozen MTT concentré | 2 mois |
| 1 flacon, 8 ml | MTT diluant | 2-8 &# 186; C | MatTek | Par dilution MTT concentré avant utilisation dans le dosage MTT | 2 mois |
| 1 bouteille, 60 ml | Isopropanol (# CAS 67-63-0) | RT | Sigma-Aldrich | Solution d'extraction | N / A |
Tableau 5: MTT-100 Assay Composants Kit.
| N ° de code | Tissu | Données brutes | Données corrigées Blank | moyenne de DO | % De viabilité | ||
| n | Aliq. 1 | Aliq. 2 | Aliq. 1 | Aliq. 2 | |||
| Caroline du Nord | 1 | 1.316 | 1.352 | 1.316 | 1.352 | 1.334 | 101,6 |
| 2 | 1.277 | 1.309 | 1.277 | 1.309 | 1.293 | 98,4 | |
| Ordinateur personnel | 1 | 0,379 | 0,397 | 0,379 | 0,397 | 0,388 | 29,6 |
| 2 | 0,419 | 0,442 | 0,419 | 0,442 | 0,431 | 32,8 | |
| TA1 | 1 | 1.213 | 1.244 | 1.213 | 1.244 | 1.229 | 93,5 |
| 2 | 1.355 | 1.355 | 1.355 | 1.355 | 1.355 | 103,2 | |
| TA2 | 1 | 1.210 | 1.122 | 1.210 | 1.122 | 1.166 | 88,7 |
| 2 | 0,828 | 0,837 | 0,828 | 0,837 | 0,833 | 63,4 | |
| TA3 | 1 | 0,167 | 0,168 | 0,167 | 0,168 | 0,167 | 12,7 |
| 2 | 0,138 | 0,136 | 0,138 | 0,136 | 0,137 | 10.4 | |
| TA4 | 1 | 1.137 | 1.160 | 1.137 | 1.160 | 1.149 | 87,4 |
| 2 | 1.262 | 1.191 | 1.262 | 1.191 | 1.227 | 93,4 | |
| TA5 | 1 | 0.610 | 0,621 | 0.610 | 0,621 | 0,616 | 46,9 |
| 2 | 0,480 | 0,484 | 0,480 | 0,484 | 0,482 | 36,7 | |
| TA6 | 1 | 0,502 | 0,513 | 0,502 | 0,513 | 0,508 | 38,7 |
| 2 | 0,396 | 0,407 | 0,396 | 0,407 | 0,402 | 30,6 | |
| TA7 | 1 | 1.048 | 1.050 | 1.048 | 1.050 | 1.049 | 79,9 |
| 2 | 1.149 | 1.150 | 1.149 | 1.150 | 1.150 | 87,5 | |
| TA8 | 1 | 1.032 | 1.034 | 1.032 | 1.034 | 1.033 | 78,7 |
| 2 | 0,941 | 0,935 | 0,941 | 0,935 | 0,938 | 71,4 | |
| TA9 | 1 | 0,022 | 0,022 | 0,022 | 0,022 | 0,022 | 1.7 |
| 2 | 0,144 | 0,149 | 0,144 | 0,149 | 0,147 | 11.2 | |
| TA10 | 1 | 0,150 | 0,150 | 0,150 | 0,150 | 0,150 | 11,4 |
| 2 | 0,254 | 0,255 | 0,254 | 0,255 | 0,255 | 19,4 | |
| signifier | Dif. | moyenne de | Dif. | Dif. / 2 | Classification | ||
| de la DO | de la DO | viabilités [%] | des viabilités | ||||
| Caroline du Nord | 1.314 | 0,041 | 100,0 | 3.12 | 1,56 | NI | qualifié |
| Ordinateur personnel | 0,410 | 0,043 | 31,2 | 3.23 | 1,62 | JE | qualifié |
| TA1 | 1.292 | 0,127 | 98,3 | 9,63 | 4.81 | NI | qualifié |
| TA2 | 0,999 | 0,333 | 76,1 | 25.36 | 12.68 | NI | D> 20 |
| TA3 | 0,152 | 0,030 | 11,6 | 2.32 | 1.16 | JE | qualifié |
| TA4 | 1.188 | 0,078 | 90,4 | 5,94 | 2.97 | NI | qualifié |
| TA5 | 0,549 | 0,134 | 41,8 | 10.16 | 5.08 | JE | qualifié |
| TA6 | 0,455 | 0,106 | 34,6 | 8.07 | 4.03 | JE | qualifié |
| TA7 | 1.100 | 0,101 | 83,7 | 7,65 | 3.82 | NI | qualifié |
| TA8 | 0,986 | 0,095 | 75,0 | 7.23 | 3,62 | NI | qualifié |
| TA9 | 0,085 | 0,125 | 6.4 | 9,48 | 4.74 | JE | qualifié |
| TA10 | 0,203 | 0,105 | 15,4 | 7,95 | 3,98 | JE | qualifié |
Tableau 6:. EIT résultats obtenus pour 10 articles d'essai, NC et PC contrôles Les tables sont produced par une feuille de calcul Excel conçu pour calculer la viabilité des tissus et des résultats de l'IET. Produits chimiques d'essai qui réduit la viabilité des tissus ≤ 60,0% par rapport à NC sont classés comme irritants ("I", TA3, TA5, TA6, TA9 et TA10) et les produits chimiques de test qui avait la viabilité des tissus> 60,0% sont classés comme non-irritants (" NI ", TA1, TA2, TA4, TA7 et TA8).
Discussion
Nous avons présenté le test d'irritation des yeux (Figure 1) qui a été développé pour le modèle de tissu EpiOcular. L'IET est capable de séparer irritants oculaires et corrosifs (SGH Catégories 1 et 2 combinés) à partir de matériaux qui ne nécessitent pas d'étiquetage (SGH Sans catégorie) avec un haut degré de sensibilité et de spécificité 17. L'IET tel que présenté ici ne fait aucune discrimination entre SGH Catégorie 1 de la catégorie 2 produits chimiques. L'IET a été validé pour la classification et l'étiquetage du potentiel d'irritation oculaire d'un large éventail de produits chimiques, y compris les ingrédients cosmétiques et pharmaceutiques. En conjonction avec d'autres tests in vitro, l'IET servira de remplacement pour le test d'irritation in vivo sur œil de lapin.
L'IET utilise deux protocoles similaires, mais distinctes pour les matières liquides et solides, qui varient dans la durée d'exposition et de périodes d'incubation post-exposition (Figure 1). Le critère d'évaluation utilisé dans l'IETest la viabilité des tissus, déterminée par le test MTT, qui a été précédemment utilisé dans les modèles validés épithéliales humaines de tissu 20,21. Pour effectuer ce test, aucun équipement spécial en sus des équipements de culture cellulaire standard est nécessaire. En raison du niveau élevé de reproductibilité tissu à tissu, n = 2 au lieu de tissus généralement recommandé n = 3 sont utilisés. La possibilité d'utiliser n = 2 tissus est un aspect essentiel du protocole, car il permet à un opérateur expérimenté pour traiter simultanément deux tissus, minimisant ainsi la variabilité de l'essai qui peuvent survenir en raison de la différence de traitement des tissus individuels 14. Aussi, en utilisant n = 2 tissus par l'article de test, le caractère irritant de 10 substances d'essai du même état physique (liquide ou solide), avec les contrôles positifs et négatifs, peut être évaluée en utilisant un kit (24 tissus).
Autres points clés qui assurent classement fiable des matériaux sont des spécifications pour le contrôle positif substance (de la viabilité des tissus ≤50.0%), la reproductibilité entre les tissus en double (différence <20,0%), et des lectures de DO de contrôle négatif (> 0,8 et <2,5).
Lorsque vous effectuez le test IET, il est important de respecter le protocole validé et le dosage suggéré et les horaires de rinçage (tableaux 3 et 4), depuis déviation du protocole ou des changements dans les périodes d'incubation peut entraîner des résultats altérée. De même, les écarts de temps de 3 heures pour les MTT incubation se traduira par des lectures différentes de MTT et peuvent affecter résultat dosage.
Occasionnellement, un produit chimique d'essai peut avoir des propriétés optiques ou autres qui peuvent interférer avec le tissu de MTT test de viabilité ou la réduction de la cause de MTT. Par exemple, un produit chimique de test peut directement réduire MTT en produit de réaction bleu-violet, ou peut être une substance colorée qui absorbe la lumière dans la même gamme que MTT formazan (~ 570 nm). Cependant, ces produits chimiques d'essai seront prESENT un problème que, si, au moment du test MTT, une quantité suffisante du matériau est encore présent sur (ou absorbé par) le tissu. Pour éviter cette interférence, les procédures de rinçage vastes sont incorporés dans le protocole de l'IET. Si rinçage ne supprime pas le TA et le TA interfère avec réduction du MTT, des contrôles supplémentaires doivent être utilisés pour détecter et corriger pour elle. En bref, si la réduction de MTT directe de la substance d'essai est suspectée, 50 pi (ou 50 mg pour les solides) du produit chimique en question est incubé pendant 3 heures avec la solution de travail MTT au CSC (NC, 50 pi d'eau déminéralisée stérile, devrait être exécuter simultanément). Si la solution de MTT tourne bleu-violet, l'article de test est présumé avoir réduit le MTT. Dans ce cas, un contrôle fonctionnel en utilisant des commandes de tissus lyophilisés tué doit être effectuée afin d'évaluer si le matériel de test est obligatoire pour le tissu et menant à un faux signal de réduction du MTT. Si il ya réduction du MTT appréciable dans le, contrôle de tissu tué TA-exposée(par rapport à la quantité dans le tissu viable non traité), la viabilité des tissus moyen de l'article d'essai doit être corrigée en soustrayant la moyenne de la viabilité contrôle tué.
L'IET se trompe sur le côté de la sécurité, comme en témoigne la faible incidence des classifications faux négatifs 14,15,18. Surtout, aucun des produits chimiques SGH Catégorie 1, qui sont corrosives pour l'œil et qui représentent le plus grave risque oculaire, ont été classés comme non-irritant dans cet essai 14,15,18,19. Enfin, l'un des principaux avantages de la certification RHCE de méthode d'essai in vitro est la possibilité de tester liquide pur et matériaux solides (ce qui est impossible avec des cultures de cellules submergées deux dimensions).
L'IET contribuera de manière significative dans la détermination du potentiel d'irritation oculaire d'un large éventail de matériaux en fonction de la classification et de l'étiquetage SGH des Nations unies. Le remplacement des animaux pour déterminer oToxicité culier a été un objectif de la recherche toxicologique, depuis de nombreuses années. La méthode d'essai IET a complété une étude de validation formelle soutenue par EURL ECVAM en 2014 et a été mis en œuvre EpiOcular IET dans les Lignes directrices de l'OCDE que d'essai OCDE TG 492 en 2015.
Déclarations de divulgation
Frais de publication de cet article ont été payés par MatTek Corporation.
Remerciements
Les auteurs tiennent à remercier le Dr John Harbell pour son soutien et le temps scientifique dédiée au projet IET. Les auteurs tiennent également à remercier Beiersdorf AG (Allemagne), IIVS (USA), Mary Kay Inc. (USA), Avon Products Inc. (USA), Procter & Gamble / Cosmital (Suisse), Laboratoire Pierre Fabre (France), Harlan Laboratories (Royaume-Uni), et LVMH Parfums (France) pour la participation au Multi-centre international de pré-validation et de validation des études du test d'irritation des yeux 15.
Références
- National Toxicology Program (NTP) Interagency Center for the Evaluation of Alternative Toxicological Methods (NICEATM). Request for Ocular Irritancy Test Data From Human, Rabbit, and In Vitro Studies Using Standardized Testing Methods. Federal Register. 72 (109), 31582-31583 (2007).
- Regulation (EC) No 1907/2006 of the European Parliament and of the Council of 18 December 2006 concerning the Registration, Evaluation, Authorisation and Restriction of Chemicals (REACH), establishing a European Chemicals Agency, amending Directive 1999/45/EC and repealing Council Regulation (EEC) No 793/93 and Commission Regulation (EC) No 1488/94 as well as Council Directive 76/769/EEC and Commission Directives 91/155/EEC, 93/67/EEC, 93/105/EC and 2000/21/EC. OJ. L396 (49), European Commission. 1-849 (2006).
- Globally Harmonized System of Classification and Labelling of Chemicals (GHS). , Fifth revised edition, United Nations. New York and Geneva. (2013).
- Draize, J. H., Woodard, G., Calvery, H. O. Methods for the Study of Irritation and Toxicity of Substances Applied Topically to the Skin and Mucous Membranes. J Pharmacol Exp Ther November. 82, 377-390 (1944).
- Adriaens, E. Retrospective analysis of the Draize test for serious eye damage/eye irritation: importance of understanding the in vivo endpoints under UN GHS/EU CLP for the development and evaluation of in vitro test methods. Arch tox. 88, 701-723 (2014).
- Balls, M., Botham, P. A., Bruner, L. H., Spielmann, H. The EC/HO international validation study on alternatives to the Draize eye irritation test. Toxicol in Vitro. 9, 871-929 (1995).
- Curren, R. D., Harbell, J. W. Ocular safety: a silent (in vitro) success story. Altern Lab Anim. 30, Suppl 2. 69-74 (2002).
- Wilhelmus, K. R. The Draize Eye Test. Survey of Ophthalmology. 45, 493-515 (2001).
- Curren, R. D., Harbell, J. W. In vitro alternatives for ocular irritation. Environ health persp. 106, 485-492 (1998).
- McCain, N. E., Binetti, R. R., Gettings, S. D., Jones, B. C. Assessment of ocular irritation ranges of market-leading cosmetic and personal-care products using an in vitro tissue equivalent. Toxicologist. 66, 243(2002).
- Niranjan, P., Dang, A. H., January, B. G., Gomez, C., Harbell, J. W. Use of the EpiOcular assay for preclinical qualification of formulas for human clinical studies. Toxicologist. 96, 249(2007).
- Yin, X. J. Prediction of ocular irritation potential of surfactants-based formulations at different concentrations using the EpiOcular model. Toxicologist. 108, 378(2009).
- Harbell, J., Curren, R. In vitro methods for the prediction of ocular and dermal toxicity. Handbook of Toxicology. , 2nd Edition, Informa Healthcare. (2001).
- Kaluzhny, Y. Development of the EpiOcular(TM) eye irritation test for hazard identification and labelling of eye irritating chemicals in response to the requirements of the EU cosmetics directive and REACH legislation. Altern Lab Anim. 39, 339-364 (2011).
- Pfannenbecker, U. Cosmetics Europe Multi-Laboratory Pre-Validation of the EpiOcular Reconstituted Human Tissue Test Method for the Prediction of Eye Irritation. Toxicol in vitro. , (2013).
- MatTek Corporation. EpiOcular™ Eye Irritation Test (OCL-200-EIT) for the prediction of acute ocular irritation of chemicals for use with Reconstructed Human EpiOcular Model (OCL-200-EIT). Protocol#MK-24-007-0055. , MatTek Corporation. (2014).
- Kaluzhny, Y. EpiOcular Eye Irritation Test (EIT) for Hazard Identification and Labeling of Eye Irritating Chemicals: Protocol Optimization for Solid Materials and Extended Shipment Times. Altern Lab Anim. 43 (2), 101-127 (2015).
- Kolle, S. N., Kandarova, H., Wareing, B., van Ravenzwaay, B., Landsiedel, R. In-house validation of the EpiOcular(TM) eye irritation test and its combination with the bovine corneal opacity and permeability test for the assessment of ocular irritation. Altern Lab Anim. 39, 365-387 (2011).
- Reconstructed Human Cornea-like Epithelium (RhCE) Test Method for Identifying Chemicals Not Requiring Classification and Labelling for Eye Irritation or Serious Eye Damage. Draft proposal for a new test guideline.. OECD Guideline for the Testing of Chemicals. , (2014).
- Evaluating the ocular irritation potential of 54 test articles using the EpiOcular Human tissue Construct Model. Toxicol. In Vitro. Blazka, M. E., Harbell, J. 42nd Annual Meeting of the Soc. of Toxicology, Salt Lake City, UT, , (2003).
- Kandarova, H. The EpiDerm Test Protocol for the Upcoming ECVAM Validation Study on In Vitro Skin Irritation Tests — An Assessment of the Performance of the Optimised Test. Altern Lab Anim. 33, 351-367 (2005).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon