Method Article
Balayage automatique pour lames et Segmentation en tissus fluorescent marqué à l’aide d’un système d’analyse Widefield haute teneur
* Ces auteurs ont contribué à parts égales
Dans cet article
Résumé
Nous décrivons ici un protocole pour la segmentation automatique des tissus fluorescent étiquetés sur les diapositives à l’aide d’un système d’analyse de haute teneur widefield (WHCAS). Ce protocole a de nombreuses applications dans n’importe quel domaine qui implique la quantification de marqueurs fluorescents dans les tissus biologiques, y compris les sciences biologiques, ingénierie médicale et sciences de la santé.
Résumé
Automatisé de numérisation de diapositives et segmentation des tissus fluorescent marqué est le moyen le plus efficace pour analyser ensemble diapositives ou des coupes de tissus grand. Malheureusement, de nombreux chercheurs passent énormément de temps et de ressources en développement et optimisation de flux de travail qui n’est pertinentes que pour leurs propres expériences. Dans cet article, nous décrivons un protocole qui permet à n’importe quel tissu monté sur glissière, avec options de personnalisation dans les modules précompilés trouvée dans le logiciel associé à l’image de ceux qui ont accès à un système d’analyse de haute teneur widefield (WHCAS). Pas prévu pour la numérisation de diapositives, les étapes détaillées dans cet article permettent d’acquérir des diapositive, numérisation des images dans le WHCAS qui peut être importé dans le logiciel associé. Dans cet exemple, la segmentation automatique des diapositives de tumeur de cerveau est démontrée, mais la segmentation automatique de n’importe quel marqueur fluorescent marqué nucléaire et cytoplasmique est possible. En outre, il y a une variété d’autres modules de logiciels quantitatives, y compris les dosages pour la localisation/la translocation des protéines, prolifération/viabilité / l’apoptose cellulaire et l’angiogenèse qui peut être exécuté. Cette technique va économiser l’effort et le temps des chercheurs et créer un protocole automatisé pour l’analyse de la diapositive.
Introduction
La quantification exacte et précise des tissus fluorescent marqué sur des lames est une technique très recherchée dans de nombreux domaines scientifiques. Cependant, chercheurs comptent des spécimens souvent manuellement ou dépensent des sommes considérables de temps à développer des techniques automatisées ésotériques pour y parvenir. Ici, nous fournissons un protocole pour la numérisation automatique pour lames et la quantification des cellules à l’aide d’un WHCAS et son logiciel associé, avec des cellules immunitaires innées dans les sections de tumeur de cerveau humain congelé à titre d’exemple. Le logiciel associé propose une large gamme de modules personnalisables intégrés de la croissance des neurites comptant à la différenciation des cellules types1,2,3,4,5, 6. l’objectif de cette méthode consiste à fournir aux chercheurs un protocole début à la fin, facilement reproductible à acquérir des images d’et à quantifier les entités fluorescent marqué dans n’importe quel tissus monté sur glissière.
Dans ce protocole, la WHCAS est principalement utilisé pour l’imagerie des plaques pour l’analyse subséquente sur les logiciels associés même si une diapo et les bases de glisser balayage7 étaient disponibles. C’était prohibitif pour diapositives d’image car l’étalonnage attention spatiale de la zone d’acquisition, la sélection des revues appropriés, la création d’équipements sur mesure et une liaison avec les représentants de produit ont été nécessaires. Dans le corps plus large de la littérature, au lieu d’acheter un dédié diapositive-imagerie et analyse appareil8, un précédent rapport technologique ayant accès à ce logiciel contourné l’acquisition d’images de diapositives sur le WHCAS au total9. Analyse d’image acquisition ou image sur différentes plateformes, nécessite un travail supplémentaire pour s’assurer que chacun est compatible avec l’autre.
La possibilité d’utiliser le WHCAS et son logiciel de capture d’image permettrait d’éviter les complications inutiles de chercher ou de développer un étranger de flux de travail à ces outils. Dans cet article, les étapes requises pour créer un scan d’aperçu de faible grossissement et les images correspondantes de fort grossissement en traitant la diapositive comme une plaque, et les analyses subséquentes en utilisant le module segmentation multi-longueur d’onde cellule marquant permettant la réaffectation de la WHCAS. Ce protocole facilement utilisable fournit un avantage sur les autres techniques car il n’y a aucune nécessité de développer des algorithmes ou multi-étapes comptage protocoles10,11 une fois que les images sont acquises sur le WHCAS. Ce protocole atténue le temps nécessaire pour optimiser une technique de dosage, est plus précis de12 et plus efficace que le comptage manuel et maximise l’utilisation de la WHCAS. Ce protocole peut être facilement et largement utilisé car il permet l’imagerie et l’analyse de n’importe quel tissus fluorescent marqué sur des lames.
Protocole
Les échantillons de tumeur ont été obtenus conformément au protocole approuvé par le Comité de Conseil et de l’éthique examen local de l’établissement et conformément à la réglementation nationale. Le WHCAS et ses logiciels associés utilisés dans cet article sont énumérés dans la Table des matières.
1. importer les journaux
- Ouvrez le logiciel associé.
- Télécharger la suite de journal indiquée dans la Table des matières.
- La suite de journal d’importation dans un répertoire approprié en cliquant sur le menu principal rubrique Journal, sélectionnez Importation Journal Suite..., puis cliquez sur Import.
2. création de paramètres d’aperçu Scan Acquisition
- Dans la boîte de dialogue D’installation de la plaque d’Acquisition , allez à l’onglet objectif et appareil photo Select 4 X que le grossissement, comme la caméra binning, 1et 2 que le profit.
- Entrez les paramètres dans la Figure 1 a sous l’onglet plaque – Slidescanning.
Remarque : Ces paramètres ont été créés pour permettre à l’utilisateur d’afficher et naviguer jusqu'à 3 toboggans. Chaque diapositive a été divisé en 3 puits adjacents pour la navigation facile et « live » visualisation des tranches de tissus ou cellules. - Dans l’onglet Sites à visiter , remplir les puits uniformément avec les sites.
- Cliquez sur Edit plaque bas paramètres... et entrez les valeurs affichées dans la Figure 1 b.
- Sous l’onglet Acquisition boucle , entrez la longueur d’onde désirée (toute souillure nucléaire dans cet exemple) pour l’aperçu de la numérisation. Pour le meilleur contraste et axée sur l’image en se concentrant, utilisez le signal fluorescent plus brillants (p. ex., souvent une coloration nucléaire).
NOTE : La coloration de tissus avec une tache lumineuse comme une tache nucléaire est recommandée car cela offre un contraste élevé par rapport à l’arrière-plan. Non seulement cette aide à l’emplacement de l’échantillon, mais quand plus d’un fluorophore dans l’acquisition de grossissement élevé suivant de l’imagerie, la couleur plus brillante serviront à l’offset d’imagerie des autres couleurs de base sur. - Activer la Correction d’ombrage en mode d’Acquisition de la plaque pour assembler les images.
- Enregistrez ces paramètres sous A.
3. Créez des paramètres pour l’Acquisition de la diapositive à fort grossissement
- Dans la boîte de dialogue D’installation de la plaque d’Acquisition , allez à l’onglet objectif et appareil photo Select 40 X que le grossissement, 1 comme la caméra binning (pour la plus haute résolution numérique) et 2 que le profit (pour augmenter le signal et la luminosité des images).
Remarque : Un réglage de grossissement objectif inférieur peut être utilisé, mais les auteurs ont trouvé 40 X pour le réglage optimal pour l’analyse des microglies humaines et des macrophages dans le tissu de tumeur de cerveau en utilisant le module Multi-longueur d’onde cellule marquant . - S’assurer que tous les paramètres pour les onglets plaque – Slidescanning et Éditer plaque bas paramètres... celle qui concernent Setting A (voir étape 2).
- Si les images obtenues ne sont pas nettes, modifier la profondeur du puits, la hauteur de la plaqueet Plaque bas paramètres pour ajuster la mise au point. S’il y a toujours un problème avec la mise au point, choisissez Laser avec récupération d’Image dans la section options de l’Autofocus .
- Sous l’onglet Acquisition boucle , entrez le nombre de longueurs d’onde présentes dans l’échantillon. Vérifiez les options de base de laser mise au point et activez axée sur l’image mise au point (pour le recouvrement d’acquisition ou laser) .
- Sous l’onglet de mise au point automatique , sélectionnez mettant l’accent sur la plaque et bien bas.
- Dans l’onglet journaux , sélectionnez les options comme indiqué dans la Figure 2, assurer la prévention matérielle asynchrone se déplace est également sélectionné.
- Enregistrer ces paramètres comme paramètre B.
4. Placer la diapositive dans le système d’analyse Widefield haute teneur
- Appuyez sur F4 pour afficher le Menu principal. Sélectionnez la diapositive numérisation. Cliquez sur la porte ouverte – Slide éjecter et insérer les diapositives et diapo (qui peut contenir jusqu'à trois diapositives) dans les WHCAS (figures 3 a et 3 b). Orienter la lame avec la lamelle vers le bas et l’étiquette sur le côté de l’encoche de la diapo (Figure 3 a).
Remarque : Les diapositives utilisées dans cette expérience étaient standard 25 x 75 x 1 mm encadrés. - Cliquez sur Fermer la porte – lame de charge.
5. acquérir un aperçu de la numérisation
- Sous la rubrique dépistage , sélectionnez plaque d’Acquisition et contrôle... et la Plaque d’installation l’Acquisition... et charger A.
- Sous l’onglet puits de visite , se déplacer dans la cupule contenant l’échantillon, en utilisant le bouton de clic-droit sur la souris. Sous l’onglet Sites à visiter , se déplacer vers des sites différents avec la capture d’image Live jusqu'à ce que les cellules sont situées. Mettre l’accent sur l’échantillon ou utiliser l' Autofocusmanuellement. Utilisez Snap pour capturer l’image.
Remarque : L’échantillon est plus facile de localiser avec plus de sites et en ajustant les sites dans le puits (voir étape 2.3). - Dans le menu principal, sélectionnez Aperçu glisse.
- Dans la boîte de dialogue qui s’ouvre automatiquement, sélectionnez l’option reflétant diapositives combien vont être analysés. Numériser une diapositive à la fois. Appuyez sur OK. Sélectionnez l’option 4 X que le grossissement. Appuyez sur OK. Sélectionnez lamelle vers le bas (0,17 mm) comme l’orientation des diapositives (utilisez une correction collier si une épaisseur de la lamelle couvre-objet différent est utilisée). Appuyez sur OK. Cliquez sur Continuer.
Remarque : Si l’utilisateur souhaite acquérir aperçu scans pour 2 ou plusieurs diapositives, chaque aperçu de la numérisation doit être ouvert individuellement avant l’acquisition de l’image correspondante de fort grossissement. - Sous Scanner diapositive réglage de charge, vérifiez que les paramètres d’Acquisition et d’étalonnages cases sont cochées. Appuyez sur Annuler. Lorsque la boîte de Paramètres de numérisation de diapositives réapparaît, sélectionnez Continuer.
- Lorsque la boîte de dialogue Numériser diapositive apparaît, réglez les paramètres comme indiqué dans la Figure 4 a-4 C. Sélectionnez Fermer lorsque vous avez terminé.
NOTE : Augmenter la caméra binning et en diminuant le temps d’exposition de caméra se traduira par un balayage plus rapide, quoiqu’à une plus faible résolution numérique et la gamme dynamique, respectivement, donc diminuer la qualité de l’image. Correction d’ombrage assurera une intensité uniforme à travers un seul champ de vision. Tournant sur le matériel et l’Autofocus Image assurera le scan est en discussion, mais ralentira la numérisation. Dans l’intérêt de gagner du temps, il est recommandé d’avoir la correction, de matériel et d’Autofocus Image hors d’ombrage tout en acquérant le scan de faible grossissement, mais d’avoir ces options activé pour étape 6 durant l’imagerie fort grossissement. La résolution de la numérisation de faible grossissement n’affectera pas la résolution de la numérisation de fort grossissement. - Sélectionnez un répertoire pour la diapositive, numérisation de données. Cliquez sur OK. Entrez un nom pour le fichier. Cliquez sur OK.
- La boîte de dialogue Tracer région apparaîtra automatiquement. Utilisez l’outil zone rectangulaire (Figure 5 a) pour sélectionner la région de scan aperçu ensemble comme sur la Figure 5 b. Cliquez sur Continuer.
- La boîte de dialogue Installation terminée s’affiche. Cliquez sur Continuer.
Remarque : L’aperçu de la numérisation diapositive débutera maintenant. - Une fois la prévisualisation terminée, la boîte de dialogue Analyse terminée s’affiche. Cliquez sur Continuer. Ne fermez pas la fenêtre de scan d’aperçu (dans cet exemple, la fenêtre de Scan DAPI ; voir Figure 6).
Remarque : L’installation et le processus d’acquisition de faible grossissement scan prendra environ 20 min. Le temps d’acquisition ultérieure fort grossissement image dépendra du nombre de sites choisis ainsi que les temps d’exposition pour chaque canal.
6. fort grossissement de numérisation
- Charger la configuration B.
- Déterminez quels puits à être photographié. Sous l’onglet puits de visite , se déplacer dans la cupule contenant l’échantillon, en utilisant le bouton de clic-droit sur la souris.
Remarque : La technique se manifeste ici par imagerie bien 1. - Sous l’onglet Sites à visiter , se déplacer vers des sites différents avec la fonction Live jusqu'à ce que les cellules ou les tissus se trouve. Mettre l’accent sur l’échantillon ou utiliser l' Autofocusmanuellement. Utilisez Snap pour capturer l’image.
Remarque : Pour vous aider à localiser l’échantillon à un fort grossissement, utilisez la boîte de dialogue de contrôle et d’Acquisition de la plaque pour ajuster la taille de palier de 5 à 100 µm pour trouver l’échantillon si l’Autofocus ne peut pas. - Sous l’onglet W1 DAPI , cliquez sur Auto exposer. S’assurer que l’image de la Plaque Acquisition Snap - DAPI soit croustillant.
- Sous le menu principal, cliquez sur Journal de révéler le menu déroulant. Sélectionnez exécuter le Journal....
- Double-cliquez sur la feuille de Glisser région Acquisition d’installation pour le lancer. Lorsque la boîte de dialogue D’installation glisser région Acquisition apparaît, sélectionnez Continuer.
- Quand vous êtes invité, sélectionnez correctement le DAPI Scan pour sélectionner l’image de la diapositive de faible grossissement. Appuyez sur OK. De même, mettez en surbrillance la plaque Acquisition Snap - DAPI interrogé pour l’accrochage d’acquisition de plaque. Cliquez sur OK.
- Lorsque la boîte de créer ou régions de charge s’affiche, utilisez l’outil zone rectangulaire pour sélectionner (a) région (s) d’intérêt sur le DAPI numérisation (Figure 6). Appuyez sur Continuer.
NOTE : La superficie maximale qui peut être sélectionnée à 40 X est 45 colonnes de 35 lignes. Si plusieurs régions d’intérêt sont sélectionnées, les régions seront redimensionnées à la boîte avec la plus grande superficie. Les boîtes peuvent être repositionnés après le redimensionnement. - Sélectionnez non dans la boîte de dialogue des Régions de charge .
Remarque : En sélectionnant Oui charges précédemment enregistré des régions pour les lots des diapos avec la même région de lieux d’intérêt. - À l’aide de l’outil de recherche , mettre en évidence la plus grande région d’intérêt et cliquez sur Continuer dans la boîte de dialogue Sélectionnez région . Lorsque la boîte de régions de confirmation s’affiche, sélectionnez Continuer. Décider si la région a besoin d’être sauvé lorsque s’affiche la boîte de dialogue Enregistrer les régions .
- La boîte de dialogue suivante, Espacement des sites, permet à l’utilisateur de choisir le sol carrelé, qui se traduit par une image sans chevauchement, ni chevauchement de 10 %. Choisissez une option, puis cliquez sur OK. Les auteurs ont choisi le sol carrelé.
- Trois boîtes de dialogue seront affiche maintenant. La boîte de Configuration complet peut être rejetée en appuyant sur Continuer. Ouvrir la boîte de Configuration du Site Acquisition pour 40 X (Figure 7 a) pour l’instant car il fait clairement le nombre de colonnes et de lignes doivent être entrés dans la boîte de Configuration d’Acquisition de plaque (Figure 7 b). Garder la boîte de WellPositions (Figure 7) qui apparaît dans le coin inférieur gauche ouverte pendant la durée de l’imagerie.
- Dans la boîte de Plaque Acquisition mise , sous le puits de visite, le même nombre de puits comme des régions d’intérêt précédemment sélectionné doit être mis en évidence (Figure 7).
Remarque : Les auteurs mis au point ce protocole pour un maximum de neuf régions d’intérêt par diapositive. S’il y a plus, tout simplement augmenter le nombre de colonnes ou de lignes dans l’onglet plaque - SlideScanning pour refléter le nombre de régions d’intérêt. Ces puits ne sont pas dans l’espace l’emplacement des régions d’intérêt en quelque sorte, mais le nombre approprié doit être mis en évidence (clic gauche). - Dans la zone D’installation de la plaque d’Acquisition , allez dans l’onglet Sites pour entrer a suggéré des colonnes et des lignes (Figure 7 b). N’oubliez pas de cliquez sur sites de tuile.
- Pour éliminer les approximations de trouver les sites contenant l’échantillon, appuyez sur Plaque acquérir sous l’onglet Résumé pour positionner la scène à la région présélectionnée d’intérêt. Une fois que la caméra effectue un panoramique avec au-dessus d’un site contenant des cellules, appuyez sur Annuler dans le coin inférieur droit pour arrêter l’acquisition de l’image. S’assurer que la scène est maintenant situé au-dessus de l’échantillon.
- Optimiser les réglages de longueur d’onde pour s’assurer qu’un ciblée et une image de gamme dynamique élevée est obtenue. Une fois satisfait, cliquez sur l’onglet Résumé et Plaque d’acquérir.
7. image Analysis
- Sélectionnez le module personnalisé souhaité.
Remarque : Les auteurs ont choisi le module Multi-longueur d’onde cellule marquant pour démontrer une segmentation automatique des diapositives tumeur cérébrale. - Exécutez l’analyse sur tous les sites. Si les paramètres de l’analyse sont les mêmes pour les nombreux toboggans, l’analyse peut être inclus dans la boîte de Plaque Acquisition d’installation sous l’onglet Post Acquisition .
- Une fois l’analyse terminée, exclure des sites de mauvaise qualité d’image pour ne pas biaiser les résultats. Étant donné que l’objectif de cette analyse est de quantifier la microglie et les macrophages dans le parenchyme de la tumeur, sélectionnez la région d’intérêt dans les bords de l’échantillon de la tumeur. En outre, exclure les sites qui sont flous et/ou de contenant les plis des tissus ou des bulles et des déchirures dans le tissu. Pour une démonstration, voir les Résultats de représentant. Vous pouvez également utiliser le score de Laser focus généré pour chaque site selon l’amplitude de la réflexion du laser comme un seuil en dessous quels sites doivent être exclus (le seuil est personnalisable et dépend des paramètres tels que la durée d’exposition et la type de support utilisé).
Remarque : Les images de fort grossissement permettent d’exclure expressément les structures telles que les gros vaisseaux sanguins et des zones de nécrose, si nécessaire. Il est également possible d’inclure uniquement les domaines d’intérêt, tels que ceux qui sont hypercellulaire. De cette façon, la spécificité et la précision des analyses peuvent être augmentés.
Résultats
Les images peuvent être visualisées dans le logiciel WHCAS. La figure 8 montre les vignettes de grossissement élevé de tous les sites dans la région définie d’intérêt. Examiner chaque site afin d’identifier celles qui doivent être exclus de l’analyse (des exemples sont montrés au grossissement faible et élevé dans la Figure 8 et Figure 9, respectivement). Par exemple, Site 149 est floue (Figure 9 a), Site 219 a bulles (Figure 9 b), et 54 Site contient un pli (Figure 9) et devrait être exclue. Il est typique pour exclure les 10-15 % de tous les sites imagés. Dans l’exemple fourni, 15,3 % des sites ont été exclus (25/300 a bulles, 17/300 étaient flous, 3/300 ont été pliées et 1/300 était sur le bord). Figure 10 a est une image représentative choisie pour l’analyse (sa vignette de faible grossissement correspondante est affichée dans la Figure 8). Ici, les recouvrements correspondants générés par le module multi-longueur d’onde cellule marquant démontrent les résultats de la segmentation automatique effectué sur Site 59, adaptés aux caractéristiques des auteurs (largeur minimale de noyaux = 2,5 µm, largeur maximale = 7,5 µm, et intensité au-dessus de fond local = 35 graylevels ; La largeur minimale des cellules CD11b positives = 4 µm, largeur maximale = 18 µm, minimal teinté zone = 15 µm2et intensité au-dessus de fond local = 310 graylevels ; et la largeur minimale des cellules CD45 positives = 4 µm, largeur maximale = 18 µm, minimal teinté zone = 15 µm2et intensité au-dessus de fond local = 50 graylevels). Après la segmentation, les données quantitatives de la proportion de cellules positives pour chaque marqueur de coloration (6,2 ± 5,1 % et 3,8 ± 2,1 % de CD11b+ et CD45+ cellules, respectivement), les deux marqueurs (3,5 ± 2,1 % CD11b+CD45+ cellules), aucun marqueur (86,6 ± 9,0 % CD11b–CD45– cellules ; Figure 10 b), signifie souillé zone (40,0 µm ± 9,2 et 36,7 ± 7,6 µm de CD11b+ et CD45+ cellules, respectivement ; Figure 10) et l’intensité de fluorescence moyenne (408,9 ± 40,3 fluorescence relative unités et 373,9 ± 38,1 fluorescence relative CD11b+ et CD45+ cellules, respectivement ; Figure 10) peut être obtenue.
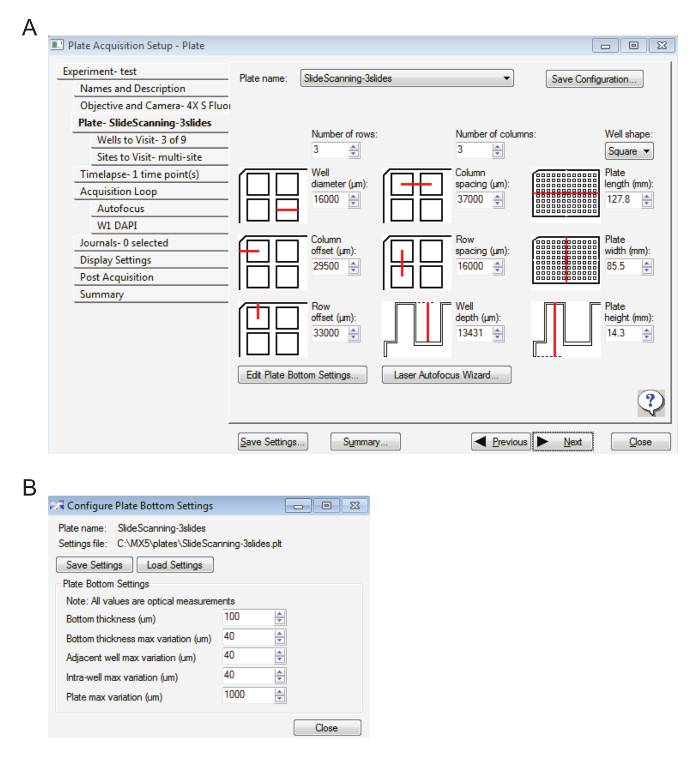
Figure 1 : paramètres d’acquisition de la lame à faible grossissement. A. cette image affiche les paramètres de la plaque. B. ici, les paramètres de fond de plaque sont affichés. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
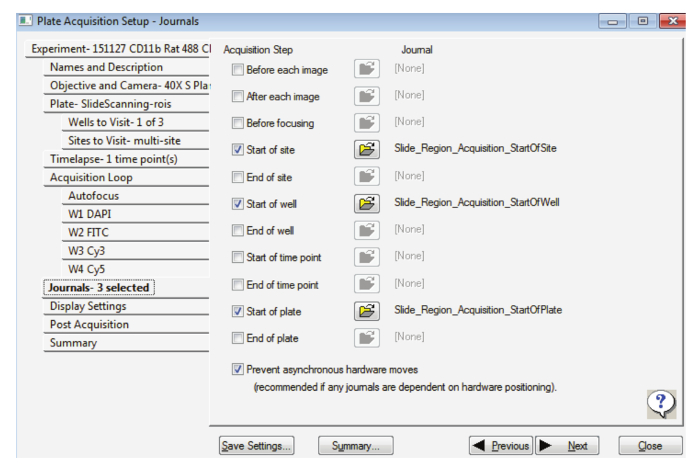
Figure 2 : paramètres d’acquisition de la diapositive à fort grossissement. Cette figure illustre la sélection des revues appropriées. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
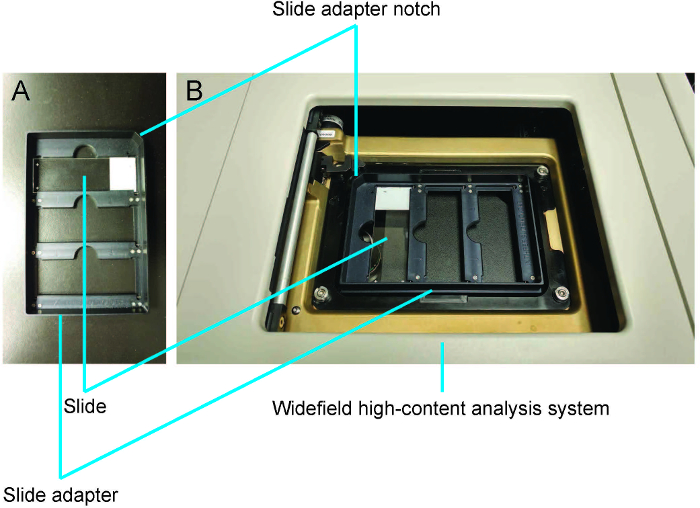
Figure 3 : démonstration de comment charger des diapositives à l’aide de l’adaptateur de diapositives. A. la lame est placée lamelle vers le bas avec l’étiquette sur le côté de l’encoche d’adaptateur de diapositives. B. la diapo est chargé dans le système d’analyse de haute teneur widefield. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
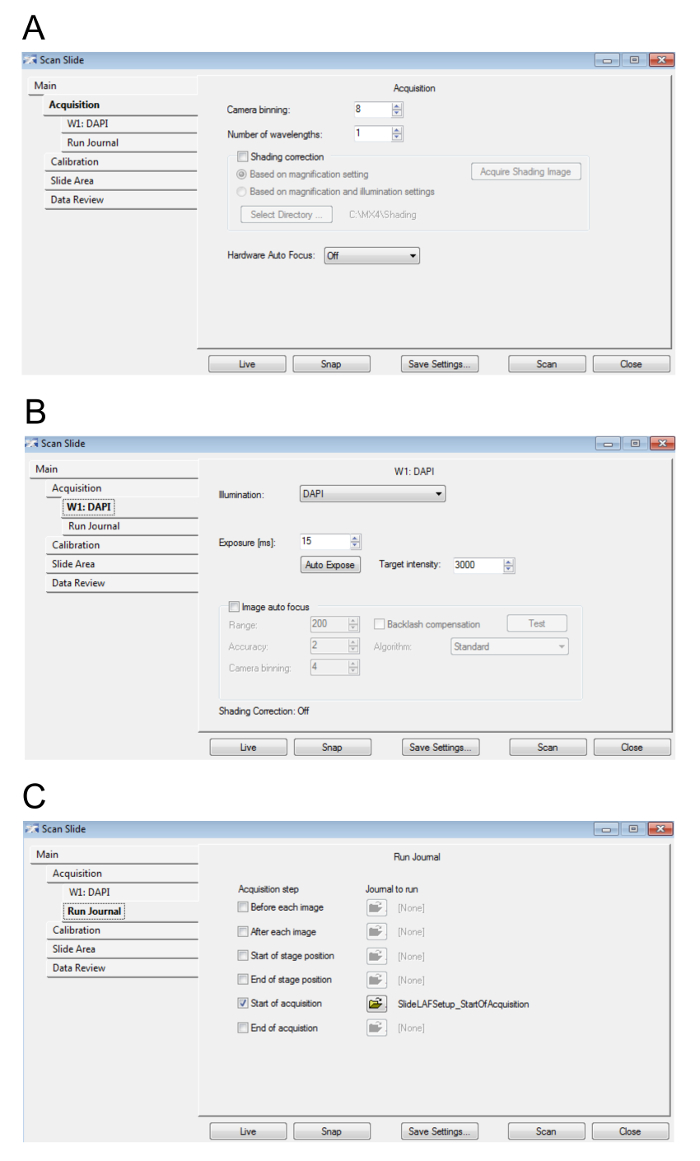
Figure 4 : paramètres d’aperçu diapositives. A. ce chiffre affiche les paramètres pour l’acquisition. B. ici, les valeurs pour les paramètres de longueur d’onde de Hoescht/DAPI sont affichées. C. cette image montre les paramètres du journal. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
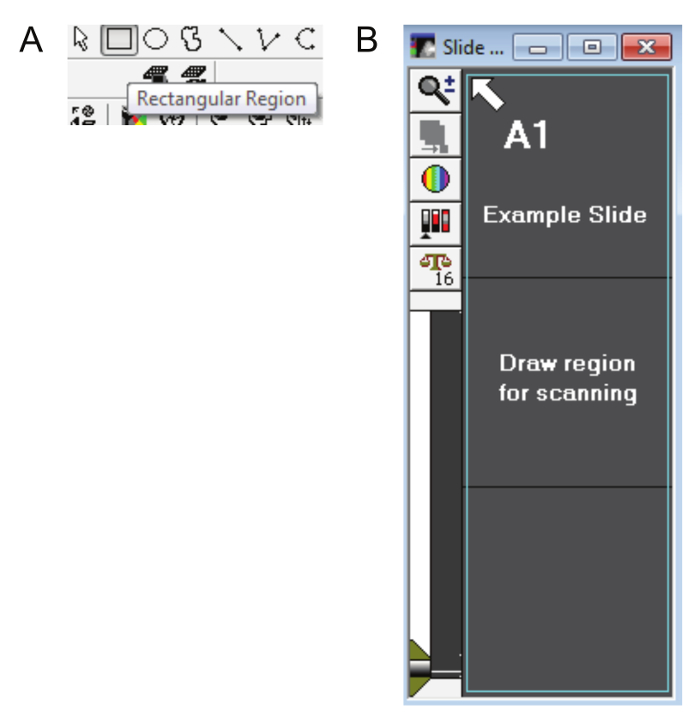
Figure 5 : dessiner une zone de diapositive. A. l’outil zone rectangulaire (les autres outils de dessin ne peut pas être utilisés) est utilisé pour sélectionner la zone aperçu de la numérisation et de créer des zones d’intérêt sur le scan DAPI. B. le contour de teal dans cette figure montre comment toute la surface de la lame (y compris l’étiquette) doit être sélectionnée. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.

Figure 6 : créer des régions d’intérêt sur l’aperçu de la numérisation. L’aperçu ou le scan DAPI représente la zone de diapositive entière. Dans cet exemple, il y a trois sections de tissu de cerveau série (les contours rectangulaires blancs solides). La zone située au-dessus de ces sections représente les étiquettes circulaires sur la diapositive. Arrangements de section différente ne limitera pas la sélection ultérieure des régions d’intérêt. La région d’intérêt dans cet exemple est illustrée avec un plan rectangulaire blanc en pointillé. L’échelle = 1 mm. s’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
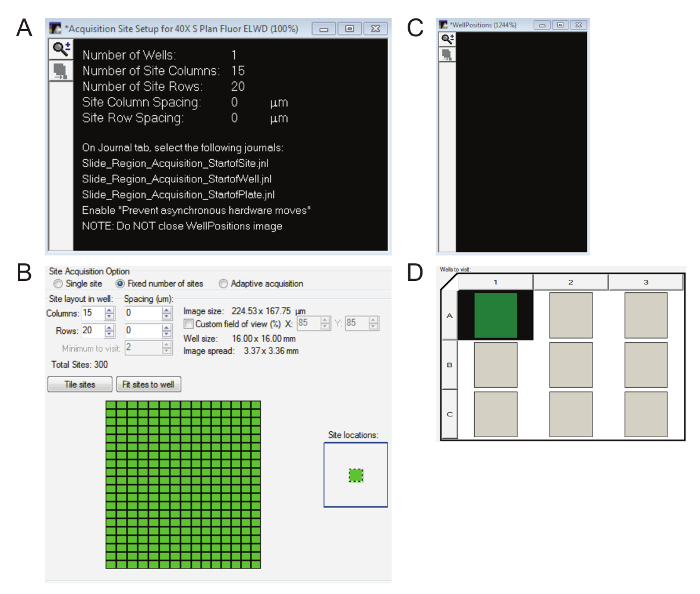
Figure 7 : acquisition d’image windows essentielles à fort grossissement. A. l’Acquisition Site fenêtre montrera combien de colonnes et de lignes sont dans l’ou les régions d’intérêt. B. assurer le bon nombre de colonnes et lignes indiquées dans la Figure 7 a sont entrés dans la boîte de configuration de Acquisition de plaque et les sites sont carrelées. C. il est nécessaire de garder la fenêtre de WellPositions ouvert pendant la durée de l’acquisition de l’image, même si elle est vide. D. le nombre de régions d’intérêt doit être mises en évidence. S’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.

Figure 8 : image représentative de la région d’intérêt. Chaque site peut être affiché dans une composite miniature de la région d’intérêt. Les sites représentatifs qui ont été exclus (marquées avec cases rouges) et un exemple d’un site inclus (marqué avec une boîte verte) est montré à un grossissement plus élevé. Il est recommandé d’examiner chaque site pour s’assurer que c’est d’une qualité suffisante pour l’analyse. L’échelle = 1 mm. s’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
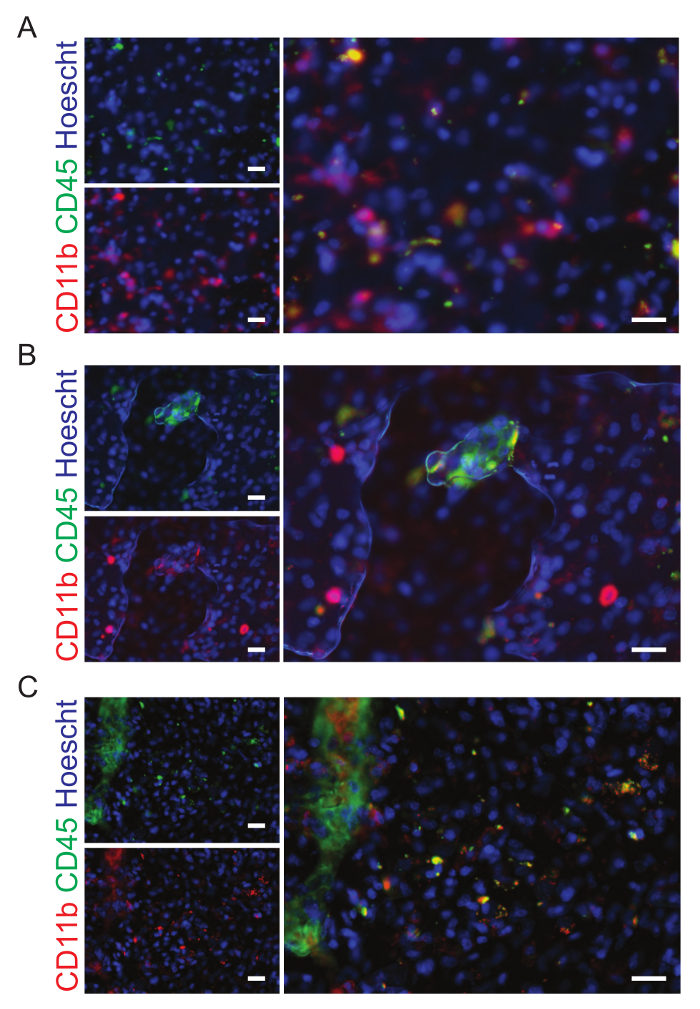
Figure 9 : exemples de sites qui doivent être exclus de l’analyse. A. les sections de tumeur du cerveau humain ont été souillées avec CD11b (vert) et CD45 (rouge), marqueurs de la microglie et des macrophages. Cette image est floue et a été exclue de l’analyse. B. bulles sont présents dans cette image qui a été exclue de l’analyse finale. C. Ce site a été exclu de l’analyse à cause du pli dans le tissu. Les barres d’échelle sont 20 µm. s’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
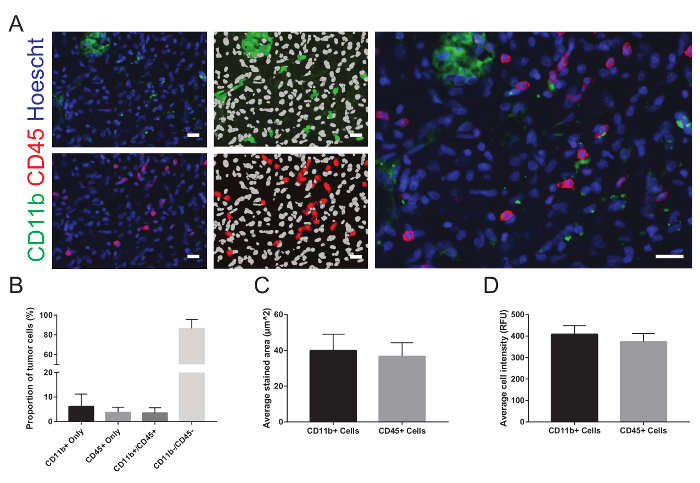
Figure 10 : images représentatives et analyse. A. chaque image est affichée en regard les superpositions représentant les résultats de la segmentation automatique. Dans l’overlay, noyaux sont affichés en blanc et cellules colorées positivement sont représentées en vert CD11b et rouge pour CD45. Après à l’exclusion des sites de qualité insuffisante de l’analyse et en combinant les résultats de tous les sites restants, B. les proportions moyennes du nombre total de cellules dans chaque site qui souillé positifs pour chaque marqueur et étiqueté conjointement pour les deux marqueurs, C. la moyenne teinté de zone et D. l’intensité moyenne des cellules sont représentés graphiquement. RFU = unités de fluorescence relative. Les données sont exprimées en moyenne ± écart-type. Les barres d’échelle sont 20 µm. s’il vous plaît cliquez ici pour visionner une version agrandie de cette figure.
Discussion
Un problème commun qui entravent l’efficacité de la recherche en sciences biologiques est l’élaboration de protocoles pour la quantification impartiale, exacte et précise des tissus fluorescent marqué et leurs structures au sein. Des quantités importantes de temps et d’efforts sont orientées vers la recherche de moyens pour analyser des lames de tissu une fois qu’ils ont été photographiés. Beaucoup de méthodes existantes fournit des algorithmes pour les utilisateurs de recréer au sein de programmes12,13,14. Ces méthodes sont acceptables, mais l’importance de ce rapport est qu’il permet à l’utilisateur de facilement et rapidement créer une acquisition d’image globale et le protocole d’analyse si l’utilisateur a accès à un WHCAS. Essais de différencient les types de cellules et de quantifier plusieurs structures et processus, analyse du cycle cellulaire et la translocation nucléaire, par exemple, sont déjà disponibles dans le logiciel associé.
La configuration implique quelques étapes cruciales. Tout d’abord, les paramètres spatiaux de la lame sont définis comme s’il s’agissait d’une plaque. Deuxièmement, un scan d’aperçu de faible grossissement est créé d'où les régions d’intérêt sont sélectionnées pour l’imagerie fort grossissement. Enfin, les sites qui affectent l’exactitude et la précision des analyses subséquentes sont exclus. La plus grande limitation de cette technique est que son applicabilité dépend de si l’utilisateur a accès à un WHCAS. Cependant, avec le besoin croissant de systèmes d’analyse de haute teneur, nombreuses institutions fournissent à leurs chercheurs de demeurer concurrentiel15. Dépannage est nécessaire plus couramment lors de coupes de tissus n’ont pas la même épaisseur. Si plusieurs régions d’intérêt sont sélectionnées, certains seront en bref tandis que d’autres ne le feront pas. Idéalement, au cours de la section, l’utilisateur prendrait soin pour créer des échantillons homogènes. Toutefois, si les échantillons sont incompatibles, se concentrer sur la longueur d’onde de la coloration nucléaire (ou fluorophore plus brillants de l’utilisateur), qui sert à la mise au point, peut être réajusté pour chaque région d’out-of-focus d’intérêt et même pour chaque champ de vision. Les autres longueurs d’onde sont simplement compensées de la longueur d’onde de la coloration nucléaire, seulement cette longueur d’onde a besoin de réajustement.
Dans ce rapport, nous détaillons comment numériser et analyser les diapositives à l’aide d’un WHCAS et des logiciels associés. Le module multi-longueur d’onde cellulaire Scoring permet à l’utilisateur de compter automatiquement des marqueurs nucléaires et cytoplasmiques qui sont étiquetés fluorescent. Après les réglages de mise au point et définissant les caractéristiques cellulaires tels que la largeur et transversale pour personnaliser le module au tissu imagé, il n’est plus nécessaire pour l’intervention de l’utilisateur d’obtenir les slides imagés et les données quantitatives. Jusqu'à trois diapositives peut être photographiée à la fois et plusieurs régions d’intérêt peuvent être définies. Cela permet de protocole WHCAS utilisateurs qui ont besoin d’analyser les diapositives profiter de personnalisable, polyvalent, automatisé des workflows qui ne nécessitent peu ou aucun optimisation et peuvent être appliquées dans tous les projets dans l’avenir qui impliquent l’analyse histologique des tissus.
Déclarations de divulgation
Les auteurs n’ont aucun intérêt financier dans les produits décrits dans ce manuscrit et n’ont rien d’autre à divulguer.
Remerciements
Ce projet a été financé par une subvention des instituts de recherche en santé du Canada et Alberta Innovates - Health Solutions/Alberta Cancer Foundation. Les auteurs tiennent à souligner l’unité de régénération dans les installations de base neurobiologie de l’utilisation de leurs équipements, les travaux de Paula Gedraitis dans la construction de la Fondation sur laquelle diapositive balayage sur le WHCAS a été rendu possible et le créateur des produits mentionnées dans cet article, Molecular Devices.
matériels
| Name | Company | Catalog Number | Comments |
| ImageXpress MicroXLS | Molecular Devices | NA | Apparatus for image acquisition |
| MetaXpress 5.1 | Molecular Devices | NA | Associated software for ImageXpress MicroXL (runs on a PC with the Windows operating system). |
| Slide adapter | Molecular Devices | NA | Metal slide holder that fits into ImageXpress MicroXL |
| Slide_Region_Acquisition_revA.jzp | Molecular Devices | NA | The journal can be obtained from metamorph.moleculardevices.com/forum/showthread.php?tid=218&highlight=slide or from contacting a Molecular Devices representative |
| Slide_Region_Acquisition _Setup.JNL | Molecular Devices | NA | Select this journal in Step 6.6. |
Références
- Hua, Y., Shun, T. Y., Strock, C. J., Johnston, P. A. High-content positional biosensor screening assay for compounds to prevent or disrupt androgen receptor and transcriptional intermediary factor 2 protein-protein interactions. Assay and Drug Development Technologies. 12 (7), 395-418 (2014).
- Rishal, I., et al. WIS-NeuroMath enables versatile high throughput analyses of neuronal processes. Developmental Neurobiology. 73 (3), 247-256 (2013).
- Kanungo, J., Lantz, S., Paule, M. G. In vivo imaging and quantitative analysis of changes in axon length using transgenic zebrafish embryos. Neurotoxicology and Teratology. 33 (6), 618-623 (2011).
- Schurmann, C., et al. Analyzing illumina gene expression microarray data from different tissues: methodological aspects of data analysis in the MetaXpress Consortium. PLoS ONE. 7 (12), e50938 (2012).
- Vogt, A., Codore, H., Day, B. W., Hukriede, N. A., Tsang, M. Development of automated imaging and analysis for zebrafish chemical screens. Journal of Visualized Experiments. (40), e1900 (2010).
- Bravo-San Pedro, J. M., et al. High-throughput quantification of GFP-LC3+ dots by automated fluorescence microscopy. Methods in Enzymology. , 71-86 (2017).
- Varga, V. S., et al. Automated multichannel fluorescent whole slide imaging and its application for cytometry. Cytometry Part A. 75 (12), 1020-1030 (2009).
- Narayan, P. J., et al. Assessing fibrinogen extravasation into Alzheimer's disease brain using high-content screening of brain tissue microarrays. Journal of Neuroscience Methods. 247, 41-49 (2015).
- Du, Y., Budman, H. M., Duever, T. A. Segmentation and quantitative analysis of apoptosis of Chinese hamster ovary cells from fluorescence microscopy images. Microscopy and Microanalysis. 23 (3), 569-583 (2017).
- Mueller, J. L., et al. Quantitative segmentation of fluorescence microscopy images of heterogeneous tissue: application to the detection of residual disease in tumor margins. PLoS One. 8 (6), e66198 (2013).
- Donnelly, D. J., Gensel, J. C., Ankeny, D. P., van Rooijen, N., Popovich, P. G. An efficient and reproducible method for quantifying macrophages in different experimental models of central nervous system pathology. Journal of Neuroscience Methods. 181 (1), 36-44 (2009).
- Kozlowski, C., Weimer, R. M. An automated method to quantify microglia morphology and application to monitor activation state longitudinally in vivo. PLoS One. 7 (2), e31814 (2012).
- Fish, K. N., Sweet, R. A., Deo, A. J., Lewis, D. A. An automated segmentation methodology for quantifying immunoreactive puncta number and fluorescence intensity in tissue sections. Brain Research. 1240, 62-72 (2008).
- Zock, J. M. Applications of high content screening in life science research. Combinatorial Chemistry & High Throughput Screening. 12 (9), 870-876 (2009).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon