Method Article
Un test électrochimiluminescence 7-plex à haut débit dépistant simultanément le diabète de type 1 et de multiples maladies auto-immunes
* Ces auteurs ont contribué à parts égales
Dans cet article
Résumé
Nous modélisons un test ECL multiplexé simple qui combine 7 tests d’auto-anticorps. Le test est capable de dépister le DT1 et plusieurs autres maladies auto-immunes, simultanément, y compris la maladie cœliaque, la maladie thyroïdienne auto-immune et le syndrome polyglandulaire auto-immun 1.
Résumé
Les autoanticorps des îlots pancréatiques (IAbs) sont largement utilisés dans le diagnostic et la prédiction du diabète de type 1 (DT1). Quatre IAbs majeurs à l’insuline (IAA), la glutamate décarboxylase-65 (GADA), l’antigène 2 de l’insulinome (IA-2A) et le transporteur de zinc 8 (ZnT8A) sont tout aussi importants dans la prédiction de la maladie. À l’heure actuelle, jusqu’à 40 % des patients diagnostiqués avec le DT1 développent d’autres maladies auto-immunes. Malheureusement, les méthodes de dépistage actuelles utilisant un seul autoanticorps pour la mesure sont laborieuses et inefficaces pour les études de dépistage à grande échelle. Nous avons récemment développé un test simple d’électrochimiluminescence multiplexée (ECL) pour résoudre ces problèmes actuels. Le test combine les 7 tests d’autoanticorps dans un seul puits. Chaque puits comprend trois IAbs (IAA, GADA et IA-2A), des autoanticorps dirigés contre la peroxydase thyroïdienne (TPOA) et la thyroglobuline (ThGA) pour détecter les maladies thyroïdiennes auto-immunes, des autoanticorps dirigés contre la transglutaminase tissulaire (TGA) pour la maladie cœliaque et des autoanticorps dirigés contre l’interféron alpha (IFNαA) pour le syndrome polyglandulaire auto-immun-1 (APS-1); qui dépister simultanément le DT1 et d’autres maladies auto-immunes pertinentes. Le test ECL multiplex est basé sur la plate-forme de dosage ECL unique, mais utilise plutôt la plaque multiplex combinant plusieurs tests d’auto-anticorps, jusqu’à 10, dans un seul puits. La principale différence par rapport au test ECL unique est que chaque complexe anticorps-antigène formé dans la phase fluide est retenu sur un point spécifique de chaque puits par un système de liaison sur la plaque multiplex. Le test ECL 7-Plex, dans la présente étude, est validé par rapport aux tests de liaison radio (RBA) standard et aux tests ECL uniques, en utilisant une grande cohorte de patients atteints de DT1 nouvellement diagnostiqués et de témoins sains appariés selon l’âge, ce qui donne une excellente sensibilité et spécificité du test.
Introduction
Le diabète de type 1 (DT1) est une maladie chronique grave qui est plus fréquente dans l’enfance. À l’heure actuelle, environ 1,4 million de personnes ont le DT1 aux États-Unis; Il est frappant de constater que l’incidence du DT1 augmente régulièrement de 3 à 5 % chaque année dans le monde et a doublé au cours des deux dernières décennies, en particulier chez les jeunes enfants[1,2]. Les autoanticorps des îlots pancréatiques (IAbs) dans la circulation sanguine sont le biomarqueur le plus fiable à l’heure actuelle. L’IAbs peut apparaître des années avant que le DT1 clinique ne se développe3. Actuellement, quatre IAbs majeurs sont largement utilisés dans le diagnostic du DT1 et le dépistage des risques, notamment les autoanticorps dirigés contre l’insuline (IAA), la glutamate décarboxylase-65 (GADA), l’antigène 2 de l’insulinome (IA-2A) et le transporteur de zinc 8 (ZnT8A). Ces quatre IAb sont tout aussi importants dans la prédiction du développement du DT1. La classification du DT1 a été redéfinie récemment comme la présence de ≥2 de 4 IAbs avec un métabolisme normal du glucose comme stade 14 de la maladie.
Dans l’étude DAISY (Diabetes Autoimmunity Study in the Young), il a été révélé qu’un enfant sur quatre à risque de DT1 était susceptible de progresser vers une auto-immunité des îlots, des cœliaques, de la thyroïde ou des rhumatoïdes et, plus frappant encore, environ 40% des patients ayant reçu un diagnostic de DT1 finissent par développer une maladie auto-immune supplémentaire 5,6,7 . L’identification des autoanticorps est essentielle pour la prédiction et le diagnostic de ces maladies auto-immunes et devrait fournir de meilleurs soins cliniques aux patients. Il n’existe actuellement aucun moyen facile et peu coûteux de dépister ces multiples maladies auto-immunes. Les méthodes de dépistage actuelles utilisant un test de liaison radio (RBA) standard, avec une seule mesure d’auto-anticorps, sont laborieuses et inefficaces pour un dépistage à grande échelle.
Ici, nous décrirons le nouveau test ECL multiplexé simple, que nous avons authentifié à l’aide d’une seule plate-forme de test ECL 8,9,10,11. Le test ECL multiplex combine 7 tests d’autoanticorps dans un seul puits, utilisant seulement 15 μL de sérum, et est capable de dépister simultanément le DT1 et plusieurs maladies auto-immunes pertinentes, y compris la maladie cœliaque, la maladie thyroïdienne auto-immune et l’APS-1. Un test ECL ZnT8A n’avait pas été développé à l’époque et n’a pas été inclus dans le test multiplexé. Le test ECL multiplex fournit un excellent outil pour le dépistage à haut débit dans la population générale pour le DT1 et les maladies auto-immunes multiples.
Protocole
Le protocole de recherche a été approuvé par le Colorado Multiple Institutional Review Board.
1. Préparation du tampon
- Fabriquez le tampon d’étiquetage (2x PBS, pH 7,9). À l’aide de 400 mL d’eau distillée désionisée (DD), ajouter 100 mL de 10x PBS. Pour ajuster le pH de la solution, ajouter NaOH jusqu’à ce qu’il atteigne 7,9.
- Créer 3 mM de biotine en dissolvant 1 mg de biotine dans 588 μL de tampon d’étiquetage préalablement créé. Faire 3 mM Ru Sulfo-NHS en dissolvant 150 nmol de Ru Sulfo-NHS dans 50 μL de tampon de marquage.
- Fabriquer le tampon antigénique (1 % de BSA) en prenant 500 mL de 1x PBS et en ajoutant 5 g d’albumine sérique bovine (BSA) à la solution. Préparer 0,5 M de solution d’acide acétique. Préparez le tampon Tris-HCl 1 M en utilisant Trizma Base et en ajustant le pH à 9,0.
- Pour le tampon de revêtement (3% Blocker A), prendre 500 mL de 1x PBS et ajouter 15 g de Blocker A. Préparer le tampon de lavage (0,05% Tween 20, PBST) en mélangeant 5000 mL de 1x PBS avec 2,5 mL de Tween 20. Créez un tampon de lecture (2x tampon de lecture T avec surfactant) en ajoutant 500 ml d’eau DD et 500 ml de tampon de lecture T 4x avec surfactant.
REMARQUE: Pour maintenir la cohérence entre les essais, il est important que les solutions de biotine et de Ru Sulfo-NHS soient créées juste avant la procédure d’étiquetage et ne soient pas créées et stockées pour une utilisation future.
2. Marquage de chaque protéine antigénique avec de la biotine et du Ru Sulfo-NHS séparément
REMARQUE: Pour avoir une réaction de marquage plus efficace, utilisez une concentration de protéines antigéniques de ≥0,5 mg / mL.
- Calculer le nombre molaire de chaque protéine antigénique et le nombre molaire de la biotine et du Ru Sulfo-NHS. Ajouter une quantité appropriée de biotine ou de Ru Sulfo-NHS à la protéine antigénique pour marquer la réaction en fonction du rapport molaire de la protéine antigénique à la biotine ou Ru Sulfo-NHS.
- Pour l’antigène qui a le plus petit poids moléculaire (≤10 kDa), comme la protéine proinsuline, utilisez un rapport molaire de 1:5 (antigène: biotine et Ru Sulfo-NHS). Pour l’antigène qui a le plus grand poids moléculaire (>50 kDa), comme la protéine GAD, utilisez un rapport molaire de 1:20. Pour l’antigène qui a un poids moléculaire moyen (10-50 kDa), utilisez un rapport molaire ajusté entre 1:5-1:20.
- Pour la biotine et le Ru Sulfo-NHS, divisez chaque poids d’antigène par leur poids moléculaire correspondant pour obtenir le nombre molaire d’antigène pour chacun. Divisez le nombre molaire par la concentration pour obtenir le volume de biotine. Répétez cette opération pour Ru Sulfo-NHS.
- Mélanger la protéine antigénique avec de la biotine en utilisant le rapport molaire approprié, déterminé à l’étape 2.2. Ensuite, faites de même pour Ru Sulfo-NHS.
REMARQUE: Pour une réaction de marquage efficace, tous les produits chimiques réducteurs tels que le Tris ou la glycine dans le système tampon doivent être remplacés par un tampon PBS 2x, pH 7,9 par la colonne de spin de dimensionnement. Les protocoles d’étiquetage pour la biotine et le Ru Sulfo-NHS sont identiques. - Couvrir les tubes de réaction avec du papier d’aluminium et les incuber à température ambiante (RT) pendant 1 h. La raison pour laquelle les tubes de réaction sont recouverts de papier d’aluminium est que les réactifs de biotine et de Ru Sulfo-NHS sont sensibles à la lumière.
- Amorcer la colonne de spin de 2 mL ou 5 mL pendant l’incubation des tubes de réaction (la taille de la colonne de spin est déterminée par le volume téléchargé sur la colonne). Remplissez la colonne de spin avec 2x tampon PBS, puis centrifugez-la à 1 000 x g pendant 2 minutes à chaque fois, pour un total de trois fois.
- Arrêtez la réaction d’étiquetage une fois que les tubes de réaction ont fini d’incuber. Pour arrêter la réaction, purifiez la protéine antigénique marquée en la faisant passer une fois dans la colonne de spin. Centrifuger ensuite la colonne à 1 000 x g pendant 2 min.
- Calculer la concentration totale d’antigène marqué en divisant la quantité de protéine antigénique présente par le volume final. Aliquote 50 μL de la protéine antigénique marquée purifiée par tube et conserver les aliquotes à -80 °C pour une utilisation à long terme.
REMARQUE: Il est important de savoir que pour chaque fois que la colonne de spin passe la protéine antigénique, il y aura un taux de rétention d’environ 90-95%.
3. Définir la meilleure concentration et les meilleurs rapports pour les deux antigènes marqués pour le test (test en damier)
REMARQUE: Étant donné que le test ECL-IAA dans ce test 7-Plex nécessite un traitement acide des échantillons de sérum, le test en damier pour chaque antigène doit passer par cette étape avant d’incuber avec le mélange d’antigènes marqué.
- Appliquez le test en damier pour chaque antigène séparément avant d’exécuter le test multiplex. Les étapes 3.2 à 3.6 utiliseront GAD65 comme exemple.
- Calculer la dilution de la protéine GAD65 marquée. La concentration ciblée recommandée de la première solution de mélange de GAD65 biotinylé est de 2000 ng / mL et Ru Sulfo-NHS marqué GAD65 est de 1000 ng / mL. Si la concentration de GAD65 biotinylé et de Ru Sulfo-NHS marqué GAD65 dans la solution mère est de 1,0 μg/μL, le volume nécessaire pour le GAD65 biotinylé dans 560 μL de solution de travail sera de 1,12 μL, et le volume nécessaire pour le Ru Sulfo-NHS marqué GAD65 dans 700 μL de solution de travail sera de 0,7 μL.
- Mélanger 1,12 μL de protéine GAD65 biotinylée avec 240 μL de linker conjugué streptavidine 1 dans un tube et 160 μL de BSA à 1%. Incuber le mélange à température ambiante pendant 30 min. Ajouter 160 μL de solution stop dans le tube et incuber le mélange à température ambiante pendant encore 30 min.
- Faire une dilution en série. Prendre 280 μL du mélange dans un nouveau tube et ajouter 280 μL de solution stop pour obtenir une dilution 1:2. Préparez plusieurs nouveaux tubes. Répétez cette étape pour exécuter une dilution en série horizontale de l’antigène GAD65 marqué à la biotine (voir la publication précédente12).
- Mélanger 0,7 μL de protéine GAD65 marquée au Ru Sulfo-NHS (1 μg/μL) avec 700 μL de solution stop. Ensuite, prendre 350 μL du mélange dans un nouveau tube et ajouter 350 μL de solution stop pour obtenir une dilution 1:2. Préparez plusieurs nouveaux tubes, répétez cette étape pour exécuter une dilution en série verticale pour l’antigène GAD65 marqué par Ru Sulfo-NHS.
- Préparer deux échantillons de sérum, un échantillon très positif pour GADA et un échantillon négatif pour GADA, chacun ayant un volume de 0,75 mL. Aliquote 15 μL de sérum positif dans chaque puits de la moitié gauche de la plaque PCR à 96 puits. Aliquote 15 μL de sérum négatif dans chaque puits de la moitié droite de la plaque PCR à 96 puits.
- Ajouter 18 μL d’acide acétique 0,5 M dans chaque puits et mélanger. Incuber pendant 45 min à TA. Préparer une nouvelle plaque PCR à 96 puits. Ajouter 17,5 μL de l’antigène marqué à la biotine et 17,5 μL de l’antigène marqué Ru Sulfo-NHS dans chaque puits selon les dilutions en série (voir la publication précédente12).
- Continuez le reste des étapes de dosage décrites aux étapes 5.2 à 9.1.
- Déterminer le rapport de signal des échantillons fortement positifs par rapport aux signaux d’échantillons négatifs correspondants. Sélectionnez la meilleure concentration pour l’antigène marqué à la biotine et l’antigène marqué Ru Sulfo-NHS en identifiant le point qui a le rapport le plus élevé ou proche du plus élevé de signal positif / négatif. Dans ce calcul de ratio, considérez le faible signal de fond obtenu à partir des échantillons négatifs.
NOTE: Les concentrations optimales de Ru Sulfo-NHS et de protéines antigéniques marquées à la biotine provenant des tests en damier sont indiquées ci-dessous: 30 ng / mL et 200 ng / mL pour GAD65, 120 ng / mL et 120 ng / mL pour la proinsuline, 10 ng / mL et 42 ng / mL pour IA-2, 80 ng / mL et 80 ng / mL pour TG, 8 ng / mL et 16 ng / mL pour TPO, 31 ng/mL et 31 ng/mL pour ThG, et 12 ng/mL et 12 ng/mL pour IFNα.
4. Créer la solution d’antigène couplé à un agent de liaison mixte
- Sélectionnez la concentration optimale pour chaque antigène en fonction du test en damier. Diluer l’antigène marqué biotine et Ru Sulfo-NHS à la concentration rationnelle de travail.
- Lier différents liants à chacune des protéines antigéniques biotinylées de manière unique. Pour un essai sur plaque à 96 puits, mélanger 4 μL de GAD65, TPO, tTG, ThG, proinsuline, protéine IFN-α et IA-2 biotinylée avec 240 μL de linker conjugué streptavidine 1, 2, 3, 4, 8, 9 et 10 dans un tube séparé (figure 1). Ajoutez ensuite 156 μL de PBS/1 % de BSA par tube. Incuber le mélange à température ambiante pendant 30 min.
- Ajouter 160 μL de solution stop dans chaque tube et les incuber à température ambiante pendant encore 30 min. Prélevez 400 μL d’antigène couplé à un agent de liaison de chaque tube et combinez les 7 antigènes ensemble. Ajouter 1,2 mL de solution stop, puis ajouter 4 μL de Ru Sulfo-NHS marqué GAD65, TPO, tTG, ThG, proinsuline, IFN-α et antigène IA-2 au mélange. Maintenant, la solution antigénique est prête à être utilisée dans le test.
5. Incuber les échantillons de sérum avec l’antigène marqué
REMARQUE: Étant donné que le test ECL-IAA de ce test 7-Plex nécessite un traitement acide des échantillons de sérum, chaque sérum nécessite l’étape de traitement acide avant d’être incubé avec un mélange d’antigènes marqué pour ce test 7-Plex.
- Aliquote 15 μL de sérum par puits pour une plaque PCR à 96 puits. Ajouter 18 μL d’acide acétique 0,5 M dans chaque puits et mélanger. Incuber pendant 45 min à TA. Préparer une nouvelle plaque de PCR à 96 puits et aliquoter 35 μL de solution antigénique dans chaque puits.
- Pendant que la plaque est encore en incubation, ajouter 13 μL de tampon Tris pH 9,0 de 1 M à chaque puits de la plaque antigénique. Ajouter un tampon sur le côté de chaque puits pour limiter le mélange du tampon Tris et de l’antigène. Une fois l’incubation terminée, prenez 25 μL du sérum traité à l’acide et pipetez-le immédiatement dans chaque puits de la plaque antigénique. Agiter la solution et couvrir la plaque avec une feuille d’étanchéité PCR pour éviter l’exposition à la lumière.
- A la RT, poser la plaque sur un shaker, réglé à basse vitesse, pendant 1 h. Ensuite, conservez la plaque à 4 °C et laissez la plaque incuber pendant 18-24 h.
6. Préparez la plaque multiplex
- Prenez une plaque multiplex du réfrigérateur à 4 °C et laissez la plaque venir à RT. Une fois que la plaque multiplex est à RT, ajouter 150 μL de bloqueur A à 3 % à chaque puits. Couvrir la plaque multiplex d’une feuille d’étanchéité. Incuber la plaque dans un réfrigérateur à 4 °C pendant une nuit.
REMARQUE : Le jour 1 du test comprend les étapes 4 à 6.
7. Transférer les incubations de sérum/antigène dans la plaque multiplex
- Le lendemain, placez des serviettes en papier sur la table et sortez l’assiette multiplex d’incubation du réfrigérateur. Videz toute la mémoire tampon de la plaque. Pour ce faire, retournez l’assiette et collez-la sur les serviettes en papier préparées jusqu’à ce qu’il n’y ait plus de tampon dans aucun des puits.
- Lavez la plaque multiplex en ajoutant 150 μL de PBST dans chaque puits. Supprimez la mémoire tampon, comme mentionné à l’étape 7.1., et répétez cette étape trois fois. Ajouter 30 μL d’incubations de sérum/antigène dans chaque puits de la plaque multiplex. Couvrir la plaque de papier d’aluminium pour limiter son exposition à la lumière. Placer la plaque sur un agitateur à plaque, réglé à basse vitesse, à TA pendant 1 h.
8. Lavez la plaque et ajoutez un tampon de lecture
- Retirez le sérum/antigène incuber de la plaque multiplex en tenant la plaque à l’envers et en faisant sortir la solution. Ajouter 150 μL de PBST dans tous les puits et retirer le tampon de la plaque en tenant à nouveau la plaque à l’envers et en faisant sortir la solution. Répétez cette étape trois fois. Une fois le troisième lavage terminé, ajoutez 150 μL de tampon de lecture dans chaque puits.
REMARQUE: Les bulles d’air interfèrent avec la capacité de la machine de lecture de plaques à analyser avec précision les résultats de la plaque et doivent être évitées à tout prix.
9. Lire l’assiette et analyser les données
- Comptez la plaque préparée sur la machine de lecture de plaques, en lisant toutes les valeurs en comptage par seconde (CPS).
- Calculer l’indice relatif pour le test, en utilisant les niveaux d’anticorps obtenus à partir de l’appareil de lecture de plaques, avec l’équation suivante:
Valeur de l’indice = [CPS (échantillon) - CPS (norme négative)] / [CPS (norme positive) - CPS (norme négative)]. - Déterminer quels résultats d’anticorps sont négatifs ou positifs à l’aide des seuils qui ont été établis.
REMARQUE : Le jour 2 du test comprend les étapes 7 à 9.
Résultats
L’analyse des résultats des essais a été présentée dans les tableaux 1, 2 et 3. Les valeurs de lecture proviennent des données des 10 points dans le même puits. Les valeurs indicatrices de chaque échantillon ont été calculées par rapport aux témoins internes positifs et négatifs correspondants, comme décrit dans le protocole d’essai. Des exemples de doublons défectueux sont présentés dans le tableau 1 et ont causé l’erreur finale de calcul de l’index dans le tableau 3. Toutes les valeurs de comptage brutes doivent être vérifiées pour éviter tout résultat faussement positif ou faux négatif.
Le test ECL à 7 multiplexés a été validé à l’aide d’une vaste cohorte d’échantillons provenant de 1026 patients nouvellement diagnostiqués atteints de DT1 et de 1022 sujets témoins sains appariés selon l’âge et le sexe. Les taux d’autoanticorps du test ECL 7-Plex pour 1026 patients atteints de DT1 ont été comparés aux niveaux de chacun de nos tests ECL uniques établis correspondants, comme illustré à la figure 2 , et de chaque RBA et ELISA standard correspondants, comme illustré à la figure 3. Les spécificités du test ont été établies identiques au 99epercentile pour tous les tests d’auto-anticorps, à l’exception des autoanticorps thyroïdiens (où le 95e percentile a été utilisé), de 1022 témoins sains pour les trois méthodes de dosage (ECL 7-Plex, ECL unique, RBA ou ELISA) comme indiqué dans le tableau 4. Les CV inter-essais de GADA, IA-2A, IAA, TPOA, ThGA, TGA et IFNαA sont respectivement de 6,4%, 4,5%, 9,1%, 4,9%, 5,7%, 11,3% et 5,9%.
Un petit nombre d’échantillons discordants pour chacun des 7 autoanticorps ont été trouvés autour de la limite des seuils pour chaque test (Figure 2 et Figure 3). Onze échantillons témoins (11/1022, 1,1%) se sont révélés positifs pour plusieurs autoanticorps positifs uniquement dans le test 7-Plex et négatifs dans chaque test unique correspondant. De même, cela s’est produit dans 9 échantillons de patients atteints de DT1 (9/1026, 0,9%). En outre, 10 TPOA et un ThGA positifs dans la cohorte de patients qui ont été observés à la fois dans le test ECL unique et RBA ont été manqués dans le test 7-Plex. Ces échantillons ont été convertis positifs dans le test 7-Plex lorsqu’ils ont été dilués davantage. En général, 100 % de la positivité dans le test ECL unique ou RBA a été couvert dans le test ECL 7-Plex, avec la même spécificité de test que celle illustrée dans le tableau 4.
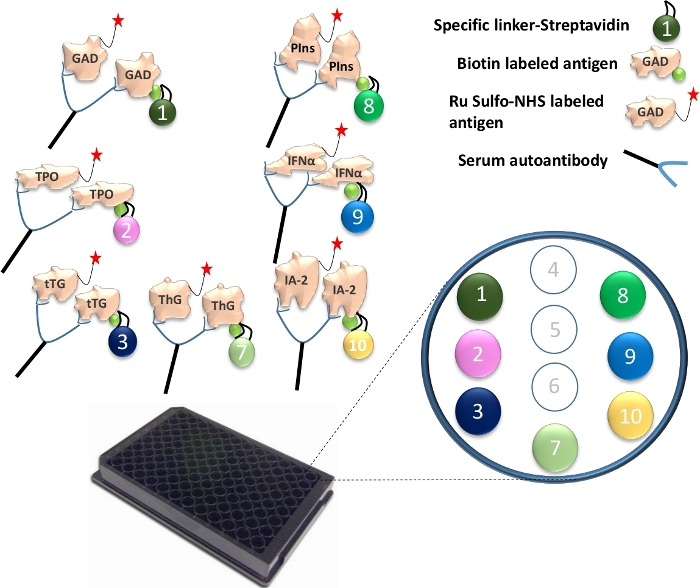
Figure 1 : Illustration du test Mutiplex ECL.
Les autoanticorps dans le sérum relieront l’antigène Ru Sulfo-NHSged à l’antigène biotinylé. Ceci est couplé avec un linker spécifique pour former un complexe antigène-anticorps-antigène-linker. Les complexes sont capturés sur la plaque et sont limités à leurs points spécifiques à travers chaque linker spécifique. Les numéros de liaison spécifiquement couplés, pour les 7 protéines antigéniques différentes, sont illustrés. La détection des signaux d’anticorps est réalisée à l’aide d’antigènes marqués Ru Sulfo-NHS avec électrochimiluminescence. Le chiffre est tiré de Gu, Y. et al.13. Veuillez cliquer ici pour voir une version agrandie de cette figure.
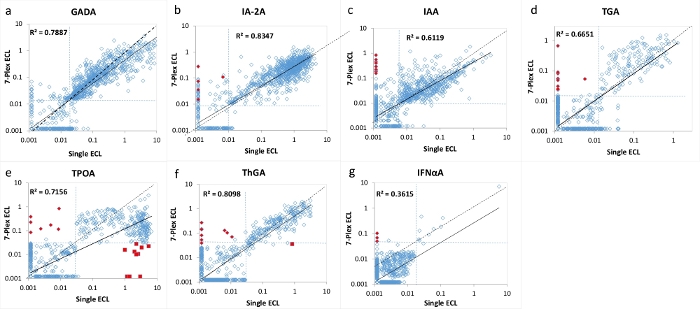
Figure 2 : Comparaison de 7 taux d’autoanticorps chez 1026 patients atteints de DT1 nouvellement apparus entre le test ECL unique et le test ECL 7-Plex.
Les panels a, b, c, d, e, f et g présentent des comparaisons des taux d’autoanticorps pour GADA, IA-2A, IAA, TGA, TPOA, ThGA et IFNαA, respectivement. Les lignes pointillées représentent les seuils de test pour chaque test d’autoanticorps. Les seuils ont été fixés au 99e centile de 1022 témoins sains appariés selon l’âge pour chaque essai (à l’exception de la TPOA et du ThGA qui ont été fixés au 95e centile), comme le montre le tableau 4, à partir de 1022 témoins sains appariés selon l’âge pour les tests ECL simples et multiplex. Les diamants rouges fermés sont marqués comme « faux » positifs dans le test ECL 7-Plex, <1% de la cohorte étudiée, et ils ont été validés comme négatifs à la fois dans l’ECL unique et la RBA. Les carrés fermés rouges sont marqués comme « faux » négatifs dans le test ECL 7-Plex causés par le phénomène « prozone », principalement dans le test TPOA chez <1% de la cohorte étudiée. Ces résultats faussement positifs et faux négatifs sont discutés dans la section de discussion. Le chiffre est tiré de Gu, Y. et al.13. Veuillez cliquer ici pour voir une version agrandie de cette figure.
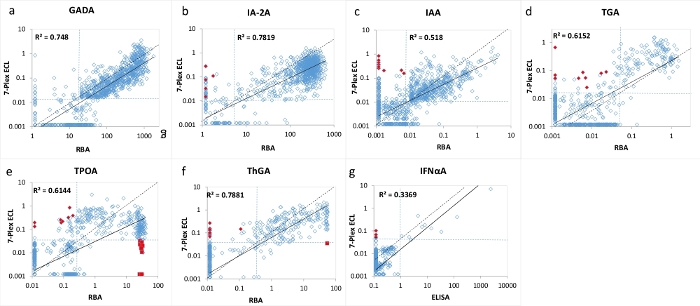
Figure 3 : Comparaison de 7 taux d’autoanticorps chez 1026 patients atteints de DT1 nouvellement apparus entre le test RBA (ELISA pour IFNαA) et le test ECL 7-Plex.
Les panels a, b, c, d, e, f et g présentent des comparaisons des taux d’autoanticorps pour GADA, IA-2A, IAA, TGA, TPOA, ThGA et IFNαA, respectivement. Les lignes pointillées représentent les seuils de dosage pour chaque test d’auto-anticorps, la même spécificité établie pour le test RBA et le test ECL 7-Plex, comme le montre le tableau 4, à partir de 1022 témoins sains appariés selon l’âge. Les losanges et les carrés fermés rouges représentent les « faux » positifs et les « faux » négatifs apparaissant dans le test ECL 7-Plex, la même chose est illustrée à la figure 2. Le chiffre est tiré de Gu, Y. et al.13. Veuillez cliquer ici pour voir une version agrandie de cette figure.
| 1 | 2 | 3 | 4 | 5 | 6 | ||
| Un | 5580 | 5674 | 105 | 117 | 125 | 139 | linker-1 |
| 100 | 108 | 102 | 102 | 3956 | 3745 | linker-2 | |
| 115 | 124 | 107 | 116 | 113 | 124 | linker-3 | |
| 67 | 64 | 68 | 61 | 65 | 69 | linker-4 | |
| 89 | 87 | 98 | 92 | 90 | 80 | linker-5 | |
| 87 | 71 | 89 | 87 | 61 | 72 | linker-6 | |
| 94 | 82 | 79 | 85 | 2154 | 2280 | linker-7 | |
| 75 | 66 | 1628 | 1594 | 81 | 83 | linker-8 | |
| 98 | 103 | 71 | 84 | 69 | 85 | linker-9 | |
| 102 | 118 | 93 | 98 | 113 | 99 | linker-10 | |
| B | 324 | 337 | 147 | 148 | 5426 | 5366 | linker-1 |
| 101 | 102 | 93 | 88 | 86 | 74 | linker-2 | |
| 111 | 119 | 119 | 123 | 66 | 72 | linker-3 | |
| 72 | 65 | 59 | 68 | 74 | 67 | linker-4 | |
| 81 | 98 | 83 | 92 | 79 | 72 | linker-5 | |
| 90 | 84 | 93 | 86 | 70 | 76 | linker-6 | |
| 101 | 105 | 101 | 97 | 956 | 944 | linker-7 | |
| 82 | 83 | 189 | 204 | 97 | 90 | linker-8 | |
| 92 | 83 | 78 | 64 | 82 | 78 | linker-9 | |
| 83 | 79 | 88 | 93 | 4722 | 4965 | linker-10 | |
| C | 110 | 110 | 87 | 81 | 2114 | 2365 | linker-1 |
| 5526 | 5680 | 88 | 70 | 86 | 93 | linker-2 | |
| 114 | 132 | 67 | 71 | 3326 | 3284 | linker-3 | |
| 64 | 62 | 88 | 74 | 64 | 80 | linker-4 | |
| 94 | 82 | 86 | 75 | 89 | 76 | linker-5 | |
| 77 | 87 | 75 | 63 | 70 | 86 | linker-6 | |
| 77 | 86 | 71 | 84 | 138 | 121 | linker-7 | |
| 73 | 86 | 80 | 79 | 59 | 73 | linker-8 | |
| 86 | 74 | 5064 | 4923 | 88 | 86 | linker-9 | |
| 105 | 113 | 85 | 80 | 124 | 114 | linker-10 | |
| D | 98 | 88 | 92 | 84 | 136 | 127 | linker-1 |
| 288 | 291 | 86 | 86 | 558 | 564 | linker-2 | |
| 109 | 101 | 74 | 73 | 141 | 127 | linker-3 | |
| 78 | 66 | 66 | 55 | 74 | 66 | linker-4 | |
| 79 | 83 | 79 | 86 | 96 | 91 | linker-5 | |
| 83 | 86 | 96 | 89 | 86 | 73 | linker-6 | |
| 87 | 89 | 77 | 87 | 841 | 855 | linker-7 | |
| 74 | 72 | 60 | 72 | 90 | 95 | linker-8 | |
| 68 | 75 | 331 | 328 | 2460 | 2580 | linker-9 | |
| 86 | 98 | 80 | 75 | 123 | 133 | linker-10 | |
| E | 101 | 114 | 101 | 106 | 532 | 548 | linker-1 |
| 101 | 96 | 110 | 104 | 682 | 675 | linker-2 | |
| 6015 | 5988 | 124 | 126 | 101 | 98 | linker-3 | |
| 66 | 71 | 82 | 71 | 80 | 62 | linker-4 | |
| 102 | 97 | 99 | 80 | 83 | 110 | linker-5 | |
| 82 | 67 | 81 | 80 | 60 | 85 | linker-6 | |
| 85 | 95 | 52 | 84 | 245 | 221 | linker-7 | |
| 72 | 78 | 82 | 74 | 486 | 503 | linker-8 | |
| 77 | 97 | 97 | 77 | 56 | 66 | linker-9 | |
| 114 | 104 | 5726 | 5814 | 259 | 253 | linker-10 | |
| F | 119 | 120 | 133 | 118 | 112 | 96 | linker-1 |
| 101 | 91 | 100 | 95 | 96 | 82 | linker-2 | |
| 406 | 395 | 111 | 123 | 2127 | 101 | linker-3 | |
| 72 | 60 | 86 | 72 | 79 | 83 | linker-4 | |
| 76 | 85 | 96 | 99 | 89 | 103 | linker-5 | |
| 88 | 78 | 91 | 83 | 89 | 95 | linker-6 | |
| 104 | 97 | 87 | 102 | 56 | 66 | linker-7 | |
| 76 | 77 | 79 | 93 | 69 | 75 | linker-8 | |
| 85 | 71 | 95 | 100 | 83 | 71 | linker-9 | |
| 131 | 131 | 358 | 364 | 92 | 86 | linker-10 | |
| G | 90 | 95 | 85 | 82 | 105 | 107 | linker-1 |
| 99 | 86 | 77 | 76 | 1250 | 1174 | linker-2 | |
| 119 | 123 | 120 | 118 | 112 | 108 | linker-3 | |
| 76 | 83 | 77 | 80 | 86 | 76 | linker-4 | |
| 88 | 86 | 86 | 93 | 107 | 92 | linker-5 | |
| 73 | 73 | 71 | 82 | 84 | 75 | linker-6 | |
| 5210 | 5173 | 72 | 69 | 76 | 85 | linker-7 | |
| 80 | 81 | 79 | 82 | 100 | 101 | linker-8 | |
| 96 | 97 | 89 | 83 | 65 | 83 | linker-9 | |
| 98 | 103 | 86 | 88 | 1933 | 1979 | linker-10 | |
| H | 114 | 124 | 81 | 86 | 299 | 295 | linker-1 |
| 107 | 92 | 69 | 72 | 4256 | 4388 | linker-2 | |
| 114 | 123 | 125 | 129 | 501 | 536 | linker-3 | |
| 77 | 70 | 67 | 64 | 74 | 62 | linker-4 | |
| 92 | 110 | 81 | 84 | 77 | 71 | linker-5 | |
| 87 | 79 | 72 | 76 | 83 | 81 | linker-6 | |
| 328 | 341 | 84 | 80 | 88 | 97 | linker-7 | |
| 75 | 84 | 75 | 90 | 74 | 83 | linker-8 | |
| 73 | 79 | 78 | 76 | 84 | 70 | linker-9 | |
| 113 | 120 | 81 | 76 | 2372 | 2350 | linker-10 | |
Tableau 1 : Analyse du test ECL 7-plex : numération CPS brute (moitié gauche de la plaque). Les comptes de CPS bruts sont acquis à partir d’une plaque d’essai (la moitié gauche de la plaque) et chaque échantillon est effectué en double. Sous chaque rangée de la plaque (A-H), il y a 10 lignes de valeurs de lecture représentant les données des 10 points dans le même puits, correspondant à chaque numéro de linker tel que marqué. Les exemples de doublons défectueux sont surlignés en gris, comme on le voit dans la ligne F-linker 3-colonnes 5 et 6.
| Ligne du tableau 1A | Colonne du tableau 1A | éditeur de liens 1 | éditeur de liens 2 | éditeur de liens 3 | éditeur de liens 7 | éditeur de liens 8 | éditeur de liens 9 | éditeur de liens 10 | |
| Un | 1-2 | GADA PC | 5627 | 104 | 120 | 88 | 71 | 101 | 110 |
| B | 1-2 | GADA Low PC | 331 | 102 | 115 | 103 | 83 | 88 | 81 |
| C | 1-2 | TPOA PC | 110 | 5603 | 123 | 82 | 80 | 80 | 109 |
| D | 1-2 | TPOA Low PC | 93 | 290 | 105 | 88 | 73 | 72 | 92 |
| E | 1-2 | TGA PC | 108 | 99 | 6002 | 90 | 75 | 87 | 109 |
| F | 1-2 | TG Low PC | 120 | 96 | 401 | 101 | 77 | 78 | 131 |
| G | 1-2 | ThGA PC | 93 | 93 | 121 | 5192 | 81 | 97 | 101 |
| H | 1-2 | ThGA Low PC | 119 | 100 | 119 | 335 | 80 | 76 | 117 |
| Un | 3-4 | IAA PC | 111 | 102 | 112 | 82 | 1611 | 78 | 96 |
| B | 3-4 | IAA Low PC | 148 | 91 | 121 | 99 | 197 | 71 | 91 |
| C | 3-4 | IFNaA PC | 84 | 79 | 69 | 78 | 80 | 4994 | 83 |
| D | 3-4 | IFNaA Low PC | 88 | 86 | 74 | 82 | 66 | 330 | 78 |
| E | 3-4 | IA-2A PC | 104 | 107 | 125 | 68 | 78 | 87 | 5770 |
| F | 3-4 | IA-2A Low PC | 126 | 98 | 117 | 95 | 86 | 98 | 361 |
| G | 3-4 | NC | 84 | 77 | 119 | 71 | 81 | 86 | 87 |
| H | 3-4 | NC | 84 | 71 | 127 | 82 | 78 | 77 | 79 |
| Un | 5-6 | échantillon1 | 132 | 3851 | 119 | 2217 | 82 | 77 | 106 |
| B | 5-6 | échantillon2 | 5396 | 80 | 69 | 950 | 94 | 80 | 4844 |
| C | 5-6 | échantillon3 | 2240 | 90 | 3305 | 130 | 66 | 87 | 119 |
| D | 5-6 | échantillon4 | 132 | 561 | 134 | 848 | 93 | 2520 | 128 |
| E | 5-6 | échantillon5 | 540 | 679 | 100 | 233 | 495 | 61 | 256 |
| F | 5-6 | échantillon6 | 104 | 89 | 1114 | 61 | 72 | 77 | 89 |
| G | 5-6 | échantillon7 | 106 | 1212 | 110 | 81 | 101 | 74 | 1957 |
| H | 5-6 | échantillon8 | 297 | 4322 | 519 | 93 | 79 | 77 | 2361 |
Tableau 2 : Analyse du test ECL 7-plex : disposition des données du tableau 1, marquées comme 7 linkers. Les données du tableau 1 ont été réorganisées, les liens 4 à 6 (non utilisés) ont été supprimés, et les valeurs moyennes ont été calculées à partir de chaque lecture en double du tableau 1. Les valeurs des témoins positifs élevés et faibles de la norme interne, correspondant à chaque test d’auto-anticorps, retenus par un agent de liaison particulier, sont en gras foncé. PC, contrôle positif. NC, contrôle normal.
| GAD-Index | Indice TPOA | Indice TGA | Indice ThGA | Indice IAA | Indice IFNaA | Indice IA-2A | |
| GADA PC | 1.000 | 0.005 | 0.000 | 0.003 | -0.006 | 0.003 | 0.004 |
| GADA Low PC | 0.045 | 0.005 | -0.001 | 0.006 | 0.002 | 0.000 | -0.001 |
| IAA PC | 0.005 | 1.000 | 0.001 | 0.002 | -0.001 | -0.001 | 0.004 |
| IAA Low PC | 0.002 | 0.039 | -0.002 | 0.003 | -0.005 | -0.003 | 0.001 |
| IA-2A PC | 0.004 | 0.004 | 1.000 | 0.004 | -0.004 | 0.000 | 0.004 |
| IA-2A Low PC | 0.007 | 0.004 | 0.048 | 0.006 | -0.002 | -0.002 | 0.008 |
| TGA PC | 0.002 | 0.003 | 0.000 | 1.000 | 0.000 | 0.002 | 0.002 |
| TG Low PC | 0.006 | 0.004 | 0.000 | 0.052 | -0.001 | -0.002 | 0.005 |
| TPOA PC | 0.005 | 0.005 | -0.001 | 0.002 | 1.000 | -0.002 | 0.001 |
| TPOA Low PC | 0.012 | 0.003 | 0.000 | 0.006 | 0.076 | -0.003 | 0.001 |
| ThGA PC | 0.000 | 0.000 | -0.008 | 0.001 | 0.000 | 1.000 | -0.001 |
| ThGA Low PC | 0.001 | 0.002 | -0.008 | 0.002 | -0.009 | 0.050 | -0.002 |
| IFNaA PC | 0.004 | 0.006 | 0.001 | 0.000 | -0.002 | 0.000 | 1.000 |
| IFNaA Low PC | 0.008 | 0.004 | 0.000 | 0.005 | 0.004 | 0.002 | 0.048 |
| NC | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 | 0.000 |
| NC | 0.000 | -0.001 | 0.001 | 0.002 | -0.002 | -0.002 | -0.001 |
| échantillon1 | 0.009 | 0.683 | 0.000 | 0.419 | 0.001 | -0.002 | 0.003 |
| échantillon2 | 0.958 | 0.001 | -0.008 | 0.172 | 0.009 | -0.001 | 0.837 |
| échantillon3 | 0.389 | 0.002 | 0.542 | 0.012 | -0.009 | 0.000 | 0.006 |
| échantillon4 | 0.009 | 0.088 | 0.003 | 0.152 | 0.008 | 0.496 | 0.007 |
| échantillon5 | 0.082 | 0.109 | -0.003 | 0.032 | 0.271 | -0.005 | 0.030 |
| échantillon6 | 0.004 | 0.002 | 0.169 | -0.002 | -0.006 | -0.002 | 0.000 |
| échantillon7 | 0.004 | 0.205 | -0.002 | 0.002 | 0.013 | -0.002 | 0.329 |
| échantillon8 | 0.039 | 0.768 | 0.068 | 0.004 | -0.001 | -0.002 | 0.400 |
Tableau 3 : Analyse du test ECL 7-plex : résultats des valeurs de l’indice. Les valeurs d’index pour chaque échantillon pour les 7 tests d’autoanticorps ont été calculées par rapport à leurs témoins internes positifs et négatifs correspondants, comme décrit dans le protocole de dosage. Toute valeur d’index supérieure à la valeur seuil était définie comme un résultat positif, indiqué en gras foncé. La valeur de l’indice TGA de sample6 a été surlignée en gris car il s’agit d’une erreur causée par de mauvais doublons indiqués dans la ligne F-linker 3-colonnes 5 et 6 du tableau 1.
| GADA | IA-2A | IAA | .TGA | TPOA | ThGA | IFNαA* | ||||||||
| Sens | Spec | Sens | Spec | Sens | Spec | Sens | Spec | Sens | Spec | Sens | Spec | Sens | Spec | |
| La RBA | 73.4% | 98.5% | 75.2% | 99.0% | 47.7% | 99.1% | 12.9% | 99.0% | 23.9% | 95.2% | 19.3% | 94.7% | 1.0% | 99.6% |
| LMTEC unique | 71.6% | 99.1% | 73.6% | 99.3% | 48.3% | 99.7% | 16.0% | 98.9% | 26.3% | 94.9% | 20.6% | 95.1% | 0.8% | 99.2% |
| ECL 7-Plex | 71.2% | 98.9% | 77.3% | 98.9% | 49.5% | 98.9% | 16.5% | 98.7% | 26.1% | 94.7% | 21.1% | 94.7% | 1.7% | 99.1% |
Tableau 4 : Sensibilité et spécificité du test chez 1026 patients atteints de DT1 et 1022 témoins, appariés pour l’âge et le sexe, dans un test ECL 7-plex, par rapport au test ECL unique correspondant et RBA ou ELISA*. Troistests différents (RBA, ECL unique et ECL 7-Plex) pour chaque autoanticorps ont été définis à des spécificités similaires en utilisant les témoins sains appariés selon l’âge et le sexe 1022. Le critère de spécificité de la cohorte témoin étudiée a été fixé à environ 95% pour TPOA et ThGA et à 99% pour les 5 autres tests. *L’astérisque marque le test IFNαA pour ELISA, tandis que d’autres sont RBA.
Discussion
Dans de nombreux essais cliniques nationaux et internationaux sur le diabète de type 1, l’efficacité du test ECL unique pour détecter les autoanticorps des îlots pancréatiques et les autoanticorps dirigés contre la transglutaminase (TGA) pour la maladie cœliaque a été confirmée 8,9,10,11. Tout au long de ces essais, ce test a augmenté la sensibilité et la spécificité pour la détection des autoantigènes lorsqu’il est évalué par rapport à la RBA de référence existante. La spécificité accrue de la maladie peut être observée lors de la distinction entre le test ECL unique et le test RBA14,15,16,17. En nous appuyant sur le test ECL unique, nous posons un nouveau test d’autoanticorps ECL multiplexé à haut débit, pour nous permettre de dépister le DT1 ainsi que plusieurs maladies auto-immunes applicables en même temps.
Le test ECL multiplex utilise la plaque multiplex, qui peut combiner jusqu’à 10 tests d’autoanticorps dans un seul puits. Pour la présente étude, 7 tests d’autoanticorps sont combinés. Les autoanticorps comprennent 3 IAbs (IAA, GADA et IA-2A), 2 autoanticorps auto-immuns contre la maladie thyroïdienne (TPOA et ThGA), des autoanticorps contre la maladie cœliaque (TGA) et des autoanticorps APS-1 contre l’interféron alpha (IFNαA). Le mécanisme de dosage est, en général, basé sur un seul test ECL tel que publié précédemment 9,10,12,18 avec quelques modifications. La principale différence entre un test ECL multiplex et un seul test ECL est que chaque complexe anticorps-antigène formé dans la phase fluide est limité à un agent de liaison spécifique (Figure 1). L’antigène marqué à la biotine est incubé avec la streptavidine conjuguée, un agent de liaison utilisé pour former un complexe antigène-liant spécifique. Le complexe immunitaire anticorps-antigène se forme après incubation avec le sérum du patient et est capturé sur un point spécifique par le système de liaison spécifique sur chaque puits de la plaque multiplex. L’antigène marqué Ru Sulfo-NHS capturé par les anticorps fournit en même temps le signal avec électrochimiluminescence. La machine de lecture de plaques peut détecter jusqu’à 10 signaux différents provenant des sources ponctuelles situées dans chaque puits. Pour maintenir la cohérence des tests d’autoanticorps entre les plaques et lors de la réalisation d’études à long terme, nous suggérons d’utiliser le même agent de liaison.
Avant de mettre en place un test ECL multiplex, les tests ECL uniques pour chaque autoanticorps doivent être optimisés sur une plaque multiplex, respectivement, et validés par rapport aux tests RBA et ECL uniques sur une plaque ECL régulière. Pour améliorer le test en damier, pour le test d’autoanticorps associé sur la plaque multiplex, un patient très positif et un échantillon de patient négatif ont été utilisés. Après le test en damier, les concentrations les plus idéales pour le Ru Sulfo-NHS et l’antigène marqué à la biotine ont été calculées pour chacun des 7 tests d’auto-anticorps. Voici ces concentrations : 30 ng/mL et 200 ng/mL pour GAD65, 120 ng/mL et 120 ng/mL pour la proinsuline, 10 ng/mL et 42 ng/mL pour l’IA-2, 80 ng/mL et 80 ng/mL pour la TG, 8 ng/mL et 16 ng/mL pour la TPO, 31 ng/mL et 31 ng/mL pour le ThG, et 12 ng/mL et 12 ng/mL respectivement pour l’IFNα13. Les concentrations de certains des antigènes du test en damier peuvent devoir être ajustées davantage en fonction des résultats de l’essai multiplex réel après avoir combiné tous les tests ensemble.
Comme l’AIA est inclus dans le présent test ECL multiplexe, le traitement acide des échantillons de sérum est obligatoire avant l’incubation du sérum avec l’antigène, comme indiqué dans l’étude précédente12. En règle générale, lorsqu’un autoanticorps supplémentaire est ajouté à un test multiplex, le fond du test est affecté et un signal extrêmement élevé provenant d’un endroit, dans le puits, peut obstruer les résultats des points voisins via la diaphonie. Par conséquent, le CPS maximal doit être limité à 20 000 comptes pour chaque autoanticorps, ou moins, pour les échantillons positifs les plus élevés. D’après nos connaissances, afin de réduire la quantité de diaphonie impliquée, les autoanticorps qui ont un arrière-plan inférieur doivent être séparés, lors de la conception de la carte ponctuelle, loin des points avec une fréquence plus élevée de comptage.
Des témoins positifs et négatifs élevés ont été utilisés à l’interne dans chaque essai pour calculer un indice précis pour les échantillons inconnus testés. Pour évaluer et surveiller avec précision la sensibilité du test, des témoins faiblement positifs, placés près de la limite supérieure du test, ont été utilisés. Ces témoins positifs et négatifs standard ont été créés en vrac et en partie aliquote pour une utilisation à long terme et stockés à -20 °C ou moins, pour assurer la cohérence entre les essais. À des fins d’assurance de la qualité, les échantillons ont été analysés deux fois dans chaque essai et chaque résultat positif a été répété et confirmé en exécutant l’échantillon dans un nouveau test ECL le lendemain. En cas de désaccord avec le premier et le deuxième test de confirmation, un troisième test était nécessaire. Sur les trois essais effectués, les résultats des deux essais qui concordent (p. ex., +, + ou -,-) ont déterminé le résultat final (positif ou négatif) de l’échantillon.
Au cours de la dernière décennie, de nombreux groupes d’étude ont cherché un test à haut débit utilisant la méthode multiplex pour combiner plusieurs tests d’autoanticorps en un seul puits pour dépister de grandes populations. Il existe quelques études qui utilisent différents types de technologies pour effectuer des tests d’autoanticorps multiplex 19,20,21,22, mais il n’y a aucune comparaison pour aucun de ces tests de sensibilité et de spécificité avec l’étalon-or RBA actuel, lors de l’étude du DT1. Ces différents types de plateformes utilisées ne sont pas validés par l’atelier international du Programme de normalisation des autoanticorps des îlots pancréatiques (IASP) ou par l’essai de grandes cohortes dans le cadre d’essais cliniques. Dans un récent dépistage basé sur la population générale en Allemagne, un test combiné à haut débit, 3 Screen ICATM ELISA distribué par Kronus, est utilisé comme outil de dépistage de première intention pour détecter trois IAbs, GADA, IA-2A et ZnT8A, afin d’obtenir un diagnostic précoce du DT123 chez l’enfant. Le test ELISA à 3 écrans mesure 3 auto-anticorps soit dans 3 puits séparés, consommant un grand volume de sérum, soit dans un seul puits avec les 3 tests mélangés. Si un puits dans le test ELISA à 3 écrans est positif, on est incapable de distinguer lequel des trois autoanticorps est présent. Le plus grand inconvénient de ce test est son incapacité à inclure la mesure de l’IAA. Tous les résultats de l’AIA réalisés par ELISA, comme l’ont prouvé les ateliers de l’IASP, n’ont pas une sensibilité et une spécificité acceptables24. L’IAA est généralement le premier IAb à apparaître et a une prévalence élevée chez les jeunes enfants. Le dépistage IAb, avec IAA, est nécessaire pour les enfants et il n’est pas jugé acceptable d’effectuer ce dépistage sans IAA pour évaluer le risque de DT1 dans la communauté. En outre, il n’y a pas d’études ou de données publiées qui montrent que le test Kronus IAb kit est plus spécifique à la maladie T1 et capable de distinguer le risque élevé de l’IAbs à faible risque. Le test ECL 7-Plex, dans la présente étude, a été validé à l’aide d’une grande cohorte de patients nouvellement diagnostiqués avec leDT11 13. Comparé à la RBA standard actuelle et au test ECL unique bien établi, le test 7-Plex est capable de conserver une positivité de 100% avec la même spécificité de test (tableau 4). Actuellement, le test ECL 4-Plex, parallèle à la RBA standard, est appliqué à un vaste essai clinique en cours: Autoimmunity Screening for Kids (ASK). Cet essai examine le DT1 et la maladie cœliaque chez les enfants de la population générale de la région métropolitaine de Denver. Par rapport à la RBA standard utilisée dans l’étude ASK, le test ECL multiplex montre une excellente sensibilité et une spécificité de la maladie plus élevée, identique à nos rapports précédents utilisant l’étude ECL unique25. De plus, notre test ECL 4-Plex a démontré une réduction prononcée de la main-d’œuvre, du coût et du volume sérique de 70%, par rapport aux 4 tests uniques correspondants pour ECL et RBA. En utilisant le test ECL multiplexé, nous pouvons personnaliser chaque puits avec différents nombres, représentant différents autoanticorps (jusqu’à 10), pour tester différentes maladies auto-immunes spécifiques aux besoins d’un emplacement clinique particulier.
Certaines limites ont été observées, démontrées dans la présente étude, pour un essai ECL multiplexé utilisant la plaque multiplex. La dilution finale du sérum, incubé avec de l’antigène, ne peut pas être ajustée pour obtenir les conditions les plus optimales pour chaque essai d’autoanticorps combiné dans un seul puits. Neuf échantillons (9/1026), provenant de patients atteints de DT1, ont été observés pour avoir un résultat faussement négatif pour des autoanticorps particuliers. 7 des faux négatifs concernaient la TPOA et 2 la ThGA, dans le test ECL 7-Plex, mais des résultats positifs élevés ont été observés à la fois dans le test ECL unique et dans la RBA (figures 2 et 3). Après une nouvelle dilution des 9 échantillons, ils sont devenus positifs sur la plaque multiplex. Ce résultat est causé par ce que nous décrivons comme le phénomène de « prozone ». Ce phénomène fait que l’échantillon affiche un résultat faussement négatif parce que les titres élevés d’anticorps affectent la formation de réseaux antigène-anticorps. Lors de la mise en place d’un test multiplex, il est recommandé d’effectuer des pré-tests pour déterminer la dilution facultative du sérum pour l’incubation de l’antigène. Alternativement, des tests d’autoanticorps avec des conditions optimisées similaires doivent être sélectionnés pour former un test combiné à partir duquel la meilleure sensibilité et spécificité du test est obtenue pour chaque autoanticorps. Dans la présente étude, 7 échantillons (7/1022), provenant de témoins normaux sains, ont donné de faux positifs pour plusieurs autoanticorps dans le test 7-Plex, mais après avoir effectué un seul test ECL et RBA (Figure 2 & 3), ces autoanticorps se sont révélés négatifs dans les deux essais. Les raisons de ces résultats faussement positifs sur la plaque multiplex, pour ce petit sous-ensemble d’échantillons, sont actuellement inconnues. Pour l’application actuelle du test ECL multiplexe, tous les échantillons positifs sont répétés avec leur test ECL unique correspondant pour confirmer la positivité, ce qui élimine cette erreur faussement positive du test ECL multiplexe.
Déclarations de divulgation
Les auteurs n’ont rien à divulguer.
Remerciements
Ce travail a été soutenu par la subvention DK32083 des NIH, les subventions 2-SRA-2015-51-Q-R et 2-SRA-2018-533-S-B de FRDJ.
matériels
| Name | Company | Catalog Number | Comments |
| 4 °C refrigerator | |||
| –80 °C and -20 °C freezers | |||
| 96-well Plate Shaker | Wallac - Delfi | ||
| 96-well round bottom plate | Fisher | 8408220 | |
| Acetic acid solution | Fisher | ||
| Aluminum foil | |||
| Antigen proteins | |||
| Human GAD65 full length protein | Diamyd | ||
| Human ThG full length protein | BioMart | ||
| Human TPO full length protein | BioMart | ||
| IA-2 intracellular domain protein | BioMart | ||
| IFN-α protein | Abcam | ||
| Proinsulin protein | AmideBio | ||
| tTG protein | DiaRect | ||
| Biotin | Sigma | ||
| Bottle-Top 500 mL , Filter Units | Fisher | 0974064A or B | |
| Bovine Serum Albumin | Sigma | A-7906 | |
| Distilled deionized (DD) water | |||
| HCl | Fisher | ||
| Ice maker | |||
| Ice trays | |||
| MSD Sector | Perkin-Elmer | ||
| Multi-channel pipette | |||
| NaOH | |||
| Paper tower | |||
| PBS | |||
| pH meter | |||
| Pipette-Aid | |||
| Pipettes/tips | |||
| Ru Sulfo-NHS | MSD (R91AN) | ||
| Trizma Base | Fisher | BP152-5 | |
| Tween 20 | Sigma | P-1379 | |
| Uplex Development Kit | MSD | ||
| 96-well UPlex plate | MSD | ||
| Blocker A | MSD | R93AA | |
| Linker-Streptavidin | MSD | ||
| Read buffer | MSD | R92TC | |
| Stop Solution | MSD | ||
| Vortex mixer | |||
| ZeBa Column | Pierce | 89892 |
Références
- Harjutsalo, V., Sjoberg, L., Tuomilehto, J. Time trends in the incidence of type 1 diabetes in Finnish children: a cohort study. Lancet. 371 (9626), 1777-1782 (2008).
- Vehik, K., et al. Increasing incidence of type 1 diabetes in 0- to 17-year-old Colorado youth. Diabetes Care. 30 (3), 503-509 (2007).
- Atkinson, M. A., Eisenbarth, G. S., Michels, A. W. Type 1 diabetes. Lancet. 383 (9911), 69-82 (2014).
- Insel, R. A., et al. Staging presymptomatic type 1 diabetes: a scientific statement of JDRF, the Endocrine Society, and the American Diabetes Association. Diabetes Care. 38 (10), 1964-1974 (2015).
- Barker, J. M., et al. Autoantibody "subspecificity" in type 1 diabetes: risk for organ-specific autoimmunity clusters in distinct groups. Diabetes Care. 28 (4), 850-855 (2005).
- Triolo, T. M., et al. Additional Autoimmune Disease Found in 33% of Patients at Type 1 Diabetes Onset. Diabetes Care. 34 (5), 1211-1213 (2011).
- de Graaff, L. C., Smit, J. W., Radder, J. K. Prevalence and clinical significance of organ-specific autoantibodies in type 1 diabetes mellitus. Netherlands Journal of Medicine. 65 (7), 235-247 (2007).
- Yu, L., et al. Proinsulin/Insulin autoantibodies measured with electrochemiluminescent assay are the earliest indicator of prediabetic islet autoimmunity. Diabetes Care. 36 (8), 2266-2270 (2013).
- Yu, L., et al. Distinguishing persistent insulin autoantibodies with differential risk: nonradioactive bivalent proinsulin/insulin autoantibody assay. Diabetes. 61 (1), 179-186 (2012).
- Miao, D., et al. GAD65 autoantibodies detected by electrochemiluminescence assay identify high risk for type 1 diabetes. Diabetes. 62 (12), 4174-4178 (2013).
- Gu, Y., Zhao, Z., High, H., Yang, T., Yu, L. Islet Autoantibody Detection by Electrochemiluminescence (ECL) Assay. Journal of Clinical & Cellular Immunology. 8 (6), (2017).
- Gu, Y., et al. Electrochemiluminescence Assays for Human Islet Autoantibodies. Journal of Visualized Experiments. (133), e57227 (2018).
- Gu, Y., et al. High-throughput multiplexed autoantibody detection to screen type 1 diabetes and multiple autoimmune diseases simultaneously. Ebiomedicine. 47, 365-372 (2019).
- Dongmei, M., A, K. S., Li Zh, K., Michelle, G., Ling, J., Taylor, A. Electrochemiluminescence Assays for Insulin and Glutamic Acid Decarboxylase Autoantibodies Improve Prediction of Type 1 Diabetes Risk. Diabetes Technology & Therapeutics. 17 (2), 119-127 (2015).
- Steck, A. K., et al. ECL-IAA and ECL-GADA Can Identify High-Risk Single Autoantibody-Positive Relatives in the TrialNet Pathway to Prevention Study. Diabetes Technology & Therapeutics. 18 (7), 410-414 (2016).
- Fouts, A., et al. Do Electrochemiluminescence Assays Improve Prediction of Time to Type 1 Diabetes in Autoantibody-Positive TrialNet Subjects. Diabetes Care. 39 (10), 1738-1744 (2016).
- Sosenko, J. M., et al. The Use of Electrochemiluminescence Assays to Predict Autoantibody and Glycemic Progression Toward Type 1 Diabetes in Individuals with Single Autoantibodies. Diabetes Technology & Therapeutics. 19 (3), 183-187 (2017).
- Zhao, Z., et al. Higher Sensitivity and Earlier Identification of Celiac Disease Autoimmunity by a Nonradioactive Assay for Transglutaminase Autoantibodies. Journal of Immunology Research. 2016, 5 (2016).
- Zhang, B., Kumar, R. B., Dai, H., Feldman, B. J. A plasmonic chip for biomarker discovery and diagnosis of type 1 diabetes. Nature Medicine. 20 (8), 948-953 (2014).
- Tsai, C. T., Robinson, P. V., Spencer, C. A., Bertozzi, C. R. Ultrasensitive Antibody Detection by Agglutination-PCR (ADAP). American Chemical Society Central Science. 2 (3), 139-147 (2016).
- Yim, S. W., et al. Four-color alternating-laser excitation single-molecule fluorescence spectroscopy for next-generation biodetection assays. Clinical chemistry. 58 (4), 707-716 (2012).
- Bale, S. S., et al. A highly sensitive microsphere-based assay for early detection of Type I diabetes. Technology. 02 (03), 200-205 (2014).
- Ziegler, A. G., et al. 3 Screen ELISA for High-Throughput Detection of Beta Cell Autoantibodies in Capillary Blood. Diabetes Technology & Therapeutics. 18 (11), 687-693 (2016).
- Schlosser, M., et al. Diabetes Antibody Standardization Program: evaluation of assays for insulin autoantibodies. Diabetologia. 53 (12), 2611-2620 (2010).
- Zhao, Z., et al. A multiplex assay combining insulin, GAD, IA-2 and transglutaminase autoantibodies to facilitate screening for pre-type 1 diabetes and celiac disease. Journal of Immunological Methods. 430, 28-32 (2016).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon