Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Analyse de l’interaction fluide-structure biomécanique basée sur la tomographie par cohérence optique de la progression de l’athérosclérose coronaire
Dans cet article
Résumé
Il est nécessaire de déterminer quelles lésions athérosclérotiques progresseront dans le système vasculaire coronaire pour guider l’intervention avant l’infarctus du myocarde. Cet article décrit la modélisation biomécanique des artères à partir de la tomographie par cohérence optique en utilisant des techniques d’interaction fluide-structure dans un solveur commercial d’éléments finis pour aider à prédire cette progression.
Résumé
Dans cet article, nous présentons un flux de travail complet pour l’analyse biomécanique de la plaque d’athérosclérose dans le système vasculaire coronaire. L’athérosclérose étant l’une des principales causes de décès, de morbidité et de fardeau économique dans le monde, de nouvelles façons d’analyser et de prédire sa progression sont nécessaires. L’une de ces méthodes de calcul est l’utilisation de l’interaction fluide-structure (FSI) pour analyser l’interaction entre le flux sanguin et les domaines de l’artère / plaque. Couplée à l’imagerie in vivo, cette approche pourrait être adaptée à chaque patient, aidant à différencier les plaques stables des plaques instables. Nous décrivons le processus de reconstruction tridimensionnelle, en utilisant la tomographie par cohérence optique intravasculaire (OCT) et l’angiographie coronarienne invasive (ICA). L’extraction des conditions aux limites pour la simulation, y compris la réplication du mouvement tridimensionnel de l’artère, est discutée avant que la configuration et l’analyse ne soient effectuées dans un solveur commercial par éléments finis. La procédure de description des propriétés hyperélastiques hautement non linéaires de la paroi artérielle et de la vitesse/pression sanguine pulsatile est décrite avec la mise en place du couplage système entre les deux domaines. Nous démontrons la procédure en analysant une plaque non coupable, légèrement sténotique et riche en lipides chez un patient après un infarctus du myocarde. Les marqueurs établis et émergents liés à la progression de la plaque d’athérosclérose, tels que la contrainte de cisaillement de la paroi et l’hélicité normalisée locale, respectivement, sont discutés et liés à la réponse structurelle dans la paroi artérielle et la plaque. Enfin, nous traduisons les résultats en pertinence clinique potentielle, discutons des limites et décrivons les domaines à développer. La méthode décrite dans cet article est prometteuse pour aider à déterminer les sites à risque de progression de l’athérosclérose et, par conséquent, pourrait aider à gérer la mortalité, la morbidité et le fardeau économique importants de l’athérosclérose.
Introduction
La maladie coronarienne (CORONA) est le type de maladie cardiaque le plus courant et l’une des principales causes de décès et de fardeau économique dans le monde1,2. Aux États-Unis, environ un décès sur huit est attribué àCAD 3,4, tandis que la plupart des décès mondiaux dus à la CAD sont maintenant observés dans les pays à revenu faible et intermédiaire5. L’athérosclérose est le principal moteur de ces décès, avec rupture ou érosion de la plaque conduisant à l’occlusion de l’artère coronaire et à l’infarctus aigu du myocarde (IAM)6. Même après la revascularisation des lésions coronariennes coupables, les patients présentent un risque important d’événements cardiovasculaires indésirables majeurs (MACE) récurrents après AMI, en grande partie en raison de la présence concomitante d’autres plaques non coupables qui sont également vulnérables à la rupture7. L’imagerie intracoronaire permet de détecter ces plaques à haut risque8. Bien que l’échographie intravasculaire (IVUS) soit la référence en matière d’évaluation du volume de plaque, elle a une résolution limitée pour identifier les caractéristiques microstructurales de la plaque vulnérable, contrairement à la haute résolution (10-20 μm) de la tomographie par cohérence optique (OCT). Il a été démontré qu’un capuchon fibreux mince et enflammé recouvrant un grand pool lipidique est la signature la plus importante d’une plaquevulnérable 9 et qu’il est préférable d’identifier et de mesurer par OCT parmi les modalités d’imagerie intracoronaires actuellement disponibles10. Il est important de noter que l’OCT est également en mesure d’évaluer d’autres caractéristiques de la plaque à haut risque, notamment: arc lipidique; infiltration de macrophages; présence d’un fibroathérome à capuchon mince (TCFA), qui est défini comme un noyau riche en lipides avec un capuchon fibreux mince sus-jacent (<65 μm); calcification inégale; et les microcanaux de plaque. La détection OCT de ces caractéristiques à haut risque dans les plaques non coupables post-AMI a été associée à un risque jusqu’à 6 fois plus élevé de MACE11future. Cependant, malgré cela, la capacité de l’angiographie et de l’imagerie OCT à prédire quelles plaques coronaires progresseront et finiront par se rompre ou s’éroder est limitée, avec des valeurs prédictives positives de seulement 20% à 30%8. Cette capacité prédictive limitée entrave la prise de décision clinique autour des plaques non coupables à traiter (par exemple, par endoprothèse)7,12.
En plus des facteurs du patient et des caractéristiques biologiques de la plaque, les forces biomécaniques dans les artères coronaires sont également des déterminants importants de la progression et de l’instabilité de la plaque13. Une technique prometteuse pour aider à évaluer de manière exhaustive ces forces est la simulation d’interaction fluide-structure (FSI)14. La contrainte de cisaillement de la paroi (WSS), également appelée contrainte de cisaillement endothélial, a été un point focal traditionnel pour la recherche en biomécanique coronaire15, avec une compréhension générale que WSS joue un rôle étiologique dans la formation de l’athérosclérose16. Principalement simulées à l’aide de techniques de dynamique des fluides computationnelle (CFD), les régions à faible WSS ont été associées à un épaississement intimal17,à un remodelage vasculaire18 et à la prédiction de la progression des lésions19 et à la future MACE20. Les progrès récents de ces analyses suggèrent que la topologie sous-jacente du champ vectoriel WSS21et ses caractéristiques multidirectionnelles22constituent un meilleur prédicteur du risque d’athérosclérose que la magnitude WSS seule. Cependant, WSS ne capture qu’un aperçu du système biomécanique global au niveau de la paroi lumineuse, et tout comme les modalités d’imagerie, aucune métrique biomécanique ne peut discerner de manière fiable les caractéristiques athérosclérotiques à haut risque.
D’autres mesures apparaissent comme potentiellement importantes dans la formation de l’athérosclérose. Les caractéristiques d’écoulement intraluminal23 en sont un exemple, avec un écoulement hélicoïdal, quantifié à travers divers indices24, suggérés comme jouant un rôle athéroprotecteur en supprimant les schémas d’écoulement perturbés25,26. Bien que les techniques CFD puissent analyser ces caractéristiques d’écoulement et présenter un large éventail de résultats utiles, elles ne tiennent pas compte des interactions sous-jacentes entre le flux sanguin, la structure artérielle et le mouvement cardiaque général. Cette simplification du système dynamique à une paroi rigide passe à côté de résultats potentiellement critiques tels que la contrainte de la coiffe fibreuse. Alors que le débat à la fois pour et contre la nécessité de FSI sur CFD se poursuit27,28,29, de nombreuses comparaisons négligent d’inclure l’impact de la fonction ventricule. Cette limitation peut être surmontée avec FSI, qui a montré que la flexion dynamique et la compression exercées sur l’artère par l’influence de la fonction ventricule peuvent avoir un impact significatif sur la contrainte structurelle de la plaque et de l’artère ainsi que sur les mesures d’écoulement telles que WSS30,31,32. Ceci est important car les contraintes structurelles sont également une mesure clé pour analyser et prédire la rupture de la plaque33,34 et ont été suggérés pour co-localiser avec les régions d’augmentation de la plaque14,35. La capture de ces interactions permet une représentation plus réaliste de l’environnement coronaire et des mécanismes potentiels de progression de la maladie.
Pour ce faire, nous décrivons ici le processus de développement d’une géométrie spécifique au patient à partir de l’imagerie OCT36 et la mise en place et l’exécution d’une simulation FSI d’artère à l’aide d’un solveur commercial par éléments finis. Le processus d’extraction manuelle de la lumière, des lipides et de la paroi artérielle externe est détaillé avant la reconstruction informatique tridimensionnelle de l’artère du patient. Nous décrivons la configuration de la simulation, le couplage et le processus de comparaison des paramètres d’imagerie de base et de suivi de l’OCT pour déterminer la progression de la lésion. Enfin, nous discutons du post-traitement des résultats numériques et de la pertinence clinique de ces données en comparant les résultats biomécaniques avec la progression/régression des lésions. La méthode globale est démontrée sur des plaques non coupables, légèrement sténotiques et riches en lipides dans l’artère coronaire droite (RCA) d’un patient de sexe masculin caucasien de 58 ans qui a présenté un infarctus aigu du myocarde avec élévation non ST dans le cadre de l’hypertension, du diabète sucré de type 2, de l’obésité (IMC 32,6) et des antécédents familiaux de coronaropathie prématurée. puis 12 mois plus tard dans le cadre d’un essai clinique en cours (essai COCOMO-ACS ACTRN12618000809235). Nous prévoyons que cette technique pourra être affinée et utilisée pour identifier les plaques coronaires à haut risque de progression.
Protocole
Les données désidentifiées suivantes ont été analysées auprès d’un patient recruté dans le cadre de l’essai contrôlé randomisé COCOMO-ACS en cours (ACTRN12618000809235; Numéro de référence HREC du Royal Adelaide Hospital : HREC/17/RAH/366), avec une approbation éthique supplémentaire accordée par les services de recherche du Central Adelaide Local Health Network (CALHN) à des fins de simulation biomécanique (numéro de référence CALHN 14179). La figure 1 résume le flux de travail complet décrit dans le protocole suivant, qui peut être appliqué à n’importe quel logiciel ou code compatible FSI.
1. Évaluation de l’image
- Faire correspondre les images de suivi de référence et d’OCT à l’aide de repères anatomiques tels que les bifurcations et en utilisant des images immédiatement proximales à la bifurcation distale et distales à la bifurcation la plus proximale. Les images appariées entre ces repères doivent être analysées, comme décrit à la figure 2A.
- Section transversale de la lumière OCT
- Chargez chaque image OCT dans le numériseur d’image et cliquez pour marquer les points au centre du cathéter et les limites de l’échelle (Figure 2B). Exportez ces points pour les utiliser ultérieurement.
- Marquez manuellement le bord du lumen, en commençant au même endroit dans chaque image, en veillant à capturer les courbes du lumen aussi précisément que possible. Laissez un espace au niveau de l’artefact du cathéter car le processus de reconstruction interpolera dans cette région à un stade ultérieur. Exportez ces fichiers au format .dat et répétez cette opération pour chaque image.
- Paroi extérieure de l’OCT et lipides
- Dans le logiciel DICOM, extrayez la paroi extérieure dans les régions à forte atténuation en utilisant des parties visibles de la membrane élastique externe pour ajuster manuellement une ellipse afin d’estimer l’emplacement de la paroi extérieure, comme décrit à la figure 3. Cliquez et faites glisser le bouton gauche de la souris pour définir l’ellipse et la position appropriée.
- Définissez manuellement l’arc lipidique, calculé en fonction du centroïde de la lumière et de l’épaisseur du capuchon fibreux, comme décrit à la figure 3, en cliquant et en faisant glisser les mesures d’angle et de distance, respectivement. Ceux-ci seront utilisés pour analyser la progression de la lésion avec la zone de la lumière.
- Importez ces images superposées dans le numériseur d’images et sélectionnez manuellement les points de paroi extérieure, en utilisant l’ellipse ajustée comme guide dans les régions à forte atténuation où la membrane élastique externe n’est pas visible. Répétez l’étape 1.2.2 pour sélectionner et exporter les points dans un format .dat.
- De même pour les lipides, sélectionnez manuellement la surface lipidique, en commençant par la même extrémité du lipide dans tous les cas. Utilisez le guide ellipsoïdal de la paroi extérieure (étape 1.3.1) pour un arc arrière cohérent. Export pointe vers un fichier .dat et répétez pour toutes les images avec des lipides présents, laissant un espace sur l’artefact guidewire comme décrit à l’étape 1.2.2.
REMARQUE: La progression de la lésion est analysée en comparant trois mesures, à savoir la zone lumineuse, l’arc lipidique et l’épaisseur du capuchon fibreux, qui peuvent être évaluées directement à partir de la visionneuse DICOM. La technique d’extraction de la paroi extérieure et de l’arrière lipidique est nécessaire en raison de la profondeur de pénétration limitée de l’OCT. L’OCT a été utilisé dans cette étude en raison de l’accent mis sur la relation entre la composition de la plaque et les forces biomécaniques.
- Ligne médiane basée sur l’angiographie
- Chargez la première image angiographique dans le numériseurd’images 37. Sélectionnez les bords du cathéter pour mettre à l’échelle l’image dans les étapes ultérieures, puis marquez manuellement l’axe du cathéter en commençant par le marqueur proximal et en se déplaçant distalement, avec des points uniformément espacés, comme illustré à la figure 4A. Exportez les données au format .dat et répétez l’opération pour le deuxième plan angiographique.
REMARQUE: Généralement, les plans avec un angle supérieur à 20 ° entre eux améliorent la robustesse de la reconstruction de l’axe tridimensionnel. Le cathéter et le fil guide OCT doivent être visibles dans chaque image.
- Chargez la première image angiographique dans le numériseurd’images 37. Sélectionnez les bords du cathéter pour mettre à l’échelle l’image dans les étapes ultérieures, puis marquez manuellement l’axe du cathéter en commençant par le marqueur proximal et en se déplaçant distalement, avec des points uniformément espacés, comme illustré à la figure 4A. Exportez les données au format .dat et répétez l’opération pour le deuxième plan angiographique.
2. Reconstruction tridimensionnelle
- Projections angiographiques
- Chargez les fichiers de données qui ont été exportés à l’étape 1.4. Utilisez les deux premiers points pour mettre à l’échelle les données en millimètres (les deux premiers points sont utilisés avec les spécifications connues du cathéter, 6F dans ce cas). Soustrayez le point de données proximal des points restants de chaque jeu de données afin que la courbe commence à l’origine du repère.
- Générez des matrices de rotation pour chaque vue angiographique, où θ et Φ représentent respectivement les angles RAO/LAO et CAU/CRA. Nous utilisons les angles LAO et CRA comme négatifs. Les deux matrices de rotation dans les directions x (Rotx) et y (Roty), respectivement, sont :
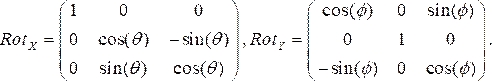 (1)
(1) - Multipliez les matrices de rotation ensemble, puis multipliez-les avec les coordonnées de chaque point de l’étape 2.1.1. L’équation résultante :
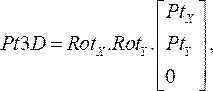 (2)
(2)
donne l’emplacement tridimensionnel du point du cathéter sur son plan d’angiographie respectif(Pt3D)en faisant pivoter les points bidimensionnels spécifiés à partir de chaque image angiographique. - Calculer le vecteur normal à chaque plan angiographique en multipliant les matrices de rotation x et y par le vecteur unitaire dans la direction z. De l’emplacement proximal à l’emplacement distal, projetez chaque point normal sur son plan respectif et calculez le point médian de la distance la plus courte entre les projections. Il en résulte le point tridimensionnel sur le fil guide de l’OCT dans l’espace.
- À l’aide de la fonction « interparc », disponible à partir de l’échange de fichiers central MATLAB38,divisez le trait d’axe tridimensionnel en points également espacés. L’espacement entre les points doit être égal à l’espacement entre les images de l’OPO, qui est déterminé par la vitesse de retrait. Ce sont les endroits où les sections transversales des PTOM seront placées.
- Rotation de la section transversale de l’OPO
- À l’aide du fichier de données contenant le centre et l’échelle du cathéter, convertissez chaque coupe transversale de pixels en mm à l’aide des deuxième et troisième points du fichier de mise à l’échelle. Pour centrer la section transversale autour de l’emplacement du cathéter, soustrayez le premier point de la fiche de mise à l’échelle (le centre du cathéter) de tous les points de section. Calculer le vecteur normal à la section transversale (parallèle au cathéter dans l’artère) en soustrayant le point central tridimensionnel du point distal suivant le long de la courbe du cathéter.
- Faites pivoter la section transversale de l’OCT pour l’aligner perpendiculairement à l’axe médian du cathéter en multipliant les points de données mis à l’échelle par la matrice de rotation :
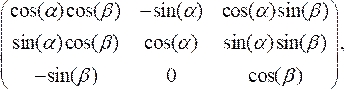 (3)
(3)
où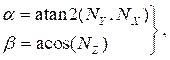 (4)
(4)
et NX, NYet NZ sont les composantes x, y et z, respectivement, du vecteur normal calculé à la section 2.1. Ajoutez le point d’axe tridimensionnel à tous les points pivotés de la section transversale, ce qui donne l’emplacement de la section transversale dans l’espace tridimensionnel (Figure 4B). - Répétez les étapes 2.2.1 à 2.2.2 pour chaque section transversale (lumière, artère et lipide). Exportez les coupes dans un fichier texte, qui peut être importé dans le logiciel de conception assistée par ordinateur (CAO) pour la création finale d’un corps solide.
- Création de modèles solides 3D
- Dans un logiciel de modélisation 3D, importez et générez les coupes un fichier à la fois. Importez les fichiers texte contenant les coupes transversales dans le logiciel de modélisation 3D en cliquant sur la liste déroulante du concept (Figure 5A-1) et en sélectionnant courbe 3D (Figure 5A-2). Cliquez sur Générer.
- Pour créer un composant solide, sélectionnez toutes les courbes dans l’ordre et rehaussez-les ensemble (Figure 5A-3), en veillant à ce que l’option ajouter figé soit sélectionnée pour générer un nouveau solide. Effectuez ces étapes pour la lumière, les lipides et la paroi externe afin de créer des solides séparés, en veillant à activer la topologie de fusion.
REMARQUE: Il peut être nécessaire d’ignorer une courbe si une géométrie problématique survient. Dans cette reconstruction, omettez un petit lipide de section médiane en raison de sa taille et du coût de calcul supplémentaire et de la complexité numérique associés à son inclusion. - Pour soustraire la lumière et les lipides de la paroi artérielle, créez une opération booléenne à partir de la liste déroulante créer et choisissez le corps cible comme mur et les lipides/lumen comme corps d’outil pour soustraire la lumière et les lipides de la paroi artérielle (Figure 5A-4).
- Partagez la topologie entre le mur et les lipides pour vous assurer que les nœuds de maillage sont partagés dans les étapes futures. Pour ce faire, mettez en surbrillance manuellement le mur et les lipides et faites un clic droit pour former une nouvelle pièce (Figure 5A-5).
REMARQUE: Cette étape garantit que les nœuds de maillage sont partagés entre les surfaces, ce qui empêche les régions de contact incorrectes ou la pénétration du maillage entre les deux couches, ce qui facilite grandement la phase de solution. La géométrie finale de l’axe médian du cathéter, des lipides, de la lumière et de la paroi artérielle est visualisée à la figure 5B.
- Prétraitement : conditions aux limites
REMARQUE: Avant de configurer la simulation, des conditions limites spécifiques au patient (BC) sont nécessaires. Ici, le déplacement extrait de l’angiographie a été utilisé, qui est appliqué à l’entrée et à la sortie de la simulation et de la vitesse / pression du flux sanguin mesurée chez des patients humains et décrite dans la littérature39.- Déplacement
- Répétez les étapes 1.4 et 2.1, mais en choisissant uniquement les marqueurs distaux et proximaux, en commençant par l’image angiographique précédant immédiatement la diastole terminale. Faites-le pour toutes les images angiographiques sur un cycle cardiaque.
- Ajuster les splines de lissage aux coordonnées x, yet z des deux ensembles de points. Il en résulte le déplacement des régions d’entrée et de sortie. Les résultats représentatifs des déplacements de patients sont présentés à la figure 6A.
REMARQUE: L’analyse du déplacement a été commencée à l’image précédant la diastole terminale afin de faire correspondre au mieux les phases entre le déplacement extrait et les profils de pression et de vitesse appliqués trouvés à la section 3.1.2, dont la phase systolique commence à 0,1 s (correspondant à l’espacement entre les images angiographiques). Lors de l’extraction d’un mouvement, assurez-vous qu’il n’y a pas de panoramique de table/mouvement d’image dans l’ensemble d’images.
- Vitesse/pression sanguine
- Créez des profils qui décrivent la vitesse et la pression sanguines pulsatiles en compilant les fonctions définies par l’utilisateur (UDF). Ici, les profils transitoires mesurés chez des patients humains dans la littérature ont été appliqués 39, modélisés comme une série de Fourier, décrite mathématiquement par:
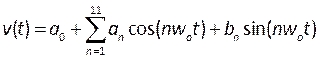 , (5)
, (5)
où t est le temps, w0 est la fréquence, T est la période du signal, n est le nombre de termes, et a0-11, b1-11 sont des coefficients adaptés aux profils décrits dans la littérature. Dans ce cas, nous utilisons les 11 premiers termes. - Remarque : Ces profils sont décrits à la figure 6B et doivent être écrits dans un fichier au format C dans un environnement de développement intégré tel que Microsoft Visual Studio. La pression de sortie est un profil plat et la vitesse d’entrée est appliquée comme un profil parabolique entièrement développé, décrit comme suffisant pour reproduire des conditions réalistes40. Le développement ultérieur de cette procédure pourrait inclure la mesure de la vitesse du sang du patient (par exemple par échocardiographie Doppler41)et de la pression (à l’aide de fils de pression) comme conditions limites plus réalistes. De plus, la mesure simultanée du déplacement, de la vitesse et de la pression du sang permettrait de s’assurer que leurs phases sont correctement adaptées.
- Créez des profils qui décrivent la vitesse et la pression sanguines pulsatiles en compilant les fonctions définies par l’utilisateur (UDF). Ici, les profils transitoires mesurés chez des patients humains dans la littérature ont été appliqués 39, modélisés comme une série de Fourier, décrite mathématiquement par:
- Déplacement
3. Artère/structure
- Pour définir les propriétés du matériau pour l’artère et le lipide, entrez des données d’ingénierie et ajoutez un nouveau matériau appelé artère. Faites glisser la densité et le modèle Mooney-Rivlin à 5 paramètres sur le nouveau matériau et définissez leurs paramètres. Entrez une densité de 1 000kg/m3 et les coefficients hyperélastiques décrits dans le tableau 1, basés sur les propriétés de l’intima42 et du lipide43 dans la littérature. Répétez ceci pour le lipide.
NOTE : Le modèle de Mooney-Rivlin est décrit par44: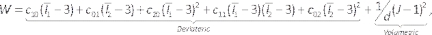 (6)
(6)
Où c10, c01, c20, c11et c02 sont des constantes de matériau et d est le paramètre d’incompressibilité (zéro pour le matériau incompressible dans ce cas). Ici, Ix est le xième invariant du tenseur de déformation et J est le déterminant du gradient de déformation élastique. - Entrez dans le composant du modèle, supprimez le composant lumen/fluide en cliquant avec le bouton droit sur le Lumen/Fluide et en sélectionnant Supprimer (Figure 7A). Affectez les matériaux définis précédemment aux solides artériels et lipidiques en les sélectionnant dans la liste déroulante des matériaux, en vérifiant si les unités sont appropriées.
- La géométrie doit maintenant être maillée. Cliquez sur le maillage(Figure 7B),définissez la préférence physique sur mécanique non linéaire et spécifiez le dimensionnement du maillage. Ici, un maillage adaptatif avec une taille cible de 0,14 mm a été utilisé. Ajustez les préférences de maillage au besoin pour obtenir des valeurs d’inclinaison de maillage raisonnables et visez au moins deux à trois éléments de maille à travers des espaces tels que le capuchon fibreux. La génération du maillage peut prendre un certain temps en raison de la géométrie complexe.
REMARQUE : Une étude sur l’indépendance des mailles doit être menée pour s’assurer que les résultats ne sont pas affectés par les caractéristiques des mailles. Diminuer progressivement le maillage et comparer les résultats jusqu’à ce que la variation soit inférieure à une limite définie; dans ce cas, nous utilisons 2%45 (mesuré au niveau de la calotte fibreuse de la troisième plaque). De plus, pour assurer la qualité du maillage, vérifier l’inclinaison du maillage; une asymétrie de maillage élevée entraînera des difficultés numériques lors de la convergence ou des résultats inexacts. Pour réduire l’asymétrie, essayez de diminuer la taille du maillage ou d’ajuster le taux de croissance, la taille maximale et / ou l’angle de courbure. Les résultats de notre test d’indépendance du maillage sont décrits dans le tableau 2, avec une variation en pourcentage des résultats par rapport au dimensionnement du maillage moyen, qui a été utilisé tout au long de cette analyse. - Cliquez sur Paramètres d’analyse (Figure 7C). Pour les simulations FSI, désactivez le pas de temps automatique et réglez le nombre de sous-étapes sur un (le couplage système contrôlera les sous-étapes), réglez l’heure de fin de la simulation, dans ce cas 0,8 s (fréquence cardiaque du patient de 75 bpm). Le couplage du système contrôlera le temps et les sous-étapes.
- Dans la liste déroulante Contrôles du solveur, définissez le type de solveur sur programme contrôlé pour utiliser la méthode directe ou itérative. Les méthodes directes sont plus robustes mais utilisent beaucoup plus de mémoire. Définissez la méthode Newton-Raphson sur complète. (En raison de la complexité de la géométrie et de la non-linéarité dans la simulation, la méthode directe et la méthode itérative complète de Newton-Raphson peuvent être nécessaires; cependant, elles augmentent considérablement le coût de calcul.)
- Spécifiez le domaine de couplage du système comme paroi interne de l’artère en insérant une interface fluide-solide. Pour ce faire, cliquez avec le bouton droit de la souris et insérez une interface fluide-solide sous l’onglet Transitoire (Figure 7D). Sélectionnez l’intérieur de la paroi de l’artère pour l’interface. Cela transmettra des données entre la structure et le fluide à cet endroit.
- Les conditions aux limites de déplacement peuvent être entrées en tant que fonction de déplacement dans les directions x, yet z appliquées à l’entrée et aux sorties. Pour ce faire, cliquez avec le bouton droit de la souris sous l’onglet Transitoire et insérez des déplacements (Figure 7E). Dupliquez le déplacement pour les directions x, yet z. Dans la liste déroulante des directions, sélectionnez fonction et copiez les déplacements extraits à l’étape 2.4.1.
REMARQUE: Le déplacement peut être entré sous forme de fonction ou de tableau de points en fonction des préférences. - Pour vous aider à résoudre les erreurs, sous l’onglet Solution, insérez quatre résidus de Newton-Raphson. Ceux-ci peuvent être visualisés si des erreurs surviennent pour trouver la géométrie gênante ou les emplacements de maillage.
REMARQUE : Pour insérer des options de post-traitement, telles que la contrainte principale maximale, cliquez avec le bouton droit de la souris sur l’onglet Solution et insérez les résultats appropriés (Figure 7F).
4. Sang/liquide
- Entrez dans l’onglet Modèle, vérifiez les unités et supprimez l’artère et la partie lipidique, en quittant le domaine fluide, de la même manière que l’étape 3.2.
- Spécifiez les métriques de maillage et générez le maillage, en vérifiant l’inclinaison et en l’ajustant si nécessaire (nous avons appliqué un maillage de 0,14 mm avec une taille de paroi maximale de 0,12 mm). Il est recommandé d’utiliser un maillage et une forme similaires, comme dans la partie structurelle, sur les zones où se produit l’interaction fluide-solide.
REMARQUE : Comme pour l’étape 3.3, un essai d’indépendance du maillage doit être effectué pour s’assurer que les résultats sont indépendants des propriétés du maillage, comme le montre le tableau 2. Vérifiez la qualité du maillage et ajustez la taille de l’élément, le taux de croissance, le raffinement ou la courbure au besoin pour vous assurer que l’asymétrie reste faible et que l’indépendance du maillage est atteinte. - Créez des sélections nommées pour l’entrée, la sortie et le mur avant d’entrer dans la configuration du fluide, en cliquant avec le bouton droit sur la surface respective et en sélectionnant insérer une sélection nommée.
- Entrez dans l’onglet Configuration et assurez-vous que la double précision est activée. Définissez le type de solveur sur Basé sur la pression et assurez-vous que l’heure est définie sur Transitoire en cochant les cases correspondantes (Figure 8A).
- Activez le modèle k-omega Viscous Turbulence et activez le transport des contraintes de cisaillement et les corrections de faible reynolds en entrant dans l’onglet Modèles visqueux(Figure 8B)et en cochant leurs cases respectives.
- Pour activer les modèles de viscosité non linéaires avec turbulence, entrez la commande '/define/models/viscous/turbulence-expert/turb-non-newtonian?' dans la console de commande (Figure 8C) et entrez 'yes' lorsque vous y êtes invité.
- Sous Matériaux (Figure 8D),définissez les propriétés du sang en entrant la densité et en sélectionnant la loi de puissance non newtonienne dans la liste déroulante de viscosité. Pour ce faire, renommez le fluide en sang, définissez une densité de 1 050 kg/m3et définissez l’indice de cohérence non newtonienne de la loi de puissance, k,à 0,035, l’indice de loi de puissance, n, à 0,6.
NOTE: Le modèle de viscosité non newtonienne power law a été choisi sur la base de la littérature pour décrire la viscosité sanguine non linéaire46, η, en termes de taux de déformation du fluide,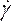 , comme:
, comme: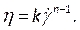 (7)
(7)
Divers modèles de viscosité du sang non newtoniens existent pour capturer la nature d’amincissement du sang. Plusieurs publications46,47,48,49 ont étudié l’efficacité de divers modèles de viscosité et leurs coefficients, qui devraient être consultés pour plus d’informations lors du choix du modèle approprié. - Compilez notre fonction définie par l’utilisateur, décrite précédemment à l’étape 2.4.2, contenant la vitesse et la pression sanguines transitoires, en vérifiant les lignes de commande pour détecter toute erreur (Figure 8C). Maintenant, chargez l’UDF en entrant dans l’onglet Défini par l’utilisateur (Figure 8E), en sélectionnant Compilé et en accédant au répertoire de l’UDF avant de l’importer et en cliquant sur Build, puis sur Load.
REMARQUE : Le texte apparaîtra dans la console (Figure 8C). Vérifiez cela attentivement pour vous assurer qu’aucune erreur ou avertissement n’apparaît. Si la FDU se charge correctement, les noms de la FDU s’affichent dans la console (mis en surbrillance à la Figure 8C). - Ceux-ci peuvent être appliqués à l’entrée et à la sortie. Pour ce faire, sélectionnez l’onglet Conditions aux limites. Double-cliquez sur Entrée (Figure 8F) et choisissez la FDU d’entrée dans la liste déroulante profil. Répétez cette étape pour définir également la pression de sortie.
- Activez le maillage dynamique (en cochant la case sous l’onglet Maillage dynamique illustré à la figure 8G), y compris les cases à cocher Lissage, Remeshing et 6° de liberté du solveur, en définissant le paramètre de diffusion sur 1,5 et les échelles maximales et minimales appropriées pour votre maillage.
- Assurez-vous que les échelles de maillage maximale et minimale se trouvent dans les limites de la zone de maillage et que l’asymétrie cible est définie sur 0,7. Les propriétés du maillage peuvent être affichées en cliquant sur l’onglet Propriétés du maillage.
- Créez une nouvelle zone de maillage dynamique en cliquant sur le bouton Créer, spécifiez la paroi du lumen dans la liste déroulante Région et sélectionnez Couplage système. Il s’agit de l’interface pour transmettre les données à la composante artérielle de la simulation.
- Créez des zones de maillage déformantes pour l’entrée, la sortie et la lumière intérieure avec des valeurs appropriées pour l’échelle de maillage. Pour ce faire, cliquez sur Créer dans l’onglet Maillage dynamique et choisissez Déformation. Activez le remaillage et le lissage et définissez les échelles de maillage en fonction des limites de chaque zone. Souvent, des erreurs de volume de cellule négatives sont associées à ce maillage dynamique, alors vérifiez soigneusement et ajustez les échelles de maillage si nécessaire pour chaque région.
- Assurez-vous que le couplage pression-vitesse est réglé sur couplé et définissez les schémas de formulation transitoire et de discrétisation spatiale sur le second ordre en entrant dans l’onglet Méthodes (Figure 8H)et en effectuant des sélections dans les listes déroulantes respectives.
- Dans les commandes (Figure 8H), entrez un nombre de courant de deux et définissez les critères de convergence résiduelle dans l’onglet Moniteurs (Figure 8I). Nous avons utilisé une valeur de 1e-5 pour la continuité et de 1e-6 pour le reste.
REMARQUE: Le nombre de Courant peut être estimé en fonction de la taille du maillage, dx, dela taille du pas de temps, de dtet de la vitesse du sang, v, en utilisant: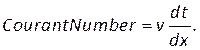 (8)
(8)
Entrez ce numéro sous la section Numéro de courant de l’onglet Contrôles (Figure 8H). Ici, nous appliquons un nombre de Courant de deux. Le nombre de Courant est généralement inférieur à un; cependant, comme on utilise un solveur pression-vitesse couplé avec des méthodes de solution implicites, le résultat est intrinsèquement plus stable et moins sensible à cette valeur; par conséquent, deux est considéré comme acceptable. - Pour définir une fonction personnalisée pour des résultats tels que l’hélicité normalisée locale (LNH), sélectionnez des fonctions de champ personnalisées sous l’onglet Paramètres et personnalisation (Figure 8J) et insérez une nouvelle fonction en cliquant avec le bouton droit de la souris et en sélectionnant Nouveau. Utilisez la fenêtre contextuelle pour définir si nécessaire. Entrez la formule à l’aide de la liste déroulante des variables du solveur. Comme résultat représentatif, nous utilisons LNH50,51, une mesure de l’alignement entre la vitesse, , et la
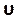 vorticité, ω, vecteurs, comme une fonction personnalisée décrite par:
vorticité, ω, vecteurs, comme une fonction personnalisée décrite par: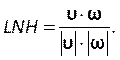 (9)
(9)
REMARQUE: D’autres variables personnalisées doivent être définies à cette étape, telles que l’indice de cisaillement oscillatoire (OSI)52,53, une mesure de l’inversion de flux. - Dans l’onglet Exécuter le calcul (Figure 8K), définissez le nombre de pas de temps sur 160 (une taille d’étape de 0,005 s et une heure de fin de 0,8 s), une taille de pas de temps de 5 ms et le nombre d’itérations sur 300 pour vous assurer que le résultat est indépendant du temps.
REMARQUE : Selon la complexité de la simulation, des itérations plus importantes par étape peuvent être nécessaires. Plusieurs cycles cardiaques peuvent être nécessaires pour une convergence numérique complète, ce que nous notons comme une limitation; cependant, cela est souvent appliqué dans les simulations de biomécanique coronaire en raison du coût de calcul associé à ces simulations. - Vérifiez si la case à cocher Échantillonnage des données pour les statistiques temporelles est activée et assurez-vous que les statistiques de mur et les contraintes de cisaillement d’écoulement sont sélectionnées, ainsi que la fonction personnalisée définie précédemment.
- Créez l’exportation des données dans l’onglet Activités de calcul et enregistrement automatique (Figure 8L),en sélectionnant l’option CFD-Post Compatible pour le post-traitement. Si l’on souhaite traiter les résultats dans un logiciel séparé, ajustez le type d’exportation si nécessaire. Sélectionnez toutes les régions (mur, maillage intérieur, entrée, sortie) et les résultats à exporter.
- Enfin, initialisez la simulation avec le schéma hybride en entrant dans l’onglet Initialisation (Figure 8M),en sélectionnant le schéma hybride, en cliquant sur Paramètreset en augmentant le nombre d’itérations à 20. Cliquez sur Initialiser.
5. Couplage du système
- Assurez-vous que les configurations structurelles et fluides sont connectées au couplage du système et mises à jour. Pour ce faire, cliquez et faites glisser la configuration structurelle et fluide vers le couplage système pour les lier, comme illustré à la figure 9A, en vous assurant que les deux configurations sont mises à jour en cliquant avec le bouton droit de la souris et en sélectionnant Mettre à jour.
- Dans Couplage système, définissez l’heure de fin sur 0,8 s et le pas de temps sur 0,005 s. Pour ce faire, sélectionnez Paramètres d’analyse (Figure 9B-1) et entrez l’heure de fin et la taille du pas de temps. Définissez le nombre maximal d’itérations sur 10.
REMARQUE: En général, entre 10 et 15 itérations suffisent si les composants structurels et fluides convergent bien. - Sélectionnez la paroi et l’interface solide parmi les composants fluide et structurel, respectivement, et ajoutez un transfert de données en maintenant la touche Ctrl enfoncée et en sélectionnant les deux interfaces fluide-structure (Figure 9B-2); faites un clic droit et créez un transfert de données entre le fluide et les composants structurels (Figure 9B-3). Ajustez la sous-relaxation ou la rampe de la force transférée du fluide à la structure pour aider à la convergence.
REMARQUE : Selon la complexité du modèle, les conditions aux limites et les propriétés du matériau, une rampe ou une sous-relaxation du transfert de données peut être nécessaire pour la convergence numérique. Ceux-ci peuvent être appliqués au transfert de données fluide (c’est-à-dire la force transférée du composant fluide à la paroi artérielle). Ces options sont disponibles dans les transferts de données créés (Figure 9B-2). - Lorsque vous êtes prêt à exécuter, cliquez sur Mettre à jour. Les données de simulation telles que la convergence structurelle et fluide et leur convergence de transfert de données respective sont imprimées dans la console.
REMARQUE: Notez que les simulations FSI sont coûteuses en calcul, cette simulation prenant 11 jours sur une machine à 16 cœurs (Intel Xeon Gold 2,6 GHz utilisant 180 Go de mémoire physique (RAM)), avec des variations supplémentaires dans les temps de simulation en fonction de la configuration matérielle et de la complexité du modèle. Les résidus représentatifs du transfert de données sont représentés dans le graphique (Figure 9B-4) et les données de solution sont imprimées dans la console (Figure 9B-5). Au cours des premières itérations, la convergence des résidus de transfert de données peut ne pas être complètement obtenue tant qu’un état d’équilibre n’est pas atteint. Ceci est décrit plus en détail dans la légende de la figure 9B. - Une fois la simulation terminée, les résultats peuvent être post-traités dans le logiciel commercial ou dans un logiciel séparé, en fonction du type d’exportation de données décrit à l’étape 4.19.
Résultats
Des résultats représentatifs sont présentés pour les marqueurs biomécaniques établis et émergents de la progression de l’athérosclérose. Les mesures établies telles que les résultats WSS et dérivés du WSS (y compris la contrainte de cisaillement de paroi moyennée dans le temps (TAWSS) et l’indice de cisaillement oscillatoire (OSI)) sont visualisées à la figure 10. La contrainte de cisaillement de la paroi au cours du cycle cardiaque est en grande partie entraînée par la...
Discussion
L’utilisation des méthodes FSI pour analyser la biomécanique coronaire est encore un domaine en développement à la fois de la modélisation numérique et des résultats cliniques. Nous avons décrit ici les grandes lignes de la mise en place d’une analyse FSI spécifique au patient, basée sur les méthodes par éléments finis / volume fini, en utilisant l’OCT et l’imagerie angiographique. Bien que la méthode que nous décrivons ici utilise un solveur d’éléments finis commercial, la procédure peut êtr...
Déclarations de divulgation
Les auteurs n’ont aucun conflit à déclarer concernant la préparation de cet article. S.J.N. a reçu le soutien à la recherche d’AstraZeneca, Amgen, Anthera, Eli Lilly, Esperion, Novartis, Cerenis, The Medicines Company, Resverlogix, InfraReDx, Roche, Sanofi-Regeneron et Liposcience et est consultant pour AstraZeneca, Akcea, Eli Lilly, Anthera, Kowa, Omthera, Merck, Takeda, Resverlogix, Sanofi-Regeneron, CSL Behring, Esperion et Boehringer Ingelheim. P.J.P. a reçu le soutien à la recherche d’Abbott Vascular, des honoraires de consultation d’Amgen et d’Esperion et des honoraires de conférencier d’AstraZeneca, Bayer, Boehringer Ingelheim, Merck Schering-Plough et Pfizer.
Remerciements
Les auteurs tiennent à remercier l’Université d’Adélaïde, le Royal Adelaide Hospital (RAH) et le South Australian Health and Medical Research Institute (SAHMRI). L’essai COCOMO-ACS est une étude initiée par un investigateur financée par des subventions de projet du National Health and Medical Research Council (NHMRC) d’Australie (ID1127159) et de la National Heart Foundation of Australia (ID101370). H.J.C. est soutenu par une bourse du Westpac Scholars Trust (Future Leaders Scholarship) et reconnaît le soutien de l’Université d’Adélaïde, de l’École de génie mécanique et de la bourse du Programme de formation en recherche sur les compétences et l’emploi (RTP) du Ministère de l’éducation. S.J.N. reçoit une bourse de recherche principale du NHMRC (ID1111630). P.J.P. reçoit une bourse future leader de niveau 2 de la National Heart Foundation of Australia (FLF102056) et une bourse de développement de carrière de niveau 2 du NHMRC (CDF1161506).
matériels
| Name | Company | Catalog Number | Comments |
| ANSYS Workbench (version 19.0) | ANSYS | Commercial finite element solver | |
| MATLAB (version 2019b) | Mathworks | Commercial programming platform | |
| MicroDicom/ImageJ | MicroDicom/ImageJ | Open Source DICOM reader | |
| Visual Studio (version 2019) | Microsoft | Commercial Integrated Development Environment |
Références
- American Heart Association. Cardiovascular disease: A costly burden for America projections through 2035. American Heart Association. , (2017).
- Gheorghe, A., et al. The economic burden of cardiovascular disease and hypertension in low-and middle-income countries: A systematic review. BMC Public Health. 18 (1), 975 (2018).
- Virani, S. S., et al. Heart disease and stroke statistics-2020 update: A report from the American Heart Association. Circulation. 141 (9), 139 (2020).
- Benjamin, E. J., et al. Heart disease and stroke statistics-2019 update: A report from the American Heart Association. Circulation. 139 (10), 56 (2019).
- Cardiovascular diseases (CVDs). World Health Organisation Available from: https://www.who.int/news-room/fact-sheets/detail/cardiovascular-diseases-(cvds) (2017)
- Calvert, J. W., Willis, M. S., Homeister, J. W., Stone, J. R. . Cellular and Molecular Pathobiology of Cardiovascular Disease. , 79-100 (2014).
- Baumann, A. A. W., Mishra, A., Worthley, M. I., Nelson, A. J., Psaltis, P. J. Management of multivessel coronary artery disease in patients with non-ST-elevation myocardial infarction: a complex path to precision medicine. Therapeutic Advances in Chronic Disease. 11, 1-23 (2020).
- Montarello, N. J., Nelson, A. J., Verjans, J., Nicholls, S. J., Psaltis, P. J. The role of intracoronary imaging in translational research. Cardiovascular Diagnosis and Therapy. 10 (5), 1480-1507 (2020).
- Narula, J., et al. Histopathologic characteristics of atherosclerotic coronary disease and implications of the findings for the invasive and noninvasive detection of vulnerable plaques. Journal of the American College of Cardiology. 61 (10), 1041-1051 (2013).
- Kim, S. -. J., et al. Reproducibility of in vivo measurements for fibrous cap thickness and lipid arc by OCT. JACC: Cardiovascular Imaging. 5 (10), 1072-1074 (2012).
- Prati, F., et al. Relationship between coronary plaque morphology of the left anterior descending artery and 12 months clinical outcome: the CLIMA study. European Heart Journal. 41 (3), 383-391 (2019).
- Nelson, A. J., Ardissino, M., Psaltis, P. Current approach to the diagnosis of atherosclerotic coronary artery disease: more questions than answers. Therapeutic Advances in Chronic Disease. 10, 1-20 (2019).
- Carpenter, H. J., Gholipour, A., Ghayesh, M. H., Zander, A. C., Psaltis, P. J. A review on the biomechanics of coronary arteries. International Journal of Engineering Science. 147, (2020).
- Wang, L., et al. Fluid-structure interaction models based on patient-specific IVUS at baseline and follow-up for prediction of coronary plaque progression by morphological and biomechanical factors: A preliminary study. Journal of Biomechanics. 68, 43-50 (2018).
- Shishikura, D., et al. The relationship between segmental wall shear stress and lipid core plaque derived from near-infrared spectroscopy. Atherosclerosis. 275, 68-73 (2018).
- Cameron, J. N., et al. Exploring the relationship between biomechanical stresses and coronary atherosclerosis. Atherosclerosis. 302, 43-51 (2020).
- Giannoglou, G. D., Soulis, J. V., Farmakis, T. M., Farmakis, D. M., Louridas, G. E. Haemodynamic factors and the important role of local low static pressure in coronary wall thickening. International Journal of Cardiology. 86 (1), 27-40 (2002).
- Stone, P. H., et al. Effect of endothelial shear stress on the progression of coronary artery disease, vascular remodeling, and in-stent restenosis in humans: In vivo 6-month follow-up study. Circulation. 108 (4), 438-444 (2003).
- Bourantas Christos, V., et al. Shear stress estimated by quantitative coronary angiography predicts plaques prone to progress and cause events. JACC: Cardiovascular Imaging. 13 (10), 2206-2219 (2020).
- Stone, P. H., et al. Role of low endothelial shear stress and plaque characteristics in the prediction of nonculprit major adverse cardiac events: The PROSPECT study. JACC: Cardiovascular Imaging. 11 (3), 462-471 (2018).
- Arzani, A., Gambaruto, A. M., Chen, G., Shadden, S. C. Wall shear stress exposure time: a Lagrangian measure of near-wall stagnation and concentration in cardiovascular flows. Biomechanics and Modeling in Mechanobiology. 16 (3), 787-803 (2017).
- Hoogendoorn, A., et al. Multidirectional wall shear stress promotes advanced coronary plaque development: comparing five shear stress metrics. Cardiovascular Research. 116 (6), 1136-1146 (2020).
- Chiastra, C., et al. Healthy and diseased coronary bifurcation geometries influence near-wall and intravascular flow: A computational exploration of the hemodynamic risk. Journal of Biomechanics. 58, 79-88 (2017).
- Gallo, D., Steinman, D. A., Bijari, P. B., Morbiducci, U. Helical flow in carotid bifurcation as surrogate marker of exposure to disturbed shear. Journal of Biomechanics. 45 (14), 2398-2404 (2012).
- De Nisco, G., et al. The atheroprotective nature of helical flow in coronary arteries. Annals of Biomedical Engineering. 47 (2), 425-438 (2019).
- De Nisco, G., et al. The impact of helical flow on coronary atherosclerotic plaque development. Atherosclerosis. 300, 39-46 (2020).
- Eslami, P., et al. Effect of wall elasticity on hemodynamics and wall shear stress in patient-specific simulations in the coronary arteries. Journal of Biomechanical Engineering. 142 (2), (2019).
- Malvè, M., García, A., Ohayon, J., Martínez, M. A. Unsteady blood flow and mass transfer of a human left coronary artery bifurcation: FSI vs. CFD. International Communications in Heat and Mass Transfer. 39 (6), 745-751 (2012).
- Chiastra, C., Migliavacca, F., Martínez, M. &. #. 1. 9. 3. ;., Malvè, M. On the necessity of modelling fluid-structure interaction for stented coronary arteries. Journal of the Mechanical Behavior of Biomedical Materials. 34, 217-230 (2014).
- Carpenter, H., Gholipour, A., Ghayesh, M., Zander, A. C., Psaltis, P. In vivo based fluid-structure interaction biomechanics of the left anterior descending coronary artery. Journal of Biomechanical Engineering. 143 (8), (2021).
- Tang, D., et al. 3D MRI-based anisotropic FSI models with cyclic bending for human coronary atherosclerotic plaque mechanical analysis. Journal of Biomechanical Engineering. 131 (6), (2009).
- Gholipour, A., Ghayesh, M. H., Zander, A. C., Psaltis, P. J. In vivo based biomechanics of right and left coronary arteries. International Journal of Engineering Science. 154, (2020).
- Pei, X., Wu, B., Li, Z. -. Y. Fatigue crack propagation analysis of plaque rupture. Journal of Biomechanical Engineering. 135 (10), (2013).
- Wang, L., et al. IVUS-based FSI models for human coronary plaque progression study: components, correlation and predictive analysis. Annals of Biomedical Engineering. 43 (1), 107-121 (2015).
- Fan, R., et al. Human coronary plaque wall thickness correlated positively with flow shear stress and negatively with plaque wall stress: an IVUS-based fluid-structure interaction multi-patient study. BioMedical Engineering OnLine. 13 (1), 32 (2014).
- Migliori, S., et al. Application of an OCT-based 3D reconstruction framework to the hemodynamic assessment of an ulcerated coronary artery plaque. Medical Engineering & Physics. 78, 74-81 (2020).
- DIGITIZE07. MATLAB Central File Exchange Available from: https://www.mathworks.com/matlabcentral/fileexchange/14703-digitize07 (2021)
- interparc. MATLAB Central File Exchange Available from: https://www.mathworks.com/matlabcentral/fileexchange/34874-interparc (2021)
- Davies Justin, E., et al. Evidence of a dominant backward-propagating "suction" wave responsible for diastolic coronary filling in humans, attenuated in left ventricular hypertrophy. Circulation. 113 (14), 1768-1778 (2006).
- Campbell, I. C., et al. Effect of inlet velocity profiles on patient-specific computational fluid dynamics simulations of the carotid bifurcation. Journal of Biomechanical Engineering. 134 (5), (2012).
- Chang, W. -. T., et al. Ultrasound based assessment of coronary artery flow and coronary flow reserve using the pressure overload model in mice. Journal of Visualized Experiments: JoVE. (98), (2015).
- Holzapfel, G. A., Sommer, G., Gasser, C. T., Regitnig, P. Determination of layer-specific mechanical properties of human coronary arteries with nonatherosclerotic intimal thickening and related constitutive modeling. American Journal of Physiology-Heart and Circulatory Physiology. 289 (5), 2048-2058 (2005).
- Versluis, A., Bank, A. J., Douglas, W. H. Fatigue and plaque rupture in myocardial infarction. Journal of Biomechanics. 39 (2), 339-347 (2006).
- ANSYS Inc. ANSYS Academic Research Mechanical, Release 19.0, Mechanical APDL Theory Reference, Structures with Material Nonlinearities, Hyperelasticity, Mooney-Rivlin. ANSYS Inc. , (2019).
- Dong, J., Sun, Z., Inthavong, K., Tu, J. Fluid-structure interaction analysis of the left coronary artery with variable angulation. Computer Methods in Biomechanics and Biomedical Engineering. 18 (14), 1500-1508 (2015).
- Johnston, B. M., Johnston, P. R., Corney, S., Kilpatrick, D. Non-Newtonian blood flow in human right coronary arteries: Steady state simulations. Journal of Biomechanics. 37 (5), 709-720 (2004).
- Abbasian, M., et al. Effects of different non-Newtonian models on unsteady blood flow hemodynamics in patient-specific arterial models with in-vivo validation. Computer Methods and Programs in Biomedicine. 186, (2020).
- Soulis, J. V., et al. Non-Newtonian models for molecular viscosity and wall shear stress in a 3D reconstructed human left coronary artery. Medical Engineering & Physics. 30 (1), 9-19 (2008).
- Liu, B., Tang, D. Influence of non-Newtonian properties of blood on the wall shear stress in human atherosclerotic right coronary arteries. Molecular & Cellular Biomechanics: MCB. 8 (1), (2011).
- Morbiducci, U., Ponzini, R., Grigioni, M., Redaelli, A. Helical flow as fluid dynamic signature for atherogenesis risk in aortocoronary bypass. A numeric study. Journal of Biomechanics. 40 (3), 519-534 (2007).
- Morbiducci, U., et al. In vivo quantification of helical blood flow in human aorta by time-resolved three-dimensional cine phase contrast magnetic resonance imaging. Annals of Biomedical Engineering. 37 (3), (2009).
- Sughimoto, K., et al. Effects of arterial blood flow on walls of the abdominal aorta: Distributions of wall shear stress and oscillatory shear index determined by phase-contrast magnetic resonance imaging. Heart and Vessels. 31 (7), 1168-1175 (2016).
- Ku, D. N., Giddens, D. P., Zarins, C. K., Glagov, S. Pulsatile flow and atherosclerosis in the human carotid bifurcation. Positive correlation between plaque location and low oscillating shear stress. Arteriosclerosis. 5 (3), 293-302 (1985).
- Mazzi, V., et al. Wall shear stress topological skeleton analysis in cardiovascular flows: Methods and applications. Mathematics. 9 (7), 720 (2021).
- Moraes, M. C., Cardenas, D. A. C., Furuie, S. S. Automatic lumen segmentation in IVOCT images using binary morphological reconstruction. BioMedical Engineering OnLine. 12 (1), 78 (2013).
- Akyildiz, A. C., et al. The effects of plaque morphology and material properties on peak cap stress in human coronary arteries. Computer Methods in Biomechanics and Biomedical Engineering. 19 (7), 771-779 (2016).
- Tang, D., et al. Quantifying effects of plaque structure and material properties on stress distributions in human atherosclerotic plaques using 3D FSI models. Journal of Biomechanical Engineering. 127 (7), 1185-1194 (2005).
- Li, J., et al. Multimodality intravascular imaging of high-risk coronary plaque. JACC: Cardiovascular Imaging. , (2021).
- Bourantas Christos, V., et al. Utility of multimodality intravascular imaging and the local hemodynamic forces to predict atherosclerotic disease progression. JACC: Cardiovascular Imaging. 13 (4), 1021-1032 (2020).
- Liao, R., Luc, D., Sun, Y., Kirchberg, K. 3-D reconstruction of the coronary artery tree from multiple views of a rotational X-ray angiography. The International Journal of Cardiovascular Imaging. 26 (7), 733-749 (2010).
- Holzapfel, G. A., Gasser, T. C., Ogden, R. W. A new constitutive framework for arterial wall mechanics and a comparative study of material models. Journal of Elasticity and the Physical Science of Solids. 61 (1), 1-48 (2000).
- Gholipour, A., Ghayesh, M. H., Zander, A., Mahajan, R. Three-dimensional biomechanics of coronary arteries. International Journal of Engineering Science. 130, 93-114 (2018).
- Akyildiz, A. C., et al. Effects of intima stiffness and plaque morphology on peak cap stress. BioMedical Engineering OnLine. 10 (1), 25 (2011).
- Baranger, J., Mertens, L., Villemain, O. Blood flow imaging with ultrafast doppler. Journal of Visualized Experiments: JoVE. (164), (2020).
- Westra, J., et al. Diagnostic performance of in-procedure angiography-derived quantitative flow reserve compared to pressure-derived fractional flow feserve: The FAVOR II Europe-Japan study. Journal of the American Heart Association. 7 (14), (2018).
- Torii, R., et al. The impact of plaque type on strut embedment/protrusion and shear stress distribution in bioresorbable scaffold. European Heart Journal - Cardiovascular Imaging. 21 (4), 454-462 (2020).
- Peirlinck, M., et al. Precision medicine in human heart modeling. Biomechanics and Modeling in Mechanobiology. , 1-29 (2021).
- Franke, K. B., et al. Current state-of-play in spontaneous coronary artery dissection. Cardiovascular Diagnosis and Therapy. 9 (3), 281 (2019).
- Alber, M., et al. Integrating machine learning and multiscale modeling-perspectives, challenges, and opportunities in the biological, biomedical, and behavioral sciences. NPJ Digital Medicine. 2 (1), 115 (2019).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationThis article has been published
Video Coming Soon