Élever le papillon blanc du chou (Pieris rapae) dans des conditions contrôlées : une étude de cas avec tolérance aux métaux lourds
Dans cet article
Résumé
Cet article présente un protocole détaillé pour l’élevage du papillon blanc du chou dans des conditions de laboratoire contrôlées avec un régime artificiel, ce qui permet des manipulations précises de la nutrition précoce et de l’exposition aux toxines. Les résultats représentatifs montrent comment la toxicité des métaux lourds peut être dosée avec ce protocole.
Résumé
Le papillon blanc du chou (Pieris rapae) est un système important pour la recherche appliquée en lutte antiparasitaire et la recherche fondamentale en écologie comportementale et nutritionnelle. Les blancs de chou peuvent être facilement élevés dans des conditions contrôlées avec un régime artificiel, ce qui en fait un organisme modèle du monde des papillons. Dans cet article, une manipulation de l’exposition aux métaux lourds est utilisée pour illustrer les méthodes de base pour élever cette espèce. Le protocole général illustre comment les papillons peuvent être capturés dans le champ, amenés à pondre dans des cages de serre et transférés sous forme de larves dans des régimes artificiels. Les méthodes montrent comment les papillons peuvent être marqués, mesurés et étudiés pour une variété de questions de recherche. Les résultats représentatifs donnent une idée de la façon dont les régimes artificiels dont les composants varient peuvent être utilisés pour évaluer la performance des papillons par rapport à un régime témoin. Plus précisément, les papillons étaient les plus tolérants au nickel et les moins tolérants au cuivre, avec une tolérance de zinc quelque part au milieu. Les explications possibles de ces résultats sont discutées, y compris l’hyperaccumulation de nickel dans certaines plantes hôtes de moutarde et des preuves récentes chez les insectes que le cuivre pourrait être plus toxique qu’on ne le pensait auparavant. Enfin, la discussion examine d’abord les variations du protocole et les instructions pour le dépannage de ces méthodes, avant d’examiner comment les recherches futures pourraient optimiser davantage le régime artificiel utilisé dans cette étude. Dans l’ensemble, en fournissant un aperçu vidéo détaillé de l’élevage et de la mesure des blancs de chou sur les régimes artificiels, ce protocole fournit une ressource pour l’utilisation de ce système dans un large éventail d’études.
Introduction
Le petit papillon blanc du chou (Pieris rapae, ci-après « chou blanc ») est une espèce cosmopolite de moutarde, comme le chou, le brocoli et le canola 1,2,3. Dans le même temps, le chou blanc est un système puissant pour la recherche en biologie et un modèle de papillon couramment utilisé, car ils peuvent être facilement élevés et manipulés dans des expériences de laboratoire contrôlées 4,5. La recherche sur les papillons blancs du chou a fourni des informations essentielles en ce qui concerne la recherche de l’hôte 6,7,8, l’utilisation des ressources en nectar9,10,11, le choix du partenaire et la sélection sexuelle 12,13,14, le développement et l’évolution du modèle des ailes15,16,17, et les réponses aux nouveaux et changeants environnements18,19. Bon nombre de ces connaissances reposent sur le fait que les blancs de chou peuvent être élevés avec des régimes artificiels 4,20,21, qui peuvent être manipulés avec précision pour refléter de mauvaises conditions nutritionnelles 22,23, des niveaux de polluants écologiquement pertinents 24,25,26,27 ou des transitions vers de nouvelles plantes hôtes28,29. La présente étude utilise une expérience sur l’exposition aux métaux lourds pour illustrer les méthodes de base pour élever des papillons blancs du chou avec un régime artificiel en laboratoire et les mesures clés de performance des larves et des adultes. De nombreux aspects de ces méthodes s’appliquent à d’autres papillons 30,31 et papillonsde nuit 32,33,34 qui peuvent être élevés avec un régime artificiel.
Dans cet article, une expérience sur la tolérance aux métaux est utilisée pour illustrer les méthodes générales d’élevage des papillons blancs du chou. Les métaux lourds sont un polluant anthropique commun découlant de la dégradation des produits humains, des procédés industriels et de la contamination héritée de l’utilisation historique dans les pesticides, les peintures et d’autres produits35,36,37,38. De nombreux métaux lourds, y compris le plomb, le cuivre, le zinc et le nickel, peuvent passer du sol et de l’eau dans les tissus végétaux 39,40,41,42, et les métaux dans la poussière peuvent se déposer sur les feuilles des plantes 43,44,45, ce qui entraîne de multiples voies d’exposition aux larves d’insectes phytophages. L’exposition aux métaux lourds tôt dans la vie peut avoir des effets négatifs sur le développement des animaux, en particulier sur le tissu neural, et des niveaux élevés peuvent être mortels 35,36,46,47,48. Un certain nombre d’études ont montré les effets négatifs de l’exposition aux métaux sur les insectes en développement, y compris les ravageurs et les insectes utiles 49,50,51. Le grand nombre de polluants de métaux lourds et le fait qu’ils coexistent souvent dans les environnements humains52 signifient que des méthodes de laboratoire précises sont nécessaires pour que les chercheurs puissent exposer les insectes en développement à différents niveaux et combinaisons de divers métaux pour comprendre et atténuer leurs effets environnementaux.
Le présent travail compare les impacts des métaux communs sur la survie et le développement du chou blanc, en se concentrant sur le cuivre (Cu), le zinc (Zn) et le nickel (Ni), trois polluants courants dans les environnements humains. Par exemple, les plantes herbacées des routes rurales du Minnesota contiennent jusqu’à 71 ppm Zn, 28 ppm Cu et 5 ppm Ni53. Cette expérience manipule les niveaux de ces métaux dans les régimes artificiels des papillons blancs du chou à des niveaux correspondant et dépassant les niveaux observés dans l’environnement. Un régime artificiel est utilisé pour contraster la toxicité relative de ces métaux, prédisant que les blancs de chou seraient plus sensibles aux polluants métalliques qui ne font pas partie intégrante de leur physiologie (nickel) par rapport à ceux qui se produisent, bien qu’à de faibles niveaux, dans les enzymes et les tissus (cuivre et zinc; Graphique 1). Tout au long de ce texte, fournit des détails méthodologiques et des visualisations vidéo d’accompagnement pour illustrer les méthodes d’élevage et de recherche de cet important système de modèles de papillons.
Protocole
Cette recherche a été menée sous le permis APHIS de l’USDA P526P-13-02979.
1. Collection de papillons expérimentaux
- Attrapez des papillons femelles adultes avec un filet à insectes aérien. Les blancs de chou se trouvent généralement dans des habitats ouverts et perturbés avec des plantes nectarifères et des plantes hôtes (de la famille des Brassicaceae).
- Cherchez quand le soleil est au rendez-vous et que la température est chaude. Pour cibler les femelles, recherchez les individus qui voltigent lentement, près du sol, et atterrissent sur les plantes pour « tambouriner » (goûter) les feuilles avec leur tarse antérieur.
- Installez les femelles dans des cages pour récolter les œufs.
REMARQUE : Les femelles prélevées sur le terrain se sont accouplées en moyenne avec un ou deux mâles12 et devraient commencer à pondre des œufs fertiles peu de temps après la capture. Les femelles capturées dans la nature ont besoin de lumière naturelle pour pondre et s’accoupler, alors placez la cage dans une serre ou un rebord de fenêtre. - Abriter les femelles avec une plante hôte pour récolter les œufs.
REMARQUE : Les femelles accepteront une variété de plantes hôtes, y compris le chou vert, le radis, le chou frisé, le chou vert et l’Arabidopsis, mais s’assureront que les plantes n’ont pas été traitées avec des pesticides.- Présentez les plantes hôtes dans des pots ou dans des récipients avec de l’eau pour maintenir la pression des feuilles, comme les tiges de chou frisé dans des tubes d’eau floraux.
- Si le chercheur souhaite prélever des œufs et les transférer directement dans l’alimentation, utilisez d’abord un élastique pour attacher une feuille de plante hôte au sommet d’une tasse d’eau en plastique, puis étirez un morceau de parafilm autour du bord - les femelles qui touchent la feuille pondront sur le parafilm (voir5).
- Assurez-vous que la cage contient également quelque chose pour maintenir l’humidité relative élevée, par exemple, en arrosant quotidiennement une plante en pot ou en mouillant une serviette, surtout dans des conditions sèches. Si les plantes en pot sont arrosées dans la cage, assurez-vous qu’une serviette est sous le pot, car les papillons peuvent rester coincés dans l’eau de l’accumulation.
- Nourrissez les papillons avec une solution d’eau de miel diluée à 10% présentée sur une éponge jaune, que les papillons apprennent rapidement à utiliser, surtout s’ils sont logés avec des personnes expérimentées.
- Pour encourager les papillons à se nourrir d’éponges, placez-les directement sur la mangeoire, surtout après avoir légèrement pulvérisé avec une bouteille d’eau, ce qui les amène souvent à sortir leur trompe.
- Pour installer la mangeoire, rincez d’abord soigneusement les éponges jaunes ou oranges, puis coupez-les en petits carrés qui s’insèrent dans des boîtes de Petri en plastique de 60 mm. Changez les mangeoires tous les jours et nettoyez les éponges dans une solution d’eau de Javel douce, suivie d’un rinçage complet pour éviter la croissance de moisissures.
2. Faire des régimes artificiels
- Tout d’abord, utilisez la recette du tableau 1, ou d’autres sources pertinentes, pour déterminer la recette pertinente pour une expérience. Apporter les modifications nécessaires spécifiques à l’espèce focale ou à l’expérience. Imprimez une recette à suivre lors de la pesée des ingrédients.
- Pesez tous les ingrédients secs, à l’exception de l’agar-agar, dans un seul récipient. Assurez-vous que les ingrédients sont remis dans leur lieu d’entreposage respectif, en notant que plusieurs ingrédients sont entreposés à 4 °C. Placez le mélange d’ingrédients sec prépesé dans un mélangeur contenant 5 ml d’huile de lin.
- Pour chaque lot de régime, suivez les étapes détaillées ci-dessous.
- Mélanger 15 g de gélose à mailles fines avec 400 mL d’eau distillée dans un bécher d’au moins 1 L. Cuire au micro-ondes jusqu’à ce que la gélose soit proche de l’ébullition, avec de fines bulles dans tout le mélange, en remuant le mélange toutes les 30-60 s pour éviter l’ébullition.
- À ce mélange de gélose chaude, ajoutez 400 ml d’eau distillée à la température du robinet pour l’amener à une température appropriée pour la mélanger aux ingrédients secs, car le mélange de vitamines est sensible à la chaleur.
- Ajouter le mélange de gélose au mélangeur et bien mélanger, en grattant les bords du mélangeur si nécessaire.
- Pendant que la gélose chauffe, placez au moins soixante-dix tasses diététiques de quatre onces sur le comptoir avec les bords se touchant. Après avoir bien mélangé le régime, versez le mélange du mélangeur dans des tasses de régime, en veillant à ce que le régime couvre le fond de chaque tasse.
- Une fois le régime refroidi, placez les couvercles sur les tasses, étiquetez les tasses diététiques avec le type de régime, empilez-les sur des plateaux et conservez-les jusqu’à 1 mois à 4 ° C jusqu’à utilisation.
3. Transfert et élevage avec des régimes artificiels
- Feuilles de plante hôte de maison avec des œufs de papillon dans des tasses de charcuterie de 30 oz avec un couvercle en maille dans une chambre climatique à 24 ° C. Après 1 semaine, vérifiez les tasses - en vous assurant que les larves sont écloses et au stade tardif du premier ou du début du deuxième stade, un bon moment pour le transfert au régime artificiel.
- Transférez les larves dans le régime artificiel avec un pinceau, désinfectez-la avec un spray d’eau de Javel et un rinçage à l’eau entre les récipients de larves. Transférer trois larves dans chaque tasse de 4 oz. Bien que le régime artificiel soit dense en énergie et puisse supporter de fortes densités de larves, évitez d’emballer les larves dans des tasses, car les maladies et les moisissures peuvent se propager dans des tasses à forte densité larvaire.
- Placez les gobelets dans un bac en plastique sur leurs côtés afin que le frass tombe au fond des tasses et loin de l’alimentation, réduisant ainsi le risque de moisissure et de maladie.
- Entreposer les tasses de régime dans des conditions de température contrôlée avec des niveaux de lumière faibles à modérés. Surveillez les tasses pour détecter les moisissures et les maladies tous les 1-2 jours en jetant un coup d’œil à travers les couvercles transparents des tasses.
- Les tasses contenant de la moisissure ou une maladie peuvent être mises en quarantaine ou congelées pour éviter de se propager à d’autres tasses.
4. Levée et manipulation des adultes
- Laissez les larves se nymphoser et émerger dans les tasses de régime. Lorsque les adultes émergent, donnez-leur quelques heures pour que leurs ailes durcissent avant de les retirer pour les marquer. Retirez les papillons adultes des tasses avec des mains propres en saisissant doucement leurs ailes, en notant que saisir les quatre ailes plus près de leur corps est une prise plus stable.
- Pour marquer les papillons, tenez les individus secs par la tête et le thorax et utilisez un sharpie à pointe fine pour marquer légèrement un numéro sur leur aile postérieure.
- Les individus sexuels utilisant une combinaison de marques alaires et d’organes génitaux; Les femelles ont généralement deux taches noires sur leur aile antérieure dorsale et des ailes postérieures plus foncées et plus jaunâtres, tandis que les mâles ont généralement une tache noire plus petite sur l’aile antérieure dorsale sur un fond blanc plus brillant54.
- Étant donné que cette coloration montre des variations individuelles et saisonnières, confirmez le sexe en utilisant des traits abdominaux - les mâles ont deux griffes à l’extrémité distale de leur abdomen et un abdomen plus étroit en général, tandis que les femelles ont une seule ouverture génitale.
- Transférer les adultes dans des enveloppes de verre ciré en ouvrant l’enveloppe d’une main, en tenant le papillon par la tête et le thorax, en le glissant dans l’enveloppe et en saisissant les ailes à travers l’enveloppe de l’autre main.
- Assurez-vous que les quatre ailes sont fermées normalement dans l’enveloppe.
- Conserver les papillons dans des conditions froides (5-6 °C) jusqu’à 1 semaine avant l’expérimentation, mais laisser au moins 1 jour s’acclimater lorsqu’ils sont sortis du réfrigérateur.
5. Mesures du rendement
- Pour mesurer les traits des ailes sur les individus morts, retirez les ailes du papillon en tenant le thorax dans une main et en utilisant une pince pour enlever chaque aile à sa base. Placez les ailes à plat dans une boîte à lumière et prenez des photos pour des mesures ultérieures.
- Pour obtenir des estimations de la fécondité, logez les adultes dans des cages d’accouplement, en laissant au moins 1 jour pour la maturation reproductive des mâles et 1 jour pour l’accouplement. Sacrifiez les femelles à des moments précis pour le comptage des œufs par dissection, ou collectez des œufs chaque jour sur les plantes hôtes.
- Pour estimer les charges d’œufs, retirez l’abdomen de la femelle, placez-le dans 1x tampon PBS et coupez une fente le long de la face ventrale.
- Utilisez des pinces pour séparer les entrailles de la cuticule, puis éloignez les ovaires de l’intestin, des trachées et d’autres contenus de l’abdomen.
- Dépliez les quatre ovarioles enroulées dans chacun des deux ovaires, en notant où les ovules matures, jaunes et décortiqués se transforment en follicules immatures. Utilisez un compteur pour aider à calculer le nombre total d’œufs matures, généralement compris entre 0 et 200 œufs.
- Pour déterminer le statut d’accouplement d’une femelle disséquée, ouvrez la bourse copulatrix et séparez les spermatophores à l’intérieur. Au fur et à mesure que les spermatophores sont digérés, ils développent généralement une « queue » et sont imbriqués les uns dans les autres.
6. Étude de cas
REMARQUE : Des papillons blancs femelles adultes ont été prélevés dans la nature en 2014 pour fonder les populations expérimentales. Les femelles adultes sont originaires des environs de Davis, en Californie (N = 8 femelles fondatrices).
- Abriter les papillons
- Hébergez les femelles dans des cages grillagées « BugDorm » (61 cm x 61 cm x 61 cm) sous lumière naturelle dans une serre. Fournir une feuille organique du chou de la plante hôte (Brassica oleracea) pour la ponte.
- Pour maintenir l’humidité dans les cages, incluez une petite plante en pot (Cosmos), arrosée quotidiennement, placée sur une serviette dans chaque cage.
- Ramassez les œufs tous les jours en transférant les feuilles avec de nouveaux œufs dans des gobelets en plastique de 473 ml percés de trous dans le couvercle et placez-les dans une chambre climatique.
- Fournir aux papillons un accès ad libitum à une solution d’eau de miel à 10% (faite en diluant du miel biologique avec de l’eau distillée), accessible par une éponge jaune dans une petite boîte de Petri qui est changée quotidiennement.
- Préparer des régimes artificiels
- Préparer des régimes artificiels pour les larves blanches de chou en utilisant des modifications des régimes de lépidoptères précédemment développés4. Un lot de régime contenait 50 g de germe de blé, 27 g de caséine, 10 g de cellulose, 24 g de saccharose, 15 g de farine de chou, 9 g de mélange de sel Wesson, 12 g de levure Torula, 3,6 g de cholestérol, 10,5 g de mélange vitaminé Vanderzant, 1,1 g de méthylparabène, 1,5 g d’acide sorbique, 3 g d’acide ascorbique et 0,175 g de streptomycine (voir le tableau des matières).
- Prépeser les ingrédients secs pour plusieurs lots de régime (tableau 1) et bien mélanger pour augmenter l’homogénéité entre les types de régime avant d’être subdivisés en lots distincts pour le mélange avec des solutions métalliques.
- Placez les ingrédients secs dans un mélangeur avec de l’huile de lin et le mélange métallique correspondant.
NOTE: L’huile de lin a été utilisée dans la présente expérience car elle a été vendue par un ancien fournisseur de régimes d’insectes. Maintenant, l’huile de lin biologique est utilisée exclusivement, qui est fabriquée à partir de la même plante, mais est moins susceptible de contenir des additifs que les fournisseurs commerciaux d’huile de lin. - Versez la diète préparée dans des gobelets de charcuterie en plastique de 118 ml (4 oz). Utilisez des sels métalliques solubles pour ajouter des métaux focaux aux régimes artificiels. Viser les concentrations de métaux basées sur les observations préalables de la teneur en métaux des plantes (par exemple, accumulation de nickel 55,56,57 ou contamination des plantes en bordure de route 58,59,60) et la tolérance des métaux chez les autres lépidoptères 49,50,51.
- Dissoudre les sels métalliques dans 500 à 1 000 mL d’eau distillée avant de prendre les quantités correspondantes à ajouter aux régimes artificiels. Par exemple, pour préparer le régime à base de nickel de 100 ppm, ajouter 317,6 mL de solution de NiCl2 1 M au régime artificiel avant de mélanger pour obtenir une concentration finale de 100 mg/g de poids sec de Ni (environ 53 mg/g de poids humide). Cette quantité se traduit par une concentration moyenne mesurée de 109,6 ppm (tableau 2) basée sur la spectroscopie d’émission atomique avec plasma à couplage inductif.
NOTE: Les niveaux de métaux ont été estimés par les laboratoires d’analyse de recherche de l’Université du Minnesota avec six échantillons.
- Entretien
- Maintenir les œufs récoltés sur les plantes hôtes dans des chambres climatiques à 23 °C pendant les photopériodes de 14h10 pendant 7 jours. Après cela, transférez les larves du début du deuxième stade dans le régime artificiel.
- Au moment du transfert, répartir uniformément les larves d’une plante donnée entre les quatre types de régime alimentaire afin d’éviter de confondre les lots de larves avec le type de régime. Transférer les larves (N = 346 au total) en deux individus par tasse diététique de 118 ml afin de réduire l’incidence de la maladie causée par le surpeuplement et de laisser suffisamment d’espace aux adultes pour qu’ils puissent éventuellement s’enfermer.
- Trous de perforation (trois par couvercle) dans les couvercles des gobelets d’élevage. Placez les gobelets dans des bacs en plastique de la taille d’une boîte à chaussures pour l’élevage, avec les différents régimes intercalés pour éviter tout effet systématique de l’emplacement dans la chambre d’élevage.
- Abriter les tasses de larves dans des chambres climatiques à 23 ° C sur des photopériodes de 14h10 (avec des bacs d’eau au fond de la chambre pour maintenir l’humidité autour de 50%-60%, surveillée avec un capteur d’humidité domestique). Dans le cas où les tasses deviendraient moisies (environ huit tasses au total dans cette étude de cas), retirez les tasses de la chambre et retirez ces individus de l’expérience.
- Laisser les larves se nymphoser et émerger dans les gobelets d’élevage (N = 162 au total).
REMARQUE : Pour les conditions d’élevage de cette étude, le temps de développement entre la collecte des œufs et l’émergence des adultes était en moyenne d’environ 25 à 30 jours (allant de 20 à 40 jours, p. ex. 25,28). - À l’approche de l’émergence des pupes, vérifiez quotidiennement les tasses pour détecter les individus nouvellement fermés et retirez les adultes dont les ailes sont séchées. Étiquetez les adultes sur leurs ailes postérieures avec leur numéro individuel correspondant (attribué au transfert larvaire) à l’aide d’un sharpie noir à pointe fine. Déterminez le sexe de chaque individu et marquez sur une enveloppe de verre leur nombre et leur date d’émergence. Placer les papillons adultes dans des enveloppes de verreine et conserver à -20 °C jusqu’à la poursuite du traitement.
REMARQUE : Une petite fraction des adultes émergents présentent des déformations des ailes qui nuiraient au vol et à la survie des adultes (5 % à 8 %); Ces personnes sont exclues des analyses de survie pour ces expériences.
- Mesure et analyse des données
- Mesurer la survie comme la survie du deuxième stade (lorsque les chenilles ont été placées sur l’alimentation) à l’émergence adulte.
NOTE: La présente étude s’est concentrée sur la survie et le temps de développement comme mesures de performance sur les différents régimes. - Mesurer le temps de développement comme le nombre de jours entre le transfert aux régimes et l’émergence des adultes dans la chambre climatique.
- Pour l’analyse des données, exécutez deux ensembles de modèles qui incluent des interactions entre le métal et la concentration.
NOTE: Comme les deux interactions étaient significatives (F 2194 = 4,56, p = 0,01 pour le temps de développement et X2 = 12,1, p = 0,002 pour la survie), l’étude a procédé à une analyse distincte de chaque métal. - Pour analyser la survie, exécutez des tests du chi carré pour chaque métal afin de tester les effets de la dose de métal (traités en quatre catégories) sur la survie à l’âge adulte avec les ailes entièrement intactes.
- Lorsqu’un effet significatif de la dose est détecté, effectuer un suivi du chi carré pour comparer chaque niveau au régime témoin. Pour analyser le temps de développement (du moment du transfert à l’émergence à l’âge adulte), testez les effets du sexe sur le temps de développement.
REMARQUE: Comme il n’y avait aucun effet du sexe sur le temps de développement, (p > 0,10) pour aucun métal dans cette expérience, nous l’avons retiré de la considération dans le modèle. - Exécuter une ANOVA distincte pour chaque métal afin de tester l’effet des quatre concentrations sur le temps de développement. De plus, exécutez des essais t pour chaque concentration par rapport au témoin afin de déterminer la concentration minimale où un effet sur la performance est observé.
REMARQUE : Dans cette étude, JMP v16 a été utilisé pour toutes les analyses. Toutes les données brutes sont disponibles sur Mendeley61.
- Mesurer la survie comme la survie du deuxième stade (lorsque les chenilles ont été placées sur l’alimentation) à l’émergence adulte.
Résultats Représentatifs
Aperçu
Le régime artificiel peut être utilisé pour élever des papillons blancs de chou dans des conditions standard pour tester les effets de certains ingrédients de régime sur la performance des papillons. Dans le présent travail, des régimes artificiels ont été utilisés pour étudier la toxicité de différents métaux trouvés dans les plantes hôtes poussant dans des zones polluées (Figure 1). Les larves ont été élevées sur des régimes contenant des concentrations croissantes de trois métaux différents (Figure 2; détails méthodologiques spécifiques présentés à la section 6 du protocole). La survie et le développement des papillons ont été plus influencés par le cuivre et le zinc et moins touchés par le nickel (figure 3 et figure 4), avec une sensibilité comparable à d’autres études sur les papillons et les papillons de nuit élevés avec des régimes artificiels (figure 5).
Survie
Les larves de papillons ont été transférées dans des régimes artificiels contenant du cuivre, du nickel, du zinc ou du témoin, où la concentration de chaque type de métal variait à trois niveaux (tableau 3). Une image représentative des larves à une dose croissante de toxine est présentée à la figure 2. Il n’y avait pas d’effet de la concentration de métal sur la survie du nickel, mais il y avait un effet significatif pour le cuivre et le zinc (tableau 3 et figure 3). Les comparaisons post-hoc du chi carré ont démontré que le zinc présentait une baisse de survie par rapport au régime témoin à seulement la plus haute concentration de zinc (1 000 ppm, comparaison post-hoc X12 = 8,41, p = 0,004; Graphique 1). Le cuivre a également montré une baisse significative de la survie uniquement aux niveaux les plus élevés utilisés (500 ppm, X12 = 7,00, p = 0,008), bien qu’il y ait eu une augmentation bénéfique non significative de la survie aux deux niveaux les plus bas (50 ppm et 100 ppm; Graphique 3).
Temps de développement
Il y avait un effet significatif de la concentration de cuivre et de zinc sur le temps de développement (tableau 4 et figure 4). À mesure que la concentration de cuivre augmentait, il y avait une augmentation du temps de développement, avec un écart significatif par rapport au témoin à partir de 50 ppm (p = 0,027; Graphique 3). À mesure que la concentration de zinc augmentait, il y avait une augmentation du temps de développement, avec un écart significatif par rapport au témoin à partir de 100 ppm (p = 0,03; Graphique 4). Il y avait une tendance à l’augmentation du nickel pour entraîner des temps de développement plus longs (p = 0,08; Tableau 4), et les comparaisons de chaque régime avec le témoin ont montré des effets significatifs à partir de 100 ppm (p = 0,022; Graphique 4).
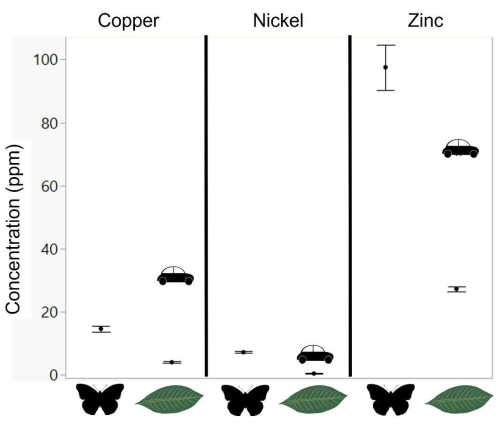
Figure 1 : Niveaux observés de métaux focaux dans les tissus des papillons et les plantes hôtes. (Données de62.) Les niveaux de cuivre, de nickel et de zinc sont indiqués pour les tissus de papillons Pieris (élevés sur bok choy en laboratoire) et les moutardes récoltées dans la nature (Bertorea sp.). Les voitures indiquent les niveaux observés dans les feuilles de plantes le long des routes à fort trafic53. Les concentrations de métaux dans les régimes artificiels utilisés dans cette étude sont indiquées au tableau 1; Les points représentent les moyennes et les barres d’erreur représentent l’erreur-type. Veuillez cliquer ici pour voir une version agrandie de cette figure.

Figure 2 : Image de larves blanches de chou transférées le même jour à des régimes artificiels de concentration croissante d’une toxine. Cette image montre des larves issues d’une étude dose-réponse (présentée dans 28 en utilisant du matériel végétal séché pour la plante toxique Aristolochia). Photo par ESR. Veuillez cliquer ici pour voir une version agrandie de cette figure.
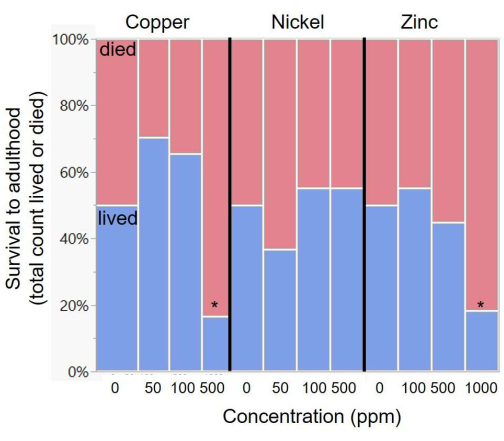
Figure 3 : Variation de la survie entre les régimes métalliques à des concentrations croissantes. Les astérisques indiquent un écart significatif dans la survie par rapport au régime témoin. Les concentrations exactes de métaux dans les régimes alimentaires sont énumérées dans le tableau 2. Veuillez cliquer ici pour voir une version agrandie de cette figure.
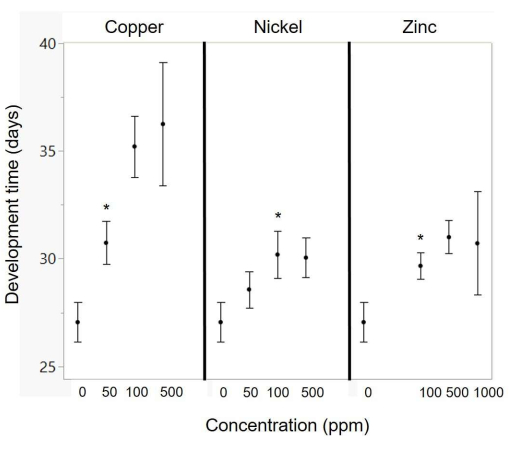
Figure 4 : Effets de la concentration de métaux sur le temps de développement. Les astérisques indiquent la concentration de métal la plus faible pour laquelle il existe une différence significative par rapport au témoin (à l’aide d’un test t). Les concentrations exactes de métaux dans les régimes alimentaires sont énumérées dans le tableau 2. Les points représentent les moyennes et les barres d’erreur représentent l’erreur type. Veuillez cliquer ici pour voir une version agrandie de cette figure.
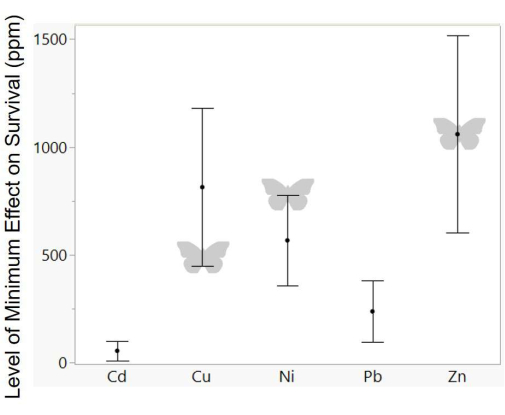
Figure 5 : Résumé de la tolérance aux métaux chez d’autres lépidoptères. Les données composites de survie présentées sont tracées à partir de 11 études existantes 49,50,51,56,63,64,65,66,67,68. La variable de réponse est le niveau (en ppm) de concentration de métal où les effets négatifs sur la survie sont observés pour la première fois. Les papillons indiquent les résultats de cette étude, notant que les valeurs de tolérance pour le nickel étaient plus élevées que celles mesurées dans cette étude. Les points représentent les moyennes et les barres d’erreur représentent l’erreur type. Veuillez cliquer ici pour voir une version agrandie de cette figure.
| Ingrédient | Peser comme | g | Ml |
| Germe de blé | Ingrédients secs | 50 | |
| Cellulose | Ingrédients secs | 10 | |
| Farine de chou | Ingrédients secs | 15 | |
| Caséine | Ingrédients secs | 27 | |
| Saccharose | Ingrédients secs | 24 | |
| Wesson Mélange de sel | Ingrédients secs | 9 | |
| Levure Torula | Ingrédients secs | 12 | |
| Cholestérol | Ingrédients secs | 3.6 | |
| Mélange de vitamines | Ingrédients secs | 10.5 | |
| Méthyl parabène | Ingrédients secs | 0.75 | |
| Acide sorbique | Ingrédients secs | 1.5 | |
| Acide ascorbique | Ingrédients secs | 3 | |
| Streptomycine | Ingrédients secs | 0.175 | |
| Huile de lin | ingrédients humides | 5 | |
| Agar-agar | agar-agar | 15 |
Tableau 1: Recette pour un régime artificiel. Les poids (et les volumes) des ingrédients dans un lot de papillon blanc de chou sont indiqués. Les ingrédients secs (et l’huile de lin) sont préparés séparément du mélange de gélose (dissous dans 400 mL d’eau bouillante, puis porté à une température plus froide avec 400 mL d’eau à température ambiante).
| Type de régime alimentaire | Cuivre (ppm) | Nickel (ppm) | Zinc (ppm) |
| Cuivre-« 100 ppm » | 96.1 | 1.75 | 69.9 |
| Nickel-« 100 ppm » | 7.29 | 109.6 | 68.9 |
| Zinc-« 100 ppm » | 7.96 | 1.06 | 186.2 |
| Zinc-« 500 ppm » | 6.51 | 1.16 | 708 |
| Contrôle | 5.89 | 0.59 | 59.3 |
Tableau 2 : Mesures des métaux dans l’alimentation. Les niveaux moyens de cuivre, de nickel et de zinc dans un sous-ensemble des régimes artificiels utilisés dans l’étude sont montrés. Le nom du régime (« type » dans l’analyse) est indiqué à gauche, les valeurs entre guillemets étant le niveau calculé. La concentration cible est indiquée entre guillemets. Un sous-ensemble de régimes alimentaires utilisés dans l’étude a été analysé pour s’assurer que les valeurs calculées correspondaient aux valeurs cibles par rapport aux valeurs réalisées; Il convient de noter qu’il y a souvent un petit degré de variation dans la composition des composants de l’alimentation, et chaque ligne rapportée ne représente qu’une seule répétition.
| Moital | Pearson X32 | P |
| Cuivre (N = 118) | 17.82 | 0.0005 |
| Nickel (N = 152) | 3.45 | 0.33 |
| Zinc (N = 152) | 12.52 | 0.006 |
Tableau 3 : Effets de la concentration de métaux sur la survie. Les résultats d’un test du chi carré pour chaque métal, contrastant trois concentrations de métal par rapport à un régime témoin.
| Métal | F | P |
| Cuivre (N = 61) | F3,57 = 9,84 | <0,0001 |
| Nickel (N = 75) | F3,71 = 2,35 | 0.079 |
| Zinc (N = 64) | F3,60= 3,79 | 0.015 |
Tableau 4 : Effets de la concentration de métaux sur le temps de développement. Les résultats des ANOVA individuelles pour chaque métal sont présentés.
Disponibilité des données :
Toutes les données sont disponibles sur Mendeley61.
Discussion
Dans cette recherche, des papillons blancs du chou (Pieris rapae) ont été élevés avec un régime artificiel pour examiner les différences de toxicité des métaux lourds. Ce faisant, cette étude fournit des méthodes générales pour l’élevage et les études en laboratoire de ce système papillon facile à manipuler. Cette discussion aborde d’abord des questions plus générales sur les méthodes examinées ici, puis passe en revue nos résultats scientifiques avant de conclure par des réflexions sur les composants de l’alimentation artificielle.
Le protocole examiné ici donne les étapes d’une méthode générale d’élevage pour les papillons blancs du chou, mais il y a beaucoup de points dans ce protocole qui peuvent être modifiés. Par exemple, alors que l’étude de cas présentée ici utilise des éponges pour se nourrir, d’autres chercheurs ont eu de la chance avec des mèches dentaires et des fleurs de soie remplies d’eau de miel5. Alors que la présente étude utilise de l’eau de miel comme nourriture, d’autres chercheurs ont utilisé des solutions de sucre et même Gatorade. Si les pupes doivent être pesées ou déplacées vers d’autres conditions d’émergence (par exemple, induisant une diapause et nécessitant un stockage au froid pendant 1 mois), le chercheur peut facilement les retirer des tasses en les aspergeant d’eau pour humidifier leurs attaches en soie et les saisir avec des pinces à plumes, puis en les accrochant à nouveau à l’aide de ruban adhésif double face. Si les chercheurs ont besoin de plus de flexibilité en ce qui concerne le moment où les papillons adultes sont déplacés dans des cages pour le comportement des adultes, ils peuvent être conservés au réfrigérateur pendant plusieurs semaines, mais ils doivent être nourris. Tous les plusieurs jours, les papillons doivent être sortis pour être nourris avec une solution d’eau de miel diluée. Sous éclairage intérieur, cela peut être fait en utilisant une épingle pour dérouler leur trompe dans la nourriture. Du côté de la performance adulte, un large éventail de mesures de condition physique peut être pris sur les papillons blancs du chou. La taille du corps peut être mesurée comme la masse humide ou sèche des larves à certains stades, des pupes ou des adultes (sacrifiés ou maintenus dans des enveloppes de verre), ou par la mesure de la longueur des ailes dans le programme ImageJ (voir 12,24,25,28). La fécondité au cours de la vie des femelles peut être mesurée par des collectes quotidiennes d’œufs sur les plantes hôtes 25,69,70, et la taille des caractères spécifiques peut être mesurée comme mesure de la performance; Par exemple, la masse ou le volume du cerveau ou des régions cérébrales individuelles 62,71,72, ou la masse ou la teneur en protéines du thorax ou du muscle de vol 62,70. Enfin, les adultes peuvent être utilisés dans des études comportementales pour tester un certain nombre de questions examinant l’effet de la manipulation du régime alimentaire sur le choix de la recherche de nourriture ou de ponte27,73.
Si le protocole d’élevage ne fonctionne pas comme prévu, il y a quelques aspects à résoudre. Tout d’abord, on peut se demander si les niveaux de lumière sont suffisamment élevés pour susciter un comportement adulte normal. Alors que les lignées de Pieris adaptées au laboratoire pondent des œufs sous une lumière fluorescente, la seule lumière artificielle qui fonctionne pour les lignées de type sauvage sont les puissantes lampes de serre à large spectre. La lumière naturelle dans les serres, les rebords de fenêtres ou à l’extérieur fonctionne mieux pour provoquer un comportement d’accouplement et de ponte. Deuxièmement, si les œufs n’éclosent pas ou si les larves meurent tôt dans le développement, il y a quelques éléments à considérer. Le matériel végétal hôte doit être biologique, notant que les plantes « biologiques » des magasins sont parfois traitées avec des produits chimiques qui peuvent tuer les larves, de sorte qu’il est souvent préférable d’élever ses propres plantes hôtes. Si le taux d’acceptation de l’hôte est plus faible, des feuilles plus jeunes avec une teneur en azote plus élevée peuvent être tentées, présentant des plantes en pot au lieu de feuilles individuelles et assurant l’accouplement des femelles. Les femelles accepteront les semis de Brassica, même les petites pousses âgées de 2 semaines. La méthode à la paraffine fonctionne bien pour transférer les œufs dans différentes conditions, mais il convient de noter que le taux d’acceptation a tendance à être inférieur à celui des plantes entières. Troisièmement, tous les composants du régime doivent être de haute qualité et non périmés. L’huile de lin doit être remplacée chaque année et conservée au réfrigérateur24,25. Le germe de blé, le mélange de vitamines et les antibiotiques doivent également être conservés au frais. Quatrièmement, on peut envisager de peaufiner la configuration de la tasse de régime. N’importe quel nombre de types de gobelets en plastique jetables peuvent être utilisés pour l’élevage, de 1 oz à 15 oz. Nous avons constaté que 4 oz est une bonne taille pour permettre l’émergence des adultes et s’emballe bien dans nos chambres climatiques. Les trous percés dans les couvercles permettent la circulation de l’air, mais trop de trous peuvent assécher le régime alimentaire dans des conditions de faible humidité, de sorte que ce nombre peut devoir être ajusté. Cinquièmement, les conditions dans la chambre climatique peuvent devoir être ajustées en combinaison avec les conditions de la tasse. Si les conditions sont trop sèches, les plantes hôtes avec des œufs peuvent se dessécher avant que les larves puissent être transférées, et les tasses avec régime alimentaire peuvent se dessécher avant que les papillons n’émergent. D’autre part, si les conditions sont trop humides, les tasses peuvent abriter des moisissures et des maladies. Les chercheurs devront peut-être ajuster le flux d’air dans les tasses en utilisant des couvercles en maille ou plus ou moins de trous dans les couvercles. Un autre problème courant est les lumières de la chambre qui sont suffisamment brillantes pour provoquer des variations de température dans les tasses et une accumulation de condensation; L’utilisation de gradateurs est une option facile pour l’élevage larvaire.
En ce qui concerne les questions de recherche de cet article, cette étude a révélé que les blancs de chou étaient relativement plus sensibles au cuivre qu’au nickel ou au zinc. Le cuivre a eu des effets négatifs importants sur le temps de développement à des concentrations aussi faibles que 50 ppm (figure 3 et tableau 3) et sur la survie à 500 ppm (figure 4, tableau 4). En revanche, il n’y avait aucun effet négatif du nickel sur la survie (jusqu’à 500 ppm; Graphique 3) ou des effets négatifs sur le temps de développement à 100 ppm (figure 4). Les blancs de chou étaient assez tolérants au zinc, avec des effets de survie observés seulement à 1 000 ppm (figure 3) et des effets négatifs sur le temps de développement à partir de 100 ppm (figure 4). D’après les concentrations relativement plus élevées de zinc dans les tissus des papillons et les moutardes (leur plante hôte; Figure 1), on s’attendait à ce qu’une tolérance relativement plus grande au zinc soit observée. Cependant, la sensibilité au cuivre et la tolérance au nickel étaient quelque peu inattendues étant donné les très faibles concentrations de nickel dans les tissus des papillons (figure 1) et la nécessité du cuivre comme micronutriment. Ces résultats inattendus sont discutés ci-dessous après avoir examiné la tolérance de ces métaux chez d’autres papillons et papillons de nuit.
Pour comparer les données actuelles avec la sensibilité aux métaux mesurée chez d’autres lépidoptères, des données provenant d’études existantes ont été compilées sur la concentration minimale, où les métaux lourds ont eu un impact négatif sur la survie 49,50,51,56,63,64,65,66,67,68; ces études ont porté sur les papillons de nuit, en particulier les espèces nuisibles (Galleria mellonella, Lymantria dispar, Plutella xylostella, Spodoptera sp.). Toutes les valeurs de sensibilité mesurées dans cette étude se rapprochent de la plage mesurée pour ces autres espèces (figure 5). Cependant, la mesure de la tolérance au nickel dans cette étude semble être plus élevée que prévu - bien qu’il n’y ait pas eu d’effet significatif de survie à 500 ppm, l’étude précédente sur Pieris rapae a également révélé une tolérance très élevée pour le nickel (effets significatifs à partir de 1 000 ppm56), malgré de faibles concentrations naturelles dans leurs tissus (Figure 1). La mesure de la sensibilité au cuivre dans cette étude semble également être à l’extrémité inférieure pour les études sur les lépidoptères. Bien que l’utilisation d’un régime artificiel permette une comparaison pratique et contrôlée de la sensibilité relative aux métaux, il est important de noter que les composants du régime pourraient modifier la mesure de la sensibilité absolue aux métaux. Par exemple, la vitamine C dans l’alimentation pourrait compenser le stress oxydatif induit par les métaux74, ou les antibiotiques dans l’alimentation pourraient modifier les effets des microbes sur le traitement des métaux75. Une ligne intéressante de recherche future serait de manipuler systématiquement de tels composants de régime pour tester les effets sur la toxicité des métaux, en particulier compte tenu des questions sur le rôle fonctionnel des microbes intestinaux lépidoptères 76,77 et des composants du nectar qui peuvent avoir des propriétés antioxydantes78. En outre, la variation des besoins alimentaires entre les espèces peut rendre les comparaisons interspécifiques difficiles, et les méthodes artificielles basées sur l’alimentation devraient être complétées par des manipulations des plantes hôtes.
Ces papillons sont particulièrement tolérants au nickel et sensibles au cuivre. Des recherches antérieures ont noté que de nombreuses plantes de la famille de la moutarde, qui comprend les plantes favorisées par les Pieridae, hyperaccumulent le nickel comme mécanisme de défense contre les herbivores 55,56,63,79,80,81. Cette hyperaccumulation est supérieure à 1 000 ppm dans les tissus végétaux, ce qui est supérieur de plusieurs ordres de grandeur à ce que l’on observe dans la plupart des plantes (figure 1). Il est possible que les Pieris aient une tolérance particulièrement élevée pour le nickel en raison de la sélection passée par de tels accumulateurs de nickel, comme on l’a supposéprécédemment 26. Bien que le cuivre ait été moins fréquemment étudié comme micronutriment dans l’alimentation des insectes, il existe certaines preuves qu’il joue un petit rôle dans la reproduction et l’immunité, bien que principalement chez les insectes hématophages (p. ex.,82,83). Il est possible que le cuivre joue un rôle physiologique moins important chez les papillons que chez d’autres animaux 84,85,86, ce qui concorde avec des travaux récents soulignant comment le cuivre peut être un polluant aussi préoccupant pour les insectes que le plomb, le cadmium et le mercure (p. ex.,87,88,89). Bien qu’il ait été démontré que les pieris évitent la contamination par le cuivre à de faibles niveaux90, la mobilité du cuivre dans les plantes (p. ex. déplacement dans les feuilles et les fleurs) l’a également signalé comme un contaminant métallique préoccupant91.
Bien que ces résultats fournissent des données intéressantes sur la toxicité relative de ces métaux pour les papillons blancs du chou, cet article vise également à être d’une utilité générale comme illustration visuelle détaillée des méthodes d’élevage de ce puissant système. Les blancs de chou sont faciles à élever et à manipuler dans des expériences de laboratoire contrôlées 4,5 facilitant les études de recherche d’hôte 6,7,8, de recherche de nourriture9,10,11 et de sélection sexuelle12,13,14. La capacité d’élever ces papillons avec un régime artificiel est essentielle pour créer des conditions de jardin communes à des fins de comparaison et pour manipuler les nutriments, les toxines et même de nouvelles plantes hôtes. Cependant, il est important de noter que ce régime artificiel n’est pas nécessairement le régime artificiel optimal pour cette espèce et pourrait probablement être amélioré avec de futures manipulations. Par exemple, le mélange de sel dans ce régime (et d’autres régimes lépidoptères) a été développé à l’origine pour les vertébrés et a des niveaux de calcium plus élevés que ce dont la plupart des insectes ont besoin92,93. Ainsi, certains de nos efforts d’élevage ont fait des mélanges de sel personnalisés avec des niveaux de calcium plus faibles (par exemple, 62), et d’autres utilisent le « mélange de sel de Beck », qui peut être plus approprié pour de nombreuses espèces d’insectes94. Dans nos propres manipulations, nous avons également constaté que les papillons se comportaient mieux avec relativement moins de germe de blé et relativement plus de cellulose par rapport aux concentrations initiales4. Un domaine nécessitant une attention particulière est la source de lipides et la concentration dans l’alimentation. Par exemple, des travaux antérieurs ont montré que le passage de l’huile de lin (utilisée dans cette étude) aux phospholipides augmentait les taux d’accouplement et les taux de croissance de Pieris sous régime artificiel95. La supplémentation en acides gras spécifiques dans les régimes artificiels peut avoir des effets positifs supplémentaires96,97. L’optimisation du régime artificiel de Pieris98,99 crée des opportunités pour répondre à des questions intéressantes sur l’écologie nutritionnelle 100,101,102, l’écologie évolutive et l’écotoxicologie. Ces approches de régime artificiel permettent aux chercheurs d’aborder des questions sur le rôle de lipides spécifiques dans l’évolution cognitive 103, la pré-adaptation aux toxines28, les composants alimentaires qui réduisent la toxicité des polluants 104, ou encore les interactions stœchiométriques entre nutriments105.
Déclarations de divulgation
Les auteurs n’ont aucun conflit d’intérêts à déclarer.
Remerciements
Nous sommes reconnaissants du soutien des assistants de premier cycle pendant l’élevage pour ce travail, en particulier Regina Kurandina et Rhea Smykalski. Carolyn Kalinowski a aidé à compiler la littérature sur la toxicité des métaux chez d’autres lépidoptères. Ce travail a été rendu possible grâce à une subvention de recherche d’été du département d’écologie, d’évolution et de comportement de l’Université du Minnesota.
matériels
| Name | Company | Catalog Number | Comments |
| 1-L Pyrex beaker | Fisher Scientific | 07-250-059 | |
| 500 mL graduated cylinder | Fisher Scientific | 03-007-43 | |
| 60-mm plastic petri dish lid | Fisher Scientific | 08-757-100B | |
| Ascorbic Acid | Frontier | 6015 | |
| Blender | Amazon - Ninja Store | BL610 Professional | |
| Cabbage Flour | Frontier | 1086 | |
| Casein | Frontier | 1100 | |
| Celluose | Frontier | 3425 | |
| Cholsterol | Sigma | C3045 | |
| Cups for rearing (4 oz) | Wasserstrom | 6094583 | purchase with matching lids |
| Fine Mesh Agar | Sigma | ||
| Flaxseed Oil | amazon | B004R63VI6 | |
| Floral water tubes, 2.8 x 0.8inch | Amazon - Yimaa Direct | B08BZ969DK | |
| Glassine envelopes (1 3/4 x 2 7/8 INCHES) | Amazon - Wizard Coin Supply | B0045FG90G | |
| Mesh Cages (15.7 x 15.7 x 23.6") | Amazon | B07SK6P94S | |
| Methyl Paraben | Frontier | 7685 | |
| Ohaus Portable Scale | Fisher Scientific | 02-112-228 | |
| Organic Honey | Amazon | B07DHQQFGM | |
| Photo studio portable lightbox | Amazon | B07T6TNYJ1 | |
| Plastic bin, shoebox size | Amazon | B09L3B3V1R | |
| Plastic disposable transfer pipets | Fisher Scientific | 13-680-50 | |
| Sorbic Acid | Sigma | S1626 | |
| Spatulas | Fisher Scientific | 14-357Q | |
| Streptomycin | Sigma | S9137 | |
| Sucrose | Target | ||
| Torula Yeast | Frontier | 1720 | |
| Vanderzant vitamin mix | Frontier | F8045 | |
| Weigh boats | Fisher Scientific | 01-549-750 | |
| Wesson Salt Mix | Frontier | F8680 | |
| Wheat Germ | Frontier | G1659 | |
| Wooden handled butterfly net, 12" hoop | Amazon - Educational Science | B00O5JDLVC | |
| Yellow sponges | Amazon-Celox | B0B8HTHY5B |
Références
- Snyder, L. D., Gomez, M. I., Mudrak, E. L., Power, A. G. Landscape-dependent effects of varietal mixtures on insect pest control and implications for farmer profits. Ecological Applications. 31 (2), 2246 (2021).
- Shelton, A., Andaloro, J. T., Barnards, J. Effects of cabbage looper, imported cabbageworm, and diamondback moth on fresh market and processing cabbage. Journal of Economic Entomology. 75 (4), 742-745 (1982).
- Cartea, M. E., Padilla, G., Vilar, M., Velasco, P. Incidence of the major Brassica pests in northwestern Spain. Journal of Economic Entomology. 102 (2), 767-773 (2009).
- Troetschler, R. G., Malone, C. M., Bucago, E. R., Johnston, M. R. System for rearing Pieris rapae (Lepidoptera: Pieridae) on a noncruciferous artificial diet developed for Manduca sexta (Lepidoptera: Sphingidae). Journal of Economic Entomology. 78 (6), 1521-1523 (1985).
- Webb, S., Shelton, A. Laboratory rearing of the imported cabbageworm. New Yorks Food and Life Sciences Bulletin. 122, 1-6 (1988).
- Root, R. B., Kareiva, P. M. The search for resources by cabbage butterflies (Pieris rapae): ecological consequences and adaptive significance of Markovian movements in a patchy environment. Ecology. 65 (1), 147-165 (1984).
- Hern, A., Edwards-Jones, G., McKinlay, R. G. A review of the pre-oviposition behaviour of the small cabbage white butterfly, Pieris rapae (Lepidoptera: Pieridae). Annals of Applied Biology. 128 (2), 349-371 (1996).
- Renwick, J. A. A., Radke, C. D. Sensory cues in host selection for oviposition by the cabbage butterfly, Pieris-Rapae. Journal of Insect Physiology. 34 (3), 251-257 (1988).
- Lewis, A. C. Memory constraints and flower choice in Pieris rapae. Science. 232 (4752), 863-865 (1986).
- Kandori, I., Ohsaki, N. The learning abilities of the white cabbage butterfly, Pieris rapae, foraging for flowers. Researches on Population Ecology. 38, 111-117 (1996).
- Alm, J., Ohmeiss, T. E., Lanza, J., Vriesenga, L. Preference of cabbage white butterflies and honey-bees for nectar that contains amino-acids. Oecologia. 84 (1), 53-57 (1990).
- Espeset, A., et al. Anthropogenic increases in nutrients alter sexual selection dynamics: a case study in butterflies. Behavioral Ecology. 30 (3), 598-608 (2019).
- Tigreros, N. Linking nutrition and sexual selection across life stages in a model butterfly system. Functional Ecology. 27 (1), 145-154 (2013).
- Morehouse, N. I., Rutowski, R. L. In the eyes of the beholders: female choice and avian predation risk associated with an exaggerated male butterfly color. American Naturalist. 176 (6), 768-784 (2010).
- Stoehr, A. M., Goux, H. Seasonal phenotypic plasticity of wing melanisation in the cabbage white butterfly, Pieris rapae L. (Lepidoptera: Pieridae). Ecological Entomology. 33 (1), 137-143 (2008).
- Stoehr, A. M., Walker, J. F., Monteiro, A. Spalt expression and the development of melanic color patterns in pierid butterflies. Evodevo. 4 (1), 6 (2013).
- Stoehr, A. M., Wojan, E. M. Multiple cues influence multiple traits in the phenotypically plastic melanization of the cabbage white butterfly. Oecologia. 182 (3), 691-701 (2016).
- Ryan, S. F., et al. Global invasion history of the agricultural pest butterfly Pieris rapae revealed with genomics and citizen science. Proceedings of the National Academy of Sciences. 116 (40), 20015-20024 (2019).
- Snell-Rood, E. C., Papaj, D. R. Patterns of phenotypic plasticity in common and rare environments: a study of host use and color learning in the cabbage white butterfly Pieris rapae. American Naturalist. 173 (5), 615-631 (2009).
- Kono, Y. Rearing Pieris rapae crucivora Boisduval (Lepidoptera: Pieridae) on artificial diets. Applied Entomology and Zoology. 3 (2), 96-98 (1968).
- Parra, J. R. . The Evolution of Artificial Diets and their Interactions in Science and Technology. Insect Bioecology and Nutrition for Integrated Pest Management. , (2012).
- Morehouse, N. I., Rutowski, R. L. Developmental responses to variable diet composition in a butterfly: the role of nitrogen, carbohydrates and genotype. Oikos. 119 (4), 636-645 (2010).
- Rotem, K., Agrawal, A. A., Kott, L. Parental effects in Pieris rapae in response to variation in food quality: adaptive plasticity across generations. Ecological Entomology. 28 (2), 211-218 (2003).
- Shephard, A. M., et al. Assessing zinc tolerance in two butterfly species: consequences for conservation in polluted environments. Insect Conservation and Diversity. 13 (2), 201-210 (2020).
- Shephard, A. M., Zambre, A. M., Snell-Rood, E. C. Evaluating costs of heavy metal tolerance in a widely distributed, invasive butterfly. Evolutionary Applications. 14 (5), 1390-1402 (2021).
- Kobiela, M. E., Snell-Rood, E. C. Nickel exposure has complex transgenerational effects in a butterfly. Integrative and Comparative Biology. 58 (5), 1008-1017 (2018).
- Philips, K. H., Kobiela, M. E., Snell-Rood, E. C. Developmental lead exposure has mixed effects on butterfly cognitive processes. Animal Cognition. 20 (1), 87-96 (2017).
- Sikkink, K. L., et al. Tolerance of novel toxins through generalized mechanism simulating gradual host shifts of butterflies. American Naturalist. 195 (3), 485-503 (2020).
- Pentzold, S., et al. excretion and avoidance of cyanogenic glucosides in insects with different feeding specialisations. Insect Biochemistry and Molecular Biology. 66, 119-128 (2015).
- Lampert, E. C., Dyer, L. A., Bowers, M. D. Dietary specialization and the effects of plant species on potential multitrophic interactions of three species of nymphaline caterpillars. Entomologia Experimentalis et Applicata. 153 (3), 207-216 (2014).
- Genc, H., Nation, J. L. An artificial diet for the butterfly Phyciodes phaon (Lepidoptera: Nymphalidae). Florida Entomologist. 87 (2), 194-198 (2004).
- Brinton, F., Proverbs, M., Carty, B. Artificial diet for mass production of the codling moth, Carpocapsa Pomonella (Lepidoptera: Olethreutidae)1. The Canadian Entomologist. 101 (6), 577-584 (1969).
- Metwally, H. M., et al. Low cost artificial diet for rearing the greater wax moth, Galleria mellonella L. (Lepidoptera: Pyralidae) as a host for entomopathogenic nematodes. Egyptian Journal of Biological Pest Control. 22 (1), 15 (2012).
- Carpenter, J. E., Bloem, S. Interaction between insect strain and artificial diet in diamondback moth development and reproduction. Entomologia Experimentalis et Applicata. 102 (3), 283-294 (2002).
- Jaiswal, A., Verma, A., Jaiswal, P. Detrimental effects of heavy metals in soil, plants, and aquatic ecosystems and in humans. Journal of Environmental Pathology Toxicology and Oncology. 37 (3), 183-197 (2018).
- Kumar, A., et al. Lead toxicity: Health hazards, influence on food chain, and sustainable remediation approaches. International Journal of Environmental Research and Public Health. 17 (7), 2179 (2020).
- Gall, J. E., Boyd, R. S., Rajakaruna, N. Transfer of heavy metals through terrestrial food webs: a review. Environmental Monitoring and Assessment. 187, 201 (2015).
- Mohammed, A. S., Kapri, A., Goel, R. . Heavy Metal Pollution: Source, Impact, and Remedies. Biomanagement of Metal-Contaminated Soils. , 1-28 (2011).
- Mitra, A., Chatterjee, S., Voronina, A. V., Walther, C., Gupta, D. K. Lead toxicity in plants: a review. Lead in Plants and the Environment. , 99-116 (2020).
- Perugini, M., et al. Heavy metal (Hg, Cr, Cd, and Pb) contamination in urban areas and wildlife reserves: Honeybees as bioindicators. Biological Trace Element Research. 140 (2), 170-176 (2011).
- Rycewicz-Borecki, M., McLean, J. E., Dupont, R. R. Bioaccumulation of copper, lead, and zinc in six macrophyte species grown in simulated stormwater bioretention systems. Journal of Environmental Management. 166, 267-275 (2016).
- Zulfiqar, U., et al. Lead toxicity in plants: Impacts and remediation. Journal of Environmental Management. 250, 109557 (2019).
- Spliethoff, H. M., et al. Estimated lead (Pb) exposures for a population of urban community gardeners. Environmental Geochemistry and Health. 38, 955-971 (2016).
- Li, C. C., et al. Foliar dust as a reliable environmental monitor of heavy metal pollution in comparison to plant leaves and soil in urban areas. Chemosphere. 287, 132341 (2022).
- Ram, S. S., et al. Plant canopies: bio-monitor and trap for re-suspended dust particulates contaminated with heavy metals. Mitigation and Adaptation Strategies for Global Change. 19, 499-508 (2014).
- Karri, V., Schuhmacher, M., Kumar, V. Heavy metals (Pb, Cd, As and MeHg) as risk factors for cognitive dysfunction: A general review of metal mixture mechanism in brain. Environmental Toxicology and Pharmacology. 48, 203-213 (2016).
- Tong, S., von Schirnding, Y. E., Prapamontol, T. Environmental lead exposure: a public health problem of global dimensions. Bulletin of the World Health Organization. 78 (9), 1068-1077 (2000).
- Liu, J. H., Lewis, G. Environmental toxicity and poor cognitive outcomes in children and adults. Journal of Environmental Health. 76 (6), 130-138 (2014).
- Gintenreiter, S., Ortel, J., Nopp, H. J. Effects of different dietary levels of cadmium, lead, copper, and zinc on the vitality of the forest pest insect Lymantria-Dispar L (Lymantriidae, Lepid). Archives of Environmental Contamination and Toxicology. 25, 62-66 (1993).
- Cheruiyot, D. J., Boyd, R. S., Moar, W. Testing the joint effects hypothesis of elemental defense using Spodoptera exigua. Journal of Chemical Ecology. 41 (2), 168-177 (2015).
- Coleman, C. M., Boyd, R. S., Eubanks, M. D. Extending the elemental defense hypothesis: Dietary metal concentrations below hyperaccumulator levels could harm herbivores. Journal of Chemical Ecology. 31 (8), 1669-1681 (2005).
- Kaushal, S. S., et al. Making 'chemical cocktails'-Evolution of urban geochemical processes across the periodic table of elements. Applied Geochemistry. 119, 104632 (2020).
- Shephard, A. M., et al. Traffic patterns, more than adjacent land use, influence element content of roadside forbs for insect pollinators. Ecological Solutions and Evidence. 3 (4), 12195 (2022).
- Scott, J. A. . The Butterflies of North America: A Natural History and Field Guide. , (1992).
- Boyd, R. S. High-nickel insects and nickel hyperaccumulator plants: A review. Insect Science. 16 (1), 19-31 (2009).
- Boyd, R. S., Martens, S. N. Nickel hyperaccumulated by thlaspi-montanum var montanum is acutely toxic to an insect herbivore. Oikos. 70 (1), 21-25 (1994).
- Cempel, M., Nickel, G. A review of its sources and environmental toxicology. Polish Journal of Environmental Studies. 15 (3), 375-382 (2006).
- Aslam, J., Khan, S. A., Khan, S. H. Heavy metals contamination in roadside soil near different traffic signals in Dubai, United Arab Emirates. Journal of Saudi Chemical Society. 17 (3), 315-319 (2013).
- Mitchell, T. S., et al. Traffic influences nutritional quality of roadside plants for monarch caterpillars. Science of the Total Environment. 724, 138045 (2020).
- Voegborlo, R., Chirgawi, M. Heavy metals accumulation in roadside soil and vegetation along a major highway in Libya. Journal of Science and Technology. 27 (3), 86-97 (2007).
- Snell-Rood, E., Kobiela, M. . Data for: Rearing the Cabbage White Butterfly (Pieris rapae) in Controlled Conditions: A Case Study with Heavy Metal Tolerance. , (2023).
- Snell-Rood, E. C., Espeset, A., Boser, C. J., White, W. A., Smykalski, R. Anthropogenic changes in sodium affect neural and muscle development in butterflies. Proceedings of the National Academy of Sciences. 111 (28), 10221-10226 (2014).
- Boyd, R. S., Moar, W. J. The defensive function of Ni in plants: response of the polyphagous herbivore Spodoptera exigua (Lepidoptera: Noctuidae) to hyperaccumulator and accumulator species of Streptanthus (Brassicaceae). Oecologia. 118 (2), 218-224 (1999).
- Cheruiyot, D. J., Boyd, R. S., Moar, W. J. Exploring lower limits of plant elemental defense by cobalt, copper, nickel, and zinc. Journal of Chemical Ecology. 39 (5), 666-674 (2013).
- Davis, M. A., Boyd, R. S., Cane, J. H. Host-switching does not circumvent the Ni-based defence of the Ni hyperaccumulator Streptanthus polygaloides (Brassicaceae). South African Journal of Science. 97 (11-12), 554-557 (2001).
- Dubovskiy, I. M., Grizanova, E. V., Ershova, N. S., Rantala, M. J., Glupov, V. V. The effects of dietary nickel on the detoxification enzymes, innate immunity and resistance to the fungus Beauveria bassiana in the larvae of the greater wax moth Galleria mellonella. Chemosphere. 85 (1), 92-96 (2011).
- Jhee, E. M., Boyd, R. S., Eubanks, M. D. Nickel hyperaccumulation as an elemental defense of Streptanthus polygaloides (Brassicaceae): influence of herbivore feeding mode. New Phytologist. 168 (2), 331-343 (2005).
- Zhou, J. L., Shu, Y. H., Zhang, G. R., Zhou, Q. Lead exposure improves the tolerance of Spodoptera litura (Lepidoptera: Noctuidae) to cypermethrin. Chemosphere. 88 (4), 507-513 (2012).
- Snell-Rood, E. C., Davidowitz, G., Papaj, D. R. Reproductive tradeoffs of learning in a butterfly. Behavioral Ecology. 22 (2), 291-302 (2011).
- Snell-Rood, E. C., Davidowitz, G., Papaj, D. R. Plasticity in learning causes immediate and trans-generational changes in allocation of resources. Integrative and Comparative Biology. 53 (2), 329-339 (2013).
- Snell-Rood, E. C., Papaj, D. R., Brain Gronenberg, W. size: A global or induced cost of learning. Brain Behavior and Evolution. 73 (2), 111-128 (2009).
- Snell-Rood, E. C., et al. Nutritional constraints on brain evolution: Sodium and nitrogen limit brain size. Evolution. 74 (10), 2304-2319 (2020).
- Jaumann, S., Snell-Rood, E. C. Adult nutritional stress decreases oviposition choosiness and fecundity in female butterflies. Behavioral Ecology. 30 (3), 852-863 (2019).
- Sahiti, H., Bislimi, K., Bajgora, A., Rexhepi, A., Dalo, E. Protective effect of vitamin C against oxidative stress in common carp (Cyprinus carpio) induced by heavy metals. International Journal of Agriculture and Biosciences. 7 (2), 71-75 (2018).
- Rothman, J. A., Leger, L., Graystock, P., Russell, K., McFrederick, Q. S. The bumble bee microbiome increases survival of bees exposed to selenate toxicity. Environmental Microbiology. 21 (9), 3417-3429 (2019).
- Hammer, T. J., Janzen, D. H., Hallwachs, W., Jaffe, S. P., Fierer, N. Caterpillars lack a resident gut microbiome. Proceedings of the National Academy of Sciences. 114 (36), 9641-9646 (2017).
- Hammer, T. J., Sanders, J. G., Fierer, N. Not all animals need a microbiome. FEMS Microbiology Letters. 366 (10), (2019).
- Baker, H. G., Baker, I. . Coevolution of Animals and Plants. , 100-140 (1975).
- Boyd, R. S., Davis, M. A., Wall, M. A., Balkwill, K. Metal concentrations of insects associated with the South African Ni hyperaccumulator Berkheya coddii (Asteraceae). Insect Science. 13 (2), 85-102 (2006).
- Boyd, R. S., Wall, M. A., Jaffre, T. Nickel levels in arthropods associated with Ni hyperaccumulator plants from an ultramafic site in New Caledonia. Insect Science. 13 (4), 271-277 (2006).
- Kramer, U. Metal hyperaccumulation in plants. Annual Review of Plant Biology. 61, 517-534 (2010).
- Cardoso-Jaime, V., Broderick, N. A., Maya-Maldonado, K. Metal ions in insect reproduction: a crosstalk between reproductive physiology and immunity. Current Opinion in Insect Science. 52, 100924 (2022).
- Rivera-Perez, C., Clifton, M. E., Noriega, F. G. How micronutrients influence the physiology of mosquitoes. Current Opinion in Insect Science. 23, 112-117 (2017).
- Lee, J. H. Micronutrient deficiency syndrome: zinc, copper and selenium. Pediatric Gastroenterology, Hepatology & Nutrition. 15 (3), 145-150 (2012).
- Nube, M., Voortman, R. L. Human micronutrient deficiencies: linkages with micronutrient deficiencies in soils, crops and animal nutrition. Combating Micronutrient Deficiencies: Food-Based Approaches. , 289-311 (2011).
- Wysocka, D., Snarska, A., Sobiech, P. Copper-An essential micronutrient for calves and adult cattle. Journal of Elementology. 24 (1), 101-110 (2019).
- Oliveira, C. S., et al. Toxic metals that interact with thiol groups and alteration in insect behavior. Current Opinion in Insect Science. 52, 100923 (2022).
- Mogren, C. L., Trumble, J. T. The impacts of metals and metalloids on insect behavior. Entomologia Experimentalis et Applicata. 135 (1), 1-17 (2010).
- Hladun, K. R., Di, N., Liu, T. X., Trumble, J. T. Metal contaminant accumulation in the hive: Consequences for whole-colony health and brood production in the honey bee (Apis mellifera L.). Environmental Toxicology and Chemistry. 35 (2), 322-329 (2016).
- Elbassiouny, S. A. Changes in food-related behavioral-patterns of some phytophagous insect species following exposures to an antifeedant. Acta Phytopathologica et Entomologica Hungarica. 26 (3-4), 483-496 (1991).
- Hladun, K. R., Parker, D. R., Trumble, J. T. Cadmium, copper, and lead accumulation and bioconcentration in the vegetative and reproductive organs of Raphanus sativus: Implications for plant performance and pollination. Journal of Chemical Ecology. 41, 386-395 (2015).
- Nation, J., Robinson, F. Concentration of some major and trace elements in honeybees, royal jelly and pollens, determined by atomic absorption spectrophotometry. Journal of Apicultural Research. 10 (1), 35-43 (1971).
- Herbert Jr, E. W., Shimanuki, H. Mineral requirements for brood-rearing by honeybees fed a synthetic diet. Journal of Apicultural Research. 17 (3), 118-122 (1978).
- Beck, S. D., Chippendale, G., Swinton, D. Nutrition of the European corn borer, Ostrinia nubilalis. VI. A larval rearing medium without crude plant fractions. Annals of the Entomological Society of America. 61 (2), 459-462 (1968).
- Junnikkala, E. Rearing Pieris-Brassicae (L.) on a phospholipid and vitamin-supplemented semi-artificial diet. Annales Zoologici Fennici. 17 (1), 39-42 (1980).
- Hixson, S. M., et al. Long-chain omega-3 polyunsaturated fatty acids have developmental effects on the crop pest, the Cabbage White Butterfly Pieris rapae. PLoS One. 11 (3), e0152264 (2016).
- Turunen, S. Lipid utilization in adult Pieris brassicae with special reference to the role of linolenic acid. Journal of Insect Physiology. 20 (7), 1257-1269 (1974).
- Vanderzant, E. S. Development, significance, and application of artificial diets for insects. Annual Review of Entomology. 19, 139-160 (1974).
- Cohen, A. C. . Insect Diets: Science and Technology. , (2003).
- Balluffi-Fry, J., Leroux, S. J., Champagne, E., Vander Wal, E. In defense of elemental currencies: can ecological stoichiometry stand as a framework for terrestrial herbivore nutritional ecology. Oecologia. 199 (1), 27-38 (2022).
- Coogan, S. C. P., Raubenheimer, D., Zantis, S. P., Machovsky-Capuska, G. E. Multidimensional nutritional ecology and urban birds. Ecosphere. 9 (4), 02177 (2018).
- Raubenheimer, D., Simpson, S. J., Mayntz, D. Nutrition, ecology and nutritional ecology: toward an integrated framework. Functional Ecology. 23 (1), 4-16 (2009).
- Arien, Y., Dag, A., Zarchin, S., Masci, T., Shafir, S. Omega-3 deficiency impairs honey bee learning. Proceedings of the National Academy of Sciences. 112 (51), 15761-15766 (2015).
- Man, K. Y., et al. Use of biochar as feed supplements for animal farming. Critical Reviews in Environmental Science and Technology. 51 (2), 187-217 (2021).
- Shephard, A. M., Knudsen, K., Snell-Rood, E. C. Anthropogenic sodium influences butterfly responses to nitrogen-enriched resources: implications for the nitrogen limitation hypothesis. Oecologia. 201 (4), 941-952 (2023).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon