Isolement simultané de types de cellules résidentes du système nerveux central chez des souris adultes atteintes d’encéphalomyélite auto-immune
* Ces auteurs ont contribué à parts égales
Dans cet article
Résumé
À ce jour, les protocoles d’isolement simultané de tous les principaux types de cellules résidentes du système nerveux central à partir d’une même souris sont une demande non satisfaite. Le protocole montre une procédure applicable chez les souris naïves et expérimentales atteintes d’encéphalomyélite auto-immune pour étudier les réseaux cellulaires complexes au cours de la neuroinflammation et réduire simultanément le nombre de souris requis.
Résumé
L’encéphalomyélite auto-immune expérimentale (EAE) est le modèle murin le plus courant pour la sclérose en plaques (SEP) et est fréquemment utilisée pour élucider davantage l’étiologie encore inconnue de la SEP afin de développer de nouvelles stratégies de traitement. Le modèle EAE du peptide de glycoprotéine oligodendrocytaire de myéline 35-55 (MOG35-55) reproduit une évolution monophasique auto-résolutive avec paralysie ascendante dans les 10 jours suivant l’immunisation. Les souris sont examinées quotidiennement à l’aide d’un système de notation clinique. La SEP est induite par différents mécanismes pathologiques avec un schéma temporel spécifique, de sorte que l’étude du rôle des types de cellules résidentes du système nerveux central (SNC) au cours de la progression de la maladie est d’un grand intérêt. La caractéristique unique de ce protocole est l’isolement simultané de tous les principaux types de cellules résidentes du SNC (microglie, oligodendrocytes, astrocytes et neurones) applicables chez les EAE adultes et les souris saines. La dissociation du cerveau et de la moelle épinière des souris adultes est suivie d’un tri cellulaire activé magnétiquement (MACS) pour isoler la microglie, les oligodendrocytes, les astrocytes et les neurones. La cytométrie en flux a été utilisée pour effectuer des analyses de qualité des suspensions unicellulaires purifiées, confirmant la viabilité après isolement cellulaire et indiquant la pureté de chaque type de cellule d’environ 90 %. En conclusion, ce protocole offre un moyen précis et complet d’analyser des réseaux cellulaires complexes chez des souris saines et EAE. De plus, le nombre de souris requis peut être considérablement réduit car les quatre types de cellules sont isolés des mêmes souris.
Introduction
La sclérose en plaques (SEP) est une maladie auto-immune inflammatoire chronique du système nerveux central (SNC) caractérisée par une démyélinisation, des lésions axonales, une gliose et une neurodégénérescence. Malgré de nombreuses approches de recherche dans ce domaine, la physiopathologie de la SEP n’est toujours pas entièrement comprise 1,2,3,4. Le modèle animal le plus courant pour l’étude de la SEP est l’encéphalomyélite auto-immune expérimentale (EAE) induite par le peptide de glycoprotéine oligodendrocytaire de myéline 35-55 (MOG35-55), qui partage bon nombre deses caractéristiques cliniques et physiopathologiques5,6,7,8,9 . Il est basé sur la réponse du système immunitaire contre les antigènes spécifiques du SNC conduisant à l’inflammation, à la démyélinisation et à la dégénérescence neuroaxonale. L’encéphalomyélite auto-immune expérimentale (EAE) est un modèle approprié pour l’étude des voies neuro-inflammatoires et des cascades de signalisation observées dans la SEP.
Les options thérapeutiques actuelles pour la SEP ne sont que partiellement efficaces et se concentrent principalement sur la phase inflammatoire initiale de la maladie. Cependant, la composante neurodégénérative de la SEP semble être le défi majeur pour les approches thérapeutiques à long terme. Par conséquent, des protocoles d’isolement cellulaire reproductibles et précis sont nécessaires pour étudier de manière exhaustive les mécanismes moléculaires et cellulaires des maladies auto-immunes. Même s’il existe des protocoles pour l’isolement d’un seul type de cellule 10,11,12,13,14,15, il existe un besoin non satisfait pour l’isolement simultané de plusieurs populations de cellules résidentes du SNC à la fois. Les protocoles précédents pour l’isolement des cellules résidentes du SNC ne préservent pas la fonctionnalité et la pureté cellulaires, ce qui entraîne une co-culture avec des cellules voisines 16,17,18 ou l’inadaptation à des analyses complexes de réseaux intracellulaires ex vivo 19,20,21,22.
L’objectif de ce protocole était d’établir une méthode reproductible et complète pour l’isolement simultané de suspensions unicellulaires pures et viables de tous les principaux types de cellules résidentes du SNC, applicable chez les souris adultes saines et EAE. Les différents types de cellules ont été isolés à l’aide du tri cellulaire activé par magnétisme (MACS)23. La séparation cellulaire peut être réalisée soit par sélection positive, c’est-à-dire par marquage magnétique de marqueurs de surface spécifiques au type cellulaire, soit par sélection négative par biotinylation et épuisement de toutes les cellules indésirables. La cytométrie en flux a été appliquée pour assurer une pureté supérieure à 90 % et une viabilité d’au moins 80 % des suspensions unicellulaires isolées.
En conclusion, l’objectif principal était d’établir un protocole pour l’isolement simultané de tous les principaux types de cellules résidentes du SNC en tant qu’outil polyvalent pour l’étude des voies neuro-inflammatoires offrant une analyse complète et précise des réseaux cellulaires complexes et des cascades de signalisation biochimique chez les souris saines et EAE.
Protocole
Toutes les expériences EAE ont été induites chez des souris femelles C57BL/6J à l’âge de 10-12 semaines et approuvées par les autorités locales (Landesamt für Natur, Umwelt und Verbraucherschutz Nordrhein-Westfalen). Le respect de la législation allemande et européenne sur la protection des animaux a également été assuré à tout moment des expériences. Toutes les souris ont été gardées dans des cages ventilées individuellement dans des conditions de logement pour animaux.
REMARQUE : Les volumes de réactifs suivants se réfèrent à un cerveau et à une moelle épinière murins adultes, qui sont appelés suspension de cellules du SNC dans ce qui suit et pèsent environ 20 mg à 500 mg. Si la dissociation de plus d’une suspension de cellules du SNC est prévue, tous les volumes de réactifs et tous les matériaux doivent être mis à l’échelle en conséquence. Il est recommandé de conserver la solution saline tamponnée au phosphate de Dulbecco (D-PBS ; 1x) avec du calcium et du magnésium, complétée par 1 g/L de glucose et 36 mg/L de pyruvate de sodium) en continu sur de la glace pendant toute la durée de l’expérience. Si la culture cellulaire est prévue par la suite, effectuez toutes les étapes dans des conditions stériles en utilisant des hottes. Sinon, aucune des sections de protocole suivantes n’a besoin d’être exécutée sous un capot. Conservez les tampons sur de la glace. N’utilisez que des solutions pré-refroidies et évitez les vortex tout au long de l’expérience. Reportez-vous à la figure 1 pour connaître l’ensemble du flux de travail.
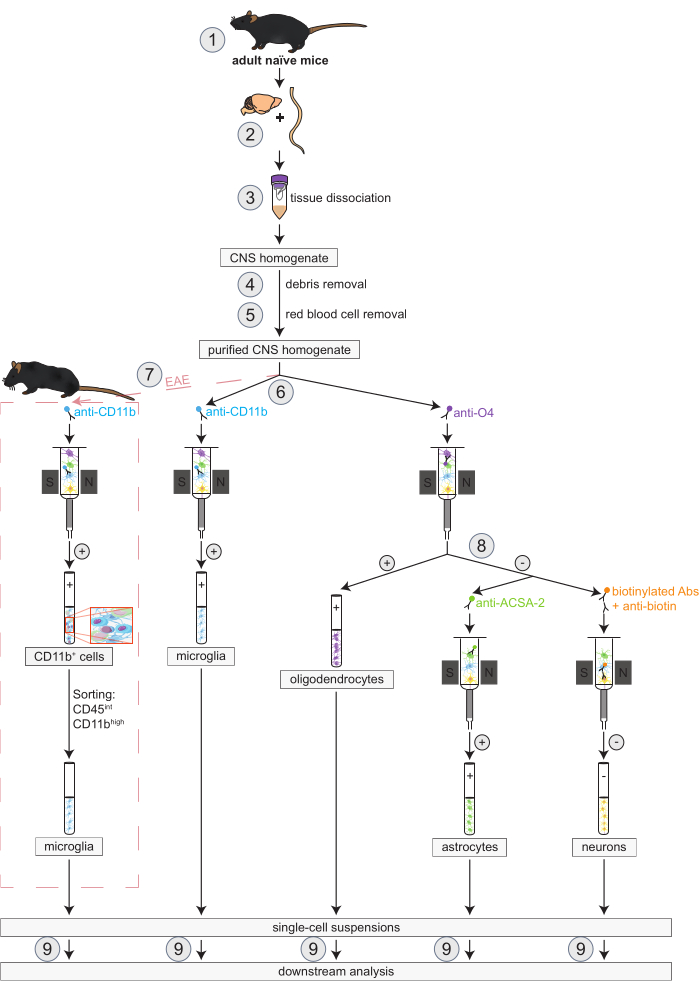
Figure 1 : Flux de travail pour l’isolement simultané d’oligodendrocytes, de microglies, d’astrocytes et de neurones chez des souris naïves et EAE. Les premières étapes du flux de travail sont les mêmes pour les souris naïves et EAE. Si l’on souhaite travailler avec une répétition EAE, l’induction EAE doit être effectuée au préalable (1). En bref, le protocole commence par la dissection (2) et la dissociation (3) du cerveau et de la moelle épinière murins, suivies de l’élimination des débris (4) et des globules rouges (5). Par la suite, la suspension de cellules du SNC purifiée qui en résulte est divisée en deux fractions pour l’isolement simultané des oligodendrocytes et de la microglie via MACS (6). Les microglies sont détectées à l’aide de microbilles anti-CD11b tandis que les oligodendrocytes sont isolés à l’aide de microbilles anti-O4 (sélections positives). À partir de l’écoulement négatif des oligodendrocytes (8), les astrocytes sont isolés via des microbilles anti-ACSA-2 (sélection positive) et des neurones par marquage à la biotine et épuisement de toutes les cellules non neuronales (sélection négative). Chez les souris EAE, l’isolement des cellules CD11b+ est suivi d’un tri cellulaire activé par fluorescence des cellules CD45intCD11bélevées afin d’éliminer d’autres cellules immunitaires CD11b+ telles que les macrophages, les cellules dendritiques, les monocytes, les granulocytes et les cellules tueuses naturelles connues pour participer aux processus de neuroinflammation au cours de l’évolution de l’EAE (7)27,28,48. Après l’isolement des différents types de cellules résidentes du SNC, des analyses de pureté peuvent être effectuées (9). Abréviations : Abs = anticorps ; ACSA-2 = antigène de surface des cellules astrocytaires-2 ; CD11b = kinase 11B dépendante de la cycline ; CD45 = tyrosine-protéine phosphatase C de type récepteur ; SNC = système nerveux central ; EAE = encéphalomyélite auto-immune expérimentale ; MACS = tri cellulaire activé par magnétisme ; O4 = marqueur oligodendrocytaire O4. Ce chiffre a été modifié par rapport à49. Veuillez cliquer ici pour voir une version agrandie de cette figure.
1. Induction de l’EAE actif
- Préparation des réactifs
- Pour la séparation cellulaire : Préparez le tampon PB et conservez-le à une température comprise entre 2 et 8 °C pendant 1 semaine maximum. Pour préparer la solution mère, ajouter 475 mL de 1x PBS sans suppléments (pH 7,2) + 25 mL d’albumine sérique bovine (BSA) à 0,5 %. Utilisez une dilution de 1 :20 préparée en BSA.
- Pour la cytométrie en flux et le tri cellulaire activé par fluorescence (FACS) : Préparez le tampon FACS, PBS avec 2 % de sérum de veau fœtal (FCS) et 2 mM d’EDTA et conservez-le à une température comprise entre 2 et 8 °C. Pour préparer, ajouter 500 mL de 1x PBS sans suppléments et 10 mL de FCS + 2 mL d’EDTA (à partir de 0,5 M de stock EDTA)
- Effectuer l’immunisation selon le protocole de Bittner et al. 5. En bref, induire l’EAE par injection sous-cutanée d’une émulsion contenant 200 μg de peptide MOG35-55 et 200 μL d’adjuvant de Freud complet dont 200 μg de Mycobacterium tuberculosis.
- Anesthésiez la souris avec de l’isoflurane à 2 % à l’aide d’une chambre d’anesthésie avec un vaporisateur d’isoflurane. Utilisez une pommade vétérinaire sur les yeux de l’animal pour prévenir la sécheresse sous anesthésie.
- Après 2 h, injecter une injection intrapéritonéale de 100 ng de toxine de la coqueluche (PTx) dissoute dans 100 μL de 1x PBS selon le protocole de Huntemann et al.24. Répétez l’injection de PTx le jour 2 après l’immunisation.
ATTENTION : Observez chaque animal jusqu’à ce qu’il ait retrouvé suffisamment de conscience pour maintenir le décubitus sternal. Les souris qui ont subi les procédures d’injection ne sont pas renvoyées en compagnie des autres souris tant qu’elles ne sont pas complètement rétablies. Pour Mycobacterium tuberculosis et PTx : Éviter l’inhalation, l’ingestion et le contact avec la peau et les yeux. Mycobacterium tuberculosis est un activateur du système immunitaire inné. Le PTx a de nombreux effets biologiques. - Surveiller quotidiennement la progression de l’EAE, effectuée par deux investigateurs en aveugle qui surveillent le poids et examinent cliniquement les souris.
- À cette fin, le système de notation suivant a été utilisé : grade 0 - aucun signe clinique d’EAE, grade 1 - parésie partielle de la queue, grade 2 - parésie complète de la queue, grade 3 - faiblesse modérée des membres postérieurs, grade 4 - faiblesse complète des membres postérieurs et démarche ataxique, grade 5 - paraparésie légère, grade 6 - paraparésie, grade 7 - paraplégie, grade 8 - tétrapparésie, grade 9 - tétraplégie, et 10e année – décès.
- Utilisez les critères d’exclusion suivants pour une participation ultérieure à l’expérience : score clinique > 7 ou perte de poids supérieure à 20 % du poids corporel initial.
- Pour la dissection du cerveau et de la moelle épinière, euthanasier les souris EAE le 16e jour après l’induction de l’EAE, ce qui représente le maximum de la maladie.
2. Préparation des tissus du SNC (durée : environ 10 min par souris)
- Après avoir sacrifié des souris avec du dioxyde de carbone, commencez par la perfusion transcardique de chaque souris avec 20 mL de 1x PBS. Répétez la perfusion avec 20 mL de 1x PBS.
- Placez la souris en décubitus dorsal et fixez les membres avec des canules. Appliquez de l’éthanol à 75 % sur le devant de l’animal. D’autres mesures de stérilité ne sont pas nécessaires à ce stade.
- Ouvrez l’abdomen et le thorax en faisant une coupe longitudinale à travers la peau et le fascia à l’aide d’un ciseau.
- Coupez les côtes latéralement et repliez le thorax pour avoir libre accès au cœur. Fixez le thorax plié vers le haut à l’aide de canules.
- Ouvrez l’oreillette droite à l’aide de ciseaux. Appliquer 20 mL de 1x PBS dans le ventricule gauche à l’aide d’une canule pour évacuer le sang par l’oreillette droite incisée.
- Exposez le crâne en coupant la peau sur le dessus de la tête murine via une section longitudinale et déplacez la peau autour de la tête à l’aide d’une pince. Inciser le crâne à l’aide d’un ciseau le long de la suture sagittale.
- Insérez la pointe d’une pince le long de la ligne d’incision pour ouvrir la calotte. Retirez les parties restantes de la calotte avec des pinces afin que le cerveau soit complètement exposé.
- Retirez le cerveau avec précaution et placez-le dans une matrice cérébrale murine. Coupez la cervelle en tranches sagittales de 1 mm d’épaisseur à l’aide d’une lame de rasoir.
- Coupez la colonne vertébrale à l’aide de ciseaux juste au-dessus de la crête iliaque afin que la seringue puisse être insérée dans le canal rachidien.
REMARQUE : Le moyen le plus simple d’enlever la moelle épinière est de l’évacuer du canal rachidien avec du PBS. Sinon, les arcs vertébraux doivent être ouverts individuellement avec des ciseaux, puis la moelle épinière peut être retirée. - Rincez la moelle épinière du canal rachidien de la caudale au crâne à l’aide d’une seringue de 20 ml avec une aiguille de 20 G contenant 1x PBS. Coupez la moelle épinière en segments de 0,5 cm de long à l’aide d’un scalpel.
- Conservez chaque suspension de cellules du SNC composée du cerveau et de la moelle épinière correspondante dans une boîte de Pétri distincte par souris remplie d’environ 3 mL de D-PBS froid. Conservez les plats sur de la glace jusqu’à ce qu’ils soient transformés.
3. Dissociation des tissus du SNC (Durée : environ 1 à 1,5 h selon le nombre de suspensions de cellules du SNC)
REMARQUE : Le tissu neural de souris adultes est dissocié en combinant la dissociation mécanique avec la dégradation enzymatique de la matrice extracellulaire. Ainsi, l’intégrité structurelle reste et la suspension cellulaire peut être utilisée pour d’autres procédures d’isolement cellulaire.
- Préparer le volume approprié du mélange enzymatique 1 composé de 50 μL d’enzyme P et de 1 900 μL de tampon Z par suspension de cellules du SNC. Les deux réactifs appartiennent au kit de dissociation cérébrale adulte.
- Préparer le volume approprié du mélange enzymatique 2 composé de 10 μL d’enzyme A et de 20 μL de tampon Y par suspension de cellules du SNC. Les deux réactifs appartiennent au kit de dissociation cérébrale adulte.
- Transférez 1 950 μL du mélange enzymatique 1 dans le tube C et ajoutez ensuite les morceaux de tissu d’une suspension de cellules du SNC. Utilisez un tube C par souris.
- Ajouter 30 μL de mélange enzymatique 2 dans chaque tube C. Fermez hermétiquement les tubes C et fixez-les à l’envers sur le manchon du dissociateur de cellule avec des éléments chauffants.
- Exécutez le programme approprié nommé 37C_ABDK_01 (prend 30 min). Observez au moins les 5 premières minutes du programme pour vous assurer que tous les tubes tournent à la même vitesse. L’apparition d’erreurs pendant l’exécution est possible. Ensuite, passez à l’étape 6.
- Dans les 2 dernières minutes du programme, placez une crépine de 70 μm sur un tube de 50 ml pour chaque suspension de cellules dissociées du SNC. Pré-humidifiez ces passoires avec 2 mL de D-PBS.
- Après la fin du programme, fixez les tubes C du dissociateur et placez-les dans une centrifugeuse. Centrifuger les échantillons à 300 x g et 4 °C pendant 1 min pour prélever l’échantillon au fond du tube.
- Remettre l’échantillon en suspension et l’appliquer sur la passoire pré-humidifiée. Ajouter 10 mL de D-PBS froid dans le tube C vide et le fermer. Secouez-le doucement et appliquez la suspension sur la passoire correspondante.
- Jetez les crépines et fermez les tubes de 50 ml. Centrifuger à nouveau la suspension cellulaire à 300 x g et 4 °C pendant 10 min. Ensuite, aspirez l’ensemble du surnageant très soigneusement.
4. Enlèvement des débris (durée : environ 1,5 à 2 h selon le nombre de suspensions de cellules du SNC)
REMARQUE : La dissociation tissulaire conduit souvent à la myéline et aux débris cellulaires qui peuvent nuire à l’analyse en aval. En ajoutant une solution d’élimination des débris, ces débris peuvent être efficacement éliminés de la suspension de la cellule du SNC.
- Remettre soigneusement la pastille cellulaire en suspension avec 3 100 μL de D-PBS pour chaque suspension de cellules du SNC. Ne pas vortex.
- Si vous travaillez avec plus d’une suspension de cellules du SNC, regroupez au maximum deux suspensions de cellules du SNC dérivées d’une condition ou d’un groupe expérimental dans un tube de 15 mL.
- Ajouter 900 μL de la solution d’élimination des débris de la trousse de dissociation cérébrale adulte à une suspension de cellules du SNC ou 1 800 μL de solution d’élimination des débris à deux suspensions de cellules du SNC regroupées.
- Retournez le tube et mélangez la suspension. Ensuite, recouvrez-le très doucement de 4 mL de D-PBS froid. Un dégradé clair doit être visible (figure 2A).
- Centrifuger les tubes pendant 10 min à 3000 x g et 4 °C avec une accélération complète et sans frein.
- Si la séparation se produit comme prévu, trois phases se forment (Figure 2C). Aspirez complètement les deux phases supérieures (Figure 2C-1,2) et jetez-les. Il est important qu’aucun résidu de myéline ne soit laissé (Figure 2E).
REMARQUE : Si le gradient n’a pas fonctionné et que les cellules sont nécessaires de toute urgence, n’aspirez pas les deux phases supérieures. Au lieu de cela, remplissez le tube de 15 mL avec du D-PBS froid jusqu’à 15 mL et retournez-le plusieurs fois. Centrifuger à nouveau à 1000 x g pendant 10 min à 4 °C avec une accélération complète et sans frein. Aspirez le surnageant et répétez les étapes 4.1 à 4.4. - Remplissez le tube de D-PBS froid jusqu’à 14 ml et fermez-le. Retournez puissamment le tube sur l’établi jusqu’à ce que la pastille de cellule se détache du fond du tube. Ne pas vortex.
- Centrifuger à nouveau l’échantillon à 1000 x g et 4 °C pendant 10 min. Réglez l’accélération et le freinage à fond. Aspirer le surnageant avec précaution et complètement.

Figure 2 : À faire et à ne pas faire lors de l’enlèvement des débris. (A) Exemple positif pour le gradient après recouvrement avec 4 mL de PBS. La phase supérieure, constituée de 4 mL de PBS, se distingue clairement de la phase inférieure, constituée de la suspension de la cellule du SNC avec la solution d’élimination des débris. (B) Exemple négatif pour le gradient après recouvrement avec 4 mL de PBS. Le gradient n’a pas de séparation claire entre le PBS et la suspension cellulaire en dessous. Une partie du PBS est diffusée dans la suspension cellulaire. (C) Exemple positif pour le gradient après centrifugation. Trois phases distinctes peuvent être facilement distinguées. Aucun résidu de myéline n’est visible dans la phase supérieure (1) ou inférieure (3) du gradient. La phase intermédiaire contient toute la myéline (2). La pastille de cellule est visible au fond du tube de 15 mL. (D) Exemple négatif pour le gradient après centrifugation. Il n’y a pas de séparation précise possible entre les trois phases. Des résidus de myéline sont visibles dans la phase supérieure (1) et inférieure (3) du gradient. (E) Exemple positif pour le gradient après aspiration des deux phases supérieures. L’échantillon obtenu ne contient que la pastille cellulaire et un surnageant clair au-dessus. Aucun résidu de myéline n’est laissé. (F) Exemple négatif pour le gradient après aspiration des deux phases supérieures. L’échantillon contient encore des résidus de myéline (flèche noire). Abréviations : SNC = système nerveux central ; PBS = solution saline tamponnée au phosphate Veuillez cliquer ici pour voir une version agrandie de cette figure.
5. Élimination des globules rouges (Durée : Environ 1 h selon le nombre de suspensions de cellules du SNC)
REMARQUE : Cette étape empêche la contamination ultérieure par les globules rouges et assure une lyse optimale des érythrocytes avec un effet minimal sur les autres types de cellules isolées du tissu du SNC. Les volumes suivants sont indiqués pour les suspensions cellulaires dérivées de 100 mg à 1 g de tissu neuronal correspondant à deux cerveaux et moelles épinières de souris adultes. Si vous travaillez avec plus de deux suspensions de cellules du SNC, augmentez la taille de tous les réactifs et des volumes totaux en conséquence.
- Commencez par la préparation de la solution d’élimination des globules rouges (RBCRS) : par deux suspensions de cellules du SNC regroupées. Diluer 100 μL de solution mère d’élimination des globules rouges (10x) du kit de dissociation cérébrale adulte dans 900 μL de ddH2O pour obtenir une dilution finale de 1 :10.
- Conservez le RBCRS à une température comprise entre 2 et 8 °C jusqu’à son utilisation. Jetez les restes inutilisés à la fin de la journée.
- Remettre en suspension la pastille cellulaire d’un maximum de deux suspensions de cellules du SNC dans 1 mL de RBCRS. Évitez les vortex. Incuber la solution pendant 10 min à 4 °C.
- Ajouter 10 mL de tampon PB froid à deux suspensions cellulaires groupées. Centrifuger l’échantillon à 300 x g et 4 °C pendant 10 min et aspirer complètement le surnageant par la suite.
- Remettre en suspension chaque pastille cellulaire d’une suspension de cellule du SNC dans 80 μL de tampon PB en pipetant lentement de haut en bas. Par conséquent, utiliser 160 μL pour remettre en suspension des pastilles cellulaires dérivées de deux suspensions de cellules du SNC.
- Lorsque vous travaillez avec plusieurs suspensions de cellules du SNC provenant de la même condition expérimentale, regroupez toutes ces suspensions cellulaires.
- Déterminer le nombre de cellules, par exemple à l’aide d’une chambre de comptage améliorée. Les suspensions cellulaires étaient généralement diluées à 1 :50 dans un tampon PB, suivies d’une dilution supplémentaire à 1 :10 dans une solution de bleu de trypan à 0,4 %.
6. Protocole de billes magnétiques chez les souris naïves et EAE (Durée : environ 1 h)
- Marquez magnétiquement les différents types de cellules du SNC avec des microbilles spécifiques à leur antigène de surface. Ensuite, placez la suspension cellulaire dans la colonne et séparez magnétiquement les cellules marquées retenues dans la colonne et les cellules non étiquetées qui la traversent.
- Après avoir retiré la colonne du champ magnétique, rincez les cellules marquées magnétiquement de la colonne dans un tube en tant que fraction cellulaire sélectionnée positivement.
REMARQUE : Les volumes pour le processus de marquage magnétique sont calculés pour un maximum de 1 x 107 cellules au total. Si vous obtenez plus de cellules, augmentez tous les volumes de réactifs et totaux en conséquence. Il est recommandé d’agir rapidement et de n’utiliser que des solutions pré-refroidies pour éviter le plafonnement des anticorps à la surface des cellules et le marquage cellulaire non spécifique, ainsi que pour assurer une viabilité élevée des populations cellulaires isolées. Il est également important d’effectuer les étapes de lavage dès que le réservoir de la colonne est vide en ajoutant le tampon PB afin que les colonnes ne se dessèchent pas. - Divisez la suspension de cellules du SNC purifiée non diluée en deux fractions pour les isolements suivants de la microglie et des oligodendrocytes. Le rapport des deux fractions dépend du nombre de cellules souhaité pour chaque type de cellule.
NOTA : De plus amples détails (durée de l’incubation, étapes détaillées du protocole, volumes, réactifs et méthode de numération cellulaire) sont indiqués dans le tableau 1.
Tableau 1 : Flux de travail pour le marquage magnétique simultané et l’isolement des oligodendrocytes et des microglies de souris naïves et EAE. Les deux types de cellules sont isolés par une sélection positive. Les étapes répertoriées sur la même ligne sont indiquées pour être exécutées en une seule fois. Abréviations : CD11b = kinase 11B dépendante de la cycline ; EAE = encéphalomyélite auto-immune expérimentale ; FcR = protéine de type récepteur Fc ; O4 = marqueur oligodendrocytaire O4. Veuillez cliquer ici pour télécharger ce tableau.
7. Modification du protocole : tri supplémentaire pour l’isolement de la microglie chez les souris EAE (Durée : environ 1,5-2 h)
REMARQUE : Lorsque l’on travaille avec des souris EAE, il est nécessaire de compléter le protocole d’isolement cellulaire basé sur MACS de FACS pour éliminer les populations de cellules CD11b+ autres que la microglie (par exemple, les monocytes, les macrophages, les cellules tueuses naturelles, les granulocytes ou les cellules dendritiques) de la fraction cellulaire CD11b+ . Dans le cas contraire, cette étape peut être ignorée.
- Préparer le mélange maître de coloration contenant 1x PBS complété par CD11b FITC (clone M1/70, 1 :50) et CD45 APC/Cy7 (clone 30-F11, 1 :200). Utiliser 100 μL de mélange maître de coloration par 5 x 106 cellules. Vortex tous les anticorps avant utilisation.
- Centrifuger la suspension de cellules microgliales à 300 x g et 4 °C pendant 10 min et aspirer le surnageant avec précaution.
- Remettre en suspension la pastille cellulaire avec 100 μL du mélange maître de coloration préparé par 5 x 106 cellules. Incuber pendant 15 min dans l’obscurité à température ambiante (RT).
- Arrêtez la réaction en ajoutant 500 μL de PBS et centrifuez à nouveau l’échantillon à 300 x g et 4 °C pendant 10 min.
- Aspirer le surnageant avec précaution et remettre en suspension la pastille cellulaire avec 1x PBS complété par 10 μg/mL d’ADN pour atteindre une concentration finale de 1 x 107 cellules par mL. Conservez les cellules à 4 °C jusqu’au début du tri.
- Appliquer la suspension cellulaire sur une crépine de 100 μm placée sur un nouveau tube FACS immédiatement avant de commencer le tri.
- Réglez le débit sur 1000 événements par seconde et utilisez la buse de 100 μm. Trier la population cellulaire souhaitée de cellules CD45intCD11bélevées dans un nouveau tube de 15 mL préparé avec 1x PBS à RT.
8. Préparation de l’écoulement négatif des oligodendrocytes pour l’isolement des neurones et des astrocytes (Durée : environ 1 h)
REMARQUE : Le flux négatif d’oligodendrocytes de l’étape 6 est collecté pour un isolement ultérieur des neurones et des astrocytes. À cette fin, la suspension cellulaire est divisée en deux parties. En raison de l’isolement préalable des oligodendrocytes à partir de la suspension des cellules du SNC, la contamination par les cellules O4+ est minimisée par rapport à ce qui aurait été observé autrement.
- Centrifuger le flux négatif des oligodendrocytes à 300 x g et 4 °C pendant 10 min et aspirer le surnageant avec précaution.
- Remettre en suspension la pastille cellulaire dans 80 μL de tampon PB par suspension cellulaire du SNC mise en commun précédemment utilisée pour l’isolement de la fraction positive des oligodendrocytes.
- Comptez les cellules. Effectuer le comptage des cellules supposées être O4- à l’aide d’une chambre de comptage améliorée après dilution de la suspension cellulaire 1 :50 dans un tampon PB suivi d’une dilution supplémentaire 1 :10 dans du bleu trypan à 0,4 %.
- Divisez la suspension cellulaire purifiée non diluée en deux fractions pour l’isolement simultané suivant des neurones et des astrocytes. Le rapport des deux fractions dépend de la quantité préférée de chaque type de cellule.
NOTA : De plus amples détails (durée de l’incubation, étapes détaillées du protocole, volumes, réactifs et méthode de numération cellulaire) sont indiqués dans le tableau 2.
Tableau 2 : Flux de travail pour le marquage magnétique simultané et l’isolement des neurones et des astrocytes chez les souris naïves et EAE. Les deux types de cellules sont isolés à partir du flux négatif des oligodendrocytes. Les astrocytes sont séparés par sélection positive par des microbilles anti-ACSA-2, tandis que les neurones sont purifiés par biotinylation et épuisement de toutes les cellules non neuronales par sélection négative. Les étapes répertoriées sur la même ligne sont indiquées pour être exécutées en une seule fois. Abréviations : Anti-ACSA-2 = antigène-2 de surface des cellules astrocytaires ; EAE = encéphalomyélite auto-immune expérimentale ; FcR = protéine de type récepteur Fc ; MACS = tri cellulaire activé par magnétisme. Veuillez cliquer ici pour télécharger ce tableau.
9. Analyses de pureté des types de cellules isolées résidant dans le SNC (Durée : environ 2 h)
REMARQUE : Il est recommandé d’effectuer une cytométrie en flux des quatre populations cellulaires isolées résidant dans le SNC pour mesurer et comparer leur pureté et leur viabilité. Par conséquent, il est nécessaire de colorer tous les types de cellules avec un anticorps marqué au fluorophore. La coloration des cellules vivantes/mortes est mise en œuvre à l’aide d’un colorant de viabilité fixable (1 :10 000).
- Panel de pureté - protocole de coloration extracellulaire
- Utiliser 1 x 105 cellules dissoutes dans 50 μL de PBS par coloration.
- Préparer le mélange maître de coloration dissous dans du PBS avec 2 % de FCS/2 mM d’EDTA constitué des anticorps monoclonaux conjugués au fluorochrome suivants ciblant des marqueurs de surface spécifiques au type cellulaire : CD11b FITC (clone 1/70, 1 :100)25,26,27,28, Biotine-PE (clone Bio3-18E7, 1 :200)29,30,31,32, ACSA-2 PE-Vio615 (clone REA-969, 1 :200)33,34,35, O4 APC (clone REA-576, 1 :400) et CD45 BV510 (clone 30-F11, 1 :150)36,37. Ajouter 1 μg d’anti-CD16/32 pour 1 x 106 cellules pour bloquer le récepteur Fc3 8,39. Vortex tous les anticorps avant utilisation.
- Centrifuger la suspension cellulaire pendant 5 min à 540 x g et 4 °C et aspirer le surnageant avec précaution.
- Remettre en suspension la pastille cellulaire dans 100 μL du mélange maître respectif et incuber l’échantillon pendant 15 min à RT dans l’obscurité.
- Laver les cellules avec 500 μL de 1x PBS avec 2% FCS/2 mM EDTA et centrifuger l’échantillon pendant 5 min à 540 x g et 4 °C.
- Aspirer le surnageant et remettre en suspension la pastille cellulaire avec 70 μL de 1x PBS avec 2 % de FCS/2 mM d’EDTA.
- Vortex l’échantillon pour dissocier complètement la pastille cellulaire. Par la suite, l’échantillon est prêt pour l’analyse par cytométrie en flux.
- Panel de pureté - protocole de coloration intracellulaire avec NeuN
- Utiliser 1 x 105 cellules de chaque population cellulaire pour la coloration intracellulaire de NeuN, qui est un marqueur nucléaire spécifique des neurones 40,41. C’est un moyen supplémentaire de colorer les neurones viables.
- Transférez 1 x 105 cellules de chaque population cellulaire dans un tube FACS. Ajouter 1 mL de PBS avec 2 % de FCS/2 mM d’EDTA par tube. Centrifuger les tubes à 540 x g et 4 °C pendant 5 min.
- Dans l’intervalle, préparer le mélange maître dissous dans du PBS avec 2 % de FCS/2 mM d’EDTA composé des anticorps monoclonaux conjugués au fluorochrome suivants ciblant des marqueurs de surface spécifiques au type cellulaire : CD11b FITC (clone M1/70, 1 :100)25,26,27,28, Biotine-PE (clone Bio3-18E7, 1 :200)29,30,31,32, ACSA-2 PE-Vio615 (clone REA-969, 1 :200)33,34,35 et CD45 BV510 (clone 30-F11, 1 :150)36,37.
- Aspirer le surnageant et remettre en suspension les cellules dans 100 μL du mélange maître préparé et incuber l’échantillon pendant 10 min à RT dans l’obscurité.
- Lavez les cellules avec 100 μL de PBS à 2 % de FCS/2 mM d’EDTA et centrifuez-les à nouveau à 540 x g et 4 °C pendant 5 min.
- Dans l’intervalle, préparer 200 μL de solution de fixation/perméabilisation : Ajouter 50 μL de la matière concentrée de concentré de fixation/perméabilisation à 150 μL de diluant de fixation/perméabilisation pour obtenir une dilution finale de 1 :4.
- Aspirer le surnageant et remettre les cellules en suspension dans 100 μL de solution de fixation/perméabilisation 1x. Incuber l’échantillon pendant 30 min à 4 °C.
- Dans l’intervalle, préparer 1 mL de tampon de perméabilisation/lavage 1x en ajoutant 100 μL de tampon de perméabilisation à 900 μL de ddH2O pour obtenir une dilution finale de 1 :10.
- Laver les cellules 1x avec 100 μL de tampon de perméabilisation/lavage 1x et centrifuger l’échantillon à 540 x g et 4 °C pendant 5 min.
- Dans l’intervalle, préparez un autre mélange maître dans un tampon de perméabilisation/lavage 1x composé uniquement de NeuN (NeuN AF647, clone EPR12763, 1 :200) et de 1 μg d’anti-CD16/32 par 106 cellules pour bloquer le récepteur Fc.
- Aspirer le surnageant. Remettre en suspension les cellules fixées et perméabilisées dans 50 μL du deuxième mélange maître et incuber pendant 30 min à 4 °C.
- Laver l’échantillon avec 100 μL de tampon de perméabilisation/lavage 1x et centrifuger à 540 x g et 4 °C pendant 5 min.
- Jeter le surnageant et remettre en suspension la pastille cellulaire dans 70 μL de PBS avec 2 % de FCS/2 mM d’EDTA. Par la suite, l’échantillon est prêt pour l’analyse par cytométrie en flux.
- Après avoir configuré le panneau sur le cytomètre en flux, acquérez des cellules pour l’analyse de pureté à l’aide d’un logiciel d’analyse par cytométrie en flux.
10. Analyse statistique
- Effectuer des analyses statistiques et concevoir des graphiques à l’aide d’un programme d’analyse graphique. Les données sont présentées sous forme de moyenne ± MEB.
Résultats Représentatifs
Le protocole actuel offre la possibilité d’isoler simultanément toutes les principales cellules résidentes du SNC, c’est-à-dire la microglie, les oligodendrocytes, les astrocytes et les neurones à partir d’une seule répétition du SNC. Ceci est important pour la réduction du nombre de souris nécessaires à ce type d’expériences et pour assurer la comparabilité des analyses moléculaires et biochimiques au niveau cellulaire. Si les différents types de cellules sont isolés à partir de différentes répétitions du SNC, les interactions cellulaires ne peuvent pas être cartographiées de manière véridique et des écarts techniques potentiels au cours des processus d’isolement pourraient biaiser d’autres analyses en aval. De plus, les résultats moléculaires et biochimiques de chaque type de cellule ne seraient pas comparables les uns aux autres, car ils ne sont pas dérivés du même contexte EAE. Un protocole MACS préexistant utilisant un système/kit commercial a été adapté pour permettre l’isolement simultané des types de cellules mentionnés ci-dessus.
L’isolement de la microglie a été réalisé à l’aide de microbilles anti-CD11b, les oligodendrocytes ont été isolés via des microbilles anti-O4 (tableau 1) et des microbilles anti-ACSA-2 ont été utilisées pour isoler les astrocytes (tableau 2). En revanche, l’isolement des neurones représente une sélection négative et a été réalisé par biotinylation et marquage magnétique de toutes les cellules non neuronales (tableau 2). Toutes les cellules non neuronales (p. ex., oligodendrocytes, microglies, astrocytes, cellules endothéliales et fibroblastes), à l’exception des cellules sanguines, peuvent être marquées magnétiquement à l’aide d’un anticorps conjugué à la biotine, spécifiquement dirigé contre un antigène de surface exprimé sur ces cellules non neuronales (tableau 2). Par épuisement de ces cellules non neuronales marquées magnétiquement, des populations de cellules neuronales hautement pures et viables peuvent être générées 30,42,43.
Deux nouveaux panels de cytométrie en flux ont été conçus pour les analyses de pureté des suspensions unicellulaires générées. Ici, des marqueurs de surface et nucléaires spécifiques au type de cellule, combinés à la discrimination des cellules vivantes et mortes, ont été utilisés.
Les rendements cellulaires obtenus par souris et par type de cellule (Figure 3A) ont été analysés et ont conduit à une moyenne de 8. 4 x 105 ± 3 x 104 microglies, 3,23 x 106 ± 1 x 105 oligodendrocytes, 8,6 x 105 ± 2 x 104 astrocytes, et 4,5 x 105 ± 1 x 104 neurones par souris naïve.
Dans le cadre de l’objectif d’étudier des modèles de maladies de neuroinflammation, le protocole a également été appliqué à un modèle murin d’EAE. Les souris ont été euthanasiées le 16e jour après l’induction de l’EAE, ce qui représente le maximum de la maladie. Dans ce contexte EAE, environ 2,9 x 106 ± 6,7 x 105 oligodendrocytes, 5,2 x 105 ± 9 x 104 astrocytes et 4,4 x 105 ± 4 x 104 neurones ont été isolés. Le rendement en cellules microgliales a été réduit à environ 1,7 x 105 ± 4 x 104 microglies par souris EAE en raison du tri cellulaire supplémentaire après les étapes MACS (Figure 3A).
Après isolement, les caractérisations phénotypiques des différentes populations cellulaires par cytométrie en flux ont montré qu’il était possible d’obtenir des suspensions unicellulaires viables d’une pureté d’environ 90 % pour tous les principaux types de cellules résidentes du SNC (Figure 3B). Les microglies ont été contrôlées comme étant CD45intCD11bélevé tel que défini dans la littérature 44,45,46,47.
Dans l’EAE, la microglie a dû être triée de toutes les cellules CD11b+ pour les différencier des autres cellules immunitaires CD11b+ comme les monocytes, les neutrophiles, les cellules tueuses naturelles, les granulocytes et les macrophages qui immigrent dans le SNC au cours de la neuroinflammation 27,28,48. Par conséquent, les microglies ont été triées en tant que cellules CD45intCD11 élevées à partir de la suspension cellulaire CD11b+. L’ensemble de la stratégie de tri des microglies est illustré à la figure 4. Chez les souris naïves, la population de microglies représentait 91,16 % de toutes les cellules vivantes (96 % de la population totale de CD11b+) (figure 4A). Chez les souris EAE, la population de microglies représentait 46,85 % de toutes les cellules vivantes (55 % de la population totale de CD11b+) (figure 4B). Bien que les procédures MACS et FACS appliquent des contraintes mécaniques aux cellules individuelles, 75,41 % ± 8,63 % des microglies purifiées triées étaient viables (figure 3B).
Les astrocytes et les neurones qui ont été directement isolés de la suspension initiale des cellules du SNC ont montré une contamination pertinente par les oligodendrocytes, ce qui a conduit à l’hypothèse que l’isolement simultané des neurones et des astrocytes du flux négatif des oligodendrocytes pourrait empêcher cette contamination. Les analyses de cytométrie en flux ont confirmé que les astrocytes isolés à partir de l’écoulement négatif des oligodendrocytes avaient une pureté de 89,23 % ± 2,78 % et ont démontré une viabilité de 80,56 % ± 1,41 %. À l’instar de ces résultats, la pureté des neurones isolés de la fraction cellulaire O4- était de 81,25 % ± 3,31 % et la viabilité était de 83,90 % ± 2,61 % (Figure 3B). Ces résultats confirment également que l’isolement simultané de ces deux types de cellules seulement après l’isolement des oligodendrocytes n’a pas d’impact sur la quantité de cellules fonctionnelles viables.
Les résultats concernant la viabilité et la pureté des suspensions unicellulaires isolées étaient très similaires chez les souris EAE par rapport à ceux reçus chez les souris naïves, confirmant que ce protocole convient aux souris saines ainsi que dans le contexte de l’EAE (Figure 3B).
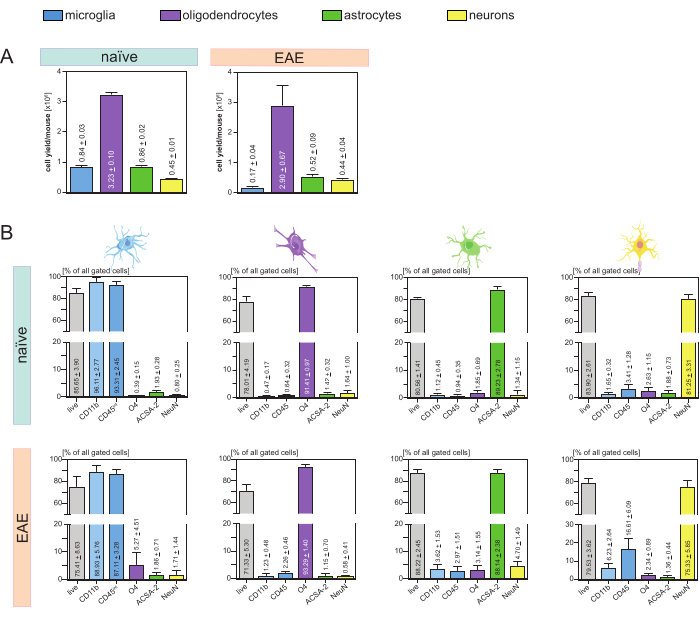
Figure 3 : Rendements cellulaires et validation par cytométrie en flux de cellules isolées résidentes du SNC. (A) Rendements cellulaires par souris et par type de cellule après isolement des cellules résidentes du SNC chez les souris naïves et EAE. Les graphiques à barres permettent de visualiser la quantité de rendements cellulaires par souris et par type de cellule après la mise en œuvre du protocole présenté. Cinq répétitions biologiques ont été traitées pour obtenir des résultats chez des souris naïves, et quatre répétitions biologiques ont été analysées chez des souris EAE. Les moyens respectifs ± SEM sont représentés. (B) Analyses correspondantes de la pureté et de la viabilité des fractions cellulaires purifiées. Les diagrammes à barres indiquent la viabilité et la pureté des suspensions unicellulaires résultantes en fonction de leur expression de marqueurs spécifiques au type de cellule. Le NeuN a été utilisé comme marqueur nucléaire spécifique au type cellulaire pour les neurones. Cinq répétitions biologiques ont été acquises et comparées pour chaque type de cellule, tant pour des souris saines que pour des souris EAE. Les moyens respectifs ± SEM sont indiqués. Abréviations : Anti-ACSA-2 = antigène-2 de surface des cellules astrocytaires ; CD11b = kinase 11B dépendante de la cycline ; CD45 = tyrosine-protéine phosphatase C de type récepteur ; SNC = système nerveux central ; EAE = encéphalomyélite auto-immune expérimentale ; MACS = tri cellulaire activé par magnétisme ; NeuN = protéine de liaison à l’ARN fox-1 homologue 3 ; O4 = marqueur oligodendrocytaire O4 ; SEM = erreur-type de la moyenne. Ce chiffre a été modifié par rapport à49. Veuillez cliquer ici pour voir une version agrandie de cette figure.
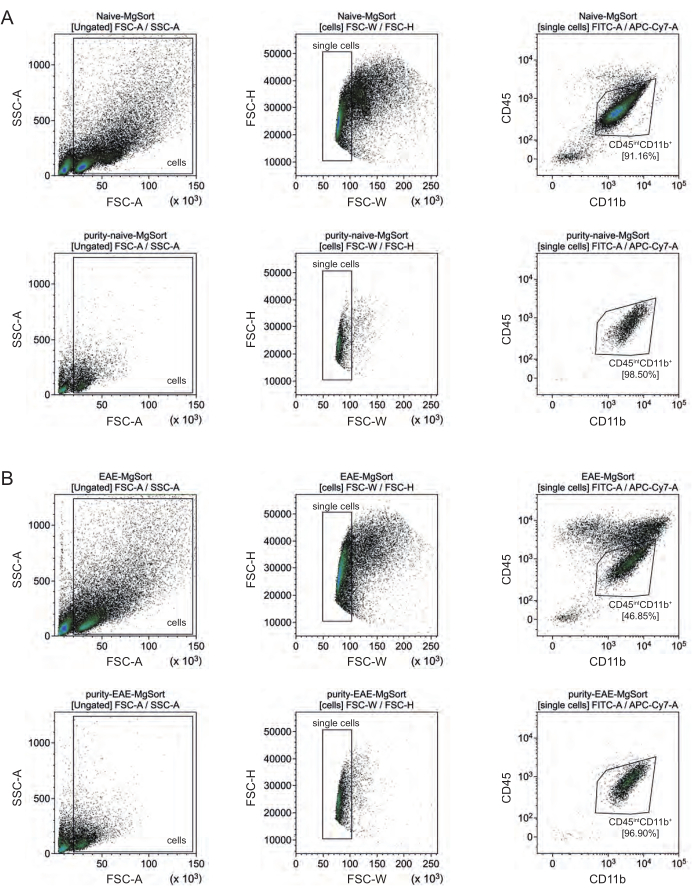
Figure 4 : Stratégie de déclenchement pour le tri cellulaire de la microglie après isolement des cellules CD11b+. (A) Stratégie de déclenchement chez les souris naïves et (B) EAE. La ligne supérieure de chaque panneau affiche des diagrammes à points avant le tri et la ligne inférieure après le tri. Après sélection de cellules vivantes (SSC-A / FSC-A) et de cellules individuelles (FCS-H / FSC-W), la population de cellules CD45intCD11b+ a été triée en population microgliale. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Discussion
Jusqu’à présent, les méthodes de cartographie ex vivo des cellules résidentes du SNC en combinant la spectrométrie de masse et le séquençage de l’ARN offrent un profilage cellulaire très précis dans la santé et la maladie, mais nécessitent des connaissances techniques et une expertise ambitieuses dans ce domaine50,51. De plus, ils ne permettent pas d’analyses fonctionnelles et sont très coûteux. En outre, les systèmes microfluidiques de cerveau sur puce permettent de dépister rapidement et à moindre coût les mécanismes de la maladie et de tester de nouvelles approches thérapeutiques avec la restriction de la croissance et de la migration cellulaires 52,53,54,55. Les organoïdes du SNC pourraient également représenter une alternative équivalente à l’avenir pour l’étude de la modélisation cellulaire, des connexions intercellulaires et des interactions au cours de l’évolution de la maladie 56,57,58,59. Cependant, le tri cellulaire activé par fluorescence et par magnétisme est actuellement la méthode la plus efficace pour générer des suspensions unicellulaires pures et viables ex vivo 35,60,61. Même si d’autres protocoles manufacturaux établis pour l’isolement des types de cellules résidentes du SNC sont similaires en ce qui concerne les étapes individuelles de l’isolement magnétique et de la dissociation cellulaire préalable, ils sont destinés à être effectués pour chaque type de cellule séparément. En revanche, le protocole actuel intègre différentes méthodes d’isolement pour chaque type de cellule résidente du SNC dans un contexte logique afin qu’elles puissent être effectuées simultanément à la fois et à partir d’une seule suspension de cellules du SNC (Tableau 1, Tableau 2). Ainsi, il permet des analyses multi-omiques à partir d’une seule suspension de cellules du SNC et, éventuellement, l’exploration de réseaux neuronaux complexes. Même s’il n’est pas indispensable de mettre en commun plusieurs tissus provenant de plusieurs animaux pour réaliser ce protocole, cette mise en commun permet d’assurer un nombre suffisant de cellules isolées pour une analyse ultérieure en aval. L’utilisation de souris différentes pour l’isolement des types de cellules individuelles exclurait la possibilité d’analyser les interactions cellulaires potentielles. En outre, la combinaison de méthodes d’isolement individuelles pour les différents types de cellules du SNC, qui suivent toutes une dissociation préalable du SNC, permet d’économiser des coûts matériels en utilisant une suspension de cellules dissociées du SNC pour toutes les étapes d’isolement magnétique suivantes. De plus, un biais technique potentiel causé par l’utilisation de souris différentes est minimisé.
L’une des limites du protocole pourrait être l’utilisation presque exclusive de souris femelles C57BL/6J. Le protocole d’immunisation EAE a été conçu et établi pour les souris femelles, de sorte que ce protocole d’isolement cellulaire a également été mis en œuvre chez les souris femelles C57BL/6J. Néanmoins, des souris mâles naïves ont également été utilisées lors du développement de ce protocole, sans reconnaître d’effet sur le nombre ou la pureté des cellules résultantes. Une autre restriction concerne l’isolement cellulaire magnétique des neurones car il n’existe pas de microbilles spécifiques pour l’isolement des neurones en termes de sélection positive. On a supposé qu’une suspension unicellulaire pure pouvait être obtenue par marquage à la biotine et épuisement de toutes les cellules non neuronales (tableau 2). Cette hypothèse a été vérifiée par l’utilisation de NeuN comme marqueur nucléaire spécifique pour les neurones, intégré dans le panel de pureté de la cytométrie en flux mentionné. Une autre limitation concerne l’isolement de la microglie chez les souris EAE. Ici, les rendements cellulaires qui en résultent sont diminués par rapport aux autres types de cellules en raison de l’étape de tri supplémentaire après le protocole MACS. De plus, on pourrait soutenir que le tri augmente le stress mécanique de la microglie par rapport aux autres populations cellulaires. Les stratégies de tri individuelles peuvent conduire à des rendements cellulaires différents. Si le nombre de cellules isolées est inférieur à ce qui est prévu ou souhaité, il est recommandé d’ajuster la configuration de la barrière et/ou d’améliorer la discrimination entre les cellules vivantes et mortes.
Une étape cruciale du protocole est l’enlèvement des débris. Le gradient doit être superposé très lentement et doucement pour créer les trois phases distinctes souhaitées (Figure 2A). Ce n’est que si la myéline et les autres résidus de débris dans les deux phases supérieures sont totalement éliminés (figure 2E) que des suspensions unicellulaires pures peuvent être générées et que la contamination peut être réduite. Si les suspensions cellulaires résultantes manquent de pureté, c’est probablement la partie du protocole qu’il faut améliorer en premier après l’assurance de la bonne utilisation de toutes les microbilles.
Recevoir des niveaux élevés de pureté et de viabilité peut être difficile dans ce type d’expérience. Voici quelques recommandations de dépannage :
-Le travail dans des conditions stériles est obligatoire pour éviter la contamination des différentes microbilles et permettre une utilisation répétée, en particulier pour la culture ultérieure.
-L’étiquetage de chaque tube pour éviter les confusions est fortement recommandé.
-Évitez l’utilisation de réactifs/tampons non refroidis. Conservez toutes les suspensions cellulaires sur de la glace pendant toute la durée de l’expérience pour assurer une viabilité élevée.
-Garder le temps entre les différentes étapes de travail aussi court que possible. Il n’y a pas de partie spécifique dans le protocole où il est recommandé de mettre l’expérience en pause.
-Il est très important de respecter les périodes d’incubation spécifiées.
En conclusion, ce protocole actuel pour l’isolement simultané de tous les principaux types de cellules résidentes du SNC à partir d’une réplique du SNC offre la possibilité d’analyser ex vivo des réseaux neuronaux complexes et des voies neuro-inflammatoires à partir d’une suspension de cellules du SNC. Ainsi, les cellules résidentes du SNC peuvent être étudiées à différents stades de l’évolution de la maladie, par exemple au cours de la neuroinflammation, de la neurodégénérescence et/ou de la rémission de l’EAE. De plus, les interactions cellule-cellule et les voies biochimiques peuvent être étudiées au niveau individuel et la variabilité au sein des groupes expérimentaux peut être réduite. Il est également possible de cultiver des fractions des cellules isolées du SNC en monoculture pour d’autres tests fonctionnels et une validation. Tout en un, ce protocole offre des avancées significatives pouvant affecter les approches de recherche préclinique et clinique.
Déclarations de divulgation
Tous les auteurs déclarent n’avoir aucun conflit d’intérêts.
Remerciements
Les figures ont été créées à l’aide d’Adobe Illustrator (version 2023) et de Servier Medical Art (https://smart.servier.com). Antonia Henes a reçu le soutien de la Jürgen Manchot Stiftung.
matériels
| Name | Company | Catalog Number | Comments |
| 70 μm cell strainers | Corning, MA, USA | 352350 | CNS tissue dissociation |
| ACSA-2 Antibody, anti-mouse, PE-Vio 615 (clone REA-969) | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-116-244 | Flow cytometry, store at 4 °C |
| Adult Brain Dissociation Kit, mouse, and rat | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-107-677 | Tissue dissociation,contains debris and red blood cell removal solutions; prepare aliquots of enzyme A and P upon arrival and store them at -20 °C; store the remaining kit at 4 °C |
| Anti-ACSA-2 MicroBead Kit, mouse | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-097-678 | MACS of astrocytes, store at 4 °C |
| Anti-mouse CD16/32 antibody | BioLegend, London, UK | 101301 | Flow cytometry, store at 4 °C |
| Anti-O4 MicroBeads, human, mouse, rat | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-094-543 | MACS of oligodendrocytes, store at 4 °C |
| AstroMACS Separation buffer | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-091-221 | MACS of astrocytes, store at 4 °C |
| Biotin Antibody, PE (clone Bio3-18E7) | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-113-853 | Flow cytometry, store at 4 °C |
| BRAND Neubauer counting chamber | Thermo Fisher Scientific,Waltham, MA, USA | 10195580 | Cell counting |
| Brilliant Violet 510 anti-mouse CD45 Antibody (clone 30-F11) | BioLegend, London, UK | 103137 | Flow cytometry, store at 4 °C |
| CD11b MicroBeads, human, mouse | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-049-601 | MACS of microglia, store at 4 °C |
| DNAse I, recombinant, Rnase-free | Merck KGaA, Darmstadt, Germany | 4716728001 | Flow cytometry, store at -20° C |
| D-PBS with Calcium, Magnesium, Glucose, Pyruvat | Thermo Fisher Scientific,Waltham, MA, USA | 14287080 | Buffer, store at 4 °C |
| D-PBS, without calcium, without magnesium | Thermo Fisher Scientific,Waltham, MA, USA | 14190250 | Buffer, store at 4 °C |
| eBioscience Fixable Viability Dye eFluor 780 | Thermo Fisher Scientific,Waltham, MA, USA | 65-0865-14 | Flow cytometry, store at 4 °C |
| eBioscience Foxp3/Transcription factor staining buffer set | Thermo Fisher Scientific,Waltham, MA, USA | 00-5523-00 | Flow cytometry, store at 4°C |
| Falcon (15 mL) | Thermo Fisher Scientific,Waltham, MA, USA | 11507411 | Cell tube |
| Falcon (50 mL) | Thermo Fisher Scientific,Waltham, MA, USA | 10788561 | Cell tube |
| Falcon Round-Bottom Polystyrene Test Tubes with Cell Strainer Snap Cap, 5 mL | Thermo Fisher Scientific,Waltham, MA, USA | 08-771-23 | Flow cytometry |
| FcR Blocking Reagent, mouse | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-092-575 | MACS of oligodendrocytes, store at 4 °C |
| Female C57BL/6J mice | Charles River Laboratories, Sulzfeld, Germany | Active EAE induction | |
| Fetal calf serum (FCS) | Merck KGaA, Darmstadt, Germany | F2442-50ML | Flow cytometry, store at -5 to -20 °C |
| FITC Rat Anti-CD 11b (clone M1/70) | BD Biosciences, San Jose, CA, USA | 553310 | Flow cytometry, store at 4 °C |
| Freund’s Complete adjuvant | Merck KGaA, Darmstadt, Germany | AR001 | Active EAE induction, store at 4 °C |
| GentleMACS C Tubes | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-093-237 | CNS tissue dissociation |
| GentleMACS Octo Dissociator with Heaters | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-096-427 | CNS tissue dissociation |
| Graphpad Prism 8.4.3 | Graphpad by Dotmatics | Graphical Analysis | |
| Isoflurane | AbbVie, North Chicago, IL, USA | Active EAE induction, store at 4 °C | |
| Kaluza Analysis Software V2.1.1 | Beckman Coulter, Indianapolis, IN, USA | Flow cytometry analysis | |
| LS Columns | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-042-401 | MACS |
| MACS BSA Stock Solution | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-091-376 | PB-buffer |
| MACS MultiStand | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-042-303 | MACS |
| MOG35–55 peptide | Charité, Berlin, Germany; alternatives: Genosphere Biotechnologies (Paris, France) or sb-Peptide (Saint Egrève, France) | Active EAE induction, store at -20 °C | |
| Mycobacterium tuberculosis strain H37 Ra | Becton, Dickinson and Company (BD),Franklin Lakes, NJ, USA | Active EAE induction, store at 4 °C | |
| Neuron Isolation Kit, mouse | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-115-390 | MACS of neurons, store at 4 °C |
| O4 Antibody, anti-human/mouse/rat, APC, (clone REA-576) | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-119-897 | Flow cytometry, store at 4 °C |
| Pertussis toxin in glycerol | Hooke Laboratories Inc., Lawrence, MA, USA | BT-0105 | Active EAE induction; store at -20 °C |
| pluriStrainer Mini 100 μm | pluriSelect Life Science UG, Leipzig, Sachsen, Germany | 43-10100-40 | Flow cytometry |
| QuadroMACS Separator | Miltenyi Biotec, Bergisch Gladbach, NRW, Germany | 130-090-976 | MACS |
| Recombinant Alexa Fluor 647 Anti-NeuN antibody (clone EPR12763) | Abcam, Cambridge, UK | EPR12763 | Flow cytometry, store at -20 °C |
| Stainless Steel Brain Matrices, 1 mm | Ted Pella, Redding, CA, USA | 15067 | CNS tissue dissection |
| Trypan blue solution, 0.4% | Thermo Fisher Scientific,Waltham, MA, USA | 15250061 | Cell counting |
| UltraPure 0.5 M EDTA, pH 8.0 | Thermo Fisher Scientific,Waltham, MA, USA | 15575020 | Flow cytometry, store at room temperature |
Références
- Trapp, B. D., Nave, K. A. Multiple Sclerosis: An Immune or Neurodegenerative Disorder. Annu Rev Neurosci. 31 (1), 247-269 (2008).
- Stys, P. K., Zamponi, G. W., van Minnen, J., Geurts, J. J. Will the real multiple sclerosis please stand up. Nat Rev Neurosci. 13 (7), 507-514 (2012).
- Korn, T. Pathophysiology of multiple sclerosis. J Neurol. 255 (Suppl 6), 2-6 (2008).
- Ward, M., Goldman, M. D. Epidemiology and Pathophysiology of Multiple Sclerosis. CONTINUUM. 28 (4), 988-1005 (2022).
- Bittner, S., Afzali, A. M., Wiendl, H., Meuth, S. G. Myelin Oligodendrocyte Glycoprotein (MOG35-55) Induced Experimental Autoimmune Encephalomyelitis (EAE) in C57BL/6 Mice. J Vis Exp. (86), 51275 (2014).
- Bittner, S., et al. The TASK1 channel inhibitor A293 shows efficacy in a mouse model of multiple sclerosis. Exp Neurol. 238 (2), 149-155 (2012).
- Göbel, K., et al. Plasma kallikrein modulates immune cell trafficking during neuroinflammation via PAR2 and bradykinin release. Proc Natl Acad Sci U S A. 116 (1), 271-276 (2019).
- Ballerini, C. Experimental Autoimmune Encephalomyelitis. Methods Mol Biol. 2285, 375-384 (2021).
- Birmpili, D., Charmarke Askar, I., Bigaut, K., Bagnard, D. The Translatability of Multiple Sclerosis Animal Models for Biomarkers Discovery and Their Clinical Use. Int J Mol Sci. 23 (19), 11532 (2022).
- Tsatas, O., Ghasemlou, N. Isolation and RNA purification of macrophages/microglia from the adult mouse spinal cord. J Immunol Methods. 477, 112678 (2020).
- Calvo, B., Rubio, F., Fernández, M., Tranque, P. Dissociation of neonatal and adult mice brain for simultaneous analysis of microglia, astrocytes and infiltrating lymphocytes by flow cytometry. IBRO Rep. 8, 36-47 (2020).
- Diaz-Amarilla, P., et al. Isolation and characterization of neurotoxic astrocytes derived from adult triple transgenic Alzheimer's disease mice. Neurochem Int. 159, 105403 (2022).
- Galatro, T. F., Vainchtein, I. D., Brouwer, N., Boddeke, E. W. G. M., Eggen, B. J. L. Isolation of Microglia and Immune Infiltrates from Mouse and Primate Central Nervous System. Methods Mol Biol. 1559, 333-342 (2017).
- Altendorfer, B., et al. Transcriptomic Profiling Identifies CD8+ T Cells in the Brain of Aged and Alzheimer's Disease Transgenic Mice as Tissue-Resident Memory T Cells. J Immunol. 209 (7), 1272-1285 (2022).
- Lanfranco, M. F., Sepulveda, J., Kopetsky, G., Rebeck, G. W. Expression and secretion of apoE isoforms in astrocytes and microglia during inflammation. Glia. 69 (6), 1478-1493 (2021).
- Swire, M., Ffrench-Constant, C. Oligodendrocyte-Neuron Myelinating Coculture. Methods Mol Biol. 1936, 111-128 (2019).
- Park, J., Koito, H., Li, J., Han, A. Microfluidic compartmentalized co-culture platform for CNS axon myelination research. Biomed Microdevices. 11 (6), 1145-1153 (2009).
- Facci, L., Barbierato, M., Skaper, S. D. Astrocyte/Microglia Cocultures as a Model to Study Neuroinflammation. Methods Mol Biol. 1727, 127-137 (2018).
- Speicher, A. M., Wiendl, H., Meuth, S. G., Pawlowski, M. Generating microglia from human pluripotent stem cells: novel in vitro models for the study of neurodegeneration. Mol Neurodegener. 14 (1), 46 (2019).
- Homayouni Moghadam, F., et al. Isolation and Culture of Embryonic Mouse Neural Stem Cells. J Vis Exp. (141), 58874 (2018).
- Santos, R., et al. Differentiation of Inflammation-Responsive Astrocytes from Glial Progenitors Generated from Human Induced Pluripotent Stem Cells. Stem Cell Reports. 8 (6), 1757-1769 (2017).
- Tcw, J., et al. An Efficient Platform for Astrocyte Differentiation from Human Induced Pluripotent Stem Cells. Stem Cell Reports. 9 (2), 600-614 (2017).
- Miltenyi, S., Müller, W., Weichel, W., Radbruch, A. High gradient magnetic cell separation with MACS. Cytometry. 11 (2), 231-238 (1990).
- Huntemann, N., et al. An optimized and validated protocol for inducing chronic experimental autoimmune encephalomyelitis in C57BL/6J mice. J Neurosci Methods. 367, 109443 (2022).
- Martin, E., El-Behi, M., Fontaine, B., Delarasse, C. Analysis of Microglia and Monocyte-derived Macrophages from the Central Nervous System by Flow Cytometry. J Vis Exp. (124), 55781 (2017).
- Sarkar, S., et al. Rapid and Refined CD11b Magnetic Isolation of Primary Microglia with Enhanced Purity and Versatility. J Vis Exp. (122), 55364 (2017).
- Rodríguez Murúa, S., Farez, M. F., Quintana, F. J. The Immune Response in Multiple Sclerosis. Annu Rev Pathol. 17, 121-139 (2021).
- Engelhardt, B., Ransohoff, R. M. Capture, crawl, cross: the T cell code to breach the blood-brain barriers. Trends Immunol. 33 (12), 579-589 (2012).
- Elia, G. Biotinylation reagents for the study of cell surface proteins. Proteomics. 8 (19), 4012-4024 (2008).
- Berl, S., et al. Enrichment and isolation of neurons from adult mouse brain for ex vivo analysis. J Neurosci Methods. 283, 15-22 (2017).
- Turvy, D. N., Blum, J. S. Biotin Labeling and Quantitation of Cell-Surface Proteins. Curr Protoc Immunol. 18 (7), (2001).
- Mao, S. Y. Biotinylation of Antibodies. Methods Mol Biol. 115, 39-41 (1999).
- Kantzer, C. G., et al. Anti-ACSA-2 defines a novel monoclonal antibody for prospective isolation of living neonatal and adult astrocytes. Glia. 65 (6), 990-1004 (2017).
- Batiuk, M. Y., et al. An immunoaffinity-based method for isolating ultrapure adult astrocytes based on ATP1B2 targeting by the ACSA-2 antibody. J Biol Chem. 292 (21), 8874-8891 (2017).
- Pan, J., Wan, J. Methodological comparison of FACS and MACS isolation of enriched microglia and astrocytes from mouse brain. J Immunol Methods. 486, 112834 (2020).
- Donovan, J. A., Koretzky, G. A. CD45 and the immune response. J Am Soc Nephrol. 4 (4), 976-985 (1993).
- Hathcock, K. S., Hirano, H., Hodes, R. J. CD45 expression by murine B cells and T cells: Alteration of CD45 isoforms in subpopulations of activated B cells. Immunol Res. 12 (1), 21-36 (1993).
- Balogh, P., Tew, J. G., Szakal, A. K. Simultaneous blockade of Fc? receptors and indirect labeling of mouse lymphocytes by the selective detection of allotype-restricted epitopes on the kappa chain of rat monoclonal antibodies. Cytometry. 47 (2), 107-110 (2002).
- Becerril-García, M. A., et al. Langerhans Cells From Mice at Birth Express Endocytic- and Pattern Recognition-Receptors, Migrate to Draining Lymph Nodes Ferrying Antigen and Activate Neonatal T Cells in vivo. Front Immunol. 11, 744 (2020).
- Dent, M. A., Segura-Anaya, E., Alva-Medina, J., Aranda-Anzaldo, A. NeuN/Fox-3 is an intrinsic component of the neuronal nuclear matrix. FEBS Lett. 584 (13), 2767-2771 (2010).
- Duan, W., et al. Novel Insights into NeuN: from Neuronal Marker to Splicing Regulator. Mol Neurobiol. 53 (3), 1637-1647 (2016).
- Monteiro, R., Sivasubramanian, M. K., Balasubramanian, P., Subramanian, M. Obesity-Induced Sympathoexcitation is Associated with Glial Senescence in the Brainstem. FASEB J. 34 (S1), 1-1 (2020).
- Li, S., Chang, L., Teissie, J. . Electroporation protocols: mircroorganism, mammalian system, and nanodevice. , (2020).
- Kettenmann, H., Hanisch, U. K., Noda, M., Verkhratsky, A. Physiology of Microglia. Physiol Rev. 91 (2), 461-553 (2011).
- Haage, V., et al. Comprehensive gene expression meta-analysis identifies signature genes that distinguish microglia from peripheral monocytes/macrophages in health and glioma. Acta Neuropathol Commun. 7 (1), 20 (2019).
- Kosior, N., Petkau, T. L., Connolly, C., Lu, G., Leavitt, B. R. Isolating cells from adult murine brain for validation of cell-type specific cre-mediated deletion. J Neurosci Methods. 328, 108422 (2019).
- Jurga, A. M., Paleczna, M., Kuter, K. Z. Overview of General and Discriminating Markers of Differential Microglia Phenotypes. Front Cell Neurosci. 14, 198 (2020).
- Man, S., Ubogu, E. E., Ransohoff, R. M. Inflammatory Cell Migration into the Central Nervous System: A Few New Twists on an Old Tale. Brain Pathol. 17 (2), 243-250 (2007).
- Schroeter, C. B., et al. One Brain-All Cells: A Comprehensive Protocol to Isolate All Principal CNS-Resident Cell Types from Brain and Spinal Cord of Adult Healthy and EAE Mice. Cells. 10 (3), 651 (2021).
- Sankowski, R., et al. Mapping microglia states in the human brain through the integration of high-dimensional techniques. Nate Neurosci. 22 (12), 2098-2110 (2019).
- Brennan, F. H., et al. Microglia coordinate cellular interactions during spinal cord repair in mice. Nat Commun. 13 (1), 4096 (2022).
- Enright, H. A., et al. Functional and transcriptional characterization of complex neuronal co-cultures. Sci Rep. 10 (1), 11007 (2020).
- Mofazzal Jahromi, M. A., et al. Microfluidic Brain-on-a-Chip: Perspectives for Mimicking Neural System Disorders. Mol Neurobiol. 56 (12), 8489-8512 (2019).
- Chin, E., Goh, E. Blood-brain barrier on a chip. Methods Cell Biol. 146, 159-182 (2018).
- Miccoli, B., Braeken, D., Li, Y. E. Brain-on-a-chip Devices for Drug Screening and Disease Modeling Applications. Curr Pharm Des. 24 (45), 5419-5436 (2019).
- Giandomenico, S. L., et al. Cerebral organoids at the air-liquid interface generate diverse nerve tracts with functional output. Nat Neurosci. 22 (4), 669-679 (2019).
- Pellegrini, L., et al. Human CNS barrier-forming organoids with cerebrospinal fluid production. Science. 369 (6500), eaaz5626 (2020).
- Chhibber, T., et al. CNS organoids: an innovative tool for neurological disease modeling and drug neurotoxicity screening. Drug Discov Today. 25 (2), 456-465 (2020).
- Tang, X. Y., et al. Human organoids in basic research and clinical applications. Signal Transduct TargetTher. 7 (1), 168 (2022).
- Sutermaster, B. A., Darling, E. M. Considerations for high-yield, high-throughput cell enrichment: fluorescence versus magnetic sorting. Sci Rep. 9 (1), 227 (2019).
- Doughty, D., et al. Development of a novel purification protocol to isolate and identify brain microglia. Exp Biol Med. 247 (16), 1433-1446 (2022).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon