Un abonnement à JoVE est nécessaire pour voir ce contenu. Connectez-vous ou commencez votre essai gratuit.
Un modèle photopolymérisable d’acide hyaluronique-collagène du microenvironnement invasif du gliome avec flux interstitiel
Dans cet article
Résumé
Nous présentons une méthode de réplication du microenvironnement tumoral du gliome sur le front invasif qui intègre le flux de liquide interstitiel. Ce modèle est un hydrogel hyaluronane-collagène I dans un insert de culture tissulaire où une tête de pression de fluide peut être appliquée. L’invasion peut être quantifiée et les cellules peuvent être isolées ou lysées.
Résumé
La récidive du glioblastome est un obstacle majeur au succès du traitement et est due à l’invasion de cellules souches de gliome (CSG) dans les tissus sains qui sont inaccessibles à la résection chirurgicale et résistent aux chimiothérapies existantes. Le mouvement du fluide au niveau des tissus, ou écoulement de fluide interstitiel (IFF), régule l’invasion de la GSC d’une manière dépendante du microenvironnement tumoral (TME), soulignant la nécessité de systèmes modèles qui intègrent à la fois l’IFF et le TME. Nous présentons une méthode accessible pour reproduire l’EUT invasif dans le glioblastome : un hydrogel hyaluronane-collagène I composé de CSG humaines, d’astrocytes et de microglies ensemencées dans un insert de culture tissulaire. Un IFF élevé peut être représenté par l’application d’une tête de pression de fluide sur l’hydrogel. De plus, ce modèle peut être réglé pour reproduire les différences inter ou intra-patients dans les rapports cellulaires, les débits ou les rigidités matricielles. L’invasion peut être quantifiée, tandis que les gels peuvent être récoltés pour divers résultats, notamment l’invasion de la GSC, la cytométrie en flux, l’extraction de protéines ou d’ARN ou l’imagerie.
Introduction
Le glioblastome est une maladie dévastatrice, caractérisée par une courte survie1 qui n’est prolongée que modérément par les traitements cliniquement disponibles 2,3. Cet obstacle à un traitement efficace est en grande partie dû à la nature hautement infiltrante des cellules souches de gliome chimiorésistantes (CSG) qui sont inaccessibles à la résection et à l’ensemencement de tumeurs récurrentes4. Parallèlement, les GSC sont très plastiques, répondant à divers stimuli dans le microenvironnement tumoral (TME) afin de survivre et d’envahir 5,6. Plus précisément, la tumeur densément peuplée et le système vasculaire perméable produisent une forte différence de pression à la limite de la tumeur, augmentant le flux de liquide interstitiel (IFF) dans des régions distinctes qui sont en corrélation avec l’invasion de la GSC7. Cette augmentation de l’IFF influence 8,9,10 et augmente souvent l’invasion de la GSC 8,9 via des voies moléculaires qui se prêtent à l’inhibition pharmacologique. Cependant, ce processus est confondu par l’influence de la glie dans l’EUT sur l’invasion du gliome ; en effet, il a été décrit que la glie module l’invasion du gliome dans de nombreux contextes11, et des preuves préliminaires dans notre laboratoire indiquent une influence similaire de la glie sur l’invasion du gliome améliorée par l’IFF12. Ainsi, notre laboratoire a développé un modèle TME 3D accordable qui réplique ces régions frontalières tumorales invasives en incorporant à la fois les interactions IFF et glia-GSC pour quantifier l’invasion de la GSC et d’autres résultats (c’est-à-dire l’expression des protéines de surface ou intracellulaires, l’expression de l’ARN, etc.) influencés par les IFF, les cellules gliales et/ou les thérapeutiques candidates12 (Figure 1).
Le modèle TME est similaire à d’autres tests d’écoulement de fluide interstitiel basés sur des inserts de culture tissulaire (c’est-à-dire des tests statiques/d’écoulement) qui ont été largement publiés 8,9,10,13,14,15,16,17,18. Les principales distinctions de ce modèle sont l’incorporation d’une matrice collagène-acide hyaluronique non exclusive et accordable, l’inclusion d’astrocytes et de microglies dans la matrice à des ratios représentatifs des TME des patients12, et le système est entièrement enfermé dans une plaque à puits, sans tube externe, réservoir ou pompe. L’acide hyaluronique est l’un des principaux composants de la matrice extracellulaire du cerveau19, mais il n’est pas suffisant pour permettre la circulation des fluides ; ainsi, le collagène I est inclus dans le mélange. La réticulation se produit en deux étapes : une polymérisation en chaîne initiée par les radicaux libres où, lors de l’exposition à la lumière ultraviolette (UV), des radicaux libres sont produits à partir du photoinitiateur et génèrent des réticulations chimiques entre les molécules d’acide hyaluronique méthacrylées20, et la neutralisation du collagène préservé à l’acide et l’exposition à la chaleur pour former des fibres de collagène 21,22,23.
Divers paramètres qui ont été optimisés pour ce test ont été décrits dans des travaux précédemment publiés dans des hydrogels d’hyaluronane-collagène modifiés au thiol 8,12. Plus précisément, les cellules (CSG24 humaines primaires, astrocytes corticaux humains primaires et microglie humaine immortalisée) utilisées pour ce test sont viables à au moins 60 % pendant 3 jours dans des gels composés de milieux astrobasaux complétés par des facteurs de croissance GSC, 0,5 % v/v N-2 et 1 % v/v B-27 sans vitamine A12. Dans les cas où les gels doivent être dégradés (par exemple, pour l’extraction de protéines ou la cytométrie en flux), la collagénase et la dispase sont utilisées et maintiennent une viabilité suffisante (Figure 2).
Pour quantifier l’invasion, les GSCs doivent être marquées par fluorescence avant d’être combinées avec la glie dans la matrice. Cela peut être réalisé par marquage avec Hoechst 33342 (comme décrit ci-dessous), des traqueurs de cellules12, une modification génétique ou une transduction. Quoi qu’il en soit, la viabilité des cellules marquées avec de nouveaux marqueurs doit être mesurée avant de les incorporer dans le modèle TME. Par ailleurs, si l’invasion n’est pas quantifiée mais que les gels sont récoltés pour des extractions de protéines, des extractions d’ARN ou d’autres résultats, les cellules n’ont souvent pas besoin d’être marquées par fluorescence pendant le processus de préparation du gel. Dans ce cas, les gels peuvent être soit fixés au formol pour l’imagerie, dégradés et les cellules lysées pour l’extraction de l’ARN, soit dégradés à l’aide de protéases pour la cytométrie en flux, puis lysés avec des tampons de lyse protéique pour les transferts Western ou d’autres travaux protéiques.
Ici, nous présentons un protocole pour incorporer des astrocytes humains, des microglies et des CSG dérivées du patient dans un rapport défini par le patient, 4:1:112, dans une matrice de collagène I de 1,2 mg/mL, 4 mg/mL d’hyaluronane dans des conditions statiques d’écoulement. Les paramètres spécifiques utilisés pour un essai (c.-à-d. les rapports cellulaires, la rigidité, les types de cellules, etc.) peuvent être modifiés pour représenter différents contextes si la viabilité est adéquate.
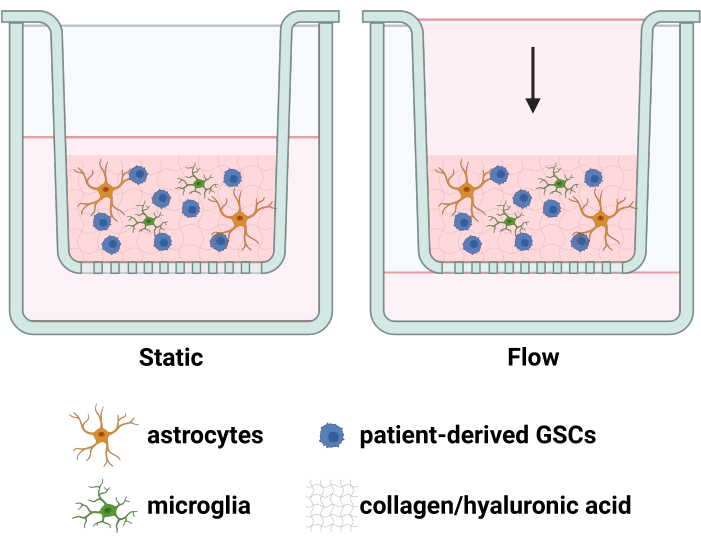
Figure 1 : Schéma du modèle TME composé de GSC, d’astrocytes et de microglies dans un hydrogel sous une charge de pression de fluide. Les cellules sont intégrées dans un hydrogel de collagène-acide hyaluronique à l’intérieur d’un insert de culture tissulaire. La force gravitationnelle entraîne l’écoulement net vers le bas. Les pores de la membrane de l’insert de culture tissulaire permettent aux cellules envahissantes vers le bas de se fixer à la surface inférieure de l’insert de culture tissulaire, et ces cellules peuvent être fixées, imagées et quantifiées. Créé avec BioRender.com. Veuillez cliquer ici pour voir une version agrandie de cette figure.
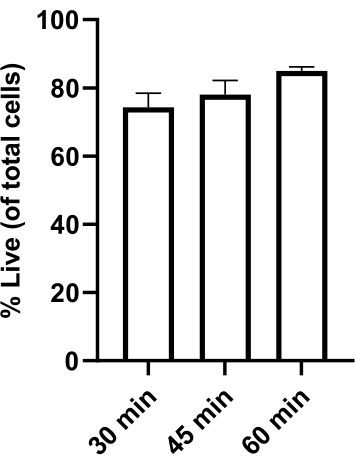
Figure 2 : Viabilité cellulaire après dégradation de l’hydrogel. Les G34 (GSC), les astrocytes et les microglies ont été ensemencés dans le modèle TME à 4:1:1 et incubés pendant 21 h à 37 °C. Les gels ont été retirés et dégradés à l’aide de 0,3 mg/mL de collagénase + 0,02 mg/mL de dispase pour un total de 30, 45 ou 60 min, en pipetant pour mélanger toutes les 15 minutes (condition de 30 minutes) ou à 30 minutes puis toutes les 15 minutes (conditions de 45 minutes et 60 minutes). Après la dégradation des gels, les cellules ont été colorées à l’orange acridine (toutes les cellules) et à l’iodure de propidium (cellules mortes) et comptées à l’aide d’un compteur de cellules automatisé. La viabilité est rapportée pour toutes les cellules du modèle TME. Les cellules ont maintenu une viabilité d’au moins 70 % pendant 30 à 60 minutes. Les données sont présentées sous forme de ± moyenne SEM ; n = 3 répétitions biologiques. Veuillez cliquer ici pour voir une version agrandie de cette figure.
Protocole
Ce protocole a été élaboré conformément aux directives établies par le comité institutionnel de biosécurité de Virginia Tech.
REMARQUE : Effectuez toutes les procédures dans une armoire de culture cellulaire BSL-2, sauf indication contraire. Veuillez consulter le comité de biosécurité de l’établissement pour obtenir des conseils sur l’utilisation des cellules humaines.
1. Calculs pour la préparation du gel
- Calculez le nombre de conditions nécessaires à l’expérience.
REMARQUE : Une « condition » est définie par le contenu de la solution (par exemple, les concentrations de cellules, les concentrations de collagène, etc.), et non par des variables appliquées de l’extérieur, comme la tête de pression du fluide utilisée dans cet exemple. - Calculez le volume total de gel nécessaire pour chaque solution de condition.
REMARQUE : Le volume requis pour les gels à 12 puits qui utilisent des inserts de culture tissulaire de 12 mm de diamètre est de 100 à 150 μL par insert. Au moins trois répétitions techniques sont recommandées pour quantifier l’invasion. De plus, pour tenir compte de la perte de volume due à une erreur de pipetage, ajoutez le volume d’une réplique supplémentaire à chaque solution de condition. - Calculer le volume total de solution de gel requis pour l’expérience à partir de l’étape 1.2.
- Calculez le volume total de solution de collagène de 3 mg/mL requis pour l’expérience. Ajoutez au moins 10 % à ce volume pour tenir compte de la perte de volume lors du pipetage.
Volume total 3 mg/mL de collagène = 0,4 × Volume total de la solution de gel - Calculez les volumes de collagène de queue de rat I à haute concentration, de NaOH 1 N stérile, de PBS 10x stérile et d’eau stérile pour chaque composant de la solution de collagène à 3 mg/mL aux concentrations finales données (cf) : collagène I cf = 3 mg/mL, NaOH cf = 2,3 % v/v du volume de collagène I et PBS cf = 1x. Diluer les solutions dans de l’eau stérile ultrapure (18,2 MΩ·cm).
- Calculer les volumes d’une solution de collagène à 3 mg/mL, d’acide hyaluronique méthacrylé à 1 % p/v et du photoinitiateur, le phényl-2,4,6-triméthylbenzoylphosphinate de lithium (LAP) à 17 mg/mL, et des milieux de culture cellulaire pour chacune des solutions d’affection aux concentrations finales données (cf) : collagène cf = 1,2 mg/mL, acide hyaluronique cf = 0,4 % p/v, LAP cf = 2% v/v du volume d’acide hyaluronique. Diluer les solutions dans des milieux de culture cellulaire contenant des cellules.
- Calculez le nombre de cellules pour chaque solution d’affection selon le rapport souhaité (p. ex., 100 000 GSC pour 100 μL d’hydrogel dans un rapport de 4:1:1 GSCs :astrocytes :microglie).
2. Préparation des matériaux
- Dans la semaine précédant l’expérience, les GSCs, les astrocytes et les microglies ont été mis en plaques.
REMARQUE : La plaque doit produire environ le double du nombre de cellules nécessaire pour les gels afin de tenir compte à la fois du passage et de la perte de cellules pendant la procédure. - Préparer une solution de travail du photoinitiateur, le LAP, à 17 mg/mL dans du PBS stérile 1x. Protégez-le de la lumière.
- Reconstituer l’acide hyaluronique méthacrylé dans 1x PBS selon les instructions du fabricant. Fermez le couvercle et secouez doucement la suspension pendant 1 h, ou jusqu’à ce qu’elle soit dissoute, à 4 °C.
REMARQUE : L’acide hyaluronique méthacrylé utilisé dans ce protocole est stable pendant environ 1 mois à 4 °C comme spécifié par le fabricant. Protégez-le de la lumière. - Installez une lampe UV à l’aide d’une diode électroluminescente (LED) collimatée d’une longueur d’onde nominale de 385 nm à une intensité de 50 mW/cm2 à la surface du gel. Placez la lampe dans l’armoire de culture cellulaire.
ATTENTION : La lumière UV peut endommager les yeux. Portez des lunettes de protection et ne regardez pas directement dans la lampe.
REMARQUE : Effectuer des expériences distinctes pour s’assurer que la viabilité ou le résultat fonctionnel mesuré n’est pas significativement affecté par une exposition à la lumière de 385 nm à 50 mW/cm2 sur la période d’exposition (45 s). - Préparez le milieu (milieu astrobasal + 0,5 % v/v N-2 + 1 % v/v B-27 sans vitamine A) pour l’expérience.
REMARQUE : Combinez les composants du média et filtrez à travers un système d’aspiration des pores de 0,22 μm pour assurer la stérilité. Éviter les cycles de gel-dégel des facteurs de croissance (N-2 et B-27) pour prévenir la dégradation. - Préparez 1 N NaOH dans une hotte avec le pare-éclaboussures en place.
ATTENTION : Le 1 N NaOH est très corrosif. Manipulez-le avec soin, portez des lunettes de protection ou utilisez un pare-éclaboussures et conservez la solution sous une hotte. - Préparez de l’eau stérile ultrapure (18,2 MΩ·cm).
3. Passage des cellules et marquage des GSC
- Passage des astrocytes, des microglies et des GSCs selon les instructions du fabricant.
- Étiqueter les GSC avec Hoechst 33342 en suivant les recommandations du fabricant.
ATTENTION : Hoescht 33342 peut provoquer une irritation oculaire grave et peut induire des dommages à l’ADN. Manipulez avec précaution. - Centrifuger toutes les cellules à 200 x g pendant 5 min à RT.
- Videz doucement le surnageant et retirez l’excédent de milieu à l’aide d’une pipette.
- Suspendez à nouveau les GSC dans 1x PBS.
- Centrifuger les GSC à 200 x g pendant 5 min.
- Remettre en suspension toutes les cellules dans le milieu (milieu astrobasal + 0,5 % N-2 v/v + 1 % v/v B-27) pour l’expérience.
- Comptez toutes les cellules.
- Ajoutez le nombre absolu de cellules nécessaires pour chaque solution d’affection dans un flacon par solution d’affection. Placez-les à 37 °C, 5% CO2 jusqu’à utilisation.
4. Préparation des hydrogels
REMARQUE : Effectuez les étapes après avoir ouvert l’acide hyaluronique méthacrylé et le photo-initiateur dans l’obscurité jusqu’à ce que les gels aient été photo-réticulés.
- Placez le collagène 8-11 mg/mL (haute concentration), le NaOH 1 N, l’eau ultra-pure stérile (18,2 MΩ·cm), le PBS stérile 10x, un tube de microcentrifugation (pour la solution de collagène 3 mg/mL), l’acide hyaluronique méthacrylé et le photoinitiateur sur de la glace.
REMARQUE : Tous les matériaux qui entrent en contact avec la solution de collagène doivent être conservés sur de la glace pour éviter une réticulation prématurée. - Placez les inserts de culture tissulaire dans la plaque et étiquetez la plaque.
- À l’aide des valeurs calculées, préparez la solution de collagène à 3 mg/mL en combinant du collagène à haute concentration, du 1 N NaOH, de l’eau ultrapure (18,2 MΩ·cm) et 10x PBS. Ajoutez les composants goutte à goutte et maintenez la pointe de la pipette immergée lors du mélange pour éviter la formation de bulles.
REMARQUE : Si des bulles se forment, la centrifugation ou le tapotement du tube sur une surface dure élimine souvent les bulles. De plus, les milieux contenant du rouge de phénol seront jaunes si le pH est trop acide ; plus de NaOH devrait être ajouté dans ce cas. - Cellules de centrifugation à 200 x g pendant 5 min à RT.
- Retirez délicatement l’excès de milieu du haut de chaque solution d’affection cellulaire, en laissant le volume de média requis pour l’affection. Placez ces solutions sur de la glace.
REMARQUE : Ne transférez pas les cellules hors de ce flacon pour éviter la perte de cellules. Au lieu de cela, ajoutez tous les composants de l’état du gel dans ce flacon, puis mélangez doucement et répartissez les gels dans la plaque. - Ajouter le volume calculé de solution de collagène de 3 mg/mL pour une concentration finale de 1,2 mg/mL à chaque solution d’état cellulaire à partir de l’étape 4.5.
- Ajouter le volume calculé d’acide hyaluronique méthacrylé à 1 % p/v pour une concentration finale de 0,4 % p/v à chaque solution d’état cellulaire à partir de l’étape 4.5.
- Ajouter le volume calculé de 17 mg/mL de LAP à chaque solution d’état cellulaire à partir de l’étape 4.5.
REMARQUE : Ajouter cette solution juste avant de distribuer les gels dans la plaque pour maximiser la viabilité ; Le LAP sous forme liquide est cytotoxique. - Un à la fois, mélangez chaque tube de condition et ajoutez 100 à 150 μL dans chaque insert de culture tissulaire. Gardez la pointe de la pipette immergée pour éviter la formation de bulles.
- Allumez la lampe UV de 385 nm (réglée à 50 mW/cm2) à courant constant.
- Photo-réticulation de chaque gel, un à la fois, en exposant chaque puits à la lumière UV pendant 45 s chacun.
- Réticulez le collagène en plaçant la plaque à 37 °C pendant 30-45 min.
- Appliquez la tête de pression de fluide sur les gels à l’aide d’astrobasal + 0,5 % N-2 v/v + 1 % v/v B-27.
- Débit net zéro (statique) : Ajouter 700 μL de milieu dans la plaque à puits et 100 μL dans l’insert de culture tissulaire.
- Débit net : Ajouter 100 μL de milieu dans la plaque à puits et 700 μL dans l’insert de culture tissulaire.
REMARQUE : Utilisez l’action capillaire pour ajouter 100 μL sous l’insert de culture tissulaire ; Ce volume ne remplira pas la plaque du puits.
- Placez l’assiette à 37 °C, 5% CO2, pendant au moins 18 h ou jusqu’à 5 jours.
REMARQUE : Les systèmes peuvent incuber jusqu’à 5 jours selon les besoins de l’essai, mais un délai de 18 à 24 heures est suffisant pour les expériences initiales d’invasion, de viabilité ou de prolifération.
5. Cellules de fixation pour l’analyse de l’invasion
REMARQUE : Ne laissez pas la membrane de l’insert de culture tissulaire se dessécher et n’appliquez pas les solutions directement sur la membrane pour éviter le détachement des cellules de la membrane.
- Aspirez le milieu des inserts de culture tissulaire et de la plaque de puits.
- Aspirez les gels des inserts de culture tissulaire à l’aide d’un embout P1000.
REMARQUE : Les gels peuvent être conservés pour l’imagerie en laissant les gels dans le puits pendant cette étape et en suivant le protocole de fixation alternatif dans la note de l’étape 5.4. - Lavez doucement le puits de la plaque avec 1x PBS afin que chaque membrane d’insertion de culture tissulaire soit couverte.
- Ajoutez 4 % v/v de formol dans du PBS dans la plaque de puits de sorte que chaque membrane d’insertion de culture tissulaire soit recouverte et incubez pendant 15 à 20 minutes à RT.
ATTENTION : Le formol est un cancérogène suspecté et peut causer de graves lésions oculaires. Utilisez du formol dans une hotte avec le pare-éclaboussures en place.
REMARQUE : Cette durée d’incubation ne fixera que les cellules sur la membrane de l’insert de culture tissulaire. Si les gels sont conservés pour l’imagerie, fixez les gels pendant 1 h à 4 °C, en les balançant doucement, et ajoutez suffisamment de formol dans l’insert de culture tissulaire pour imprégner le gel. Après la fixation, lavez soigneusement les gels avec du PBS pendant au moins 20 min. - Lavez bien chaque puits avec 1x PBS. Ensuite, ajoutez 1x PBS supplémentaire à chaque puits de plaque et insert de culture tissulaire.
- À l’aide d’un coton-tige, retirez les fragments de gel en essuyant la partie supérieure de chaque membrane d’insertion de culture tissulaire. Remettez tout 1x PBS perdu dans chaque puits après l’essuyage pour éviter de dessécher les membranes.
- Lavez chaque puits et insert de culture tissulaire dans 1x PBS.
REMARQUE : La plaque peut être scellée et placée à 4 °C si nécessaire, mais imagez les membranes dès que possible pour éviter la perte de fluorescence.
6. Imagerie et quantification
- Sur le canal DAPI, imagez chaque membrane. Si possible, prenez une image de fluorescence en mosaïque de l’ensemble du puits. Si cela n’est pas possible, à 20x, imagez le centre du puits et quatre régions dans une formation transversale qui coupe le point central.
REMARQUE : Excluez les bords du puits pour éviter les fragments de gel et ne pas chevaucher les régions d’intérêt (ROI). - Comptez le nombre de cellules dans chaque image.
- Calculez le pourcentage de CSG ensemencées qui ont envahi chaque puits :
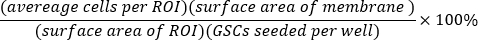
- Calculez la moyenne et l’écart-type du pourcentage d’invasion dans les répétitions techniques.
7. Autre critère d’évaluation : cytométrie en flux
REMARQUE : En plus ou au lieu d’analyser l’invasion, les gels non fixés peuvent être dégradés et les cellules récoltées pour la cytométrie en flux ou d’autres analyses de points finaux. Un exemple de protocole analysant la viabilité cellulaire (coloration vivante/morte fixable), la prolifération (anticorps Ki67) et la souche (anticorps CD71) est fourni. D’autres marqueurs d’intérêt peuvent être substitués dans ce protocole après validation de l’efficacité de la coloration. En particulier, il existe une grande variété de marqueurs qui ciblent les GSCs (examinés dans25). Ce protocole commence après l’étape 4.14.
- Dégrader les hydrogels.
REMARQUE : Une concentration de 2x de solutions de collagénase et de dispase est d’abord préparée avec des milieux expérimentaux (astrobasal + 0,5% v/v N-2 + 1% v/v B-27 sans vitamine A), qui est ensuite ajouté dans un volume égal d’hydrogel pour atteindre une concentration finale de 1x. Comme différentes cellules ont des réponses différentes à la dégradation enzymatique, il est fortement recommandé de vérifier la viabilité et le rendement des cellules (Figure 2). La plage de concentration finale de collagénase doit être de 0,2 à 0,4 mg/mL, et la plage de concentration finale de dispase doit être de 0,01 à 0,04 mg/mL ; dans cet exemple, 0,3 mg/mL de collagénase et 0,02 mg/mL de dispase sont utilisés pour dégrader les hydrogels.- Préparez 2 solutions de collagénase et de dispase (solution de milieu de dégradation sur gel). Diluer la collagénase à 0,6 mg/mL et la dispase à 0,04 mg/mL avec des milieux expérimentaux (astrobasale + 0,5 % N-2 v/v + 1 % v/v B-27 sans vitamine A).
- Retirez les gels des inserts de culture tissulaire et transférez-les dans une plaque à fond en V de 96 puits.
- Ajouter le volume équivalent de solution de milieu de dégradation du gel par hydrogel dans chaque puits. Par exemple, ajoutez 100 μL de solution de milieu de dégradation de gel à 100 μL d’hydrogel.
- Incuber la plaque sur un agitateur à 300-500 tr/min (orbite : 2 mm) à 37 °C pendant 15-30 min.
REMARQUE : Essayez l’intervalle minimum, 15 minutes d’incubation, si les cellules sont sensibles à la dégradation enzymatique. - Pipetez chaque hydrogel de haut en bas 30 à 50 fois pour briser les hydrogels.
REMARQUE : Les hydrogels seront faciles à pipeter une fois qu’ils seront complètement dégradés. Si les gels ne peuvent pas être facilement pipetés, ils doivent être incubés sur un agitateur à 300-500 tr/min (orbite : 2 mm) à 37 °C pendant 15 minutes supplémentaires. Ensuite, pipetez chaque hydrogel de haut en bas 30 à 50 fois pour briser les gels.Il est important de noter que le temps d’incubation des hydrogels dégradants ne doit pas dépasser 1 h ; Cela pourrait conduire à une faible viabilité cellulaire. - Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
REMARQUE : Le surnageant peut être retiré soit par pipetage, soit en inversant rapidement la plaque au-dessus d’un bac à déchets. - Réinjectez dans une boîte de PBS de 50 μL de 1x PBS et regroupez trois réplicats techniques dans un seul puits pour obtenir une seule réplique biologique.
- Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant pour poursuivre la cytométrie en flux.
- Bloquer la liaison non spécifique.
- Lavez les cellules avec 200 μL de 1x PBS/puits, centrifugez la plaque à 625 x g pendant 1 min à 4 °C et jetez le surnageant. Effectuez toutes les étapes suivantes sur la glace, sauf indication contraire.
- Remettre les cellules en suspension avec 200 μL de solution de blocage (1x PBS avec 10% v/v FBS) et incuber la plaque pendant 15 min à RT.
- Lavez les cellules avec 200 μL de 1x PBS/puits, centrifugez la plaque à 625 x g pendant 1 min à 4 °C et jetez le surnageant.
- Étiquetez les cellules avec une coloration vivante/morte.
- Testez la viabilité cellulaire à l’aide d’une coloration proche infrarouge vivante/morte fixable. Diluez la tache vivante/morte avec 1x PBS à 1:1000.
- Remettez les cellules en suspension dans un puits avec 200 μL d’éthanol à 70 % pour un contrôle négatif.
- Remettre les cellules en suspension dans les puits restants avec 200 μL de 1x PBS.
- Incuber la plaque pendant 5 à 10 minutes sur de la glace, centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
- Ajouter 50 μL de solution vivante/morte dans les puits respectifs et incuber la plaque sur de la glace pendant 15 min.
- Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
- Lavez les cellules deux fois avec 200 μL de tampon d’écoulement (HBSS avec 2 % p/v BSA) par puits.
- Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
- Effectuer un immunomarquage de surface pour les marqueurs cellulaires d’intérêt (anticorps CD71).
- Diluer l’anticorps CD71 avec un tampon de débit (HBSS avec BSA à 2 % p/v) à 1:50.
- Ajouter 50 μL de solution d’anticorps dans les puits respectifs et incuber la plaque sur de la glace pendant 15 min.
- Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
- Lavez les cellules une fois avec 200 μL de tampon d’écoulement (HBSS avec 2 % p/v BSA) par puits.
- Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
- Effectuer un immunomarquage intracellulaire pour les marqueurs cellulaires d’intérêt (anticorps Ki67).
- Utilisez le jeu de tampons de coloration du facteur de transcription Foxp3 pour fixer et perméabiliser les cellules. Ajouter 100 μL de solution de fixation/perméabilisation Foxp3 dans chaque puits. Remettez les granulés de cellule en suspension en les pipetant de haut en bas.
- Incuber la plaque sur de la glace ou à RT pendant 30 à 60 min dans l’obscurité.
- Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
- Lavez les cellules deux fois avec 200 μL de 1x tampon de perméabilisation par puits.
- Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
- Ajouter 100 μL de solution bloquante (1x PBS avec 2% v/v FBS) pendant 15 min à RT.
- Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
- Diluer l’anticorps Ki67 avec une solution bloquante (1x PBS avec 2% v/v FBS) à 1:25.
- Ajouter 50 μL de solution d’anticorps 1:25 Ki67 dans les puits respectifs et incuber la plaque pendant 30 min à RT dans l’obscurité.
- Centrifuger la plaque à 625 x g pendant 1 min à 4 °C et jeter le surnageant.
- Lavez les cellules deux fois avec 200 μL de 1x tampon de perméabilisation par puits.
- Remettez les cellules en suspension avec 200 μL de tampon d’écoulement.
- Traitez les échantillons à l’aide d’un cytomètre en flux. Un exemple de stratégie de contrôle est détaillé dans Cornelison et al. 202212.
Résultats
Des données représentatives de l’invasion (figure 3), de la viabilité et de l’expression de Ki67 et CD71 par cytométrie en flux (figure 4) sont fournies pour les lignées GSC publiées précédemment pour un hydrogel d’hyaluronane et de collagène12 modifié par des thio. La présence d’astrocytes et de microglies dans le modèle TME a un effet différentiel sur l’invasion de la GSC en fonct...
Discussion
L’assemblage du modèle TME comprend six étapes fondamentales : 1) le passage des cellules et la séparation des cellules entre des conditions similaires, 2) l’assemblage d’une solution concentrée de collagène pour toutes les conditions, 3) la combinaison des composants du gel (cellules, collagène, acide hyaluronique méthacrylé et photo-initiateur) pour chaque condition 4) le placage des gels, 5) la réticulation par exposition aux UV et à la chaleur, et 6) l’ajout de la t...
Déclarations de divulgation
Les auteurs n’ont aucun conflit d’intérêts pertinent à divulguer.
Remerciements
Nous tenons à remercier les sources de financement de ce travail : le National Institutes of Health National Cancer Institute (R37 CA222563 à J.M.), la Fondation Coulter (J.M.) et Virginia Tech ICTAS-CEH (J.M. & J.H.). Les GSC utilisées dans ce test ont été dérivées par Jakub Godlewski, Ph.D. (Harvard Medical School).
matériels
| Name | Company | Catalog Number | Comments |
| 12 Well Tissue Culture Plate, Sterile | Celltreat Scientific Products | 229112 | |
| 250 mL Filter System, PES Filter Material, 0.22 µm, 50 mm, Sterile | DOT Scientific | 667706 | |
| 385 nm, 1650 mW (Min) Mounted LED, 1700 mA | Thorlabs | M385LP1-C1 | |
| 75cm2 Tissue Culture Flask - Vent Cap, Sterile | Celltreat Scientific Products | 229341 | |
| 8.0 μm Cell Culture Plate Insert 12 mm Diameter | Millicell | PI8P01250 | |
| Absolute Ethanol, 200 proof, Molecular Biology Grade | Thermo Fisher Scientific | T038181000CS | Ethanol for flow cytometry dead cell control. |
| Astrocyte Medium (Astrofull) | ScienCell Research Laboratories | 1801 | Contains astrobasal, FBS, and penicillin/streptomycin. |
| B-27 Supplement (50x), minus vitamin A (Gibco) | Thermo Fisher Scientific | 12587010 | |
| BSA (MACS) | Miltenyi Biotec | 130-091-376 | |
| CD71 antibody (eBioscience, Invitrogen) | Fisher Scientific | 25-0719-41 | |
| Cell Counting Chambered Slides | Nexcelom Bioscience | CHT4-PD100-002 | |
| Cell Scrapers | Biologix USA | 70-1250 | |
| Cellometer K2 Fluorescent Cell Counter (Nexelcom Bioscience) | VWR | NEXCCMK2-SK150-FCS | |
| Centrifuge - Low-Speed | Eppendorf | 5702 R | Centrifuge for cell culture. |
| Clear Polystyrene 96-Well Microplates, Corning | Fisher Scientific | 07-200-108 | V-bottom plates for flow cytometry staining. |
| CO2 Incubator, 150L, Heracell 150i (Thermo Scientific) | Thermo Fisher Scientific | 50116047 | |
| Collagen I, High Concentration, Rat Tail | Corning | 354249 | |
| Collagen I, Rat Tail | Corning | 354236 | "Low" concentration for coating adherent flasks. |
| Collagenase (CAS# 9001-12-1) | United States Biological | C7511-30 | |
| Collimation Adapter for Olympus BX & IX, AR Coating: 350 - 700 nm | Thorlabs | COP1-A | |
| Cotton Swabs, Q-tips Precision Tips | Amazon | B01KCJB3R2 | |
| Dispase (CAS# 9001-92-7) | United States Biological | D3760 | |
| DMEM, high glucose (Gibco) | Thermo Fisher Scientific | 11330032 | |
| EVOS FL | Invitrogen | AMF4300 | |
| Fetal Bovine Serum (Gibco) | Thermo Fisher Scientific | 26140079 | For microglia culture. |
| Formalin solution, neutral buffered, 10% (Sigma-Aldrich) | Millipore Sigma | HT501128 | |
| Foxp3 / Transcription Factor Staining Buffer Set (eBioscience, Invitrogen) | Thermo Fisher Scientific | 00-5523-00 | |
| Glioma stem cells | n/a | n/a | Can be patient derived or commercial glioma stem cell lines. |
| Guava easyCyte HT System | Millipore Sigma | 0500-4008 | Flow cytometer. |
| HBSS (Sigma-Aldrich) | Millipore Sigma | H6648 | |
| HEPES (1 M) (Gibco) | Thermo Fisher Scientific | 15630080 | |
| High-Power 1-Channel LED Driver with Pulse Modulation, 10.0 A Max, 50.0 V Max | Thorlabs | DC2200 | Interface for UV Lamp. |
| Hoechst 33342 Solution (20 mM) (Thermo Scientific) | Thermo Fisher Scientific | 62249 | |
| Human Astrocytes | ScienCell Research Laboratories | 1800 | Primary astrocytes derived from the cerebral cortex. |
| Human EGF Recombinant Protein (Gibco) | Thermo Fisher Scientific | PHG0311 | |
| Human FGF-basic (FGF-2/bFGF) (aa 10-155) Recombinant Protein (Gibco) | Thermo Fisher Scientific | PHG0021 | |
| Immortalized Human Microglia - hTERT | Applied Biological Materials | T0251 | |
| Incu-mixer MP Heated Microplate Vortexer, 2 position | Benchmark Scientific | H6002 | |
| Ki67 REAfinity, PerCP-Vio 700 antibody | Miltenyi Biotec | 130-120-420 | |
| LED UV Curing Meter | Gigahertz-Optik | X1-RCH-116 | Optometer to measure UV light intensity. |
| Lithium phenyl-2,4,6-trimethylbenzoylphosphinate (LAP) | Advanced Biomatrix | 5269-100MG | Photoinitiator. |
| LIVE/DEAD Fixable Near-IR (Invitrogen) | Thermo Fisher Scientific | L24975 | |
| Methacrylated hyaluronic acid (photoHA) | Advanced Biomatrix | 5212-100MG | |
| Microcentrifuge, Sorvall ST8R (Thermo Scientific) | Fisher Scientific | 75-997-203 | Centrifuge for flow cytometry staining. |
| N-2 Supplement (100X) (Gibco) | Thermo Fisher Scientific | 17502048 | |
| Neurobasal-A Medium (Gibco) | Thermo Fisher Scientific | 10888022 | |
| PBS (10X), pH 7.4 without Ca & Mg | Quality Biological | 119-069-101 | |
| Sodium hydroxide, pellets ACS (CAS# 1310-73-2) | VWR | 97064-476 | |
| Synergy Ultrapure Water Purification System (MilliporeSigma) | Fisher Scientific | SYNS0HFUS | |
| Trypsin-EDTA (0.25%), phenol red (Gibco) | Thermo Fisher Scientific | 25200056 | |
| ViaStain AOPI Staining Solution | Nexcelom Bioscience | CS2-0106 |
Références
- Ostrom, Q. T., et al. CBTRUS statistical report: Primary brain and other central nervous system tumors diagnosed in the United States in 2016-2020. Neuro Oncol. 25, 1-99 (2023).
- Stupp, R., et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma. N Engl J Med. 352 (10), 987-996 (2005).
- Stupp, R., et al. Effect of tumor-treating fields plus maintenance temozolomide vs maintenance temozolomide alone on survival in patients with glioblastoma: A randomized clinical trial. JAMA. 318 (23), 2306-2316 (2017).
- Lathia, J. D., Mack, S. C., Mulkearns-Hubert, E. E., Valentim, C. L. L., Rich, J. N. Cancer stem cells in glioblastoma. Genes Dev. 29 (12), 1203-1217 (2015).
- Roos, A., Ding, Z., Loftus, J. C., Tran, N. L. Molecular and microenvironmental determinants of glioma stem-like cell survival and invasion. Front Oncol. 7, 120 (2017).
- Yabo, Y. A., Niclou, S. P., Golebiewska, A. Cancer cell heterogeneity and plasticity: A paradigm shift in glioblastoma. Neuro Oncol. 24 (5), 669-682 (2022).
- Geer, C. P., Grossman, S. A. Interstitial fluid flow along white matter tracts: A potentially important mechanism for the dissemination of primary brain tumors. J Neurooncol. 32 (3), 193-201 (1997).
- Munson, J. M., Bellamkonda, R. V., Swartz, M. A. Interstitial flow in a 3D microenvironment increases glioma invasion by a CXCR4-dependent mechanism. Cancer Res. 73 (5), 1536-1546 (2013).
- Kingsmore, K. M., et al. Interstitial flow differentially increases patient-derived glioblastoma stem cell invasion via CXCR4, CXCL12, and CD44-mediated mechanisms. Integr Biol. 8 (12), 1246-1260 (2016).
- Qazi, H., Shi, Z. -. D., Tarbell, J. M. Fluid shear stress regulates the invasive potential of glioma cells via modulation of migratory activity and matrix metalloproteinase expression. PLoS One. 6 (5), e20348 (2011).
- Parmigiani, E., Scalera, M., Mori, E., Tantillo, E., Vannini, E. Old stars and new players in the brain tumor microenvironment. Front Cell Neurosci. 15, 709917 (2021).
- Cornelison, R. C., et al. A patient-designed tissue-engineered model of the infiltrative glioblastoma microenvironment. NPJ Precis Oncol. 6 (1), 54 (2022).
- Tchafa, A. M., Shah, A. D., Wang, S., Duong, M. T., Shieh, A. C. Three-dimensional cell culture model for measuring the effects of interstitial fluid flow on tumor cell invasion. J Vis Exp. (65), e4159 (2012).
- Shields, J. D., et al. Autologous chemotaxis as a mechanism of tumor cell homing to lymphatics via interstitial flow and autocrine CCR7 signaling. Cancer Cell. 11 (6), 526-538 (2007).
- Shieh, A. C., Rozansky, H. A., Hinz, B., Swartz, M. A. Tumor cell invasion is promoted by interstitial flow-induced matrix priming by stromal fibroblasts. Cancer Res. 71 (3), 790-800 (2011).
- Miteva, D. O., et al. Transmural flow modulates cell and fluid transport functions of lymphatic endothelium. Circ Res. 106 (5), 920-931 (2010).
- Kingsmore, K. M., et al. MRI analysis to map interstitial flow in the brain tumor microenvironment. APL Bioeng. 2 (3), 031905 (2018).
- Roberts, L. M., et al. Myeloid derived suppressor cells migrate in response to flow and lymphatic endothelial cell interaction in the breast tumor microenvironment. Cancers. 14 (12), 3008 (2022).
- Bellail, A. C., Hunter, S. B., Brat, D. J., Tan, C., Van Meir, E. G. Microregional extracellular matrix heterogeneity in brain modulates glioma cell invasion. Int J Biochem Cell Biol. 36 (6), 1046-1069 (2004).
- Choi, J. R., Yong, K. W., Choi, J. Y., Cowie, A. C. Recent advances in photo-crosslinkable hydrogels for biomedical applications. Biotechniques. 66 (1), 40-53 (2019).
- Artym, V. V., Matsumoto, K. Imaging cells in three-dimensional collagen matrix. Curr Protoc Cell Biol. , 11-20 (2010).
- Gelman, R. A., Williams, B. R., Piez, K. A. Collagen fibril formation. Evidence for a multistep process. J Biol Chem. 254 (1), 180-186 (1979).
- Williams, B. R., Gelman, R. A., Poppke, D. C., Piez, K. A. Collagen fibril formation. Optimal in vitro conditions and preliminary kinetic results. J Biol Chem. 253 (18), 6578-6585 (1978).
- Mineo, M., et al. The long non-coding RNA HIF1A-AS2 facilitates the maintenance of mesenchymal glioblastoma stem-like cells in hypoxic niches. Cell Rep. 15 (11), 2500-2509 (2016).
- Tang, X., et al. Targeting glioblastoma stem cells: A review on biomarkers, signal pathways and targeted therapy. Front Oncol. 11, 701291 (2021).
- Dirkse, A., et al. Stem cell-associated heterogeneity in glioblastoma results from intrinsic tumor plasticity shaped by the microenvironment. Nat Commun. 10 (1), 1787 (2019).
- Sofroniew, M. V. Astrocyte reactivity: Subtypes, states, and functions in CNS innate immunity. Trends Immunol. 41 (9), 758-770 (2020).
- Tate, K. M., Munson, J. M. Assessing drug response in engineered brain microenvironments. Brain Res Bull. 150, 21-34 (2019).
- Cai, X., et al. Application of microfluidic devices for glioblastoma study: Current status and future directions. Biomed Microdevices. 22 (3), 60 (2020).
- Kleinman, H. K., Martin, G. R. Matrigel: Basement membrane matrix with biological activity. Semin Cancer Biol. 15 (5), 378-386 (2005).
- Jadin, L., et al. Hyaluronan expression in primary and secondary brain tumors. Ann Transl Med. 3 (6), 80 (2015).
- Cornelison, R. C., Munson, J. M. Perspective on translating biomaterials into glioma therapy: Lessons from in vitro models. Front Mater. 5, 27 (2018).
- Kapałczyńska, M., et al. 2D and 3D cell cultures - a comparison of different types of cancer cell cultures. Arch Med Sci. 14 (4), 910-919 (2018).
- Nelson, C. M., Bissell, M. J. Of extracellular matrix, scaffolds, and signaling: Tissue architecture regulates development, homeostasis, and cancer. Annu Rev Cell Dev Biol. 22, 287-309 (2006).
- Phon, B. W. S., Kamarudin, M. N. A., Bhuvanendran, S., Radhakrishnan, A. K. Transitioning pre-clinical glioblastoma models to clinical settings with biomarkers identified in 3D cell-based models: A systematic scoping review. Biomed Pharmacother. 145, 112396 (2022).
- Pampaloni, F., Reynaud, E. G., Stelzer, E. H. K. The third dimension bridges the gap between cell culture and live tissue. Nat Rev Mol Cell Biol. 8 (10), 839-845 (2007).
- Ortiz-Cárdenas, J. E., et al. Towards spatially-organized organs-on-chip: Photopatterning cell-laden thiol-ene and methacryloyl hydrogels in a microfluidic device. Organs Chip. 4, 100018 (2022).
- Ozulumba, T., et al. Mitigating reactive oxygen species production and increasing gel porosity improves lymphocyte motility and fibroblast spreading in photocrosslinked gelatin-thiol hydrogels. bioRxiv. , (2024).
- Lim, K. S., et al. Fundamentals and applications of photo-cross-linking in bioprinting. Chem Rev. 120 (19), 10662-10694 (2020).
- Ghosh, R. N., et al. An insight into synthesis, properties and applications of gelatin methacryloyl hydrogel for 3D bioprinting. Mater Adv. 4 (22), 5496-5529 (2023).
- Venkataramani, V., et al. Glutamatergic synaptic input to glioma cells drives brain tumour progression. Nature. 573 (7775), 532-538 (2019).
- Venkataramani, V., et al. Glioblastoma hijacks neuronal mechanisms for brain invasion. Cell. 185 (16), 2899-2917 (2022).
Réimpressions et Autorisations
Demande d’autorisation pour utiliser le texte ou les figures de cet article JoVE
Demande d’autorisationExplorer plus d’articles
This article has been published
Video Coming Soon