Analisi del flusso a doppio reporter basata su biglie fluorescenti magnetiche del blocco anticorpale indotto dal peptide PDL1-Vaxx dell'interazione PD-1/PD-L1
* Questi autori hanno contribuito in egual misura
In questo articolo
Riepilogo
Gli inibitori del checkpoint sono obiettivi importanti nello sviluppo di terapie per la lotta contro il cancro. Questo rapporto introduce un nuovo vaccino contro il cancro a base di peptide PDL1, PDL1-Vaxx, che induce la produzione di anticorpi policlonali neutralizzanti che bloccano la formazione del complesso PD-1/PDL1. Questo lavoro descrive anche in dettaglio lo sviluppo e il test di un saggio basato su microsfere fluorescenti per l'analisi di questa attività.
Abstract
L'inibizione dei recettori del checkpoint (PD-1, PD-L1 e CTLA-4) con anticorpi monoclonali ha mostrato grandi benefici negli studi clinici per il trattamento dei pazienti oncologici ed è diventata un approccio fondamentale nella moderna immunoterapia del cancro. Tuttavia, solo un sottogruppo di pazienti risponde all'immunoterapia con anticorpi monoclonali checkpoint. Pertanto, è urgente sviluppare nuove strategie terapeutiche contro il cancro. È stato sviluppato un nuovo vaccino contro il cancro dell'epitopo del peptide a cellule B PDL1 (ligando di morte programmata 1), con gli amminoacidi 130-147 legati al peptide MVF (proteina di fusione del virus del morbillo a cellule T "promiscue") tramite un linker GPSL. I test preclinici hanno indicato che questo vaccino PDL1 (PDL1-Vaxx) stimola efficacemente gli anticorpi altamente immunogenici negli animali. Gli animali immunizzati con PDL1-Vaxx mostrano una riduzione del carico tumorale e tassi di sopravvivenza estesi in vari modelli di cancro animale. I meccanismi d'azione indicano che gli anticorpi inibiti dal vaccino inibiscono la proliferazione delle cellule tumorali, inducono l'apoptosi e bloccano l'interazione PD-1/PD-L1. Questo manoscritto introduce un saggio basato su biglie magnetiche che utilizza un sistema di analisi del flusso a doppio reporter per valutare l'interazione PD-1/PD-L1 e il suo blocco da parte degli anticorpi anti-PDL1 sollevati contro il PDL1-Vaxx.
Introduzione
Nelle cellule T, nelle cellule B e nei checkpoint intracellulari del sistema immunitario, le vie di segnalazione regolano le attività immunitarie. Alcune cellule tumorali si proteggono dall'attacco immunitario stimolando i bersagli dei checkpoint, che inibiscono la funzione immunitaria e promuovono la sopravvivenza e la proliferazione neoplastica. L'immunoterapia oncologica mediante inibizione dei checkpoint utilizza anticorpi per colpire e bloccare i checkpoint di segnalazione e, quindi, ripristinare le funzioni antineoplastiche del sistema immunitario 1,2,3. Le terapie antitumorali altamente efficaci includono attualmente gli anticorpi monoclonali nivolumab, che ha come bersaglio la proteina di morte programmata 1 (PD-1)4, e atezolizumab, che ha come bersaglio il ligando di morte programmata 1 (PD-L1)5. Questo approccio ha dimostrato un grande successo clinico nel trattamento dei pazienti oncologici. Tuttavia, l'utilità clinica delle attuali strategie di inibizione del checkpoint è mitigata dagli eventi avversi e dalla resistenza al trattamento, specialmente nella terapia con un singolo agente6. Una combinazione di immunoterapia e strategie terapeutiche più efficaci con una minore tossicità è urgentemente necessaria nel trattamento del cancro 1,3,6.
Negli ultimi 30 anni, il laboratorio del Dr. Kaumaya ha sviluppato vaccini contro il cancro peptidico e agenti correlati al mimo peptidico per la terapia del cancro, alcuni dei quali sono in studi clinici in corso 1,2,7,8,9,10,11,12,13,14 . Ad esempio, B-Vaxx con immunoterapia di combinazione HER-2 ha mostrato benefici per i pazienti contro tumori solidi metastatici e/o ricorrenti in studi clinici12. Gli ultimi vaccini antitumorali del laboratorio sono PD1-Vaxx 2,13 e PDL1-Vaxx14, che hanno mostrato grandi vantaggi negli studi preclinici, soprattutto nel trattamento combinato. Il PD1-Vaxx ha completato gli studi clinici di dose-escalation negli Stati Uniti e in Australia. Il PD1-Vaxx sarà combinato con atezolizumab nello studio di fase 1b che inizierà a maggio 2023. Questo rapporto si concentra sulla valutazione della capacità degli anticorpi indotti da PDL1-Vaxx di bloccare l'interazione PD-1/PD-L1.
Il vaccino contro il cancro PDL1-Vaxx è un nuovo vaccino epitopo del peptide delle cellule B con gli amminoacidi PD-L1 130-147 collegati al peptide di fusione del virus del morbillo delle cellule T promiscue (MVF) tramite un linker peptidico GPSL. Studi preclinici hanno dimostrato che PDL1-Vaxx è altamente immunogenico nello stimolare la produzione di anticorpi antitumorali in vari modelli animali, prolunga la sopravvivenza e riduce il carico tumorale14. Questi anticorpi generati contro il peptide PD-L1 possono bloccare con successo l'interazione PD1/PD-L1, determinando così un'attività anti-neoplastica. Questo rapporto introduce un test che analizza il blocco della formazione del complesso PD1/PD-L1 da parte degli anticorpi indotti da PDL1-Vaxx utilizzando un formato basato su microsfere magnetiche con una lettura a doppio reporter su uno strumento di citometria a flusso.
Protocollo
1. Preparazione sperimentale
NOTA: I dettagli di tutti i reagenti/apparecchiature menzionati in questo passaggio sono elencati nella Tabella dei materiali.
- Ottenere PD-1 umano ricombinante (rhPD-1; poliistidina-marcato). Ricostituire rhPD1 liofilizzato con soluzione salina tamponata con fosfato (PBS) filtrata sterile, pH 7,4, prima dell'uso.
- Ottenere PD-L1 umano ricombinante biotinilato (rhPD-L1). Ricostituire rhPD-L1 liofilizzato con acqua deionizzata sterile prima dell'uso.
- Ottenere il reagente per la rilevazione della R-ficoeritrina coniugato con streptavidina (SAPE). Conservare tutte le soluzioni SAPE al riparo dalla luce a temperature di frigorifero (es. 2-8 °C).
- Ottenere microsfere magnetiche colorate in fluorescenza (diametro 6,5 μm, polistirene con magnetite incorporata) e il Kit di Accoppiamento Perline15 (se utilizzato, vedere la Tabella dei Materiali). L'accoppiamento covalente alle microsfere richiede solfo-NHS (sulfo-N-idrosuccinimide) e EDC (N-[3-dimetilamminopropil]-N′-etilcarbodiimmide cloridrato).
NOTA: I set di perline magnetiche sono disponibili con uno qualsiasi dei 500 tag fluorescenti unici, che consentono l'identificazione e la differenziazione da diversi set di perline16. Le perle sono disponibili in concentrazioni standard di 2,5 × 10,6 perline/mL e 12,5 × 10,6 perline/mL. Conservare le perle al riparo dalla luce a temperature di frigorifero (es. 2-8 °C). Non congelare le sospensioni del tallone. - Ottenere anticorpi di controllo positivi e negativi e anticorpi di rilevamento secondario marcati con Brilliant Violet 421 (BV421). Conservare tutte le molecole coniugate fluorescenti al riparo dalla luce.
- Eseguire tutte le reazioni di accoppiamento in provette a basso legame proteico e tutte le reazioni di saggio in piastre per microtitolazione a basso legame proteico, a fondo tondo, a 96 pozzetti. Sigillare le piastre con una pellicola adesiva monouso o coperchi per micropiastre in plastica a 96 pozzetti per le fasi di incubazione del saggio. Utilizzare un separatore magnetico a piastre per immobilizzare le perle durante le fasi di lavaggio del saggio.
NOTA: Il sistema di analisi del flusso a doppio reporter è dotato di tre laser: (1) uno che identifica e quantifica la fluorescenza specifica del set di microsfere (canale di classificazione); (2) uno che rileva e quantifica la fluorescenza della ficoeritrina (PE) bersaglio-specifica (Reporter Channel 1; eccitazione 532 nm, emissione "arancione" 565-585 nm); e (3) uno che rileva e quantifica la fluorescenza BV421 target-specifica di un secondo analita target (Reporter Channel 2; eccitazione 405 nm, emissione "blu" 421-441 nm).
2. Accoppiamento di rhPD-1 a perline magnetiche
NOTA: La proteina da accoppiare deve essere priva di albumina sierica bovina (BSA), azoturo di sodio, glicina, glicerolo, tris(idrossi-metil)amminometano (Tris) o additivi contenenti ammine e deve essere sospesa in PBS a pH 7,4. È disponibile un kit di accoppiamento commerciale che include tutti i reagenti e i tamponi necessari descritti nel presente documento (vedere la tabella dei materiali).
- Rimuovere tutti i reagenti di accoppiamento dal frigorifero e lasciarli equilibrare a temperatura ambiente (RT, 18-22 °C) per 20-30 min.
- Risospendere le microsfere di serie mediante un breve vortice, sonicazione o rotazione (15 minuti a 15-30 giri/min), secondo la scheda informativa del prodotto.
- Trasferire 1 × 106 microsfere magnetiche in una provetta per microcentrifuga a basso legame proteico da 1,5 mL (vedere la tabella dei materiali).
- Microsfere di lavaggio con 100 μL di tampone di attivazione15: 0,1 M NaH2PO4 (monobasico), pH 6,2.
NOTA: L'accoppiamento può essere eseguito anche utilizzando un kit di accoppiamento preconfigurato, che include acido 2-morfolinoetanosolfonico (MES) 0,1 M, pH 6,0, come tampone alternativo di attivazione e accoppiamento (vedere la Tabella dei materiali).- Mettere la provetta contenente le perline in un separatore magnetico per 1-2 minuti.
NOTA: In alternativa, le perle possono essere separate mediante microcentrifugazione a ≥8.000 × g per 1-2 min. - Aspirare il surnatante con una pipetta dalle microsfere immobilizzate o pellettate con la provetta ancora posizionata nel separatore magnetico.
- Rimuovere la provetta per microcentrifuga dal magnete e aggiungere 80 μL di tampone di accoppiamento (vedere la tabella dei materiali).
- Agitare delicatamente il tubo di reazione e sonicare per 20 secondi per disperdere le perle.
- Mettere la provetta contenente le perline in un separatore magnetico per 1-2 minuti.
- Attivare le perle con sulfo-NHS e EDC.
NOTA: La soluzione madre di sulfo-NHS è di 50 mg/mL disciolta nel tampone di attivazione. La soluzione madre di EDC è anche 50 mg/mL disciolti nel tampone di attivazione. Sia il tampone di attivazione che l'umidità nell'atmosfera causano la degradazione dell'EDC. Non è consigliabile utilizzare una soluzione EDC immagazzinata. Prepara una soluzione EDC fresca quanto basta prima del passaggio e usala immediatamente quando la soluzione è pronta. Scartare la soluzione EDC in eccesso.
ATTENZIONE: L'EDC provoca grave irritazione oculare ed è irritante per le vie respiratorie e la pelle.- Aggiungere 10 μL di sulfo-NHS alla provetta microfugo contenente le perle lavate e attivate.
- Aggiungere 10 μL di soluzione madre EDC alla provetta microfuge contenente le microsfere e il sulfo-NHS.
- Proteggere le microsfere fotosensibili dalla luce e ruotare sul rotatore per 20 min a 15-30 giri/min, a RT (18-22 °C). In alternativa, il tubo può rimanere fermo durante la fase di attivazione se viene delicatamente vorticato per ridistribuire le perline a intervalli di 10 minuti.
- Lavare via i reagenti di accoppiamento in eccesso dalle perle.
- Posizionare la provetta contenente le perle attivate in un separatore magnetico per 1-2 minuti.
- Aspirare il surnatante con una pipetta da microsfere immobilizzate o pellettate con il tubo ancora posizionato nel separatore magnetico.
- Rimuovere la provetta per microcentrifuga dal magnete e aggiungere 100 μL di tampone di attivazione.
- Agitare delicatamente il tubo di reazione per disperdere le perle.
- Ripetere i passaggi 2.6.1-2.6.4 altre due volte per un totale di tre lavaggi. Al termine del lavaggio, le perle saranno sospese in 100 μL di tampone di attivazione ad una concentrazione approssimativa di 10 × 106 perline/mL.
- Accoppiare il peptide rhPD-1 alle perle attivate.
- Aggiungere 390 μL di tampone di attivazione alla provetta contenente le perle attivate per portare il volume totale della sospensione delle microsfere a 490 μL.
- Aggiungere 1 μg di peptide PD-1 alla sospensione di microsfere attivate aggiungendo 10 μL di soluzione di peptide PD-1 (1 mg/mL disciolto in PBS) alla provetta contenente le perle attivate.
- Ruotare brevemente la provetta per microcentrifuga per distribuire uniformemente il PD-1 e le perle attivate.
- Incubare le perle con PD-1 per 2 ore al buio a RT (18-22 °C) con rotazione (15-30 giri/min).
- Lavare le perle due volte (2x) utilizzando il tampone di saggio/lavaggio (PBS-TBN: 1x PBS, pH 7,4 + 0,1% BSA + 0,05% Tween-20 + 0,05% NaN315).
- Posizionare la provetta contenente le perle attivate in un separatore magnetico per 1-2 minuti.
- Aspirare il surnatante con una pipetta dalle microsfere immobilizzate o pellettate con la provetta ancora posizionata nel separatore magnetico.
- Rimuovere la provetta per microcentrifuga dal magnete e aggiungere 100 μL di tampone di attivazione.
- Agitare delicatamente il tubo di reazione per disperdere le perle.
- Ripetere i passaggi 2.8.1-2.8.4 un'altra volta per un totale di due lavaggi. Al termine del lavaggio, le microsfere saranno sospese in 100 μL di tampone di attivazione ad una concentrazione di 10 × 106 perline/mL.
NOTA: Il tampone di saggio/lavaggio può essere prodotto senza azoturo di sodio (conservante) se il tampone non viene utilizzato anche come mezzo di conservazione. - Conservare le perline accoppiate rhPD-1 al buio in frigorifero a 2-8 °C se non utilizzate immediatamente. Le perle accoppiate a proteine sono stabili fino a 18 mesi.
3. Valutazione del successo dell'accoppiamento rhPD-1 alle perline
NOTA: Le microsfere accoppiate a rhPD-1 vengono fatte reagire con rhPD-L1 biotinilato, l'ultimo dei quali viene rilevato mediante incubazione con SAPE seguita da una valutazione sul citometro a flusso. Ciò verifica sia il successo dell'accoppiamento di PD-1 alle biglie magnetiche sia l'interazione funzionale tra le proteine rhPD-1 e rhPD-L1.
- Creare una serie di diluizioni seriali doppie di rhPD-L1 biotinilato in PBS-TBN (la soluzione madre di rhPD-L1 è 1 mg/mL). L'intervallo di concentrazione finale di rhPD-L1 da testare è una soluzione da 8 μg/mL fino a una soluzione da 313 pg/mL. Creare volumi da 150 μL di ciascuna diluizione rhPD-L1: 50 μL per ogni reazione e due reazioni per condizione, più un eccesso sufficiente per compensare le perdite di pipettaggio.
- Etichettare le provette per microfugo di diluizione rhPD-L1 come 8 μg/mL, 4 μg/mL, 2 μg/mL, 1 μg/mL, 0,5 μg/mL, 0,25 μg/mL, 0,125 μg/mL, 0,063 μg/mL e 0,031 μg/mL. Una provetta da 0 μg/mL (solo PBS-TBN) funge da controllo no-PD-L1.
- Precaricare 150 μL di PBS-TBN su tutte le provette di diluizione rhPD-L1 etichettate.
NOTA: La concentrazione finale più alta di rhPD-L1 da testare è di 8 μg/mL e rhPD-L1 verrà diluito 1:1 al momento dell'aggiunta alla miscela di reazione, quindi la provetta di diluizione etichettata "8 μg/mL" si riferisce alla concentrazione finale e contiene effettivamente 16 μg/mL rhPD-L1. Le etichette su tutte le provette di diluizione indicano la concentrazione finale di rhPD-L1 dopo l'aggiunta alla reazione. - Creare la diluizione rhPD-L1 a più alta concentrazione (16 μg/mL effettivi). Si tratta di una diluizione in due fasi, 62,5 volte, della soluzione madre rhPD-L1 da 1 mg/mL (1.000 μg/16 μg = 62,5).
- Combinare 84 μL di PBS-TBN con 16 μL di soluzione madre rhPD-L1 (1 mg/mL, cioè 1.000 μL) in una provetta per microcentrifuga. Si tratta di una diluizione di 6,25 volte e la concentrazione risultante è di 160 μg/mL rhPD-L1.
- Nella provetta etichettata "8 μg/mL", combinare 270 μL di PBS-TBN con 30 μL della diluizione rhPD-L1 creata nella fase precedente (160 μg/mL). Si tratta di una diluizione di 10 volte e la concentrazione risultante è in realtà di 16 μg/mL. L'etichetta della provetta "8 μg/mL" si riferisce alla sua concentrazione finale dopo l'aggiunta alla reazione.
- Trasferire 150 μL della diluizione rhPD-L1 creata al punto 3.1.3 ("8 μg/mL") nella provetta "4 μg/mL", chiudere il tappo della provetta per microcentrifuga e vorticare brevemente per miscelare la soluzione.
- Ripetere il passaggio 3.1.4 in sequenza fino al completamento della serie di diluizioni rhPD-L1. Dopo la creazione, tutte le provette comprese tra "8 μg/mL" e "0,063 μg/mL", così come il controllo 0 μg/mL, devono contenere 150 μL di soluzione e l'ultima provetta, "0,031 μg/mL", deve contenere 300 μL di soluzione. In questo modo si crea un volume sufficiente di ciascuna diluizione per testare 50 μL di ciascuna diluizione di rhPD-L1 biotinilato in reazioni duplicate, con un eccesso sufficiente a compensare le perdite di pipettaggio.
- Contare le perline accoppiate a rhPD-1 usando un emocitometro17.
- Diluire le perle accoppiate a rhPD-1 a 5 × 104 perline/mL, con un volume sufficiente per 2.500 perline/50 μL/reazione.
- Ruotare la sospensione a microsfere accoppiate rhPD-1 da 5 × 104 microsfere/mL e pipettare 50 μL della sospensione in ciascun pozzetto marcato/mappato di una piastra per microtitolazione a fondo tondo a 96 pozzetti in modo da creare pozzetti duplicati per ogni diluizione rhPD-L1 in fase di test.
- Aggiungere 50 μL di ciascuna provetta di diluizione rhPD-L1 biotinilata creata nella fase 3.1 nei pozzetti appropriati sulla piastra per microtitolazione.
- Coprire la piastra per microtitolazione con un foglio monouso o un sigillante adesivo in plastica e incubare la piastra per 1 ora al buio a RT (18-22 °C) su un agitatore orbitale (600 giri/min).
- Lavare l'eccesso di rhPD-L1 biotinilato dalle perline.
- Trasferire la piastra sigillata dall'agitatore orbitale al separatore magnetico per piastre per 2 minuti per immobilizzare le perline.
- Rimuovere con cautela il sigillante per piastre adesive, verificare che il magnete e la piastra per microtitolazione siano saldamente insieme, capovolgere la piastra e scaricare i surnatanti in un lavandino o in un contenitore per rifiuti liquidi a rischio biologico, a seconda dei casi. Picchiettare delicatamente ma energicamente la piastra capovolta su un cuscino di carta assorbente per rimuovere il surnatante rimanente.
- Rimuovere la piastra per microtitolazione dal separatore magnetico a piastre e pipettare 150 μL di PBS-TBN in ciascun pozzetto.
- Posizionare la piastra non sigillata sul separatore magnetico per 2 minuti per immobilizzare le perline.
- Verificare che il magnete e la piastra per microtitolazione siano saldamente uniti, quindi capovolgere la piastra e scaricare i surnatanti in un lavandino o in un contenitore per rifiuti liquidi a rischio biologico, a seconda dei casi. Picchiettare delicatamente ma energicamente la piastra capovolta su un cuscino di carta assorbente per rimuovere il surnatante rimanente.
- Ripetere le fasi di lavaggio delle lastre 3.7.3-3.7.5 due volte per un totale di tre lavaggi con 150 μL di PBS-TBN ciascuno. Assicurarsi che non rimanga alcun surnatante nei pozzetti alla fine dell'ultima fase di lavaggio. Lavorare costantemente per evitare che le perline immobilizzate si secchino sul fondo del pozzo.
- Aggiungere il reagente di rilevamento SAPE.
- Diluire la soluzione madre SAPE in PBS-TBN a una concentrazione di lavoro di 6 μg/mL. Preparare un volume sufficiente di soluzione di lavoro SAPE in modo che tutti i pozzetti di reazione possano ricevere 100 μL/pozzetto, con un extra sufficiente per sopportare le perdite di pipettaggio.
- Rimuovere la piastra per microtitolazione dal separatore magnetico per piastre.
- Aggiungere 100 μL di soluzione di lavoro SAPE in ciascun pozzetto di reazione e risospendere le microsfere lavate mediante pipettaggio.
- Sigillare la piastra per microtitolazione a 96 pozzetti con un sigillante per piastre adesive in alluminio o plastica e incubare per 1 ora al buio a RT (18-22 °C) su un agitatore orbitale a 600 giri/min.
- Rimuovere la piastra per microtitolazione dall'incubatore, trasferirla nel separatore magnetico per piastre per immobilizzare le sfere, rimuovere il sigillante per piastre adesive e lavare le microsfere tre volte con 150 μL PBS-TBN, come descritto nei passaggi 3.7.3-3.7.5.
- Dopo aver rimosso il lavaggio finale, rimuovere la piastra dal separatore magnetico a piastre e risospendere le microsfere in 100 μL di PBS-TBN per pozzetto.
- Analizza i risultati.
- Leggere la targhetta sullo strumento di analisi del flusso (vedere la Tabella dei materiali) per determinare l'intensità mediana della fluorescenza (MFI) di ciascuna reazione utilizzando le seguenti impostazioni dello strumento: volume di aspirazione = 50 μL; numero minimo di perline = 100 perline; impostazione timeout = 40 s; gating = 7.000-17.000; modalità di funzionamento = Single Reporter. Vengono eseguiti pozzetti duplicati per ogni condizione e viene calcolata la media dei due valori MFI di output per ciascuna condizione prima di eseguire ulteriori calcoli e grafici dei dati.
NOTA: Il valore MFI di ciascuna diluizione deve mostrare un legame dipendente dalla concentrazione, indicando un'efficienza di accoppiamento rhPD-1 accettabile alle perle e confermando una buona interazione delle proteine ricombinanti PD-1/PD-L1.
- Leggere la targhetta sullo strumento di analisi del flusso (vedere la Tabella dei materiali) per determinare l'intensità mediana della fluorescenza (MFI) di ciascuna reazione utilizzando le seguenti impostazioni dello strumento: volume di aspirazione = 50 μL; numero minimo di perline = 100 perline; impostazione timeout = 40 s; gating = 7.000-17.000; modalità di funzionamento = Single Reporter. Vengono eseguiti pozzetti duplicati per ogni condizione e viene calcolata la media dei due valori MFI di output per ciascuna condizione prima di eseguire ulteriori calcoli e grafici dei dati.
4. Saggio di blocco PD-1/PD-L1 basato su microsfere magnetiche PD-L1
NOTA: Questo test valuta l'attività bloccante dei mediatori solubili (ad esempio, anticorpi anti-PDL1-peptidici) sulle interazioni ricombinanti PD1/PD-L1. In breve, rhPD-L1 biotinilato viene preincubato con anticorpi generati nei conigli dopo diverse inoculazioni di peptidi PDL1-Vaxx. La miscela di anticorpi rhPD-L1 + anti-PDL1 viene quindi catturata utilizzando microsfere magnetiche accoppiate a rhPD-1 e il legame di rhPD-L1 alle perle accoppiate a rhPD-1 viene quantificato mediante l'aggiunta di streptavidina-PE. Il segnale di fluorescenza PE è inversamente correlato con l'attività bloccante degli anticorpi/inibitori anti-PDL1 testati. Il legame dell'anticorpo anti-PDL1-peptide viene simultaneamente valutato mediante il legame di un anticorpo secondario anti-coniglio accoppiato a BV421 (per gli anticorpi anti-peptide PDL1) o anti-umano (per gli anticorpi di controllo) e valutando la fluorescenza BV421 nel secondo canale dello strumento. Le fasi del saggio sono illustrate in dettaglio nella Figura 1.
- Preparare una doppia serie di diluizioni seriali degli anticorpi del test, inclusi candidati anticorpi policlonali indotti da PDL1-Vaxx, un anticorpo di controllo negativo (trastuzumab, Herceptin, anticorpo monoclonale anti-HER2 umanizzato) e un anticorpo di controllo positivo (atezolizumab; anticorpo monoclonale umanizzato anti-PDL1 IgG1). Ogni reazione utilizzerà 25 μL della diluizione dell'anticorpo assegnata, quindi i volumi indicati sono sufficienti per eseguire ogni reazione in pozzetti duplicati per condizione (cioè 50 μL per condizione), con un po' di eccesso rimanente per compensare le perdite di pipettaggio.
- Per ciascun anticorpo anti-peptide PDL1 indotto dal vaccino e anticorpo di controllo, assicurarsi che l'intervallo delle concentrazioni finali di anticorpi testate sia compreso tra 1.000 μg/mL e 8 μg/mL. Preparare le soluzioni madre di tutti gli anticorpi a 2.000 μg/mL.
- Per ciascun anticorpo, etichettare le provette di diluizione come 1.000 μg/mL, 500 μg/mL, 250 μg/mL, 125 μg/mL, 63 μg/mL, 31 μg/mL, 16 μg/mL e 8 μg/mL e includere il nome dell'anticorpo. Per ogni anticorpo, aggiungere anche una provetta "0 μg/mL", che sarà il controllo solo per il veicolo (PBS-TBN).
NOTA: Quando viene aggiunto alla miscela di reazione, la concentrazione di anticorpi sarà diluita 1:1. Le provette di diluizione dell'anticorpo sono etichettate come concentrazione finale di anticorpi dopo l'aggiunta alla reazione e contengono effettivamente il doppio della quantità di anticorpo rispetto a quella etichettata. - Aggiungere 75 μL di PBS-TBN a tutte le provette di diluizione degli anticorpi etichettate "500 μg/mL" e inferiori, comprese le provette di controllo "0 μg/mL" solo per veicoli.
- Per ciascun anticorpo, pipettare 150 μL della soluzione madre da 2.000 μg/mL nella rispettiva provetta etichettata "1.000 μg/mL". Questo verrà utilizzato per effettuare tutte le successive diluizioni per ciascun anticorpo.
- Per ciascun anticorpo, creare una serie completa di diluizioni trasferendo con una pipetta 75 μL dalla provetta "1.000 μg/mL" alla provetta con la diluizione immediatamente inferiore della serie (cioè "500 μg/mL"). Chiudere la provetta di diluizione appena completata, farla vorticare brevemente e continuare la costruzione della serie di diluizione trasferendo 75 μL dalla provetta "500 μg/mL" alla provetta "250 μg/mL". Ripetere questo schema fino a quando non è stata effettuata l'ultima diluizione, "8 μg/mL", per tutti gli anticorpi.
NOTA: Nella serie di diluizione completa per ciascun anticorpo, deve esserci un volume di 75 μL per tutte le provette ad eccezione della diluizione più bassa, 8 μg/mL, che deve contenere un volume di 150 μL. Ogni reazione utilizzerà 25 μL di diluizione dell'anticorpo, quindi questi volumi sono sufficienti per eseguire ogni reazione in pozzetti duplicati per condizione (cioè 50 μL per condizione), con un extra per adattarsi alle perdite di pipettaggio.
- Inserire 25 μL degli anticorpi diluiti nei pozzetti designati di una piastra per microtitolazione a 96 pozzetti.
- Diluire rhPD-L1 biotinilato a una concentrazione di lavoro di 4 μg/mL in PBS-TBN a un volume sufficiente a includere 25 μL in pozzetti duplicati per condizione (cioè 50 μL per condizione), con un extra per compensare le perdite di pipettaggio.
NOTA: In questo lavoro, rhPD-L1 biotinilato a 4 μg/mL ha prodotto circa il 50% del segnale MFI massimo misurato nella precedente valutazione dell'accoppiamento ed è stato utilizzato per l'analisi del blocco PD-1/PD-L1. - Aggiungere 25 μL di rhPD-L1 biotinilato (4 μg/mL) a ciascun pozzetto di reazione, coprire la piastra per microtitolazione con un sigillo adesivo in lamina o plastica e incubare a RT (18-22 °C) per 1 ora agitando su un agitatore orbitale a 600 giri/min.
- Diluire le microsfere accoppiate a rhPD-1 a 50.000 microsfere/mL, con un volume sufficiente per 50 μL/pozzetto (2.500 microsfere/pozzetto) più un extra per compensare le perdite di pipettaggio.
- Rimuovere la piastra di reazione per microtitolazione a 96 pozzetti dall'agitatore e rimuovere la guarnizione della piastra adesiva.
- Aggiungere 50 μL della miscela di microsfere accoppiate rhPD-1 a ciascun pozzetto.
- Sigillare la piastra e incubare per 1 ora al buio a RT (18-22 °C) su un agitatore orbitale a 600 giri/min.
- Trasferire la piastra sigillata dall'agitatore orbitale al separatore magnetico per piastre per 2 minuti per immobilizzare le perline.
- Rimuovere con cautela il sigillante per piastre adesive, verificare che il magnete e la piastra per microtitolazione siano saldamente insieme, capovolgere la piastra e scaricare i surnatanti. Picchiettare delicatamente la piastra capovolta su un cuscino di carta assorbente per rimuovere il surnatante in eccesso.
- Lavare i reagenti di reazione in eccesso dalle perle.
- Rimuovere la piastra per microtitolazione dal separatore magnetico a piastre e aggiungere 150 μL di PBS-TBN a ciascun pozzetto.
- Posizionare la piastra per microtitolazione sul separatore magnetico per piastre per 2 minuti per immobilizzare le perle.
- Verificare che il magnete e la piastra per microtitolazione siano saldamente uniti, quindi capovolgere la piastra e scaricare i surnatanti. Picchiettare delicatamente la piastra capovolta su un cuscino di carta assorbente per rimuovere il surnatante in eccesso.
- Ripetere due volte le fasi di lavaggio delle lastre 4.11.1-4.11.3, per un totale di tre lavaggi con PBS-TBN. Assicurarsi che il reagente SAPE sia preparato (sotto) prima di rimuovere l'ultima (terza) soluzione di lavaggio.
- Aggiungere il reagente di rilevamento SAPE.
- Diluire la soluzione madre SAPE ad una concentrazione di lavoro di 6 μg/mL in PBS-TBN; creare un volume sufficiente per 100 μL/pozzetto, più un volume aggiuntivo per compensare le perdite di pipettaggio.
- Aggiungere 100 μL/pozzetto di soluzione di lavoro SAPE in ciascun pozzetto di reazione e risospendere le microsfere mediante pipettaggio.
- Sigillare la piastra e incubare per 1 ora al buio a RT (18-22 °C) su un agitatore orbitale a 600 giri/min.
- Decantare la SAPE in eccesso dalla reazione.
- Trasferire la piastra sigillata dall'agitatore orbitale al separatore magnetico per piastre per 2 minuti per immobilizzare le perline.
- Rimuovere con cautela il sigillante adesivo della piastra, verificare che il magnete e la piastra per microtitolazione siano saldamente insieme, quindi capovolgere la piastra e scaricare il surnatante. Picchiettare delicatamente la piastra capovolta su un cuscino di carta assorbente per rimuovere il surnatante contenente SAPE in eccesso.
- Lavare via il SAPE in eccesso dalle perline.
- Rimuovere la piastra per microtitolazione dal supporto per piastra magnetica.
- Aggiungere 150 μL di PBS-TBN a ciascun pozzetto per risospendere le perle.
- Posizionare la piastra per microtitolazione sul separatore magnetico per piastre per 2 minuti per immobilizzare le perle.
- Verificare che il magnete e la piastra per microtitolazione siano saldamente uniti, quindi capovolgere la piastra e scaricare il surnatante. Picchiettare delicatamente la piastra capovolta su un cuscino di carta assorbente per rimuovere il surnatante in eccesso.
- Eseguire due ulteriori fasi di lavaggio con PBS-TBN per un totale di tre lavaggi ripetendo i passaggi 4.15.1-4.15.4. Preparare gli anticorpi di rilevamento secondario con BV421 (passaggio successivo) prima di rimuovere la soluzione di lavaggio finale (terza).
- Aggiungere gli anticorpi secondari BG421-congugati.
- Diluire le IgG anti-umane congugate BV421 (per la rilevazione di anticorpi di controllo umanizzati) e le IgG anti-coniglio congugate BV421 (per la rilevazione di anticorpi policlonali indotti da PDL1-Vaxx) (vedere la tabella dei materiali) 1:400 in tampone di lavaggio/saggio a volumi sufficienti per l'utilizzo di 100 μL/pozzetto di ciascuno, con un supplemento per compensare le perdite di pipettaggio.
- Aggiungere 100 μL di IgG anti-umano coniugate BV421-diluite o IgG anti-coniglio coniugate BV421 nei pozzetti appropriati.
- Sigillare la piastra e incubare per 1 ora al buio a RT (18-22 °C) su un agitatore orbitale a 600 giri/min.
- Decantare gli anticorpi secondari coniugati BV421 in eccesso dalle perline.
- Trasferire la piastra sigillata dall'agitatore orbitale al separatore magnetico per piastre per 2 minuti per immobilizzare le perline.
- Rimuovere con cautela il sigillante adesivo della piastra, verificare che il magnete e la piastra per microtitolazione siano saldamente insieme, quindi capovolgere la piastra e scaricare il surnatante. Picchiettare delicatamente la piastra capovolta su un cuscino di carta assorbente per rimuovere il surnatante contenente gli anticorpi secondari coniugati BV421 in eccesso.
- Lavare gli anticorpi secondari coniugati BV421 in eccesso dalle perle.
- Aggiungere 150 μL di PBS-TBN a ciascun pozzetto per risospendere le perle.
- Posizionare la piastra per microtitolazione sul separatore magnetico per piastre per 2 minuti per immobilizzare le perle.
- Verificare che il magnete e la piastra per microtitolazione siano saldamente uniti, quindi capovolgere la piastra e scaricare il surnatante. Picchiettare delicatamente la piastra capovolta su un cuscino di carta assorbente per rimuovere il surnatante in eccesso.
- Eseguire tre ulteriori fasi di lavaggio con PBS-TBN per un totale di quattro lavaggi ripetendo i passaggi 4.19.1-4.19.3.
- Dopo aver rimosso l'ultimo (quarto) tampone di lavaggio, rimuovere la piastra per microtitolazione dal separatore magnetico a piastre e risospendere le microsfere in PBS-TBN/pozzetto da 100 μL con un pipettatore.
- Analizza i risultati.
- Leggere la piastra sul sistema di analisi del flusso a doppio reporter per determinare l'MFI di ciascuna reazione utilizzando le seguenti impostazioni dello strumento: volume di aspirazione = 50 μL; numero minimo di perline = 100 perline; impostazione timeout = 40 s; gating: 7.000-17.000; modalità di funzionamento = Dual Reporter.
- Con il sistema a doppio reporter, assicurarsi che il Canale Reporter 1 misuri la fluorescenza PE arancione (quantità di rhPD-L1 attaccata alle perle coniugate rhPD-1) e che il Canale Reporter 2 misuri la fluorescenza blu BV421 (quantità di anticorpo bloccante attaccato legato a rhPD-L1).
- Eseguire pozzetti duplicati per ogni condizione e calcolare la media dei due valori MFI di output per ogni condizione prima di eseguire ulteriori calcoli e grafici dei dati.
- Standardizzare il valore MFI di ciascun campione rispetto al controllo negativo e calcolare la percentuale di inibizione per ciascun campione:
Inibizione% = (100 × [MFI di controllo negativo − MFI campione])/MFI di controllo negativo
NOTA: I valori MFI del controllo negativo (nessuna inibizione) sono i valori più alti; l'MFI del segnale PD-L1 legato è del 100% e l'inibizione del legame di rhPD-L1 a rhPD-1 è definita come 0%.
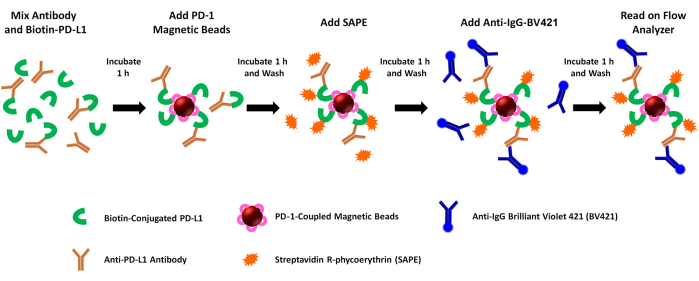
Figura 1: Schema del saggio di blocco PD-1/PD-L1 a doppio reporter. Il PD-L1 umano ricombinante biotinilato (rhPD-L1) viene pre-incubato con anticorpi anti-PDL1 indotti da PDL1-Vaxx selezionati prima di combinarsi con microsfere magnetiche accoppiate a rhPD-1 per consentire la formazione del complesso del checkpoint PD-1/PD-L1. La rhPD-L1 complessata viene quindi rilevata e marcata con l'aggiunta di ficoeritrina accoppiata a streptavidina (SAPE, fluoroforo arancione). Gli anticorpi contro gli epitopi PDL1-Vaxx hanno come bersaglio rhPD-L1 che si è complessato con rhPD-1 pre-accoppiato alle biglie magnetiche e sono illuminati utilizzando un anticorpo secondario coniugato Brilliant Violet 421 (BV421, fluoroforo blu). Sia gli anticorpi rhPD-L1 biotinilati che sono complessati con PD-1 (segnale PE) che gli anticorpi anti-PDL1 che riconoscono e legano rhPD-L1 (segnale BV421) vengono analizzati contemporaneamente utilizzando uno strumento citometrico a flusso a doppio reporter che interroga i campioni per entrambi i fluorofori in due canali reporter separati. I valori di output per ciascun campione sono l'intensità mediana della fluorescenza di ciascun fluoroforo. L'inibizione della formazione del complesso PD1/PD-L1 da parte di diversi anticorpi indotti da PDL1-Vaxx viene quindi estrapolata confrontando i segnali sperimentali con quelli generati utilizzando un anticorpo monoclonale di controllo negativo che non lega rhPD-L1 (0% di inibizione). Fare clic qui per visualizzare una versione più grande di questa figura.
Risultati Rappresentativi
Il test è stato in grado di quantificare con precisione l'inibizione dell'interazione PD-1/PD-L1 da parte di quattro anticorpi policlonali unici, generati contro i peptidi del vaccino rhPD-L1, che sono in fase di studio come potenziali agenti terapeutici del cancro. Lo schema di questo test è riportato nella Figura 1. La quantità di rhPD-L1 biotinilato che si lega alle perle coniugate con rhPD-1 e l'inibizione di questo legame da parte dei quattro candidati anticorpi indotti da PLD1-Vaxx sono stati misurati nel Canale Reporter 1 utilizzando un reagente di rilevamento streptavidina-PE che lega direttamente rhPD-L1 (Figura 2).
Tutti e quattro gli anticorpi policlonali anti-PDL1-peptide hanno bloccato l'interazione rhPD-L1 con PD-1 che era stata immobilizzata su microsfere in misura variabile. La percentuale di inibizione dei diversi anticorpi anti-peptide PDL1 variava dal 48% al 74% alla concentrazione massima testata di 1.000 μg/mL. L'anticorpo monoclonale di controllo positivo atezolizumab ha raggiunto un blocco del 92% dell'interazione PD-1/PD-L1 alla concentrazione massima testata14 di 4 μg/mL (Figura 2). Tutti gli anticorpi sperimentali PDL1-Vaxx hanno mostrato un'inibizione concentrazione-dipendente del legame di rhPD-L1 alle perle coniugate rhPD-1 rispetto a trastuzumab, l'anticorpo di controllo negativo che non si prevedeva interagisse con il sistema PD-1/PD-L1.
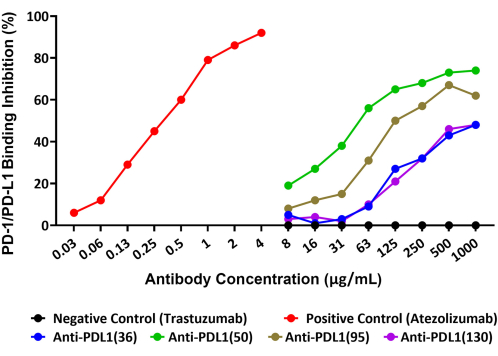
Figura 2: Blocco dell'interazione di rhPD-L1 con rhPD-1 accoppiato a biglie magnetiche da parte di anticorpi anti-peptide PDL1, come mostrato da un nuovo test immunologico basato su microsfere fluorescenti. PD-1 umano ricombinante è stato accoppiato a microsfere magnetiche e le perle sono state quindi incubate con rhPD-L1 biotinilato che era stato pre-incubato con diversi anticorpi anti-peptide PDL1. È stato utilizzato un reagente per la rilevazione di streptavidina-ficoeritrina per legare la biotina e, quindi, valutare la quantità relativa di rhPD-L1 disponibile per legarsi a PD-1. Gli anticorpi policlonali allevati nei conigli contro i vaccini peptidici PDL1 (anti-PDL1[36], anti-PDL1[50], anti-PDL1[95] e anti-PDL1[130]) sono stati testati per l'attività inibitoria e hanno mostrato un blocco del 48%-74% delle interazioni ricombinanti PD-1/PD-L1 alla massima concentrazione testata. Atezolizumab (un diverso anticorpo monoclonale anti-PDL1) è stato utilizzato come controllo positivo. L'anticorpo monoclonale commerciale trastuzumab (anti-HER2) non correlato è stato utilizzato come controllo negativo. Questa figura è adattata da Guo et al.14. Fare clic qui per visualizzare una versione più grande di questa figura.
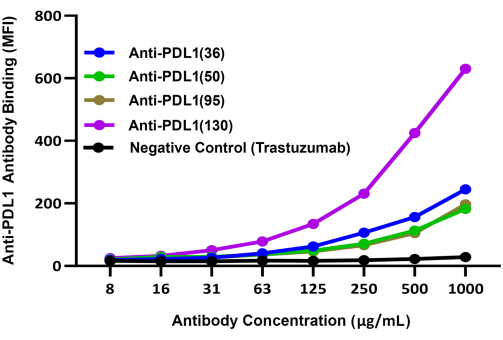
Figura 3: Legame comparativo di diversi anticorpi indotti da PDL1-Vaxx a rhPD-L1 complessati con microsfere magnetiche rivestite con rhPD1. L'anticorpo di rilevamento secondario coniugato viola brillante 421 è stato utilizzato per confrontare il legame di diversi anticorpi policlonali anti-PDL1-peptide di coniglio a rhPD-L1 tramite perline rivestite di rhPD-1. Il segnale di fluorescenza blu BV421 è stato registrato nel Canale Reporter 2 dello strumento a doppio reporter; questo segnale è correlato con l'efficienza di legame relativa degli anticorpi sperimentali anti-PDL1-peptide. Trastezumab (anti-HER2), un anticorpo monoclonale che ha come bersaglio un checkpoint diverso da PD-1/PD-L1, è stato utilizzato come controllo negativo. L'MFI rappresenta l'intensità media di fluorescenza delle microsfere, misurata in pozzetti di reazione duplicati per condizione. Questa figura è adattata da Guo et al.14. Fare clic qui per visualizzare una versione più grande di questa figura.
Le capacità relative dei quattro anticorpi candidati sperimentali indotti da PDL1-Vaxx di legare rhPD-L1 sono state confrontate utilizzando un sistema di rilevamento separato (IgG anti-coniglio coniugato con BV421) che è stato valutato sul secondo canale reporter dello strumento. Questi risultati hanno indicato che tutti e quattro gli anticorpi policlonali anti-PDL1-peptide si legano a rhPD-L1 in modo concentrazione-dipendente14 (Figura 3). L'anticorpo anti-PDL1(130) ha mostrato il più alto segnale di legame rhPDL1 tra i quattro candidati anticorpi indotti da PDL1-Vaxx.
Discussione
Lo scopo dell'immunoterapia del cancro correlata al checkpoint è quello di interrompere l'interazione tra le proteine del checkpoint e i loro importanti ligandi nella sopravvivenza e nella progressione del tumore2. Questo gruppo di ricerca sta attivamente sviluppando nuovi vaccini PD-1 e PD-L1 che suscitano una risposta anticorpale che prende di mira e interrompe il checkpointPD-1/PD-L1 3,8,13,14. In precedenza, sono state eseguite due varianti di saggi di immunoassorbimento enzimatico (ELISA) per valutare gli effetti degli anticorpi anti-peptide PDL1 sull'inibizione dell'interazione ricombinante PD1/PD-L114. (1) Nella prima variante, rhPD-L1 è stato rivestito su una piastra per microtitolazione, quindi la piastra è stata incubata con anticorpi diluiti indotti dal candidato vaccino anti-PDL1. L'inibizione dell'interazione ricombinante PD-1/PD-L1 da parte degli anticorpi è stata quindi valutata aggiungendo rhPD-1 biotinilato e quantificando il legame con rhPD-L1 immobilizzato utilizzando un coniugato streptavidina-perossidasi di rafano e un substrato colorimetrico. Lo abbiamo definito come il test del blocco diretto. (2) Nella seconda variante, PD-1 è stato rivestito sulla piastra per microtitolazione. rhPD-L1 biotinilato è stato pre-incubato con ciascuno degli anticorpi policlonali indotti dal candidato anti-PLD1 in provette di reazione separate. Le miscele rhPDL1/anti-PDL1 sono state quindi aggiunte ai pozzetti a piastre contenenti rhPD-1 immobilizzato e lasciate reagire. Qualsiasi rhPDL1 che ha reagito con rhPD-1 immobilizzato in presenza degli anticorpi indotti da PDL1-Vaxx potenzialmente bloccanti è stato rilevato con successiva streptavidina-HRP e incubazione colorimetrica del substrato. Lo abbiamo definito come il test di blocco inverso.
Il blocco inverso dell'interazione ricombinante PD-1/PD-L1 da parte degli anticorpi anti-PDL1-peptide ha mostrato l'inibizione del segnale (cioè il blocco PD-1/PD-L1) in modo dipendente dalla concentrazione dell'anticorpo14, mentre l'approccio del blocco diretto non ha fornito risultati coerenti (non mostrato). Il test di blocco dual-reporter basato su microsfere è stato sviluppato per verificare i risultati ELISA e per studiare il blocco dell'interazione PD-1/PD-L1 in una fase fluida, che elimina i potenziali problemi di ostacolo sterico/disponibilità dell'epitopo di legame associati all'immobilizzazione delle proteine ricombinanti sul fondo del pozzo. L'analisi delle microsfere è stata direttamente correlata ai risultati del blocco ELISA utilizzando il saggio di blocco inverso (Figura 2). Inoltre, i test immunologici basati sulla fluorescenza possono fornire una migliore sensibilità del test e un intervallo dinamico più ampio rispetto agli ELISA colorimetrici18 e, inoltre, il test basato su microsfere multiplexate consente l'esecuzione simultanea di due test immunologici indipendenti all'interno di una singola reazione. Il sulfo-NHS e l'EDC utilizzati per l'accoppiamento covalente delle microsfere a rhPD-1 potrebbero aver portato alle differenze di prestazioni osservate tra i saggi di blocco diretto e di blocco inverso e le differenze di sensibilità osservate tra i saggi di interazione PD-1/PD-L1 ricombinante basati su microsfere ELISA e Luminex. Ulteriori indagini a livello chimico e molecolare sono necessarie per studiare i possibili meccanismi responsabili di queste differenze.
Sia lo studio ELISA14 che i saggi basati su microsfere dimostrano che gli anticorpi anti-PDL1-PDL1 indotti da PDL1-Vaxx possono inibire la formazione del complesso del checkpoint PD1/PD-L1. Il PDL1-Vaxx a base di peptidi induce con successo anticorpi anti-PDL1 che possono bloccare l'interazione PD-1/PD-L1. Questo approccio può servire come nuova strategia terapeutica per il trattamento del cancro, come supportato da studi preclinici sugli animali 3,13,14. Gli studi clinici pianificati determineranno l'efficacia del PDL1-Vaxx per l'immunoterapia del checkpoint e il controllo della malattia nei pazienti oncologici.
Divulgazioni
Pravin T.P. Kaumaya è un consulente di Imugene, Ltd.
Riconoscimenti
Gli autori ringraziano Sherry Dunbar PhD, MBA di Luminex Corporation (Austin, TX) per il supporto alla ricerca e Matthew Silverman PhD di Biomedical Publishing Solutions (Panama City, FL; mattsilver@yahoo.com) per l'assistenza scientifica e di scrittura. Questo lavoro è stato sostenuto da premi a Pravin T. P. Kaumaya del National Institutes of Health (R21 CA13508 e R01 CA84356) e Imugene Ltd, Sydney, Australia (OSU 900600, GR110567 e GR124326).
Materiali
| Name | Company | Catalog Number | Comments |
| Buffers | |||
| Activation Buffer: 0.1 M NaH2PO4, pH 6.2 | Millipore/Sigma | S3139 | |
| Assay/Wash Buffer: PBS-TBN (1x PBS, pH 7.4 + 0.1% BSA + 0.05 % (v/v) Tween-20; 0.05% NaN3) | Millipore/Sigma | P3563 (PBS+Tween20), A7888 (Bovine serum albumin), S8032 (sodium azide) | |
| Coupling Buffer: 50 mM 2-morpholinoethanesulfonic acid (MES), pH 5.0 | MilliporeSigma | M2933 | |
| Coupling Reagents | |||
| 1-Ethyl-3-[3-dimethylaminopropyl]carbodiimide hydrochloride (EDC) | ThermoFisher Scientific (Waltham, MA) | 77149 | |
| xMAP Antibody Coupling Kit (if desired), includes: | Luminex Corp. (Austin, TX) | 40-50016 | |
| EDC, 10 mg | |||
| sNHS solution, 250 µL | |||
| Activation/Coupling Buffer: 0.1 M 2-morpholinoethanesulfonic acid (MES), pH 6.0 | |||
| Wash Buffer: 1x PBS, pH 7.4 + 0.1% BSA + 0.05 % (v/v) Tween-20; 0.05% NaN3 (PBS-TBN) | |||
| Sulfo-NHS (N-hydroxysulfosuccinimide) | ThermoFisher Scientific (Waltham, MA) | 24510 | |
| Instrumentation and Ancillary Lab Supplies | |||
| xMAP INTELLIFLEX (dual-reporter instrument) | Luminex Corp. (Austin, TX) | INTELLIFLEX-DRSE-RUO | |
| Low protein-binding round bottom 96-well plate | ThermoFisher Scientific (Waltham, MA) | 07-200-761 | |
| Luminex Magnetic Plate Separator (or comparable) | Luminex Corp. (Austin, TX) | CN-0269-01 | |
| Luminex Magnetic Tube Separator (or comparable) | Luminex Corp. (Austin, TX) | CN-0288-01 | |
| MagPlex Microspheres (magnetic, fluorescent, 6.5-µm-diameter beads) | Luminex Corp. (Austin, TX) | MC-1**** (varies by bead label) | |
| Protein LoBind microcentrifuge tubes | ThermoFisher Scientific (Waltham, MA) | 022431081 | |
| Peptides, Antibodies, & Detection Reagents | |||
| Atezolizumab (humanized anti-PDL1 IgG1 monoclonal antibody), positive control | Genentech/Roche (San Francisco, CA) | n/a (prescription medications) | |
| Biotinylated recombinant human PDL1 | Sino Biological (Wayne, PA) | 10084-H49H-B | |
| Brilliant Violet 421-congugated donkey anti-human IgG | Jackson Immunoresearch Laboratories Inc. (Westgrove, PA) | 709-675-149 | |
| Brilliant Violet 421-congugated donkey anti-rabbit IgG | Jackson Immunoresearch Laboratories Inc. (Westgrove, PA) | 711-675-152 | |
| Recombinant human PD-1 (poly-histidine tagged) | Acro Biosystems (Newark, DE) | PD1-H5256 | |
| Streptavidin-conjugated R-phycoerythrin (SAPE) | Agilent (Santa Clara, CA) | PJRS34-1 | |
| Trastuzumab (Herceptin, humanized anti-HER2 monoclonal antibody), negative control | Genentech/Roche (San Francisco, CA) | n/a (prescription medications) |
Riferimenti
- Kaumaya, P. T. B-cell epitope peptide cancer vaccines: a new paradigm for combination immunotherapies with novel checkpoint peptide vaccine. Future Oncology. 16 (23), 1767-1791 (2020).
- Pandey, P., et al. Revolutionization in cancer therapeutics via targeting major immune checkpoints PD-1, PD-L1 and CTLA-4. Pharmaceuticals. 15 (3), 335 (2022).
- Guo, L., Overholser, J., Good, A. J., Ede, N. J., Kaumaya, P. T. P. Preclinical studies of a novel human PD-1 B-cell peptide cancer vaccine PD1-Vaxx from BALB/c mice to beagle dogs and to non-human primates (cynomolgus monkeys). Frontiers in Oncology. 12, 826566 (2022).
- Brahmer, J. R., Hammers, H., Lipson, E. J. Nivolumab: Targeting PD-1 to bolster antitumor immunity. Future Oncology. 11 (9), 1307-1326 (2015).
- Shah, N. J., Kelly, W. J., Liu, S. V., Choquette, K., Spira, A. Product review on the Anti-PD-L1 antibody atezolizumab. Human Vaccines & Immunotherapeutics. 14 (2), 269-276 (2018).
- Postow, M. A., Sidlow, R., Hellmann, M. D. Immune-related adverse events associated with immune checkpoint blockade. The New England Journal of Medicine. 378 (2), 158-168 (2018).
- Kaumaya, P. T. A paradigm shift: Cancer therapy with peptide-based B-cell epitopes and peptide immunotherapeutics targeting multiple solid tumor types: Emerging concepts and validation of combination immunotherapy. Human Vaccines & Immunotherapeutics. 11 (6), 1368-1386 (2015).
- Guo, L., Kaumaya, P. T. P. First prototype checkpoint inhibitor B-cell epitope vaccine (PD1-Vaxx) en route to human Phase 1 clinical trial in Australia and USA: Exploiting future novel synergistic vaccine combinations. British Journal of Cancer. 125 (2), 152-154 (2021).
- Dakappagari, N. K., Douglas, D. B., Triozzi, P. L., Stevens, V. C., Kaumaya, P. T. Prevention of mammary tumors with a chimeric HER-2 B-cell epitope peptide vaccine. Cancer Research. 60 (14), 3782-3789 (2000).
- Dakappagari, N. K., et al. Conformational HER-2/neu B-cell epitope peptide vaccine designed to incorporate two native disulfide bonds enhances tumor cell binding and antitumor activities. The Journal of Biological Chemistry. 280 (1), 54-63 (2005).
- Kaumaya, P. T., et al. Phase I active immunotherapy with combination of two chimeric, human epidermal growth factor receptor 2, B-cell epitopes fused to a promiscuous Tcell epitope in patients with metastatic and/or recurrent solid tumors. Journal of Clinical Oncology. 27 (31), 5270-5277 (2009).
- Bekaii-Saab, T., et al. Phase I immunotherapy trial with two chimeric HER-2 B-cell peptide vaccines emulsified in montanide ISA 720VG and Nor-MDP adjuvant in patients with advanced solid tumors. Clinical Cancer Research. 25 (12), 3495-3507 (2019).
- Kaumaya, P. T. P., Guo, L., Overholser, J., Penichet, M. L., Bekaii-Saab, T. Immunogenicity and antitumor efficacy of a novel human PD-1 B-cell vaccine (PD1-Vaxx) and combination immunotherapy with dual trastuzumab/pertuzumab-like HER-2 B-cell epitope vaccines (B-Vaxx) in a syngeneic mouse model. Oncoimmunology. 9 (1), 1818437 (2020).
- Guo, L., Overholser, J., Darby, H., Ede, N. J., Kaumaya, P. T. P. A newly discovered PD-L1 B_cell epitope peptide vaccine (PDL1-Vaxx) exhibits potent immune responses and effective anti-tumor immunity in multiple syngeneic mice models and (synergizes) in combination with a dual HER-2 B-cell vaccine (B-Vaxx). Oncoimmunology. 11 (1), 2127691 (2022).
- . Luminex Corporation. The xMAP® Cookbook, 5th edition Available from: https://info.luminexcorp.com/en-us/research/download-the-xmap-cookbook?utm_referrr=https%3A%2F%2Fwww.luminexcorp.com%2F (2022)
- MagPlex® Microspheres Documentation. Product information sheet. Luminex Corporation Available from: https://www.luminexcorp.com/magplex-microspheres/#overview (2014)
- Green, M. R., Sambrook, J. . Estimation of cell number by hemocytometry counting. 2019 (11), (2019).
- Selecting the Detection System - Colorimetric, Fluorescent, Luminescent Methods for ELISA Assays. Corning Inc Available from: https://www.corning.com/catalog/cls/documents/application-notes/CLS-DD-AN-458.pdf (2019)
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon