È necessario avere un abbonamento a JoVE per visualizzare questo. Accedi o inizia la tua prova gratuita.
Un modello fotopolimerizzabile di acido ialuronico-collagene del microambiente di glioma invasivo con flusso interstiziale
In questo articolo
Riepilogo
Presentiamo un metodo per replicare il microambiente tumorale del glioma nella parte anteriore invasiva che incorpora il flusso di liquido interstiziale. Questo modello è un idrogel di acido ialuronico I in un inserto di coltura tissutale in cui è possibile applicare una testa di pressione del fluido. L'invasione può essere quantificata e le cellule possono essere isolate o lisate.
Abstract
La recidiva del glioblastoma è uno dei principali ostacoli al successo del trattamento ed è guidata dall'invasione di cellule staminali del glioma (GSC) in tessuti sani che sono inaccessibili alla resezione chirurgica e sono resistenti alle chemioterapie esistenti. Il movimento del fluido a livello tissutale, o flusso interstiziale del fluido (IFF), regola l'invasione delle GSC in modo dipendente dal microambiente tumorale (TME), evidenziando la necessità di sistemi modello che incorporino sia l'IFF che il TME. Presentiamo un metodo accessibile per replicare il TME invasivo nel glioblastoma: un idrogel di acido ialuronico e collagene I composto da GSC umane, astrociti e microglia seminate in un inserto di coltura tissutale. L'IFF elevato può essere rappresentato applicando una testa di pressione del fluido all'idrogel. Inoltre, questo modello può essere regolato per replicare le differenze inter o intra-paziente nei rapporti cellulari, nelle velocità di flusso o nelle rigidità della matrice. L'invasione può essere quantificata, mentre i gel possono essere raccolti per una varietà di risultati, tra cui l'invasione di GSC, la citometria a flusso, l'estrazione di proteine o RNA o l'imaging.
Introduzione
Il glioblastoma è una malattia devastante, caratterizzata da una breve sopravvivenza1 che viene estesa solo moderatamente dai trattamenti clinicamente disponibili 2,3. Questo impedimento a una terapia efficace è in gran parte guidato dalla natura altamente infiltrativa delle cellule staminali del glioma chemioresistente (GSC) che sono inaccessibili alla resezione e seminano tumori ricorrenti4. Allo stesso tempo, le GSC sono altamente plastiche e rispondono a diversi stimoli nel microambiente tumorale (TME) per sopravvivere e invadere 5,6. In particolare, il tumore densamente popolato e la vascolarizzazione permeabile producono un ripido differenziale di pressione al bordo del tumore, aumentando il flusso di liquido interstiziale (IFF) in regioni distinte che sono correlate all'invasione di GSC7. Questo aumento dell'IFF influenzal'8,9,10 e spesso aumenta l'invasionedell'8,9 GSC attraverso vie molecolari suscettibili di inibizione farmacologica. Tuttavia, questo processo è confuso dall'influenza della glia nel TME sull'invasione del glioma; infatti, è stato descritto che la glia modula l'invasione del glioma in numerosi contesti11, e prove preliminari nel nostro laboratorio indicano un'influenza simile della glia sull'invasione del glioma12 potenziata da IFF. Pertanto, il nostro laboratorio ha sviluppato un modello TME 3D sintonizzabile che replica queste regioni invasive del bordo tumorale incorporando sia l'IFF che le interazioni glia-GSC per quantificare l'invasione di GSC e altri esiti (ad esempio, espressione proteica superficiale o intracellulare, espressione dell'RNA, ecc.) influenzati da IFF, glia e/o terapie candidate12 (Figura 1).
Il modello TME è simile ad altri saggi di flusso di fluidi interstiziali basati su inserti di colture tissutali (ad es. saggi statici/di flusso) che sono stati ampiamente pubblicati 8,9,10,13,14,15,16,17,18. Le principali distinzioni di questo modello sono l'incorporazione di una matrice di collagene-acido ialuronico non proprietaria e sintonizzabile, l'inclusione di astrociti e microglia nella matrice a rapporti rappresentativi delle TME12 del paziente e il sistema è interamente racchiuso in una piastra a pozzetti, priva di tubi esterni, serbatoi o pompe. L'acido ialuronico è tra i principali componenti della matrice extracellulare cerebrale19, ma non è sufficiente a consentire il flusso di liquidi; quindi, il collagene I è incluso nella miscela. La reticolazione avviene in due fasi: una polimerizzazione a catena iniziata da radicali liberi in cui dopo l'esposizione alla luce ultravioletta (UV), i radicali liberi vengono prodotti dal fotoiniziatore e generano legami incrociati chimici tra le molecole di acido ialuronico metacrilato20 e la neutralizzazione del collagene conservato in acido e l'esposizione al calore per formare fibre di collagene 21,22,23.
Vari parametri che sono stati ottimizzati per questo test sono stati descritti in lavori precedentemente pubblicati in idrogel di acido ialuronico-collagene modificatocon tiolo 8,12. In particolare, le cellule (GSC24 umane primarie, astrociti corticali umani primari e microglia umane immortalizzate) utilizzate per questo test sono vitali per almeno il 60% per 3 giorni in gel composti da terreni astrobasali integrati con fattori di crescita GSC, 0,5% v/v N-2 e 1% v/v B-27 senza vitamina A12. Nei casi in cui i gel devono essere degradati (ad esempio, per l'estrazione di proteine o la citometria a flusso), vengono utilizzate collagenasi e dispasi e mantengono una vitalità sufficiente (Figura 2).
Per quantificare l'invasione, le GSC devono essere marcate in fluorescenza prima di essere combinate con la glia nella matrice. Ciò può essere ottenuto mediante marcatura con Hoechst 33342 (come descritto di seguito), tracciatori cellulari12, modificazione genetica o trasduzione. Indipendentemente da ciò, la vitalità delle cellule marcate con nuovi marcatori deve essere misurata prima di incorporarle nel modello TME. In alternativa, se l'invasione non sarà quantificata ma i gel verranno raccolti per l'estrazione di proteine, estrazioni di RNA o altri risultati, le cellule spesso non hanno bisogno di essere marcate in fluorescenza durante il processo di preparazione del gel. In tal caso, i gel possono essere fissati in formalina per l'imaging, degradati e lisati con cellule per l'estrazione dell'RNA, oppure degradati utilizzando proteasi per la citometria a flusso e successivamente lisati con tamponi di lisi proteica per Western blot o altri lavori proteici.
Qui, presentiamo un protocollo per incorporare astrociti umani, microglia e GSC derivate da pazienti in un rapporto definito dal paziente, 4:1:112, in una matrice di collagene I da 1,2 mg/mL e 4 mg/mL di acido ialuronico in condizioni statiche di flusso. I parametri specifici utilizzati per un test (ad esempio, rapporti cellulari, rigidità, tipi di cellule, ecc.) possono essere modificati per rappresentare contesti diversi se la vitalità è adeguata.
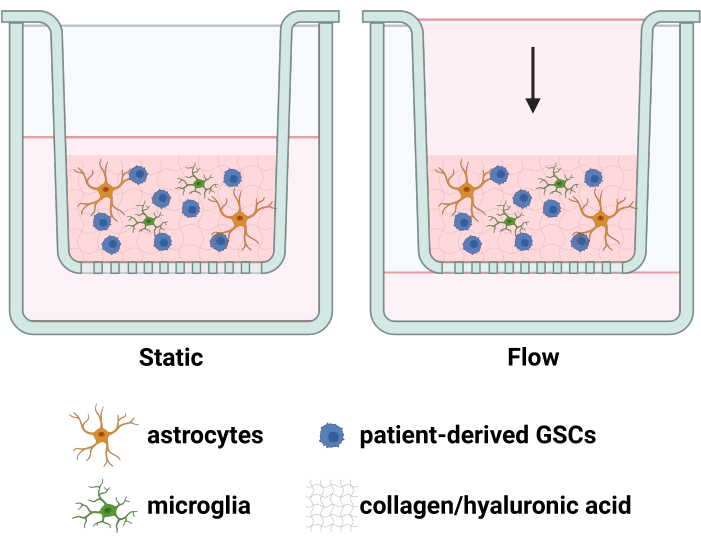
Figura 1: Diagramma del modello TME costituito da GSC, astrociti e microglia in un idrogel sotto una testa di pressione del fluido. Le cellule sono incorporate in un idrogel di collagene-acido ialuronico all'interno di un inserto di coltura tissutale. La forza gravitazionale spinge il flusso netto verso il basso. I pori della membrana dell'inserto di coltura tissutale consentono alle cellule che invadono verso il basso di attaccarsi alla superficie inferiore dell'inserto di coltura tissutale e queste cellule possono essere fissate, visualizzate e quantificate. Creato con BioRender.com. Clicca qui per visualizzare una versione più grande di questa figura.
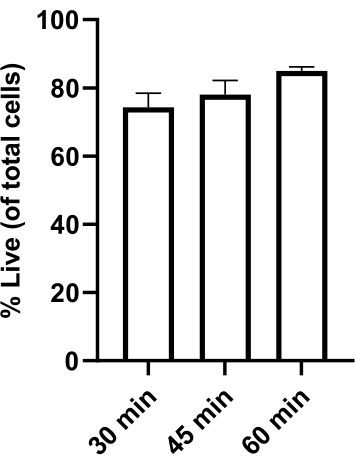
Figura 2: Vitalità cellulare dopo la degradazione dell'idrogel. I G34 (GSC), gli astrociti e le microglia sono stati seminati nel modello TME a 4:1:1 e incubati per 21 ore a 37 °C. I gel sono stati rimossi e degradati utilizzando 0,3 mg/mL di collagenasi + 0,02 mg/mL di dispasi per un totale di 30, 45 o 60 minuti, pipettando per miscelare ogni 15 minuti (condizione di 30 minuti) o a 30 minuti e poi ogni 15 minuti (condizioni di 45 minuti e 60 minuti). Dopo che i gel sono stati degradati, le cellule sono state colorate con arancio acridina (tutte le cellule) e ioduro di propidio (cellule morte) e contate utilizzando un contatore di cellule automatizzato. La vitalità è riportata per tutte le cellule all'interno del modello TME. Le cellule hanno mantenuto almeno il 70% di vitalità per 30-60 minuti. I dati sono presentati come media ± SEM; n = 3 repliche biologiche. Clicca qui per visualizzare una versione più grande di questa figura.
Protocollo
Questo protocollo è stato sviluppato in conformità con le linee guida stabilite dal Virginia Tech Institutional Biosafety Committee.
NOTA: Eseguire tutte le procedure in una cella per colture cellulari BSL-2, se non diversamente specificato. Si prega di consultare il comitato per la biosicurezza dell'istituzione per indicazioni sull'uso delle cellule umane.
1. Calcoli per la preparazione del gel
- Calcola il numero di condizioni necessarie per l'esperimento.
NOTA: Una "condizione" è definita dal contenuto della soluzione (ad esempio, concentrazioni di cellule, concentrazioni di collagene, ecc.), non da variabili applicate esternamente, come la testa di pressione del fluido utilizzata in questo esempio. - Calcolare il volume totale di gel necessario per ciascuna soluzione di condizione.
NOTA: Il volume richiesto per i gel a 12 pozzetti che utilizzano inserti per colture tissutali di 12 mm di diametro è di 100-150 μl per inserto. Si raccomandano almeno tre repliche tecniche per quantificare l'invasione. Inoltre, per tenere conto della perdita di volume dovuta all'errore di pipettaggio, aggiungere il volume di una replica aggiuntiva a ciascuna soluzione di condizione. - Calcolare il volume totale di soluzione in gel richiesto per l'esperimento dal passaggio 1.2.
- Calcolare il volume totale di 3 mg/mL di soluzione di collagene necessaria per l'esperimento. Aggiungere almeno il 10% a questo volume per tenere conto della perdita di volume durante il pipettaggio.
Volume totale 3 mg/mL di collagene = 0,4 × Volume totale della soluzione in gel - Calcolare i volumi di collagene I ad alta concentrazione di coda di ratto, NaOH sterile 1 N, PBS sterile 10x e acqua sterile per ciascun componente della soluzione di collagene da 3 mg/mL alle concentrazioni finali date (cf): collagene I cf = 3 mg/mL, NaOH cf = 2,3% v/v del volume di collagene I e PBS cf = 1x. Diluire le soluzioni in acqua sterile ultrapura (18,2 MΩ·cm).
- Calcolare i volumi di soluzione di collagene 3 mg/mL, acido ialuronico metacrilato all'1% p/v e fotoiniziatore, 17 mg/mL di litio fenil-2,4,6-trimetilbenzoilfosfinato (LAP) e terreni di coltura cellulare per ciascuna delle soluzioni condizionali alle concentrazioni finali date (cf): collagene cf = 1,2 mg/mL, acido ialuronico cf = 0,4% p/v, LAP cf = 2% v/v del volume di acido ialuronico. Diluire le soluzioni nei terreni di coltura cellulare contenenti cellule.
- Calcolare il numero di cellule per ciascuna soluzione di condizione al rapporto desiderato (ad esempio, 100.000 GSC per 100 uL di idrogel con un rapporto di 4:1:1 GSC:astrociti:microglia).
2. Preparazione dei materiali
- Nella settimana precedente l'esperimento, piastre GSC, astrociti e microglia.
NOTA: La piastra deve produrre circa il doppio del numero di cellule rispetto a quello necessario per i gel per tenere conto sia del passaggio che della perdita di cellule durante la procedura. - Preparare una soluzione di lavoro del fotoiniziatore, LAP, a 17 mg/mL in 1x PBS sterile. Proteggilo dalla luce.
- Ricostituire l'acido ialuronico metacrilato in 1x PBS secondo le istruzioni del produttore. Sigillare il coperchio e agitare delicatamente la sospensione per 1 ora, o fino a quando non si scioglie, a 4 °C.
NOTA: L'acido ialuronico metacrilato utilizzato in questo protocollo è stabile per circa 1 mese a 4 °C come specificato dal produttore. Proteggilo dalla luce. - Installare una lampada UV utilizzando un diodo a emissione di luce collimato (LED) con una lunghezza d'onda nominale di 385 nm a un'intensità di 50 mW/cm2 sulla superficie del gel. Posizionare la lampada nell'armadio per colture cellulari.
ATTENZIONE: I raggi UV possono danneggiare gli occhi. Indossare occhiali protettivi e non guardare direttamente nella lampada.
NOTA: Condurre esperimenti separati per garantire che la vitalità o il risultato funzionale misurato non siano influenzati in modo significativo dall'esposizione alla luce a 385 nm a 50 mW/cm2 durante il periodo di esposizione (45 s). - Preparare i terreni (terreni astrobasali + 0,5% v/v N-2 + 1% v/v B-27 senza vitamina A) per l'esperimento.
NOTA: Combinare i componenti del terreno e filtrare attraverso un sistema di vuoto a poro da 0,22 μm per garantire la sterilità. Evitare cicli di gelo-disgelo dei fattori di crescita (N-2 e B-27) per prevenire la degradazione. - Preparare 1 N NaOH in una cappa aspirante con il paraspruzzi in posizione.
ATTENZIONE: 1 N NaOH è altamente corrosivo. Maneggiare con cura, indossare una protezione per gli occhi o utilizzare un paraspruzzi e tenere la soluzione sotto una cappa aspirante. - Preparare acqua ultrapura sterile (18,2 MΩ·cm).
3. Celle passanti e GSC di marcatura
- Passaggio di astrociti, microglia e GSC secondo le istruzioni del produttore.
- Etichettare le GSC con Hoechst 33342 seguendo le raccomandazioni del produttore.
ATTENZIONE: Hoescht 33342 può causare grave irritazione oculare e può indurre danni al DNA. Maneggiare con cura. - Centrifugare tutte le celle a 200 x g per 5 minuti a RT.
- Scaricare delicatamente il surnatante e rimuovere il terreno in eccesso con una pipetta.
- Risospendere le GSC in 1x PBS.
- Centrifugare le GSC a 200 x g per 5 min.
- Risospendere tutte le cellule nel terreno (terreno astrobasale + 0,5% N-2 v/v + 1% v/v B-27) per l'esperimento.
- Conta tutte le celle.
- Aggiungere il numero assoluto di cellule necessarie per ciascuna soluzione di condizione in una fiala per soluzione di condizione. Posizionarli a 37 °C, 5% di CO2 fino al momento dell'uso.
4. Preparazione degli idrogel
NOTA: Eseguire i passaggi dopo aver aperto l'acido ialuronico metacrilato e il fotoiniziatore al buio fino a quando i gel non sono stati foto-reticolati.
- Mettere sul ghiaccio il collagene 8-11 mg/mL (alta concentrazione), 1 N NaOH, acqua ultrapura sterile (18,2 MΩ·cm), PBS sterile, una provetta da microcentrifuga (per la soluzione di collagene da 3 mg/mL), acido ialuronico metacrilato e il fotoiniziatore.
NOTA: Tutti i materiali che entrano in contatto con la soluzione di collagene devono essere mantenuti su ghiaccio per evitare la reticolazione prematura. - Posizionare gli inserti di coltura tissutale nella piastra ed etichettare la piastra.
- Utilizzando i valori calcolati, preparare la soluzione di collagene da 3 mg/mL combinando collagene ad alta concentrazione, 1 N NaOH, acqua ultrapura (18,2 MΩ·cm) e 10x PBS. Aggiungere i componenti a goccia e tenere il puntale della pipetta immerso durante la miscelazione per evitare la formazione di bolle.
NOTA: Se si formano bolle, la centrifugazione o il picchiettamento della provetta su una superficie dura spesso rimuove le bolle. Inoltre, i terreni contenenti rosso fenolo saranno gialli se il pH è troppo acido; in questo caso dovrebbe essere aggiunto più NaOH. - Centrifugare le celle a 200 x g per 5 minuti a RT.
- Rimuovere delicatamente il terreno in eccesso dalla parte superiore di ciascuna soluzione per la condizione cellulare, lasciando il volume di terreno necessario per la condizione. Metti queste soluzioni sul ghiaccio.
NOTA: Non trasferire le cellule da questo flaconcino per evitare la perdita di cellule. Invece, aggiungi tutti i componenti della condizione del gel a questa fiala, quindi mescola delicatamente e distribuisci i gel nella piastra. - Aggiungere il volume calcolato di 3 mg/mL di soluzione di collagene per una concentrazione finale di 1,2 mg/mL a ciascuna soluzione per condizioni cellulari dal passaggio 4.5.
- Aggiungere il volume calcolato di acido ialuronico metacrilato all'1% p/v per una concentrazione finale dello 0,4% p/v a ciascuna soluzione per la condizione cellulare del passaggio 4.5.
- Aggiungere il volume calcolato di 17 mg/mL LAP a ciascuna soluzione per condizioni cellulari del passaggio 4.5.
NOTA: Aggiungere questa soluzione appena prima di distribuire i gel nella piastra per massimizzare la vitalità; Il LAP in forma liquida è citotossico. - Una alla volta, mescolare ciascuna provetta e aggiungere 100-150 μl a ciascun inserto di coltura tissutale. Tenere il puntale della pipetta immerso per evitare la formazione di bolle.
- Accendere la lampada UV da 385 nm (impostata a 50 mW/cm2) a corrente costante.
- Fotoreticolare ogni gel, uno alla volta, esponendo ogni pozzetto alla luce UV per 45 s ciascuno.
- Reticolare il collagene posizionando la piastra a 37 °C per 30-45 min.
- Applicare la testina di pressione del fluido ai gel utilizzando astrobasal + 0,5% N-2 v/v + 1% v/v B-27.
- Flusso netto zero (statico): aggiungere 700 μl di terreno nella piastra a pozzetti e 100 μl nell'inserto di coltura tissutale.
- Flusso netto: aggiungere 100 μl di terreno nella piastra a pozzetti e 700 μl nell'inserto di coltura tissutale.
NOTA: Utilizzare l'azione capillare per aggiungere 100 μl sotto l'inserto di coltura tissutale; Questo volume non riempirà la piastra del pozzetto.
- Porre la piastra a 37 °C, 5% CO2, per almeno 18 ore o fino a 5 giorni.
NOTA: I sistemi possono incubare per un massimo di 5 giorni a seconda delle esigenze del saggio, ma un intervallo di tempo di 18-24 ore è sufficiente per gli esperimenti iniziali di invasione, vitalità o proliferazione.
5. Fissaggio delle celle per l'analisi dell'invasione
NOTA: Non lasciare che la membrana dell'inserto per colture tissutali si asciughi e non applicare le soluzioni direttamente sulla membrana per evitare il distacco delle cellule dalla membrana.
- Aspirare i terreni dagli inserti di coltura tissutale e dalla piastra a pozzetti.
- Aspirare i gel dagli inserti di coltura tissutale con una punta P1000.
NOTA: I gel possono essere conservati per l'imaging lasciando i gel nel pozzetto durante questa fase e seguendo il protocollo di fissazione alternativo nella nota del passaggio 5.4. - Lavare delicatamente il pozzetto della piastra con 1x PBS in modo che ogni membrana dell'inserto di coltura tissutale sia coperta.
- Aggiungere il 4% v/v di formalina in PBS alla piastra a pozzetti in modo che ogni membrana dell'inserto di coltura tissutale sia coperta e incubare per 15-20 minuti a RT.
ATTENZIONE: La formalina è un sospetto cancerogeno e può causare gravi danni agli occhi. Utilizzare la formalina in una cappa aspirante con il paraspruzzi in posizione.
NOTA: Questa lunghezza di incubazione fisserà solo le cellule sulla membrana dell'inserto di coltura tissutale. Se i gel vengono conservati per l'imaging, fissarli per 1 ora a 4 °C, facendoli oscillare delicatamente, e aggiungere abbastanza formalina all'inserto di coltura tissutale per permeare il gel. Dopo il fissaggio, lavare accuratamente i gel con PBS per almeno 20 minuti. - Lavare ogni pozzetto con 1x PBS. Successivamente, aggiungere un ulteriore 1x PBS a ciascun pozzetto della piastra e all'inserto di coltura tissutale.
- Utilizzare un batuffolo di cotone per rimuovere i frammenti di gel strofinando il lato superiore di ciascuna membrana dell'inserto di coltura tissutale. Restituire l'eventuale 1x PBS perso in ciascun pozzetto dopo la pulizia per evitare di seccare le membrane.
- Lavare ogni pozzetto e l'inserto di coltura tissutale in 1x PBS.
NOTA: La lastra può essere sigillata e posizionata a 4 °C se necessario, ma le membrane dell'immagine il prima possibile per evitare la perdita di fluorescenza.
6. Imaging e quantificazione
- Sul canale DAPI, creare un'immagine di ciascuna membrana. Se possibile, scatta un'immagine a fluorescenza piastrellata dell'intero pozzo. Se ciò non è possibile, a 20x, riprendi il centro del pozzo e quattro regioni in una formazione a croce che interseca il punto centrale.
NOTA: Escludere i bordi del pozzetto per evitare frammenti di gel e non sovrapporre le regioni di interesse (ROI). - Conta il numero di celle in ogni immagine.
- Calcola la percentuale di GSC seminate che hanno invaso per ogni pozzo:
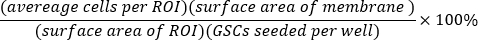
- Calcola la media e la deviazione standard della percentuale di invasione tra le repliche tecniche.
7. Endpoint alternativo: citometria a flusso
NOTA: Oltre o al posto dell'analisi dell'invasione, i gel non fissati possono essere degradati e le cellule raccolte per la citometria a flusso o altre analisi degli endpoint. Viene fornito un protocollo di esempio che analizza la vitalità cellulare (colorazione viva/morta riparabile), la proliferazione (anticorpo Ki67) e la staminalità (anticorpo CD71). Altri marcatori di interesse possono essere sostituiti in questo protocollo dopo aver convalidato l'efficacia della colorazione. In particolare, esiste un'ampia varietà di marcatori che prendono di mira le GSC (esaminati in25). Questo protocollo inizia dopo il passaggio 4.14.
- Degradare gli idrogel.
NOTA: Una concentrazione 2x di soluzioni di collagenasi e dispasi viene preparata prima con terreni sperimentali (astrobasale + 0,5% v/v N-2 + 1% v/v B-27 senza vitamina A), che viene poi aggiunta in un volume uguale di idrogel per raggiungere una concentrazione finale di 1x. Poiché cellule diverse hanno risposte diverse alla degradazione enzimatica, si raccomanda vivamente di controllare la vitalità e la resa cellulare (Figura 2). L'intervallo della concentrazione finale di collagenasi dovrebbe essere 0,2-0,4 mg/mL e l'intervallo della concentrazione finale di dispasi dovrebbe essere 0,01-0,04 mg/mL; in questo esempio, 0,3 mg/mL di collagenasi e 0,02 mg/mL di dispasi vengono utilizzati per degradare gli idrogel.- Preparare 2 soluzioni di collagenasi e dispasi (soluzione di terreno di degradazione in gel). Diluire la collagenasi a 0,6 mg/mL e la dispasi a 0,04 mg/mL con terreni sperimentali (astrobasale + 0,5% N-2 v/v + 1% v/v B-27 senza vitamina A).
- Rimuovere i gel dagli inserti di coltura tissutale e trasferirli in una piastra a 96 pozzetti con fondo a V.
- Aggiungere il volume equivalente di soluzione del terreno di degradazione del gel per idrogel a ciascun pozzetto. Ad esempio, aggiungere 100 μl di soluzione di terreno di degradazione su gel a 100 μl di idrogel.
- Incubare la piastra su un agitatore a 300-500 RPM (orbita: 2 mm) a 37 °C per 15-30 min.
NOTA: Provare l'intervallo minimo, 15 minuti di incubazione, se le cellule sono sensibili alla degradazione enzimatica. - Pipettare ogni idrogel su e giù 30-50 volte per rompere gli idrogel.
NOTA: Gli idrogel saranno facili da pipettare una volta che saranno completamente degradati. Se i gel non possono essere pipettati facilmente, i gel devono essere incubati su un agitatore a 300-500 giri/min (orbita: 2 mm) a 37 °C per altri 15 minuti. Quindi, pipettare ogni idrogel su e giù 30-50 volte per rompere i gel.È importante sottolineare che il tempo di incubazione per la degradazione degli idrogel non deve superare 1 ora; Ciò potrebbe portare a una bassa vitalità cellulare. - Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
NOTA: Il surnatante può essere rimosso mediante pipettaggio o capovolgendo rapidamente la piastra su un vassoio di scarto. - Risospendere le cellule con 50 μL di PBS 1x e raggruppare tre repliche tecniche in un unico pozzetto per ottenere una singola replica biologica.
- Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante per continuare con la citometria a flusso.
- Blocca l'associazione non specifica.
- Lavare le celle con 200 μl di 1x PBS/pozzetto, centrifugare la piastra a 625 x g per 1 min a 4 °C ed eliminare il surnatante. Eseguire tutti i passaggi seguenti sul ghiaccio, se non diversamente specificato.
- Risospendere le cellule con 200 μL di soluzione bloccante (1x PBS con FBS al 10% v/v) e incubare la piastra per 15 minuti a RT.
- Lavare le celle con 200 μl di 1x PBS/pozzetto, centrifugare la piastra a 625 x g per 1 min a 4 °C ed eliminare il surnatante.
- Etichettare le celle con una macchia viva/morta.
- Testare la vitalità cellulare utilizzando una colorazione fissabile nel vicino infrarosso vivo/morto. Diluire la macchia viva/morta con 1x PBS a 1:1000.
- Risospendere le cellule in un pozzetto con 200 μL di etanolo al 70% per un controllo negativo.
- Risospendere le cellule nei pozzetti rimanenti con 200 μl di 1x PBS.
- Incubare la piastra per 5-10 minuti con ghiaccio, centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
- Aggiungere 50 μl di soluzione viva/morta nei rispettivi pozzetti e incubare la piastra su ghiaccio per 15 minuti.
- Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
- Lavare le celle due volte con 200 μL di tampone di flusso (HBSS con 2% p/v BSA) per pozzetto.
- Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
- Eseguire l'immunocolorazione di superficie per i marcatori cellulari di interesse (anticorpo CD71).
- Diluire l'anticorpo CD71 con tampone di flusso (HBSS con 2% p/v BSA) a 1:50.
- Aggiungere 50 μl di soluzione di anticorpi nei rispettivi pozzetti e incubare la piastra su ghiaccio per 15 minuti.
- Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
- Lavare le celle una volta con 200 μL di tampone di flusso (HBSS con 2% p/v BSA) per pozzetto.
- Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
- Eseguire l'immunocolorazione intracellulare per i marcatori cellulari di interesse (anticorpo Ki67).
- Utilizzare il set di tamponi di colorazione del fattore di trascrizione Foxp3 per fissare e permeabilizzare le cellule. Aggiungere 100 μl di soluzione di lavoro per fissazione/permeabilizzazione Foxp3 a ciascun pozzetto. Risospendere i pellet cellulari pipettandoli su e giù.
- Incubare la piastra su ghiaccio o a RT per 30-60 minuti al buio.
- Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
- Lavare le cellule due volte con 200 μl di tampone di permeabilizzazione 1x per pozzetto.
- Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
- Aggiungere 100 μL di soluzione bloccante (1x PBS con FBS al 2% v/v) per 15 minuti a RT.
- Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
- Diluire l'anticorpo Ki67 con una soluzione bloccante (1x PBS con FBS al 2% v/v) a 1:25.
- Aggiungere 50 μl di soluzione di anticorpi Ki67 1:25 ai rispettivi pozzetti e incubare la piastra per 30 minuti a RT al buio.
- Centrifugare la piastra a 625 x g per 1 minuto a 4 °C ed eliminare il surnatante.
- Lavare le cellule due volte con 200 μl di tampone di permeabilizzazione 1x per pozzetto.
- Risospendere le cellule con 200 μL di tampone di flusso.
- Processare i campioni utilizzando un citometro a flusso. Un esempio di strategia di gating è descritto in dettaglio in Cornelison et al. 202212.
Risultati
Dati rappresentativi per l'invasione (Figura 3), la vitalità e l'espressione di Ki67 e CD71 tramite citometria a flusso (Figura 4) sono forniti per le linee GSC come precedentemente pubblicato per un idrogel di ialuronano-collagene12 tio-modificato. La presenza di astrociti e microglia all'interno del modello TME ha un effetto differenziale sull'invasione delle GSC a seconda della linea cellulare (
Discussione
L'assemblaggio del modello TME comprende sei passaggi fondamentali: 1) passaggio e separazione delle cellule tra condizioni simili, 2) assemblaggio di una soluzione di collagene concentrata per tutte le condizioni, 3) combinazione dei componenti del gel (cellule, collagene, acido ialuronico metacrilato e fotoiniziatore) per ciascuna condizione 4) placcatura dei gel, 5) reticolazione mediante esposizione ai raggi UV e calore e 6) aggiunta della testina di pressione del fluido. Dopo 18 ore...
Divulgazioni
Gli autori non hanno conflitti di interesse rilevanti da rivelare.
Riconoscimenti
Vorremmo ringraziare le fonti di finanziamento per questo lavoro: il National Institutes of Health National Cancer Institute (R37 CA222563 a J.M.), la Coulter Foundation (J.M.) e Virginia Tech ICTAS-CEH (J.M. & J.H.). Le GSC utilizzate in questo test sono state derivate da Jakub Godlewski, Ph.D. (Harvard Medical School).
Materiali
| Name | Company | Catalog Number | Comments |
| 12 Well Tissue Culture Plate, Sterile | Celltreat Scientific Products | 229112 | |
| 250 mL Filter System, PES Filter Material, 0.22 µm, 50 mm, Sterile | DOT Scientific | 667706 | |
| 385 nm, 1650 mW (Min) Mounted LED, 1700 mA | Thorlabs | M385LP1-C1 | |
| 75cm2 Tissue Culture Flask - Vent Cap, Sterile | Celltreat Scientific Products | 229341 | |
| 8.0 μm Cell Culture Plate Insert 12 mm Diameter | Millicell | PI8P01250 | |
| Absolute Ethanol, 200 proof, Molecular Biology Grade | Thermo Fisher Scientific | T038181000CS | Ethanol for flow cytometry dead cell control. |
| Astrocyte Medium (Astrofull) | ScienCell Research Laboratories | 1801 | Contains astrobasal, FBS, and penicillin/streptomycin. |
| B-27 Supplement (50x), minus vitamin A (Gibco) | Thermo Fisher Scientific | 12587010 | |
| BSA (MACS) | Miltenyi Biotec | 130-091-376 | |
| CD71 antibody (eBioscience, Invitrogen) | Fisher Scientific | 25-0719-41 | |
| Cell Counting Chambered Slides | Nexcelom Bioscience | CHT4-PD100-002 | |
| Cell Scrapers | Biologix USA | 70-1250 | |
| Cellometer K2 Fluorescent Cell Counter (Nexelcom Bioscience) | VWR | NEXCCMK2-SK150-FCS | |
| Centrifuge - Low-Speed | Eppendorf | 5702 R | Centrifuge for cell culture. |
| Clear Polystyrene 96-Well Microplates, Corning | Fisher Scientific | 07-200-108 | V-bottom plates for flow cytometry staining. |
| CO2 Incubator, 150L, Heracell 150i (Thermo Scientific) | Thermo Fisher Scientific | 50116047 | |
| Collagen I, High Concentration, Rat Tail | Corning | 354249 | |
| Collagen I, Rat Tail | Corning | 354236 | "Low" concentration for coating adherent flasks. |
| Collagenase (CAS# 9001-12-1) | United States Biological | C7511-30 | |
| Collimation Adapter for Olympus BX & IX, AR Coating: 350 - 700 nm | Thorlabs | COP1-A | |
| Cotton Swabs, Q-tips Precision Tips | Amazon | B01KCJB3R2 | |
| Dispase (CAS# 9001-92-7) | United States Biological | D3760 | |
| DMEM, high glucose (Gibco) | Thermo Fisher Scientific | 11330032 | |
| EVOS FL | Invitrogen | AMF4300 | |
| Fetal Bovine Serum (Gibco) | Thermo Fisher Scientific | 26140079 | For microglia culture. |
| Formalin solution, neutral buffered, 10% (Sigma-Aldrich) | Millipore Sigma | HT501128 | |
| Foxp3 / Transcription Factor Staining Buffer Set (eBioscience, Invitrogen) | Thermo Fisher Scientific | 00-5523-00 | |
| Glioma stem cells | n/a | n/a | Can be patient derived or commercial glioma stem cell lines. |
| Guava easyCyte HT System | Millipore Sigma | 0500-4008 | Flow cytometer. |
| HBSS (Sigma-Aldrich) | Millipore Sigma | H6648 | |
| HEPES (1 M) (Gibco) | Thermo Fisher Scientific | 15630080 | |
| High-Power 1-Channel LED Driver with Pulse Modulation, 10.0 A Max, 50.0 V Max | Thorlabs | DC2200 | Interface for UV Lamp. |
| Hoechst 33342 Solution (20 mM) (Thermo Scientific) | Thermo Fisher Scientific | 62249 | |
| Human Astrocytes | ScienCell Research Laboratories | 1800 | Primary astrocytes derived from the cerebral cortex. |
| Human EGF Recombinant Protein (Gibco) | Thermo Fisher Scientific | PHG0311 | |
| Human FGF-basic (FGF-2/bFGF) (aa 10-155) Recombinant Protein (Gibco) | Thermo Fisher Scientific | PHG0021 | |
| Immortalized Human Microglia - hTERT | Applied Biological Materials | T0251 | |
| Incu-mixer MP Heated Microplate Vortexer, 2 position | Benchmark Scientific | H6002 | |
| Ki67 REAfinity, PerCP-Vio 700 antibody | Miltenyi Biotec | 130-120-420 | |
| LED UV Curing Meter | Gigahertz-Optik | X1-RCH-116 | Optometer to measure UV light intensity. |
| Lithium phenyl-2,4,6-trimethylbenzoylphosphinate (LAP) | Advanced Biomatrix | 5269-100MG | Photoinitiator. |
| LIVE/DEAD Fixable Near-IR (Invitrogen) | Thermo Fisher Scientific | L24975 | |
| Methacrylated hyaluronic acid (photoHA) | Advanced Biomatrix | 5212-100MG | |
| Microcentrifuge, Sorvall ST8R (Thermo Scientific) | Fisher Scientific | 75-997-203 | Centrifuge for flow cytometry staining. |
| N-2 Supplement (100X) (Gibco) | Thermo Fisher Scientific | 17502048 | |
| Neurobasal-A Medium (Gibco) | Thermo Fisher Scientific | 10888022 | |
| PBS (10X), pH 7.4 without Ca & Mg | Quality Biological | 119-069-101 | |
| Sodium hydroxide, pellets ACS (CAS# 1310-73-2) | VWR | 97064-476 | |
| Synergy Ultrapure Water Purification System (MilliporeSigma) | Fisher Scientific | SYNS0HFUS | |
| Trypsin-EDTA (0.25%), phenol red (Gibco) | Thermo Fisher Scientific | 25200056 | |
| ViaStain AOPI Staining Solution | Nexcelom Bioscience | CS2-0106 |
Riferimenti
- Ostrom, Q. T., et al. CBTRUS statistical report: Primary brain and other central nervous system tumors diagnosed in the United States in 2016-2020. Neuro Oncol. 25, 1-99 (2023).
- Stupp, R., et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma. N Engl J Med. 352 (10), 987-996 (2005).
- Stupp, R., et al. Effect of tumor-treating fields plus maintenance temozolomide vs maintenance temozolomide alone on survival in patients with glioblastoma: A randomized clinical trial. JAMA. 318 (23), 2306-2316 (2017).
- Lathia, J. D., Mack, S. C., Mulkearns-Hubert, E. E., Valentim, C. L. L., Rich, J. N. Cancer stem cells in glioblastoma. Genes Dev. 29 (12), 1203-1217 (2015).
- Roos, A., Ding, Z., Loftus, J. C., Tran, N. L. Molecular and microenvironmental determinants of glioma stem-like cell survival and invasion. Front Oncol. 7, 120 (2017).
- Yabo, Y. A., Niclou, S. P., Golebiewska, A. Cancer cell heterogeneity and plasticity: A paradigm shift in glioblastoma. Neuro Oncol. 24 (5), 669-682 (2022).
- Geer, C. P., Grossman, S. A. Interstitial fluid flow along white matter tracts: A potentially important mechanism for the dissemination of primary brain tumors. J Neurooncol. 32 (3), 193-201 (1997).
- Munson, J. M., Bellamkonda, R. V., Swartz, M. A. Interstitial flow in a 3D microenvironment increases glioma invasion by a CXCR4-dependent mechanism. Cancer Res. 73 (5), 1536-1546 (2013).
- Kingsmore, K. M., et al. Interstitial flow differentially increases patient-derived glioblastoma stem cell invasion via CXCR4, CXCL12, and CD44-mediated mechanisms. Integr Biol. 8 (12), 1246-1260 (2016).
- Qazi, H., Shi, Z. -. D., Tarbell, J. M. Fluid shear stress regulates the invasive potential of glioma cells via modulation of migratory activity and matrix metalloproteinase expression. PLoS One. 6 (5), e20348 (2011).
- Parmigiani, E., Scalera, M., Mori, E., Tantillo, E., Vannini, E. Old stars and new players in the brain tumor microenvironment. Front Cell Neurosci. 15, 709917 (2021).
- Cornelison, R. C., et al. A patient-designed tissue-engineered model of the infiltrative glioblastoma microenvironment. NPJ Precis Oncol. 6 (1), 54 (2022).
- Tchafa, A. M., Shah, A. D., Wang, S., Duong, M. T., Shieh, A. C. Three-dimensional cell culture model for measuring the effects of interstitial fluid flow on tumor cell invasion. J Vis Exp. (65), e4159 (2012).
- Shields, J. D., et al. Autologous chemotaxis as a mechanism of tumor cell homing to lymphatics via interstitial flow and autocrine CCR7 signaling. Cancer Cell. 11 (6), 526-538 (2007).
- Shieh, A. C., Rozansky, H. A., Hinz, B., Swartz, M. A. Tumor cell invasion is promoted by interstitial flow-induced matrix priming by stromal fibroblasts. Cancer Res. 71 (3), 790-800 (2011).
- Miteva, D. O., et al. Transmural flow modulates cell and fluid transport functions of lymphatic endothelium. Circ Res. 106 (5), 920-931 (2010).
- Kingsmore, K. M., et al. MRI analysis to map interstitial flow in the brain tumor microenvironment. APL Bioeng. 2 (3), 031905 (2018).
- Roberts, L. M., et al. Myeloid derived suppressor cells migrate in response to flow and lymphatic endothelial cell interaction in the breast tumor microenvironment. Cancers. 14 (12), 3008 (2022).
- Bellail, A. C., Hunter, S. B., Brat, D. J., Tan, C., Van Meir, E. G. Microregional extracellular matrix heterogeneity in brain modulates glioma cell invasion. Int J Biochem Cell Biol. 36 (6), 1046-1069 (2004).
- Choi, J. R., Yong, K. W., Choi, J. Y., Cowie, A. C. Recent advances in photo-crosslinkable hydrogels for biomedical applications. Biotechniques. 66 (1), 40-53 (2019).
- Artym, V. V., Matsumoto, K. Imaging cells in three-dimensional collagen matrix. Curr Protoc Cell Biol. , 11-20 (2010).
- Gelman, R. A., Williams, B. R., Piez, K. A. Collagen fibril formation. Evidence for a multistep process. J Biol Chem. 254 (1), 180-186 (1979).
- Williams, B. R., Gelman, R. A., Poppke, D. C., Piez, K. A. Collagen fibril formation. Optimal in vitro conditions and preliminary kinetic results. J Biol Chem. 253 (18), 6578-6585 (1978).
- Mineo, M., et al. The long non-coding RNA HIF1A-AS2 facilitates the maintenance of mesenchymal glioblastoma stem-like cells in hypoxic niches. Cell Rep. 15 (11), 2500-2509 (2016).
- Tang, X., et al. Targeting glioblastoma stem cells: A review on biomarkers, signal pathways and targeted therapy. Front Oncol. 11, 701291 (2021).
- Dirkse, A., et al. Stem cell-associated heterogeneity in glioblastoma results from intrinsic tumor plasticity shaped by the microenvironment. Nat Commun. 10 (1), 1787 (2019).
- Sofroniew, M. V. Astrocyte reactivity: Subtypes, states, and functions in CNS innate immunity. Trends Immunol. 41 (9), 758-770 (2020).
- Tate, K. M., Munson, J. M. Assessing drug response in engineered brain microenvironments. Brain Res Bull. 150, 21-34 (2019).
- Cai, X., et al. Application of microfluidic devices for glioblastoma study: Current status and future directions. Biomed Microdevices. 22 (3), 60 (2020).
- Kleinman, H. K., Martin, G. R. Matrigel: Basement membrane matrix with biological activity. Semin Cancer Biol. 15 (5), 378-386 (2005).
- Jadin, L., et al. Hyaluronan expression in primary and secondary brain tumors. Ann Transl Med. 3 (6), 80 (2015).
- Cornelison, R. C., Munson, J. M. Perspective on translating biomaterials into glioma therapy: Lessons from in vitro models. Front Mater. 5, 27 (2018).
- Kapałczyńska, M., et al. 2D and 3D cell cultures - a comparison of different types of cancer cell cultures. Arch Med Sci. 14 (4), 910-919 (2018).
- Nelson, C. M., Bissell, M. J. Of extracellular matrix, scaffolds, and signaling: Tissue architecture regulates development, homeostasis, and cancer. Annu Rev Cell Dev Biol. 22, 287-309 (2006).
- Phon, B. W. S., Kamarudin, M. N. A., Bhuvanendran, S., Radhakrishnan, A. K. Transitioning pre-clinical glioblastoma models to clinical settings with biomarkers identified in 3D cell-based models: A systematic scoping review. Biomed Pharmacother. 145, 112396 (2022).
- Pampaloni, F., Reynaud, E. G., Stelzer, E. H. K. The third dimension bridges the gap between cell culture and live tissue. Nat Rev Mol Cell Biol. 8 (10), 839-845 (2007).
- Ortiz-Cárdenas, J. E., et al. Towards spatially-organized organs-on-chip: Photopatterning cell-laden thiol-ene and methacryloyl hydrogels in a microfluidic device. Organs Chip. 4, 100018 (2022).
- Ozulumba, T., et al. Mitigating reactive oxygen species production and increasing gel porosity improves lymphocyte motility and fibroblast spreading in photocrosslinked gelatin-thiol hydrogels. bioRxiv. , (2024).
- Lim, K. S., et al. Fundamentals and applications of photo-cross-linking in bioprinting. Chem Rev. 120 (19), 10662-10694 (2020).
- Ghosh, R. N., et al. An insight into synthesis, properties and applications of gelatin methacryloyl hydrogel for 3D bioprinting. Mater Adv. 4 (22), 5496-5529 (2023).
- Venkataramani, V., et al. Glutamatergic synaptic input to glioma cells drives brain tumour progression. Nature. 573 (7775), 532-538 (2019).
- Venkataramani, V., et al. Glioblastoma hijacks neuronal mechanisms for brain invasion. Cell. 185 (16), 2899-2917 (2022).
Ristampe e Autorizzazioni
Richiedi autorizzazione per utilizzare il testo o le figure di questo articolo JoVE
Richiedi AutorizzazioneEsplora altri articoli
This article has been published
Video Coming Soon