Method Article
薄膜における拡散を用いた環境プルトニウムのスペシエーションと生物学的利用能の測定
要約
薄膜における拡散勾配(DGT)の技術は、プルトニウムの分化の研究のために提案されています。このプロトコルは、有機物の存在下でのPu(IV)とPu(V)の動作をプロービング拡散実験について説明します。カルスト春に配備DGTSはプルトニウムの生物学的利用能の評価を可能にします。
要約
それは潜在的に生物相とヒトの暴露に貢献することができる長い半減期を有するアルファ粒子放射体であるため、水界生態系におけるプルトニウム(プルトニウム)の生物学的な取り込みは、特に懸念されます。薄膜技術における拡散勾配は、プルトニウムの生物学的利用能および分化のその場測定のために、ここで紹介されています。プルトニウムと新たに開発されたプロトコルで室内実験のために構築拡散セルは、それが可能な種々の化学組成のモデル溶液中のプルトニウムの環境挙動をシミュレートすることを可能にします。プルトニウムの酸化状態の調節(IV)とPu(V)は、このプロトコルに記載された環境でプルトニウムの複雑なレドックス化学作用を調べるために不可欠です。この技術の較正および実験室実験で得られた結果は、淡水中でその場でのPuの測定のために、特定のDGT装置を開発することが可能になります。加速器ベースの質量分析測定カルスト春にDGTSによって蓄積されたプルトニウムのは、鉱物淡水環境中のPuの生物学的利用能を決定することができました。 DGT装置を使用するプルトニウムの測定のために、このプロトコルの適用は、分化と水生生態系におけるプルトニウムの生物学的な転送の我々の理解を改善するための大きな可能性を秘めています。
概要
プルトニウムは核爆弾の実験や原発事故、以下のグローバルフォールアウトの結果として環境中の人工放射性核種が存在します。プルトニウムの酸化還元化学は環境水生システム1での移行と生物地球化学的循環に重要な意味を持っています。プルトニウムは、複雑な化学的性質を有しており、同時に4酸化状態(III、IV、V、VI)で存在することができます。したがって、天然水中のプルトニウムの酸化還元種の分布は局所的な化学的環境2,3に極めて敏感です。プルトニウムの酸化状態は、ソースの起源に依存して - この声明は、汚染された環境や処分のためのほとんどの関連です。高い酸化状態(V +と+ VI)は、他のアクチニドの崩壊生成物の中から見つけることができますしながら削減プルトニウム種(+ IIIとは、+ IV)、廃棄物の排出物を無酸素環境で主に発見され、世界的な放射性降下物に由来し、ストックしていますそして、有酸素環境での4。
モビリティとプルトニウムの環境の動作は、レドックス分化からある程度予測することができます。 + IIIおよびIV +の酸化状態でのプルトニウムは、固相に主に存在し、無機コロイドに収着する能力を増加させ、自然に有機物(NOM)分子を発生しました。 + IIIおよびIV +酸化状態でプルトニウムが少なく、モバイルであると考えられています。プルトニウム(+ Vと+ VI、+ V最も可能性が高いという)5のより可溶性の酸化形態は、潜在的に、より高い移動度水生生物に高い生物学的移転に貢献することができます。それにもかかわらず、特にフミン酸のNOMの存在下で、プルトニウム(V)は降水量の賛成で大きさの分割数桁をずらし、17に減少しています。プルトニウム(IV)をプルトニウム(V)の還元速度が速く逆反応よりも大きさの4〜5オーダー、酸化条件の下ミリアンペアのPu(IV)のremobilizationであるという事実にもかかわらずYはまた、場所1を取ります 。ミネラル堆積物のPu(IV)を用いて補正されたおよび天然の酸化条件に供に関する最近の実験データは、水相に可溶性のPuの濃度は、時間1,6とともに増加することを実証しました。著者らは、酸化プルトニウムの脱離(IV)およびより可溶性のPu(V)を形成することによってそれを説明するとPu(VI)種。プルトニウム(IV)の酸化はまた、天然7マンガン酸化物に遭遇したことが原因で発生することがあります。これらの観察は、生物学的利用能のモデル化と廃棄物処理や汚染された場所の環境リスク評価のために重要です。
プルトニウムの生物学的利用能と分化に関する研究は、両方の研究室でとその場で条件困難な作業です。低環境中の濃度は、酸化還元種の多様性と自然なコロイドとの相互作用は、それが困難なプルトニウムの生物地球化学的挙動をシミュレートすることを可能にします。薄膜における拡散勾配の技術(DGT)は、に基づいポリアクリルアミド(PAM)ゲルを通して自由に不安定な汚染物質種の拡散が広く微量元素8の環境の測定のために使用されます。 DGTサンプラーは、拡散性のゲル層(厚さを変化させるPAMゲル)とゲルを保護するフィルタ膜と(これはPAMゲルに含まキレックス樹脂である微量金属の大部分)の結合相からなる三層デバイスを表します一緒にアセンブリを保持します。水の85%からなるポリアクリルアミドゲルの薄膜は、大きなNOM分子または天然のコロイド粒子に結合されたプルトニウムよりも急速に拡散するように自由と不安定な錯体種を有効にしてください。実験室条件で薄いPAMゲル膜中のプルトニウムの拡散を研究するために設計されたセットアップは、拡散セル9と呼ばれています 。
拡散セルは、二つの別個の区画が所与の表面の開口部によって相互接続された2つの区画の容器です。開口部、 すなわち、二つの室Cとの間の窓所定の厚さの拡散ゲルのディスクをontains。我々は2つの100ミリリットルの区画と円形拡散窓直径1.7 CMとテフロンセルを構築しました。一つの区画は、組立を容易にする、取り外し可能です。固定コンパートメントに拡散窓の周りに刻まれた0.5センチメートル広い溝が拡散ゲルディスクを配置するのに役立ちます。溝の深さは、使用することを意図し、PAMゲルの厚さのようになります。そこで我々は、我々の拡散セルの溝の深さは0.39ミリメートルで、0.39ミリメートルのPAMゲルで動作するように選択します。拡散セルの詳細な画像が図1に示されています。
最初にプルトニウムを含む溶液は、1つの区画(A)にあるとき、Puの種を拡散するゲル濃度勾配を確立する第2の区画(B)に蓄積し始め、最初はプルトニウムなく、同じ化学組成の溶液を含みます。コンパートメントA中のPuの種の初期濃度は、remaiように定義されます拡散実験を通して(1%-2%で最もによって)非常に少ない定数または変更NS。時間に対する拡散プルトニウムの量をプロットすると、別のシミュレートされた環境条件に支配的なPuの種の移動度を分析するための手段を提供します。薄膜における拡散は、プルトニウムの移動と分化の研究のための貴重な代替手段を提供し、正常にフィールド条件10で適用することができます。一つは、拡散Puの種を蓄積するのに役立つ結合相として、PAM拡散ゲルとキレックス樹脂で作製したパッシブサンプラーによって、拡散セルを置き換えることができます。このようなサンプラーは、現場条件に露出させることができる-樹脂に蓄積されたプルトニウムの量が分化し、それぞれの環境 10中のPuの生物学的利用能の指標となります。
本研究では、実験室条件でNOMでのPu(IV)とPu(V)の種とそれらの相互作用の移動性を調査するために拡散セルを使用していました。フーrthermore、我々は、プルトニウムのかなりの部分がで水生コケの細胞内部分で発見されたスイスのジュラ山脈(Venoge川)のカルスト春にプルトニウムの生物学的利用能を研究105 cm 2の表面の大受動DGTサンプラーを適用しました前作11。このため、自然のままの環境中に存在するプルトニウムの非常に低レベルで、ETHチューリッヒで利用可能な加速器質量分析(AMS)技術は、プルトニウム同位体を測定しました。
プロトコル
1.プルトニウムトレーサーの準備
- プルトニウム(IV)トレーサーの準備
- Puのストック溶液から、25ミリリットルのガラス製ビーカーに、実験用のプルトニウムの所望量を含む適切な分量を転送します。一度に239 Puの10ベクレルで動作します。
- HNO 3、0.6ミリリットルの1MのNaHSO 4、0.4ミリリットルの濃H 2 SO 4、濃縮1ミリリットルを追加します。ホットプレート上で蒸発乾固します。酸突起を回避するために初めにゆっくり200℃に加熱します。
- 白い煙が出てくるなくなるまで、500℃ - に液体をビーカーに残っていないされたら、400℃で残留物をアニール。実験のために選択されたバッファに冷却し、可溶性時残留物は白です。
注:このようにして調製のPu(IV)供給源は、数ヶ月12まで乾燥保存することができます。
- プルトニウム(V)トレーサーの準備13
- プルトニウム酸化
- PuのSTOからアリコートを転送漏れ防止キャップ付きプラスチック20ミリリットルの液体シンチレーションバイアルにCKソリューション。一度に239 Puの10ベクレルで動作します。 KMnO 4、0.01Mの0.01ミリリットルを追加し、少なくとも6時間、暗所での混合物を残します。
- プルトニウム(VI)の抽出
- シクロヘキサン中0.5 Mテノイルトリフルオロアセトン(TTA)の溶液を調製し、抽出および光露光から保護する前に。必ず、各実験の直前に、この溶液を調製。
- シクロヘキサン中0.5Mテノイルトリフルオロアセトン(TTA)のpHは4.7と2ミリリットルでM CH 3 COONa 0.1の酸化プルトニウム溶液2 mlに追加します。暗所での反応混合物を維持するためにアルミホイルで瓶を包む、10分間振とうします。きれいなガラスバイアルにピペットと転送にプルトニウム(VI)を含む有機相を分離します。
- PUにプルトニウム(VI)(V)光還元
- 2時間室内光でシクロヘキサン中のPu(VI)-tTA錯体を含むガラスバイアルのままにしておきます。
- PU(V)の抽出
- pHは4.7で露光されたソリューション、0.1M CH 3 COONaの1ミリリットルに加え、5分間振とうします。プルトニウム(V)を含む、水相を除去します。 100μlのアリコートを取って、液体シンチレーション計数によって、この源の濃度を決定します。
注:+ Vの酸化状態のプルトニウムの長期安定性が疑問視されているので、各実験の前にすぐにプルトニウム(V)溶液を調製します。
- pHは4.7で露光されたソリューション、0.1M CH 3 COONaの1ミリリットルに加え、5分間振とうします。プルトニウム(V)を含む、水相を除去します。 100μlのアリコートを取って、液体シンチレーション計数によって、この源の濃度を決定します。
- プルトニウム酸化
実験で使用したソリューションの調製
- 緩衝溶液を準備
- MOPSの10 mM溶液(3-(N-モルホリノ)プロパンスルホン酸)緩衝液を作ります。この溶液200mlを取り、0.1 MのHCl(PU(V)で使用するためのPu(IV)およびpH 5.5での使用のためのpH 6.5)を滴下することによって所望のpHに調整します。
- プルトニウム(IV)を用いた実験のためのソリューションを準備
- 溶液A
- プルトニウム(IV)は、それ自体にステップ1.1で調製ディゾルブpH6.5の緩衝溶液10mMのMOPSのveralミリリットル。徹底的に同じ溶液を入れたビーカーを洗います。
- pH6.5の10mMのMOPS緩衝液で72ミリリットルにボリュームをもたらします。 pH値をチェックし、0.1M NaOHで6.5に再調整してください。きれいなビーカーに、この溶液の72ミリリットル転送 - これは拡散セルのコンパートメントAに導入される(A)ソリューションです。
- 溶液B
- pH6.5の緩衝溶液10mMのMOPSの72ミリリットルを取ります。 1 M の Na 2 SO 4 0.75mlのを追加します。 pH値をチェックし、必要に応じて6.5に再調整します。きれいなビーカーに移す。この溶液の72ミリリットル - これは«Bの»拡散セルの区画内に導入する«B»ソリューションです。
- NOMの溶液を準備します
- 20 ppmで得る濃度に凍結乾燥フルボまたはフミン酸の1.4ミリグラムを秤量し、«»ソリューションcontainiでそれを溶かしますNGのPu(IV)。実験すると平衡を可能にするために、前にこのソリューションの24時間を準備します。
- 溶液A
- プルトニウム(V)を用いた実験のためのソリューションを準備
- 溶液A
- pH5.5で緩衝液10mMのMOPSの72 mlのステップ1.2.4で得られたプルトニウム(V)を溶解します。 1 MのNaNO 3の0.75ミリリットルを追加します。 pH値を確認し、必要に応じて5.5に調整します。きれいなビーカーに、このソリューションの72ミリリットルを転送します。実験の直前のPu(V)との溶液を調製します。
- 溶液B
- pH5.5で緩衝溶液10mMのMOPSの72ミリリットルを取ります。 1 MのNaNO 3の0.75ミリリットルを追加します。 pH値を確認し、必要に応じて5.5に調整します。きれいなビーカーに、このソリューションの72ミリリットルを転送します。
- NOMの溶液を準備します
- 20ppmの濃度を得るとPu(V)を含有する溶液に溶解する凍結乾燥されたフルボまたはフミン酸の1.4ミリグラムを秤量します。 24時間のためのソリューションを残しますプルトニウム(IV)とPu(V)の種の間で定常状態に到達します。拡散実験の前には、3.4.2項で説明したようにプルトニウム(V)の割合を決定するために、液相の抽出を行います。
- 溶液A
3.実験拡散実験
- PAMゲルを準備
- 電解質の数ミリリットル(例えば、10mMののNaNO 3)を有するプラスチックトレイを湿らせ、中のPAMゲルストリップを配置し、表面上に均一に展開します。ゲル表面上の直径に慎重2.7センチメートルの鋭いパンチを配置します。ゲル表面の上にパンチをスライドしないでください。
- 必要であれば、それは透明PAMゲルを視覚化するのを助けることができる、地元の集中照明を使用してください。ゲル表面にしっかりとパンチを押して、それが切断されたら離します。
- 拡散セルの組立
- スムーズな顔をしたようにして拡散窓を介して溝にピンセットでPAMゲルディスクを置きます。 TWは、このようなネジを回しO拡散セルの区画は、PAMゲルディスクを介して相互接続、一緒に保持します。
- マークA及びBの拡散セルのコンパートメント。各実験の直前にゲルディスクと拡散セルを組み立てます。ゲルが乾燥することはできません。
- 拡散実験を起動
- ゆっくりと、対応する区画にAとBのソリューションを注ぎます。両方のソリューションは、そうでなければ、拡散ゲルが損傷することができ、いつでも各区画で、等量を提供するために、同じ速度で注がれていることを確認します。
- ソリューションは、セルでは1回、タイマーを起動します。拡散セルの上に小型の電動ミキサーを置きます。この時点で考えられている拡散実験が開始されました。
- 拡散実験を通してサンプルを取ります
- 同時にexperimeを通じて一定容積を維持するために、AとBの区画から一定の時間間隔内に、等量のサンプルを取りますNT。
- A区画初期プルトニウム濃度を決定するために、実験の開始時にすぐに各区画に同時に1.00 mlのサンプルを取ります。
- NOMとフミン酸を用いた実験で、いくつかの時間に20分を加えずに実験で10分のサンプリング時間間隔を使用してください。 2.00 mlのアリコートを、α-分光測定のために良好な感度を提供するのに十分です。
- プルトニウム(IV)とPu(V)の液相抽出
- 拡散実験の終わりに漏れ防止キャップでプラスチック製の試験管にAとB室とは別に4ミリリットルのサンプルを取ります。 1 mlの2 M HClを用いてサンプルを酸性化。
- シクロヘキサン中0.5 Mビス - 5mlの(2-エチルヘキシル)リン酸(HDEHP)溶液を加え、5分間激しく試験管を攪拌します。相分離を可能にするためにサンプルを残します。プルトニウム(V)を含む水相を除去します。
- プルトニウムの逆抽出(IV)
- バックEX5%の5 mlの(NH 4)2 C 2 O 4と、残りの有機相から管のPu(IV)。
- 同時にexperimeを通じて一定容積を維持するために、AとBの区画から一定の時間間隔内に、等量のサンプルを取りますNT。
4.サンプル処理
- 内部標準でスパイクサンプル
- スパイクサンプルを収率トレーサーを用いて分析します。アルファ分光測定のための25 MBQ mlの242 Puのトレーサ-1放射能濃度の1.00ミリリットルのスパイクを使用してください。
- サンプル「マトリックスを酸化
- 濃HNO 3の2.00ミリリットルでホットプレート上で乾燥するまでサンプルを蒸発させ。
プルトニウムの放射化学分離5.
- プルトニウムの酸化状態を調整します
- 10分の間、70℃で、NaNO 2を熱サンプルを20 mgの追加、5ミリリットル8 M HNO 3のポイント4.2.1からの乾燥試料を溶解します。このステップは、+ IVにプルトニウムの酸化状態を調整することができます。
- プルトニウムの固相抽出
- 1.5 mlの8 M HNO 3を用いて(例えば、TEVAなど)、第四級アミン系陰イオン交換樹脂カラムを濡らします。 1.5ミリリットル8 M HNO 3で調整100mgの樹脂と1ミリリットルピペットチップで作られたマイクロカラムを使用してください。
- 約1ml分の流量で樹脂カラムを通してポイント5.1.1の溶液を渡し-1。樹脂カラムに2ミリリットル8 M HNO 3 3回転送washoutsでサンプルビーカーを洗い流します。
- 溶出のPu
- 3ミリリットル9 M HClでカラムを洗浄します。 3ミリリットルソリューション9 MのHCl / 0.1MのHIで溶出プルトニウム。ホットプレート上で溶出液を蒸発させます。乾燥するまで蒸発させ、 濃 HNO 3 2mlで扱います。必要に応じて、茶色のヨウ素の色が消えるまで繰り返します。
- 利用可能な任意の方法により、試料中のプルトニウム濃度を決定します。
注。このプロトコルアルファ分析に使用される239プルトニウムの濃度範囲については、良好な感度を提供します。アルファspectrometriのソースを準備しますCステンレス鋼ディスク14に電気めっきすることによってカウント。分析計でPIPS検出器(450ミリメートル2)のソースをカウントします。
データの分析6.
- プロットは、時間に対するプルトニウム拡散しました
- 時間(分)対Bコンパートメント内に蓄積されたプルトニウム(MBQ)の活性をプロットします。拡散実験中に取り出されたサンプルの量の正しい:時刻tにおける累積プルトニウム(MBQ)の活性は濃度の溶液(ミリリットル)の容量を掛けたサンプル中(MBQ ml -1の)決定に等しく、サンプリングの瞬間にB室(スプレッドシートの例を参照してください- 図2)。
- 異なるのPu濃度のいくつかの実験から、同じグラフデータにプロットするには、使用濃度は、区画Aの最初のプルトニウム濃度に正規化
- 拡散係数を算出します
- 拡散係数Dを算出する(cm 2の 秒 -1)、各実験のための10 Puの種の。 (1)式を使用します。
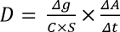 (1)
(1)
Δgと拡散ゲルの厚さ(cm)、C最初のプルトニウム濃度(MBQ mlの-1)、S拡散面積(cm 2)であり、時刻tにおける区画Bに拡散プルトニウム種の活性(MBQ)であります(秒)。ΔA/Δtは時間に対するBコンパートメントに拡散プルトニウムの直線プロットの傾きです。
- 拡散係数Dを算出する(cm 2の 秒 -1)、各実験のための10 Puの種の。 (1)式を使用します。
天然淡水中のPuの7.バイオアベイラビリティ研究
- DGTサンプラーを準備
- 電解質の数ミリリットル(例えば、10mMののNaNO 3)を有するプラスチックトレイを湿らせ、DGTサンプラーの( 図3参照)底板を配置します。必要に応じて、ローカルな照明を使用し、それが透明なゲルを視覚化するのを助けることができます。
- POSITI6センチ×22センチキレックス樹脂ゲルストリップ上にプレートの表面上に均一に展開します。樹脂ゲル層6センチ×22センチPAM拡散ゲルストリップの上に置き、表面上に均一に展開します。ゲルがスライドされておらず、スムーズな顔をした方法で配置されていることを確認します。
- フィルター膜6センチ×22センチの切れ端で拡散ゲル層をカバーしています。 DGTサンプラーのカバーフレームを置き、フィルター膜の上に( 図3を参照)、わずかにエッジにフレームを押して、アセンブリを閉じます。
- オープン、鋭いランセットで延長ゲル部分をカットし、必要に応じて、滑らかなプレート表面が得られるまで、ゲル層を再調整。ネジでアセンブリを固定してください。
- 電解質の数ミリリットル(例えば、10mMののNaNO 3)とDGTサンプラーを湿ら。 4-5℃で数週間に密封されたビニール袋までウェット保管してください。
- 水の自然な体でDGTSの展開
- はビニール袋の外にDGTサンプラーを取ります。 図4に示すように、ホルダーにDGTサンプラーを修正。
- 強いロープでそれらを懸濁またはDGTの表面に沿って一定の接線方向の水流を提供する方法で安定した垂直支持にインストールするのいずれかの水ボディにDGTSを展開します。測定のために十分な濃度でプルトニウムを蓄積するために、2〜3週間の淡水でDGTデバイスを展開します。
- 検索されたDGTSの治療
- 水からDGTSを取得します。フィルター膜を取り出して廃棄し、アセンブリを外します。上位ゲル層(PAM拡散ゲル)を取り出し、廃棄します。
- 収量トレーサーを用いて分析する20 mlの8 M HNO 3およびスパイクサンプルを含有するガラスビーカーに樹脂のゲルを移します。 0.25 MBQのml -1のAMS測定用(1.7 PG ml -1の)放射能濃度の242 Puのトレーサの1.00ミリリットルのスパイクを使用してください。よくAGIた後tated、Puの溶出のためのサンプルのO / Nのままにしておきます。
- 条件DGT溶出液
- 樹脂ゲルサンプルからソリューションをフィルタリングします。 5ミリリットル8 M HNO 3で残りの樹脂のゲルを洗浄し、サンプルとwashoutsを兼ね備えています。各サンプルにNaNO 2を20 mgの追加10分間、70℃での溶液を加熱します。このステップは、+ IVにプルトニウムの酸化状態を調整することができます。
- プルトニウムの固相抽出
- 10 mlの8 M HNO 3との第四級アミン系陰イオン交換樹脂カートリッジを濡らします。約1ml分-1の流量で交換樹脂カートリッジを通してポイント7.4.1のソリューションを渡します。 5ミリリットル8 M HNO 3で3回サンプルビーカーをすすぎ、交換樹脂カートリッジにwashoutsを転送します。
- 溶出のPu
- 10ミリリットル9 M HClでカートリッジを洗浄します。 15ミリリットルソリューション9 MのHCl / 0.1MのHIで溶出プルトニウム。ホットプレート上で溶出液を蒸発させます。 濃 HNO 3 2mlで扱い、電子乾燥するまでvaporate。茶色のヨウ素の色が完全に消失するまで必要に応じて繰り返します。
- 高い精製が必要な場合は2回以上にプルトニウム一方の反復放射化学的分離 - Puの検出システムの性能に応じ。第1.5ミリリットル8 M HNO 3で調整交換樹脂100mgのと1ミリリットルピペットチップで作られたマイクロカラム上に第3の分離を実行します。
- サンプル中のPu濃度を決定します。なぜなら自然のままの環境でのプルトニウムの非常に低レベルの239 Puのを測定するための質量分析技術を使用してください。
注:この作業では、チューリッヒのスイス連邦工科大学でのイオンビーム物理学の研究所のアクチニドの分析のための調整されたAMS機能を使用しています。
データの解析8。
- 濃度を計算し、(C DGTでμBqミリリットル-1)生物学的に利用可能なの(不安定な)プルトニウムSP展開期間中に国税総局によって蓄積されたプルトニウムの量からバルク水でECIES。 (2)式を使用します。
 (2)
(2)
Aは、結合相に蓄積されたプルトニウム、Δgと拡散層(ゲル+フィルター膜)の厚さ(cm)、D PAMゲル(CM 2秒 -1)中のPuの拡散係数、Sの活性(μBq)であります拡散面積(cm 2)で、および展開(秒)の持続時間をTと - バルク水の中だけでなく、他の利用可能な種分化データと合計のPu濃度のDGTSによって決定プルトニウムのC DGTを比較してください。
バルク水中の全プルトニウムの決意9.放射化学分離
- 条件水サンプル
- プラストに45ミクロンの膜フィルターを通して水の研究体から水をポンプIC受信者。 AMS測定のために10〜50 Lのサンプルで動作します。直前に研究室に輸送することを採取部位でサンプリングした後、HNO 3でpH 2に水を酸性化。
- 鉄水酸化物でプルトニウムを析出
- 研究室ではレシピエントにオーバーヘッド撹拌機を導入。 Puの収量トレーサーでサンプルをスパイク。 0.25 MBQのml -1のAMS測定用(1.7 PG ml -1の)放射能濃度の242 Puのトレーサの1.00ミリリットルのスパイクを使用してください。
- 約0.25グラム、L 10あたりのサンプルを採取するのFeCl 3・6H 2 Oを追加します。 30分間攪拌した後、pHを8にNH 4 OH鉄水酸化物を沈殿。
- 鉄水酸化物のプルトニウムの2回目の沈殿
- ポイント9.2.2から水試料からの上清を除去。 2Lのガラスビーカーに水酸化鉄の沈殿を回収、脱イオン水で受信者をすすぎ、SAMPでwashoutsを組み合わせますル。
- 炭酸塩を分解するために90℃に約100 mlの5 M HCl中の沈殿物、熱溶解します。溶液を冷却する際に必要に応じてフィルタリングします。再沈殿pHが8で、NH 4 OHと鉄水酸化物。
- 分析条件鉄水酸化物
- ポイント9.3.2からのサンプルから上清を除去。遠心分離容器に水酸化鉄の沈殿を回収。遠心し、上清を捨てます。脱イオン水で沈殿物を洗浄します。 2〜3回繰り返します。
- セクション7.4から7.6に、前述のように10ミリリットル8 M HNO 3で沈殿物を溶解し、プルトニウムの放射化学分離に提出します。
10. AMS測定のためのサンプルを調製
- 鉄水酸化物でプルトニウムを析出
- 放射化学分離後、2.5 mlのガラスバイアル中へプラスチックピペットで試料を移す、0.5 mlの1 M HClに最終試料を溶解します。サンプルビーカーTWICをすすぎます0.5ミリリットル1 M HClでeは、同じバイアルにwashoutsを転送します。
- 0.5 mlの2 mgのmlに加える-1のFe 3+のストック溶液は、鉄1mgを提供します。濃NH 4 OH数滴を加える鉄水酸化物を沈殿。遠心し、上清をデカントします。
- 、脱イオン水で沈殿物を洗浄し、遠心分離し、上清をデカント。 90℃のホットプレート上に沈殿物を乾燥させます。
- AMSの測定のためにターゲットを作製
- 水酸化物を650℃で2〜3時間のための炉の中でポイント10.1.3から沈殿焼きます。徹底的AMS測定のために、Tiターゲットホルダーにニオブ金属粉末とプレスの3-4 MGと混合。
注:私たちは、アクチニド15,16の測定のために調整されたスイス連邦工科大学(ETHチューリッヒ)でコンパクト(0.6 MV)AMSシステム」TANDY」のサンプルを測定しました。
- 水酸化物を650℃で2〜3時間のための炉の中でポイント10.1.3から沈殿焼きます。徹底的AMS測定のために、Tiターゲットホルダーにニオブ金属粉末とプレスの3-4 MGと混合。
結果
拡散実験
時間に対する拡散セルのBコンパートメント内に拡散239プルトニウムの活動をプロットすると、PAMゲルを通して拡散する239 Puの種のフラックスの視覚的な表現を提供します。拡散係数は、様々な化学的環境( 図2)内の異なる239 Puの酸化還元種の移動度を比較するための追加の手段を提供する、式1によれば、これらのプロットから計算した。 図5は、プルトニウム(IV)とプルトニウム(IV)-Puと拡散実験を示している図 (V)の混合種は、それぞれ、MOPSでバッファとHAの20 ppmでの存在下で実施されます。これらのプロットの比較は、プルトニウム(V)のプルトニウムよりも有意に多くの携帯電話は、(IV).Thisがプルトニウムのために特に有効であることを示している(IV)及びPuのHA(MW実験で5-40 kDaのは、特徴(V) Cusnir ら SI)10は、錯化分子として添加されます。プルトニウム(V)ソースsolutこの論文に記載されているプロトコルに従って調製したイオンは、主にプルトニウム(V)の種が含まれています。緩衝溶液MOPSで拡散実験の終了時にHDEHPと液相抽出プルトニウム(V)の±10%、80%を見つけました。この抽出の化学収率は80%です。 HAの20 ppmでの存在下でのPu(V)との溶液を24時間の間に平衡化し、このモデル溶液中のPu(V)分率は35%±10%でした。
自然の淡水中のPuの生物学的利用能に関する研究
我々の研究室で構成されたいくつかのDGT装置が正常にスイスのジュラ山脈のカルスト春に2〜3週間の期間のために露出させました。これは、6.5〜7.5の範囲内の水のpHとの鉱泉である400μScmの上記導電性-1と酸素で飽和。これらの実験は、おそらくためにも、tの、生物付着の痕跡を有するゲルアセンブリの優れた適用性と堅牢性を実証しました彼のスプリング(7℃)での低温。展開後に回収DGTSはよく初期形と外観を節約、無傷のゲル層と、保存しました。 DGTSによって蓄積されたプルトニウムは、AMSにより分析しました。 AMSは、他の分析技術と比較して顕著な利点を提供します。それが(サブFGレベルまで)非常に敏感であり、α-分析法またはICP-MS技術よりもはるかに低い初期サンプル量が必要です。また、このような水素化ウラン(238 UH)、または他の分子のような分子同重体干渉が、効率的にAMSの測定中に抑制され、239 Puの検出を妨害しません。いくつかの技術的な理由(化学分離時の239 Puのと、おそらく汚染)のために、我々は、フィールド内のDGTSの最初のアプリケーションのための239 Puのためのデータを使用することができませんでした。それにもかかわらず、240 Puの結果は公正でした。そこで、測定の239 Puの含有量を算出し、 240 Puの、240のように放射性降下物のプルトニウムのためのPu / 239 Puの原子比が0.18を取ります。 結果を表1に要約されています。
バルク水試料で測定された239 Puの濃度は、以前にこの帯水層(1-7μBqL -1)11について報告濃度に似ています。また、DGT測定値から算出した239 Puの濃度は、測定の不確実性の中に類似しています。 DGTSのみ無料と不安定なPuの種を蓄積するので、一つはこの水に生物学的に利用可能なプルトニウムの割合を推定することができます。 表1に示すデータは、バルク水中に存在する全ての239 Puの種が生物学的に利用可能な形で見出されることを示しています。これは、と比較して、春に成長している水生コケの細胞内画分で239 + 240 Puのの主な蓄積を明らかにした以前の知見11の光の中で興味深い結果であります 241アムと90シニア著者ら11は 、この自然の帯水層中のPuの強化移動度が同様のが自然ウラニル炭酸錯体を発生するために、可能性のPu(V)plutonyl形態として、可溶性炭酸Puの複合体の形成によるものであることを示唆しました。 Venogeスプリングの水は、高炭酸塩濃度と非常に低いのNOMコンテンツ(約1ppm)で、硬水です。
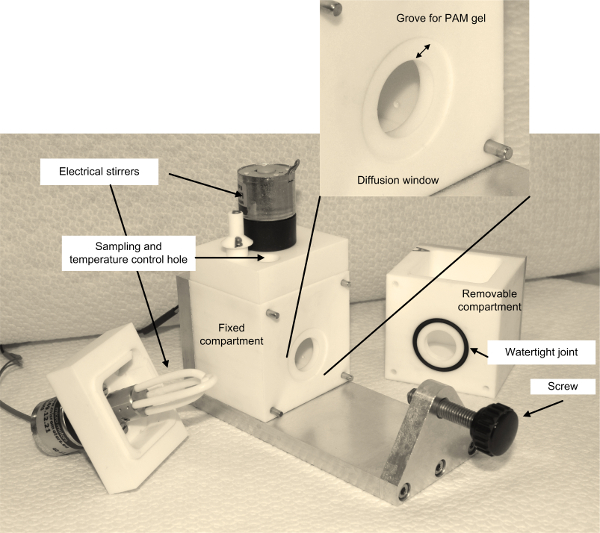
PAMゲルによるプルトニウムの拡散に実験に使用し、図1の拡散セル。溝厚さ0.5センチメートル、溝の深さ0.39ミリメートル。 この図の拡大版をご覧になるにはこちらをクリックしてください。
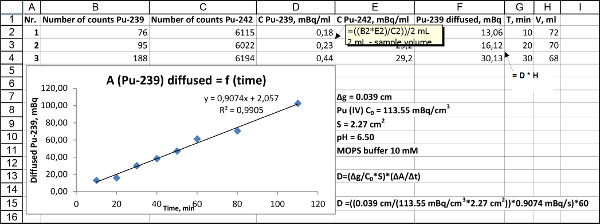
図2. SnapshExcelワークシートのOTは、拡散係数の計算に使用されます。 この図の拡大版をご覧になるにはこちらをクリックしてください。

図3.環境のPuの分化測定用の大表面DGTデバイス DGT機器の部品- 。底板とカバーフレーム- 。左に描かれ、右側のクルー穴とアセンブリ拡大版を表示するには、こちらをクリックしてくださいこの図の。

ホルダーに固定し、図4 DGTサンプラーデバイス(左)Venoge SPRIにさらさNG(右)プルトニウムの生物学的利用能の測定のために。 この図の拡大版をご覧になるにはこちらをクリックしてください。
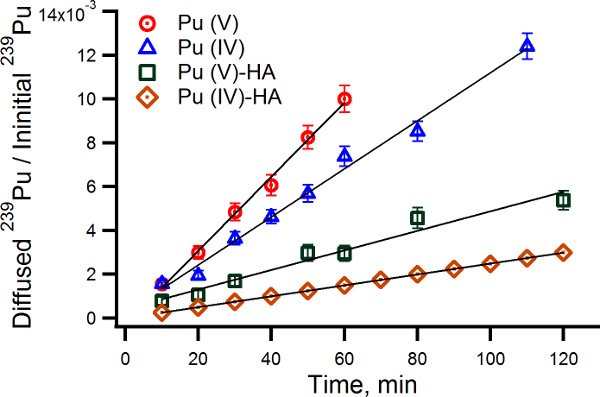
239の図5のプロットPUは実験データポイントが239のPu(IV)が挙げられる。種々の化学的環境における拡散セルのBコンパートメント内に拡散し、239 Puの(V)、それぞれ、MOPSで239 Puのためだけでなく、バッファ(IV) - 239プルトニウム(V)混合種(プルトニウム(V)の35%±10%)のHAの存在下で実施されます。 239のPu(IV)のために示したラインは-HAは、0.50×10 -6 cm 2で10秒 -1、以前に決定さの拡散係数を用いて計算しました。式1から計算拡散係数であります:MOPS緩衝液中のPu(IV) - 2.29×10 -6 cm 2の秒 -1、プルトニウム(V)MOPS緩衝液中で- 3.50×10 -6 cm 2の秒 -1、プルトニウム(IV) -プルトニウム(V)HAと- 0.92×10 -6 cm 2の秒 -1。上から下へ:MOPS緩衝液中のPu(V)(赤白丸)、プルトニウム(IV)MOPS緩衝液(青白三角)で、プルトニウム(IV) - プルトニウム(V)、HAの20 ppmでの存在下で、(緑白四角)、PuのHAの20 ppmでの存在下で、(IV)(茶色白菱形)が。 この図の拡大版をご覧になるにはこちらをクリックしてください。
| サンプル型 | 測定値の数 | 239 Puの濃度、μBqL -1 |
| バルク水 | 2 | 1.9±0.55 |
| DGT 0.39ミリメートル | 2 | 1.74±0.9 |
| DGT 0.78ミリメートル | 1 | 1.79±0.9 |
239バルク水におけるAMSによってプルトニウムの測定とDGTサンプラー。バルク水239 Puの表1.代表的な結果をアクチニド固有交換樹脂に抽出し、AMSによって測定され、水酸化鉄と水20 Lからの同時沈殿させましたプルトニウム(IV)の式2および拡散係数を用いて計算DGT測定の239 Puの濃度。 K = 2の不確実性。 U(95)。
ディスカッション
拡散セルを使用してプルトニウムを用いた実験のために、ここで説明DGTの方法論は、プルトニウムの酸化還元種と有機分子、コロイド粒子とシミュレートされた環境システムとの相互作用に関する様々な研究のための信頼性の高いアプローチを提供します。プルトニウムの環境測定のためのDGTSのさらなる用途は、生物学的利用能および水生生態系におけるこの放射性核種の運命の我々の理解に貢献していきます。
実験室での拡散実験
特定の化学物質の環境に関する意味のあるプルトニウムの移動性に関する結論との相互作用で成功拡散実験を行うためには、明確に定義され、制御条件が提供されなければなりません。実験の前にプルトニウムの酸化状態の調節、データの解釈を簡素化するだけでなく、プルトニウムの酸化還元種の様々な生物地球化学的挙動をシミュレートすることが不可欠です。 Puの種の感受性にpH値の変化は必見ソリューションをバッファリングすることができます。特に注意が拡散セルの機能とセットアップに描画する必要がある:非収着テフロンポリマー材料の使用は、細胞壁への吸着を回避し、実験中に解決策を拡散するプルトニウムの損失を防ぐ、強固な漏れ防止アセンブリを可能にします。
A区画に導入される初期のPu濃度と同様に、サンプリング間隔と拡散実験中に撮影した各試料の量は、実験室で利用可能な分析方法によって異なります。任意の利用可能な分析方法は、拡散セルからのサンプル中のPu濃度の決意に使用することができ、しかしこの選択は、しっかりと実験のために採取プルトニウムの初期活性に結合しています。このプロトコルで推奨されているように239 Puの10ベクレルはmeasuremのために十分な感度を提供するのに十分である(100〜140 MBqのmlの-1〜×10 -13モルml -1の2を与えます)一般的に、アルファ - 分析およびによってエントは放射線防護規制のための特定の問題を提起しません。他の、より高感度、分析技術は、プルトニウムの決意(例えば、質量分析)のために利用可能である場合のPuの初期濃度を低減することができます。サンプリング間隔は、Puの初期濃度、及びPAMゲルを通して拡散の予想速度に応じて、各拡散実験のために選択することができます。拡散実験からのアリコートをプルトニウム以外の放射性核種を含有しないという事実にもかかわらず、無機塩およびMOPS緩衝液の存在下、効率及び定量分析の精度を低下させる、分析手順を妨害することができます。したがって、これらの試料でのPuの化学的分離を行うことが好ましいです。
拡散セルは、ゲルが十分に撹拌した溶液に直接露出しているため、PAMゲル中で拡散を研究するための最良のアプローチを提供します。拡散BOのしたがって、効果ゲル表面にundary層(DBL)は無視できると考えています。拡散実験中のソリューションの良い撹拌をDBLの影響の最小化を可能にする、必要不可欠です。同じ時間では、1は、PAMゲルを妨害しないようにするために、慎重に進めるべき。
自然の淡水中のPuの生物学的利用能の研究
このプロトコルによって生成された結果は、DGT機器と測定プルトニウムは淡水でプルトニウムの生物学的利用能を研究するための効率的なツールを提供することを示しています。 DGT測定は無料で、不安定な種の時間平均濃度、生物による生物学的取り込みのための2つの最も重要なフォームが得られます。また、有機物とプルトニウムの相互作用の動力学は、異なる厚さのゲルを用いて調べることができます。ゲルを通して拡散するのPu-NOMの種のために必要な時間が解離するための最も不安定な複合体を可能にします。 DGT測定は、Bを補完することができます指定されたサイズ(例えば、8キロダルトン)の上にプルトニウムコロイド種のパーセンテージを得るY限外ろ過技術。 Puのコロイド種は、通常、非生物学的に利用可能な種と見なされ、DGTを使用して測定できないプルトニウム画分の一部です。
この時点で、DGTデバイスのみがスイスのジュラ山脈のカルスト春の淡水に配備されました。プルトニウムの低環境濃度は、潜在的な欠点に遭遇する可能性がDGTデバイスの長期的な展開を必要とします。 DGT表面の生物付着は、DBLの厚さを増加させ、したがって、PAMゲルでのPuの流量を制限する、重大な欠点を表します。高鉱化の海域または海域にさらさDGTSの結合相は、急速にプルトニウムの蓄積のためのデータを詐称、その他の微量金属で飽和することができます。環境プルトニウムの痕跡レベルの決意は徹底的な放射化学分離と非常に敏感な分析方法を必要とします。 AMS測定このプロトコルに適用されるのは、広く利用可能ではなく、他の質量分析技術によって置き換えることができます。しかし、厳密な放射化学的分離が自然にウランを発生する同重体干渉238 UHを排除することが必要です。
式2は、DGT装置の大きさが所定の展開時間の間に蓄積プルトニウムの量を増加させるように調整することができる本質的なパラメータであることを示しています。市販のゲルストリップのみ6センチメートル×22 cmで最大表面で利用可能です。したがって、DGTサンプラーのウィンドウが比較的短い展開時間についてPuの種を十分に蓄積することが可能になって105 cm 2の(21センチメートル×5センチ)に増えました。操作しながら、このようなDGTサンプラーのアセンブリは、PAMゲルシート特性の精度と特定の配慮が必要です。それはhomogeを提供するために、滑らかな顔をした均一な「サンドイッチ」にゲル層を組み立てるために基本的に重要です拡散性ゲルを介してバルク水からのPu種のジニアスフラックス。 DGT表面における良好な水の流れも重要なパラメータである、まだそれは主に帯水層内の流れの状態によって決定されます。これは、安定した水の供給を提供し、DBLの影響を最小限に抑えるために、約45°の水の流れの方向に向かってでPuの測定のためのDGT装置を配置することが推奨されます。
水の検討体の温度は、拡散係数が決定された温度と異なる場合、式(2)で用いられる拡散係数を補正しなければなりません。拡散係数の温度の影響は、ストークス - アインシュタイン方程式(式3)で与えられます: 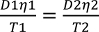 (3)
(3)
D 1及び D 2 は、拡散係数(cm 2の秒 -1)、ηである場合1、η2は、Wの粘度(MPA秒)ですそれぞれの温度T 1とT 2(K)でATER。
現在、熱力学計算に基づいて、 例えば、pHと酸化還元パラメータを除いて、自然のままの環境でのPuの分化を調査する方法はありません。これらのパラメータは、このような炭酸塩、鉄やマンガンカチオンなどのマクロコンポーネントでのみ使用可能です。このように、プルトニウムの分化は、これらの測定可能な種に由来するが、「本物」の測定値を表すものではありません。ここでは、それがplutonyl種を証明、おそらく、 その場で自由で不安定な種で測定することが可能とするため、この論文で提示されるような薄いPAMゲルフィルム技術における拡散はプルトニウムの分化の問題の解決の重要なステップであると考えています。淡水の環境プルトニウムのわずか数DGT測定は、これまで行われてきたが、得られた結果は、プルトニウムの分化および生物学的利用能の研究のためのDGT技術のさらなる用途のために奨励されています。有機物に富む海域でDGTSの展開は、潜在的にNOM分子の存在下でのPuのモビリティとの相互作用に関する重要な情報が得られます。興味深い結果は、セラフィールド核再処理工場周辺海域および損傷を受けた福島第一原子力発電所のような汚染された海洋環境ではDGT測定から予想されるべきです。
開示事項
The authors have nothing to disclose.
謝辞
This work was funded by the Swiss National Science Foundation (grant n° 200021-140230) and by the Swiss Federal Office of Public Health (PF and PS). We thank the Swiss Federal Office of Public Health for providing financial support for the open-access publication of this paper.
資料
| Name | Company | Catalog Number | Comments |
| 239Pu tracer | CEA | Source PU239-ELSC10 | |
| 242Pu tracer | LNSIRR | Source Pu242 N° 790 from Laboratory for National Standards of Ionizing Radiation of Russia | |
| 25 ml Beakers | |||
| Pipette | Socorex | ||
| Disposable plastic pipettes | Semadeni | ||
| 20 ml Plastic scintillation vial | Semadeni | ||
| Aluminium foil | |||
| Hot plate | |||
| Tweezers | |||
| Actinide exchange resin - TEVA - B | Triskem | TE-B50-A | |
| Actinide exchange resin - TEVA - R cartridges | Triskem | TE-R10-S | |
| 1 ml Pipette tips | Socorex | ||
| PAM gel strip 6×21 cm | DGT Research Ltd | 0.39 mm and 0.78 mm thickness / www.dgtresearch.com | |
| Chelex gel strip 6×21 cm | DGT Research Ltd | 0.40 mm thickness / www.dgtresearch.com | |
| Diffusion cell | Fabricated / in-house workshop | ||
| Ø 27 mm Punch | Fabricated / in-house workshop | ||
| Plastic tray | |||
| DGT set-up | Fabricated / in-house workshop | ||
| Membrane filter | PALL Corporation | HT-450 Tuffryn Polysulfone Membrane Disc Filter 0.45 μm / 145 μm thickness | |
| Nitric acid | Carlo Erba | 408025 | |
| Sulfuric acid | Sigma-Aldrich | 84720 | |
| Hydrocloric acid | Carlo Erba | 403981 | |
| Hydriodic acid | Merck | 100341 | |
| Potassium permanganate | Merck | 105082 | |
| Sodium hydrogen sulfate | Merck | 106352 | |
| Sodium sulfate | Merck | 106647 | |
| Sodium nitrate | Sigma-Aldrich | 31440 | |
| Sodium nitrite | Fluka | 71759 | |
| Sodium acetate | Merck | 106281 | |
| Ammonium oxalate | Fluka | 9900 | |
| Bis-(2-ethyl hexyl) phosphoric acid (HDEHP) | Merck | 177092 | |
| 2-thenoyltrifluoroacetone (TTA) | Fluka | 88300 | |
| MOPS buffer | Sigma-Aldrich | M9381 | MOPS sodium salt |
| Cyclohexane | Carlo Erba | ||
| Humic acid | Extracted from an organic-rich soil of an Alpine Valley, freeze-dried, MW 5-40 kDa | ||
| NH4OH | Carlo Erba | 419943 | |
| FeCl3·H2O | Sigma-Aldrich | 44944 |
参考文献
- Kaplan, D. I., et al. Influence of oxidation states on plutonium mobility during long-term transport through an unsaturated subsurface environment. Environ. Sci. Technol. 38 (19), 5053-5058 (2004).
- Taylor, D. M. Environmental plutonium - Creation of the universe to twenty-first century mankind. Plutonium in the Environment. 1, 1-14 (2001).
- Maher, K., Bargar, J. R., Brown, G. E. Environmental Speciation of Actinides. Inorganic Chemistry. 52 (7), 3510-3532 (2013).
- Kurosaki, H., Kaplan, D. I., Clark, S. B. Impact of environmental curium on plutonium migration and isotopic signatures. Environ. Sci. Technol. 48 (23), 13985-13991 (2014).
- Orlandini, K. A., Penrose, W. R., Nelson, D. M. Pu(V) as the stable form of oxidized plutonium in natural-waters. Marine Chemistry. 18 (1), 49-57 (1986).
- Kaplan, D. I., et al. Eleven-year field study of Pu migration from Pu III, IV, and VI sources. Environ. Sci. Technol. 40 (2), 443-448 (2006).
- Morgenstern, A., Choppin, G. R. Kinetics of the oxidation of Pu(IV) by manganese dioxide. Radiochim. Acta. 90 (2), 69-74 (2002).
- Davison, W., Zhang, H. In-situ speciation measurements of trace components in natural-waters using thin-film gels. Nature. 367 (6463), 546-548 (1994).
- Zhang, H., Davison, W. Diffusional characteristics of hydrogels used in DGT and DET techniques. Anal. Chim. Acta. 398 (2-3), 329-340 (1999).
- Cusnir, R., Steinmann, P., Bochud, F., Froidevaux, P. A DGT Technique for Plutonium Bioavailability Measurements. Environ. Sci. Technol. 48 (18), 10829-10834 (2014).
- Froidevaux, P., Steinmann, P., Pourcelot, L. Long-Term and Long-Range Migration of Radioactive Fallout in a Karst System. Environ. Sci. Technol. 44 (22), 8479-8484 (2010).
- Bajo, S., Eikenberg, J. Preparation of a stable tracer solution of plutonium (IV). Radiochim. Acta. 91 (9), 495-497 (2003).
- Saito, A., Roberts, R. A., Choppin, G. R. Preparation of solutions of tracer level plutonium (V). Anal. Chem. 57 (1), 390-391 (1985).
- Bajo, S., Eikenberg, J. Electrodeposition of actinides for alpha-spectrometry. Journal of Radioanalytical and Nuclear Chemistry. 242 (3), 745-751 (1999).
- Dai, X. X., Christl, M., Kramer-Tremblay, S., Synal, H. A. Ultra-trace determination of plutonium in urine samples using a compact accelerator mass spectrometry system operating at 300 kV. Journal of Analytical Atomic Spectrometry. 27 (1), 126-130 (2012).
- Christl, M., et al. The ETH Zurich AMS facilities: Performance parameters and reference materials. Nuclear Instruments and Methods in Physics Research B. 294, 29-38 (2013).
- Blinova, O., et al. Redox interactions of Pu(V) in solutions containing different humic substances. Journal of Alloys and Compounds. 444, 486-490 (2007).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved