Method Article
分化およびアポトーシス恒常性を通じアダルト生物における脂肪細胞の数の調節のメカニズム
要約
Adipose tissue (AT) can influence whole body homeostasis, therefore understanding the molecular mechanisms of adipocyte differentiation and function is of importance. We provide a protocol for gaining new insights into these processes by analyzing adipocyte homeostasis, differentiation and hypoxia exposure as a model for induced adipocyte apoptosis.
要約
Considering that adipose tissue (AT) is an endocrine organ, it can influence whole body metabolism. Excessive energy storage leads to the dysregulation of adipocytes, which in turn induces abnormal secretion of adipokines, triggering metabolic syndromes such as obesity, dyslipidemia, hyperglycemia, hyperinsulinemia, insulin resistance and type 2 diabetes. Therefore, investigating the molecular mechanisms behind adipocyte dysregulation could help to develop novel therapeutic strategies. Our protocol describes methods for evaluating the molecular mechanism affected by hypoxic conditions of the AT, which correlates with adipocyte apoptosis in adult mice. This protocol describes how to analyze AT in vivo through gene expression profiling as well as histological analysis of adipocyte differentiation, proliferation and apoptosis during hypoxia exposure, ascertained through staining of hypoxic cells or HIF-1α protein. Furthermore, in vitro analysis of adipocyte differentiation and its responses to various stimuli completes the characterization of the molecular pathways behind possible adipocyte dysfunction leading to metabolic syndromes.
概要
世界保健機関(WHO)から2014年の報告によると、世界の成人人口の39%が太りすぎであり、13%は1肥満です。近い将来、太りすぎの人々は、高齢者人口のかなりの割合を含むことになります。肥満および老化の重要な特徴は、罹患率および死亡率2に関連して脂肪の調節不全です。アディポカイン、脂肪組織(AT)によって分泌されるタンパク質は、肥満などの代謝症候群を誘発し、2型糖尿病3を入力することができます 。代謝性疾患は、主に拡張4 ATで、その結果、脂肪細胞の脂肪滴の過剰なエネルギー貯蔵、によって引き起こされます。それを制御するための機会を見つけるために原因と拡張ATの分子機構を決定することは興味深いことです。
脂肪細胞の脂肪滴に過剰なエネルギー貯蔵プロセス:過栄養二つの事象により調節されるATの拡大につながり肥大(脂肪細胞のサイズの増大)につながる、とも脂肪細胞の肥大5として知られ、脂肪生成を増加させました。脂肪生成は、脂肪細胞への多分化間葉系幹細胞(MSC)の分化の過程です。まず、MSCはコミットメントフェーズ中に前駆脂肪細胞へと発展します。第二に、前脂肪細胞は、さらに成熟した機能的な脂肪細胞6の特徴を獲得するために分化します。いくつかの転写因子は、亜鉛フィンガータンパク質423(Zfp423)および早期B細胞因子1(EBF1)として、前脂肪細胞の決意のマスター調節因子として同定されています。 Zfp423は早期のコミットメントを誘導するのに対し、EBF1は、脂肪細胞の前駆細胞6の生成に必要とされます。分化はしっかりペルオキシソーム増殖因子活性化受容体γ(PPARγ)は、必須の転写因子7となる転写カスケードによって制御されます。さらに重要な転写因子はCCAAT /エンハンサー結合タンパク質(Cです/ EBP)ファミリーのメンバー( すなわち 、C /EBPα、C /EBPβ、およびC /EBPδ)、クルッペル様因子(KLFs)、cAMP応答エレメント結合タンパク質(CREB)および早期成長応答20(Krox20)6。
最近では、アクチベータータンパク質-1(AP-1)ファミリーは、脂肪細胞の分化プロセス8,9に関与することが示されています。 AP-1ファミリーはフォス、Junおよび/または活性化転写因子(ATF)のメンバーからなる二量体タンパク質複合体により形成されます。 FOS関連抗原1および2(FRA-1とフラ-2)脂肪細胞の分化を調節することができます。フラ-1はFRA - 2コントロール脂肪細胞のターンオーバー9のに対し、C /EBPα8を阻害することにより、脂肪細胞分化を阻害します。フラ-2は、それによってだけでなく、脂肪細胞分化の間にPPARγ2の発現を抑制することにより、脂肪細胞の数が減少するだけでなく、低酸素誘導因子(HIFS)式の直接の抑制を介して脂肪細胞のアポトーシスを減少させます。 HIFファミリーはHETEですHIF-1α、HIF-2αとHIF-1βから成るrodimeric転写因子複合体、。ヘテロは、酸素感受性HIF-αタンパク質(HIF-1αまたはHIF-2α)と酸素と小文字を区別しないHIF-1βサブユニット10から構成されています。酸素正常状態の間に、HIF-αタンパク質は、ポリユビキチン化され、最終的にプロテアソーム11によって分解されます。低酸素条件下では、拡張時にATで発生する、HIF-αタンパク質は、もはや、ヒドロキシル化されません。したがって、これらは、恒常的に発現するHIF-1βで安定化し、フォームダイマーになります。 HIF応答要素によって制御される遺伝子の転写活性化は、血管形成、代謝、炎症12の調節に関与しています。確かに、HIF-1αは、エネルギー消費や脂質の末梢利用を阻害し、グルコース耐性を誘導することにより、同様にレプチンレベルとHFD誘発性脂肪肝13を増加させることにより機能不全AT推進しています。また、HIF-1αはadipocyを調節しますテアポトーシスのin vivoおよびin vitro 9インチ
現在のプロトコルは、成体マウスに脂肪細胞の恒常性の分子的特徴を解明する状態で勉強するための方法を説明します。これは、 インビボおよびインビトロで脂肪細胞のアポトーシス、増殖および分化は、低酸素によって調節することができる方法を示しています。そうするために、我々は、FABP4-CreERTマウス9とフラ-2フロックス対立遺伝子を持つマウスを交配させることによって生成されたフラ-2の脂肪細胞特異的欠失を有するマウスを使用します。 FABP4-CreをERTマウスを使用することにより、削除は、脂肪細胞タモキシフェン注射14による特定および誘導性です。大人のモデルでは、タモキシフェンの腹腔内注射は6週齢で始まる連続5日間にわたって行われています。分析が行われる前に、このように、マウスを6週間、通常食または高脂肪食に供します。本研究で用いたマウスは、雄のようなエストロゲンなどの女性ホルモンを避けるためにのC57BL6背景に基づいていました、体脂肪分布15を調節することが示さ。別の遺伝的背景を使用すると、脂質管理16の歪み関連の違いに起因する代謝表現型を、変更される場合があります。
このプロトコルは、組織学を用いて、低酸素下でATを分析する方法および免疫組織化学とプロファイリング分析遺伝子を用いたin vivoでの脂肪細胞のアポトーシス、増殖および分化を定量化する方法を示しています。研究は、低酸素に暴露することによって変更された一次脂肪細胞分化及びアポトーシスを分析する方法を示す、 インビトロ実験によって完成されます。
プロトコル
倫理の声明:動物は、ドイツ動物保護法のガイドラインに従って、標準化された状態で収納されています。動物は、標準的な食事と水を自由に供給し、12時間の昼/夜サイクルに保たれています。動物と全ての実験は、地元の倫理委員会によって承認されています。
成人男性における脂肪細胞恒常性のin vivo解析では 1
- インビボで低酸素症を定量最初のマウスの体重を決定し、次いで固体ピモニダゾール塩酸腹腔内に60 mg / kg体重を注入する(例:25gのマウスに1.5 mgの注入)。ピモニダゾールは、タンパク質、ペプチドおよびアミノ酸におけるチオール基と付加物を形成し、特異的抗体によって検出された有効な低酸素のマーカーです。
- マウスを犠牲にし、perigonadal脂肪パッド( 図1)を取り外します。
- 45分の注射後、CO 2窒息とその後の頸椎脱臼によりマウスを生け贄に捧げます。
- ( 図1に示されるように)マウスの四肢を突き止めるし、腹腔を開きます。腹腔内部の左右perigonadal(精巣上体)脂肪パッドを取り外します。
注: 図1に示すように、脂肪パッドは、腹膜リーフレットによって精巣上体にバインドされている(perigonadal脂肪パッドは矢印で示されています)。 - 脂肪パッドから生殖腺組織を削除するように注意してください。体重(グラム)あたりの脂肪パッドの重量(g):比率を計算するために脂肪パッドの重みを決定します。
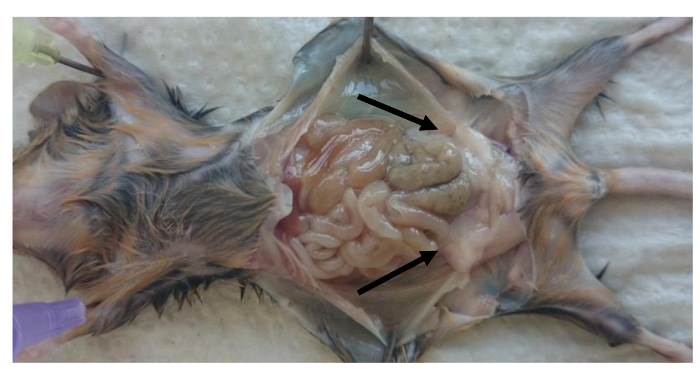
図1: マウスの腹腔内perigonadal脂肪パッドの場所 。犠牲後の成体マウスにおけるperigonadal脂肪局在の絵。 Perigonadal脂肪パッドは、矢印で示されている。 Vにはこちらをクリックしてくださいこの図の拡大版をIEW。
- 定量的な遺伝子発現プロファイルをコンパイルするには、RNAを単離するために、1 perigonadal脂肪パッドを使用します。注:組織をストア組織サンプルを-80℃または液体窒素中でRNA安定化溶液中に、処理されるまで。
- 脂肪パッドを均一化するには、グアニジンイソチオシアネートとフェノールの1ミリリットル単相溶液に脂肪パッドを追加します。 (30秒のポーズで、2回20秒)6500 rpmでホモジナイザーで組織を粉砕するセラミックビーズ(1.4ミリメートル)を含むチューブを使用してください。
- (Chomczynskiとサッキ17によるシングルステップ法)は次のようにRNAを分離します。
- 5分間、12,000×gでの、相分離マイクロチューブに均質化された脂肪パッドを転送し、0.2ミリリットルボリュームクロロホルムを追加し、15秒間振る、室温で5分間インキュベートし、遠心分離します。新しいマイクロチューブにRNAが含まれている上部の水相(約400μl)を、転送します。 DNA-含んを含めないでくださいる間期またはタンパク質含有フェノール相。
- (-20℃で一晩インキュベートすることも可能です)混合し、4℃で15分間インキュベートし、RNAを沈殿1容量のイソプロパノールを追加します。 10分間、12,000×gで遠心分離します。慎重イソプロパノール上清を取り除きます。 10分間、12,000×gでの遠心分離ステップで75%のエタノールで2回洗浄します。
- 室温で約10分間、沈殿したRNAを乾燥させた後、50μl中に溶解し、H 2 O(RNaseフリー)。これを容易にするために、65℃で2分間インキュベートします。
注:-80℃で、または長期保存のために液体窒素中75%エタノールでRNAを保ちます。 - (最適な商が1.8と2.2の間にある)260/280によってRNA調製物を定量化し、260によって濃度を計算します:
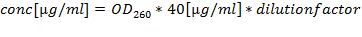
- DNAの混入を避けるために、RNA調製1μgのダイジェスト10μlの容量で37℃で30分間、1 UのDNase Iと。 10分間65℃で不活性化します。
注:このステップはオプションです。 - 定量的PCRの用途に適した一本鎖cDNAを生成するために逆転写酵素反応のために1μgのRNAを含むRNA調製物10μLを使用します。成分およびそれらの量を表1に示します。
- 定量的リアルタイムPCR反応のためのPCRマスターミックスを使用してください。全体の脂肪パッド内の代謝変化を決定するために、特定のATの恒常性に関与する遺伝子のためのプライマー( 表2)および表3に記載されているPCR条件を使用します。
- リアルタイムPCRデータ解析。
- ベースライン( 図2)、蛍光シグナルの変化がない1〜15の通常のサイクルを規定します。リアルタイムPCRソフトウェアは、その結果、ベースライン蛍光を、内部リファレンス色素、ROXに特定の蛍光シグナルを正規化しますプライマーによる特定の信号の大きさ、デルタRnを(ΔRn)。
- 増幅曲線の指数関数相内にしきい値を設定します。交点は、閾値サイクル(Ct)を定義します。 CT値に基づいて、相対的な発現(ΔCt値)と変化倍率(ΔΔCT)を計算します。
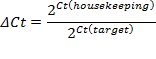
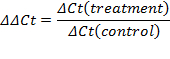
| 成分 | ボリュームμL/反応 |
| 10×RTバッファー | 2.0 |
| 25倍のdNTPミックス(100ミリモル) | 0.8 |
| 10倍RTランダムプライマー | 2.0 |
| MultiScribe逆転写酵素 | 1.0 |
| ヌクレアーゼフリーH 2 O | 4.2 |
| 1μgのRNA | 10 |
| 反応あたりの合計 | 20 |
表1:一本鎖cDNAを生成するために逆転写酵素反応のためのそれぞれの体積を有する部品。
| 公式フルネーム | シンボル | シーケンス3 ' - > 5' | ||
| フォワード | 逆 | |||
| 脂質生成 | デルタ様1ホモログ(県-1) | DLK1 | GACACTCGAAGCTCA CCTGG | GGAAGGCTGGGACGG GAAAT |
| 初期のB細胞因子1 | EBF1 | CCACCATCGACTACGG CTTC | TCCTGGTTGTTGTGGGG CATC | |
| ジンクフィンガータンパク質423 | Zfp423 | GTGCCCAGGAAGAAGA CGTA | GGCGACGTGGATCTGA ATCT | |
| 脂肪酸結合タンパク質4(AP2) | FABP4 | TCACCTGGAAGACAGCT CCTC | AAGCCCACTCCCACTTC TTTC | |
| CCAAT /エンハンサー結合タンパク質(C / EBP)、アルファ | CEBPA | AAGAGCCGCGACA AGGC | GTCAGCTCCAGCACCT TGTG | |
| CCAAT /エンハンサー結合タンパク質(C / EBP)、ベータ | Cebpb | TTTCGGGACTTGATGC AATC | CCGCAGGAACATCTTT AAGG | |
| タンパク質1結合cAMP応答エレメント | CREB1 | ACTCAGCCGGGTACT ACCAT | TTGCTGCCTCCCTGTT CTTC | |
| CCAAT /エンハンサー結合タンパク質(C / EBP)、デルタ | Cebpd | CAGCGCCTACATTGAC TCCA | GTTGAAGAGGTCGGCG AAGA | |
| クルッペル様因子4 | Klf4の | GCAGTCACAAGTCCCC TCTC | TAGTCACAAGTGTGGG TGGC | |
| 早期成長反応2(Krox20) | EGR2 | AGGCGGTAGACAAAATC CCAG | GATACGGGAGATCCAG GGGT | |
| ペルオキシソーム増殖因子活性化受容体γ | PPARG | AGAGGTCCACAGAGCTG ATTC | GATGCACTGCCTATGAGC ACTT | |
| 脂質生成 | アセチルコエンザイムAカルボキシラーゼアルファ | Acaca | TGGGGACCTTGTCTTCA TCAT | ATGGGCGGAATGGTCTC TTTC |
| 脂肪酸合成酵素 | FASN | ACATCCTAGGCATCC GAGA | CCGAGTTGAGCTGGGT TAGG | |
| ステアロイルコエンザイムデサチュラーゼ1 | SCD1 | CGGGATTGAATGTTCTTG TCGT | TTCTTGCGATACACTCTG GTGC | |
| 脂肪分解 | パタチンのようなホスホリパーゼドメインcontainingの2 | Pnpla2 | AAGGACCTGATGACCA CCCT | CCAACAAGCGGATGGT GAAG |
| 脂肪酸の取り込み | リポタンパク質リパーゼ | LPL | GTATCGGGCCCAGCAA CATTATCC | GCCTTGCTGGGGTTTTC TTCATTC |
| CD36抗原 | CD36 | GTCTTCCCAATAAGCATGT CTCC | ATGGGCTGTGATCGGA ACTG | |
| 低酸素症 | 低酸素誘導因子1、アルファサブユニット | HIF1A | CCTGCACTGAATCAAGAG GTGC | CCATCAGAAGGACTTGCT GGCT |
| (別名:HIF-2alpha)内皮PASドメインタンパク質1 | EPAS1 | CAAGCTGAAGCTAAAG CGGC | TTGGGTGAATTCATCG GGGG | |
| フォン・ヒッペル - リンダウ腫瘍抑制 | VHL | ACCGAGGTCATCTTTG GCTC | TTCCGCACACTTGGGT AGTC | |
| (別名:HIF-1β)アリール炭化水素受容体核輸送 | ARNT | TGGGTCATCTTCTCGC GGTT | TGTCCTATCTGAGCAT CGTG | |
表2: 脂肪細胞の恒常性を分析するために使用される各プライマーの配列を有する遺伝子のリスト。
| ステップ | 温度(℃) | 時間(分:秒) | ||
| ポリメラーゼ活性化 | ホールド | 95 | 10時 | |
| PCR | 40サイクル | Denaturize | 95 | 0時15分 |
| アニーリング/伸長 | 60 | 午前一時 | ||
| 融解曲線 | 60〜95 | 0.5℃/秒 | ||
表3:リアルタイムPCR条件。
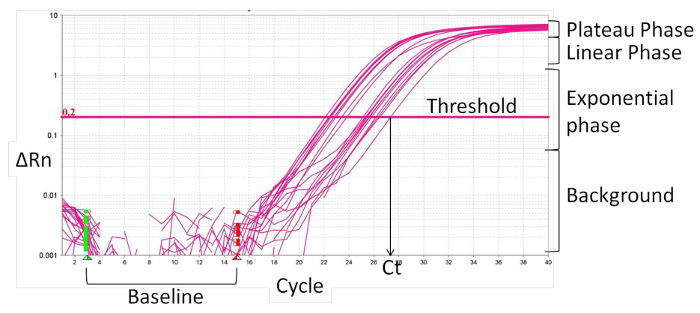
図2: リアルタイムPCR増幅曲線の特徴は、 この図の拡大版をご覧になるにはこちらをクリックしてください。
- 脂肪細胞の恒常性の組織学的分析を実行するには、第二perigonadal脂肪パッドを使用します。組織を乾燥するしないでください!
- 3.7%で、パラフィンに埋め込 んで一晩、PBS緩衝ホルムアルデヒドを、脂肪パッドを修正しました。(他の場所で18説明するように指示に従ってください)し、2-5μmの厚さの切片(最大5ミクロン)に埋め込 まれた組織を切断します。
- ヘマトキシリンおよびエオシン(H&E)染色した後、明視野顕微鏡でのフィールドと脂肪細胞のサイズあたりの脂肪細胞の数を決定します<オール>
- キシレン中で5分間3回洗浄し、100%エタノールで2分間および96%エタノールで2分間、2回部を2回再水和することによって脱パラフィン切片。最後に、5分間蒸留H 2 O中部を洗浄します。
- 室温で10分間、蒸留H 2 Oで5,5分間H 2 Oで洗浄する:ヘマトキシリンで染色は、1に希釈しました。 30秒間エオシン溶液で染色(20ミリリットルの5%エオシンY / H 2 O / 25μlの氷酢酸を蒸留210ミリリットル)と5分間のH 2 Oで再び洗います。
- 2分間2回、各96%エタノールおよび100%エタノールを用いて切片を脱水し、5分間、3回キシレン。無水実装剤とのセクションをマウントします。
- 明視野顕微鏡下でセクションを評価します。 ImageJの1.48v 19と脂肪細胞を分析する方法の代表的な例を図4に示します。 3:単位面積当たりのセル(μmの2)、多数のセル面積(×10 3μm2で)、セルサイズ(μm)で。
- ImageJ 1.48vのセクションの画像を開きます。画像のパラメータは、代わりに長さの単位のピクセルで表示された場合は、スケールを調整します。
- ツールバーの[*ストレートライン*を選択し、スケールバーを参照することにより、既知の距離にラインを調整します。 分析のための移動- > セットスケールラインの距離をピクセル単位で示されています。既知の距離と長さの単位、 例えば 、ミクロンを追加します。 [OK]をクリックして確定します。画像のサイズやパラメータの分析は、所与の長さの単位で示されています。
- 脂肪細胞のパラメータを決定するために、しきい値を調整します。 イメージに移動- > 調整 - > しきい値は、 しきい値ウィンドウを開きます。以下の設定を選択します: 閾値化方法 :デフォルト; しきい値の色 :B&W; 色空間 :HSB。絵は今、黒と白で示されています。調整します明るさは白色脂肪細胞をクリアすると、 図のように、黒の間隙を閉じます。図3b。
- ツールバーの*マルチポイント*選択してμmの2( 図 3E)あたりの脂肪細胞の数をカウントし、カウントのために、各セルをマーク。
- 脂肪細胞のサイズを決定するには、ツールバーで再び*ストレートライン*を選択して、脂肪細胞( 図3c)の直径を描きます。 分析のための移動- > 測定と新しいウィンドウがミクロンの直径の長さと、表示されます。
- 脂肪細胞の面積を決定するには、*ワンド(トレース)ツール*を選択して 、脂肪細胞の内側をクリックします。脂肪細胞の内壁には、赤色( 図3d)で選択されています。 分析のための移動- > 測定と新しいウィンドウが2μmで、この脂肪細胞の面積と、表示されます。
- immunohistのため次のようにochemistry、抗体とのTdT媒介dUTPをビオチンニック末端標識(TUNEL)染色のためのセクションを準備します。
- キシレン中で5分間3回洗浄し、100%エタノールで2分間および96%エタノールで2分間、2回部を2回再水和することによって脱パラフィン切片。最後に、蒸留H 2 O中にセクションを洗います
- 抗原回復のために、(10 mMトリス/塩酸、pHが7.4から8で20μgの/ mlの)プロテイナーゼKワーキング溶液を用いて37℃で30分間、組織切片を消化し、PBSですすいでください。
- 湿ったチャンバー内で抗体染色を実行します。
- 内因性ペルオキシダーゼをブロックするために、続いてPBSで5分間2回洗浄して、10分間、PBS中の3%過酸化水素を使用します。抗体の非特異的結合をブロックするには、PBS中の10%血清を使用しています。この場合、ヤギに、二次抗体のホストの血清を使用してください。
- 染色のために、アポトーシス、増殖および低酸素症の検出のための抗体を使用します( 表4)。 PBS / 10%ヤギ血清で抗体を希釈します。 4℃で一晩インキュベートします。 PBSで5分間のセクションを3回洗浄します。
- 信号を強化するために、表5に記載されているように希釈して、ビオチン化二次抗体を使用しています。低酸素の検出のために、二次抗体としてHRP結合ウサギ抗FITCを使用します。室温で1時間インキュベートします。セクションを2回PBSで5分間洗浄します。
注:)FITC-MAB1と低酸素染色のために、ステップ1.4.4.4をスキップ)、ステップ1.4.4.5に進みます。 - 別の45分間のセクションを追加し、各スライド、室温で30分間、50μlのビオチン化ペルオキシダーゼHとのプレインキュベーション50μlのアビジン溶液(この方法はまた、アビジン/ビオチンABC複雑な製剤と呼ばれる)のためにと。 PBSで5分間、2回洗浄します。
- 染色は(5〜10分の間)より強くなるまでペルオキシダーゼ基質溶液中のセクションをインキュベートします。蒸留で5分間洗浄H 2 O.
- 室温で10分間蒸留H 2 Oで5,5分間H 2 Oで洗浄する:対比染色のために、ヘマトキシリンで染色は1に希釈しました。
- 5分間、2分間、キシレン96%エタノール、100%エタノール中で3回、2回、それぞれのセクションを脱水。カバースリップし、無水封入剤とのセクションを封印。明視野顕微鏡下でセクションを評価します。
- TUNELアッセイによりアポトーシスを決定し、製造元の指示に従ってください。
- 450μlのラベル溶液に50μlの酵素溶液を追加します。その後、組織切片に50μlのTUNEL反応混合物を適用し、暗所で加湿雰囲気中で37℃で60分間インキュベートします。 5分間、PBSで切片を3回洗浄し、対比するためのDAPI(4 '、6-ジアミジノ-2-フェニルインドール)を含む蛍光マウンティング培地でマウント。
- 100倍のマニフィカと蛍光顕微鏡下でセクションを評価しますイオン。フルオレセインの測定のために488 nmでの励起波長を使用し、515から565ナノメートル(緑レーザ)との間で検出し、 DAPIは約360 nmで励起し、DNA(青色レーザー)に結合した場合、約460nmで発光します。
- DAPIおよびフルオレセインのオーバーレイを定量化:
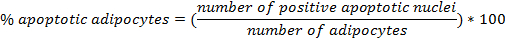

図3: 脂肪パッド部における脂肪細胞の特性明視野顕微鏡で高脂肪食(HFD)または正常食(ND)で処置した雄マウスのperigonadal脂肪パッドの断面画像を分析する(A)。閾値は、(b)は、白黒に調整され、脂肪細胞の大きさ(長さ; C)mm 2の(e)に当たり、面積(d)および脂肪細胞数のImageJ 1.48vで定量されます。F = "https://www.jove.com/files/ftp_upload/53822/53822fig3large.jpg"ターゲット= "_空白">この図の拡大版をご覧になるにはこちらをクリックしてください。
| ストック濃度 | 希釈 | |
| アポトーシス | 切断されたカスパーゼ3(Asp175)(5A1E)ウサギモノクローナル抗体 | 1:2000 |
| 増殖 | 精製したマウス抗ヒトのKi-67クローンB56(RUO) | 午前1時50分 |
| 低酸素症 | HIF-1アルファ抗体 | 1:100 |
| FITC-MAB1 | 1:100 |
表4:AT 切片の免疫組織染色のために使用されるそれぞれの希釈した抗体。
| 抗体 | 希釈 |
| ビオチン化抗マウスIgG(H + L) | 1:200 |
| ビオチン化抗マウスIgG(H + L) | 1:200 |
| HRPコンジュゲートウサギ抗FITC | 1:100 |
表5:免疫組織染色のために使用される希釈と二次抗体。
脂肪細胞恒常性のインビトロ分析2.低酸素の影響を受け
- マウスを犠牲にし、皮下脂肪組織を除去します。
- CO 2窒息とその後の頸椎脱臼によりマウスを生け贄に捧げます。
- 図4に示すように、マウスの四肢ダウン・ピン。上脚、ロースとサイドから肌を外し、 図4のように針でそれを突き止める。その後の基部に後方に位置している皮下脂肪組織を、削除図4に示すように、(鼠径部リンパ節を囲む後ろ足は、左:皮下脂肪パッド矢印で示されているの。右:矢印の鼠径リンパ節)。

図4: 皮下脂肪パッドの場所 。皮下脂肪パッドの絵。左の矢印は、皮下脂肪パッドを示し、右の矢印は、鼠径リンパ節を示している。 この図の拡大版をご覧になるにはこちらをクリックしてください。
- 以前に20を説明したように脂肪由来幹細胞(ADSC)を分離します。
- ダルベッコ改変イーグル培地、HamのF-12 10%正常ウシ血清を補充した、1%ペニシリン/ストレプトマイシン、0.5%アムホテリシンBで/ cm 2のシードADSC 4,000細胞を、16μMのビオチン、18μMパントテン酸および100μMアスコルビン酸及び70〜80の周りに密集するまでの文化を育てます培養4〜6日後に到達される%、。
- 脂肪細胞への分化を誘導します。
- トリプシン処理により表面から付着ADSCを削除します。
- (細胞が表面から剥がれるまで)、培地を除去し、PBSで洗浄し、0.025%トリプシン溶液を追加し2分間(37℃に予熱)。すぐに培地を追加し、細胞を洗浄。
- ノイバウアーチャンバーを用いて細胞を数えます。
- ノイバウアー室の中央部にガラスカバーを置きます。細胞懸濁液1:10に希釈し、細胞懸濁液を希釈して10μlのチャンバーをロードします。角に位置する4乗、16小さい正方形で構成される各内のセルをカウントします。 1ml当たりの細胞数を計算します。
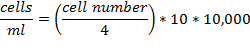
- ノイバウアー室の中央部にガラスカバーを置きます。細胞懸濁液1:10に希釈し、細胞懸濁液を希釈して10μlのチャンバーをロードします。角に位置する4乗、16小さい正方形で構成される各内のセルをカウントします。 1ml当たりの細胞数を計算します。
- (4〜6日後に到達した)12ウェル培養プレート中に(点2.2に記載のように)と約70〜80%のコンフルエンスまで培養物を成長させる種ADSC。
- adipogeを誘導培養液に5μg/ mlのインスリン、1μMのデキサメタゾンおよび5μMの3-イソブチル-1-メチルキサンチン(IBMX)を添加することによってNIC分化。 2日ごとに培地を更新。細胞が完全に7日後に分化します。
- トリプシン処理により表面から付着ADSCを削除します。
- 脂肪細胞への分化を分析するために、成熟脂肪細胞のトリグリセリドを染色するオイルレッドOで染色します。
注意:作業は換気フードの下で実行する必要があります!- 、培地を除去し、PBSで穏やかに脂肪細胞を洗浄し、2ミリリットルの10%ホルマリンで60分間細胞を固定。
- 、オイルレッドO染色溶液を調製し、蒸留2の部分と赤色のオイルOのストック溶液(100mL、99%イソプロパノール中に溶解し300mgの赤色のオイルOの粉末)H 2 Oの3部を混合し、室温で10分間インキュベートします。 0.2μmの注入フィルターを通してオイルレッドO作業溶液をフィルタリングします。
注意:作業溶液は、2時間安定しています。 - オイルレッドO染色のために、H 2と脂肪細胞を洗浄し、ホルマリンを除去 O、5分間2ミリリットルの60%イソプロパノールでインキュベートイソプロパノールを除去し、5分間2ミリリットルオイルレッドO作業溶液を追加します。水が透明になるまで水道水で細胞を洗浄します。ポイント1.4.4.5のように、ヘマトキシリンで対比染色)。
- 100倍の倍率で位相差顕微鏡下でプレートを評価します。脂肪細胞の脂質は赤表示され、核は青色表示されます。
- オプションの手順:shRNAを用いたトランスフェクションすることにより、目的の遺伝子を沈黙。
- 培地を変更し、無血清培地を追加します。
- 脂肪細胞のトランスフェクションのために、リポフェクションを使用します。製造元の指示に従い、12ウェル組織プレートあたり1μgのshRNAを使用します。脂質DNA複合体を加えた後、37℃で48時間脂肪細胞をインキュベートします。
- 低酸素にさらさ脂肪細胞を分析するために、低酸素条件下で細胞を維持するために低酸素ワークステーションまたは低酸素培養器を使用しています。研究に依存し、低酸素のC0.5、1または2%の酸素でウルド。
- Vおよびその後のフローサイトメトリー分析FITC標識アネキシンによってアポトーシスを分析します。
- 余分なソフトセルスクレーパーで脂肪細胞を収集し、PBSで洗浄し、100μlのアネキシンV結合緩衝液(10mMのHepes / NaOHを、pHが7.4; 140mMの塩化ナトリウム、2.5mMのCaCl 2を)に1×10 6個の細胞を追加します。製造業者が推奨するアネキシンV-FITCの量を追加し、室温で15分間インキュベートします。
- 測定のフローサイトメトリーのために、200μlのアネキシンV結合緩衝液および核対比の1μMを追加します。緑と紫のチャンネルで蛍光を決定します。アネキシンV + /核対比+細胞は、二次壊死性およびアネキシンV + /核対比として定義されている-細胞がアポトーシスを起こした細胞のように定義されている( 図5)。
- 定量的に、低酸素条件下での恒常性を決定するために、脂肪細胞のRNAレベルを分析します。
- 加えます1ミリリットル単相を各ウェルにグアニジンイソチオシアネートとフェノールの溶液及び1.3.5.2に)[Chomczynskiとサッキ17によるシングルステップ法(ステップ1.3.2)を使用して] RNAを分離し、ステップ1.3.2.1のように進んでください) 。
- Vおよびその後のフローサイトメトリー分析FITC標識アネキシンによってアポトーシスを分析します。
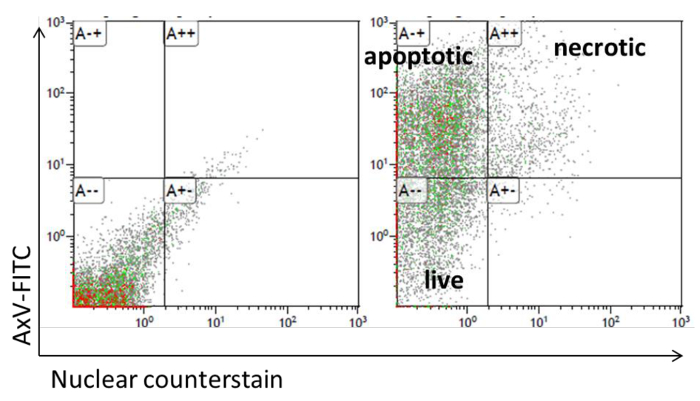
図5:フローサイトメトリーによる脂肪細胞のアポトーシス分析 。アネキシンV-FITCおよびTO-PRO-3脂肪細胞の染色FACSのドットプロットのプレゼンテーション。 この図の拡大版をご覧になるにはこちらをクリックしてください。
結果
我々は、野生型同腹子と比較して、フラ-2 FL / FL FABP4-CreERTマウスの例を用いて、 インビボおよびインビトロで脂肪細胞の恒常性を決定する方法を示しています。私たちのプロトコルが増加し、脂肪細胞のアポトーシスによって示されるように、低酸素状態によって増加したHIFの発現が脂肪細胞の機能不全と相関する方法を定義します。
高脂肪食で増加した脂肪細胞の大きさや面積(HFD)で処置したマウス
過栄養、他の要因の中で、脂肪滴に過度のエネルギー蓄積によって引き起こされる、脂肪細胞の肥大をもたらします。脂肪細胞の大きさおよび面積は、肥大の指標です。正常からの脂肪パッドのセクション(ND; 図6a)と高脂肪食(HFD; 図6b)が 6週間後に、脂肪細胞の大きさや面積のマウスと同様に定量化が明確に示す脂肪細胞の肥大HFD処置したマウス( 図6cおよびd)に増加した脂肪細胞のサイズによって示されHFDの秒。
増加し、成人の脂肪組織(AT)における低酸素フラ-2 FL / FL FABP4-CreERTマウスが増加し、HIF-1αレベルと脂肪細胞のアポトーシスに導きます
ATで低酸素症のin vivoでの状態を決定するために、フラ-2 FL / FL FABP4-CreERTマウス6週、12週齢でフラ-2削除後に分析し、野生型同腹子と比較しています。ピモニダゾールは、効果的な低酸素症マーカーとしてマウスの腹腔内に投与されます。それは無毒でATに配布することが可能です。 in vivoでの ATで低酸素脂肪細胞を免疫組織化学的抗体染色( 図7a)によって定義されています。また、マウスでのATの増加、低酸素状態が増加したHIF-1αの正ADIPを伴っていますHIF-1αの発現レベルとその標的遺伝子9の定量化によって確認された免疫組織染色図7B)によって示されるようにocytes。さらに、脂肪細胞のアポトーシスは、低酸素およびHIF-1α発現の存在と相関しているの増加フラ-2 FL / FL FABP4-CreERTマウスおよび対照同腹子からAT切片のTUNEL染色( 図7c)を示しています。
低酸素誘導性の脂肪細胞のアポトーシスを介して一次脂肪細胞におけるHIF-1αの発現を増加させました
他の場所で20説明したように、in vitroで脂肪細胞のアポトーシスを分析するために、我々は、皮下脂肪パッドから生成された脂肪細胞を使用しています。予想されたように、脂肪細胞におけるHIF-1αの発現は、低酸素( 図8a)の24時間後に増加されます。さらに、HIF-1α活動、HIF標的のRNAレベルを分析するために、このようなイノス(誘導型一酸化窒素合成酵素)などの遺伝子を定量PCRによって定量化されている。 図8bは、低酸素条件下でHIF-1αの発現増加がアイノスmRNAレベルの増加につながることを示しています。我々はすでに、in vivoで示されているので、脂肪細胞におけるHIF-1αの発現を増加させた( 図8)が増加した脂肪細胞のアポトーシスと相関し、アポトーシスはまた、低酸素条件下でアネキシンV染色によりin vitroでの培養において定量化されます。 in vivoデータ( 図7)と一致して、増加したHIF-1αレベルは、低酸素状態( 図8b)によって誘発される増加した脂肪細胞のアポトーシスを伴っています。また、その低酸素誘導性アポトーシスを証明するためには、HIF-依存します。 HIF-1αまたはHIF-2αは、野生型またはフラ-2欠損マウス由来の脂肪細胞におけるRNA干渉によってサイレンシングされます。アネキシンによって示されるように増加した脂肪細胞のアポトーシスは、HIF-1αまたはHIF-2αをサイレンシングすることによって復元されます低酸素センサHIF-αは、脂肪細胞のアポトーシスを調節することを証明する図8bにおけるV染色、。
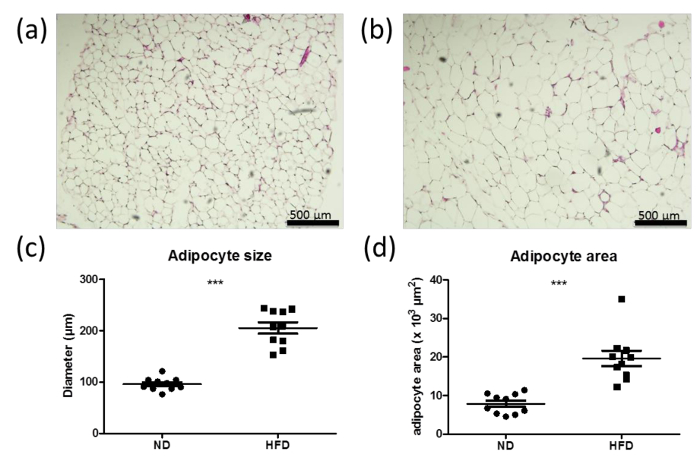
図6:高脂肪食(HFD)マウスにおける脂肪細胞の大きさや面積の増加普通食(ND)を与えた雄の野生型マウスのperigonadal脂肪パッドからのセクションの(a、b)は、H&E染色(a)または高いです。 6週間-fat食(HFD)(B)。バーは500μmで表します。 (C、D)、(b)は、6週間のND(a)またはHFDを与えた野生型マウスのperigonadal脂肪パッドから脂肪細胞の大きさ(C)と領域(D)の定量。 n = 10のデータは、平均値±SEMとして示されています。統計分析は、スチューデントさt検定を用いて行きました。 ***はp <0.0001。://www.jove.com/files/ftp_upload/53822/53822fig6large.jpg "ターゲット=" _空白 ">この図の拡大版をご覧になるにはこちらをクリックしてください。
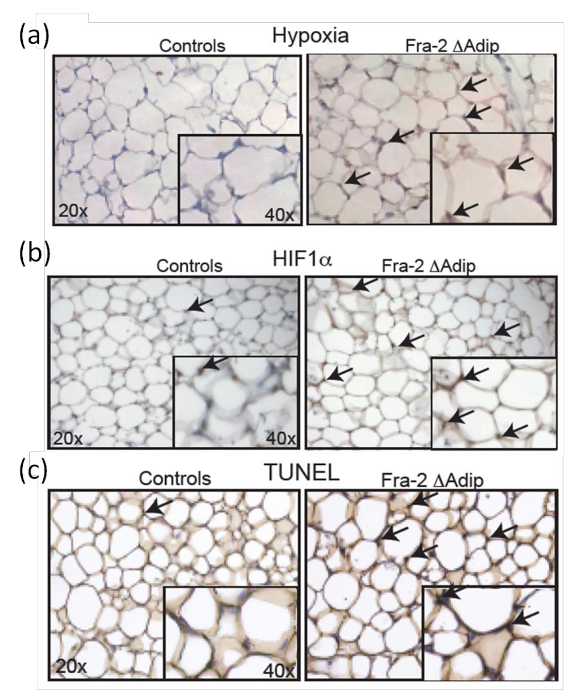
図7:大人フラ-2の脂肪細胞においてHIF-1αレベルおよびアポトーシスの増加 FL / FL FABP4-CreERTマウス 。低酸素(a)とHIF-1α男性フラ-2 FL / FL FABP4-creERTマウスと男性の対照同腹子タモキシフェン注射後6週間のATにおける(b)の染色。倍率20Xは、40Xを挿入します。黒矢印は、低酸素領域とHIF-1α陽性細胞を示しています。 (c)のタモキシフェン注射後6週間ATフラ-2 FL / FL FABP4-CreERTマウスおよび対照同腹子におけるTUNEL染色。倍率20Xは、40Xを挿入します。黒矢印はTUNEL陽性細胞を示しています。この図は、ルターらから変更されていますアル。9。 この図の拡大版をご覧になるにはこちらをクリックしてください。
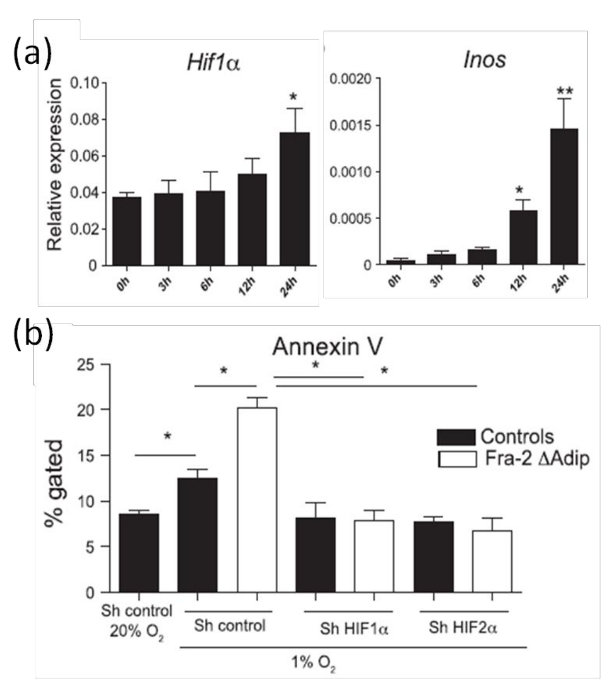
図8: 低酸素によって誘導される一次脂肪細胞における増加したHIF-1αの発現と脂肪細胞のアポトーシス低酸素室に配置された一次脂肪細胞におけるHIF-1αとHIFSターゲットアイノスmRNAレベルの(a)のリアルタイムPCR分析は、指示された時点で分析しました。単離された初代脂肪細胞におけるアネキシンV FACS染色によるアポトーシスの(b)の定量フラ-2 FL / FL shの制御またはHIF-1αまたはHIF-2αに対するshのプラスミドでトランスフェクトし、低酸素下に置かFABP4-CreERTマウスまたは野生型対照24時間(1%O 2)。この図は、ルターらから変更されています。 9。データはSD統計分析±値はスチューデントのt検定を用いて行った、平均示されています。 * P <0.05、**はP <0.01を有意であると受け入れられた。 この図の拡大版をご覧になるにはこちらをクリックしてください。
ディスカッション
脂肪細胞は、過栄養5に起因する過剰なエネルギー貯蔵により誘導される脂肪細胞の過形成および肥大を、明らかにし、その大きさ、数および面積によって表現型を特徴とします。脂肪酸の調節不全とその後のメタボリック症候群につながるこれらのイベントはまた、「健康な」脂肪拡張と呼ばれる保存代謝と増加脂肪塊の状態です。例えば、Kusminski ら 21は、大量の脂肪の膨張を有するマウスが脂肪拡大は必ずしもメタボリックシンドロームにリンクされ、脂肪細胞の特性を評価するために慎重に決定する必要がないことを示唆する、代謝的に健康なままであることを示しました。脂肪組織(AT)は、身体の代謝の調節において重要な役割を果たしています。 ATは、脂質異常症、アテローム性動脈硬化症、高インスリン血症および高血糖症3に影響を与える可能性が最大の内分泌器官です。恒常性と分子メートルATの評価それを規制echanismsは、代謝系疾患のより良い理解を可能性があります。したがって、脂肪細胞分化を調節するメカニズムを解明、脂肪細胞のサイズおよび脂肪パッド質量は、肥満障害のための新たな治療的処置を開発するために役立つだろう。 インビボおよびインビトロ方法で使用することにより、脂肪細胞分化および活性の食品および遺伝子発現への影響の役割を決定することが可能です。 ATの恒常性を決定するために、我々のプロトコルによって示唆されているように、脂肪細胞の分化、増殖およびアポトーシスの間のバランスを決定することは、グルコースおよびインスリンの代謝反応22-24の分析と同様に重要です。
発現プロファイリングは、一次脂肪細胞における脂肪生成、脂質生成、脂肪分解、脂肪酸の取り込み、低酸素症、アポトーシスおよび増殖に関与する遺伝子の解析と内臓ATは、脂肪細胞の恒常性とその可能性機能障害の概要を取得するためのハイスループット法です。興味深い候補は、さらにウエスタンブロットまたは免疫組織染色によりタンパク質レベルで分析する必要があります。非対称シアニン色素を用いてリアルタイムPCRシステムを介して最適な結果を得るために、1から10 ngの範囲のcDNAの濃度は、50から900nmの範囲の最適なプライマー濃度は、非特異的増幅を最小限にするために試験されるべきです。重要なコンポーネントは、プライマーです。各実験のために、融解曲線は、厳密な特異性を確保し、プライマーダイマーの形成を排除するように制御される必要があります。そのため、代わりにcDNAのH 2 Oでネガティブコントロールを使用することをお勧めします。また、市販の非対称シアニン色素は、内部基準信号を提供するために(例えば、ROXなど)、パッシブリファレンス色素を含有するマスターミックスとして提供されます。 cDNAの信号は、ウェル間の信号の変動を補正するROX信号にデータ分析中に正規化されます。もう一つのポイントは、グーを確立するために考慮されますD定量PCRシステムは、ハウスキーピング遺伝子の選択です。各条件について、いくつかのハウスキーピング遺伝子が使用されている、 例えば、HPRT、β アクチン 、GAPDH、β-2-MGまたはHSP90。
低酸素条件によって安定化されたHIFタンパク質は、マスターだけでなく、脂肪細胞生存率を決定する制御因子でなく、例えばグルコース、インスリン耐性及び脂質代謝11,25,26などの代謝の変化です。脂肪パッドに低酸素領域を確認するには、HIF-1αは、免疫組織化学によるセクションATで決定されます。 HIFタンパク質は急速に正常酸素条件下で5〜10分以内に分解されるので、手順及び組織学的分析のために脂肪パッドの固定を強固に待ち時間を回避するように制御されるべきです。したがって、だけでなくHIF染色を介して低酸素症を確実にするために、ピモニダゾールは、ATにおける低酸素領域を決定するために使用されます。それはすでに骨27に示されたようにピモニダゾールは、組織内に配布することができ、、かつ効果的にさらに28を特異的抗体結合によって、組織切片中に検出された特異的低酸素細胞中のチオール含有タンパク質に結合することによって、低酸素領域をマーク。しかしながら、他のマーカーおよび方法は、低酸素経路を分析するために使用することができます。例えば、ヒドロキシル化プロリンを認識し、プロテアソームHIFを媒介するポリユビキチン化を誘導正常酸素下でのプロリン残基のヒドロキシル化を誘導するプロリルヒドロキシラーゼ(PHD)酵素、ならびにフォン・ヒッペル - リンダウ(VHL)タンパク質の関与劣化は、経路29,30の完全な概要について分析する必要があります。また、HIFSのユビキタス検出はまた、31,32を変更することができ、タンパク質の安定性および分解を決定するであろう。
また、TUNEL染色によるのKi67による増殖とアポトーシスは、AT組織切片の染色を介して生体内で決定されます。 Ki67のとAによる増殖の定量化フローサイトメトリー分析を通じTUNELまたはアネキシンV染色によるpoptosisも33で実施されます。増殖はもちろんのKi67陽性細胞の測定によって対処されていないような脂肪細胞周期の分析のような他の技術によって測定することができます。 FACSは、アポトーシス細胞死のプロセス対壊死のレベルを決定するアネキシンVとTOP-PR-3の分析によってまた、TUNELによるアポトーシスの研究を完成させることができます。アポトーシスは、ATの恒常性に重要である、細胞死のプログラムの基本的な過程です。確かに、脂肪細胞のアポトーシスの調節不全は、肥満や脂肪異栄養症34に貢献する過程で以前に関与しています。また、2011年には、Keuper ら脂肪細胞のアポトーシスに脂肪組織の炎症をリンクされています。それらは順番にマクロファージを誘引する、マクロファージが前脂肪細胞および脂肪細胞においてアポトーシスを誘導することが示されました。マクロファージの動員は、炎症、CONTRを加速しますこのようなグルコースおよびインスリン寛容35としてメタボリックシンドロームにibutes。しかし、脂肪細胞のアポトーシスが誘導された脂肪細胞のアポトーシスが減少した体重につながる可能性の仮説にもかかわらず、まだよく研究された現象です。
現在のプロトコルは、in vivoでの増殖、アポトーシスおよび低酸素症などのさまざまな現象を研究するために免疫組織化学的手法を使用しています。したがって、組織は重要なステップである4%ホルムアルデヒドで固定しました。拡張された組織固定時間は、抗体のための非アクセス可能となるエピトープの変化をもたらします。対照的に、短い固定時間は、試薬のエピトープの感受性を増加させます。固定の推奨最適な時間は24時間です。また、切片の厚さは、それらのエピトープに結合する抗体に影響を及ぼす。最適な厚さは2から5μmの間です。 5ミクロンより厚い部分は、増加した結合部位に偽陽性の結果が得られます。対照的に、よections薄い2μmよりは少ない結合部位を含有し、正の領域が十分に定義されていません。さらに重要な要素は、エピトープへの特異的結合の品質に影響を与える抗体自体、インキュベーション時間、濃度、さらに温度があります。したがって、抗体濃度およびインキュベーション時間を検証すると、各条件のために必要です。
調査を完了するために、我々は、異なる処理、刺激または共培養することによって拡張することができ、インビトロ脂肪細胞分化プロトコルを提供します。 インビトロで脂肪細胞の培養に用いることにより、脂肪細胞分化及び機能における欠陥を決定することが可能です。信頼性の高い結果を得るためには、すべての主要な細胞用として、ADSCをおよび脂肪細胞の健全な動作と外観は非常に重要です。粒度、細胞質vacuolationsおよび/または剥離は、一次の不十分な媒体であって、微生物汚染や老化を示す劣化の兆候であり、細胞。他のプロトコル36で説明したように、骨髄から単離された間葉系幹細胞を使用することも可能であるのに対し、このプロトコルは、脂肪体組織から単離された脂肪細胞を使用しています。最新の脂肪細胞分化の非常に早い段階で発生する追加の分化の問題を反映しているのかもしれない間質前駆細胞を、含まれ、これは、当社の現在のプロトコルでは見逃される可能性があります。また、ADSCをは急速に(1週間以内に10回以上)に拡張することができ、いくつかの継代後の長期培養したADSCはまだ彼らの間葉系多能性37,38を保持しています。 ADSCをを使用して、もう一つの利点は、ADSCを簡単かつ低侵襲性の方法である脂肪吸引により患者から採取することができるので、一つは簡単に、人間に切り替えることができるということです。
ATは内分泌方法でいくつかの他の臓器に影響を与えるように、プロトコルは、アディポカインに延長すべきです。このようなレプチン、アディポネクチン、腫瘍壊死因子α(TNF)Aとアディポカイン、ND脂肪細胞によって分泌されるレジスチンは、脂肪代謝、エネルギー恒常性およびインスリン感受性39を制御することにより、代謝性疾患に影響を与えることが知られています。したがって、血清および脂肪細胞secretome分析が行われるべきです。 AT機能不全、アディポカインならびにIL-6などの炎症性サイトカインの場合において、例えば肝臓や膵臓などの器官の調節不全につながる、および筋肉機能の4ことができます。全身の臓器不全を排除するために、動物モデルまたは細胞培養物はグルコース刺激および取り込みに対するそれらの応答について試験することができます。
ここでは、ATおよびインビボにおける脂肪細胞の基本的な状態を分析するためのプロトコルを提供し、 インビトロで脂肪細胞の恒常性と機能性の分子機構を明らかにします。
開示事項
著者らは、開示することは何もありません。
謝辞
著者は、原稿を校正するためのデータと博士B.Grötschを製造するための博士J・ルターとK. Ubietaを親切に感謝したいと思います。この作品は、ドイツ学術協会(BO3811 / 1-1-エミー・ネーター)によってサポートされていました。
資料
| Name | Company | Catalog Number | Comments |
| RNAlater solution | Ambion | AM7021 | RNA stabilization solution |
| High-Capacity cDNA Reverse Transcription Kit | Applied Biosystems | 4368813 | |
| SYBR Select Master Mix | 4472908 | ||
| Purified Mouse Anti-Human Ki-67 | BD Biosciences | 550609 | Clone B56 (RUO) |
| Purified Mouse Anti-Human Ki-67 Clone B56 (RUO) | 550609 | Proliferation marker | |
| FITC Annexin V | BioLegend | 640906 | |
| Cleaved Caspase-3 Rabbit mAb | Cell signalling | 9664S | Clone 5A1E |
| Cleaved Caspase-3 (Asp175) (5A1E) Rabbit mAb | 9664 | Apoptosis marker | |
| Lipofectamine2000 Reagent | Invitrogen | 11668-027 | |
| TO-PRO-3 Iodide | T3605 | Nuclear counterstain, Monomeric cyanine nucleic acid stain, Excitation⁄Emission: 642⁄661 nm | |
| Mayer’s hemalum | Merck | 109249 | hematoxylin |
| pegGOLD TriFast | Peqlab | 30-2030 | TRIzol, single-phase solution of guanidine isothiocyanate and phenol |
| Percellys Ceramic Kit 1.4 mm | 91-PCS-CK14 | tubes containing ceramic beads (1.4 mm) | |
| Precellys 24 | 91-PCS24 | homogenizer | |
| HIF-1 alpha Antibody | Pierce | PA1-16601 | |
| HIF-1 alpha Antibody, 16H4L13 | 700505 | Hypoxia marker | |
| In Situ Cell Death Detection Kit, Fluorescein | Roche | 11 684 795 001 | TdT-mediated dUTP-biotin nick end labeling (TUNEL) |
| Eosin | Sigma | 318906 | |
| DNase I Solution (1 unit/µl) | Thermo Scientific | EN0525 | |
| biotinylated anti mouse IgG (H+L) | Vector Laboratories | BA-9200 | |
| biotinylated anti mouse IgG (H+L) | BA-1000 | ||
| Vectastain ABC Kit | PK-4000 | ||
| VECTASHIELD Mounting Medium with DAPI | H-1200 |
参考文献
- Obesity and Overweight. Fact Sheet °113. WHO. , (Jan 2014) (2014).
- Gong, Z., Muzumdar, R. H. Pancreatic function, type 2 diabetes, and metabolism in aging. Int J Endocrinol. , 320482(2012).
- Deng, Y., Scherer, P. E. Adipokines as novel biomarkers and regulators of the metabolic syndrome. Ann N Y Acad Sci. 1212, 1-19 (2010).
- Rezaee, F., Dashty, M. Role of Adipose Tissue in Metabolic System Disorders Adipose Tissue is the Initiator of Metabolic Diseases. J Diabetes Metab. , 008(2013).
- Rutkowski, J. M., Stern, J. H., Scherer, P. E. The cell biology of fat expansion. J Cell Biol. 208, 501-512 (2015).
- Ma, X., Lee, P., Chisholm, D. J., James, D. E. Control of adipocyte differentiation in different fat depots; implications for pathophysiology or therapy. Front Endocrinol (Lausanne). 6, 1(2015).
- Farmer, S. R. Transcriptional control of adipocyte formation. Cell Metab. 4, 263-273 (2006).
- Luther, J., et al. Elevated Fra-1 expression causes severe lipodystrophy. J Cell Sci. 124, 1465-1476 (2011).
- Luther, J., et al. Fra-2/AP-1 controls adipocyte differentiation and survival by regulating PPARgamma and hypoxia. Cell Death Differ. , (2014).
- Semenza, G. L. Regulation of mammalian O2 homeostasis by hypoxia-inducible factor 1. Annu Rev Cell Dev Biol. 15, 551-578 (1999).
- Kim, W., Kaelin, W. G. The von Hippel-Lindau tumor suppressor protein: new insights into oxygen sensing and cancer. Curr Opin Genet Dev. 13, 55-60 (2003).
- Aragones, J., Fraisl, P., Baes, M., Carmeliet, P. Oxygen sensors at the crossroad of metabolism. Cell Metab. 9, 11-22 (2009).
- Sun, K., Halberg, N., Khan, M., Magalang, U. J., Scherer, P. E. Selective inhibition of hypoxia-inducible factor 1alpha ameliorates adipose tissue dysfunction. Mol Cell Biol. 33, 904-917 (2013).
- Imai, T., Jiang, M., Chambon, P., Metzger, D. Impaired adipogenesis and lipolysis in the mouse upon selective ablation of the retinoid X receptor alpha mediated by a tamoxifen-inducible chimeric Cre recombinase (Cre-ERT2) in adipocytes. Proc Natl Acad Sci U S A. 98, 224-228 (2001).
- Clegg, D. J., Brown, L. M., Woods, S. C., Benoit, S. C. Gonadal hormones determine sensitivity to central leptin and insulin. Diabetes. 55, 978-987 (2006).
- Haluzik, M., et al. Genetic background (C57BL/6J versus FVB/N) strongly influences the severity of diabetes and insulin resistance in ob/ob mice. Endocrinology. 145, 3258-3264 (2004).
- Chomczynski, P., Sacchi, N. Single-step method of RNA isolation by acid guanidinium thiocyanate-phenol-chloroform extraction. Analytical biochemistry. 162, 156-159 (1987).
- Paraffin Processing of Tissue. Protocolsonline. , Available from: http://protocolsonline.com/histology/sample-preparation/paraffin-processing-of-tissue/ (2012).
- Schneider, C. A., Rasband, W. S., Eliceiri, K. W. NIH Image to ImageJ: 25 years of image analysis. Nat Methods. 9, 671-675 (2012).
- Planat-Benard, V., et al. Plasticity of human adipose lineage cells toward endothelial cells: physiological and therapeutic perspectives. Circulation. 109, 656-663 (2004).
- Kusminski, C. M., et al. MitoNEET-driven alterations in adipocyte mitochondrial activity reveal a crucial adaptive process that preserves insulin sensitivity in obesity. Nat Med. 18, 1539-1549 (2012).
- Trajcevski, K. E., et al. Enhanced lipid oxidation and maintenance of muscle insulin sensitivity despite glucose intolerance in a diet-induced obesity mouse model. PLoS One. 8, 71747(2013).
- Montgomery, M. K., et al. Mouse strain-dependent variation in obesity and glucose homeostasis in response to high-fat feeding. Diabetologia. 56, 1129-1139 (2013).
- de Queiroz, K. B., et al. Molecular mechanism driving retroperitoneal adipocyte hypertrophy and hyperplasia in response to a high-sugar diet. Mol Nutr Food Res. 58, 2331-2341 (2014).
- Ye, J. Emerging role of adipose tissue hypoxia in obesity and insulin resistance. Int J Obes (Lond). 33, 54-66 (2009).
- Xiong, Y., et al. The local corticotropin-releasing hormone receptor 2 signalling pathway partly mediates hypoxia-induced increases in lipolysis via the cAMP-protein kinase A signalling pathway in white adipose tissue. Mol Cell Endocrinol. 392, 106-114 (2014).
- Bozec, A., et al. Osteoclast size is controlled by Fra-2 through LIF/LIF-receptor signalling and hypoxia. Nature. 454, 221-225 (2008).
- Varia, M. A., et al. Pimonidazole: a novel hypoxia marker for complementary study of tumor hypoxia and cell proliferation in cervical carcinoma. Gynecol Oncol. 71, 270-277 (1998).
- Park, M. H., Choi, K. Y., Jung, Y., Min do, S. Phospholipase D1 protein coordinates dynamic assembly of HIF-1alpha-PHD-VHL to regulate HIF-1alpha stability. Oncotarget. 5, 11857-11872 (2014).
- Tennant, D. A., et al. Reactivating HIF prolyl hydroxylases under hypoxia results in metabolic catastrophe and cell death. Oncogene. 28, 4009-4021 (2009).
- Kim, J., So, D., Shin, H. W., Chun, Y. S., Park, J. W. HIF-1alpha Upregulation due to Depletion of the Free Ubiquitin Pool. Journal of Korean medical science. 30, 1388-1395 (2015).
- Amelio, I., et al. TAp73 opposes tumor angiogenesis by promoting hypoxia-inducible factor 1alpha degradation. Proceedings of the National Academy of Sciences of the United States of America. 112, 226-231 (2015).
- Suga, H., et al. Adipose tissue remodeling under ischemia: death of adipocytes and activation of stem/progenitor cells. Plast Reconstr Surg. 126, 1911-1923 (2010).
- Moreno-Indias, I., Tinahones, F. J. Impaired adipose tissue expandability and lipogenic capacities as ones of the main causes of metabolic disorders. J Diabetes Res. 2015, 970375(2015).
- Keuper, M., et al. An inflammatory micro-environment promotes human adipocyte apoptosis. Mol Cell Endocrinol. 339, 105-113 (2011).
- Sera, Y., et al. Hematopoietic stem cell origin of adipocytes. Experimental hematology. 37, 1108-1120 (2009).
- Zuk, P. A., et al. Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue engineering. 7, 211-228 (2001).
- Zuk, P. A., et al. Human adipose tissue is a source of multipotent stem cells. Molecular biology of the cell. 13, 4279-4295 (2002).
- Scherer, P. E. Adipose tissue: from lipid storage compartment to endocrine organ. Diabetes. 55, 1537-1545 (2006).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved