Method Article
眼内レンズ用ソフト ポリシロキサン尿素エラストマーの合成
* これらの著者は同等に貢献しました
要約
本研究では、アミノプロピル終了 polydimethylsiloxanes とジメチルビニル メチル フェニル シロキサン ブロック共重合体および柔らかいポリシロキサンを用いた尿素 (PSU) エラストマー合成経路について説明します。それは、眼内レンズを収容として Psu のアプリケーションを提示します。生体外の細胞毒性の評価法についても述べる.
要約
本研究では、眼内レンズ (a モールド) を収容として応用のソフト ポリシロキサンを用いた尿素 (PSU) エラストマーの合成経路について説明します。アミノプロピル終了 polydimethylsiloxanes (PDMS) は以前環状シロキサン octamethylcyclotetrasiloxane (4D) と 1, 3-bis(3-aminopropyl)-tetramethyldisiloxane (APTMDS) の平衡を介してリング チェーンを用意しました。フェニル基は、シロキサン バックボーン経由でに導入された D4と 2,4,6,8-テトラメチル-2,4,6,8-tetraphenyl-オクタフェニルシクロテトラシロキサン中 (D4私 Ph) の共重合。ポリシロキサンの屈折を高めるためこれらジメチルビニル メチル フェニル シロキサン ブロック共重合体を合成しました。IOL としてアプリケーション、ポリシロキサンの屈折が若い人間の目のレンズと同等である必要があります。ポリシロキサンの分子量は endblocker APTMDS に環状シロキサンの比によって制御されます。紫外可視分光光度計を使用して 200 および 750 nm 間膜の透過率測定による PSU エラストマーの透明性を調べた750 で透過値ポリジメチルシロキサンの分子量に対する nm (可視スペクトルの上部端) のプロットし、18,000 g·mol− 1の分子量まで透過率 > 90% を観察。ダイカット犬骨状の試験片に応力-ひずみテストを使用して、PSU のエラストマーの機械的性質を調べた。機械的安定性を評価するため機械的ヒステリシス、繰り返し (10 倍) を伸ばして測定 5% と 100% 伸長のための標本。ヒステリシスはかなりポリジメチルシロキサンの分子量の増加に伴い減少します。いくつかの選択した PSU のエラストマーの生体外の細胞毒性は、MTS セル実行可能性の試金を使用して評価されます。記載方法は、若い人間の目のレンズのそれとほぼ等しい屈折率のソフト ・透明・ noncytotoxic PSU エラストマーの合成を許可します。
概要
老人性白内障は、60 歳以上の年齢層に影響を与えるは、天然の水晶の高度な混濁につながります。この年齢関連の条件の原因となるは、おそらく、UV 照射1,2,3が加速酸化変更。老人性白内障のため従来の治療法には、人工の眼内レンズ (IOL) の注入によって、空のレンズ カプセルを介して注入システム2に続いて白内障のレンズの摘出が含まれます。ただし、モールドの大半は非常に堅い構造を持つアクリル系ポリマー (疎水性と親水性のアクリル酸またはメタクリル酸ポリマー) から製造されました。したがって、目は様々 な距離2,4に対応する能力を失います。したがって、固定焦点の眼内レンズのインプラント症例近いビジョン用の眼鏡に依存している (e.g。、新聞や本を読みながら)5。
白内障手術後の宿泊施設の能力を復元する方法の違いが報告されています。2 つの主要な戦略これらのアプローチの間で区別できる: 液体やゲル状のポリマーを注入して開発ソフト、折り畳み式、モールド6,7,8空水晶体カプセルを補充します。自然な人間の目のレンズ (約1-2 kPa)9; の低ヤング率でゲルを準備することができますので、「補充」はレンズの概念は有望ですただし、この方法はまだ実験的8、動物の目に関する研究のみ。
膨脹可能なシリコーン風船10液状シリコーンでいっぱいをはめ込むことによってまたは直接注入カプセル経由でヒドロシリル化で治った後シリコーン11,12レンズ カプセルが補充されています。.ただし、術前の状態と比較して低い宿泊施設振幅は、バルーンの表面のしわに関連する問題、深刻な二次白内障 (前部と後部のカプセルの混濁) の形成が注目される7をされています。 8,12,13。特に、長い硬化時間 70 分 (12 h) は、術後炎症10,14に主要な周囲の目のコンパートメントに漏洩のリスクの増加を引き起こします。水晶を交換するための他の材料の推奨したがって、ヒドロゲル ポリエチレング リコール レートに基づくビニル アルコール (N-ビニルピロリドン)15、メタクリル酸変性アクリレート変更共重合体を含むポリシロキサン16,17、poloxamer18、およびジイソシアネート架橋ホルマリン9。ただし、粘度モノマー (すなわち、注入および架橋後の腫れのゲル)、非常に低または高屈折、機械的安定性と完全性、予測不可能な術後の屈折値、低宿泊施設の範囲と白内障の形成は、主な問題6,7,8,9,15,18を構成します。商業的に、収容能力は主に折りたたみ式の眼内を開発することによって復元されます。このようなモールドのべきである毛様体筋の収縮、レンズ カプセルを介しての前歯に眼内レンズの光の動きで宿泊施設を提供します。いくつかのモデルは、1996 年、2001 年の市場および 2002年7,8で導入されています。ただし、臨床試験中に推定宿泊施設振幅それらの注入は-モールドが非常に低い (≤ 1.5 D) 裸眼 (3-4 D) を読んで6,7,8,19を許可するには,20します。 したがって、6、21の範囲 (iol)、構成の 2 つ接続されている光学 (デュアル光学 IOL) は、宿泊施設を増やすことで開発されています。相反する結果が報告されている22,23,24,25をされているにもかかわらず、人間の目で、その緩和性能の 1 つだけのレンズの設計を検討されています。
通常、シリコーンエラストマー同視される生物学的に不活性および無毒。したがって、シリコーンエラストマー医学と医用工学 (例えば、乳房インプラント、顎顔面インプラント、共同義肢、創傷被覆材、カテーテル、排水溝、シャント) における生体適合性材料として適用されている長い歴史があります。26,27. 彼らの柔らかさと、透明性と高い酸素透過性によりシリコーンエラストマーもアプリケーションを見つけるコンタクト レンズとモールド2,28,29。ただし、シリコーンは、架橋を共有して往々 にして十分な機械的完全性を得るためにフィラーを補強する必要があります。架橋エラストマーの後続の処理を禁止熱可塑性メソッドによっていずれか不利である (例えば、射出成形)、ソリューションから処理 (例えば、溶液キャスト法)。対照的に、熱可塑性ポリウレタンは機械的安定性を示すが、ポリエステルやポリエーテル系 macrodiols を使用している場合は特に生物学的環境の低下に敏感であります。したがって、機械的特性に優れた柔軟性、加水分解や酸化安定性を組み合わせることで取り組みにポリウレタン、ウレタン-ウレア、ソフト セグメントとしての水酸基やアミノ-汎 PDMS 定款に集中しているとpolyureas27。異なるポリエーテル系 macrodiols が PDMS30,31 と一緒に組み込まれている非常に無極性 PDMS ソフト セグメントと極ウレタンまたは尿素ハード セグメントの互換性を強化して機械的性質を改善するには、 ,32。特に、Thilak ・ グナティラカ グループが体系的に改善された biostability との長期的な開発と応用や人工ペース メーカーの断熱材など機械的性質によるポリウレタンのシリコーンの開発を検討します。心臓弁33。彼らは水酸基 PDMS 異なるポリエーテルと脂肪族ポリカーボネート ジオールを構成する混合のソフト セグメントを持つ芳香族ポリウレタンを合成しました。すべての合成ポリウレタンへ酸化物 (PHMO) と PDMS 展示の組み合わせの中では、ハードに関して最高の機械的性質は、互換性30をセグメント化します。その後の研究でさらに PDMS-PHMO 比の影響とシシロキサン ベース チェーン エクステンダー シリコン ポリウレタン34,35,の機械的性質に定款を検討彼ら36. 結果が 80 wt %pdms の 1, 3-bis(4-hydroxybutyl)-tetramethyldisiloxane (BHTD) などの共同チェーン エクステンダーに加えて 20 wt %phmo、macrodiol 構成が良好な機械的性質と柔らかいポリウレタンを生成することを明らかにし、熱可塑性樹脂の加工性。さらに、これらのシリコーン ポリウレタンは、一般的応用ソフト ポリエーテル ウレタン37,38,39に比べて強化された biostability を展示します。
生体適合性および同じような材料とその使用心血管用の安定性はまた報告された40,41,42をされています。これらの結果に基づいて、シリコーン系ポリウレア エラストマー (Psu) チェーンのシシロキサン ベースのエクステンダーと考えられている高い柔軟性と、柔らかさをもたらすとはいえの適用後の形状を保持するための十分な機械的強度繰り返し強調します。例えば、以前にシリコーンを用いた作製に使用した、デザイン内で荷重を処理する非常にソフトだったのでハーマンズらは実験的ポリウレタン ベース デュアル光は (iol) プロトタイプを構築しました。除核豚目43。
この資料では、親切な眼内レンズとしてアプリケーションの機械的及び光学特性の面で最適化されているソフト シロキサン ベース PSU の合成について説明します。PSU エラストマーの機械的性質は、シロキサンの分子量によって変更できると、同じプロシージャはコーティングのアプリケーションを見つけるとドレッシングを皮膚シロキサン ベース電源ユニットの開発に適用できます。さらに、この手順は、カルビノール PDMS が使用される場合、シロキサン系ポリウレタンまたはポリウレタン尿素エラストマーを準備する使用できます。合成用ジイソシアネート (すなわち、脂肪族または芳香族) の種類によって反応条件 (時間、温度、およびおそらく溶媒組成を含む) を変更する必要があります。4,4-methylenebis(cyclohexylisocyanate) (H12MDI) やイソホロン ジイソシアネートなど脂肪族ジイソシアネートのアプリケーションの反応はジブチルスズ酸などの有機スズ化合物触媒を用いて、高速化、またはdiacetoxytetrabutyl distannoxane。たとえば、ヒドロキシプロピル終了 PDMS、H12MDI 間反応の触媒の存在下で進行します。さらに、反応温度が 50-60 ° c. に増加する必要があります。4,4-methylenebis(phenylisocyanate) (MDI) などの芳香族ジイソシアネートのアプリケーションの反応温度増やす必要があります適度が十分に芳香族ジイソシアネート、通常より反応性よりも求核基脂肪族ジイソシアネートです。カルビノール PDMS の MDI の反応を無水テトラヒドロ フラン(THF 溶媒混合系を使用して昇格できる) ジメチルホルムアミド (DMF) やジメチルアセトアミド (DMAc) 三級アミンとしていくつかの触媒活性を示します。
プロトコル
注意: 使用前に関連するすべての材料安全データ用紙 (MSDS) を参照してください。合成で使用されるいくつかの化学物質は、急性毒性や強い刺激だけでなく、吸入、皮膚や目に展示します。個人保護具 (実験室のコート、保護メガネ、手袋、フルレングス パンツ ・閉鎖つま先の靴) を着用、ヒューム フードの下で可能であれば、またはよく換気された場所で、化学物質を処理してください。ヒューム フードの下ですべての合成を実行します。テトラメチル アンモニウム水酸化五水和物 (TMAH):飲み込んだ場合、TMAH は強力な基盤、急性毒性、肌に接触した時にそれは皮膚や目に重度の化学熱傷を引き起こします。それは空気に敏感で、吸放湿。冷凍および窒素の下で保管してください。その強力なアンモニア臭のためよく換気された場所で TMAH を処理します。APTMDS:APTMDS は空気に敏感で、窒素下で保存する必要があります。それは重度の皮膚熱傷、目の損傷を引き起こします。H12MDI:H12MDI は吸入毒性があり、皮膚と目に炎症を引き起こします。D4:D4は、豊饒を損なうことがあります。THF:THF は有害である吸入に炎症の原因や発がん性がおそらく。クロロホルム (CHCl3):CHCl3は吸入、おそらく発ガン性の有害な豊饒と胎児、その蒸気を可能な損傷を引き起こすことができます眠気を引き起こすかもしれません。
1. 触媒とアミノ基終端ポリシロキサン マクロモノマーの合成
-
テトラメチル アンモニウム 3-アミノプロピル dimethylsilanolate 触媒の合成
注: 触媒は、ホフマンとレア44によって報告されたメソッドによると合成されました。- 前に真空下でドガの APTMDS を使用し、窒素下で保存します。注射器を使用して APTMDS の約 10 g のピペットします。
- 脱 APTMDS ・ 100 mL 三首丸底フラスコに TMAH の 11.88 g (66.0 モル) 8.13 g (33.0 mmol) を追加します。20 mL の thf APTMDS を溶解して大きな楕円形電磁攪拌棒と一緒に TMAH を中断するを追加します。
注意: TMAH は強いアンモニアのようなにおいを持つ吸放湿、腐食性、有毒な物質で、冷蔵庫で密閉保存する必要があります。よく換気された場所で直ちに TMAH の重量を量る保護手袋と扱っている間安全メガネを着用してください。APTMDS は、空気敏感で皮膚の火傷や目の損傷を引き起こします。注射器; を使用して密封された瓶から APTMDS の重量を量る保護手袋と扱っている間安全メガネを着用してください。 - 還流凝縮器と口とコンセントの窒素と熱は 80 ° C までグリセリンまたはシリコーン オイルの熱浴を使用して反応混合物三首丸底フラスコを装備します。2 時間わずかな、連続的な窒素フローと還流下で反応混合物をかき混ぜなさい。
注意: 初期、わずかに濁った懸濁液は 2 時間以内の透明な溶液に変わります。 - 還流凝縮器を外し、蒸留 THF 真空吸引装置を使用しています。シュレンク管を使用して 70 ° C で 5 時間 0.1 mbar の真空下でわずかに黄色の粗製品を乾かします。
注: この手順後粗製品に格納できる 10 ° C で冷蔵庫次の日まで。 - 50 ml の THF の粗製品を再懸濁します。必要に応じて、細断処理する大きな塊へらを使用し、真空吸引装置を使用して懸濁液をフィルタ リングします。製品は白色の粉末のような固体になるまでは、20 mL の THF 部分沈殿物の少なくとも 3 倍を洗います。
- 3 時間室温で 0.1 mbar の真空下で製品を乾燥させます。その後、触媒を窒素下 10 ° C で冷蔵庫で使用するまで保存します。
-
合成Α, ω-bis(3-aminopropyl)-polydimethylsiloxanes
〜 15,500 g·mol-1の分子量と PDMS のメモ: 合成。- ドガ D4使用する前に真空下で APTMDS。注射器を使用して APTMDS の約 1.5 g のピペットします。
- 脱 D4の PTFE コーティング遠心攪拌機と窒素入口と出口が装備されている 100 mL 三首丸底フラスコに APTMDS の 0.9 g (3.6 m モル) 19.5 g (65.7 mmol) を追加します。
- 触媒の ~ 26 mg を追加 (セクション 1.1) から、わずかな、連続的な窒素フロー下 80 ° C で 30 分間反応混合物をかき混ぜます。
注: 加熱浴グリセリンやシリコン オイルは使用できます。 - (内で 2-3 時間)、滴下漏斗を使用して、反応混合物を滴下 45.5 g (153.4 モル) D4を追加し、さらに 24 h 連続窒素フローの下 80 ° C で攪拌します。
注: 反応が一晩に進むことができます。 - 150 ° C に反応混合物を加熱し、触媒を分解する 2 時間のためにそれをかき混ぜます。部屋の温度に冷却する PDMS を許可します。
- 大きな楕円形磁気攪拌棒遠心攪拌機を交換し、2 つのストッパーを三首丸底フラスコを密封します。バルブ アダプターを使用、シュレンク管を使用して繰返し側製品を蒸留する 0.1 mbar の真空下で 150 ° C に PDMS をゆっくりと加熱します。部屋の温度に冷却する PDMS を許可します。
注: 真空蒸留は 4-5 時間で通常発生します。
-
合成 α, ω-bis(3-aminopropyl)-ジメチルビニル-メチル-phenylsiloxane
注: このセクションは 〜 15,500 g·mol-1と 14 mol % メチル フェニル シロキサン; の分子量とポリシロキサンの合成法を説明しますこの手順は、セクション 1.2 で説明する PDMS 合成に匹敵します。- ドガ D4使用する前に真空下で APTMDS。注射器を使用して APTMDS の約 1.5 g のピペットします。場所 D4Ph、私完全に溶かすし、使用する前に製品を均質化する真空チャンバー内で 3-5 h 70 ° C で。
- D44.54 g (15.3 ミリ モル)、14.96 g (27.5 ミリ モル)、私は、PhD4と 0.9 g (3.6 m モル) APTMDS の PTFE コーティング遠心攪拌機と窒素入口と出口が装備されている 100 mL 三首丸底フラスコに追加します。
- (セクション 1.1) から触媒の ~ 26 mg を追加し、連続窒素フローの下 30 分 80 ° C で反応混合物をかき混ぜます。
- (2-3 時間) 以内の滴下漏斗を使用して、反応混合物に滴下 45.5 g (153.4 モル) D4を追加し、さらに 24 h 連続窒素フローの下 80 ° C で攪拌します。
注: 反応が一晩に進むことができます。 - 1.2.5 と 1.2.6 以下の手順で合成を続行します。
2. ポリシロキサンの分子量測定
-
ポリシロキサンの理論分子量
- 理論の分子量を計算する
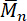 次の式によるとポリシロキサンの。
次の式によるとポリシロキサンの。 (1)
(1)
ここでは、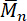 ポリジメチルシロキサンの数平均分子量mが使用されるモノマー D4と APTMDS の質量 (g)、 nはモルの APTMDS の量。
ポリジメチルシロキサンの数平均分子量mが使用されるモノマー D4と APTMDS の質量 (g)、 nはモルの APTMDS の量。
- 理論の分子量を計算する
-
1H NMR 分光法によるポリシロキサンの分子量測定
- CDCl3の 0.5 mL 中にポリシロキサンの 10-20 mg を溶解、その NMR スペクトルを記録し、化学シフト [δ] 7.26 ppm で溶剤の信号を調整します。
- 分子の重量を計算する
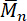 次の式に従って整数値からポリシロキサンの。
次の式に従って整数値からポリシロキサンの。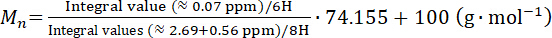 (2)
(2)
-
滴定法によるポリシロキサンの分子量測定
- 250 mL の三角フラスコにポリシロキサンの 1.5-2 g を追加し、電磁攪拌棒を使用して連続的に攪拌下で 50 mL の thf に溶解します。
- 0.1 M HCl の色が青色から黄色に変更されるまで、ブロモフェノール ブルーを使用しての観察によるアミノ基を滴定しなさい。数平均分子量を計算する 3 つのサンプルとの滴定を繰り返します。
3. ポリシロキサン尿素エラストマーの合成
注: このセクションは PDMS による尿素エラストマー 10 w % ハード セグメント内容 (HS %) の合成手順を説明します。(PDMS: 15,500 g·mol-1)。
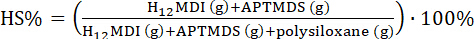 (3)
(3)
- 2.939 g (11.2 ミリ モル) H12MDI、目標到達プロセスと窒素の入口と出口をドロップ、PTFE コーティング遠心攪拌が装備されている 250 mL の 4 首丸底反応フラスコを追加し、20 mL の thf に溶解します。
注意: H12MDI は低揮発性ジイソシアネートと皮膚と目に炎症を引き起こします。保護手袋、保護メガネを着用します。
注: また、H1250 mL ビーカーに THF で MDI を溶解、反応フラスコに漏斗、チューリップ ガラス溶液を追加します。ビーカーを洗いし、10 ml の THF の漏斗します。- 100 mL の thf; に脱 PDMS 45.0 g (2.9 mmol) の解散します。室温で連続的に攪拌し窒素フロー下滴下漏斗を使用して H12MDI 溶液に滴下このソリューションを追加します。ビーカーと 50 ml の THF の目標到達プロセスの削除をすすいで、このソリューションを反応混合物に追加します。
- プレポリマーによる赤外分光法の形成を制御します。
注: 反応の進行は、2 つの方法で監視できる: インラインまたはオフラインの ATR FTIR 分光法を使用しています。- インライン ATR FTIR 分光用インライン ATR-FTIR プローブ、分光計に接続されているを反応の開始時に中央のジョイントに挿入します。PTFE 被覆の攪拌ではなく大きな楕円形電磁攪拌棒を使用します。H12MDI 溶液のスペクトルを記録を開始し、イソシアネートの変換に従う 2266 cm-1に下士官吸収ピークを選択します。
- オフライン ATR ftir、パスツール ピペットを使用して反応混合物のサンプルを取るし、ATR 結晶を数滴を追加します。ATR 結晶表面に薄膜が残っているまでの窒素フロー下で溶媒を蒸発させます。(PDMS の完全な付加の後でおよび APTMDS の各部分の付加の後で) 異なる反応段階で記録のスペクトル。
- プレポリマー溶液に鎖エクステンダー APTMDS 化学量論量の部分を追加します。
注: チェーン エクステンダーの追加 (手順 3.1.3.1 と 3.1.3.2 参照) 2 つの方法で進むことができます。- 5-10 mL の thf に鎖エクステンダーの重量を量られた量を溶解し、滴下反応混合物は、パスツール ピペットを使用してまたは 3 mL の thf で洗浄再度続いて滴下漏斗を使用してソリューションを追加します。
- 注射器に鎖エクステンダーの部分、反応混合物を滴下チェーン エクステンダーを追加します。この場合、シールのゴム中隔のストッパーを使用して 4 番目の接合箇所。
- プレポリマーに APTMDS の計算された量の 80% に対応する APTMDS の 1.65 g (6.6 m モル) を追加します。赤外分光法による反応の進行状況を制御します。
- (計算量の合計の 90%) の APTMDS の 0.21 g (0.8 mmol) を反応混合物に追加し、FTIR による反応の進行を制御します。
- 0.1 g (0.4 モル) APTMDS の (の合計の 95%) を追加します。反応混合物、調節反応に FTIR を用いた進行。
- 最後に、反応混合物に鎖エクステンダー (0.102 g、0.41 mmol) の最後の部分を追加し、FTIR スペクトルの下士官吸収帯の消失を確認します。
注: チェーン エクステンダーの最初の部分の付加の後で粘度の増加が示されています。
- PSU ソリューションを PTFE の箔で覆われたガラス シャーレに注ぎ、一晩ヒューム フードの下で溶剤を蒸発します。さらに、80 ° C、12 時間で真空チャンバー内で PSU を乾燥させます。
4. 機械のテスト手順
-
ポリシロキサン尿素エラストマー膜の作製
- CHCl3 300 mL 三角フラスコでの 200-250 ml の PSU 小片の 7-8 g を溶解、緩くガラス ストッパーを使用してフラスコを密封し、少なくとも 24 時間電磁攪拌棒を使用して混合物をかき混ぜます。必要に応じて、溶媒の追加部分を追加します。
注意: クロロホルムはおそらく発がん性があります。蒸気は、吸入時に眠気を引き起こす可能性があります。よく換気された場所でクロロホルムを処理します。 - ガラス シャーレに均一溶液を追加し、多孔アルミ箔でカバーします。やヒューム フード サッシ窓を開けてよく換気された場所にペトリ皿を配置するかゆっくりと蒸発する溶剤を許可します。
注: ヒューム フードにペトリ皿を置くこと、可能であれば空気の流れを減らします。溶媒の非常に急速な蒸発は、不均一性と透明の膜内の不透明な汚れの形成に します。 - 80 ° c 12 h 真空チャンバー内でフィルムを乾燥させます。
- 慎重に小さな薄いヘラを使用してガラス表面から映画を削除し、ストアの力学特性評価のための後の使用時に透明封筒内で PSU フィルム。
- CHCl3 300 mL 三角フラスコでの 200-250 ml の PSU 小片の 7-8 g を溶解、緩くガラス ストッパーを使用してフラスコを密封し、少なくとも 24 時間電磁攪拌棒を使用して混合物をかき混ぜます。必要に応じて、溶媒の追加部分を追加します。
-
応力-ひずみ試験ポリシロキサン尿素エラストマー フィルム
- エームズ45 (型 S2) によると PSU 膜からダイカット犬状骨標本を作製します。図 4に示すように、図形を持つパンチング ナイフ ユニット下の封筒箔で覆われている PSU の映画を配置します。レバーを押して、試験片をパンチを周囲温度 (23 ± 2 ° C) で、少なくとも 72 時間保存します。
- 引張試験機とコンピューターに切り替えます。アイコンをクリックして、ソフトウェアを起動します。引張試験と方法を選択し、テスト マシンで正しいロードセル (100 N) がインストールされているかどうかはチェックしてください。
- メソッド アシスタントを選択し、設定が正しい場合は、すべてのテストを確認します。事前テストに移動し、次の設定がアクティブ化されるかどうかを確認してください: 20 mm、0.1 MPa 時の予圧、予圧が 5 mm/分に達するまでの速度で元の試料の長さ (L0)。
- パラメーターをテストするのには移動し、次の設定がアクティブ化されるかどうかをチェック: 速度 1 mm/分、速度 25 mm/分、80 %f最大でサンプル ブレークの検出でサンプル改までのヤング率の定量、回帰, 2% ひずみ時のヤング係数測定の最初と 6% ひずみ時のヤング係数測定の最後のヤング率の定量。法助をまま、ソフトウェアのメイン ウィンドウへ切り替えます。
- テスト コンピューター上の電源ボタンを押して、ボタン開始位置へソフトウェアのメイン ウィンドウでをクリックします。
- 保護箔を削除し、任意の内部応力を除外するクロス偏光下でサンプルを検査します。試料の厚さと口径を使用してサンプル幅を測定します。その後、ソフトウェアのメイン ウィンドウ内の対応するフィールドにサンプル厚さおよび幅の値を挿入します。
- 試験機の上部クランプ間試験片を修正します。ソフトウェアのメイン ウィンドウでボタンゼロの力をクリックします。試験機の顎をクランプ下部間試験片の下端を修正します。
注: 場合は、クランプの表面は滑りやすい、細粒紙やすり試料の測定時に滑りを防ぐために、試料の両端を配置します。 - 引張試験を開始する測定を開始ボタンをクリックします。
- 測定が終わったら、4.2.6 と 4.2.7 の手順に進みます。修正後上部クランプとゼロの力を選択する試験片をボタン開始位置へソフトウェアのメイン ウィンドウで選択します。クランプの顎下の試験片の下端を修正し、再度計測を開始] をクリックします。
- 4.2.6 - 1 電源ユニットについてはサンプルの 3 x 少なくともヤング弾性率、引張強さ、伸びの統計的評価休憩 4.2.8 の手順を繰り返します。
-
PSU エラストマー膜のヒステリシス試験
- 引張試験機とコンピューターに切り替えます。アイコンをクリックして、ソフトウェアを起動します。繰返し引張試験としてメソッドを選択し、試験機の正しい負荷セル (100 N) のインストールを確認します。
- メソッド アシスタントを選択し、設定が正しい場合は、すべてのテストを確認します。事前テストに移動し、次の設定が有効かどうかを確認してください: 20 mm、0.05 MPa 時の予圧、予圧が 5 mm/分に達するまでの速度で元の試料の長さ (L0)。
- パラメーターをテストするのには移動し、次の設定の活性化をチェック: 10 0% ひずみと 25 mm/分の速度で荷降ろし setpoint 100% ひずみ時の読み込み setpoint でサイクル数を残す方法アシスタントとソフトウェアのメイン ウィンドウに切り替えます。
- 4.2.8 4.2.5 - の手順に進みます。
- 統計的評価の 2 つの標本とヒステリシス測定を繰り返します。各サイクルで次の式に従って機械的ヒステリシスを計算します。
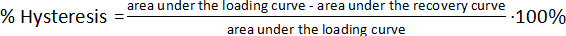 (4)
(4)
5. 栽培手順 HaCaT 細胞
- HaCaT 細胞と cryotube を暖める、ダルベッコ修飾イーグル培地 (DMEM) 37 ° C の水浴中。微生物学的安全ワークベンチの下で急速に細胞懸濁液を温かい DMEM で満ちている 10 mL の円錐形遠心管に転送します。
- 845 x gで 6 分間の遠心分離の細胞懸濁液を対象します。使い捨てガラス パスツール ピペット、真空ポンプに接続されているを使用して上清の大半を破棄し、残りの液体でエッペン ピペットを使って細胞塊を軽くピペッティングにより細胞ペレットを再懸濁します。
- 25 cm2細胞培養用フラスコに再懸濁のセルを転送し、DMEM は、10% を添加した 9 mL を加える FBS。37 ± 1 ° C および 5% CO2キャビネット インキュベーター内で細胞を孵化させなさい。毎日倒立顕微鏡を用いた細胞増殖を制御します。各 3 日目のセルが 10mj/cm ^2 になるまで、DMEM を変更します。
- 使い捨てガラス パスツール ピペットを使用して DMEM を外して安全ワークベンチの下セル一節を実行します。10 mL の細胞層を洗浄する PBS バッファーを追加します。もう一度使い捨てガラス パスツール ピペットを使用して PBS バッファーを削除します。
- 25 cm2細胞培養用フラスコ細胞をデタッチし、キャビネットの CO2インキュベーターで孵化させなさいそれらに/トリプシン EDTA 溶液 1 mL を追加します。細胞懸濁液、倒立顕微鏡を使用して存在しているかどうかを確認します。
- トリプシンを不活化する細胞培養用フラスコに DMEM の 3 mL を追加します。細胞懸濁液を遠心管に転送 845 x gで 6 分間の遠心分離のセルを対象とします。ガラス パスツール ピペットを使用して、上清の大半を削除します。残り DMEM に細胞を再懸濁します、10% を添加した新鮮なの暖かい DMEM の 10 mL を追加し政府短期証券。
- 75 cm2細胞培養フラスコのそれぞれに細胞懸濁液 5 mL を転送し、15 mL の 10% と新鮮な暖かい DMEM を追加 FBS。セルが 10mj/cm ^2 になるまで 37 ± 1 ° C および 5% CO2キャビネットの CO2インキュベーター内で細胞を養います。
- 5.1.3 - 今回は 5.1.6 の手順に従ってセル通過を繰り返し、DMEM の 6 mL のトリプシン/EDTA 溶液 2 mL を使用してトリプシンを不活化します。
6. HaCaT 細胞を用いた MTS 細胞生存率測定の手順
注:生体外の細胞毒性試験は、Wenzelewski46, 細胞培地抽出液を用いたに従って行われました。PSU のサンプルとバイオメディカル グレード ウレタンのサンプルは、酸化エチレンを使用して滅菌されました。
- 37 ± 1 ° C および 5% CO2の 10% と補われる DMEM で HaCaT 細胞の培養 75 cm2細胞培養用フラスコの FBS。生体外の細胞毒性試験の少なくとも 4 通過後セルを使用します。
- 50 mL コニカル遠沈管に PSU の参考資料 (0.7 g) 滅菌サンプルを追加し、72 ± 0.1 g/mL の抽出率で CO2を 37 ° C、5% で 2 h の FBS、なし、DMEM にサンプルを抽出します。電源ユニットの各サンプルに対して 3 つのエキスを使用します。50 mL コニカル遠沈管に DMEM、FBS、なしを記入ブラインド サンプルを準備し、同じ抽出を実行します。
- 抽出プロシージャの 2 日目、5.1.3 - 2 ml のトリプシン/EDTA、DMEM 6 mL 5.1.5 の手順に従って細胞の剥離を実行します。細胞懸濁液の分注 100 μ L を取る、DMEM の 100 μ L を追加します。この希薄懸濁液から因数の 20 μ L を取るし、死んだ細胞を染色する 0.5% トリパン ブルー溶液 10 μ L を追加します。
- 2 分塗り細胞にピペットを使用して検定をインキュベートし、すぐに 4 本のチャンバー内のセルをカウントします。割合で細胞の生存率を評価して実行可能な細胞数を計算します。
注: 別の方法として、セル数えることができるセルのカウント システムを使用しています。 - シード HaCaT 細胞/ウェルの 96 ウェル マイクロ プレートに DMEM を 200 μ l 添加 20 x 103の濃度で細胞の (第 4 道) と 37 ° C、5% CO2で 24 時間細胞をインキュベートします。
- 抽出後 3 日、追加 10% エキスとブラインドのそれぞれに FBS サンプルし、サンプルを暖かい水のお風呂を使用して 37 ° C まで。まあシードそれぞれから、DMEM を削除し、抽出物、ブラインド サンプル、および対応する正と負のコントロールによってメディアを置き換えます。各電源ユニット (PSU の各サンプルに対して 3 つのエキスを使用) を抽出し、六つの井戸にエキス 200 μ L をピペットします。
- ブラインド サンプルの 200 μ L をピペット (DMEM + 10 %fbs) 六つの井戸に。10% の新鮮な DMEM の 200 μ L をピペット 6 井戸に FB (マイナス コントロール)。肯定的な制御の 200 μ L をピペット (DMEM + 10 %fbs + 1 %sds) 六つの井戸に。エキスと 37 ° C、5% CO2で 24 時間コントロールでセルを孵化させなさい。
注: 肯定的な制御の準備のため水で 20 %sds の溶液を準備し、DMEM 1:2 でそれを希釈します。その後、さらにそれを希釈 DMEM 1 %sds の溶液を調製します。 - 日 4、インキュベーション時間の終了直前に、(各ウェル、MTS ソリューションの使用 20 μ L + DMEM の 100 μ L) の MTS と FBS なし DMEM のストック溶液を準備します。インキュベーション時間後抽出物、盲目のソリューション、およびコントロールを削除し、セルの背景を特定することがなく六つの井戸と同様、各ウェルに MTS 原液の 120 μ L をピペットします。37 ° C、5% CO2で 4 時間細胞を孵化させなさい。
- 492 で各ウェルの吸光度を測定日 4 MTS ソリューションのインキュベーション後、nm、マイクロ プレート リーダーを使用しています。シードの井戸のバック グラウンドの測定した吸光度を減算します。肯定的な制御から測定した吸光度値 0% 増殖を表し、これらの吸光度の値を 0 に設定すると仮定します。否定的な制御から測定した吸光度値が 100% 増殖を表すし、これらの値を 100 に設定と仮定します。
- ネガティブ コントロール (100% 増殖) と肯定的な制御 (0% 増殖) の吸光度値の割合として吸光度値から細胞増殖を計算します。最大 81% ない細胞としての細胞増殖を示すサンプル抽出を評価します。
注: サプライヤーの情報47, によると、後の吸光度を測定します。反応を停止して加湿チャンバーに室温で光から保護された 18 h までのマイクロ プレートを格納を各ウェルに 10 %sds 溶液の 25 μ L をピペットします。
結果
4 D と D4Ph、私endblocker APTMDS のリング チェーン平衡と得られたアミノプロピル終了 polydimethylsiloxanes ジメチルビニル-メチル-フェニル-シロキサンの共重合体、それぞれ、作製されました。分子量 3,000 と 33,000 g·mol-1 D4と APTMDS (図 6) のモノマーの比率を調整することによって。分子量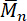 1H-NMR スペクトル (図 5) と決定された準備の PDMS の滴定から取得した値に類似していた。これらの値は最大 15,000 g·mol-1の計算の理論分子量と一致していた。高分子量の PDMS の準備時に得られた分子量若干大きかった理論的計算で推定しました。ペンダント フェニル グループ D4私は、Phと環状シロキサンの共重合はわずかに増加するポリシロキサンの屈折のために成功とみなされました。(37 ° C でアッベ屈折計を使用して決定される) 屈折 1.401 (非修飾 PDMS) から 1.4356 (14 mol % メチル-フェニル-シロキサン) に増加した (図 7)。PSU のエラストマーを準備 - アミノプロピル PDMS、脂肪族ジイソシアネート H12MDI、溶媒として THF を使用して APTMDS を使用して 2 つのステップで合成しました。このメソッドは、(ジイソシアネート + 尿素) ハード セグメントとソフト セグメント (PDMS) のセグメント化された構造をもつ高分子量の Psu の建設を許可しました。インライン赤外分光法は、PDMS や連鎖延長剤 APTMDS (図 3および図 8) からアミノ基とイソシアネートの非常に急速な反応を確認しました。いくつかの時間がかかる、ポリウレタン エラストマーの準備とは違って PSU エラストマーの準備は便利でした。透明性と PSU エラストマーの機械的性質は、ポリジメチルシロキサンの分子量に依存していた。透明な PSU エラストマー フィルム展示の透過率 > 90 %18,000 g·mol-1のポリジメチルシロキサンの分子量まで。高いポリジメチルシロキサンの分子量、PSU 膜なったますます不透明 (図 9)。ポリジメチルシロキサンの分子量の増加に伴い、ソフトの PSU エラストマーを準備でした。PSU エラストマーのヤング ~5.5 PDMS 分子の重量 3,000 g·mol-1) (MPa から 0.6 MPa (≥26、000 g·mol-1の PDMS 分子量) に減少した (図 10)。さらに、繰り返し応力下の機械的安定性を評価に使用している機械的ヒステリシスは、彼らの高分子量の PDMS 調製時 PSU エラストマーの減少しました。100% ひずみ時の最初のサイクルのヒステリシス値が 6% (PDMS 分子量 33,000 の g·mol-1) の (PDMS 分子の重量 3,000 g·mol-1) と 54% から低下した (図 11)。応用合成法許可 HaCaT 細胞 (図 12) いくつかの選択した PSU のエラストマーのエキスで細胞生存率検査の例として細胞傷害性残差を解放しないでください PSU エラストマーの準備です。
1H-NMR スペクトル (図 5) と決定された準備の PDMS の滴定から取得した値に類似していた。これらの値は最大 15,000 g·mol-1の計算の理論分子量と一致していた。高分子量の PDMS の準備時に得られた分子量若干大きかった理論的計算で推定しました。ペンダント フェニル グループ D4私は、Phと環状シロキサンの共重合はわずかに増加するポリシロキサンの屈折のために成功とみなされました。(37 ° C でアッベ屈折計を使用して決定される) 屈折 1.401 (非修飾 PDMS) から 1.4356 (14 mol % メチル-フェニル-シロキサン) に増加した (図 7)。PSU のエラストマーを準備 - アミノプロピル PDMS、脂肪族ジイソシアネート H12MDI、溶媒として THF を使用して APTMDS を使用して 2 つのステップで合成しました。このメソッドは、(ジイソシアネート + 尿素) ハード セグメントとソフト セグメント (PDMS) のセグメント化された構造をもつ高分子量の Psu の建設を許可しました。インライン赤外分光法は、PDMS や連鎖延長剤 APTMDS (図 3および図 8) からアミノ基とイソシアネートの非常に急速な反応を確認しました。いくつかの時間がかかる、ポリウレタン エラストマーの準備とは違って PSU エラストマーの準備は便利でした。透明性と PSU エラストマーの機械的性質は、ポリジメチルシロキサンの分子量に依存していた。透明な PSU エラストマー フィルム展示の透過率 > 90 %18,000 g·mol-1のポリジメチルシロキサンの分子量まで。高いポリジメチルシロキサンの分子量、PSU 膜なったますます不透明 (図 9)。ポリジメチルシロキサンの分子量の増加に伴い、ソフトの PSU エラストマーを準備でした。PSU エラストマーのヤング ~5.5 PDMS 分子の重量 3,000 g·mol-1) (MPa から 0.6 MPa (≥26、000 g·mol-1の PDMS 分子量) に減少した (図 10)。さらに、繰り返し応力下の機械的安定性を評価に使用している機械的ヒステリシスは、彼らの高分子量の PDMS 調製時 PSU エラストマーの減少しました。100% ひずみ時の最初のサイクルのヒステリシス値が 6% (PDMS 分子量 33,000 の g·mol-1) の (PDMS 分子の重量 3,000 g·mol-1) と 54% から低下した (図 11)。応用合成法許可 HaCaT 細胞 (図 12) いくつかの選択した PSU のエラストマーのエキスで細胞生存率検査の例として細胞傷害性残差を解放しないでください PSU エラストマーの準備です。
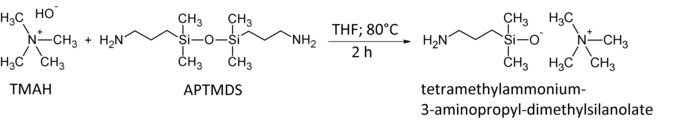
図 1: テトラメチル アンモニウム 3-アミノプロピル dimethylsilanolate 触媒の合成。
テトラメチル アンモニウム水酸化五水和物 (TMAH) と 1, 3-Bis(3-aminopropyl)-tetramethyldisiloxane (APTMDS) は 80 ° C の thf 中で 2 h を反応されました。THF で粗製品を洗浄後白色固体として触媒テトラメチル アンモニウム-3-アミノプロピル-dimethylsilanolate を受けた。この図の拡大版を表示するのにはここをクリックしてください。
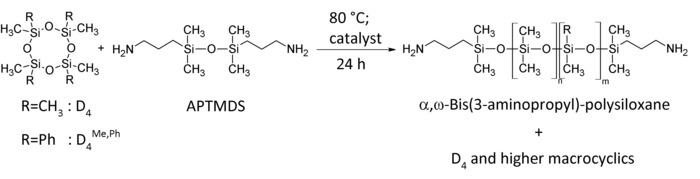
図 2: アミノプロピル終了 polydimethylsiloxanes (PDMS) とジメチルビニル-メチル-フェニル-シロキサンの共重合体の合成ルート。私、Ph環状モノマー D4/D4は、テトラメチル アンモニウム 3-アミノプロピル dimethylsilanolate 触媒を用いた 24 時間 80 ° c シシロキサン endblocker APTMDS を使用して平衡です。この図は、Riehleらから変更されています。48.この図の拡大版を表示するのにはここをクリックしてください。
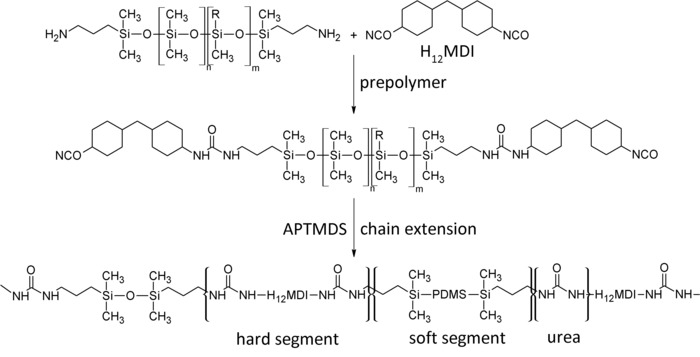
図 3: セグメント化されたポリシロキサンを用いた尿素エラストマー (PSU) の 2 段階合成。最初のステップでアクティブなイソシアネートを含むプレポリマーが H12MDI アミノプロピル終了ポリシロキサンと反応後形成される (R = CH3: PDMS;R = Ph;共重合体)。2 番目の手順では、ポリマーの分子量が増加を介してチェーン エクステンダー APTMDS で残りのアクティブなイソシアネート基の反応です。結果のエラストマーは、尿素のハード セグメントとソフト セグメントのシリコーンを含むセグメント化されたポリマーです。この図は、Riehleらから変更されています。48.この図の拡大版を表示するのにはここをクリックしてください。
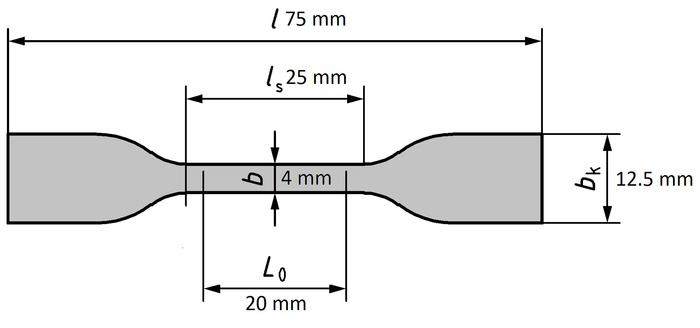
図 4: 応力-ひずみテスト用犬骨形試験体の仕様。この図は、エームズ45から変更されています。この図の拡大版を表示するのにはここをクリックしてください。
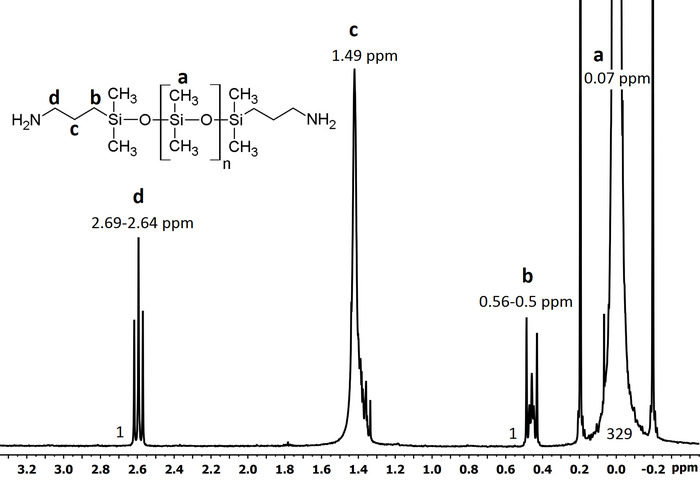
図 5:1 1H NMR スペクトル アミノプロピル終了ポリジメチルシロキサンの。分子量計算、メチレン プロトン d の整数値 (δ 2.69 ppm) と b (δ 0.56 ppm) およびメチル プロトン、(δ 〜 0.07 ppm) 利用されました。HDO ピーク49、溶剤 CDCl3; 水跡のプロトン交換に対応するによってピーク c (δ ~1.5 ppm) をオーバーレイします。したがって、このピークは分子量の計算には使用されません。このスペクトルのポリジメチルシロキサンの分子量は 〜 16,365 g·mol-1です。この図の拡大版を表示するのにはここをクリックしてください。
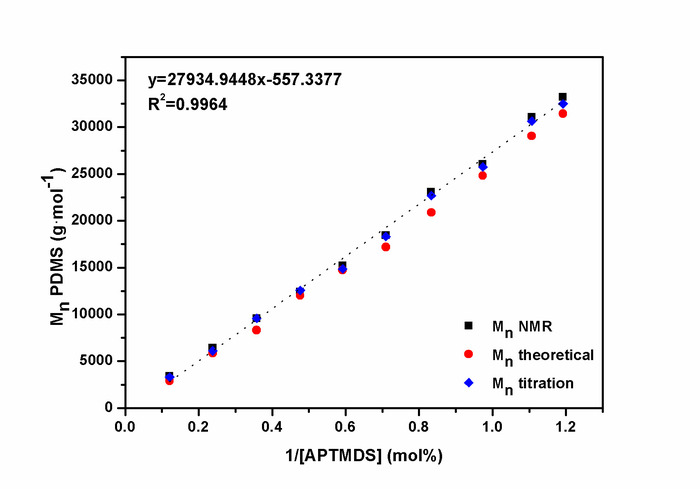
図 6: 線形相関分子量 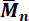 アミノプロピル終了の polydimethylsiloxanes と endblocker の濃度の。
アミノプロピル終了の polydimethylsiloxanes と endblocker の濃度の。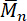 1H NMR 分光決定を介して、アミノ末端の滴定および式 (1) によると理論計算値であった。この図は、Riehleらから許可を得て転載します。48.この図の拡大版を表示するのにはここをクリックしてください。
1H NMR 分光決定を介して、アミノ末端の滴定および式 (1) によると理論計算値であった。この図は、Riehleらから許可を得て転載します。48.この図の拡大版を表示するのにはここをクリックしてください。
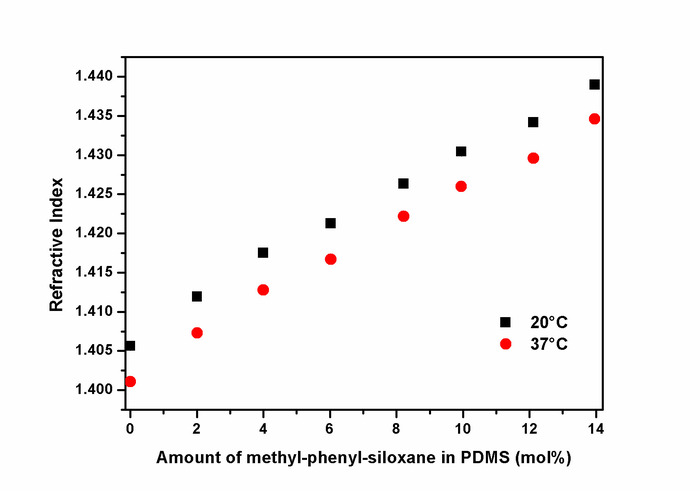
図 7: アミノプロピル終了ジメチルビニル-メチル-フェニル-シロキサンの共重合体の屈折します。ジメチルビニル-メチル-フェニル-シロキサンの共重合体の屈折率 (RI) は、20 ° C (黒い正方形)、37 ° C (赤丸) アッベ屈折計を使用して測定しました。組み込まれたメチル-フェニル-シロキサン単位の量の直線的増加 RI 値。0 mol % で RI 値を表す分子量、ジメチルビニル-メチル-フェニル-シロキサンの共重合体に匹敵する非修飾 PDMS から。1.4346 (37 ° C) の最適な RI 14 mol % メチル-フェニル-シロキサンの共重合体が得られました。この図は、Riehleらの許可を得て転載されています48.この図の拡大版を表示するのにはここをクリックしてください。
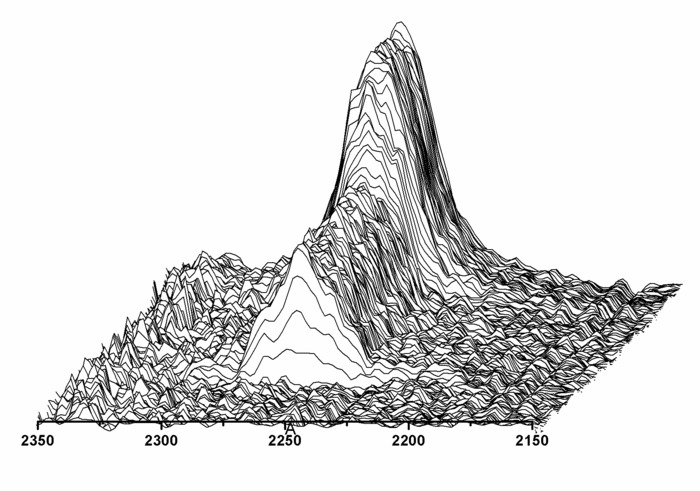
図 8: ポリジメチルシロキサン尿素 (PSU) の合成中にイソシアネート変換します。この図は、2,266 cm1の PSU の合成時にインライン赤外分光によって後で下士官吸収帯の時間依存プロットを示します。アミノプロピル終了ポリジメチルシロキサンの付加の後で下士官バンドの高さの減少、下士官終わるプレポリマー鎖の形成を示す。チェーン エクステンダー APTMDS の付加の後で下士官のバンドは完全に IR スペクトルから姿を消した。この図は、Riehleらの許可を得て転載されています50この図の拡大版を表示するにはここをクリックしてください。 。
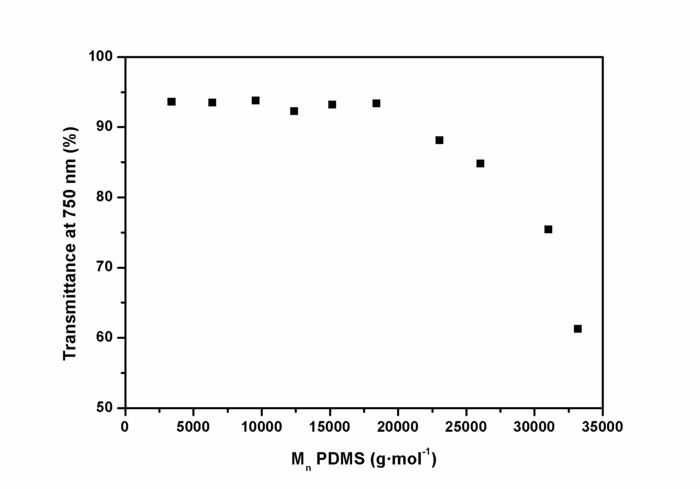
図 9: PSU エラストマーの透過率の依存性膜 750 nm 及びポリジメチルシロキサンの分子量。PSU 膜の透過率は可視・紫外分光法によって定められました。750 で Psu の透過率 nm (可視スペクトルの上部の端) は > 90% の Psu は PDMS を用いて分子量 3,000 および 18,000 g·mol-1の間まで合成した場合。増加の PDMS の分子重量と映画の不透明度が増加しました。この図は、Riehleらの許可を得て転載されています48.この図の拡大版を表示するのにはここをクリックしてください。
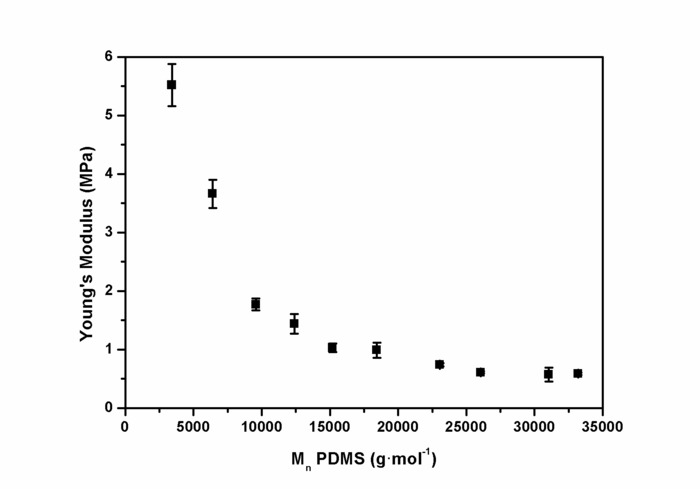
図 10: ポリジメチルシロキサンの分子量の関数として PSU のエラストマーのヤング率。ヤング率 (YM) は、PSU 膜の応力-ひずみ測定から決定しました。値は、5 つの繰り返しの測定から得られた平均値として表されます。誤差範囲は、標準偏差を表します。YM の最も高い減少した PDMS 3,000 から 9,000 g·mol-1に至るまでから合成した Psu のため。PDMS 分子量 12,000 および 18,000 g·mol-1の間で YM 値は 1.5 MPa と 1.0 MPa の間だった。26,000 g·mol-1より大きい分子量、YM 値 ~0.6 MPa でした。この図は、Riehleらの許可を得て転載されています48.この図の拡大版を表示するのにはここをクリックしてください。
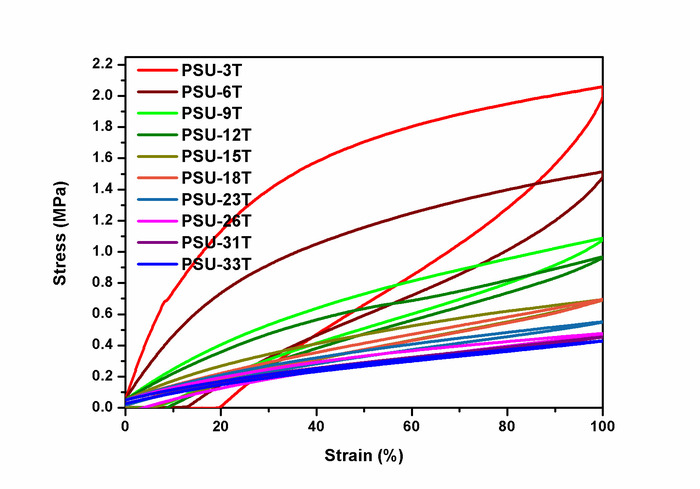
PSU エラストマーの図 11: 100% ヒステリシス曲線。伸び率 100% 時の PSU のエラストマーの最初サイクル ヒステリシス曲線が表示されます。高分子表記と PDMS 分子の重量は、(例えば、電源ユニット 3 t は分子量 3,000 g·mol-1の PDMS から調製したポリ尿素エラストマー)。最高の機械的ヒステリシス (43%-54%)顕著なヒステリシス曲線によって示されるように、低分子ポリジメチルシロキサンから合成した PSU エラストマーで観察されました。ヒステリシスは 14% (15,000 g·mol-1) から 6% (33,000 g·mol-1) にポリジメチルシロキサンの分子量の増加に伴い減少しました。この図は、Riehleらの許可を得て転載されています48.この図の拡大版を表示するのにはここをクリックしてください。
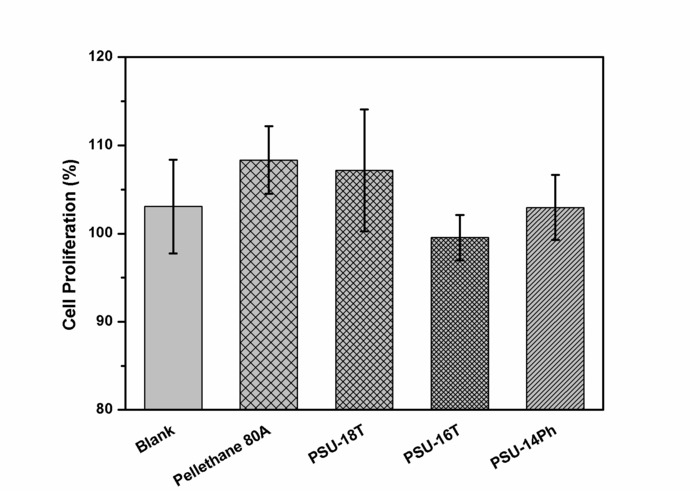
図 12: HaCaT 細胞の in vitro細胞毒性試験の結果は PSU の抽出物と扱われる。この図は、PSU エラストマー セル培地抽出液による HaCaT 細胞の細胞増殖を示しています。値は、サンプル、各エキス (合計 18 レプリケートします) の六つの繰り返された測定ごとの 3 つのテスト エキスから得られた平均値として表されます。誤差範囲は、これらの測定値から標準偏差を表しています。空白は、細胞培地抽出に使用された細胞の培地に類似して治療した DMEM (サンプル)、なしを表します。医療グレード ポリエーテル ウレタンは、参考資料として選ばれました。ポリウレアのシリコーン系エラストマー (PSU 18T、PSU-16T と PSU 14Ph) 電源ユニット 14Ph に基づいていたに対し、分子量 18,000 と 16,000 g·mol-1 (PSU 18T と PSU 16T) PDMS に基づいていた、代表的なテスト サンプルとして選ばれた、ジメチルビニル-メチル-フェニル-シロキサンの共重合体メチル-フェニル-シロキサンの 14 の mol % と 〜 16,600 g·mol-1の分子量。HaCaT 細胞、PSU エラストマーと参照ポリウレタンの抽出物の平均拡散だった 100% と高い。したがって、PSU エラストマー参照ポリウレタンのエキスは細胞毒性ではありません。この図の拡大版を表示するのにはここをクリックしてください。
ディスカッション
高分子量のアミノプロピル終了 PDMSを介してリング チェーンの平衡を無水、使用を達成するためには、強塩基性触媒が重要です。水酸化カリウム (KOH) や水酸化テトラメチル アンモニウム (TMAH) など、他の一般的に適用される触媒側反応を促進する水の残基を含むしたがって、44二、光、および同じような分子量が機能しない PDMS 鎖の混合物が得られます。さらに、TMAH を使用している場合、反応が必要です。 > 完了し、48 h は常にではない完全なモノマー消費44を続行します。
特に、計量、endblocker APTMDS は、PDMS の所望の分子量を取得する重要です。たとえば、APTMDS の 0.9 g の代わりにプロトコルのセクション 2.1 で説明されているように、PDMS を合成に 0.85 g を使用する場合これにつながる理論分子量約 > 900 g·mol-1。さらに、理論分子量、変換によって異なります。環状側製品はかなり削除された経由で減圧蒸留ではない場合は、高変換値が取得されます。たとえば、同じ合成手順 (プロトコルのセクション 2.1) のように、使用する 90% の計算された変換につながる理論的に計算される分子量;85% の変換が推定される場合、この値は 910 g·mol-1よりも大きいです。滴定法によるポリシロキサンの分子量測定の誤差は、滴定の 50 mL ビュレットを使用する場合に特に可能性、フラスコに PDMS の重さに関連しています。ポリシロキサンの 0.06 g の重さに関連する偏差は、〜 650 g·mol-1の計算違いにつながる可能性があります。したがって、半自動滴定装置の使用をお勧めします。
PDMS の屈折率フェニル グループ17,51の定款によって増加することができます, ハロゲン化フェニル グループ52硫黄を含むグループ53。Yilgör、さざ波、マグラス54のとおり PDMSを介してoctaphenylcyclotetrasiloxane (D4Ph) との共重合にフェニル基を組み込む試みは応用の反応条件下で成功しなかったおそらくかさばるリング バックボーン選択反応温度でシロキサン結合を分割する応用の触媒の不可能となったため。島が 160 ° C の反応温度で使用される場合、D4Phリングを開くことができます。しかし、おそらく機能しない不純物の多量を含んでいる非常に高分子量のポリシロキサンが得られます。さらに、これらの共重合体の触媒コの取り外しは簡単ではないと触媒水溶液抽出に続いて、エタノールの HCl を使用して中和手順が必要です。その後、PDMS は PDMS を含む有機相から水相を分離する CH2Cl2などの有機溶媒に溶解します。最後に、有機相は MgSO4、続いてろ過と54回転蒸発器を用いて真空蒸留で乾燥する必要があります。対照的に、本稿で紹介した方法によりする触媒熱分解を介してすぐに削除します。したがって、固体モノマー D4Phを使用する代わりにフェニル基が正常に導入される PDMS のバックボーンに液体モノマー D4Ph、私共重合による29Si 核磁気共鳴による確認分光50。
合成の PSU エラストマー展示 0.6 - YM 5.5 MPa ・最大 1,000% の伸び値を持つ高弾性。このような高い伸び値 PSU エラストマーの高分子量にも高分子を分割するだけでなく関連していた (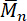 > 100,000 g·mol-1)48。アミノ基と急速に分子量の増加につながる、室温で脂肪族 isocyanyate グループ間に瞬時の反応が発生します。この結果さらに支えられ、溶媒中で反応を行う反応速度を大幅に遅く粘度のわずかな増加は表示されませんでしたのでほぼバランスの分子量を劇的に影響するだろうそれ以外の場合化学量論比。対照的に、チェーンの延長として 1, 4-ブタンジ オールなどの短鎖ジオールを使用すると、結果ウレタン-ウレア エラストマーが少ない弾性のみならず失われたかなりの機械的安定性高分子量の PDMS だった場合は特に合成に使用されます。この結果 (結果は公開されていません)、エラストマーのかなり低分子量に関連していたおそらく重の最後の段階ですべてのイソシアネートの不完全な変換に対応します。さらに、脂肪族ジイソシアネートに向かってアミノ基とヒドロキシル グループの反応性の違いは、生体外の細胞毒性試験から得られた結果を大幅に影響。アミノ鎖エクステンダー APTMDS から調製した PSU エラストマーの抽出 (図 12)、細胞に細胞毒素の効果は展示していません。ただし、シロキサン ベース ウレタン-ウレア エラストマーの抽出物を使用した場合細胞生存率は大幅に削減 (公開されていません)、結果、おそらく低分子量の浸出物と残留未反応イソシアネートに関連していた。
> 100,000 g·mol-1)48。アミノ基と急速に分子量の増加につながる、室温で脂肪族 isocyanyate グループ間に瞬時の反応が発生します。この結果さらに支えられ、溶媒中で反応を行う反応速度を大幅に遅く粘度のわずかな増加は表示されませんでしたのでほぼバランスの分子量を劇的に影響するだろうそれ以外の場合化学量論比。対照的に、チェーンの延長として 1, 4-ブタンジ オールなどの短鎖ジオールを使用すると、結果ウレタン-ウレア エラストマーが少ない弾性のみならず失われたかなりの機械的安定性高分子量の PDMS だった場合は特に合成に使用されます。この結果 (結果は公開されていません)、エラストマーのかなり低分子量に関連していたおそらく重の最後の段階ですべてのイソシアネートの不完全な変換に対応します。さらに、脂肪族ジイソシアネートに向かってアミノ基とヒドロキシル グループの反応性の違いは、生体外の細胞毒性試験から得られた結果を大幅に影響。アミノ鎖エクステンダー APTMDS から調製した PSU エラストマーの抽出 (図 12)、細胞に細胞毒素の効果は展示していません。ただし、シロキサン ベース ウレタン-ウレア エラストマーの抽出物を使用した場合細胞生存率は大幅に削減 (公開されていません)、結果、おそらく低分子量の浸出物と残留未反応イソシアネートに関連していた。
このプロトコルでは、その後高分子量、柔らかく、そして弾性ポリシロキサン尿素エラストマーの合成 macrodiamines として使用することができますアミノ酸機能ポリシロキサンを準備するための便利な方法について説明します。電源ユニットの機械的性質は、PDMS 分子量に従って変えることができる、他のアプリケーションの分野でこれらのポリマーを使用することが可能です。さらに、経由でペンダント ビニル基 (結果は示されていない) を有する環状シロキサンの共重合側グループ、ビニル基などの導入のためアミノ酸機能ポリシロキサンを準備するための手順を使用できます。これが新しい応用分野を開く可能性があります、ソフト架橋の準備を含むポリシロキサン ゲル (例えば、水素機能シリコーン Pt 触媒ヒドロシリル化やメルカプト機能 PDMS の UV 重合チオール-エン付加によって) (結果は示されていない)。
開示事項
著者申告するものがあります。
謝辞
著者は連邦教育省を感謝したいし、下でこの作業を資金調達のための研究 (BMBF) 許可番号 13FH032I3。ドイツ研究振興協会 (DFG Gepris プロジェクト 253160297) による財政援助は感謝します。さらに著者は、 1H NMR と29Si 核磁気共鳴測定を実行するためのテュービンゲン大学から Priska コルブとポール ・ シューラーに感謝を捧げるみたい。おかげで、また CSC Jäkle Chemie GmbH & Co. KG のため H12MDI の供給のため。著者は、応力-ひずみヒステリシス測定と彼女のサポートのためハーバート Thelen、エチレンオキ サイド滅菌の PSU のサンプルを実行するための Biotronik からアンドレ ・ レムとラダ Kitaeva (ロイトリンゲン大学) を感謝したいです。
資料
| Name | Company | Catalog Number | Comments |
| Octamethylcyclotetrasiloxane (D4), 97 % | ABCR GmbH | AB111277 | presumably impairs fertility, must be degassed before use CAS: 556-67-2 |
| 1,3-Bis(3-aminopropyl)-tetramethyldisiloxane, 97% | ABCR GmbH | 110832 | sensitive to air, must be stored under nitrogen CAS: 2469-55-8 |
| 2,4,6,8-Tetramethyl-2,4,6,8-tetraphenylcyclotetrasiloxane | Sigma Aldrich | 40094 | technical grade CAS: 77-63-4 |
| Tetramethylammonium hydroxide pentahydrate | Alfa Aesar | L09658 | toxic if swallowed and upon skin contact, strong base, sensitive to air, hygroscopic, store under refrigeration and under nitrogen CAS: 10424-65-4 |
| 4,4¢-Methylenbis(cyclohexylisocyanate) (H12MDI) | Covestro via CSC Jäkle Chemie GmbH & Co. KG | toxic if inhaled, skin and eye irritant CAS: 5124-30-1 | |
| Tetrahydrofuran (anhydrous) 99.8 % | Alfa Aesar | 44608 | stabilized with BHT CAS: 109-99-9 |
| Chloroform 99 % | Grüssing GmbH Analytica | 1025125000 | stabilized with ethanol, presumably carcinogenic, can impair fertility and cause damage to an unborn child CAS: 67-66-3 |
| Chloroform-d, 99.8 % | Sigma Aldrich | 151823 | CAS: 865-49-6 |
| Dulbecco's modified Eagle's medium (DMEM) high glucose | Thermo Fisher Scientific Life Technologies GmbH | 41965-039 | |
| Fetal bovine serum (FBS) | Thermo Fisher Scientific Life Technologies GmbH | A3160801 | |
| Trypsin/EDTA, 0.25 % phenol red | Thermo Fisher Scientific Life Technologies GmbH | 25200056 | |
| Cell Titer Aqueous One Solution cell proliferation assay (MTS) | Promega GmbH | G3580 | |
| HaCaT-cells | CLS Cell Lines Service GmbH | 300493 | |
| BioComFold | Morcher GmbH | foldable accommodating intraocular lens | |
| Accommodative 1CU | Human Optics AG | foldable accommodating intraocular lens | |
| CrystaLens | Bausch and Lomb Inc. | foldable accommodating intraocular lens | |
| Silmer OH-Di10 | Siltech Corp. | Carbinol-terminated Polydimethylsiloxane | |
| Synchrony | Visiogen Inc. | dual-optic foldable accommodating intraocular lens | |
| Elast-Eon | AorTech International plc | thermoplastic PDMS-PHMO-based polyurethane for medical applications | |
| Pellethane 2363-80A | Lubrizol Life Sciences | thermoplastic polyether-based polyurethane for medical applications | |
| Zwick universal tensile testing machine model 81565 and software testXpert II | Zwick GmbH & Co. KG | tensile testing machine | |
| CASY | Roche Innovatis AG | cell counting system | |
| Multisizer | Beckman Coulter Life Sciences | cell counting system |
参考文献
- Berman, E. R. . Biochemistry of the Eye. , (1991).
- Bozukova, D., Pagnoulle, C., Jérôme, R., Jérôme, C. Polymers in modern ophthalmic implants-Historical background and recent advances. Materials Science and Engineering: R: Reports. 69 (6), 63-83 (2010).
- Kohnen, T., Baumeister, M., Kook, D., Klaproth, O. K., Ohrloff, C. Kataraktchirurgie mit Implantation einer Kunstlinse. Deutsches Ärzteblatt International. 106 (43), 695-702 (2009).
- Lace, R., Murray-Dunning, C., Williams, R. Biomaterials for ocular reconstruction. Journal of Materials Science. 50 (4), 1523-1534 (2015).
- Ong, H. S., Evans, J. R., Allan, B. D. S. Accommodative intraocular lens versus standard monofocal intraocular lens implantation in cataract surgery. Cochrane Database of Systematic Reviews. 5 (5), 1-44 (2014).
- Sheppard, A. L., Bashir, A., Wolffsohn, J. S., Davies, L. N. Accommodating intraocular lenses: a review of design concepts, usage and assessment methods. Clinical and Experimental Optometry. 93 (6), 441-452 (2010).
- Menapace, R., Findl, O., Kriechbaum, K., Leydolt-Koeppl, C. Accommodating intraocular lenses: a critical review of present and future concepts. Graefe's Archive for Clinical and Experimental Ophthalmology. 245 (4), 473-489 (2007).
- Dick, H. B. Accommodative intraocular lenses: current status. Current Opinion in Ophthalmology. 16 (1), 8-26 (2005).
- De Groot, J. H., et al. Hydrogels for an Accommodating Intraocular Lens. An Explorative Study. Biomacromolecules. 4 (3), 608-616 (2003).
- Nishi, O., et al. Refilling the lens with an inflatable endocapsular balloon: surgical procedure in animal eyes. Graefe's Archive for Clinical and Experimental Ophthalmology. 230 (1), 47-55 (1992).
- Nishi, O., Nishi, K. Accommodation amplitude after lens refilling with injectable silicone by sealing the capsule with a plug in primates. Archives of Ophthalmology. 116 (10), 1358-1361 (1998).
- Nishi, O., Nishi, K., Mano, C., Ichihara, M., Honda, T. Lens refilling with injectable silicone in rabbit eyes. Journal of Cataract & Refractive Surgery. 24 (7), 975-982 (1998).
- Nishi, O., Nakai, Y., Mizumoto, Y., Yamada, Y. Capsule opacification after refilling the capsule with an inflatable endocapsular balloon. Journal of Cataract & Refractive Surgery. 23 (10), 1548-1555 (1997).
- Koopmans, S. A., et al. Accommodative Lens Refilling in Rhesus Monkeys. Investigative Ophthalmology & Visual Science. 47 (7), 2976-2984 (2006).
- de Groot, J. H., et al. Injectable intraocular lens materials based upon hydrogels. Biomacromolecules. 2 (3), 628-634 (2001).
- Hao, X., et al. Functionalised polysiloxanes as injectable, in situ curable accommodating intraocular lenses. Biomaterials. 31 (32), 8153-8163 (2010).
- Hao, X., et al. High refractive index polysiloxane as injectable, in situ curable accommodating intraocular lens. Biomaterials. 33 (23), 5659-5671 (2012).
- Han, Y. K., et al. In vitro and in vivo study of lens refilling with poloxamer hydrogel. British Journal of Ophthalmology. 87, 1399-1402 (2003).
- Glasser, A. Accommodation: Mechanism and Measurement. Ophthalmology Clinics. 19 (1), 1-12 (2006).
- Glasser, A. Restoration of accommodation. Current Opinion in Ophthalmology. 17 (1), 12-18 (2006).
- Tomas-Juan, J., Murueta-Goyena, L. A. Axial movement of the dual-optic accommodating intraocular lens for the correction of the presbyopia: Optical performance and clinical outcomes. Journal of Optometry. 8 (2), 67-76 (2015).
- McLeod, S. D., Vargas, L. G., Portney, V., Ting, A. Synchrony dual-optic accommodating intraocular lens: Part 1: Optical and biomechanical principles and design considerations. Journal of Cataract & Refractive Surgery. 33 (1), 37-46 (2007).
- McDonald, J. P., et al. Sarfarazi Elliptical Accommodating IntraOcular Lens (EAIOL) in Rhesus Monkey Eyes In Vitro and In Vivo. Investigative Ophthalmology & Visual Science. 44 (13), 256 (2003).
- Ossma, I. L., et al. Synchrony dual-optic accommodating intraocular lens: Part 2: Pilot clinical evaluation. Journal of Cataract & Refractive Surgery. 33 (1), 47-52 (2007).
- Alio, J. L., Plaza-Puche, A. B., Montalban, R., Ortega, P. Near visual outcomes with single-optic and dual-optic accommodating intraocular lenses. Journal of Cataract Refractive Surgery. 38 (9), 1568-1575 (2012).
- Chen, Q., Liang, S., Thousas, G. A. Elastomeric biomaterials for tissue engineering. Progress in Polymer Science. 38, 584-671 (2013).
- Ward, R. S., Jones, R. L., Ducheyne, P. Polyurethanes and Silicone Polyurethane Copolymers. Comprehensive Biomaterials. , 431-477 (2011).
- Yoda, R. Elastomers for biomedical applications. Journal of Biomaterials Science, Polymer Edition. 9 (6), 561-626 (1998).
- Nicolson, P. C., Vogt, J. Soft contact lens polymers: an evolution. Biomaterials. 22 (24), 3273-3283 (2001).
- Adhikari, R., Gunatillake, P. A., McCarthy, S. J., Meijs, G. F. Mixed macrodiol-based siloxane polyurethanes: effect of the comacrodiol structure on properties and morphology. Journal of Applied Polymer Science. 78 (5), 1071-1082 (2000).
- Sheth, J. P., et al. Structure-property behavior of poly(dimethylsiloxane) based segmented polyurea copolymers modified with poly(propylene oxide). Polymer. 46 (19), 8185-8193 (2005).
- Yilgor, I., Yilgor, E. Silicone-urea copolymers modified with polyethers. ACS Symposium Series. 964, 100-115 (2007).
- . Elast-EonTM biocompatible polyurethane - CSIROpedia Available from: https://csiropedia.csiro.au/elast-eon-biocompatible-polyurethane/ (2008)
- Gunatillake, P. A., Meijs, G. F., McCarthy, S. J., Adhikari, R. Poly(dimethylsiloxane)/poly(hexamethylene oxide) mixed macrodiol based polyurethane elastomers. I. Synthesis and properties. Journal of Applied Polymer Science. 76 (14), 2026-2040 (2000).
- Adhikari, R., Gunatillake, P. A., McCarthy, S. J., Meijs, G. F. Low-modulus siloxane-based polyurethanes. I. Effect of the chain extender 1,3-bis(4-hydroxybutyl)1,1,3,3-tetramethyldisiloxane (BHTD) on properties and morphology. Journal of Applied Polymer Science. 83 (4), 736-746 (2002).
- Adhikari, R., Gunatillake, P. A., McCarthy, S. J., Bown, M., Meijs, G. F. Low-modulus siloxane-polyurethanes. Part II. Effect of chain extender structure on properties and morphology. Journal of Applied Polymer Science. 87 (7), 1092-1100 (2003).
- Martin, D. J., et al. Polydimethylsiloxane/polyether-mixed macrodiol-based polyurethane elastomers: biostability. Biomaterials. 21 (10), 1021-1029 (2000).
- Simmons, A., et al. Long-term in vivo biostability of poly(dimethylsiloxane)/poly(hexamethylene oxide) mixed macrodiol-based polyurethane elastomers. Biomaterials. 25 (20), 4887-4900 (2004).
- Gunatillake, P. A., Martin, D. J., Meijs, G. F., McCarthy, S. J., Adhikari, R. Designing biostable polyurethane elastomers for biomedical implants. Australian Journal of Chemistry. 56 (6), 545-557 (2003).
- Briganti, E., et al. Silicone based polyurethane materials: a promising biocompatible elastomeric formulation for cardiovascular applications. Journal of Materials Science: Materials in Medicine. 17 (3), 259-266 (2006).
- Lim, F., Buchko, C., Shah, A., Simhambhatla, M. Medical device formed of silicone-polyurethane. U.S. Patent Application. , (2002).
- Ward, R., Anderson, J., McVenes, R., Stokes, K. In vivo biostability of polysiloxane polyether polyurethanes: Resistance to biologic oxidation and stress cracking. Journal of Biomedical Materials Research Part A. 77 (3), 580-589 (2006).
- Hermans, E. A., et al. Development of a ciliary muscle-driven accommodating intraocular lens. Journal of Cataract & Refractive Surgery. 34 (12), 2133-2138 (2008).
- Hoffman, J. J., Leir, C. M. Tetramethylammonium 3-aminopropyl dimethylsilanolate-A new catalyst for the synthesis of high purity, high molecular weight α,ω-bis(aminopropyl) polydimethylsiloxanes. Polymer International. 24, 131-138 (1991).
- Keiper, F. D. I. N. Prüfung von Kautschuk und Elastomeren - Bestimmung von Reißfestigkeit, Zugfestigkeit, Reißdehnung und Spannungswerten im Zugversuch. Deutsches Institut für Normung e.V. , (2017).
- Wenzelewski, K. DIN EN ISO 10993-5. Biologische Beurteilung von Medizinprodukten - Teil 5: Prüfungen auf In-vitro-Zytotoxizität (ISO 10993-5:2009); Deutsche Fassung EN ISO 10993-5:2009. Deutsches Institut für Normung e.V. , (2009).
- . CellTiter 96® AQueous One Solution Cell Proliferation Assay. Technical Bulletin Available from: https://www.promega.com/-/media/files/resources/protocols/technical-bulletins/0/celltiter-96-aqueous-one-solution-cell-proliferation-assay-system-protocol.pdf (2012)
- Riehle, N., et al. Influence of PDMS molecular weight on transparency and mechanical properties of soft polysiloxane-urea-elastomers for intraocular lens application. European Polymer Journal. 101, 190-201 (2018).
- Gottlieb, H. E., Kotlyar, V., Nudelman, A. NMR Chemical Shifts of Common Laboratory Solvents as Trace Impurities. Journal of Organic Chemistry. 62 (21), 7512-7515 (1997).
- Riehle, N., Götz, T., Kandelbauer, A., Tovar, G. E. M., Lorenz, G. Data on the synthesis and mechanical characterization of polysiloxane-based urea-elastomers prepared from amino-terminated polydimethylsiloxanes and polydimethyl-methyl-phenyl-siloxane-copolymers. Data in Brief. 18, 1784-1794 (2018).
- Christ, R., Nash, B. A., Petraitis, D. J. Optically clear reinforced silicone elastomers of high optical refractive index and improved mechanical properties for use in intraocular lenses. U.S. Patent 5494946 A. , (1993).
- Jha, G. S., Seshadri, G., Mohan, A., Khandal, R. K. Sulfur containing optical plastics and its ophthalmic lenses applications. e-Polymers. 8 (1), 376-402 (2008).
- Rogulska, M., Kultys, A., Olszewska, E. New thermoplastic poly(thiourethane-urethane) elastomers based on hexane-1,6-diyl diisocyanate (HDI). Journal of Thermal Analysis and Calorimetry. 114 (2), 903-916 (2013).
- Yilgör, I., Riffle, J. S., McGrath, J. E., Harris, F. W., Spinelli, H. J. Reactive Siloxane Oligomers. Reactive Oligomers. , 161-174 (1985).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved