このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
Method Article
ヒト人工多能性幹細胞由来心筋細胞における単細胞光学作用電位測定
要約
ここでは、高速モジュラーフォトメトリーシステムを用いた誘導多能性幹細胞由来心筋細胞からの作用電位の光学的獲得および特性評価について述べている。
要約
従来の細胞内微小電極技術は、心筋細胞電気生理学を定量する、極めて複雑で、労働集約的であり、典型的には低スループットで行われる。誘導多能性幹細胞(iPSC)技術の急速かつ継続的な拡大は、心血管研究における新しい標準を提示し、単一細胞レベルでの電気生理学的データのスループットを向上させるために代替方法が必要になりました。VF2.1Clは、膜電位の変動に対する急速な単一チャネル、高い強度応答を提供する最近得られた電圧感受性色素です。他の既存の電圧指標よりも優れた運動学を有し、従来の微小電極技術と同等の機能データを利用できます。ここでは、モジュール式で手頃な価格のフォトメトリーシステムを用いて、外部ペースのヒトiPSC由来心筋細胞における、単純化された非侵襲的作用電機の特性を実証する。
概要
心筋細胞の電気生理学的モデリングと心臓薬物スクリーニングのための効率的なプラットフォームの構築は、様々な不整脈障害の治療戦略の開発に不可欠です。誘導多能性幹細胞(iPSC)技術の急速な拡大は、単離患者由来心筋細胞(iPSC-CM)を用いたヒト疾患モデリングおよび薬理学的調査への有望な進出を生み出した。パッチクランプ(電流クランプ)を介してこれらの細胞の電気生理学的特徴付けのための「ゴールドスタンダード」技術は、作用電位(AP)形態および持続時間を定量化することができるが、この方法は非常に複雑で遅く、高スループットデータ取得1に適していない。iPSC-CMは、成人の天然心筋細胞2と比較して、拡張期膜電位が増加し、リーク電流が増加すると定期的に報告されている。iPSC-CMで観察される小さな細胞サイズおよび減少した膜容量は、電流クランプ技術を使用する際に系統的な誤差を生じさせる可能性があり、これらの偏差を説明する可能性が示唆される3。iPSC-CMプラットフォームの有用性を最大限に高めるためには、iPSC-CMで膜貫通電圧変化を単一のセルレベルで特性化する際のスループットとデータ精度を高めるため、追加の方法が重要です。
電圧感受性色素(VSD)は、従来の技術4と比較して、心臓AP動態のより速く、非侵襲的かつ同等の分析を提供する方法として提案されてきた。最近の研究では、レシオメトリック電圧感受性プローブフォトメトリーの適合性が、心臓AP5を正確に定量化することが実証されました。さらに、光学的な光測定のアプローチを容易にスケールアップする能力は、治療薬の開発に重要な大規模な心毒性スクリーン(例えば、CiPA)にこの技術を貸す。微小電極アレイと電圧感知光学技術を用いたブラインドマルチサイト研究における標準化された心毒性プロトコルの開発は、このアプローチの重要な価値を実証した6。
多くのポテンショメトリック色素は市販されており、新しいプローブの継続的な合成開発は、様々な心臓および神経構造にわたってその有効性を合理化するためのエキサイティングな可能性を示しています。理想的なVSDは、容量性負荷、光漂白および細胞毒性の低下を示しながら、運動および感受性を増強する。最近合成されたVF2.1Cl(FluoVolt)は、新しい電圧蛍光(VF)ファミリー7の他のメンバーが共有する、その新しいワイヤベースの分子構造に大きく起因するこれらの有益な特性の多くを表す。単純なプローブが分子的および電気的に化学接合する一般的なエレクトロクロミックVSDとは対照的に、この色素は、電子リッチドナーと修飾フルオロフォア(FITC)を組み合わせた受動的に挿入された膜スパン合成ワイヤーで構成されています。機械の詳細は 図 1に示されています。この色素は、膜電圧変動に対する優れた感度を示し、同等の速度で他の一般的なプローブに見られる〜10%とは対照的に、100mV当たりの発光強度の27%の変化を示す7。さらに、ワイヤベースのPeTシステムは、最小限の電気的干渉と細胞容量負荷のわずかな変化を生じるセルラー電界と直接相互作用しません。
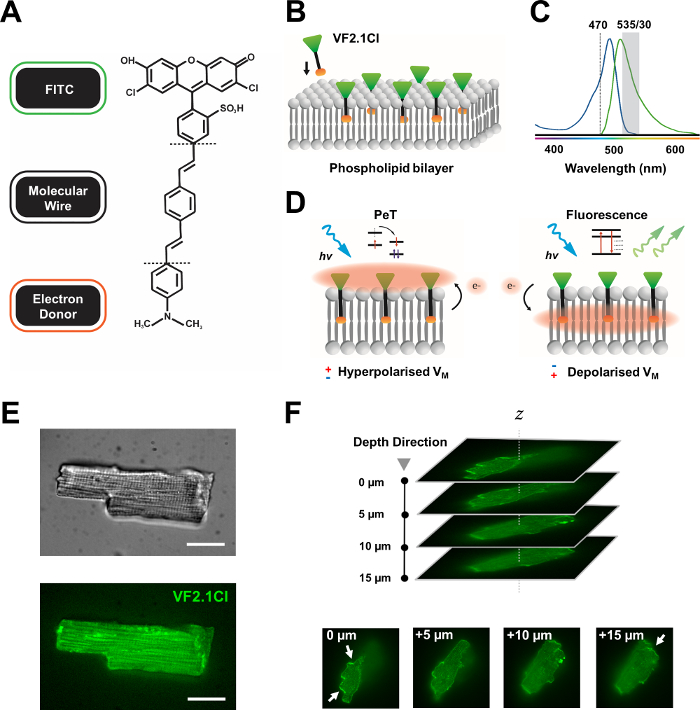
図1:VF2.1Cl色素の化学的、スペクトル的および機械的なパラメータ。(A)VF2.1Clの化学的構造. 注意すべき分子的特徴は、フェニレンビニレン分子線内の複数のアルキル基を含み、この細胞膜への挿入を容易にする。FITCプローブに結合した負の帯電スルホン酸基は、細胞外表面のフッ素酸安定化を保証し、脂質二重層の電界に対する垂直挿入に近い助けとなります。(B)標的細胞の細胞膜に埋め込む垂直VF2.1Clの簡略図である。(C)VF2.1Cl色素の吸収および発光スペクトル。スペクトルは、標準的なFITCおよびGFPプローブのそれと同じです。(D) VF2.1Clの作用の機械モードの描写。安静状態(過分極)では、負の細胞内電圧は、rostralフルオロフォアに向かって自由電子を駆動します。電子の存在量は光励起後の励起状態から外れる経路として光誘導電子移動(PeT)が好ましいこと、蛍光を効果的に消光することを保証する。これに対して、脱分極膜電位は、光学励起時に蛍光を好む下向きの電子移動に影響を与える。得られた蛍光応答は膜電圧に直線的に関連しており、細胞電生理学的運動に関する詳細な時間情報を収集するために正確に利用することができる。(E)VF2.1Clを搭載したレポリン心筋細胞の470nm(下)画像における代表的な明視野(上)および蛍光(F)単一の装填された心筋細胞のZスタック。矢印は、細胞膜へのVF2.1Clの明確な局在の領域を示す。画像は、50 μmのピンホールパターンを持つX-lightv3回転ディスク共焦点ヘッドからなる回転ディスク共焦点システムで取得されました。LDI-7イルミエーター;Prime95BカメラとPlanApoラムダ100xの目的。スケールバー:20 μm.この図の大きなバージョンを表示するには、ここをクリックしてください。
VF2.1Clに結合したFITCプローブは、標準フィルタ構成およびGFPフィルタ構成下で効果的に使用できることを保証し、単一のチャネル取得システムのみが必要であり、どちらも蛍光イメージングプラットフォームの共通の特徴です。この色素を用いた高密度ヒトiPSC-CM単層の解析は、最近8、9、10、11と報告されている。我々のプロトコルは、緻密な一層の電気的およびパラクリンの影響によって妨げられない単一の孤立したiPSC-CMの調査と、複雑な共焦点または広視野イメージングの取り決めとは対照的に、手頃でカスタマイズ可能なフォトメトリーシステムの使用のために、これらの研究とは異なる。
ここでは、孤立したヒトiPSC由来の心筋細胞およびネイティブ心筋細胞からの堅牢な光学APの迅速な取得と分析のためのプロトコルについて説明 します(補足ファイルを参照)。我々は、単一細胞のフォトメトリー測定のための最先端のプラットフォームのカスタマイズ可能な状態と結合されたVF2.1Clを使用する。これらの実験プロトコルは、大学医療センターゲッティンゲン(No. 10/9/15)の倫理委員会によって承認されています。
プロトコル
1. 細胞製剤
注:このプロトコルで使用されるヒトiPSCは、健康なドナーから誘導され、前述の12、13、14のように、WNTシグナルおよび乳酸精製技術の完全に定義された小分子変調を使用して単層で区別された。iPSC-CMは、以下に概説する培養培地で2〜3日ごとに維持された。
- 基礎培地(RPMI 1640)および2%サプリメント(B27)の培地を調製する。4 °Cで保管。 室温(RT)で使用してください。
- 基底培地(RPMI 1640)、2%サプリメント(B27)および1:2000 ROCK阻害剤のめっき培地を調製します。4 °Cで保管。 RT で使用します。
- コートは10 mmの丸いガラス#0のカバースリップを1:60の1:60の気に入った基膜マトリックスの150のmmと4の4時間の4°Cでインキュベートする。
注:カバースリップの体積の最適化は、こぼれを防ぐために十分な表面張力を維持しながら、ガラス全体が覆われていることを確認するために必要です。150 μL は、10 mm の丸いカバーリップに推奨されます。バッチサイズ、カバースリップタイプ、カバースリップ容積および培養プレートタイプは、実験者のニーズに適することができる。 - EDTAベースの細胞解離試薬とのiPSC-CM解離を開始します。1,000 μL ピペットで静かに洗い流して、単層が完全に切り離されていることを確認します。
- 細胞懸濁液を15mLチューブに移し、二重容積メッキ媒体を加えます。遠心分離機 10分 100 x g.
- ペレットを、メッキ媒体の所望の容積(再懸濁液量)で再懸濁する。手動または電子的にセルをカウントします。
- カバースリップ当たりの最適密度(15,000)を選択し、後で単離された細胞分析を可能にします。
- この望ましい密度ですべてのカバーリップをプレートするために必要な「アクティブ」細胞懸濁液(A)の体積を計算します。次の式を適用し、別のチューブに引き出します。

- 各カバースリップを所望のボリュームに収めるために必要な追加めっき媒体(B)の体積を計算します。次の式を適用し、結果のボリュームをアクティブサスペンションのチューブに追加します。
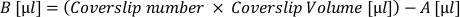
- カバースリップからマトリックスを取り外し、セルサスペンション(A+B)の「カバースリップボリューム」を各カバースリップに適用します。細胞の分布を確保するためにチューブ内で定期的に再中断します。
- 37°Cで1時間インキュベートする。めっき培地でウェルを軽く充填します。
- 24時間後、培地を通常の培養培地と交換し、2~3日毎に維持する。
2. 実験的なセットアップ
- 反転した蛍光顕微鏡に40倍の拡大率、高い開口レンズ(N.A:>0.75)を装備して実験を行います。
- 高速切り替え暖かい白色LEDを顕微鏡の送信された照明ポートに結合する。透過光路にシンプルな赤色660 nmフィルタを挿入します。
注:この光は、緑色の蛍光信号を汚染することなくサンプルを観察するために、光測定実験を通して活性化することができます。 - フォトメトリー記録用の高速スイッチング470 nm LEDヘッドを取り付けます。470/40励起フィルターを顕微鏡の蛍光ポートに挿入して、LEDによって発生する光をクリーンアップします。
メモ:最適な信号定量を行うため、光出力の高速フィードバック制御を備えた照明システムを推奨します。 - 顕微鏡内の鏡ユニットカルーセルに495nmのロングパスビームスプリッターを含む顕微鏡キューブを挿入します。
- 可変フィールドダイヤフラムを含む検出アームを顕微鏡Cマウントポートに装着し、対象領域を選択できるようにします。
- 別に顕微鏡に光増倍検出器(PMT)とUSBカメラを組み合わせる。これは、排出ガス検出システムの基礎を形成します。
- 565 nmのロングパスビームスプリッターと535/50のエミッションフィルタを含むフィルタキューブをPMTポートに挿入します。これは2つの探知器間の放出の光を割る。
注:発光検出システムの送信ポートに取り付けられたカメラは、すべての実験を通して明視野下で透過光を検出することができます。 - PMT を電源装置と PMT アンプに結合します。PMTアンプ出力をデータ収集システムのアナログ入力ピンに接続します。
- PMTからのアナログデータを1kHz以上でフィルタリングします。
- ナイキスト基準を満たし、エイリアスを防ぐために、アナログ信号(2 kHz以上)に存在する最も高い周波数の2倍以上の周波数でデータをデジタル化します。
VF2.1Cl によるセルラーローディング
注:この染料を含むすべてのステップは、低照度条件で行う必要があります。
- タイロードの浴液(mM)を準備する:140 NaCl、10 HEPES、10グルコース、4KCl、1 MgCl2、2CaCl2、pH= 7.35、37°Cに暖かい。
- 1,000x VF2.1Clの5 μLと20%可溶化ポロクサマー溶液の50 μLを混合して、マイクロ遠心チューブに溶液をローディングするアリコートを用意します。
- 20 mm ペトリ皿に 5 μL の加温タイローデ溶液(合計0.1x染料濃度)を5 mL塗布します。
注意: 最終染料濃度は0.1倍です。これはメーカーが提案した1/10thです 。これにより、リソースを節約し、ごくわずかな細胞毒性を保証し、重要なことに、高い信号対雑音比を持つロードされた細胞からの明確な光信号を保持します。 - iPSC-CMカバースリップを1枚皿に加え、37°Cで20分間インキュベートします。
- 加熱された生細胞イメージングチャンバーを組み立てます。顕微鏡の段階に取付け、500 μL の新鮮なタイローデの溶液で満たします。
- 37 °Cで新鮮なタイロードの溶液でカバースリップを洗います。
- iPSC-CMカバースリップを、細かいポイント鉗子を使用して、あらかじめ温めた浴室に慎重に塗布してください。
注:チャンバーとその内容物が常に生理学的温度で加熱されていることを確認してください。必要に応じて、温めたタイローデの溶液の連続灌流から始めます。
4. 電界刺激
注: iPSC-CM の外部トリガーはオプションですが、セルラーダイナミクスと実験パラメータの標準化に役立ちます。分析の容易さを高め、周波数依存効果の調査を可能にします。
- 5 mm離れた場所に2つの白金電極を付けて、刺激インサートを記録チャンバーに取り付けます。
- 外部刺激装置を刺激インサートに接続します。0.5 Hz の 5 ms バイポーラ フィールド パルスに設定します。
- 1 Vから上向きの刺激を増加させることにより、最適な刺激電圧を決定します。閾値刺激は、セルが収縮し始める最も低い電圧として定義されます。このしきい値を約25%上回る電圧を適用します。通常の範囲は1 V~30Vです。
- 外部刺激器で刺激周波数を固定するか、取得ソフトウェアでトリガーします。
5. 光学的なアクションポテンシャル獲得
注: このプロトコルは、取得および分析に商用ソフトウェアを使用します。
- 透過光路とUSBカメラを使用して、明視野ビューで筋細胞を可視化します。
- 孤立した細胞を選択し、対象の細胞からの光のみを監視することを保証するフィールドダイヤフラムで光学路をしっかりと切り取ります。
- PMTアンプを起動し、PMT電源を750Vに設定します。
- 刺激プロトコル(ステップ4を参照)を取得ソフトウェアと一緒に実行し、同時に470 nm励起光をアクティブにします。後者はリモートパネルを介して行うか、固定強度(TTL信号)で自動化することができます。
- PMTアンプのゲインとオフセットを調整して、信号が飽和せず、記録システムの検出範囲に最適化されていることを確認します。
- 安定したアクション電位を確実に検出する、10のスイープを記録します。
- 記録を続け、すぐに顕微鏡ステージを動かして、細胞を欠いた領域からバックグラウンド信号を短時間取得します。励起ライトをオフにします。
注: この背景値 (Fオフセット ) は、任意のバックグラウンド蛍光を考慮するために使用されます。 - 所望ならば、1μMニフェジピンなどの参照薬を局所的にパーフューズし、薬理学的操作に対する細胞応答を同定する。
- 順次的に、新しいセルを選択するたびに、ステップ 5.2 ~ 5.7 を繰り返します。必要に応じてカバーリップを交換して、1座って高い実験回転率を確保します。
注 : 読み込みおよびイメージ取得のプロトコルについては 、図 2を参照してください。
6. データ分析
- 解析ソフトウェアで保存された記録を開き、1つのセルから刺激されたアクション電位を含む平均10スイープを開きます。
- Fオフセット を表すベースライン信号の平均を取り、平均されたトレースからこれを減算します。
- 次の式∆F/F0を計算します(Fは蛍光を測定し、F0は拡張蛍光です)。
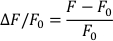
- トレースベースライン(拡張期)と対象領域(AP)を特定し、所望の心臓行動電位パラメータを測定する。これには、50%(APD50)および90%(APD90)の再分極の減衰時間が含まれますが、これらに限定されません。
- この単一のセルからスプレッドシート ソフトウェアにデータをエクスポートします。
- すべての録画について、手順 6.1 ~ 6.5 を繰り返します。適切な不対検定または分散分析で結果を評価します。
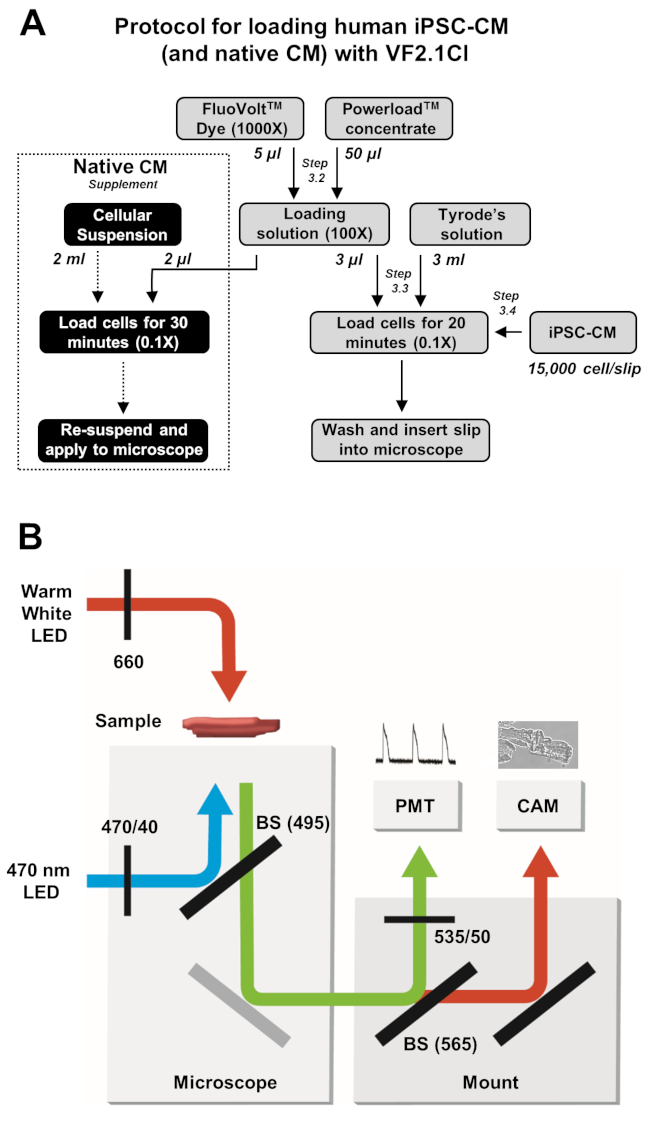
図2:読み込みおよび画像取得プロトコル(A) iPSC-CM およびネイティブ心筋細胞用の完全な VF2.1Cl 負荷プロトコルのフローチャート。(B) ビームスプリッタ(BS)と、このプロトコルで使用されるフィルタ構成の簡略化された概略で、膜貫通電圧の変化に応じてVF2.1Cl発光の励起および検出を行う。 この図の大きなバージョンを表示するには、ここをクリックしてください。
結果
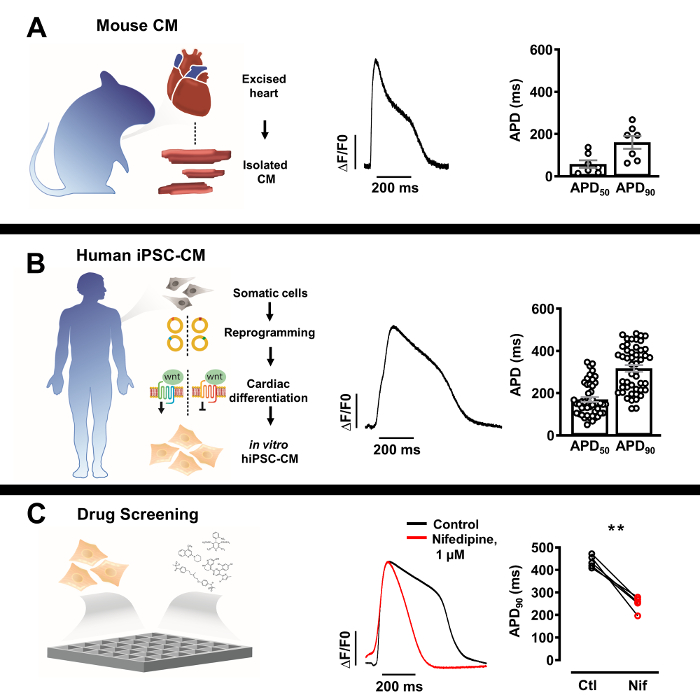
図3:単離した天然型心筋細胞およびヒト誘導多能性幹細胞由来心筋細胞(iPSC-CM)の光学作用電位(AP)プロファイル。(A)APD50およびAPD90の平均±SEMを有する単一のマウス心筋細胞(中央)の代表的な光学AP(n = 7、右)。(B) APD50およびAPD90の平均±SEM?...
ディスカッション
電気生理学的モデリングや心臓薬スクリーニングに適した単離されたiPSC-CMから詳細なAPプロファイルを容易に取得するための基本的なプロトコルについて説明する。私たちは、インジケーター機能と方法論的忠実性の両方を示唆する、まばらなシードのiPSC-CMから定期的で堅牢なAPを検出します。
iPSCリプログラミングのための商業的方法論の広いスペクトルと心臓分化プ?...
開示事項
ケアンリサーチ社は、ビデオファイルの制作コストをカバーすることにより、この出版物をサポートしました。
謝辞
著者らは、この出版物の生産コストをカバーする彼らの種類の財政的貢献のためにケアンリサーチ株式会社を認めたいと思います。さらに、イネス・ミューラー氏とステファニー・ケステル氏の優れた技術サポートに感謝します。
著者らの研究は、ドイツ心臓血管研究センター(DZHK)、ドイツフォルシュングスゲミンシャフト(DFG、 ドイツ研究財団、VO 1568/3-1、IRTG1816 RP12、SFB1002 TPA13、ドイツのエクセレンス戦略の下で - EXC 2067/1- 390729940)とエルゼ・クレナー・フレゼニウス・スティフトゥン(EKFS)2016_A20 FS)。
資料
| Name | Company | Catalog Number | Comments |
| Reagents | |||
| 0.25 Trypsin EDTA | Gibco | 25200056 | |
| B27 Supplement | Gibco | 17504044 | |
| CaCl2 | Carl Roth | HN04.2 | |
| D(+)-Glucose anhydrous BioChemica | ITW Reagents | A1422 | |
| Fetal Bovine Serum | Gibco | 10270-106 | |
| FluoVolt Membrane Potential Kit | Invitrogen | F10488 | |
| HEPES | Carl Roth | HN77.4 | |
| KCl | Sigma-Aldrich | 6781.1 | |
| Lamanin | Sigma-Aldrich | 114956-81-9 | |
| Matrigel | BD | 354230 | |
| NaCl | Sigma-Aldrich | 9265.2 | |
| Nifedipine | Sigma-Aldrich | 21829-25-4 | |
| Penicillin/Streptomycin | Invitrogen | 15140 | |
| ROCK Inhibitor Y27632 | Stemolecule | 04-0012-10 | |
| RPMI 1640 Medium | Gibco | 61870010 | |
| Versene EDTA | Gibco | 15040033 | |
| Equipment | |||
| 495LP Dichroic Beamsplitter | Chroma Technology | ||
| Axopatch 200B Amplifier | Molecular Devices | ||
| Circle Coverslips, Thickness 0 | Thermo Scientific | CB00100RA020MNT0 | |
| Digidata 1550B | Molecular Devices | ||
| Dual OptoLED Power Supply | Cairn Research | ||
| ET470/40x Excitation Filter | Chroma Technology | ||
| ET535/50m | Chroma Technology | ||
| Etched Neubauer Hemacytometer | Hausser Scientific | ||
| Filter Cubes | Cairn Research | ||
| IX73 Inverted Microscope | Olympus | ||
| MonoLED | Cairn Research | ||
| Multiport Adaptors | Cairn Research | ||
| Myopacer Cell Stimulator | IonOptix | ||
| Optomask Shutter | Cairn Research | ||
| Optoscan System Controller | Cairn Research | ||
| PH-1 Temperature Controlled Platform | Warner Instruments | ||
| Photomultiplier Detector | Cairn Research | ||
| PMT Amplifier Insert | Cairn Research | ||
| PMT Supply Insert | Cairn Research | ||
| RC-26G Open Bath Chamber | Warner Instruments | ||
| SA-OLY/2AL Stage Adaptor | Olympus | ||
| T565lpxr Dichroic Beamsplitter | Chroma Technology | ||
| T660lpxr Dichroic Beamsplitter | Chroma Technology | ||
| TC-20 Dual Channel Temperature Controller | npi Electronic | ||
| UPLFLN 40X Objective | Olympus | ||
| USB 3.0 Colour Camera | Imaging Source | ||
| Software | |||
| Clampex 11.1 | Molecular Devices | ||
| Clampfit 11.1 | Molecular Devices | ||
| IC Capture 2.4 | Imaging Source | ||
| Prism 8 | Graphpad |
参考文献
- Miller, E. W. Small molecule fluorescent voltage indicators for studying membrane potential. Current Opinion in Chemical Biology. 33, 74-80 (2016).
- Liang, P., et al. Drug screening using a library of human induced pluripotent stem cell-derived cardiomyocytes reveals disease-specific patterns of cardiotoxicity. Circulation. 127 (16), 1677-1691 (2013).
- Horváth, A., et al. Low resting membrane potential and low inward rectifier potassium currents are not inherent features of hiPSC-derived cardiomyocytes. Stem Cell Reports. 10 (3), 822-833 (2018).
- Salama, G., Morad, M. Merocyanine 540 as an optical probe of transmembrane electrical activity in the heart. Science. 191 (4226), 485-487 (1976).
- Hortigon-Vinagre, M., et al. The use of ratiometric fluorescence measurements of the voltage sensitive dye Di-4-ANEPPS to examine action potential characteristics and drug effects on human induced pluripotent stem cell-derived cardiomyocytes. Toxicological Sciences. 154 (2), 320-331 (2016).
- Blinova, K., et al. International multisite study of human-induced pluripotent stem cell-derived cardiomyocytes for drug proarrhythmic potential assessment. Cell Reports. 24 (13), 3582-3592 (2018).
- Miller, E. W., et al. Optically monitoring voltage in neurons by photo-induced electron transfer through molecular wires. Proceedings of the National Academy of Sciences. 109 (6), 2114-2119 (2012).
- Bedut, S., et al. High-throughput drug profiling with voltage- and calcium-sensitive fluorescent probes in human iPSC-derived cardiomyocytes. American Journal of Physiology-Heart and Circulatory Physiology. 311 (1), 44-53 (2016).
- McKeithan, W. L., et al. An automated platform for assessment of congenital and drug-induced arrhythmia with hiPSC-derived cardiomyocytes. Frontiers in Physiology. 8, 766 (2017).
- Duncan, G., et al. Drug-mediated shortening of action potentials in LQTS2 human induced pluripotent stem cell-derived cardiomyocytes. Stem Cells and Development. 26 (23), 1695-1705 (2017).
- Asakura, K., Hayashi, S., Ojima, A., Taniguchi, T., Miyamoto, N. Improvement of acquisition and analysis methods in multi-electrode array experiments with iPS cell-derived cardiomyocytes. Journal of Pharmacological and Toxicological Methods. 75, 17-26 (2015).
- Lian, X., et al. Directed cardiomyocyte differentiation from human pluripotent stem cells by modulating Wnt/β-catenin signaling under fully defined conditions. Nature Protocols. 8 (1), 162-175 (2013).
- Burridge, P. W., et al. Chemically defined generation of human cardiomyocytes. Nature methods. 11 (8), 855-860 (2014).
- Kleinsorge, M., Cyganek, L. Subtype-directed differentiation of human iPSCs into atrial and ventricular cardiomyocytes. STAR Protocols. , 100026 (2020).
- Knollmann, B. C., Katchman, A. N., Franz, M. R. Monophasic action potential recordings from intact mouse heart: validation, regional heterogeneity, and relation to refractoriness. Journal of Cardiovascular Electrophysiology. 12 (11), 1286-1294 (2001).
- Leopold, J. A., Loscalzo, J. Emerging role of precision medicine in cardiovascular disease. Circulation Research. 122 (9), 1302-1315 (2018).
- Voigt, N., Zhou, X. B., Dobrev, D. Isolation of human atrial myocytes for simultaneous measurements of Ca2+ transients and membrane currents. Journal of Visualized Experiments. (77), e50235 (2013).
- Voigt, N., et al. Enhanced sarcoplasmic reticulum Ca2+ Leak and increased Na+-Ca2+ exchanger function underlie delayed afterdepolarizations in patients with chronic atrial fibrillation. Circulation. 125 (17), 2059-2070 (2012).
- Voigt, N., et al. Cellular and molecular mechanisms of atrial arrhythmogenesis in patients with paroxysmal atrial fibrillation. Circulation. 129 (2), 145-156 (2014).
- Fakuade, F. E., et al. Altered atrial cytosolic calcium handling contributes to the development of postoperative atrial fibrillation. Cardiovascular Research. , 162 (2020).
- Gross, E., Bedlack, R. S., Loew, L. M. Dual-wavelength ratiometric fluorescence measurement of the membrane dipole potential. Biophysical Journal. 67 (1), 208-216 (1994).
- Matiukas, A., et al. Near-infrared voltage-sensitive fluorescent dyes optimized for optical mapping in blood-perfused myocardium. Heart Rhythm. 4 (11), 1441-1451 (2007).
- Mutoh, H., et al. Spectrally-resolved response properties of the three most advanced fret based fluorescent protein voltage probes. PLoS One. 4 (2), 4555 (2009).
- Hochbaum, D. R., et al. All-optical electrophysiology in mammalian neurons using engineered microbial rhodopsins. Nature Methods. 11 (8), 825-833 (2014).
- Huang, Y. L., Walker, A. S., Miller, E. W. A photostable silicon rhodamine platform for optical voltage sensing. Journal of the American Chemical Society. 137 (33), 10767-10776 (2015).
- Deal, P. E., Kulkarni, R. U., Al-Abdullatif, S. H., Miller, E. W. Isomerically pure tetramethylrhodamine voltage reporters. Journal of the American Chemical Society. 138 (29), 9085-9088 (2016).
- Fluhler, E., Burnham, V. G., Loew, L. M. Spectra, membrane binding, and potentiometric responses of new charge shift probes. Biochemistry. 24 (21), 5749-5755 (1985).
- Fromherz, P., Muller, C. O. Voltage-sensitive fluorescence of amphiphilic hemicyanine dyes in neuron membrane. Biochimica et Biophysica Acta. 1150 (2), 111-122 (1993).
- Salama, G., et al. Properties of new, long-wavelength, voltage-sensitive dyes in the heart. Journal of Membrane Biology. 208 (2), 125-140 (2005).
- Jin, L., et al. Single action potentials and subthreshold electrical events imaged in neurons with a fluorescent protein voltage probe. Neuron. 75 (5), 779-785 (2012).
- Kralj, J. M., Douglass, A. D., Hochbaum, D. R., MacLaurin, D., Cohen, A. E. Optical recording of action potentials in mammalian neurons using a microbial rhodopsin. Nature Methods. 9 (1), 90-95 (2012).
- Tsutsui, H., Karasawa, S., Okamura, Y., Miyawaki, A. Improving membrane voltage measurements using FRET with new fluorescent proteins. Nature Methods. 5 (8), 683-685 (2008).
- Lundby, A., Mutoh, H., Dimitrov, D., Akemann, W., Knöpfel, T. Engineering of a genetically encodable fluorescent voltage sensor exploiting fast Ci-VSP voltage-sensing movements. PLoS One. 3 (6), 2514 (2008).
- Bradley, J., Luo, R., Otis, T. S., DiGregorio, D. A. Submillisecond optical reporting of membrane potential in situ using a neuronal tracer dye. The Journal of neuroscience. 29 (29), 9197-9209 (2009).
- Herron, T. J., Lee, P., Jalife, J. Optical imaging of voltage and calcium in cardiac cells & tissues. Circulation Research. 110 (4), 609-623 (2012).
- Kappadan, V., et al. High-resolution optical measurement of cardiac restitution, contraction, and fibrillation dynamics in beating vs. blebbistatin-uncoupled isolated rabbit hearts. Frontiers in Physiology. 11, 464 (2020).
- Kettlewell, S., Walker, N. L., Cobbe, S. M., Burton, F. L., Smith, G. L. The electrophysiological and mechanical effects of 2,3-butane-dione monoxime and cytochalasin-D in the Langendorff perfused rabbit heart. Experimental Physiology. 89 (2), 163-172 (2004).
- Képiró, M., et al. para-Nitroblebbistatin, the non-cytotoxic and photostable Myosin inhibitor. Angewandte Chemie International Edition. 53 (31), 8211-8215 (2014).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved