このコンテンツを視聴するには、JoVE 購読が必要です。 サインイン又は無料トライアルを申し込む。
アキレス腱インピンジメントのメカノバイオロジー研究のためのマウス後肢外植モデル
要約
マウス後肢外植片におけるアキレス腱挿入のインピンジメントによって引き起こされる線維軟骨性変化を再現するカスタム実験プラットフォームと組織培養プロトコルを提示し、腱インピンジメントのメカノバイオロジーを探索するのに適したモデルを提供します。
要約
骨への腱の衝突は、横方向の圧縮ひずみが著しく上昇した多軸の機械的ひずみ環境を生成し、グリコサミノグリカン(GAG)に富むマトリックスの蓄積とコラーゲンネットワークのリモデリングを特徴とする局所的な線維軟骨表現型を誘発します。線維軟骨は健康な腱の侵食領域では正常な特徴ですが、過剰なGAG沈着とコラーゲンネットワークの混乱は腱鞘炎の特徴です。したがって、インピンジメントは、腱鞘炎の開始と進行における重要な外因性因子として臨床的に認識されています。それにもかかわらず、腱インピンジメントの根底にあるメカノバイオロジーは研究が不十分なままです。腱インピンジメントに対する細胞応答を解明するための以前の取り組みは、細胞に一軸圧迫を適用し、in vitroで腱外植片を切除しました。しかし、単離された細胞は、機械応答に重要な3次元の細胞外環境を欠いており、 in vitro および切除外植片研究の両方で、in vivoでの腱の衝突によって生成される多軸ひずみ環境を再現することができず、これは衝突領域の解剖学的特徴に依存します。さらに、腱インピンジメントの in vivo モデルでは、機械的ひずみ環境を制御できません。これらの限界を克服するために、アキレス腱インピンジメントのメカノバイオロジーを研究するのに適した新しいマウス後肢外植片モデルを提示します。このモデルは、アキレス腱を その場で 維持して局所的な解剖学的構造を維持し、受動的に加えられた足首背屈時にアキレス腱が踵骨に挿入されることによって発生する多軸ひずみ環境を再現し、細胞を本来の環境に保持します。このモデルに不可欠な組織培養プロトコルについて説明し、7日間にわたる持続的な外植片の生存率を確立するデータを提示します。代表的な結果は、組織学的GAG染色の亢進とインピンジメントに続発するコラーゲン線維のアライメントの低下を示しており、線維軟骨形成の上昇を示唆しています。このモデルは、さまざまな機械的負荷レジメンの調査に容易に適応でき、インピンジメントに応答してアキレス腱の表現型変化を媒介するメカニズムを特定するために、目的の分子経路を操作することができます。
概要
アキレス腱や回旋筋腱板腱を含む多くの腱は、正常な解剖学的位置により骨のインピンジメントを経験します1,2,3,4.腱の衝突は、縦方向の繊維軸に横方向に向けられた圧縮ひずみを生成します5,6,7.腱インピンジメントの領域は、グリコサミノグリカン(GAG)含量が著しく増加した無秩序なコラーゲンネットワーク内に、縮小した丸い細胞(線維軟骨細胞)が埋め込まれている独特の線維軟骨表現型を示します2,3,4,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24.これまでの研究では、腱のインピンジメントによって生じる異種の機械的環境が、凝集したプロテオグリカン(特にアグリカン)の沈着を促進し、このGAGに富むマトリックスを維持していることが示唆されているが、その根底にあるメカニズムは不明である1,3,12,13,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39.線維軟骨は健康な腱の侵食領域では正常な特徴ですが、過剰な線維軟骨形成に関連する異常なプロテオグリカン代謝は、慢性的に侵迫した腱に不釣り合いに出現する一般的で衰弱性疾患である腱鞘炎の特徴です1,40,41,42,43,44,45,46,47,48,49.したがって、腱インピンジメントは、回旋筋腱板疾患や挿入性アキレス腱炎(IAT)など、最も一般的な腱鞘炎のいくつかを引き起こす重要な外因性要因として臨床的に認識されています50,51,52.現在、腱鞘炎の治療は非効率的です。例えば、IAT患者の約47%は、保存的管理に失敗した後に外科的介入を必要とし、術後の転帰はさまざまである53,54,55,56.インピンジメントと腱鞘炎の間には明らかな関係があるにもかかわらず、インピンジメントされた腱の細胞が機械的環境を感知して応答するメカノバイオロジカルメカニズムは十分に説明されておらず、腱鞘炎の病因の理解が曖昧になり、不十分な治療につながります。
外植モデルは、腱メカノバイオロジーの研究において有用なツールである57,58.腱インピンジメントのメカノバイオロジーを理解するための最初のステップとして、いくつかの先行研究は、細胞または腱外植片を切除した単純な一軸圧迫を適用した後の細胞応答を調査しています27,29,30,31,32,33,34,39。しかし、in vitroの細胞は、菌株伝達を促進し、機械的変形によって放出される重要な成長因子とサイトカインを隔離し、メカノトランスダクションに関与する焦点接着複合体の基質を提供する細胞外および細胞周囲マトリックスを欠いています57,59。さらに、in vitroおよび切除された外植片研究は、in vivoでの腱の衝突によって生成される多軸機械的ひずみ環境を再現することができず、これは衝突領域の解剖学的特徴に依存します5,6。インピンドされたアキレス腱挿入の文脈では、これには、踵骨後滑液包およびケーガー脂肪パッド60,61,62,63などの周囲組織が含まれる。逆に、腱インピンジメントのin vivoモデル25,28,36,37,38,64,65,66は、腱に直接加えられる荷重の大きさと周波数を最小限に制御することを可能にし、これは腱メカノバイオロジーを研究するためのin vivoモデルのよく知られた限界である57,58、67,68,69,70。in vivoでの腱のひずみ測定が困難なため、これらのモデル内で発生する内部ひずみ環境は、多くの場合、十分に特徴付けられていません。
この原稿では、マウス後肢外植片全体の踵骨へのアキレス腱挿入のインピンジメントを再現するカスタム実験プラットフォームを提示し、この組織培養プロトコルと組み合わせると、外植片培養で7日間にわたって生存率を維持し、腱インピンジメントの生物学的後遺症の研究を可能にします。このプラットフォームは、3Dプリントされたポリ乳酸(PLA)ベースに基づいて構築されており、グリップと3DプリントされたPLAボリュームリダクションインサートの取り付けの基礎を提供します。グリップは、後肢の尾側を上に向けて、上肢と膝をアキレス筋腱接合部に近位に固定するために使用され、超音波プローブまたは倒立顕微鏡を使用してアキレス腱を上から画像化できます(図1A)。減容インサートは、ベースのトラックに沿ってスライドし、組織培養培地の必要量を減らします。後ろ足に巻き付けられた編み込みラインは、ベースデザインと3DプリントされたPLAクリップを利用してプラットフォームからルーティングされます。紐を引っ張ることで、後足が背屈し、アキレス腱の挿入が踵骨に押し付けられ、横方向の圧縮歪みが上昇します5,6(図1A)。プラットフォームは、組織培養培地に浸された後肢の外植片を維持するアクリル浴内に含まれています。ピンと張った紐を粘着テープで浴槽の外側に固定すると、足首の背屈が維持され、アキレス腱挿入の静的インピンジメントが発生します。3DプリントされたコンポーネントのCADファイルは、複数のフォーマット(補足ファイル1)で提供されており、実験のニーズに合わせて変更するために、さまざまな商用および無料のオープンソースCADソフトウェアにインポートできます。製造に3Dプリンターを利用できない場合は、CADファイルをオンライン3Dプリントサービスに提供して、低コストで部品をプリントして出荷することができます。
重要なことに、上腕三頭筋-アキレス腱複合体は、膝関節と足首関節の両方にまたがっています71,72,73。その結果、アキレス腱の引張ひずみは膝の屈曲の影響を受けます。膝の伸展はアキレス腱に緊張をかけますが、膝の屈曲は緊張を軽減します。最初に膝を伸ばし、次に足首を受動的に背屈させることで、衝突した挿入時の圧縮ひずみを引張ひずみに重ね合わせることができます。逆に、膝を屈曲させた状態で足首を受動的に背屈させることで、引張ひずみが軽減され、圧縮ひずみが残ります。現在のプロトコルでは、そのような 3 つの条件が検討されています。1)静的インピンジメントの場合、足を脛骨に対して110°<に背屈させて挿入をインピンディングし、膝を曲げて緊張を軽減します。2)ベースラインテンショングループでは、膝を伸ばした状態で足首を背屈145°以上に伸ばし、挿入時に主に引張緊張を発生させます。3)無負荷群の場合、外植片は、外部から負荷がかからない状態で、膝と足首を中立位置にしてペトリ皿で培養します。上記の角度は、足と脛骨が180°の角度で平行で、90°の角度で垂直である座標系に対して写真で測定されます。
プロトコルの主なステップには、1)後肢の外植片の解剖と皮膚と足底腱の慎重な除去が含まれます。2)48時間のデキサメタゾン前処理後の外植片培養。3)組織切片および組織学的染色;4)線維軟骨形成を評価するためのカラー画像解析。解剖後、各後肢外植片をデキサメタゾン74を添加した培地中で48時間前処理する。各マウスの対側肢は、ペアワイズ比較のために別々の実験グループに割り当てられ、生物学的変動を制御するのに役立ちます。前処理後、外植片を上記のようにプラットフォームに配置し、さらに7日間培養します(図1B)。48時間の前処理の直後に外植片を除去する前処理(0日目)グループへの追加の比較が行われます。
外植片培養後、後肢を切り落とし、ホルマリンを固定し、脱灰し、パラフィンに包埋します。矢状方向の連続切片は、筋腱接合部から踵骨挿入までのアキレス腱を視覚化し、腱全体を切片の深さを追跡することができます。末端デオキシヌクレオチジルトランスフェラーゼ(TdT)を介したdUTP X-nickラベリング(TUNEL)は、アポトーシスに続発するDNA損傷を可視化し、生存率を評価するために使用されます。トルイジンブルーの組織学とカスタムカラー画像解析を行い、GAG染色の変化を定量化します。次に、トルイジンブルーで染色した組織切片をSHGイメージングに使用し、コラージュ線維組織の変化を特徴付けます(図1B)。
提供された代表的な結果は、GAGリッチマトリックスの組織学的染色の変化と、モデル内の7日間の静的衝突によって生成された細胞外コラーゲンネットワークの混乱を示唆しています。このモデルは、インピンジメントによる線維軟骨性変化の根底にある分子メカニズムを探るために利用することができます。
プロトコル
すべての動物実験は、ロチェスター大学動物資源委員会によって承認されました。
1. 組織培養培地の調製
- すべての外植片を、1% v/v ペニシリン-ストレプトマイシンと 200 μM L-アスコルビン酸を含む Dulbecco Modified Eagle 培地 (1x DMEM) で、37 °C および 5% CO2 のインキュベーターで培養します。最初の48時間前処理では、100 nMのデキサメタゾン74を添加した70 mLの培地で各外植片を培養します。前処理後、デキサメタゾンなしでさらに7日間培養手足を培養し、48〜72時間ごとに培地を交換します。
注:ウシ胎児血清などの血清を培地に添加することは、Wunderli、Blache、およびSnedeker57によって提供された推奨事項と一致して推奨されません。簡単に言うと、無血清条件は、 生体内に存在する無血管性で栄養価の低い腱微小環境をよりよく表しています。さらに、血清補給は、特定の培養条件下で組織の分解を促進し75 、腱の病理学57の両方の特徴である細胞増殖および組織外への遊走を刺激することができる。 - 荷降ろし群の場合、各外植片を70 mLの培地で培養します。ベースライン張力および静的インピンジメントグループの場合、各プラットフォームでは、四肢を水没させ続けるために約125 mLの培地が必要です。この体積は、グリップにおける上腿の位置と3Dプリントパラメータ(主にインフィル密度)によって変化します。
2.外植片の解剖とデキサメタゾンの前処理
- CO2吸入と二次子宮頸部脱臼によって、または施設のガイドラインに従ってマウスを安楽死させます。このプロトコルは、1歳未満のC57BL/6マウスを利用します。後肢のサイズは年齢とともに大きくなり、グリップに収まるのが難しくなる可能性があります。
- 解剖前に、予熱した(37°C)培地70 mLを、滅菌生物学的安全キャビネット(BSC)内の100 mm(直径)x 25 mm(高さ)のシャーレに移します。デキサメタゾンを添加して、100 nMの使用濃度を達成します。
- 解剖は、吸収性のアンダーパッドを使用してベンチトップで行うことができ、後肢の外植をBSCに移す前に、解剖を迅速に行うことができます。この解剖に必要な手術器具を組み立てます 滑らかでまっすぐで細い先端鉗子を含む。鋸歯状の歯を備えたまっすぐで細い先端鉗子。そしてまっすぐで、鋭く、細かいはさみ。
- 後肢外植片の解剖では、マウスを仰臥位に置き、股関節を特定します。細いハサミを使用して、上肢の近位部と前部(頭蓋部)をオーバーレイする皮膚を小さく(5〜10 mm)切開します。
- 切開部を引き離して拡大し、露出した上肢を指でつまみ、皮膚を遠位に慎重に引っ張って、後肢を足首の高さまで手袋を外します。足の背側に沿って皮膚の下に1枚のハサミの刃をそっと挿入し、つま先まで切開します。皮膚を遠位に引っ張り続けて、完全に取り除きます。
- マウスを配置して、足首近くの踵骨の後部(尾側)へのアキレス腱の挿入を視覚化します。アキレス腱挿入の近位にある足底腱は、アキレス腱の内側境界に直接隣接し、足の足底側に向かって遠位に伸び、踵骨の後側を通過します。
- 足底腱を除去するには、滑らかで細い先端鉗子の1つの先端を2つの腱の間に慎重に挿入し、足底腱の下を通る先端を内側に伸ばします。先端を近位に描き、足底筋を引き裂きます。細い先端の鋸歯状の鉗子を使用して、足底腱の切り離された近位端をつかみ、遠位に引っ張って取り外します。
- 股関節では、細いハサミを使用して骨盤を切り裂き、後肢を分離します。ハサミを使って残りの骨盤をこじ開け、大腿骨頭を露出させます。
- 後肢外植片をBSCに移し、デキサメタゾンを含む細胞培養培地を含むディッシュに移します。皿をインキュベーターに移し、48時間前処理します。
3. 外植片の文化およびローディングのプラットホーム
- 48時間の前処理が終了したら、十分な量の培地を予温します(セクション1)。この時点から、培地にデキサメタゾンは添加されません。この時点で、前処理(0日目)群の四肢を固定、脱灰し、パラフィンに包埋して、将来の切片化、染色、分析を行うことができます。
- 荷を下ろしたグループについては、前処理培地を吸引し、外植片を新鮮なペトリ皿に移し、それぞれ70 mLの培地を加えてインキュベーターに戻します。
- ベースライン張力および静的インピンジメントグループについては、外植片プラットフォームを準備します。グリッププラテンと同じ大きさのサンドペーパーをカットします。静的インピンジメントグループの場合、編組ラインの長さを約18インチカットし、ラインの長さの半分に緩いオーバーハンドノットを事前に結びます。アルミホイルをちぎって各アクリル浴を覆い、70%エタノール(EtOH)をスプレーします。準備をBSCに移します。
- 各プラットフォームには、アクリルバス、ベース、ボリュームリダクションインサート、クリップ、グリップが含まれています。各グリップには、2つのプラテンと、グリップをベースに取り付けるM5 x 0.8 mmのネジ x 長さ10 mmのネジ1本を含む3種類のネジが含まれています。2本のM6 x 1 mmネジ x 20 mmの長さのネジで、プラテンを伸ばしてグリップをクランプします。4本のM3 x 0.5 mmネジ x 長さ14 mmのネジは、4つの圧縮スプリングと組み合わせて、プラテンを引っ込めてグリップを開きます。
- すべての成分を、漏れが発生した場合にすべての培地を捕捉できる二次容器に入れます。10%漂白剤溶液≥浸し、少なくとも1時間浸します。漂白剤溶液を水道水(必要に応じてオートクレーブ)で洗い流し、BSCに移動します。
注意: 汚染のトラブルシューティングについては、すべての水道水をオートクレーブ滅菌するか、精製水を使用することを検討してください。コンタミネーションに対処する際の追加のヒントについては、 ディスカッション を参照してください。 - M3ネジと圧縮スプリングを使用してプラテンをグリップに取り付け、M5ネジを使用してグリップをベースに固定し、プラテンにかみ合うまでM6ネジを挿入します。両面テープでサンドペーパーをプラテンに貼り付け、グリップを閉じてサンドペーパーのプラテンへの接着を促進します。すべてのプラットフォームに対して繰り返します。
- プラットフォームをロードする準備ができたら、グリップを完全に開き、鉗子を使用して、アキレス腱の表層面を上に向けて、上肢と膝をプラテンの間に置きます(図1A)。グリップをゆるく閉じて、ゆっくりと固定します。
- 鉗子を使用して露出した大腿骨頭または足をつかみ、膝の屈曲角度を操作しながら、グリップを徐々に閉じて所定の位置に固定します。ベースライン張力グループでは、前述のように膝関節を伸ばします。膝を伸ばしてグリップが締まると、足首も自然に伸びます。静的インピンジメントグループの場合、前述のようにグリップ間の膝関節を曲げます。
- 静的インピンジメントグループの場合は、ストリングのオーバーハンドノットを遠位足の周りに置き、締めます。外植片の下にあるベースのスロットに弦を通し、クリップ穴に通します。ベースをアクリルバスに入れ、クリップをバスの上端に固定します(図1A)。
- 紐を引いて脛骨に対して足を少なくとも110°に屈させ、クリップから出るときに油性マーカーを使用して紐に印を付けます。この位置で外植片の写真を撮り、後で背屈角度を定量化します(図1A)。
- ベースを取り外し、ベースのトラックに沿ってスライドさせてボリュームリダクションインサートを取り付けます。ベース(ボリュームリダクションインサートに取り付けられている)をアクリルバスに戻し、クリップを上端に再配置します。印を付けた紐を目安に紐を引っ張って元の背屈角度に戻し、紐をテープでお風呂の外側に固定して静的な背屈を維持します。
- ベースラインテンショングループの場合、外植片がグリップの間に配置されたら、ボリュームリダクションインサート付きのベースをアクリルバスに入れ、背屈角度を定量化するための写真を撮るだけです。
- 予熱した(37°C)培地125 mLを各プラットフォームに加え、外植片を浸します。浴槽の上部をアルミホイルで覆い、二次容器に入れ、インキュベーターに移動します。さらに7日間培養し、48〜72時間ごとに培地を交換します。
注意: 浴槽の上部にテープを貼ると、PLA部品が浮くのを防ぐことができます。
4.固定、脱灰、パラフィン包埋
- 外植片培養後、ハサミを使用して足指の爪/遠位足指を切り取り、アキレス筋腱接合部に近位の上肢を切り取ります。トリミングされた各足首関節を、フォーム生検パッドで裏打ちされた処理カセットに入れます。足首をカセットの隅に押し込んで足首を約90°の背屈に置き、カセットを閉じて所定の位置に保持します。
- 10%中性緩衝ホルマリン(NBF)で3日間固定し、氷酢酸でpHを7.4〜7.6に調整した蒸留水(diH2O)に溶解した14%エチレンジアメン四酢酸(EDTA)で2週間脱灰します。
- 塩分を除去するには、サンプルを 1x リン酸緩衝生理食塩水(PBS)の両方で 3 回、続いてジH2O でそれぞれ 5 分間徹底的にすすぎます。パラフィン組織学のルーチンサンプル処理:段階的な一連のEtOHで脱水し、キシレンで透明にし、パラフィンワックスを浸透させます。サンプルをパラフィンに配向して包埋し、以下のセクション5(図1B)で説明するように、アキレス腱を介して矢状組織切片を内側から外側に進行させて取得します。
5. 組織切片化
- ミクロトームを使用して、切片がブロック面と平行になるまでサンプルを慎重にトリミングします。関節の内側から足首に大きくトリミングし、アキレス腱挿入の内側境界に達する前に停止します。
- サンプルを氷の塊に移して温度と水分を調整し、ブレードを交換します(または現在のブレードの新しいセクションにシフトします)。10 μmの厚さでサンプルの切片化を続け、明視野顕微鏡でアキレス腱挿入部への入口を注意深く特定します。特定されたら、アキレス腱の挿入全体を通してセクション番号(つまり、組織の深さ)を連続して追跡します。
6. 脱パラフィン/再水和とスライドの選択
- 以下の各アッセイでは、対側肢の各ペアからレベルが一致した組織切片を選択します。染色する前に、スライドラックに置き、キシレンを3回、100%EtOHを2回、95%EtOHを2回、70%EtOHを1回、それぞれ5分間移動させます。diH2Oで水分補給を終了します。
7.アキレス腱の生存率を評価するためのTUNEL
- TUNELラベリングの場合は、メーカーのプロトコルに従って染色してください。20 μg/mL プロテイナーゼ K 中で室温で 20 分間インキュベートし、diH2O ですすぎ、50 μL の TUNEL 染色液 (5 μL 酵素溶液、45 μL 標識溶液) 中で 37 °C で 1 時間インキュベートします。 DIHPIとカバーガラスを含む褪色防止剤でdiH2O.マウントをすすぎます。
- アキレス腱の挿入を4倍の対物レンズ付き蛍光顕微鏡で撮影します。すべての原子核を可視化するためのDAPIチャンネル(励起/発光波長 = 360/460 nm)、アポトーシス核を可視化するためのTUNEL(TMR Red)チャンネル(励起/発光波長 = 540/580 nm)、および可能であれば明視野チャンネルを含めます。
- 画像解析の場合は、FIJI/ImageJ や MATLAB などの ROI ベースの処理に適した画像解析ソフトウェアに画像をインポートします。アキレス腱全体の概要を示す関心領域(ROI)を定義し(図2A)、解剖や培養時の環境条件の急激な変化によって死に至りやすい上膜の細胞を除外します。
- これを行うには、明視野イメージをインポートし、関数 drawpolygon() を使用して腱の境界をトレースして囲むことで、MATLAB で ROI 選択を実行します。MATLAB は ROI の Polygon オブジェクトを作成し、それを DAPI および TUNEL チャネル イメージに適用して、アキレス腱内の核のみを解析するために createMask() を使用して ROI の外側のピクセル強度データをマスクできます。
- DAPIおよびTUNELチャンネルの画像をインポートし、骨、筋肉、脂肪などの非生存組織におけるアポトーシス核の最大蛍光強度に正規化することにより、アポトーシス(TUNEL+)核を定義するための蛍光強度閾値を特定します。画像がマスクされたら、アキレス腱内のアポトーシス核(TUNEL+核/DAPI核)の割合を計算します。
8.線維軟骨形成を特徴付けるトルイジンブルー組織学
- 再水和したら(セクション6)、外植片の対側の組織切片をレベルマッチしたスライドラックを、氷酢酸を使用してpHを4.0に調整した0.1 M酢酸ナトリウム緩衝液中の0.4%w/vトルイジンブルーOに移します。室温で10分間インキュベートした後、ジH2Oでそれぞれ30秒間3回すすぎます。
- 95% EtOH を 3 回、100% EtOH を 2 回、それぞれ 30 秒ずつ変更して脱水します。キシレンを1分ずつ3回交換してクリアします。キシレンベースの封入剤を使用したカバーガラス。
- アキレス腱挿入の 24 ビット赤青緑 (RGB) カラー画像を取得します。たとえば、このプロトコルでは、アダプタを使用して、デジタルカラーカメラを4倍対物レンズを備えた単純な明視野顕微鏡の接眼レンズにインターフェースします。
- アキレス腱挿入時の圧縮性腱線維軟骨(CTF)16 内のトルイジンブルー染色の違いを定量化するには(図3A、B)、RGB画像を複数のROIを定義および管理できる画像解析ソフトウェアにインポートします。オプションには、FIJI/ImageJ の選択ツールと ROI マネージャー ツール、MATLAB の画像処理ツールボックスなどがあります。まず、ピクセル/長さのスケールを設定します。
注:ソフトウェアの選択は研究者の裁量に委ねられており、MATLABやFIJI/ImageJに限定されるものではありません。著者は、MATLAB コード (補足ファイル 2)、実装を説明するドキュメント (補足ファイル 3)、およびサンプル画像 (補足ファイル 4) を提供しています。研究者には、必要に応じて、または必要に応じて、このコードを他のソフトウェアで使用するために代替プログラミング言語に変換することをお勧めします。 - 選択したソフトウェアに表示された画像を使用して、深部腱の境界と踵骨の交点を特定します。ここから、深部腱境界に沿って近位800μmをトレースし、CTFの深部境界を確立します。たとえば、MATLAB の関数 drawpolyline() を使用して、RGB イメージ上にポリラインを対話的に描画します。MATLAB は、ラインの頂点を含む Polyline オブジェクトを作成し、このオブジェクトを処理して 800 μm の長さにトリミングできます。
- この位置から、局所繊維配向に垂直な表面腱境界に接続する線分を描画して、CTFの近位境界を作成します。
- 深部腱縁と踵骨の交点に戻り、CTFと付着部線維軟骨(AZF)16 を隔てる明確な潮汐マークに沿って表在性腱縁に接続する線分を引いて、CTFの遠位境界を定義します(図3A、B)。最後に、表在性腱境界をなぞって囲むことにより、CTFの表在境界を生成します。
- 挿入部におけるGAG染色の空間的変動を説明するために、総CTFを4象限に分割します(図3A、B)。深いCTF境界と表面CTF境界の中間点を線分で接続して、遠位/近位境界を作成します。この境界の中点を通過して、遠位CTF境界と近位CTF境界の中点を繊維配向に沿って接続し、表面/深部境界を作成します。
- これらの 6 つの境界は、CTF 全体を表す ROI を定義するために使用できる情報を提供しますが、CTF を細分化する 4 つの象限も定義します。たとえば、MATLAB では、個々の ROI (CTF、象限 1 から 4) の境界を定義する頂点をベクトルにコンパイルし、images.roi.Polygon() を使用して各 ROI の囲まれた Polygon オブジェクトを生成します。
- ROIを定義したら、FIJIのカラートランスフォーマープラグイン、MATLABのrgb2hsv()関数、または適切な変換方程式76を適用する他のソフトウェアを使用して、RGBピクセルデータを色相-彩度-値(HSV)色空間に変換する。その後、HSVデータを2Dの色相彩度空間に投影し、色相と彩度の各組み合わせが一意の色をエンコードします(図3C)。
- 各 ROI 内で、ROI の平均染色を表す平均色相と彩度を計算します。これは、たとえば、各 ROI を定義する Polygon オブジェクトを使用して、createMask() を使用してイメージをマスクし、各 ROI 内の色相彩度ピクセル データを具体的に分析することで実現できます。
- 骨膜線維軟骨(PF)16 内に別の小さなROIを定義し(図3A、B)、平均色相と彩度を計算します。次に、CTFの各ROIの平均色をPFの平均色に分離するユークリッド距離を計算します(図3C)。
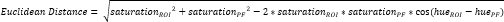
注:ユークリッド距離の計算は、ROIの平均色と典型的な線維軟骨組織であるPFの平均色との類似度を表します16,17,77。ユークリッド距離が小さいほど、ROIの色は外観がより線維軟骨性であることを示します。 - この距離を使用して線維軟骨スコアを計算し、ROI 色が PF 色と同一の場合は最大値を 1 とし、ROI 色と PF 色が色相彩度色空間内で最大間隔に達する場合は最小値を -1 とします。
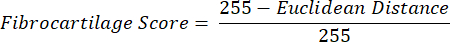
- 色相、彩度、および線維軟骨スコアの平均データは、各四肢の組織切片にわたる各 ROI 内にあります。対側肢のグループ間で対応のある統計的比較を実行します。
9. コラーゲンネットワーク構造の変化を調べるためのSHGイメージング
- 20倍の対物レンズを備えた有能な顕微鏡システムを使用して、トルイジンの青色染色切片のSHGイメージングを実行します。切片の厚さからzスタックを取得し、必要に応じてタイルスキャンを実行して、アキレス腱の挿入を完全にキャプチャします。
- SHG画像を任意の画像解析ソフトウェアにインポートし、セクション8のトルイジンブルー画像解析で説明したように、アキレス腱挿入時のCTFを包含および細分化するROIを定義します(図4A、B)。
- SHG イメージを MATLAB にインポートする場合は、セクション 8 で概説されているように、MATLAB で CTF ROI を定義する方法を使用します。ROI を定義した後、MATLAB から ROI 頂点を .txt ファイルとしてエクスポートし、[ ファイル > インポート > XY 座標] を使用して FIJI にインポートすることで、ROI 座標を FIJI に転送します。選択範囲をオーバーレイし、分析のためにROIマネージャーに送信します。
- コラーゲン組織を定量化するには、フーリエスペクトル解析を実行して、ROIにまたがる小さなウィンドウにわたる繊維配向の分布を計算するFIJIのDirectionalityプラグインを使用します。分散と呼ばれるこの分布の広がりは、ファイバーのアライメントに反比例します。
注:コラーゲン繊維は、アライメント/組織化の欠如ではなく、腱の総湾曲により、CTF全体のさまざまなウィンドウでさまざまな配向をとる場合があります。挿入時の腱の総湾曲とコラーゲン組織の変化をよりよく区別するには、より小さなROIを定義する必要があります。 - SHG画像をFIJIにインポートし、ピクセル/長さのスケールを設定します。最大ピクセル強度データを 2D 合成イメージに投影し、ROI マネージャーに ROI を追加します。各CTF ROIを画像に順次オーバーレイし、ROI内に一貫したサイズの10個の小さなサブROIを描画して、サブROIをROIマネージャーに追加します。
- 各サブROI内で、フィジーで方向性プラグインを実行して、ファイバー分散を計算します。各 CTF ROI 内のサブ ROI 間の平均分散データ、および各エクスプラントのセクションにわたる各 CTF ROI 内の平均分散データ。対側肢のグループ間で対応のある統計的比較を実行します。
結果
TUNELで染色した組織切片の代表的な画像は、実験グループ全体で7日間の外植片培養後のアキレス腱の体内のアポトーシス核が最小であることを示しています(図2A)。これらの画像の定量化により、組織培養プロトコルは、ロード条件全体で 7 日間の外植片培養後、アキレス腱内で平均最大 78% の生存率を維持するという証拠が得られます(図 2B)。
...ディスカッション
この研究で説明した組織培養プロトコルと組み合わせた実験的なマウス後肢外植片プラットフォームは、アキレス腱挿入時のインピンジメント駆動線維軟骨形成のメカノバイオロジーを研究するための適切なモデルを提供します。この外植片モデルの有用性は、7日間の静的衝突後のトルイジン青色染色の有意かつ空間的に不均一な変化に伴う細胞生存率の維持を示す代表的な結果によって実...
開示事項
著者は何も開示していません。
謝辞
著者らは、P30AR06965ロチェスター大学筋骨格研究センターの組織学、生化学、分子イメージング(HBMI)コアのJeff Fox氏とVidya Venkatramani氏による支援と支援に感謝しています。さらに、著者らは、多光子顕微鏡法の支援について、ロチェスター大学医療センターの光学顕微鏡およびナノスコピーセンター(CALMN)に感謝します。この研究は、R01 AR070765 と R01 AR070765-04S1、および 1R35GM147054 と 1R01AR082349 から資金提供を受けました。
資料
| Name | Company | Catalog Number | Comments |
| Absorbent underpads | VWR | 82020-845 | For benchtop dissection |
| Acrylic bath | Source One | X001G46CB1 | Contains the explant platform submerged in culture media |
| Autoclave bin | Thermo Scientific | 13-361-20 | Used as secondary containment, holds two platforms |
| Base | - | - | 3D printed from CAD files provided as Supplementary Files |
| Braided line | KastKing | 30lb test | Used to wrap around paw and apply ankle dorsiflexion |
| Clip | - | - | 3D printed from CAD files provided as Supplementary Files |
| Cover glass | Fisherbrand | 12-541-034 | Rectangular, No. 2, 50 mm x 24 mm |
| Cytoseal XYL | VWR | 8312-4 | Xylene-based mounting media for coverslipping Toluidine blue stained tissue sections |
| Dexamethasone | MP Biomedical LLC | 194561 | CAS#50-02-2 |
| Dimethyl sulfoxide (DMSO), anhydrous | Invitrogen by ThermoFisher | D12345 | CAS#67-68-5, use to solubilize dexamethasone into concentrated stock solutions |
| Double-sided tape | Scotch Brand | 34-8724-5195-9 | To attach sandpaper to Grip platens |
| Dulbecco's Modified Eagle Medium (1X DMEM) | Gibco by ThermoFisher | 11965092 | high glucose, (-) pyruvate, (+) glutamine |
| EDTA tetrasodium salt dihydrate | Thermo Scientific Chemicals | J15700.A1 | CAS#10378-23-1, used to make 14% EDTA solution for sample decalcifcation |
| Ethanol, 200 proof | Thermo Scientific | T038181000 | CAS#64-17-5, 1 L supply |
| Foam biopsy pads | Leica | 3801000 | Used with processing cassettes, help hold ankle joints in desired position during fixation and decalcification |
| Forceps, #SS Standard Inox | Dumont | 11203-23 | Straight, smooth, fine tips |
| Forceps, Micro-Adson 4.75" | Fisherbrand | 13-820-073 | Straight, fine tips with serrated teeth |
| Garnet Sandpaper, 50-D Grit | Norton | M600060 01518 | Or other coarse grit sandpaper |
| Glacial acetic acid | Fisher Chemical | A38S-500 | CAS#64-19-7, for adjusting pH of sodium acetate buffer used for Toluidine blue histology, as well as 14% EDTA decalcification solution |
| Grips | ADMET | GV-100NT-A4 | Stainless steel vice grips, screws and springs described in the protocol are included |
| Histobond Adhesive Microscope Slides | VWR | 16005-108 | Sagittal sections of hind limbs explants reliably adhere to these slides through all staining protocols |
| In situ Cell Death Detection Kit, TMR Red | Roche | 12156792910 | TUNEL assay |
| Labeling tape | Fisherbrand | 15-959 | Or any other labeling tape of preference |
| L-ascorbic acid | Sigma-Aldrich | A4544-100G | CAS#50-81-7, for culture media formulation |
| Neutral buffered formalin, 10% | Leica | 3800600 | For sample fixation, 5 gallon supply |
| Nunc petri dishes | Sigma-Aldrich | P7741-1CS | 100 mm diameter x 25 mm height, maintain explants submerged in 70 mL of culture media as described in protocol |
| Penicillin-streptomycin (100X) | Gibco by ThermoFisher | 15140122 | Add 5 mL to 500 mL 1X DMEM for 1% v/v (1X) working concentration |
| Polylactic acid (PLA) 1.75 mm filament | Hatchbox | - | Choose filament diameter compatible with your 3D printer extruder, in color of choice. |
| Processing cassettes | Leica | 3802631 | For fixation, decalcification and paraffin embedding |
| Prolong Gold Antifade Reagent with DAPI | Invitrogen by ThermoFisher | P36931 | Mounting media for coverslipping tissue sections after TUNEL |
| Proteinase K | Fisher BioReagents | BP1700-50 | CAS#39450-01-6, used for antigen retrieval in TUNEL protocol |
| Scissors, Fine | FST | 14094-11 | Straight, sharp |
| Slide Staining Set, 12-place | Mercedes Scientific | MER 1011 | Rack with 12 stain dishes and slide dippers for Toluidine blue histology |
| Sodium acetate, anhydrous | Thermo Scientific Chemicals | A1318430 | CAS#127-09-3, used to make buffer for Toluidine blue histology |
| Tissue-Tek Accu-Edge Low Profile Microtome Blades | VWR | 25608-964 | For paraffin sectioning |
| Toluidine Blue O | Thermo Scientific Chemicals | 348601000 | CAS#92-31-9 |
| Volume Reduction Insert | - | - | 3D printed from CAD files provided as Supplementary Files |
| Xylenes | Leica | 3803665 | 4 gallon supply for histological staining |
参考文献
- Cook, J. L., Purdam, C. Is compressive load a factor in the development of tendinopathy. Br J Sports Med. 46 (3), 163-168 (2012).
- Benjamin, M., Qin, S., Ralphs, J. R. Fibrocartilage associated with human tendons and their pulleys. J Anat. 187 (Pt 3), 625-633 (1995).
- Benjamin, M., Ralphs, J. R. Fibrocartilage in tendons and ligaments - an adaptation to compressive load. J Anat. 193 (4), 481-494 (1998).
- Benjamin, M., Theobald, P., Suzuki, D., Toumi, H. The anatomy of the Achilles tendon. The Achilles Tendon. 3, 5-16 (2007).
- Chimenti, R. L., et al. Insertional achilles tendinopathy associated with altered transverse compressive and axial tensile strain during ankle dorsiflexion. J Orthop Res. 35 (4), 910-915 (2017).
- Mora, K. E., et al. Ultrasound strain mapping of the mouse Achilles tendon during passive dorsiflexion. J Biomech. 132, 110920 (2022).
- Pringels, L., et al. Intratendinous pressure changes in the Achilles tendon during stretching and eccentric loading: Implications for Achilles tendinopathy. Scand J Med Sci Sports. 33 (5), 619-630 (2023).
- Koob, T. J., Vogel, K. G. Site-related variations in glycosaminoglycan content and swelling properties of bovine flexor tendon. J Orthop Res. 5 (3), 414-424 (1987).
- Vogel, K. G., Koob, T. J. Structural specialization in tendons under compression. Int Rev Cytol. 115, 267-293 (1989).
- Vogel, K. G., Ordög, A., Pogány, G., Oláh, J. Proteoglycans in the compressed region of human tibialis posterior tendon and in ligaments. J Orthop Res. 11 (1), 68-77 (1993).
- Vogel, K. G., Sandy, J. D., Pogány, G., Robbins, J. R. Aggrecan in bovine tendon. Matrix Biol. 14 (2), 171-179 (1994).
- Robbins, J. R., Vogel, K. G. Regional expression of mRNA for proteoglycans and collagen in tendon. Eur J Cell Biol. 64 (2), 264-270 (1994).
- Vogel, K., Gordon, S. I., Blair, S. J., Fine, L. J. . Repetitive motion disorders of the upper extremity. , (1995).
- Benjamin, M., Tyers, R. N., Ralphs, J. R. Age-related changes in tendon fibrocartilage. J Anat. 179, 127-136 (1991).
- Ralphs, J. R., Benjamin, M., Thornett, A. Cell and matrix biology of the suprapatella in the rat: a structural and immunocytochemical study of fibrocartilage in a tendon subject to compression. Anat Rec. 231 (2), 167-177 (1991).
- Rufai, A., Benjamin, M., Ralphs, J. R. Development and ageing of phenotypically distinct fibrocartilages associated with the rat Achilles tendon. Anat Embryol (Berl). 186 (6), 611-618 (1992).
- Rufai, A., Ralphs, J. R., Benjamin, M. Ultrastructure of fibrocartilages at the insertion of the rat Achilles tendon. J Anat. 189 (Pt 1), 185-191 (1996).
- Waggett, A. D., Ralphs, J. R., Kwan, A. P. L., Woodnutt, D., Benjamin, M. Characterization of collagens and proteoglycans at the insertion of the human achilles tendon. Matrix Biol. 16 (8), 457-470 (1998).
- Ralphs, J., et al. Regional differences in cell shape and gap junction expression in rat Achilles tendon: relation to fibrocartilage differentiation. J Anat. 193 (pt 2), 215-222 (1998).
- Milz, S., et al. Three-dimensional reconstructions of the Achilles tendon insertion in man. J Anat. 200 (Pt 2), 145-152 (2002).
- Tischer, T., Milz, S., Maier, M., Schieker, M., Benjamin, M. An immunohistochemical study of the rabbit suprapatella, a sesamoid fibrocartilage in the quadriceps tendon containing aggrecan. J Histochem Cytochem. 50 (7), 955-960 (2002).
- Esquisatto, M. A., Joazeiro, P. P., Pimentel, E. R., Gomes, L. The effect of age on the structure and composition of rat tendon fibrocartilage. Cell Biol Int. 31 (6), 570-577 (2007).
- Matuszewski, P. E., et al. Regional variation in human supraspinatus tendon proteoglycans: Decorin, biglycan, and aggrecan. Connect Tissue Res. 53 (5), 343-348 (2012).
- Buckley, M. R., Huffman, G. R., Iozzo, R. V., Birk, D. E., Soslowsky, L. J. The location-specific role of proteoglycans in the flexor carpi ulnaris tendon. Connect Tissue Res. 54 (6), 367-373 (2013).
- Gillard, G. C., Reilly, H. C., Bell-Booth, P. G., Flint, M. H. The influence of mechanical forces on the glycosaminoglycan content of the rabbit flexor digitorum profundus tendon. Connect Tissue Res. 7 (1), 37-46 (1979).
- Giori, N. J., Beaupre, G. S., Carter, D. R. Cellular shape and pressure may mediate mechanical control of tissue composition in tendons. J Orthop Res. 11 (4), 581-591 (1993).
- Wren, T. A., Beaupré, G. S., Carter, D. R. Mechanobiology of tendon adaptation to compressive loading through fibrocartilaginous metaplasia. J Rehabil Res Dev. 37 (2), 135-143 (2000).
- Malaviya, P., et al. An in vivo model for load-modulated remodeling in the rabbit flexor tendon. J Orthop Res. 18 (1), 116-125 (2000).
- Shim, J. W., Elder, S. H. Influence of Cyclic Hydrostatic Pressure on Fibrocartilaginous Metaplasia of Achilles Tendon Fibroblasts. Biomech Model Mechanobiol. 5 (4), 247-252 (2006).
- Koob, T. J., Clark, P. E., Hernandez, D. J., Thurmond, F. A., Vogel, K. G. Compression loading in vitro regulates proteoglycan synthesis by tendon fibrocartilage. Arch Biochem Biophys. 298 (1), 303-312 (1992).
- Evanko, S. P., Vogel, K. G. Proteoglycan Synthesis in Fetal Tendon Is Differentially Regulated by Cyclic Compression in Vitro. Arch Biochem Biophys. 307 (1), 153-164 (1993).
- Vogel, K. G. The effect of compressive loading on proteoglycan turnover in cultured fetal tendon. Connect Tissue Res. 34 (3), 227-237 (1996).
- Thornton, G. M., et al. Changes in mechanical loading lead to tendon specific alterations in MMP and TIMP expression: influence of stress deprivation and intermittent cyclic hydrostatic compression on rat supraspinatus and Achilles tendons. Br J Sports Med. 44 (10), 698-703 (2010).
- Robbins, J. R., Evanko, S. P., Vogel, K. G. Mechanical Loading and TGF-β Regulate Proteoglycan Synthesis in Tendon. Arch Biochem Biophys. 342 (2), 203-211 (1997).
- Docking, S., Samiric, T., Scase, E., Purdam, C., Cook, J. Relationship between compressive loading and ECM changes in tendons. Muscles Ligaments Tendons J. 3 (1), 7-11 (2013).
- Wang, X., et al. Aberrant TGF-β activation in bone tendon insertion induces enthesopathy-like disease. J Clin Invest. 128 (2), 846-860 (2018).
- Cong, G. T., et al. Evaluating the role of subacromial impingement in rotator cuff tendinopathy: Development and analysis of a novel murine model. J Orthop Res. 36 (10), 2780-2788 (2018).
- Liu, Y., et al. Evaluating the role of subacromial impingement in rotator cuff tendinopathy: development and analysis of a novel rat model. J Shoulder Elbow Surg. 31 (9), 1898-1908 (2022).
- Majima, T., et al. Compressive compared with tensile loading of medial collateral ligament scar in vitro uniquely influences mRNA levels for aggrecan, collagen type II, and collagenase. J Orthop Res. 18 (4), 524-531 (2000).
- Hopkins, C., et al. Critical review on the socio-economic impact of tendinopathy. Asia Pac J Sports Med, Arthrosc, Rehabil Technol. 4, 9-20 (2016).
- Scott, A., Ashe, M. C. Common tendinopathies in the upper and lower extremities. Curr Sports Med Rep. 5 (5), 233-241 (2006).
- Maffulli, N., Wong, J., Almekinders, L. C. Types and epidemiology of tendinopathy. Clin Sports Med. 22 (4), 675-692 (2003).
- Bah, I., et al. Tensile mechanical changes in the Achilles tendon due to Insertional Achilles tendinopathy. J Mech Behav Biomed Mater. 112, 104031 (2020).
- Maffulli, N., Reaper, J., Ewen, S. W. B., Waterston, S. W., Barrass, V. Chondral Metaplasia in Calcific Insertional Tendinopathy of the Achilles Tendon. Clin J Sport Med. 16 (4), 329-334 (2006).
- Corps, A. N., et al. Increased expression of aggrecan and biglycan mRNA in Achilles tendinopathy. Rheumatology (Oxford). 45 (3), 291-294 (2006).
- Scott, A., et al. Increased versican content is associated with tendinosis pathology in the patellar tendon of athletes with jumper's knee. Scand J Med Sci Sports. 18 (4), 427-435 (2008).
- Attia, M., et al. Greater glycosaminoglycan content in human patellar tendon biopsies is associated with more pain and a lower VISA score. Br J Sports Med. 48 (6), 469-475 (2014).
- Kujala, U. M., Sarna, S., Kaprio, J. Cumulative Incidence of Achilles Tendon Rupture and Tendinopathy in Male Former Elite Athletes. Clin J Sport Med. 15 (3), 133-135 (2005).
- Corps, A. N., et al. Changes in matrix protein biochemistry and the expression of mRNA encoding matrix proteins and metalloproteinases in posterior tibialis tendinopathy. Ann Rheum Dis. 71 (5), 746-752 (2012).
- Neer, C. S. Anterior acromioplasty for the chronic impingement syndrome in the shoulder: a preliminary report. J Bone Joint Surg Am. 54 (1), 41-50 (1972).
- Bigliani, L. U., Ticker, J. B., Flatow, E. L., Soslowsky, L. J., Mow, V. C. The relationship of acromial architecture to rotator cuff disease. Clin Sports Med. 10 (4), 823-838 (1991).
- Chimenti, R. L., Cychosz, C. C., Hall, M. M., Phisitkul, P. Current Concepts Review Update Insertional Achilles Tendinopathy. Foot Ankle Int. 38 (10), 1160-1169 (2017).
- Nicholson, C. W., Berlet, G. C., Lee, T. H. Prediction of the Success of Nonoperative Treatment of Insertional Achilles Tendinosis Based on MRI. Foot Ankle Int. 28 (4), 472-477 (2007).
- Lohrer, H., David, S., Nauck, T. Surgical treatment for achilles tendinopathy - a systematic review. BMC musculoskelet disord. 17 (1), 207 (2016).
- McGarvey, W. C., Palumbo, R. C., Baxter, D. E., Leibman, B. D. Insertional Achilles Tendinosis: Surgical Treatment Through a Central Tendon Splitting Approach. Foot Ankle Int. 23 (1), 19-25 (2002).
- Maffulli, N., et al. Surgery for chronic Achilles tendinopathy produces worse results in women. Disabil Rehabil. 30 (20-22), 1714-1720 (1714).
- Wunderli, S. L., Blache, U., Snedeker, J. G. Tendon explant models for physiologically relevant in vitro study of tissue biology - a perspective. Connect Tissue Res. 61 (3-4), 262-277 (2020).
- Dyment, N. A., et al. A brief history of tendon and ligament bioreactors: Impact and future prospects. J Orthop Res. 38 (11), 2318-2330 (2020).
- Screen, H. R. C., Berk, D. E., Kadler, K. E., Ramirez, F., Young, M. F. Tendon Functional Extracellular Matrix. J Orthop Res. 33 (6), 793-799 (2015).
- Theobald, P., et al. The functional anatomy of Kager's fat pad in relation to retrocalcaneal problems and other hindfoot disorders. J Anat. 208 (1), 91-97 (2006).
- Ghazzawi, A., Theobald, P., Pugh, N., Byrne, C., Nokes, L. Quantifying the motion of Kager's fat pad. J Orthop Res. 27 (11), 1457-1460 (2009).
- Malagelada, F., et al. Pressure changes in the Kager fat pad at the extremes of ankle motion suggest a potential role in Achilles tendinopathy. Knee Surg Sports Traumatol Arthrosc. 28 (1), 148-154 (2020).
- Shaw, H. M., Benjamin, M. Structure-function relationships of entheses in relation to mechanical load and exercise. Scand J Med Sci Sports. 17 (4), 303-315 (2007).
- Soslowsky, L. J., et al. Rotator cuff tendinosis in an animal model: role of extrinsic and overuse factors. Ann Biomed Eng. 30 (8), 1057-1063 (2002).
- Schneeberger, A. G., Nyffeler, R. W., Gerber, C. Structural changes of the rotator cuff caused by experimental subacromial impingement in the rat. J Shoulder Elbow Surg. 7 (4), 375-380 (1998).
- Croen, B. J., et al. Chronic subacromial impingement leads to supraspinatus muscle functional and morphological changes: Evaluation in a murine model. J Orthop Res. 39 (10), 2243-2251 (2021).
- Andarawis-Puri, N., Flatow, E. L. Tendon fatigue in response to mechanical loading. J Musculoskelet Neuronal Interact. 11 (2), 106-114 (2011).
- Gains, C. C., Giannapoulos, A., Zamboulis, D. E., Lopez-Tremoleda, J., Screen, H. R. C. Development and application of a novel in vivo overload model of the Achilles tendon in rat. J Biomech. 151, 111546 (2023).
- Williamson, P. M., et al. A passive ankle dorsiflexion testing system to assess mechanobiological and structural response to cyclic loading in rat Achilles tendon. J Biomech. 156, 111664 (2023).
- Pedaprolu, K., Szczesny, S. E. A Novel, Open-Source, Low-Cost Bioreactor for Load-Controlled Cyclic Loading of Tendon Explants. J Biomech Eng. 144 (8), 084505 (2022).
- Orishimo, K. F., et al. Effect of Knee Flexion Angle on Achilles Tendon Force and Ankle Joint Plantarflexion Moment During Passive Dorsiflexion. J Foot Ankle Surg. 47 (1), 34-39 (2008).
- Liu, C. L., et al. Influence of different knee and ankle ranges of motion on the elasticity of triceps surae muscles, Achilles tendon, and plantar fascia. Sci Rep. 10 (1), 6643 (2020).
- Cruz-Montecinos, C., et al. Soleus muscle and Achilles tendon compressive stiffness is related to knee and ankle positioning. J Electromyogr Kinesiol. 66, 102698 (2022).
- Connizzo, B. K., Grodzinsky, A. J. Lose-dose administration of dexamethasone is beneficial in preventing secondary tendon damage in a stress-deprived joint injury explant model. J Orthop Res. 38 (1), 139-149 (2020).
- Wunderli, S. L., et al. Tendon response to matrix unloading is determined by the patho-physiological niche. Matrix Biol. 89, 11-26 (2020).
- Yabusaki, K., et al. A Novel Quantitative Approach for Eliminating Sample-To-Sample Variation Using a Hue Saturation Value Analysis Program. PloS one. 9 (3), e89627 (2014).
- Gao, J., Messner, K., Ralphs, J. R., Benjamin, M. An immunohistochemical study of enthesis development in the medial collateral ligament of the rat knee joint. Anat Embryol. 194 (4), 399-406 (1996).
- Han, S. K., Wouters, W. A. J., Clark, A., Herzog, W. Mechanically induced calcium signaling in chondrocytes in situ. J Orthop Res. 30 (3), 475-481 (2012).
- Han, W., et al. Impact of cellular microenvironment and mechanical perturbation on calcium signalling in meniscus fibrochondrocytes. Eur Cell Mater. 27, 321-331 (2014).
- Rossetti, L., et al. The microstructure and micromechanics of the tendon-bone insertion. Nat Mater. 16 (6), 664-670 (2017).
- Sartori, J., Köhring, S., Witte, H., Fischer, M. S., Löffler, M. Three-dimensional imaging of the fibrous microstructure of Achilles tendon entheses in Mus musculus. J Anat. 233 (3), 370-380 (2018).
- Eliasberg, C. D., et al. Identification of Inflammatory Mediators in Tendinopathy Using a Murine Subacromial Impingement Model. J Orthop Res. 37 (12), 2575-2582 (2019).
- Zhang, Y., et al. Expression of alarmins in a murine rotator cuff tendinopathy model. J Orthop Res. 38 (11), 2513-2520 (2020).
- Zhang, X., et al. Assessment of Mitochondrial Dysfunction in a Murine Model of Supraspinatus Tendinopathy. J Bone Joint Surg. Am. 103 (2), 174-183 (2021).
- Liu, Y., et al. The role of Indian Hedgehog Signaling in tendon response to subacromial impingement: evaluation using a mouse model. Am J Sports Med. 50 (2), 362-370 (2022).
- Wang, T., et al. Load-induced regulation of tendon homeostasis by SPARC, a genetic predisposition factor for tendon and ligament injuries. Sci Transl Med. 13 (582), eabe5738 (2021).
- Passini, F. S., et al. Shear-stress sensing by PIEZO1 regulates tendon stiffness in rodents and influences jumping performance in humans. Nat Biomed Eng. 5 (12), 1457-1471 (2021).
- Jones, D. L., et al. Mechanoepigenetic regulation of extracellular matrix homeostasis via Yap and Taz. Proc Natl Acad Sci U S A. 120 (22), e2211947120 (2023).
- Connizzo, B. K., Grodzinsky, A. J. Release of pro-inflammatory cytokines from muscle and bone causes tenocyte death in a novel rotator cuff in vitro explant culture model. Connect Tissue Res. 59 (5), 423-436 (2018).
- Rees, S. G., et al. Catabolism of aggrecan, decorin and biglycan in tendon. Biochem J. 350 (Pt 1), 181-188 (2000).
- Samiric, T., Ilic, M. Z., Handley, C. J. Large aggregating and small leucine-rich proteoglycans are degraded by different pathways and at different rates in tendon. Eur J Biochem. 271 (17), 3612-3620 (2004).
- Rees, S. G., Curtis, C. L., Dent, C. M., Caterson, B. Catabolism of aggrecan proteoglycan aggregate components in short-term explant cultures of tendon. Matrix Biol. 24 (3), 219-231 (2005).
- Taye, N., Karoulias, S. Z., Hubmacher, D. The "other" 15-40%: The Role of Non-Collagenous Extracellular Matrix Proteins and Minor Collagens in Tendon. J Orthop Res. 38 (1), 23-35 (2020).
- Carvalho, H. F., Felisbino, S. L. The development of the pressure-bearing tendon of the bullfrog, Rana catesbeiana. Anat Embryol. 200 (1), 55-64 (1999).
- Carvalho, H. F., Felisbino, S. L., Covizi, D. Z., Della Colleta, H. H., Gomes, L. Structure and proteoglycan composition of specialized regions of the elastic tendon of the chicken wing. Cell Tissue Res. 300 (3), 435-446 (2000).
- van Sterkenburg, M. N., Kerkhoffs, G. M., Kleipool, R. P., Niek van Dijk, C. The plantaris tendon and a potential role in mid-portion Achilles tendinopathy: an observational anatomical study. J Anat. 218 (3), 336-341 (2011).
- Lee, A. H., Elliott, D. M. Comparative multi-scale hierarchical structure of the tail, plantaris, and Achilles tendons in the rat. J Anat. 234 (2), 252-262 (2019).
- Lee, A. H., Elliott, D. M. Multi-Scale Loading and Damage Mechanisms of Plantaris and Rat Tail Tendons. J Orthop Res. 37 (8), 1827-1837 (2019).
- Fan, H. M., Shrestha, L., Guo, Y., Tao, H. R., Sun, Y. L. The twisted structure of the rat Achilles tendon. J Anat. 239 (5), 1134-1140 (2021).
- Cutlip, R. G., Stauber, W. T., Willison, R. H., McIntosh, T. A., Means, K. H. Dynamometer for rat plantar flexor muscles in vivo. Med Biol Eng Comput. 35 (5), 540-543 (1997).
- Rijkelijkhuizen, J. M., Baan, G. C., de Haan, A., de Ruiter, C. J., Huijing, P. A. Extramuscular myofascial force transmission for in situ rat medial gastrocnemius and plantaris muscles in progressive stages of dissection. J Exp Biol. 208 (Pt 1), 129-140 (2005).
- Saxena, A., Bareither, D. Magnetic Resonance and Cadaveric Findings of the Incidence of Plantaris Tendon. Foot Ankle Int. 21 (7), 570-572 (2000).
- dos Santos, M. A., Bertelli, J. A., Kechele, P. R., Duarte, H. Anatomical study of the plantaris tendon: reliability as a tendo-osseous graft. Surg Radiol Anat. 31 (1), 59-61 (2009).
- Sartori, J., Köhring, S., Bruns, S., Moosmann, J., Hammel, J. U. Gaining Insight into the Deformation of Achilles Tendon Entheses in Mice. Adv Eng Mater. 23 (11), 2100085 (2021).
転載および許可
このJoVE論文のテキスト又は図を再利用するための許可を申請します
許可を申請さらに記事を探す
This article has been published
Video Coming Soon
Copyright © 2023 MyJoVE Corporation. All rights reserved