Method Article
Um Supramolecular hidrogel injetável e carregado com a droga para a injeção local por cateter no coração de porco
* Estes autores contribuíram igualmente
Neste Artigo
Resumo
Hydrogelators supramoleculares baseados em ureido-pirimidinonas permitir o controle total sobre as propriedades do gel macroscópicas e o comportamento de comutação sol-gel utilizando pH. Aqui, apresentamos um protocolo para a formulação e injetando um hydrogelator tais supramolecular através de um sistema de entrega de cateter para entrega local diretamente em áreas relevantes no coração de porco.
Resumo
Regeneração do miocárdio perdido é uma meta importante para as terapias futuras, devido à crescente ocorrência de insuficiência cardíaca isquêmica crônica eo acesso limitado aos corações dos doadores. Um exemplo de um tratamento para recuperar a função do coração consiste da entrega local de drogas e bioactivos a partir de um hidrogel. Neste trabalho um método é introduzido para formular e injetar um hidrogel carregado de drogas não-invasiva e no coração de porco usando um cateter longo e flexível específicos de lado. O uso de 3-D mapeamento electromecânico e a injecção através de um cateter permite um tratamento específico do lado do miocárdio. Para proporcionar um hidrogel compatível com este cateter, um hidrogel supramolecular é usado por causa da comutação conveniente a partir de um gel para um estado de solução utilizando gatilhos ambientais. Poli A pH básico desta ureido-pirimidinona modificado (etileno-glicol) actua como um fluido newtoniano, que pode ser facilmente injectada, a pH fisiológico, mas a solução muda rapidamente emum gel. Estes estados de comutação moderadas permitir a incorporação de drogas bioactivos e espécies bioactivas, tais como factores de crescimento e os exossomas como apresentamos aqui em ambos in vitro e in vivo. As experiências in vitro em dar uma indicação do golpe da estabilidade do gel e a libertação do fármaco, o que permite o ajuste do gel e propriedades de libertação antes da aplicação subsequente in vivo. Esta combinação permite o ajuste óptimo do gel para os compostos bioactivos e utilizados espécies, e o sistema de injecção.
Introdução
Embora o tratamento do infarto agudo do miocárdio tem melhorado significativamente as taxas de sobrevivência, a insuficiência cardíaca isquêmica crônica é um importante problema de saúde pública, que evolui com o envelhecimento da população. Há aproximadamente 6 milhões de pacientes com insuficiência cardíaca em os EUA com um aumento estimado de 25% na prevalência em 2030 1,2. Perda inicial de tecido do miocárdio leva à remodelação cardíaca e, eventualmente, provoca insuficiência cardíaca crônica. Excepto para o transplante de coração, não há nenhum tratamento real para este grupo de doentes. A lacuna crescente de corações doados enfatiza a necessidade de desenvolver novas terapias disponíveis para reverter esse processo de remodelação. Portanto, uma meta para futuras terapias é a regeneração do miocárdio perdido.
Os hidrogeles são materiais de interesse no campo da medicina regenerativa devido à sua biocompatibilidade, e a sua sensibilidade aos disparadores 3 externos. Hidrogéis oferecem injetáveis anúnciovantages mais de hidrogéis não-injetáveis na sua utilização em cirurgia minimamente invasiva 4. Estes hidrogéis injectáveis pode ser aplicada através de uma seringa por causa da sua switchability dentro condições fisiológicas 5, e, em princípio, permitir a injecção à base de cateter se aproxima 6. Várias estratégias têm sido utilizadas para materiais injectáveis, variando de reticulação química após a injecção de reticulação física, quer por temperatura, pH e 4,7,8 comportamento de pseudoplasticidade. Embora vários sistemas têm mostrado de fácil injectabilidade através de uma seringa 9,10, cheio cateter-compatibilidade não tem sido demonstrado 6 vezes.
Os hidrogeles preparados a partir de polímeros supramoleculares são formados por interacções não-covalentes, que podem ser comutadas convenientemente a partir de um gel a uma solução do estado, e vice-versa, utilizando accionadores 11 ambiental. Além disso, os precursores de baixo peso molecular permitem a fácil 12,13 processabilidade . As condições suaves necessários para interrupção permite a adição de vários componentes biológicos activos, tais como muitas vezes difícil de lidar com factores de crescimento.
Redes transitórias supramoleculares em água à base de poli (etileno glicol) (PEG), em fim modificada com ureido-pirimidinona (UPy) porções de 14 mostraram os benefícios de interacções não-covalentes em combinação com aplicações biomédicas e têm sido utilizados como sistema de entrega de droga no coração e 6 sob a cápsula renal 15. Estas redes formam-se por dimerização dos UPy grupos protegidos a partir do meio aquoso por meio de espaçadores de alquilo, formando uma bolsa hidrofóbica. Ligação de hidrogénio ureia facilita o empilhamento subsequente destes dímeros em nanofibras. Devido à interacção reversível do dímero UPy-UPy, desencadeia tais como o pH e temperatura podem ser utilizados para exibir a partir de soluções de géis. O uso de um motivo sintética permite a criação das propriedades da molécula e por gel para examecomprimento sintonia PLE do PEG-correntes e espaçadores alquilo 14,16.
Além disso, vários componentes bioactivos podem ser incorporados por simples mistura da solução hydrogelator supramolecular antes da injecção, com drogas ou espécies bioactivas, tais como factores de crescimento ou de exossomas, respectivamente. Os exossomas são pequenas vesículas de membrana que contêm derivados citosólicas. Eles são segregadas por muitas células e estão envolvidos na comunicação intercelular. Os exossomas provenientes de células progenitoras de cardiomiócitos são sugerido para desempenhar um papel na protecção cardíaca 17.
Aqui, nós descrevemos o protocolo de formulação, e no miocárdio injecção in vivo de um hidrogel tal supramolecular bioactivo. Em experiências in vitro, que são descritos em forehand dar uma indicação da estabilidade do gel e a libertação do fármaco, o que permite o ajuste do gel e propriedades de libertação antes aplicação in vivo.
Protocolo
NOTA: Todos os experimentos in vivo foram conduzidos de acordo com o Guia para o Cuidado e Uso de Animais de Laboratório do Institute of Laboratory Animal Resources. Os experimentos foram aprovados pelo Comitê de Experimentação Animal da Faculdade de Medicina da Universidade de Utrecht, na Holanda.
1. Formulação do hidrogel
- Para preparar 1 mL de gel de 10% em peso, dissolve-se 100 mg do UPy-hydrogelator num frasco em 900 ul de PBS pH 11,7 por agitação a 70 ° C durante 1 hora utilizando um agitador magnético. Depois arrefece-se a solução viscosa até à temperatura ambiente. A solução agora deve ter um pH de aproximadamente 9,0. Esta solução pode ser armazenada durante vários dias.
- Pipetar a quantidade apropriada de droga ou de biomoléculas que é dissolvido em PBS neutro na solução viscosa e agitou-se durante 10 min para atingir uma distribuição uniforme. Se a solução torna-se muito viscoso, pouco aquecê-lo com água quente.
- Coloque a solução durante 1 hora sob uma lâmpada UV para esterilizar.
2. Análise do Hidrogel
- Avaliação reológico da solução
- Antes de carregar o gel, a montagem 25 milímetros geometria placa-placa no reómetro, ajustar a temperatura para 20 ° C e carregar a placa com água para evitar a evaporação do gel durante a medição.
- Pipete 300 pi da solução de 25 mm para geometria da placa-placa por um reómetro mantida a 20 ° C e inferiores das placas para obter uma distância de folga de 0,5 mm.
- Viscosidade de corte recorde em função da tensão de cisalhamento 0,1-500 Pa com 10 pontos por década.
- Avaliação reológica do gel
- Pipetar 300 ul da solução na placa e pipetar um total de 4,2 mL de 1 M de HCl em locais diferentes na solução de induzir a formação de gel.
- Diminuir as placas a uma distância de folga de 0,5 mm e deixe a cura de gel para cerca de 30 min. Durante este processo de cura, medir o armazenamento e perda de módulos em baixa freqüência e tensão, por exemplo, respectivamente, 1 rad / seg e 0,5%.
- Depois que o gel tem curado (após cerca de 30 min) módulos, de armazenamento de registros e perdas em função da frequência (0,1-100 rad / seg) e, posteriormente, em função da tensão (0.1-1,000%).
3. Erosão e lançamento Experiments
- Transferir 100 ul da solução viscosa que contém o fármaco ou uma biomolécula em poli (tereftalato de etileno) inserção de cultura de células de suspensão de 24-poços de placas com tamanho de poro de 8,0 um. Para prevenir fugas da solução de polímero, enquanto na fase líquida, cobrir o fundo das inserções com Parafilm (Figura 2A).
- Imediatamente depois pipeta 1,4 ul de 1 M de HCl em cima da solução viscosa para reduzir o pH para cerca de 7,0-7,2 e deixar a curar o gel dentro da pastilha de cerca de 30 min.
- Remova o Parafilm from as inserções, colocar o inserto numa placa de 24 poços e encher o poço com 800 ul de PBS, pH 7,4. Incubar a placa a 37 ° C com agitação lenta ou movimento de agitação. Para evitar a evaporação do solvente, preencher vazios restantes poços com PBS e selar a placa de 24 poços com Parafilm (Figura 2B).
- Periodicamente atualize a PBS e analisar a PBS removido para lançado produto erosão UPy ou droga / biomolécula.
- Quantificar produtos de erosão UPy pirfenidona ou por medição da absorvância de UV a 265 nm ou 320 nm, respectivamente. Para a proteína fluorescente medida mRuby2 emissão de fluorescência a 587 nm após excitação a 559 nm.
- Traduzir valores de absorção / emissão medidos a concentrações através de curvas de calibração predeterminados.
- Preparar curvas de calibração para dissolução de uma série de concentrações conhecidas do analito em tampão e medir a absorvância de UV ou emissão fluorescente dessas amostras. Interpolar os dados utilizando uma função linear para detarminho a concentração das amostras desconhecidas. Para as proteínas não fluorescentes utilizar a detecção ELISA 6.
4. injeção local por meio de um cateter
- A indução do infarto do miocárdio
- Após 12 horas de jejum, excluindo a água, sedar o porco em seu estábulo, injetando midazolam 0,4 mg / kg, cetamina 10 mg / kg e atropina 0,014 mg / kg por via intramuscular.
- Administrar tiopental sódico 5 mg / kg por via intravenosa para induzir a anestesia e intubação o porco com um tubo endotraqueal. Execute balão-ventilação a uma taxa de 12 / min, se necessário durante o transporte do animal para a sala de operação.
- Na chegada ao teatro operação começar imediatamente a ventilação mecânica com pressão positiva FiO 2 de 0,50, 10 ml / kg de volume corrente e uma frequência de 12 / min sob capnografia contínua. Use veterinário pomada sobre os olhos para prevenir o ressecamento.
- Iniciar a anestesia balanceada por intraven contínuaous infusão de midazolam 0,5 mg / kg / h, sufentanil 2,5 ug / kg / h e o brometo de pancurónio 0,1 mg / kg / h. Para assegurar a anestesia adequada monitorizar continuamente o ECG, pressão sanguínea arterial, temperatura e capnografia.
- Infundir por via intravenosa de 4,3 mg / kg de amiodarona e colocar o cateter intracardíaca desfibrilação no ventrículo direito usando o Sheeth venosa 18.
- Ocluir a artéria distal descendente anterior esquerda (LAD) para o segundo ramo diagonal pela oclusão do balão intracoronário, durante 90 minutos, de acordo com o protocolo descrito anteriormente 18.
- Mapeamento eletromecânico
- Às quatro semanas após o infarto do miocárdio, planejar o procedimento de mapeamento. Prepara-se o sistema (Figura 4) no cathlab para mapeamento eletromecânico 3D (EMM) do ventrículo esquerdo. Com este sistema de miocárdio viável, hibernando e infartado podem ser identificados sem orientação fluoroscópica. Para construir um mapa-EM tal adquirir um series de pontos em vários locais na superfície endocárdica do VE usando uma fonte de energia do campo magnético ultralow e um cateter com ponta de sensor de 19,20.
- Anestesiar o porco, seguindo o protocolo passos 4.1.1-4.1.4.
- Coloque o patch referência externa na parte traseira do porco.
- Fixe o acesso vascular (artéria femoral) de acordo com o protocolo 18.
- Após a obtenção de um biplano deixou angiograma ventricular no 25 ° oblíqua anterior direita (RAO) e 40 ° esquerda oblíqua anterior (LA) para estimar o tamanho do ventrículo esquerdo, dar 75 U / kg de heparina.
- Avance um 8 Francês-mapping (D ou F curva) cateter sob orientação fluoroscópica à aorta descendente, do arco aórtico e através da válvula aórtica no ventrículo esquerdo (VE).
- Orientar a ponta do cateter para o ápice do VE para adquirir os primeiros dados, seguido por via de saída, lateral e posterior pontos para formar uma silhueta 3D, que define as fronteiras do Ventricle.
- Obter pontos subseqüentes, até que todos os segmentos do endocárdio foram amostrados, arrastando o cateter de mapeamento sobre o endocárdio e aquisição sequencialmente a localização da ponta, enquanto em contacto com o endocárdio 21,22.
- Definir a área de alvo, que é onde a actividade eléctrica é (quase) o movimento normal e prejudicada mecânica, denominada miocárdio em hibernação (Figura 6).
- A injeção
- Substituir o cateter de mapeamento do cateter por injecção intramiocardial que é composto de uma agulha de calibre 27 e um núcleo dentro de um lúmen do cateter Francês 8 (Figura 5A e B). Para distribuir quantidades específicas, carregar uma seringa graduada em volume com cerca de 2 ml de solução de hidrogel e colocá-lo em uma bomba de seringa.
- Ajustar a extensão de agulha, a 0 ° e 90 ° flex e colocar 0,1 ml da solução de hidrogel para encher a agulha do espaço morto. Em seguida, coloque oponta do cateter de injecção através da válvula aórtica e para a área de destino.
- Seguir os seguintes critérios para uma posição de injecção dentro da área do alvo determinado em 4.2.9: (1) posição perpendicular do cateter à parede do VE; (2) uma estabilidade excelente ciclo (<4 mm) como calculado pelo sistema de EMM; e (3) tensão subjacente> 6,9 mV 21.
- Avançar a agulha no miocárdio, (4) confirmada por uma contracção ventricular prematura do VE, e injectar 0,1-0,3 ml do hidrogel na forma de bolus, a uma taxa constante de cerca de 0,4-0,5 ml / min usando a bomba de seringa. Repita este em 6-10 posições diferentes quanto difuso quanto possível. O pH natural do tecido irá neutralizar a solução após a injecção, em que o hidrogel é formado.
- Sacrifício
- Pós-procedimento, humanamente sacrificar o animal por sangria. Corte a veia cava inferior e remover o sangue com um dispositivo de sucção. Induzir fi ventricularfibrilação colocando uma bateria de 9 V no ápice.
Resultados
Os resultados típicos obtidos a partir das medições reológicas oscilatórias em ambas a solução e o gel são mostradas na Figura 1. Para a injecção através de um cateter longo, um fluido Newtoniano com baixa viscosidade é desejável. A viscosidade foi medida como função da velocidade de corte, que mostra que a pH 8,5, a solução é adelgaçamento do esforço transverso, mas a pH 9,0 e 9,5 as soluções se comportam como líquidos Newtonianos como evidenciado pela viscosidade constante de 0,54 e 0,36 Pa · s, respectivamente (Figura 1A) . Depois de se neutralizar as amostras, as amostras mostram uma resposta do tipo sólido observada por um módulo de armazenamento G 'que é maior do que o módulo de perda G "e, por conseguinte, um tanδ = G" / G' <1 (Figura 1B). O gel obtém sua resistência final dentro de 30 minutos. Oscilatórios medidas reológicas mostram uma resposta sólida-like típico com G 'quase independente da freq angularuency e G '> G "para todas as frequências de medição (Figura 1C).
Essencial para a utilização como sistema de entrega de drogas é a erosão do hidrogel ao longo do tempo. As interacções supramoleculares são inerentemente dinâmico e para permitir uma erosão lenta do gel in vitro. Experimentos de erosão e liberação são realizados a 37 ° C usando inserções bem porosas (Figura 2A e B). Ao ajustar o comprimento do bloco hidrofóbico e hidrofilico 14, um gel que corrói ao longo de um período de várias semanas, podem ser obtidos (Figura 3A). O gel corrói a 25% em 2 semanas com uma erosão inicial de 10% no primeiro dia, presumivelmente devido ao inchaço inicial do hidrogel. Como exemplo, tanto a libertação de uma droga de moléculas pequenas (pirfenidona), e a libertação de uma proteína modelo fluorescente (mRuby2) foi estudada. Uma proteína fluorescente modelo permite uma leitura fácil; No entanto, in vitro Experiências de libertação também pode ser realizada em outras proteínas utilizando ELISA para quantificação 6. A droga de moléculas pequenas é libertado dentro de um dia, enquanto que as moléculas maiores tais como proteínas são libertadas gradualmente ao longo de 1 semana (Figura 3B). Montagem do perfil de libertação de mRuby2 até 60% com o lançamento do modelo Korsmeyer-Peppas semi-empírica indica libertação devido à difusão (n = 0,44) 23. A ausência de um deslocamento no (adaptado) modelo Korsmeyer-Peppas mostra que não há explosão liberação presente para mRuby2 24. Devido à quantidade limitada de pontos de dados com uma libertação inferior a 60% para pirfenidona, nenhuma adaptação foi realizada sobre este perfil de libertação.
O sistema de navegação do cateter é constituído por uma consola de unidade de comunicação, uma estação de trabalho (Figura 4), um bloco de localização triangular (que geram um campo magnético de baixo) com um remendo de referência externo e dois cateteres, o mapeamento com ponta de sensor e o injection cateter (Figura 5).
Após a análise pós-processamento foi filtrada pontos instáveis da reconstrução 3D do endocárdio do VE é atualizado em tempo real, com a aquisição de cada novo ponto de dados e é exibido continuamente como potenciais de tensão unipolar e bipolar em uma escala de cor graduada (Figura 6A). A função encurtamento linear local (LLS) quantifica movimentação parietal regional através da obtenção da variação média de distância entre o local de amostra e pontos adjacentes no final da sístole e diástole final. Os valores médios de tensão e LLS são calculados para cada segmento e exibidos no mapa polar. (Figura 6B). A presença de um potencial de anormal ou baixo unipolar (≤6 mV) e atividade mecânica diminuída (LLS ≤4%) caracteriza áreas infartadas 22.
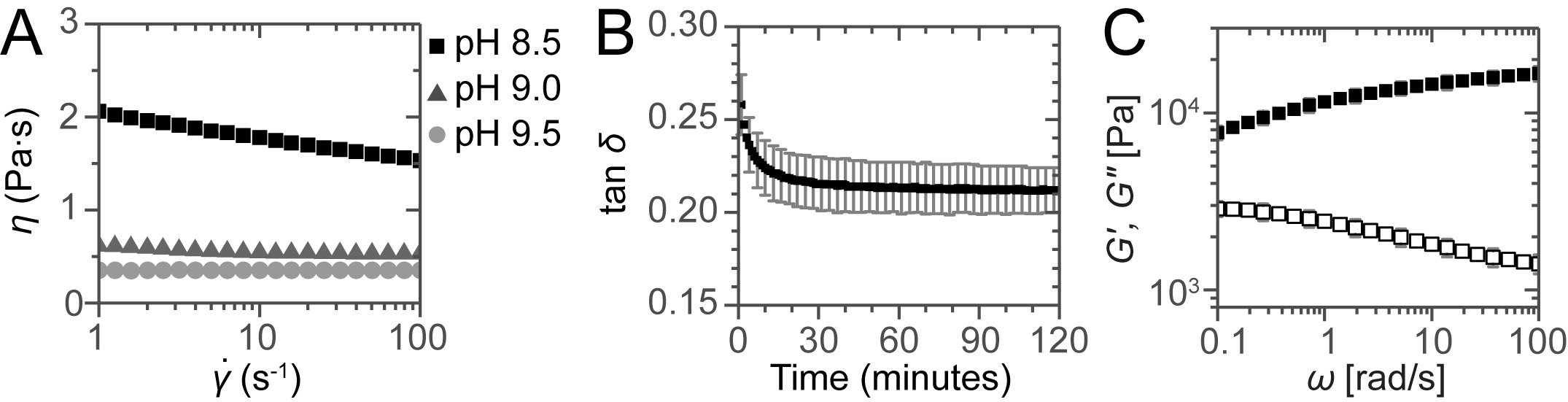
A Figura 1 :. avaliação reológica das soluções e géis. (A) A viscosidade como uma função da taxa de cisalhamento para as soluções com um pH diferente. Para a amostra a pH 8,5 de cisalhamento desbaste mas é observada para as amostras a pH 9,0 e 9,5 viscosidades constantes são obtidos, mostrando o comportamento newtoniano das soluções. De cura (B) em gel seguida representando graficamente tan δ como uma função do tempo. Sweep (C) Freqüência para uma amostra neutralizada depois de 2 horas de cura. As barras de erro mostram os desvios-padrão de três medições independentes, indicando um erro experimental típico.

Figura 2:. Configuração para degradação e liberam experimentos (A) poli (tereftalato de etileno) bem insert cobertas com Parafilm para evitar fugas during preparação. (B) 24-poços de placa com pastilhas, embrulhado com Parafilm para evitar a evaporação do solvente.

Figura 3:. Erosão e Release (A) Erosão do hidrogel ao longo do tempo. Erosão gradual do gel durante pelo menos 2 semanas é observada. (B) Libertação de uma molécula de fármaco pequena e uma proteína modelo. Embora a molécula pequena é libertado dentro de um dia, a proteína modelo é gradualmente libertado ao longo de uma semana, sem uma libertação significativa de ruptura. A linha mostra o ajuste do modelo Korsmeyer-Peppas para a fase inicial da libertação.

Figura 4: O sistema de navegação do cateter. consola unidade de comunicação com NOGA XP Cardiac Sistema de Navegação.
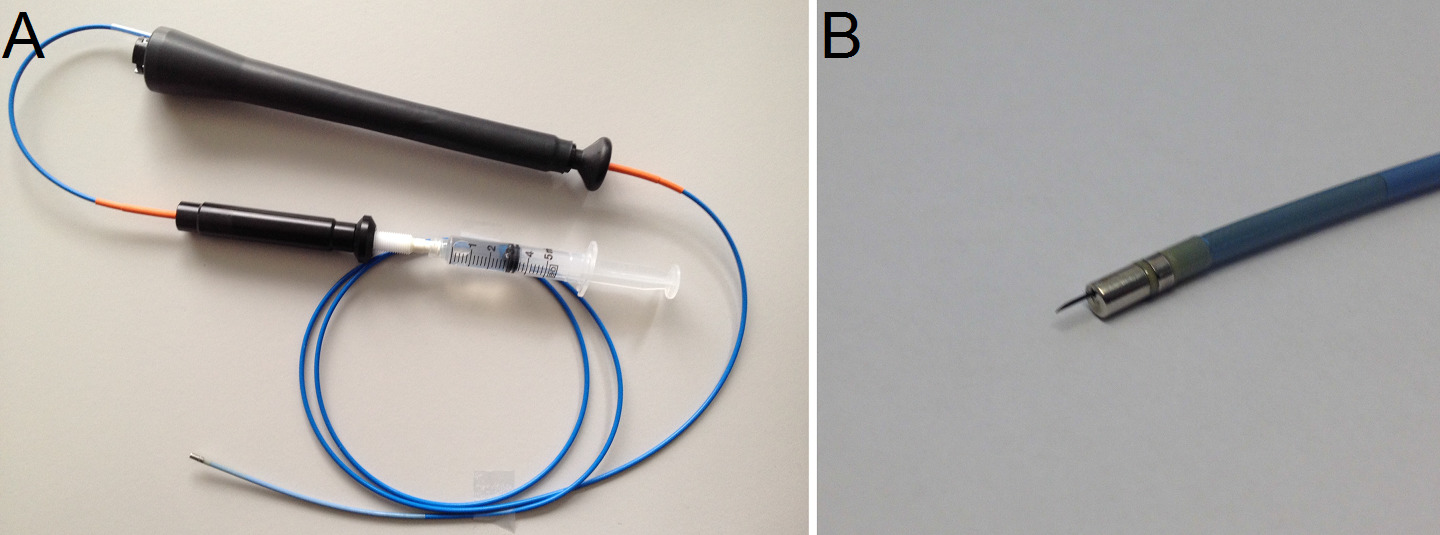
Figura 5: (A) o cateter de injecção com seringa ligada intramiocardial. (B) Detalhe da agulha de injeção.
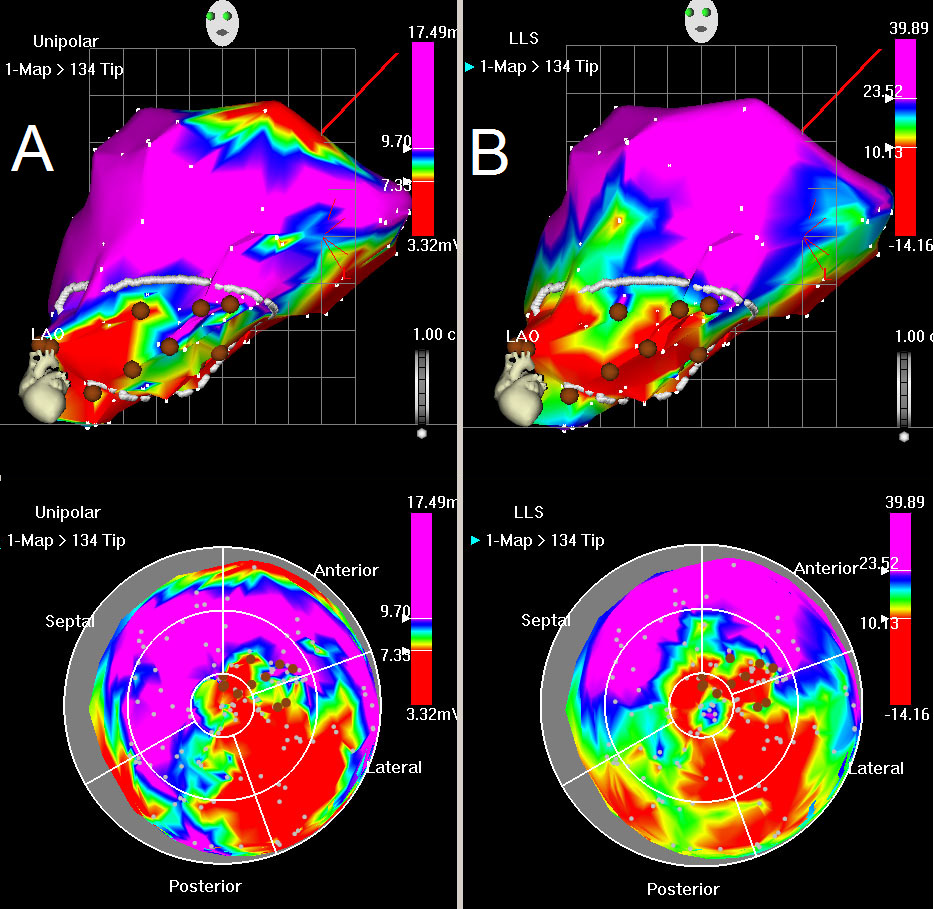
Figura 6: tensão unipolar e mapa LLS. (A) mapa unipolar, vista LAO (topo) e olho de touros (abaixo). A cor vermelha indica valores de baixa tensão unipolar na base do miocárdio (normal), com perda de póstero atividade elétrica. Azul indica miocárdio normal, embora as cores verdes e amarelas indicam diminuição da viabilidade. (B) Mapa de LLS, vista LAO (topo) e olho de touros (abaixo). Cor vermelha indicates akinesia na parede póstero, verde e amarelo indicam diminuição do movimento da parede. Os pontos de mapeamento estão apresentados por pontos brancos. A linha branca desenhada mostra a área de interesse, caracterizado por tensões diminuíram unipolares e propostas de parede com deficiência. Pontos marrons representam os locais de injecção.
Discussão
Um desafio chave é a obtenção de uma solução injectável, que é através de um cateter longo, mantendo a solução compatível com os compostos bioactivos. Embora o pH deve ser aumentada para aumentar a injectabilidade, os compostos bioactivos tais como factores de crescimento são moléculas frágeis que devem ser manuseadas com cuidado. Nós monitorar o pH da solução rigorosamente usando um medidor de pH após a adição da hydrogelator para confirmar que é pH 9,0 antes de adicionar quaisquer componentes bioactivos. Inicialmente, várias rodadas de ajustar o pH de partida da PBS eram necessárias para acabar com o pH certo. Além disso, porque usar soluções relativamente viscosos e um cateter de longa e fina, uma grande queda de pressão está presente (na ordem de 0,5 MPa, dependendo da velocidade de injecção). Portanto, cuidado especial deve ser tomado na seleção das conexões corretas entre a seringa eo cateter. A injeção suportes bomba de seringa controlada, como a aplicação de tais forças com a mão é um desafio. Pois em vitrO experiências, a solução foi gelificado por neutralização da solução com HCl, enquanto in vivo, isto é feito por o pH natural do tecido. Portanto, é importante adicionar a quantidade certa de HCl para evitar uma ultrapassagem do pH. A difusão deste ácido é provavelmente o fator limitante na gelificação do hidrogel em experiências in vitro; No entanto, in vivo, o líquido terá uma área de superfície elevada contacto com tecido neutralizantes, que provavelmente irão resultar numa mais rápida e uniformemente gelificação em comparação com adição gota a gota de ácido concentrado. Além disso, a comutação de gel é muito mais rápida com este procedimento leve em comparação com os métodos utilizados previamente (0,5 hr vs 2 h) 25. Usando pH natural do corpo para a mudança das propriedades do material é muito atraente desde a transição é rápida, reversível, não pode ocorrer dentro do cateter e in vivo é totalmente automático. Estas propriedades dão vantagens sobre eg swit térmicachable gelifica 26, onde o risco de gelificação num cateter devido a mudanças de temperatura estiver presente, que requerem géis polimerização foto-induzida, que é um desafio devido à penetração limitada luz e 27 de formação de radicais, ou géis, que requerem a co-injecção de um iniciador de polimerização ou accellerator 28.
Libertação bem sucedida de um fármaco a partir do hidrogel depende em grande parte do tamanho do fármaco. Como mostrado, a pequena molécula é liberada imediatamente, enquanto a liberação gradual do modelo de proteína sobre uma semana mostra a promessa desses hidrogéis como sistemas de liberação de fatores de crescimento. Em geral, os hidrogéis são mais promissoras como ferramenta de entrega de objetos maiores, como proteínas, exossomos e células 29,30.
O procedimento de mapeamento e de injecção electromecânico 3-D fornece uma abordagem de entrega baseados em cateter clinicamente validado para várias terapias de regeneração do miocárdio, tais como hidrogéis. O added valor desta tecnologia em comparação com outras técnicas de administração não cirúrgica é o planeamento do tratamento, tornando-se possível diferenciar miocárdio normal, enfartada e hibernação e orientar terapias na área de interesse. Inconvenientes desta abordagem preocupação as habilidades técnicas necessárias eo procedimento demorado e caro 20. No modelo suíno apresentados de infarto do miocárdio mapeamento eletromecânico foi seguido por injeções intramiocárdicas guiadas com o bioativo supramolecular UPy-hidrogel. Outras combinações com terapias regenerativas têm de ser testados in vitro e in vivo para ganhar mais sucesso neste campo emergente. Além disso, a optimização dos processos de injectabilidade e esterilização tem que ser realizada com sucesso para traduzir este método para um ambiente clínico.
Divulgações
The authors have nothing to disclose.
Agradecimentos
Este trabalho foi financiado pelo Ministério da Educação, Cultura e Ciência (programa de Gravidade 024.001.035), a Organização Holandesa para Pesquisa Científica (NWO), o Conselho Europeu de Investigação (FP7 / 2007-2013) Convenção de subvenção CEI 308045 e realizado no âmbito do quadro LSH TKI. Isso faz parte de pesquisa do Projeto P1.03 PENT do programa do BioMedical Materiais instituto de pesquisa, co-financiado pelo Ministério dos Assuntos Económicos neerlandês. Este projecto foi apoiado por icin - Instituto Holandês Coração ( www.icin.nl ) eo "Wijnand M. Pom Stichting". Os autores gostariam de agradecer Henk Janssen e Joris Peters para a síntese do UPy-hydrogelator e Remco Arts para fornecer o mRuby2. Agradecemos Bert Meijer, Tonny Bosman, Roxanne Kieltyka, Stijn Kramer, Joost Sluijter, Imo Hoefer, e Frebus van Slochteren para as muitas discussões úteis e Marlijn Jansen, Joyce Visser, Grace Croft e Martijn van Nieuwburg para teassistência chnical.
Materiais
| Name | Company | Catalog Number | Comments |
| 1 M HCl | |||
| 1 M NaOH | |||
| Polystyrene 24-well plate | Falcon | 353047 | |
| Amiodarone | Cordaron I.V. (Sanofini) | ||
| Anton Paar Physica MCR501 | Anton Paar GmbH | Equipped with a parallel-plate geometry (25 mm) | |
| Atropine | PCH | ||
| Balloon ventilator | |||
| Cary 50 Scan UV-Visible Spectrophotometer | Varian | ||
| Cary Eclipse Fluorescence Spectrophotometer | Varian | ||
| Defibrillation patches | |||
| DMSO | Biosolve | 44705 | |
| Endotracheal tube | Covidien | ||
| Heparin | |||
| Ketamine | Narketan 10 Vétoquinol | ||
| Mapping catheter 115 cm | Biosense Webster | ||
| Midazolam | Actavis | ||
| MilliQ | MD Milipore MilliQ Integral Water Purification System | ||
| mRuby2 | |||
| NaCl 0.9% 500 cc | Braun | ||
| NOGA guided Myostar injection catheter | Biosense Webster | ||
| NOGA-RefStar EFO-patch | Biosense Webster | ||
| Pancuronium bromide | |||
| Parafilm | VWR | IKAA3801100 | |
| PBS | Sigma Aldrich | P4417 | |
| PET millicel | Millipore | PIEP12R48 | |
| Pirfenidone | Sigma Aldrich | P2116 | Used from 100 mM stock in DMSO |
| Sodiumthiopental | Inresa | ||
| Sufentanil | Sufentanil-Hameln | ||
| Tegaderm | |||
| UPy-PEG10k | |||
| UV-Lamp | |||
| Vet ointment | |||
| Visipaque contrastfluid 100 cc |
Referências
- Levy, D., et al. Long-Term Trends in the Incidence of and Survival with Heart Failure. The New England Journal of Medicine. 347 (18), 1397-1402 (2002).
- Roger, V. L., et al. Heart disease and stroke statistics—2012 update: a report from the American Heart Association. Circulation. 120 (1), 2-220 (2012).
- Peppas, N. A., Huang, Y., Torres-Lugo, M., Ward, J. H., Zhang, J. Physicochemical foundations and structural design of hydrogels in medicine and biology. Annual Review of Biomedical Engineering. 2 (1), 9-29 (2000).
- Olsen, B. D., Kornfield, J. A., Tirrell, D. A. Yielding Behavior in Injectable Hydrogels from Telechelic Proteins. Macromolecules. 43 (21), 9094-9099 (2010).
- Guvendiren, M., Lu, H. D., Burdick, J. A. Shear-thinning hydrogels for biomedical applications. Soft Matter. 8 (2), 260 (2012).
- Bastings, M., et al. A Fast pH-Switchable and Self-Healing Supramolecular Hydrogel Carrier for Guided, Local Catheter Injection in the Infarcted Myocardium. Advanced Healthcare Materials. 3 (1), 70-78 (2014).
- Pawar, G. M., et al. Injectable Hydrogels from Segmented PEG-Bisurea Copolymers. Biomacromolecules. 13 (12), 3966-3976 (2012).
- Yoon, H. -. J., Jang, W. -. D. Polymeric supramolecular systems for drug delivery. Journal of Materials Chemistry. 20 (2), 211-222 (2009).
- Christman, K. L., Lee, R. J. Biomaterials for the treatment of myocardial infarction. Journal of the American College of Cardiology. 48 (5), 907-913 (2006).
- Yu, L., Ding, J. Injectable hydrogels as unique biomedical materials. Chemical Society Reviews. 37 (8), 1473-1481 (2008).
- Krieg, E., Rybtchinski, B. Noncovalent Water-Based Materials: Robust yet Adaptive. Chemistry – A European Journal. 17 (33), 9016-9026 (2011).
- Davis, M. E., et al. Injectable self-assembling peptide nanofibers create intramyocardial microenvironments for endothelial cells. Circulation. 111 (4), 442-450 (2005).
- Li, J., Ni, X., Leong, K. W. Injectable drug-delivery systems based on supramolecular hydrogels formed by poly(ethylene oxide)s and alpha-cyclodextrin. Journal of Biomedical Materials Research. Part A. 65 (2), 196-202 (2003).
- Dankers, P. Y. W., et al. Hierarchical formation of supramolecular transient networks in water: a modular injectable delivery system. Advanced materials. 24 (20), 2703-2709 (2012).
- Dankers, P. Y. W., et al. Development and in-vivo characterization of supramolecular hydrogels for intrarenal drug delivery. Biomaterials. 33 (20), 5144-5155 (2012).
- Kieltyka, R. E., et al. Mesoscale modulation of supramolecular ureidopyrimidinone-based poly(ethylene glycol) transient networks in water. Journal of the American Chemical Society. 135 (30), 11159-11164 (2013).
- Vrijsen, K. R., et al. Cardiomyocyte progenitor cell-derived exosomes stimulate migration of endothelial cells. Journal of Cellular and Molecular Medicine. 14 (5), 1064-1070 (2010).
- Koudstaal, S., et al. Myocardial infarction and functional outcome assessment in pigs. Journal of Visualized Experiments. (86), (2014).
- Koudstaal, S., et al. Sustained delivery of insulin-like growth factor-1/hepatocyte growth factor stimulates endogenous cardiac repair in the chronic infarcted pig heart. Journal of Cardiovascular Translational Research. 7 (2), 232-241 (2014).
- Spoel, T. I., et al. Non-surgical stem cell delivery strategies and in vivo cell tracking to injured myocardium. International Journal of Cardiovascular Imaging. 27 (3), 367-383 (2011).
- Gepstein, L., Hayam, G., Shpun, S., Ben-Haim, S. A. Hemodynamic evaluation of the heart with a nonfluoroscopic electromechanical mapping technique. Circulation. 96 (10), 3672-3680 (1997).
- Gyöngyösi, M., Dib, N. Diagnostic and prognostic value of 3D NOGA mapping in ischemic heart disease. Nature Reviews Cardiology. 8 (7), 393-404 (2011).
- Siepmann, J., Siepmann, F. Modeling of diffusion controlled drug delivery. Journal of Controlled Release Official Journal of the Controlled Release Society. 161 (2), 351-362 (2012).
- Kim, H., Fassihi, R. Application of binary polymer system in drug release rate modulation. 2. Influence of formulation variables and hydrodynamic conditions on release kinetics. Journal of Pharmaceutical Sciences. 86 (3), 323-328 (1997).
- Pape, A. C. H., et al. Mesoscale characterization of supramolecular transient networks using SAXS and rheology. International Journal Of Molecular Sciences. 15 (1), 1096-1111 (2014).
- Lee, B. H., Vernon, B. . In Situ-Gelling, Erodible N-Isopropylacrylamide Copolymers. Macromolecular Bioscience. 5 (7), 629-635 (2005).
- Annabi, N., et al. 25th Anniversary Article: Rational Design and Applications of Hydrogels in Regenerative Medicine. Advanced Materials. 26 (1), 85-124 (2014).
- Asai, D., et al. Protein polymer hydrogels by in situ, rapid and reversible self-gelation. Biomaterials. 33 (21), 5451-5458 (2012).
- Peppas, N. A., Hilt, J. Z., Khademhosseini, A., Langer, R. Hydrogels in Biology and Medicine: From Molecular Principles to Bionanotechnology. Advanced Materials. 18 (11), (2006).
- Lutolf, M. P., Hubbell, J. A. Synthetic biomaterials as instructive extracellular microenvironments for morphogenesis in tissue engineering. Nature Biotechnology. 23 (1), 47-55 (2005).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados