É necessária uma assinatura da JoVE para visualizar este conteúdo. Faça login ou comece sua avaliação gratuita.
Method Article
Eletroforese Capilar para monitorar Peptide Enxertia em quitosana Films em Tempo real
Neste Artigo
Resumo
Free solution capillary electrophoresis is a fast, cheap and robust analytical method that enables the quantitative monitoring of chemical reactions in real time. Its utility for rapid, convenient and precise analysis is demonstrated here through analysis of covalent peptide grafting onto chitosan films for improved cell adhesion.
Resumo
electroforese capilar de solução livre (CE) separa os analitos, compostos geralmente praticados na solução por meio da aplicação de um campo eléctrico. Em comparação com outras técnicas de separação analíticas, tais como cromatografia, CE é barato, robusto e eficaz não requer a preparação da amostra (por um certo número de matrizes naturais complexas ou amostras poliméricas). CE é rápido e pode ser utilizado para seguir a evolução de misturas em tempo real (por exemplo, cinética de reacção química), tal como os sinais observados para os compostos são separados são directamente proporcional à sua quantidade em solução.
Aqui, a eficiência da CE é demonstrada para a monitorização do enxerto covalente de péptidos sobre os filmes de quitosana para aplicações biomédicas subsequentes. propriedades antimicrobianas e biocompatíveis da quitosana torná-lo um material atraente para aplicações biomédicas, tais como substratos de crescimento celular. Enxerto covalentemente os RGDS péptido (arginina - glicina -ácido aspártico - serina) sobre a superfície de filmes de quitosano tem por objectivo melhorar a fixação celular. Historicamente, a cromatografia e a análise de aminoácidos têm sido utilizados para fornecer uma medida directa da quantidade de péptido enxertado. No entanto, a separação rápida e ausência de preparação de amostras fornecidas pela CE permite o monitoramento em tempo real igualmente precisa ainda do processo de enxertia peptídeo. CE é capaz de separar e quantificar os diferentes componentes da mistura reaccional: o (não enxertados) péptido e os agentes de acoplamento químico. Deste modo, o uso de CE resulta em filmes melhoradas para aplicações a jusante.
Os filmes de quitosana foram caracterizados por meio de estado sólido RMN (ressonância magnética nuclear) espectroscopia. Esta técnica é mais demorada e não pode ser aplicada em tempo real, mas produz uma medição directa do péptido e, assim, valida a técnica CE.
Introdução
Electroforese capilar solução livre (CE) é uma técnica que separa os compostos em soluções com base na sua razão de carga de 1,2-para-fricção. Relação carga-to-size é frequentemente mencionado na literatura, mas essa simplificação não se aplica a polielectr�itos, incluindo polipeptídeos neste trabalho, e também foi mostrado para não ser apropriado para pequenas moléculas orgânicas 3. CE difere de outras técnicas de separação em que o mesmo não possui uma fase estacionária, apenas uma electrólito fundo (geralmente um tampão). Isso permite que a técnica para ser robusto em sua capacidade de analisar uma grande variedade de amostras com matrizes complexas 4, tais como fibras de plantas 5, cervejas de fermentação 6 de enxertia em polímeros sintéticos 7, amostras de alimentos 8, e peptídeos dificilmente solúveis 9 sem preparação da amostra tedioso e purificação. Isto é especialmente significativo para polielectrólitos complexos que têm problemas de dissolução (suito como quitosano 10 e goma de gelano 11) e, por conseguinte, existir como agregados ou precipitado na solução e foram analisados com sucesso sem a filtração da amostra. Além disso, a análise de açúcares em cereais de pequeno almoço envolveu injetar amostras com partículas de amostras de cereais de pequeno-almoço precipitado em água 8. Isto também se estende para a análise de polielectrólitos ou copolímeros ramificados 12,13. Extenso trabalho também foi concluído no desenvolvimento de técnicas de CE especificamente para a análise de proteínas para proteómica 14, separação quiral de péptidos naturais ou sintéticos 15 e separações microchip de proteínas e péptidos 16. Uma vez que a separação e a análise ter lugar em um capilar, apenas pequenos volumes de amostra e são usados solventes que permite CE ter um custo de exploração mais baixa do que outras técnicas de separação, incluindo 5,6,17 cromatografia. Uma vez que a separação por CE é rápido, que permite que o monitoanel de cinética da reacção. Isto foi demonstrado no caso do processo de enxerto de péptidos sobre os filmes de quitosano para uma melhor adesão da célula 18.
O quitosano é um polissacárido derivado do -deacetylation N de quitina. Filmes de quitosano pode ser usado para várias aplicações biomédicas, tais como bio-adesivos 19 e substratos de crescimento de células 18,20, devido à biocompatibilidade do quitosano 21. Ligação de células a proteínas de matriz extracelular específicos, tais como fibronectina, laminina e colagénio, está directamente relacionada com a sobrevivência das células 22. Notavelmente, tipos de células diferentes, muitas vezes exigem apego a diferentes proteínas da matriz extracelular para a sobrevivência e funcionamento correto. A fixação de células de filmes de quitosana foi mostrado para ser melhorada através da enxertia de fibronectina 23; No entanto, a preparação, purificação e enxertia de tais proteínas grandes não é economicamente viável. Em alternativa uma variedade de pequenos péptidos Have foi mostrado ser capaz de imitar as propriedades de grandes proteínas da matriz extracelular. Por exemplo, péptidos, tais como os miméticos de fibronectina RGD (arginina - glicina - ácido aspártico) e RGDS (arginina - glicina - ácido aspártico - serina) têm sido usadas para facilitar e aumentar a ligação de células 24. Covalente enxerto de RGDS sobre os filmes de quitosana resultou na fixação das células melhorado para células conhecidas para anexar a fibronectina in vivo 18. Substituindo proteínas maiores gosta fibronectina com péptidos mais pequenos que têm a mesma funcionalidade proporciona uma significativa redução de custos.
Aqui, o péptido de enxertia para a quitosana foi realizada como publicado anteriormente 18. Como demonstrado previamente, esta abordagem fornece enxerto simples e eficiente, utilizando os agentes de acoplamento de EDC-HCl (1-etil-3- (3-dimetilaminopropil) carbodiimida) e NHS (N-hidroxissuccinimida) para funcionalizar o ácido carboxílico da RGDS ser enxertado nafilme de quitosana. Duas vantagens deste método são que o enxerto não exige qualquer modificação do quitosano ou do péptido, e é realizada em meio aquoso, para maximizar a compatibilidade com as aplicações de cultura de células futuras 18,20. Como os agentes de acoplamento e o péptido pode ser cobrado, CE é um método adequado para a análise da cinética de reacção. Mais importante, a análise da cinética da reacção por meio de CE permite a monitorização em tempo real da reacção de enxerto, e, portanto, permite a optimização tanto e quantificar o grau de enxertamento.
Embora não seja necessário rotineiramente, os resultados da análise de CE pode ser validado off-line por uma medição directa do péptido enxertando sobre os filmes de quitosano usando espectroscopia de 25,26-RMN de estado sólido (ressonância magnética nuclear) para demonstrar o enxerto covalente do péptido sobre a película 18. No entanto, em comparação com a do estado sólido espectroscopia de RMN, a análise em tempo real fornecida pelaCE permite a quantificação do consumo de péptido em tempo real e, assim, a capacidade de avaliar a cinética da reacção.
O método acima mencionado é simples e permite a análise em tempo real de péptido enxertia em filmes de quitosana com quantificação indirecta da extensão da enxertia. O método demonstrado pode ser estendido para a avaliação quantitativa em tempo real de diferentes reacções químicas, desde que os reagentes ou os produtos a serem analisados pode ser carregada.
Protocolo
1. Preparação de quitosano Films
- Pesar 2 g de ácido acético glacial, completa a 100 ml com água ultrapura.
- Pesar 1,7 g de pó de quitosano, juntar 100 ml de solução a 2% m / m de ácido acético aquoso. Agita-se durante 5 dias, com uma barra de agitação e placa de agitação magnética à temperatura ambiente, quer coberto com folha de alumínio ou, no escuro.
- Centrifugar a dispersão de quitosano a 1076 xg a 23 ° C durante 1 h. Recolhe-se o sobrenadante com uma seringa e descartar o precipitado.
- Para cada película, uma alíquota de 10 ml da suspensão de quitosana em plástico de 9 cm de caixa de Petri à temperatura ambiente. Deixar os filmes cobertos para secar por pelo menos 7 dias.
- Usando uma tesoura cortar os filmes secos em 1 x 1 cm quadrados. Nota: O experimento pode ser pausado nesta fase.
2. Preparação de solução salina tamponada com fosfato (PBS)
- Pesar 8 g de cloreto de sódio, 0,2 g de cloreto de potássio, 1,44 g de hidrogenofosfato dissódico PhosPhate e 0,24 g de di-hidrogenofosfato de potássio.
- Dissolve-se estes produtos químicos pesados em 800 ml de água ultrapura e titula-se a solução com ácido clorídrico concentrado para pH 7,4.
Nota: O experimento pode ser pausado nesta fase.
3. Preparação de tampão de borato de sódio 75 mM a pH 9,2
- Pesar 3,0915 g de ácido bórico. Dissolve-lo em 75 ml de água ultrapura.
- Titula-se a solução de ácido bórico a um pH de 9,2 com uma solução de hidróxido de sódio a uma concentração de 10 M ou superior.
Atenção: soluções concentradas de hidróxido de sódio são corrosivos e devem ser manuseados com luvas. - Completar com água ultrapura para se obter 100 ml de solução. Obteve-se um tampão de borato de sódio 500 mM a pH 9,2.
- Diluir o tampão de borato de sódio 500 mM com água ultrapura com tampão de borato de sódio 75 mM. Nota: O experimento pode ser pausado nesta fase.
4. Preparação de quitosano Films para a reacção de enxerto
- Lavagem de 10 filmes de quitosana quadrados (1 x 1 cm) em 5 ml de PBS durante 2 h em placas de Petri à temperatura ambiente.
- Durante este tempo, preparar e validar o instrumento de electroforese capilar (passo 5).
5. Preparação e validação do Instrumento de Eletroforese Capilar
- Prepara-se uma de 43,5 cm nua capilar de sílica fundida, com um diâmetro interno de 50 mm (43,5 centímetros é o comprimento total, o comprimento efectivo para a janela de detecção é normalmente 35 cm), enfraquecendo o revestimento exterior de polímero do capilar com o comprimento conjunto com um utensílio contundente, em seguida, encaixe o capilar.
- Criar uma janela para o capilar usando um isqueiro para queimar o revestimento de polímero de 8,5 cm da entrada e depois que esfria limpe-o com etanol. Queimar o revestimento do capilar em cada extremidade por alguns milímetros, com um isqueiro, e depois que esfria limpe-o com etanol.
- insi capilar lugarjanela de detecção e instalá-lo na cassete capilar, colocando-o em distâncias iguais na entrada e na saída e enrolando-a em torno dos eixos da cassete. Em seguida, instale a cassete no instrumento eletroforese capilar.
- Definir os parâmetros do método para cada separação. No menu do software selecione "método" e depois "editar o método inteiro". Ajustar a temperatura, o tempo, a tensão, e os frascos utilizados para a separação (por exemplo 25 ° C, 10 min, 30 kV).
- Na secção de pré-condicionamento, definir os rubores consecutivos: 10 minutos com hidróxido de sódio a 1 M (em água), 5 min com hidróxido de sódio 0,1 M (em água), 5 min com água ultrapura e 5 min com tampão de borato de sódio 75 mM a pH 9,2 para o primeiro método de uma série de análises.
- Para os métodos subsequentes, definir o conjunto das ondas consecutivas na secção de pré-condicionamento: 1 min com hidróxido de sódio a 1 M (em água), 5 min com tampão de borato de sódio 75 mM a pH 9.2.
- Na secção de injecção, para definir os parâmetros de uma injecção com pressão hidrodinâmico 30 mbar durante 10 segundos para todos os métodos. Na secção de separação, definir as condições de separação a 30 kV, a 25 ° C durante 9 min para todos os métodos.
NOTA: Consulte o manual do usuário do instrumento específico CE como procedimento para operar o instrumento CE pode variar entre os fabricantes. Preparar a solução de hidróxido de sódio 1 M no dia.
- Injectar e separar um padrão interno de neutro (10 ul de 10% v / v de sulfóxido de dimetilo (DMSO), em água diluída em 450 ul de tampão de borato de sódio 75 mM). Injetar e separar da mesma forma um padrão oligoacrylate (dissolvido em água ultrapura em 10 g ∙ L -1; veja Lista de Materiais) para verificar a validade do capilar. Pausar a sequência aqui até a reacção de enxerto está pronto para começar.
6. Alongamento das RGDS Onto Quitosana Film
- Pesar o péptido (1 mg RGDS)e os agentes de acoplamento (3 mg de EDC-HCl e 2 mg de NHS).
- 2 horas após o início da imersão filme de quitosano em PBS, dissolve-se o péptido e os agentes de acoplamento em 5 ml de PBS.
- Tomar uma aliquota de 50 ul desta solução. Adicionar 2 mL de 10% v / v de DMSO em água, como um padrão interno neutro à alíquota. Analisar a alíquota com CE (veja o passo 7).
- Remover os 5 ml de PBS utilizada para enxaguar os filmes de quitosana da placa de Petri. Adicionar a solução de 5 ml de agentes de acoplamento de péptidos e para a placa de Petri contendo os filmes de quitosana.
- Cubra o prato de Petri com filme de parafina e colocá-lo em um agitador orbital à temperatura ambiente. Tome 50 mL alíquotas de meios de reacção em tempos do jogo.
NOTA: O tempo total de análise de CE é de 15 minutos, assim, uma alíquota pode ser feita a cada 15 minutos (ou a cada 30 min se duas reacções são monitorizadas em paralelo, etc).- Adicionar 2 mL de 10% v / v de DMSO em água, como um padrão interno para cada ponto morto aiIQUOT.
NOTA: As aliquotas devem ser analisadas com CE, logo que eles são levados (ver passo 7).
- Adicionar 2 mL de 10% v / v de DMSO em água, como um padrão interno para cada ponto morto aiIQUOT.
- Após 4 horas de agitação e remoção de alíquotas, remova a placa de Petri do shaker. Remover o meio de reacção a partir da placa de Petri. Adicionar 5 ml de PBS para lavar os filmes de quitosana.
- Remover o PBS a partir da placa de Petri, lavar o filme quitosana com água ultrapura e permitir-lhes a secar durante a noite. Remover a água ultrapura e armazenar as películas à temperatura de -20 ° C em uma placa de Petri de plástico.
7. Monitoramento de Reação Enxerto Usando CE
- Injectar e alíquotas separadas de meio de reacção imediatamente após a remoção da placa de Petri utilizando as condições de análise como na secção 5.2.
- Após a conclusão das separações enxaguar o capilar com água ultrapura durante 10 min. Seque-o através de um flush com um frasco vazio (ar) durante 10 min.
NOTA: O experimento pode ser pausado nesta fase.
8. Dados Trea tamento para CE
- Verificar a validade de cada separação, por verificar que tanto a corrente durante a separação e o tempo de migração do marcador mobilidade electro-osmótico (DMSO neste caso) são semelhantes aos observados para a separação padrão oligoacrylate.
NOTA: até 10-15% de variação é aceitável do valor atual esperado de cerca de 50 mA e valor tempo de migração de 1,3 min (valores de mobilidade eletroforética deve ser usado em vez de tempos de migração se um repetibilidade superior é exigido). - Para cada separação bem-sucedida, exportar os dados brutos do software eletroforese capilar, selecionando um conjunto de dados específico, clique direito sobre a exportação e selecionar um sinal apropriado.
- Converter os dados em bruto gravados pela CE (apresentada como absorvância de UV em função do tempo de migração). Converter o eixo X (tempo de migração T m) para uma mobilidade electroforética μ seguinte equação 1:
n 1 "src =" / files / ftp_upload / 54549 / 54549eq1.jpg "/> (1)
em que L é o comprimento d ao detector, G t é o comprimento total do tubo capilar, V é a tensão, e t EO é o tempo de migração de uma espécie neutra (padrão interno DMSO neste caso) 27.
Converter o eixo Y dos dados em bruto (absorvância em AU) para uma distribuição de mobilidades electrof W (μ) seguinte equação 2: 28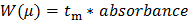 (2)
(2)
9. Caracterização Adicional dos enxertado com Peptídeo 18 Films
- Insira filmes de quitosana enxertado com peptídicos, laminados em torno de si, em um solid-state rotor NMR 4 mm. Encher o rotor com solução salina tamponada com fosfato a inchar dos filmes, e fechar o rotor. Espere por algumas horas.
- Analisar o filme com 13 </ sup> C espectroscopia de RMN 18.
Resultados
CE está bem adaptado para monitorar a enxertia de péptidos (por exemplo, RGDS) sobre os filmes de quitosano. Os agentes de acoplamento adequados incluem EDC-HCl e NHS que activam o péptido a ser enxertado na quitosano (Figura 1). CE é capaz de separar os diferentes moléculas de interesse a partir do meio de reacção. Para designar os picos no electroferograma, RGDS puros, EDC-HCl e NHS foram dissolvidos, injectados separadamente e separada. Após a atribui...
Discussão
A simplicidade do protocolo descrito aqui torna-o idealmente adequado para aplicação generalizada. No entanto, uma atenção especial deve ser dada a uma das seguintes etapas principais.
Preparação instrumento adequado CE
É importante para separar um padrão conhecido, imediatamente antes da separação de amostras desconhecidas (bem como no fim de uma série de separações) para verificar a validade do capilar e instrumento no dia. Este pa...
Divulgações
Os autores declaram que não têm interesses financeiros concorrentes.
Agradecimentos
MG, MO'C and PC thank the Molecular Medicine Research Group at WSU for Research Seed Funding, as well as Michele Mason (WSU), Richard Wuhrer (Advanced Materials Characterisation Facility, AMCF, WSU) and Hervé Cottet (Montpellier) for discussions.
Materiais
| Name | Company | Catalog Number | Comments |
| Water | Millipore | All water used in the experiment has to be of Milli-Q quality | |
| Chitosan powder (medium molecular weight) | Sigma-Aldrich | 448877 | lot MKBH1108V was used. Significant batch-to-batch variations occur with natural products such as polysaccharides |
| Acetic acid - Unilab | Ajax Finechem | 2-2.5L GL | laboratory reagent |
| Dimethylsulfoxide | Sigma-Aldrich | D4540 | laboratory reagent, slightly hazardous to skin, hazardous if ingested |
| Sodium hydroxide | Sigma-Aldrich | 221465 | laboratory reagent, corrosive |
| 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide | Sigma-Aldrich | D80002 | Irritant to skin |
| N-hydroxysuccinimide | Sigma-Aldrich | 130672 | Irritant to skin |
| Sodium chloride | Ajax Finechem | 466-500G | laboratory reagent |
| Potassium chloride - Univar | Ajax Finechem | 384-500G | analytical reagent, slight skin irritant |
| Disodium hydrogen phosphate - Unilab | Ajax Finechem | 1234-500G | laboratory reagent, slight skin irritant |
| Potassium dihydrogen phosphate - Univar | Ajax Finechem | 4745-500G | analytical reagent, slight skin irritant |
| Oligoacrylate standard | custom made | See reference for synthetic protocol: Castignolles, P.; Gaborieau, M.; Hilder, E. F.; Sprong, E.; Ferguson, C. J.; Gilbert, R. G. Macromol. Rapid Commun. 2006, 27, 42-46 | |
| Boric acid | BDH AnalR, Merck Pty Ltd | 10058 | Corrosive |
| Hydrochloric acid - Unilab | Ajax Finechem | A1367-2.5L | laboratory reagent, corrosivie |
| Fused silica tubing | Polymicro (Molex) | TSP050375 | Flexible fused silica capillary tubing with standard polyimide coating, 50 µm internal diameter, 363 µm outer diameter |
| Agilent 7100 CE | Agilent Technologies | G7100CE | Capillary electrophoresis instrument |
| Orbital shaker | IKA | KS260 | |
| Electronic balance | Mettler Toledo | MS204S | |
| Milli-Q Synthesis | Millipore | ZMQS5VF01 | Ultrapure water filtration system |
| Parafilm | Labtek | PM966 | Parrafin wax |
Referências
- Muthukumar, M. Theory of electrophoretic mobility of a polyelectrolyte in semidilute solutions of neutral polymers. Electrophoresis. 17, 1167-1172 (1996).
- Barrat, J. L., Joanny, J. F. . in Advances in Chemical Physics, Vol Xciv Vol. 94 Advances in Chemical Physics. , 1-66 (1996).
- Fu, S. L., Lucy, C. A. Prediction of electrophoretic mobilities. 1. Monoamines. Anal. Chem. 70, 173-181 (1998).
- Harvey, D. . Modern Analytical Chemistry. , (2000).
- Oliver, J. D., Gaborieau, M., Hilder, E. F., Castignolles, P. Simple and robust determination of monosaccharides in plant fibers in complex mixtures by capillary electrophoresis and high performance liquid chromatography. J. Chromatogr. A. 1291, 179-186 (2013).
- Oliver, J. D., Sutton, A. T., Karu, N., Phillips, M., Markham, J., Peiris, P., Hilder, E. F., Castignolles, P. Simple and robust monitoring of ethanol fermentations by capillary electrophoresis. Biotechnology and Applied Biochemistry. 62, 329-342 (2015).
- Thevarajah, J. J., Sutton, A. T., Maniego, A. R., Whitty, E. G., Harrisson, S., Cottet, H., Castignolles, P., Gaborieau, M. Quantifying the Heterogeneity of Chemical Structures in Complex Charged Polymers through the Dispersity of Their Distributions of Electrophoretic Mobilities or of Compositions. Anal. Chem. 88, 1674-1681 (2016).
- Toutounji, M. R., Van Leeuwen, M. P., Oliver, J. D., Shrestha, A. K., Castignolles, P., Gaborieau, M. Quantification of sugars in breakfast cereals using capillary electrophoresis. Carbohydr. Res. 408, 134-141 (2015).
- Miramon, H., Cavelier, F., Martinez, J., Cottet, H. Highly Resolutive Separations of Hardly Soluble Synthetic Polypeptides by Capillary Electrophoresis. Anal. Chem. 82, 394-399 (2010).
- Mnatsakanyan, M., Thevarajah, J. J., Roi, R. S., Lauto, A., Gaborieau, M., Castignolles, P. Separation of chitosan by degree of acetylation using simple free solution capillary electrophoresis. Anal. Bioanal. Chem. 405, 6873-6877 (2013).
- Taylor, D. L., Ferris, C. J., Maniego, A. R., Castignolles, P., in het Panhuis, M., Gaborieau, M. Characterization of Gellan Gum by Capillary Electrophoresis. Australian Journal of Chemistry. 65, 1156-1164 (2012).
- Thevarajah, J. J., Gaborieau, M., Castignolles, P. Separation and characterization of synthetic polyelectrolytes and polysaccharides with capillary electrophoresis. Adv. Chem. 2014, 798503 (2014).
- Sutton, A. T., Read, E., Maniego, A. R., Thevarajah, J., Marty, J. -. D., Destarac, M., Gaborieau, M., Castignolles, P. Purity of double hydrophilic block copolymers revealed by capillary electrophoresis in the critical conditions. J. Chromatogr. A. 1372, 187-195 (2014).
- Righetti, P. G., Sebastiano, R., Citterio, A. Capillary electrophoresis and isoelectric focusing in peptide and protein analysis. Proteomics. 13, 325-340 (2013).
- Ali, I., Al-Othman, Z. A., Al-Warthan, A., Asnin, L., Chudinov, A. Advances in chiral separations of small peptides by capillary electrophoresis and chromatography. J. Sep. Sci. 37, 2447-2466 (2014).
- Kasicka, V. Recent developments in capillary and microchip electroseparations of peptides (2011-2013). Electrophoresis. 35, 69-95 (2014).
- Taylor, D. L., Thevarajah, J. J., Narayan, D. K., Murphy, P., Mangala, M. M., Lim, S., Wuhrer, R., Lefay, C., O'Connor, M. D., Gaborieau, M., Castignolles, P. Real-time monitoring of peptide grafting onto chitosan films using capillary electrophoresis. Anal. Bioanal. Chem. 407, 2543-2555 (2015).
- Rinaudo, M. Chitin and chitosan: Properties and applications. Prog. Polym. Sci. 31, 603-632 (2006).
- Li, Z., Leung, M., Hopper, R., Ellenbogen, R., Zhang, M. Feeder-free self-renewal of human embryonic stem cells in 3D porous natural polymer scaffolds. Biomaterials. 31, 404-412 (2010).
- Domard, A. A perspective on 30 years research on chitin and chitosan. Carbohydr. Polym. 84, 696-703 (2011).
- Shekaran, A., Garcia, A. J. Nanoscale engineering of extracellular matrix-mimetic bioadhesive surfaces and implants for tissue engineering. Biochim. Biophys. Acta Gen. Subj. 1810, 350-360 (2011).
- Custodio, C. A., Alves, C. M., Reis, R. L., Mano, J. F. Immobilization of fibronectin in chitosan substrates improves cell adhesion and proliferation. J. Tissue Eng. Regen. Med. 4, 316-323 (2010).
- Boateng, S. Y., Lateef, S. S., Mosley, W., Hartman, T. J., Hanley, L., Russell, B. RGD and YIGSR synthetic peptides facilitate cellular adhesion identical to that of laminin and fibronectin but alter the physiology of neonatal cardiac myocytes. Am. J. Physiol. Cell Physiol. 288, C30-C38 (2005).
- Lefay, C., Guillaneuf, Y., Moreira, G., Thevarajah, J. J., Castignolles, P., Ziarelli, F., Bloch, E., Major, M., Charles, L., Gaborieau, M., Bertin, D., Gigmes, D. Heterogeneous modification of chitosan via nitroxide-mediated polymerization. Polym. Chem. 4, 322-328 (2013).
- Gartner, C., Lopez, B. L., Sierra, L., Graf, R., Spiess, H. W., Gaborieau, M. Interplay between Structure and Dynamics in Chitosan Films Investigated with Solid-State NMR, Dynamic Mechanical Analysis, and X-ray Diffraction. Biomacromolecules. 12, 1380-1386 (2011).
- Castignolles, P., Gaborieau, M., Hilder, E. F., Sprong, E., Ferguson, C. J., Gilbert, R. G. High resolution separation of oligo(acrylic acid) by capillary zone electrophoresis. Macromol. Rapid Commun. 27, 42-46 (2006).
- Chamieh, J., Martin, M., Cottet, H. Quantitative Analysis in Capillary Electrophoresis: Transformation of Raw Electropherograms into Continuous Distributions. Anal. Chem. 87, 1050-1057 (2015).
- Maniego, A. R., Ang, D., Guillaneuf, Y., Lefay, C., Gigmes, D., Aldrich-Wright, J. R., Gaborieau, M., Castignolles, P. Separation of poly(acrylic acid) salts according to topology using capillary electrophoresis in the critical conditions. Anal. Bioanal. Chem. 405, 9009-9020 (2013).
- Chung, T. W., Lu, Y. F., Wang, S. S., Lin, Y. S., Chu, S. H. Growth of human endothelial cells on photochemically grafted Gly-Arg-Gly-Asp (GRGD) chitosans. Biomaterials. 23, 4803-4809 (2002).
Reimpressões e Permissões
Solicitar permissão para reutilizar o texto ou figuras deste artigo JoVE
Solicitar PermissãoThis article has been published
Video Coming Soon
Copyright © 2025 MyJoVE Corporation. Todos os direitos reservados